Policy predictive model for better management of chronic obstructive pulmonary disease: economic-organisational implications in the Italian healthcare system
Background:
Chronic obstructive pulmonary disease (COPD) represents a significant public health problem in Italy, with a high prevalence and a substantial economic burden on the National Health Service (NHS). Effective management of the disease is crucial for reducing exacerbations and improving patients’ quality of life.
Methods:
This study employs a dynamic predictive model to assess the economic impact of implementing three specific health policies aimed at improving COPD management over a five-year horizon. The analysis is conducted from the perspective of the NHS, focusing on the direct costs associated with disease management.
Results:
The implementation of the proposed policies demonstrated potential significant savings in direct healthcare costs. The first policy, focused on increasing therapeutic adherence, generated an estimated savings of 202 million €. The second, concerning the wider use of triple therapies, led to savings of about 142 million €. Finally, the third policy, aimed at reducing the delay in prescribing appropriate therapies, contributed to an additional saving of over 175 million € in the time horizon considered in the analysis. Overall, these results suggest a substantial improvement opportunity in COPD management, with significant economic benefits for the Italian NHS.
Conclusion:
The study confirms the importance of targeted policies in the management of COPD, highlighting how strategic interventions can lead to significant resource savings while simultaneously improving patient care. These results provide a solid foundation for further research and serve as a useful guide for decision-makers in planning effective intervention strategies, aimed at optimizing resources and enhancing disease management in the Italian healthcare context.
Keywords: Budget impact model, Chronic obstructive pulmonary disease, Policy making in healthcare, Predictive model
Introduzione
La broncopneumopatia cronica ostruttiva (BPCO) è una malattia dell’apparato respiratorio caratterizzata da un’ostruzione irreversibile delle vie aeree di entità variabile a seconda della gravità. La condizione è solitamente progressiva ed è associata a uno stato di infiammazione cronica delle vie aeree (1, 2). Le Linee Guida Global Initiative for Chronic Obstructive Lung Disease (GOLD) 2023 evidenziano come la BPCO sia una delle principali cause di mortalità a livello globale (3). Inoltre, le esacerbazioni da cui è caratterizzata la condizione possono determinare frequenti ricoveri ospedalieri, con conseguenti effetti significativi sui costi sanitari e sulla qualità della vita dei pazienti (3). In Italia, la BPCO rappresenta un importante problema di salute pubblica, con una prevalenza stimata tra il 2,40% e il 3,30% della popolazione adulta (4). Tuttavia, si ritiene che la prevalenza attesa della condizione sia del 5-6%. Tali dati evidenziano una significativa sottostima del numero di pazienti con diagnosi di BPCO a causa di una diagnosi mancata o tardiva. Secondo le principali Linee Guida internazionali e nazionali la diagnosi di BPCO è fondata sulla presenza di una sintomatologia respiratoria persistente (p. es., tosse, escreato, dispnea da sforzo) in pazienti con una storia di esposizione a fattori di rischio e sulla successiva esecuzione, al fine di verificare l’effettiva presenza di un’ostruzione bronchiale persistente, dell’esame spirometrico (3, 5-7). Attualmente non esiste una cura efficace per ripristinare la funzionalità respiratoria persa a causa della patologia. Esistono comunque dei trattamenti per la gestione della malattia che consentono il rallentamento del declino della funzionalità respiratoria, la riduzione dei sintomi, la prevenzione di eventuali complicanze, come le riacutizzazioni, e un miglioramento in termini di sopravvivenza. I farmaci più indicati per la BPCO sono i broncodilatatori, somministrati per via inalatoria singolarmente o in combinazione, che permettono di migliorare la dilatazione delle vie aeree, garantendo così il maggior flusso possibile di aria. Per le forme più gravi si utilizzano i corticosteroidi per via inalatoria (ICS), i quali sono associati ai broncodilatatori per ridurre il numero delle riacutizzazioni, in particolare in coloro che presentano eosinofilia.
Oltre ai farmaci sopra definiti, esistono altre possibili opzioni terapeutiche non farmacologiche, come per esempio l’ossigenoterapia e la ventilazione meccanica non invasiva, per le forme più gravi caratterizzate da insufficienza respiratoria ipossica o ipossico-ipercapnica (2, 8). La gestione della BPCO prevede una continua valutazione della risposta al trattamento, con eventuali aggiustamenti in base all’evoluzione della malattia. Tuttavia, dato il rilevante burden epidemiologico che contraddistingue la BPCO, un’adeguata gestione della condizione non è priva di problematiche. Nel corso degli anni sono state messe in atto modifiche organizzative per una migliore gestione, in termini sia di diagnosi che di trattamento. Tra queste, la più recente modifica è stata apportata dalla Nota 99, entrata in vigore il 1° settembre 2021, la quale prevede, per favorire una migliore gestione della BPCO, una stratificazione funzionale dei pazienti e il riconoscimento del ruolo del Medico di Medicina Generale (MMG) per la prescrizione dei farmaci inalatori (in mono, duplice o triplice associazione estemporanea) indicati nella terapia di mantenimento dei pazienti con BPCO, lasciando allo specialista la prescrizione delle triplici associazioni fisse (9).
In aggiunta agli aspetti prettamente organizzativi, per una corretta gestione della BPCO è fondamentale che i pazienti siano ben informati sui farmaci prescritti e che comprendano i corretti dosaggi e le modalità di somministrazione, al fine di promuovere l’aderenza al trattamento e di massimizzare i benefici terapeutici. Di fatto, dalle Linee Guida GOLD 2023 (3) emerge come, per una più efficace gestione della BPCO, occorra incentivare innanzitutto un più alto livello di aderenza al trattamento, agendo contestualmente a una riduzione della complessità terapeutica. Per promuovere tali azioni, attualmente si hanno programmi di auto-monitoraggio e di auto-gestione dei medicinali, nonché la prescrizione e l’utilizzo di regimi semplificati di trattamento (9-12). In questo contesto, la triplice terapia a unico inalatore rappresenta un approccio ideale, poiché consente di somministrare più farmaci in un’unica soluzione, migliorando l’aderenza e l’efficacia del trattamento. Pertanto, l’implementazione di policy volte ad aumentare l’aderenza terapeutica e il maggiore utilizzo delle triplici terapie a unico inalatore può determinare un miglioramento della qualità della vita dei pazienti e ottimizzare al contempo l’uso delle risorse sanitarie. In aggiunta a tali aspetti, le Linee Guida GOLD 2023 (3) evidenziano come, per una migliore gestione della condizione, sia di fondamentale importanza la prescrizione tempestiva del trattamento più adeguato per i pazienti. Questo di fatto permetterebbe di prevenire le esacerbazioni e di migliorare gli esiti clinici. Tuttavia, attualmente si osserva un ritardo significativo nella prescrizione delle triplici terapie, il che impedisce ai pazienti eleggibili di beneficiare dei trattamenti più efficaci in maniera tempestiva. Pertanto, l’implementazione di policy volte a ridurre il delay prescrittivo delle triplici terapie permetterebbe di ottimizzare l’uso delle risorse sanitarie, attraverso una riduzione del carico della malattia e dei costi associati alle esacerbazioni evitabili.
Sulla base delle osservazioni evidenziate rispetto all’attuale gestione della BPCO, il presente lavoro si pone l’obiettivo di definire policy utili per una più adeguata ed efficiente gestione dei pazienti affetti dalla condizione e di valutare l’impatto in termini economico-organizzativi che la loro introduzione comporterebbe all’interno del contesto sanitario italiano.
Metodi
Al fine di valutare l’impatto economico derivante dall’implementazione di policy volte a migliorare l’attuale gestione dei pazienti affetti da BPCO nel contesto sanitario italiano, è stato sviluppato un modello predittivo dinamico dal punto di vista epidemiologico, in un orizzonte temporale pari a cinque anni. La prospettiva di analisi è del Servizio Sanitario Nazionale (SSN), con la conseguente valutazione degli input diretti sanitari legati alla gestione della BPCO nel contesto sanitario italiano. Per quanto concerne la valorizzazione dell’impatto economico, è stata utilizzata un’analisi di budget impact (BIA). La BIA prevede la comparazione di due scenari: lo scenario corrente (scenario “AS IS”), il quale rispecchia l’attuale pratica clinica per i pazienti affetti da BPCO, e lo scenario revised (scenario “TO BE”), nel quale si implementerà la policy scelta. Successivamente alla definizione dei due scenari, al fine di identificare l’impatto che l’introduzione di ciascuna policy comporta nel contesto indagato, si effettuerà un’analisi differenziale degli stessi. Più nel dettaglio, sulla base dei principali unmet clinical needs dei pazienti affetti da BPCO, sono 3 le policy di cui si valuterà l’impatto:
Policy 1: policy volta ad aumentare l’aderenza alle terapie prescritte;
Policy 2: policy volta a incentivare un maggiore utilizzo di triplici terapie a unico inalatore;
Policy 3: policy volta a una riduzione del delay prescrittivo delle triplici terapie per la popolazione eleggibile.
Infine, con l’obiettivo di analizzare la robustezza dei risultati ottenuti, è stata condotta una valutazione analitica, mediante molteplici simulazioni basate su valori predefiniti, di ciascun parametro principale delle tre policy indagate, ovvero: la percentuale di aderenza alle terapie prescritte, la percentuale di utilizzo delle triplici terapie a unico inalatore e l’arco temporale relativo al ritardo diagnostico nella prescrizione delle triplici terapie per la popolazione eleggibile.
Popolazione
Il modello considera una popolazione iniziale di 32.387.825 soggetti, ovvero la popolazione italiana con un’età superiore a 45 anni residente al 1° Gennaio 2023 (13). A partire da tale popolazione e utilizzando il tasso di prevalenza della BPCO, rispettivamente pari al 2,40% per le donne e al 3,30% per gli uomini (3), è stato possibile stimare il numero di soggetti con diagnosi di BPCO a livello nazionale, complessivamente pari a 914.088.
A partire dall’edizione del 2017, le raccomandazioni internazionali GOLD classificano i pazienti con BPCO in diversi gruppi di rischio, al fine di determinare l’approccio terapeutico iniziale più adeguato. Le quattro classi di rischio (A, B, C e D) sono basate sull’intensità della sintomatologia respiratoria e sul numero/gravità di riacutizzazioni bronchiali verificatesi nell’anno precedente (14).
Pertanto, per un’analisi più dettagliata, tenendo conto delle classi di rischio GOLD 2017 (14), sono stati identificati, sulla base delle informazioni presenti nello studio condotto da Soriano J.B. et al. (15), gli indici epidemiologici di prevalenza di tali sottogruppi di pazienti e le probabilità di transizione tra le diverse classi di rischio. Più nel dettaglio, lo studio condotto da Soriano J.B. et al. (15) ha visto la definizione delle probabilità di transizione (Materiali Supplementari, Tab. S1 (844.1KB, pdf) ) di un modello di Markov a 4 stadi, i quali rappresentano i diversi stadi di gravità che contraddistinguono la BPCO nel corso del tempo, vale a dire stadio A, stadio B, stadio C e stadio D (Fig. 1).
Fig. 1 -.
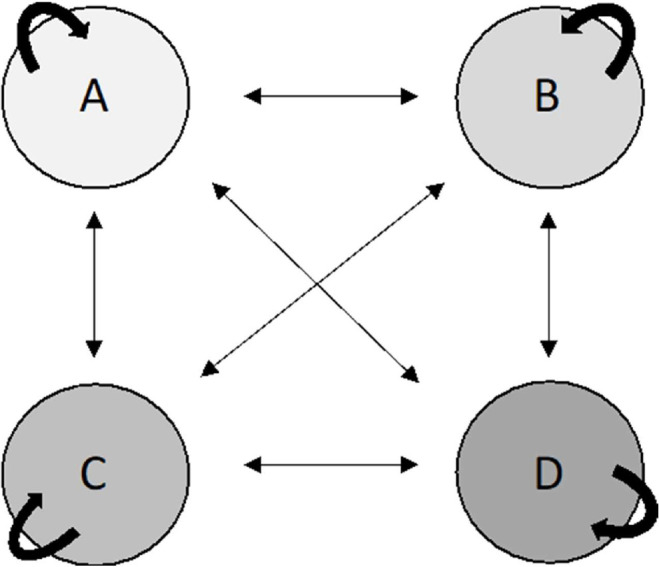
Rielaborazione dei Modelli di Markov dello studio condotto da Soriano J.B. et al. nel 2018 (15)
È tuttavia importante sottolineare come la classificazione delle quattro classi di rischio sia stata recentemente revisionata nell’edizione del report GOLD 2023 (3), mantenendo le precedenti classi di rischio A e B, ma fondendo le precedenti classi C e D in un’unica classe denominata “E” (elevato rischio di riacutizzazioni indipendentemente dalla sintomatologia).
Pertanto, in assenza di evidenze scientifiche in riferimento alla distribuzione della popolazione aggiornate rispetto alla nuova classificazione rappresentata dalle classi A, B ed E, all’interno della presente analisi si è assunto che i pazienti affetti da BPCO di stadio E siano la somma dei pazienti affetti da BPCO di stadio C e D.
Data input
Coerentemente con la prospettiva del SSN, si è proceduto ad identificare, per ciascuna classe di rischio della condizione, le principali risorse dirette sanitarie legate alla gestione della BPCO, in termini di diagnosi, di trattamento e di gestione degli eventi avversi. La definizione di tali parametri ha posto le basi per lo sviluppo dello scenario “AS IS” (Materiali Supplementari, Tab. S2 (844.1KB, pdf) ) (16-18).
In termini di strategie di trattamento, all’interno del modello è stata definita la percentuale di utilizzo, per ciascuno stadio di gravità della malattia, delle principali strategie terapeutiche attualmente utilizzate per la gestione della BPCO nel contesto sanitario italiano (Materiali Supplementari, Tab. S3 (844.1KB, pdf) ) (19). Dall’analisi della letteratura sono state inoltre identificate una percentuale generale di aderenza al trattamento farmacologico per la gestione della BPCO pari al 19,5% (10) e una specifica aderenza terapeutica per l’utilizzo delle triplici terapie fisse pari al 29,0% (11). Infine, per una rappresentazione quanto più fedele dell’attuale gestione della condizione, all’interno dello scenario “AS IS”, sulla base delle attuali evidenze in letteratura, si è definito un delay nella prescrizione delle triplici terapie pari a 12 mesi (20), il quale comporta un aumento del 60% nel numero di esacerbazioni moderate e severe (21).
Sulla base dei data input definiti per lo scenario “AS IS”, all’interno del modello sono stati definiti i parametri specifici per l’implementazione di ciascuna policy indagata. La specifica variazione dell’input caratteristico di ciascuna policy, ovvero l’aderenza terapeutica (Policy 1), l’utilizzo delle triplici terapie (Policy 2) e il ritardo nella prescrizione delle triplici terapie (Policy 3), determina la trasformazione di determinati parametri per ciascuna policy indagata, risultando essenziale per lo sviluppo dei diversi scenari “TO BE”.
Nel dettaglio, in riferimento alla Policy 1, è stata assunta, a seguito di una maggiore aderenza terapeutica, una riduzione per i pazienti aderenti delle visite ospedaliere del 18,50% (22), delle visite ambulatoriali dello 0,20% (23) e degli accessi al Pronto Soccorso (PS) del 18,50% (22) (Tab. 1). Relativamente alla Policy 2, all’interno del modello è stato assunto un maggiore utilizzo delle triplici terapie e in particolare delle triplici terapie fisse (Tab. 1). Infine, per lo sviluppo dello scenario “TO BE” relativo alla Policy 3 è stato assunto un ritardo nella prescrizione delle triplici terapie pari a 3 mesi, il quale comporta un aumento del 15% nel numero di esacerbazioni moderate e severe (21) (Tab. 1).
TABELLA 1 -.
Parametri indagati dalle tre policy all’interno dello scenario “AS IS” e dello scenario “TO BE”
| Parametri Policy 1: policy volta ad aumentare l’aderenza alle terapie prescritte | ||||||
| Scenario “AS IS” | Scenario “TO BE” | |||||
| Input | Stadio A | Stadio B | Stadio E | Stadio A | Stadio B | Stadio E |
| Aderenza alle strategie terapeutiche (%) | 19,5% | 39,5% | ||||
| Aderenza alle triplici terapie fisse (%) | 29,0% | 58,0% | ||||
| Ospedalizzazioni (n) | 0,35 | 0,41 | 0,63 | 0,29 | 0,33 | 0,51 |
| Visite ambulatoriali (n) | 1,93 | 2,52 | 3,76 | 1,93 | 2,51 | 3,75 |
| Accessi al PS (n) | 0,09 | 0,10 | 0,35 | 0,07 | 0,08 | 0,29 |
| Parametri Policy 2: policy volta a incentivare un maggiore utilizzo di triplici terapie a unico inalatore | ||||||
| Strategie terapeutiche | Scenario “AS IS” | Scenario “TO BE” | ||||
| Stadio A | Stadio B | Stadio E | Stadio A | Stadio B | Stadio E | |
| ICS/LABA | 16,20% | 19,75% | 11,63% | 16,20% | 19,75% | 11,63% |
| LABA/LAMA | 19,01% | 11,76% | 16,63% | 14,01% | 6,76% | 11,63% |
| Anticolinergici (LAMA) | 30,99% | 20,59% | 15,02% | 30,99% | 20,59% | 15,02% |
| Triplici terapie | 14,08% | 34,03% | 40,94% | 19,08% | 43,03% | 45,94% |
| • Triplici terapie fisse (ICS/LABA/LAMA) | 14,34% | 14,34% | 14,34% | 85,00% | 85,00% | 85,00% |
| • Triplici terapie estemporanee
(ICS + LABA/LAMA ICS/LABA + LAMA) |
85,66% | 85,66% | 85,66% | 15,00% | 15,00% | 15,00% |
| LABA | 4,23% | 2,94% | 2,14% | 4,23% | 2,94% | 2,14% |
| Altre terapie | 4,93% | 2,94% | 2,02% | 4,93% | 2,94% | 2,02% |
| Nessuna terapia | 10,56% | 7,99% | 11,62% | 10,56% | 3,99% | 11,62% |
| Parametri Policy 3: policy volta a una riduzione del delay prescrittivo delle triplici terapie per la popolazione eleggibile | ||||||
| Scenario “AS IS” | Scenario “TO BE” | |||||
| Input | Stadio A | Stadio B | Stadio E | Stadio A | Stadio B | Stadio E |
| Delay prescrittivo | 12 mesi | 3 mesi | ||||
|
% di aumento delle esacerbazioni
moderate/severe a seguito dell’utilizzo tardivo di triplici terapie |
60% | 15% | ||||
| Esacerbazioni moderate (n) | 0,66 | 0,64 | 3,44 | 0,47 | 0,46 | 2,47 |
| Esacerbazioni severe (n) | 0,14 | 0,16 | 0,56 | 0,10 | 0,12 | 0,40 |
Cost analysis
La valorizzazione economica degli input diretti sanitari è stata stimata attraverso l’utilizzo dei tariffari nazionali e delle fonti disponibili in letteratura che riportano i costi relativi al contesto sanitario italiano.
Nello specifico, per la definizione dei costi legati agli esami ematochimici, alle visite ambulatoriali, all’emogasanalisi, alla radiografia al torace e alla diagnostica di II livello è stato utilizzato il “Nomenclatore tariffario delle prestazioni di assistenza specialistica ambulatoriale” (24). Per la valorizzazione economica delle ospedalizzazioni è stato utilizzato lo studio condotto da Koleva D. et al. nel 2007, attualizzato al 2023 (25, 26). Tale processo ha determinato un costo unitario per le ospedalizzazioni correlate alla BPCO pari a 2.700,00 €. Per la definizione dei costi derivanti dall’insorgenza di esacerbazioni, queste ultime sono state differenziate sulla base del livello di gravità. Più nel dettaglio, alle esacerbazioni di grado moderato che richiedono il trattamento farmacologico è stato associato un costo unitario pari a 9,13 € (27), per le esacerbazioni di grado severo che richiedono l’accesso al PS è stato utilizzato un costo unitario pari a 261,35 € (28) e per le esacerbazioni di grado severo che richiedono un’ospedalizzazione è stato utilizzato il costo unitario di ospedalizzazione pari a 2.700,00 €. Infine, per la definizione dei costi legati alle diverse strategie terapeutiche utilizzabili per la gestione della BPCO, sono state utilizzate le liste di trasparenza dell’Agenzia Italiana del Farmaco (AIFA) (29, 30).
Risultati
Popolazione
Sulla base degli aspetti epidemiologici e delle probabilità di transizione definite all’interno dello studio condotto da Soriano J.B. et al. (15), si riporta nella Tabella 2 la popolazione di pazienti affetti da BPCO considerata all’interno del modello predittivo nei 5 anni di analisi (Fig. 2).
TABELLA 2 -.
Ripartizione della popolazione italiana affetta da BPCO rispetto alle Linee Guida GOLD 2023
| Anno 0 | Anno 1 | Anno 2 | Anno 3 | Anno 4 | |
|---|---|---|---|---|---|
| A | 334.576 | 423.433 | 434.292 | 465.025 | 411.422 |
| B | 339.001 | 300.392 | 308.137 | 278.324 | 332.580 |
| E | 211.544 | 161.296 | 142.692 | 141.772 | 141.118 |
Fig. 2 -.
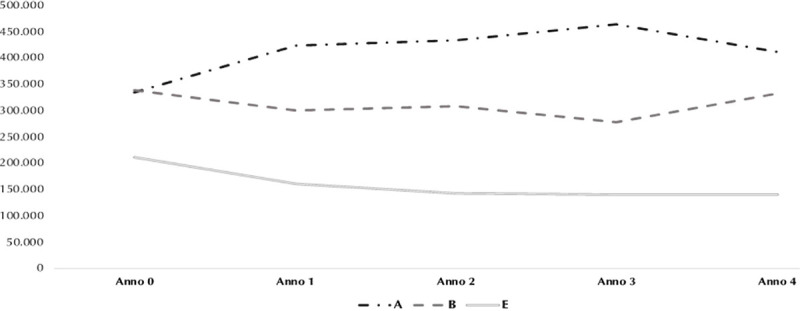
Andamento epidemiologico della popolazione nei 3 stadi di crescente gravità della BPCO nei 5 anni oggetto di analisi
Analisi di Budget Impact
I risultati derivanti dall’introduzione delle tre policy definite all’interno del presente modello predittivo hanno evidenziato un generale risparmio di risorse dirette sanitarie nei 5 anni oggetto di indagine.
Maggiori dettagli dei risultati dello scenario “AS IS” e dei tre diversi scenari “TO BE” definiti nell’analisi sono riportati in Tabella 3 e graficamente in Figura 3.
TABELLA 3 -.
Risultati dell’analisi di Analisi di Budget Impact (BIA) - comparazione dello scenario “AS IS” e dello scenario “TO BE”
| SCENARIO “AS IS” | |||||
| Anno 0 | Anno 1 | Anno 2 | Anno 3 | Anno 4 | |
| 2.075.525.281 € | 2.022.153.501 € | 1.997.696.717 € | 2.003.314.564 € | 1.990.249.147 € | |
| SCENARIO “TO BE” | |||||
| Anno 0 | Anno 1 | Anno 2 | Anno 3 | Anno 4 | |
| Policy 1 | 2.029.725.450 € | 1.981.713.424 € | 1.958.897.006 € | 1.965.299.416 € | 1.951.034.063 € |
| Policy 2 | 2.039.128.889 € | 1.995.307.151 € | 1.971.355.754 € | 1.976.768.499 € | 1.964.132.205 € |
| Policy 3 | 2.041.837.614 € | 1.986.458.704 € | 1.962.534.615 € | 1.966.365.802 € | 1.956.560.356 € |
| Implementazione simultanea delle tre policy | 1.931.863.136 € | 1.898.365.473 € | 1.878.300.224 € | 1.882.564.333 € | 1.872.461.730 € |
Fig. 3 -.
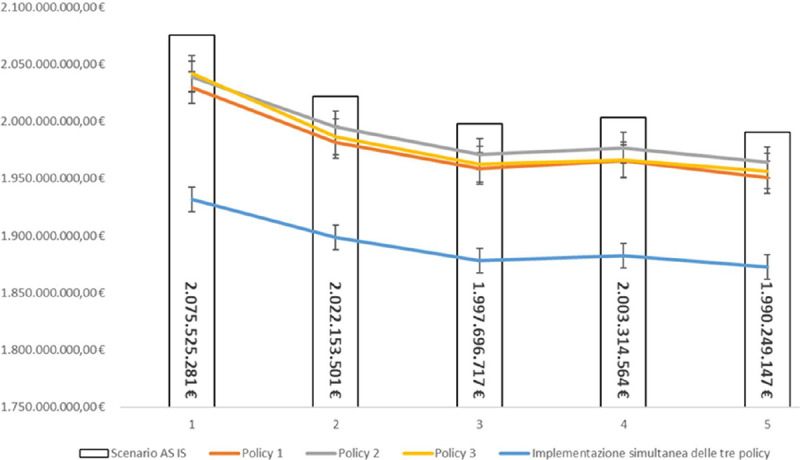
Rappresentazione grafica dei risultati dello scenario “AS IS”, dei tre scenari “TO BE” derivanti dall’implementazione della singola specifica policy indagata e dello scenario “TO BE” derivante dall’implementazione simultanea di tutte le policy indagate
Dall’analisi differenziale tra lo scenario “AS IS” e lo scenario “TO BE” relativo alla Policy 1 è emerso come nell’orizzonte temporale oggetto di analisi vi sia un costante risparmio di risorse sanitarie dirette. Più nel dettaglio, i risultati derivanti dall’introduzione della Policy 1 nel contesto sanitario italiano evidenziano un risparmio complessivo in termini economici nell’orizzonte temporale indagato pari a 202.269.852 €. Risultati simili sono emersi dall’analisi delle ulteriori due policy indagate all’interno del modello predittivo. Di fatto, l’implementazione della Policy 2 ha evidenziato un potenziale risparmio complessivo di risorse sanitarie nei 5 anni oggetto di analisi pari a 142.246.714 €. Analogamente, l’introduzione della Policy 3 ha rilevato un possibile risparmio di risorse sanitarie pari a 175.182.121 €. Infine, dal momento che ogni policy incide su parametri specifici, l’implementazione simultanea delle tre policy non comporta un impatto economico complessivo equivalente alla somma dei risultati delle singole policy. Di fatto, dall’analisi è emerso come l’implementazione simultanea delle tre policy comporti un potenziale risparmio complessivo di risorse sanitarie nei 5 anni oggetto di analisi pari a 625.384.313 €, il quale si tradurrebbe in un risparmio medio annuo del numero di ospedalizzazioni e di accessi al PS pari rispettivamente a 13.809 e 10.133.
Complessivamente, i risultati del modello predittivo suggeriscono dunque come l’introduzione delle tre policy indagate possa comportare contestualmente un miglioramento della gestione della BPCO e un generale beneficio in termini economico-organizzativi del contesto sanitario italiano.
L’impatto positivo, in termini di riduzione dei costi diretti sanitari, derivante dall’implementazione delle tre policy nel contesto sanitario italiano è stato confermato dalle tre simulazioni analitiche condotte sui principali parametri di ciascuna policy. Più nel dettaglio, dalla simulazione condotta sulla Policy 1 è emerso come, all’aumentare del livello di aderenza alle strategie terapeutiche per la gestione della BPCO, aumenti il risparmio di risorse sanitario per il SSN. Al contrario, al diminuire del livello di aderenza terapeutica si determinerebbe un aggravio economico per il SSN (Materiali Supplementari, Tab. S4 (844.1KB, pdf) ). Simili risultati sono altresì emersi dall’analisi condotta per la Policy 2 (Materiali Supplementari, Tab. S5 (844.1KB, pdf) ). Infine, dall’analisi mediante simulazione relativa al delay prescrittivo delle triplici terapie (Policy 3) è emerso come al diminuire del ritardo nelle tempistiche di prescrizione delle triplici terapie si ha un aumento dei risparmi di risorse economiche per il SSN (Materiali Supplementari, Tab. S6 (844.1KB, pdf) ).
Discussione
La BPCO è una malattia cronica dell’apparato respiratorio caratterizzata da frequenti riacutizzazioni che determinano un peggioramento del declino di funzionalità respiratoria, qualità di vita e mortalità; inoltre, spesso evolvono in ricoveri ospedalieri, comportando non solo un peggioramento della qualità della vita dei pazienti, ma anche un notevole burden economico per il contesto sanitario. Per tale ragione risulta essere di fondamentale importanza una corretta gestione della condizione. Diversi sono i fattori che determinano una buona presa in carico della BPCO, come l’incremento dell’aderenza terapeutica e un’adeguata tempistica nella definizione e nella prescrizione della strategia di trattamento.
Attualmente, nel contesto sanitario italiano, nonostante siano stati attuati programmi per una più adeguata gestione della condizione (9), i pazienti affetti da BPCO presentano ancora molteplici unmet clinical needs. Per tale ragione, al fine di ottimizzare l‘utilizzo delle già limitate risorse sanitarie, appare impellente la necessità di definire e introdurre strategie utili per migliorare la gestione dei pazienti con BPCO, in termini sia di corretta diagnosi che di percorsi terapeutici.
Per tale ragione, l’obiettivo del presente studio è stato quello di valutare l’impatto in termini economici di tre principali policy, definite sulla base degli unmet clinical needs emersi dall’analisi della letteratura corrente della BPCO, nel contesto sanitario italiano.
Dall’analisi dei risultati è emerso come la policy con un maggiore impatto in termini di benefici sia legata a una maggiore aderenza terapeutica. Dal modello si evidenzia come incentivare l’aderenza terapeutica per una migliore gestione della BPCO comporti un risparmio medio annuale per paziente in termini di costi diretti pari a 45,70 €. Simili risultati sono stati riscontrati anche a seguito dell’introduzione delle altre policy analizzate all’interno del presente studio. Di fatto, dai risultati è emerso come un’adeguata definizione della strategia terapeutica utile per la gestione della condizione e la riduzione nel ritardo di prescrizione della più adeguata terapia comportino un risparmio medio annuo per paziente rispettivamente pari a 32,14 € e 39,58 €.
Dalla valutazione complessiva delle tre policy analizzate emerge dunque come una migliore gestione della BPCO, incentivando una maggiore aderenza terapeutica, un maggiore utilizzo di strategie terapeutiche volte a promuovere l’aderenza, nonché un minor ritardo prescrittivo delle strategie terapeutiche più adeguate alla gestione di questa condizione, comportino un beneficio in termini economici per il SSN. Inoltre, un efficientamento nella presa in carico dei pazienti affetti da BPCO, favorendo un miglioramento clinico per il paziente, potrebbe comportare un impatto positivo nella potenziale produttività da esso generata e dunque un potenziale impatto positivo in termini sia sociali che fiscali. A conferma di tali considerazioni, il modello predittivo illustrato è stato progettato con la capacità di incorporare simultaneamente stime relative ai costi indiretti e fiscali, ampliando così il suo ambito di applicazione. Ad esempio, ipotizzando per ciascuna delle tre policy proposte all’interno dello studio un impatto positivo del 10% sulla riduzione delle perdite di produttività legate alla condizione dei pazienti, ai risparmi calcolati in termini di costi diretti si dovrebbero aggiungere i potenziali risparmi in termini di costi indiretti derivanti da ciascuna policy indagata, in media pari a circa 45 milioni di euro annui. Tuttavia tali approfondimenti non sono stati riportati nel dettaglio a causa della scarsità di evidenze in letteratura utili per lo sviluppo di un modello predittivo robusto rispetto alla prospettiva sociale e fiscale.
Anche se con un diverso impatto, tutte le policy analizzate hanno evidenziato a seguito della loro implementazione un risparmio in termini economici, il quale, considerando il rilevante burden epidemiologico che contraddistingue la BPCO, risulta essere di particolare rilevanza per il contesto sanitario italiano.
A nostra conoscenza, questo è il primo studio condotto con l’obiettivo di valutare l’impatto che l’introduzione di diverse policy comporterebbe nella gestione della BPCO in Italia. Esso rappresenta dunque un possibile punto di partenza per ulteriori e più dettagliate indagini sulla tematica, nonché uno strumento utile per valutare la possibile introduzione di policy che comporterebbero, in termini sia clinici che economici, maggiori benefici per i pazienti, per il SSN e per la società.
L’analisi tuttavia non è priva di limitazioni. La prima limitazione concerne il mancato inserimento all’interno del modello dei costi derivanti dall’effettiva implementazione delle diverse policy indagate. Tale approccio è stato adottato in considerazione del fatto che per l’introduzione delle policy indagate non si renderebbero necessari ingenti investimenti finanziari, ma che al contrario sarebbe sufficiente un maggiore livello di raccomandazione rispetto a tali punti all’interno delle Linee Guida internazionali e nazionali.
La seconda limitazione riguarda i dati di prevalenza usati nel modello. Per rappresentare adeguatamente l’andamento epidemiologico della BPCO in Italia, non è stato possibile utilizzare i tassi di prevalenza dei diversi stadi di gravità disponibili in letteratura. Al contrario, sono stati impiegati i tassi di prevalenza dello studio di Soriano J.B. et al. (15), che ci hanno permesso di stimare, sulla base delle probabilità di transizione, la distribuzione della popolazione nei diversi stadi di salute durante l’orizzonte temporale dello studio. Questo approccio, validato da un panel di esperti della condizione nel contesto sanitario italiano, ha assicurato un allineamento con il modello comportamentale proposto dagli autori dello studio, garantendo coerenza e affidabilità nelle stime di prevalenza della malattia. La terza limitazione riguarda i tassi di incidenza e mortalità della BPCO. A causa della natura cronica della patologia, non esistono studi internazionali o nazionali che consentano di stimare un tasso di incidenza della condizione. Pertanto, basandoci su un’analisi temporale della prevalenza, abbiamo assunto un andamento parallelo tra il tasso di incidenza e il tasso di mortalità della BPCO. La quarta limitazione è legata alla scarsa disponibilità di evidenze scientifiche specifiche per il contesto italiano. Di fatto, in assenza di studi specifici per l’Italia, all’interno del modello sono stati introdotti parametri provenienti da altri contesti internazionali. Tuttavia, per limitare il più possibile tale bias, abbiamo identificato dati relativi ad aree geografiche che potessero fornire stime ragionevolmente coerenti anche per il contesto italiano. La quinta limitazione dello studio è correlata alla necessità di allineare le evidenze scientifiche identificate in letteratura e utilizzate all’interno dell’analisi con le nuove raccomandazioni GOLD 2023 (3). Con tale obiettivo, per rappresentare i dati della nuova classe di rischio E, si è proceduto ad aggregare le informazioni identificate in letteratura relative alle classi C e D. Tale approccio ha lo scopo al contempo di semplificare la classificazione dei pazienti e di riflettere adeguatamente le raccomandazioni attuali per la gestione e il trattamento della BPCO. La sesta limitazione dello studio è legata ai parametri che variano a seguito dell’implementazione delle policy e che dunque incidono sui risultati. Di fatto, l’implementazione di ciascuna policy determina la variazione di specifici parametri e non dell’intero data input incluso nel modello. Infine, l’ultima limitazione dello studio riguarda la mancata valutazione del beneficio economico indiretto derivante dall’implementazione delle diverse policy, portando a una possibile sottostima dei risultati. Di fatto, il modello considera esclusivamente le variazioni economiche dirette legate ai parametri inclusi nell’analisi, senza tenere conto degli ulteriori benefici che una gestione più efficace della condizione e un miglioramento della qualità di vita dei pazienti potrebbero comportare. Ad esempio, un aumento dell’aderenza terapeutica ridurrebbe le ospedalizzazioni, come previsto dal modello. Tuttavia, la riduzione delle ospedalizzazioni non solo comporterebbe una riduzione dei costi ospedalieri diretti, ma rallenterebbe anche l’evoluzione della malattia, generando ulteriori risparmi grazie ad una gestione più efficiente della patologia e ad una riduzione di interventi futuri.
Conclusioni
L’analisi presentata ha dimostrato come l’implementazione di policy volte a migliorare la gestione della BPCO, e in particolare una maggiore aderenza terapeutica comporterebbe non solo un efficientamento in termini economici e organizzativi del contesto sanitario italiano, ma anche un potenziale miglioramento in termini di qualità della vita dei pazienti, grazie alla diminuzione degli eventi acuti e delle ospedalizzazioni.
Il presente studio può essere considerato un punto di partenza sia per l’identificazione che per la misurazione degli elementi che influenzano maggiormente policy volte a un efficientamento nella gestione della BPCO. Ciò al fine di definire priorità di intervento e di orientare le decisioni. Modelli come questo possono rappresentare uno strumento prezioso per i policy maker nel settore sanitario, offrendo la possibilità di ottimizzare l’allocazione delle risorse nell’ambito della gestione delle patologie croniche, che rappresentano una delle voci più importanti di spesa per il SSN. Attraverso l’impiego di questi modelli predittivi, è possibile identificare con maggiore precisione le aree di intervento prioritario, contribuendo significativamente all’efficienza del sistema sanitario nel suo complesso e migliorando l’outcome dei pazienti.
Funding Statement
Financial support: The realization of this research was financed with an unconditional contribution from AstraZeneca S.p.A.
AstraZeneca S.p.A. was not involved in the conduct of the study, the collection, analysis, interpretation of the data, the writing of this article or the decision to submit it for publication.
Footnotes
Conflict of interest: The Authors declare no conflict of interest.
This article includes Supplementary Material
Bibliografia
- 1.Istituto Superiore di Sanità (ISS), - EpiCentro – L’epidemiologia per la sanità pubblica. Broncopneumopatia cronica ostruttiva. [Accessed May; 2024 ]. Online
- 2.National Heart, Lung, and Blood Institute. What is COPD? [Accessed May; 2024 ]. Online
- 3.Global Initiative for Chronic Obstructive Lung Disease. Global strategy for prevention, diagnosis and management of COPD: 2023 Report. [Accessed May; 2024 ]. Online
- 4.Rapporto Osservasalute 2022. Stato di salute e qualità dell’assistenza nelle regioni italiane. [Accessed May; 2024 ]. Online
- 5.National Institute for Health and Care Excellence (NICE). Chronic obstructive pulmonary disease in over 16s: diagnosis and management. [Accessed May; 2024 ]. Online [PubMed]
- 6.Ministero della Salute. La continuità assistenziale: Broncopneumopatia Cronica Ostruttiva (BPCO). [Accessed May; 2024 ]. Online
- 7.IQVIA. Gestione della BPCO in Italia: impatto della pandemia e della Nota 99 sull’assistenza terapeutica. [Accessed May; 2024 ]. Online
- 8.National Heart, Lung, and Blood Institute. Treatment COPD. [Accessed May; 2024 ]. OnlineOnline
- 9.Agenzia Italiana del Farmaco (AIFA). AIFA pubblica la Nota 99 per la prescrizione dei farmaci per la BPCO. [Accessed May; 2024 ]. Online
- 10.Agenzia Italiana del Farmaco (AIFA). L’uso dei farmaci in Italia – Rapporto Nazionale Anno 2022. [Accessed May; 2024 ]. Online
- 11.Mannino D, Bogart M, Wu B et al. Adherence and persistence to once-daily single-inhaler versus multiple-inhaler triple therapy among patients with chronic obstructive pulmonary disease in the USA: A real-world study. Respir Med. 2022;197:106807. doi: 10.1016/j.rmed.2022.106807. [DOI] [PubMed] [Google Scholar]
- 12.Agenzia Italiana del Farmaco (AIFA). Aderenza alle terapie e strategie per migliorare l’uso sicuro ed efficace dei farmaci. [Accessed May; 2024 ]. Online
- 13.Istituto Nazionale di Statistica (ISTAT). Popolazione residente al 1° gennaio: Per fascia di età. [Accessed May; 2024 ]. Online
- 14.Global Initiative for Chronic Obstructive Lung Disease. Strategia Globale per la diagnosi, il trattamento e la prevenzione della BPCO – Revisione 2017. [Accessed May; 2024 ]. Online
- 15.Soriano JB, Hahsler M, Soriano C et al. CHAIN investigators. Temporal transitions in COPD severity stages within the GOLD 2017 classification system. Respir Med. 2018;142:81–85. doi: 10.1016/j.rmed.2018.07.019. [DOI] [PubMed] [Google Scholar]
- 16.Wallace AE, Kaila S, Bayer V et al. Health Care Resource Utilization and Exacerbation Rates in Patients with COPD Stratified by Disease Severity in a Commercially Insured Population. J Manag Care Spec Pharm. 2019;25(2):205–217. doi: 10.18553/jmcp.2019.25.2.205. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 17.Johansson G, Mushnikov V, Bäckström T et al. Exacerbations and healthcare resource utilization among COPD patients in a Swedish registry-based nation-wide study. BMC Pulm Med. 2018 Jan 25;18(1):17. doi: 10.1186/s12890-018-0573-0. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 18.Miravitlles M, Kostikas K, Bizymi N, Tzanakis N. A Novel Figure and Algorithm for the Gold ABE Classification. Arch Bronconeumol. 2023;59(11):702–704. doi: 10.1016/j.arbres.2023.06.001. [DOI] [PubMed] [Google Scholar]
- 19.Palmiotti GA, Lacedonia D, Liotino V et al. Adherence to GOLD guidelines in real-life COPD management in the Puglia region of Italy. Int J Chron Obstruct Pulmon Dis. 2018;13:2455–2462. doi: 10.2147/COPD.S157779. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 20.Agenzia Italiana del Farmaco (AIFA). Domande e risposte relative all’applicazione della Nota 99 per la prescrizione dei farmaci inalatori indicati nella terapia di mantenimento della BPCO. [Accessed May; 2024 ]. Online
- 21.Weir DL, Bai YQ, Thavorn K, Guilcher S et al. Non-adherence to COPD medications and its association with adverse events: A longitudinal population based cohort study of older adults. Ann Epidemiol. 2024 Aug;96:88–96. doi: 10.1016/j.annepidem.2023.12.003. [DOI] [PubMed] [Google Scholar]
- 22.Toy EL, Beaulieu NU, McHale JM et al. Treatment of COPD: relationships between daily dosing frequency, adherence, resource use, and costs. Respir Med. 2011;105(3):435–441. doi: 10.1016/j.rmed.2010.09.006. [DOI] [PubMed] [Google Scholar]
- 23.Strange C, Tkacz J, Schinkel J et al. Exacerbations and Real-World Outcomes After Single-Inhaler Triple Therapy of Budesonide/Glycopyrrolate/Formoterol Fumarate, Among Patients with COPD: results from the EROS (US) Study. Int J Chron Obstruct Pulmon Dis. 2023;18:2245–2256. doi: 10.2147/COPD.S432963. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 24.Ministero della Salute. Tariffario delle prestazioni di assistenza ambulatoriale. [Accessed May; 2024 ]. Online
- 25.Koleva D, Motterlini N, Banfi P, Garattini L. Study Group BIC. Healthcare costs of COPD in Italian referral centres: a prospective study. Respir Med. 2007;101(11):2312–2320. doi: 10.1016/j.rmed.2007.06.020. [DOI] [PubMed] [Google Scholar]
- 26.Istituto Nazionale di Statistica (ISTAT). Rivalutazioni e documentazione su prezzi, costi e retribuzioni contrattuali. [Accessed May; 2024 ]. Online
- 27.Kendall R, Martin AA, Shah D, Shukla S, Compton C, Ismaila AS. Cost-Effectiveness of Single-Inhaler Triple Therapy (FF/UMEC/VI) versus Tiotropium Monotherapy in Patients with Symptomatic Moderate-to-Very Severe COPD in the UK. Int J Chron Obstruct Pulmon Dis. 2023;18:1815–1825. doi: 10.2147/COPD.S400707. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 28.Rettifica decreto commissariale N°U00265 1° settembre 2014. [Accessed May; 2024 ]. Online
- 29.Agenzia Italiana del Farmaco (AIFA). Elenco dei Farmaci di Fascia A per principio attivo. [Accessed May; 2024 ]. Online
- 30.Agenzia Italiana del Farmaco (AIFA). Elenco dei Farmaci di Fascia H per principio attivo. [Accessed May; 2024 ]. Online
Associated Data
This section collects any data citations, data availability statements, or supplementary materials included in this article.


