Resumen
El programa de «Elaboración de guías de práctica clínica en enfermedades digestivas, desde la atención primaria a la especializada» es un proyecto compartido por la Asociación Española de Gastroenterología (AEG), la Sociedad Española de Medicina de Familia y Comunitaria (semFYC) y el Centro Cochrane Iberoamericano (CCI). Presentamos la actualización de la guía sobre el manejo de la dispepsia que se publicó en el año 2003. En su elaboración se han tenido en cuenta los criterios esenciales contemplados en el instrumento Appraisal of Guidelines, Research and Evaluation for Europe (AGREE). Para clasificar la evidencia científica y fuerza de las recomendaciones se ha utilizado el sistema Grading of Recommendations Assessment, Development and Evaluation Working Group (GRADE).
Palabras clave: Guía de práctica clínica, Dispepsia, Manejo
Abstract
The “Preparation of Clinical Practice Guidelines in Digestive Diseases, from Primary Care to Specialist Care” Program, is a joint project by the Spanish Gastroenterology Association (AEG), the Spanish Society of Family and Community Medicine (SEMFyC), and the IberoAmerican Cochrane Center (CCI). We present the update of the Guidelines on the Management of Dyspepsia, which was published in 2003. The essential criteria provided in the AGREE (Appraisal of Guidelines, Research and Evaluation for Europe) Instrument were taken into account in the preparation of this document. The GRADE (Grading of Recommendations Assessment, Development and Evaluation) system was used to classify the scientific evidence and strengthen the recommendations.
Keywords: Clinical practice guideline, Dyspepsia, Management
Introducción
La dispepsia es un término que se utiliza ampliamente para describir cualquier tipo de molestia gastrointestinal. Distintos expertos han tratado de uniformizar este concepto, destacando la naturaleza crónica y la presencia de malestar o dolor abdominal centrado en el hemiabdomen superior1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12. Las definiciones y criterios de dispepsia utilizados en la guía de práctica clínica (GPC) que presentamos se describen en la tabla 17, 8, 9.
Tabla 1.
Definiciones y criterios de dispepsia utilizados en la guía de práctica clínica
| Dispepsia: presencia en hemiabdomen superior o retroesternal de dolor, molestia, ardor, náuseas, vómito o cualquier otro síntoma que se considere originado en el tracto gastrointestinal superior |
| Dispepsia no investigada: dispepsia (de acuerdo con la definición anterior) en ausencia de estudio diagnóstico |
| Dispepsia orgánica o de causa conocida: dispepsia (de acuerdo con la definición anterior) en la que se ha detectado alguna causa que razonablemente justifique los síntomas |
| Dispepsia funcional (criterios de acuerdo con la clasificación de Roma III): «síntoma o conjunto de síntomas que la mayoría de médicos considera que tienen su origen en la región gastroduodenal, siendo estos síntomas la pesadez posprandial, saciedad precoz, dolor y ardor epigástrico». Los síntomas pueden ser continuos o intermitentes y estar o no relacionados con la ingesta de alimentos. Los síntomas deben haber aparecido al menos 6 meses antes del diagnóstico y estar activos durante al menos 3 meses. Requiere un estudio diagnóstico adecuado que incluya, al menos, una endoscopia normal y la ausencia de infección por Helicobacter pylori y que excluya cualquier enfermedad orgánica, sistémica o metabólica que justifique los síntomas |
La dispepsia es un motivo de consulta común, tanto en la consulta de medicina de familia como en la de atención especializada. Su elevada frecuencia conlleva un consumo considerable de recursos sanitarios y tiene un impacto importante sobre la calidad de vida y la productividad laboral.
Los síntomas dispépticos ocasionales se presentan a menudo en individuos sanos y la mayoría de las veces carecen de significado patológico. Definir qué síntomas dispépticos son banales y cuáles merecen evaluación y tratamiento no siempre es fácil. Generalmente es el propio paciente el que decide qué síntomas dispépticos son lo suficientemente molestos como para consultar al médico.
Epidemiología
Magnitud del problema
La prevalencia de la dispepsia se estima entre el 23 y el 45% cuando se utiliza una definición amplia (síntomas gastrointestinales en abdomen superior) y del 7 al 34% cuando se define como «dolor en el abdomen superior»13, 14, 15, 16. Con esta definición amplia, un estudio realizado en España estima que el 39% de la población ha presentado síntomas dispépticos alguna vez en su vida y el 24% en los últimos 6 meses16.
El porcentaje de consultas por síntomas dispépticos es muy variable (entre el 26 y el 70%) y guarda relación con los factores asociados de manera consistente (nivel socioeconómico bajo e infección por Helicobacter pylori)17, 18. Los estudios realizados en nuestro medio estiman una prevalencia del 8% de las consultas en atención primaria.
Este amplio abanico de resultados se explica por la gran variabilidad, tanto en la descripción de los síntomas por parte de los pacientes, como en su interpretación por parte de los profesionales sanitarios.
Factores de riesgo
Los fármacos, especialmente los antiinflamatorios no esteroideos (AINE), son una causa frecuente de dispepsia15. También se han relacionado los síntomas dispépticos con las situaciones de estrés y con la ansiedad, especialmente en el caso de la dispepsia funcional15. Los estudios disponibles no consideran que la edad, el tabaco y la ingesta regular de alcohol sean factores de riesgo asociados a la dispepsia15.
Los factores asociados a la dispepsia funcional no están claramente establecidos2, 11, 19. Entre los mecanismos propuestos se incluyen alteraciones de la función motora y de la sensibilidad visceral, mecanismos relacionados con la respuesta a las infecciones o a alteraciones de la inmunidad o manifestaciones de desajustes psicológicos. Algunos estudios también sugieren una cierta predisposición genética.
Los AINE y la aspirina (ácido acetilsalicílico, AAS) incrementan el riesgo de úlcera péptica. Una revisión sistemática identifica, como factores de riesgo de úlcera péptica entre las personas que utilizan AINE, la historia de úlcera péptica, la edad mayor de 60 años, el uso de anticoagulantes o de corticosteroides, y la utilización simultánea de múltiples AINE y/o AAS20.
La infección por H. pylori se asocia estrechamente con la úlcera duodenal y gástrica21, 22. Entre un 10 y un 20% de los individuos infectados por H. pylori desarrollarán una úlcera péptica en algún momento de su vida. La respuesta individual a esta infección guarda relación con las diferencias genéticas de los individuos, la virulencia del propio microorganismo y los factores ambientales.
Aproximación inicial al paciente con síntomas dispépticos
Las actuaciones propuestas son fruto del consenso entre los diferentes autores y revisores de la guía. Para establecer la calidad de la evidencia científica y la fuerza de las recomendaciones se han seguido las etapas propuestas por el sistema GRADE23, 24, 25. Se han tenido en cuenta las características de nuestra población, con una gran prevalencia de infección por H. pylori, y de nuestro sistema sanitario, incluidos los recursos diagnósticos disponibles.
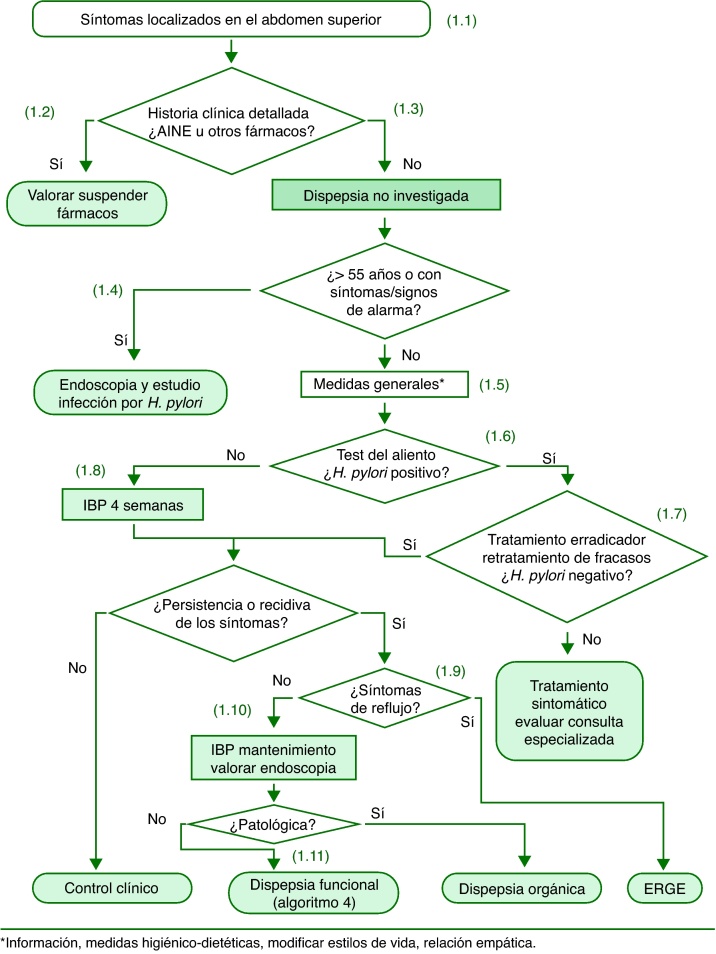
Dispepsia no investigada (fig. 1)
Figura 1.
Algoritmo de la dispepsia no investigada.
Cualquier síntoma localizado en el abdomen superior incluyendo dolor o malestar, ardor, náuseas o vómitos, debe orientar a un diagnóstico inicial de dispepsia no investigada. En los pacientes con dispepsia no investigada, la superposición de síntomas y enfermedades justifica recomendar la aplicación de una estrategia de abordaje común, sin excluir a los pacientes con síntomas inditivos de enfermedad por reflujo gastroesofágico (ERGE).
En el caso de la dispepsia asociada con AINE y/o AAS se recomienda, si es posible, la supresión del fármaco y/o asociar un antisecretor. Si tras suspender los fármacos y después de un período razonable persisten los síntomas, se puede orientar el cuadro como una dispepsia no investigada y aplicar el algoritmo correspondiente.
La historia clínica detallada debe incluir preguntas sobre estilos de vida, toma de fármacos, sobre todo AINE y/o AAS, y antecedentes personales (úlcera péptica previa, cirugía gástrica, cáncer gástrico, infección por H. pylori, entre otros) y/o familiares significativos.
En los pacientes con uno o más síntomas y signos de alarma y en los pacientes cuyos síntomas se han iniciado a una edad mayor de 55 años, aun en ausencia de síntomas de alarma, se recomienda una endoscopia digestiva alta para descartar una neoplasia gastroesofágica.
En los pacientes con dispepsia no investigada se recomienda dejar de fumar, reducir la ingesta de alcohol y tratar el sobrepeso como medidas higiénico-dietéticas coadyuvantes al tratamiento específico.
En los pacientes con dispepsia no investigada menores de 55 años y sin signos ni síntomas de alarma se recomienda la estrategia «test and treat», consistente en realizar una prueba del aliento con urea marcada con 13C. En caso de que exista un tiempo de espera prolongado para realizar la prueba se puede optar por administrar antiácidos hasta la realización de la prueba del aliento o, si el control sintomático es inadecuado con antiácidos, tratamiento con inhibidores de la bomba de protones (IBP) durante 4 semanas y realizar la prueba del aliento tras haber suspendido este tratamiento al menos durante 14 días.
En los pacientes infectados por H. pylori se debe administrar tratamiento erradicador. Se recomienda control mediante prueba del aliento y retratamiento de todos los pacientes con infección persistente después del tratamiento erradicador inicial. Tras 2 fracasos del tratamiento debe valorarse cuidadosamente la indicación del tratamiento erradicador conjuntamente con el paciente y la posibilidad de remisión a una unidad especializada.
En los pacientes no infectados por H. pylori se debe administrar un tratamiento antisecretor con IBP durante 4 semanas.
La persistencia de los síntomas de reflujo (pirosis y regurgitación) en ausencia o tras la curación de la infección por H. pylori debe de orientar a ERGE.
La posibilidad de endoscopia debe valorarse en función de la sintomatología y del riesgo subyacente de enfermedad grave, especialmente neoplásica. Se sugiere mantener un gran índice de sospecha clínica y no retrasar excesivamente la endoscopia en pacientes con síntomas recurrentes.
La endoscopia normal en pacientes con síntomas dispépticos recurrentes nos permitirá establecer el diagnóstico de dispepsia funcional. Podría ser razonable incluir la práctica de una biopsia de duodeno para descartar una enteropatía sensible al gluten, aunque actualmente no queda claro que sea una práctica coste-efectiva.
Tratamiento erradicador de la infección por Helicobacter pylori
Antes de iniciar el tratamiento erradicador de H. pylori se ha de preguntar al paciente si es alérgico a la penicilina.
Dependiendo de las tasas locales de resistencia de H. pylori a la claritromicina y de la eficacia local del tratamiento triple, se recomendarán diferentes estrategias.
Se recomienda como tratamiento erradicador de primera elección la terapia triple clásica (IBP, claritromicina [500 mg/12 h] + amoxicilina [1 g/12 h]) durante un período de 10 a 14 días.
Se recomienda que los IBP se administren en dosis dobles y con una pauta de dos veces al día.
En pacientes que viven en áreas con gran tasa de resistencia a la claritromicina (> 15-20%) o donde la eficacia de la triple terapia es baja (< 80%) se sugiere como primera elección la terapia cuádruple, preferentemente sin bismuto «concomitante» (IBP [dosis estándar/12 h] + claritromicina [500 mg/12 h] + amoxicilina [1 g/12 h] + metronidazol [500/12 h], durante 10 días) o bien la cuádruple clásica con bismuto (IBP [dosis estándar/12 h] + bismuto [120 mg/6 h] + tetraciclina [500 mg/6 h] + metronidazol [500/8 h], durante 7-14 días).
Si fracasa el tratamiento inicial se recomienda como terapia de rescate (segunda línea) el tratamiento triple con levofloxacino (IBP [dosis estándar/12 h] + amoxicilina [1 g/12 h] + levofloxacino [500/12-24 h]; durante 10 días).
Tras 2 fracasos del tratamiento erradicador, se sugiere derivar al paciente a un centro especializado para valorar la necesidad de recibir un tratamiento de tercera línea y/o efectuar un tratamiento sintomático.
Tratamiento erradicador de la infección por Helicobacter pylori en pacientes alérgicos a la penicilina
Dependiendo de las tasas locales de resistencia de H. pylori a claritromicina, se recomendarán diferentes estrategias.
En pacientes alérgicos a la penicilina se sugiere como tratamiento erradicador el empleo de un IBP, claritromicina y metronidazol (IBP [dosis doble/12 h] + claritromicina [500 mg/12 h] + metronidazol [500 mg/12 h], durante 10-14 días).
En pacientes alérgicos a la penicilina de áreas con gran tasa de resistencia a la claritromicina (> 15-20%) o donde la eficacia de la triple terapia es baja (< 80%) se sugiere como tratamiento erradicador de primera elección la terapia cuádruple «clásica» (IBP [dosis estándar/12 h] + bismuto [120 mg/6 h] + tetraciclina [500 mg/6 h] + metronidazol [500/8 h], duración de 7-14 días).
Tras un fracaso del tratamiento erradicador, se sugiere derivar al paciente alérgico a la penicilina a un centro especializado para valorar la necesidad de recibir un tratamiento de segunda línea.
Seguimiento posterior al tratamiento erradicador
Tras el tratamiento erradicador se recomienda evaluar la curación de la infección mediante una prueba del aliento, siempre que sea posible.
En los pacientes con úlcera duodenal que reciben tratamiento erradicador de H. pylori se recomienda prescribir el IBP únicamente durante el período de administración de los antibióticos.
En los pacientes con úlcera gástrica de gran tamaño (> 1 cm) se recomienda que, tras haber finalizado el tratamiento erradicador, se prolongue el tratamiento con IBP entre 4 y 8 semanas.
En los pacientes con úlcera gástrica de pequeño tamaño (≤ 1 cm) se sugiere que, tras haber finalizado el tratamiento erradicador, no se prolongue el tratamiento con IBP.
En los pacientes con hemorragia digestiva por úlcera péptica, una vez confirmada la curación de la infección por H. pylori, no se recomienda administrar tratamiento de mantenimiento con IBP.
Recomendaciones prácticas para el tratamiento de la dispepsia funcional
El diagnóstico de dispepsia funcional incluye la exclusión razonable de cualquier causa de dispepsia orgánica, entre ellas la infección por H. pylori.
En pacientes infectados con endoscopia normal se recomienda descartar o curar la infección por H. pylori antes de establecer el diagnóstico de dispepsia funcional. Esta estrategia induce un número limitado pero significativo de remisiones a largo plazo.
Es importante proporcionar una adecuada información al paciente sobre la naturaleza benigna y crónica de su problema de salud, y de cómo pueden influir los tratamientos propuestos en la mejora de sus síntomas. También deben recomendarse las medidas higiénico-dietéticas adecuadas y si es necesario las modificaciones de los estilos de vida. Finalmente, es muy importante establecer una relación médico-paciente empática.
El tratamiento farmacológico está orientado a la resolución de los episodios sintomáticos. Como opción terapéutica de primera línea se recomiendan los antisecretores, especialmente los IBP en dosis estándar durante 4 semanas. En pacientes con síndrome de distrés posprandial, con predominio de la distensión y la saciedad precoz, se recomienda administrar un procinético.
Si la respuesta al tratamiento inicial es satisfactoria, iniciar la retirada del fármaco. Ante una nueva recidiva de los síntomas valorar la utilización del mismo fármaco en forma de tratamiento a demanda o intermitente.
Si la respuesta a los IBP no es satisfactoria se ha de tranquilizar al paciente, insistir en las medidas higiénico-dietéticas, y aumentar la dosis del fármaco. También son opciones aceptables realizar tratamiento inicial con IBP en todos los pacientes o empezar con la combinación de un IBP y un procinético. Se recomienda ensayar siempre la combinación de IBP en dosis altas asociado a un procinético antes de iniciar fármacos psicotrópicos.
En pacientes con dispepsia funcional y síntomas resistentes al tratamiento de primera línea y a la combinación de IBP y procinéticos se sugiere considerar el uso de antidepresivos. Si los síntomas no ceden o no mejoran, es necesario reevaluar al paciente, valorar la necesidad de estudios adicionales y/o la derivación a atención especializada. En caso de sintomatología psiquiátrica evidente se debería considerar la evaluación por parte del psiquiatra.
Fuentes de financiación
Esta guía de práctica clínica ha contado con la financiación externa de Laboratorios Almirall-Prodesfarma. Los patrocinadores no han influido en ninguna etapa de su elaboración.
Conflicto de interés
- Pablo Alonso Coello: no tiene conflictos de interés.
- Javier P. Gisbert: asesoramiento científico, soporte para investigación y actividades formativas: Almirall, Janssen-Cilag, Nycomed, AstraZeneca, Pfizer, MSD, Abbott, Ferring, Faes, Shire, Chiesi, Casen, Otsuka, Uriach, Dr. Falk.
- Xaviet Calvet Calvo: asesoramiento científico: Astra Zeneca, Pfizzer, Uriach- Prodesfarma, MSD, Abbott. Soporte para investigación: Janssen-Cilag. Actividades formativas: Astra-Zeneca, Almirall-Prodesfarma, Schering-Plough, Shire.
- Juan Ferrandiz Santos: no tiene conflictos de interés.
- Juan José Mascort Roca: no tiene conflictos de interés.
- Mercè Marzo Castillejo: no tiene conflictos de interés.
Bibliografía
- 1.Grupo de trabajo de la guía de práctica clínica sobre dispepsia. Manejo del paciente con dispepsia. Guía de práctica clínica. Barcelona: Asociación Española de Gastroenterología, Sociedad Española de Medicina de Familia y Comunitaria y Centro Cochrane Iberoamericano; Actualización 2011. Programa de Elaboración de Guías de Práctica Clínica en Enfermedades Digestivas, desde la Atención Primaria a la Especializada; p. 3.
- 2.Talley N.J., Choung R.S. Whither dyspepsia? A historical perspective of functional dyspepsia, and concepts of pathogenesis and therapy in 2009. J Gastroenterol Hepatol. 2009;24(Suppl. 3):S20–S28. doi: 10.1111/j.1440-1746.2009.06067.x. [DOI] [PubMed] [Google Scholar]
- 3.Scottish Intercollegiate Guidelines Network (SIGN) SIGN (SIGN publication n.° 67); Edinburgh: 2007. Dyspepsia. A national clinical guideline. [Google Scholar]
- 4.Talleg N.J. American Gastroenterological Association Medical Position Statement: Evaluation of dyspepsia. Gastroenterology. 2005;129:1753–1755. doi: 10.1053/j.gastro.2005.09.019. [DOI] [PubMed] [Google Scholar]
- 5.Veldhuyzen van Zanten S.J., Bradette M., Chiba N., Armstrong D., Barkun A., Flook N. Evidence-based recommendations for short and long term management of uninvestigated dyspepsia in primary care: an update of the Canadian Dyspepsia Working Group (CanDys) clinical management tool. Can J Gastroenterol. 2005;19:285–303. doi: 10.1155/2005/674607. [DOI] [PubMed] [Google Scholar]
- 6.Dyspepsia – Management of Dyspepsia in Adults in Primary Care – Full Guidelines CG17 2004. London: NICE [consultado 10 Nov 2010]. Disponible en: http://www.nice.org.uk/page.aspx?o=218381
- 7.Heading R.C. Definitions of dyspepsia. Scand J Gastroenterol Suppl. 1991;182:1–6. doi: 10.3109/00365529109109529. [DOI] [PubMed] [Google Scholar]
- 8.Tack J., Talley N.J., Camilleri M., Holtmann G., Hu P., Malagelada J.R. Functional gastroduodenal disorders: a working team report for the Rome III consensus on functional gastrointestinal disorders. Gastroenterology. 2006;130:1466–1479. doi: 10.1053/j.gastro.2005.11.059. [DOI] [PubMed] [Google Scholar]
- 9.Drossman D.A. The functional gastrointestinal disorders and the Rome III process. Gastroenterology. 2006;130:1377–1390. doi: 10.1053/j.gastro.2006.03.008. [DOI] [PubMed] [Google Scholar]
- 10.Kellow J.E. Organic causes of dyspepsia, and discriminating functional from organic dyspepsia. Best Pract Res Clin Gastroenterol. 2001;15:477–487. doi: 10.1016/s0950-3528(98)90019-7. [DOI] [PubMed] [Google Scholar]
- 11.Longstreth GF. Approach to the patient with dyspepsia. Editor Talley NJ. This topic last updated: july 22, 2010. Uptodate. http://www.uptodate.com/home/index.html
- 12.van Kerkhoven L.A., Laheij R.J., Meineche-Schmidt V., Veldhuyzen-van Zanten S.J., de Wit N.J., Jansen J.B. Functional dyspepsia: not all roads seem to lead to Rome. J Clin Gastroenterol. 2009;43:118–122. doi: 10.1097/MCG.0b013e31815591f7. [DOI] [PubMed] [Google Scholar]
- 13.Heading R.C. Prevalence of upper gastrointestinal symptoms in the general population: a systematic review. Scand J Gastroenterol Suppl. 1999;231:3–8. [PubMed] [Google Scholar]
- 14.El-Serag H.B., Talley N.J. Systemic review: the prevalence and clinical course of functional dyspepsia. Aliment Pharmacol Ther. 2004;19:643–654. doi: 10.1111/j.1365-2036.2004.01897.x. [DOI] [PubMed] [Google Scholar]
- 15.Mahadeva S., Goh K.L. Epidemiology of functional dyspepsia: a global perspective. World J Gastroenterol. 2006;12:2661–2666. doi: 10.3748/wjg.v12.i17.2661. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 16.Caballero Plasencia A.M., Sofos Kontoyannis S., Martín Ruiz J.L., Valenzuela Barranco M. La prevalencia de la dispepsia en España. Med Clin (Barc) 1994;103:717. [PubMed] [Google Scholar]
- 17.Talley N.J. Dyspepsia: management guidelines for the millennium. Gut. 2002;50(Suppl. 4):72–78. doi: 10.1136/gut.50.suppl_4.iv72. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 18.Hungin A.P., Hill C., Raghunath A. Systematic review: frequency and reasons for consultation for gastro-oesophageal reflux disease and dyspepsia. Aliment Pharmacol Ther. 2009;15:331–342. doi: 10.1111/j.1365-2036.2009.04047.x. [DOI] [PubMed] [Google Scholar]
- 19.Mimidis K., Tack J. Pathogenesis of dyspepsia. Dig Dis. 2008;26:194–202. doi: 10.1159/000121346. [DOI] [PubMed] [Google Scholar]
- 20.Tielemans M.M., Eikendal T., Jansen J.B., van Oijen M.G. Identification of NSAID users at risk for gastrointestinal complications: a systematic review of current guidelines and consensus agreements. Drug Saf. 2010;33:443–453. doi: 10.2165/11534590-000000000-00000. [DOI] [PubMed] [Google Scholar]
- 21.Furuta T., Delchier J.C. Helicobacter pylori and non-malignant diseases. Helicobacter. 2009;14(Suppl. 1):29–35. doi: 10.1111/j.1523-5378.2009.00697.x. [DOI] [PubMed] [Google Scholar]
- 22.McColl K.E. Clinical practice. Helicobacter pylori infection. N Engl J Med. 2010;362:1597–1604. doi: 10.1056/NEJMcp1001110. [DOI] [PubMed] [Google Scholar]
- 23.Working Group Rating quality of evidence and strength of recommendations GRADE: an emerging consensus on rating quality of evidence and strength of recommendations. BMJ. 2008;336:924–926. doi: 10.1136/bmj.39489.470347.AD. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 24.Marzo Castillejo M., Montaño Barrientos A. El sistema GRADE para la toma de decisiones clínicas y la elaboración de recomendaciones y guías de práctica clínica. Aten Primaria. 2007;39:457–460. doi: 10.1157/13109491. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 25.Gisbert J.P., Alonso-Coello P., Piqué J.M. How can we find, design, evaluate and use clinical practice guidelines? Gastroenterol Hepatol. 2008;31:239–257. doi: 10.1157/13117903. [DOI] [PubMed] [Google Scholar]