Zusammenfassung
Die Verwendung eines extrakorporalen Unterstützungsystems stellt bei kardialem und/oder pulmonalem Versagen eine etablierte Therapieoption dar. Auch wenn die wissenschaftliche Evidenz quantitativ noch nicht ausreichend gesichert ist, gibt es zunehmend Hinweise aus einzelnen Studien [z. B. Conventional Ventilation or ECMO for Severe Adult Respiratory Failure (CESAR) Trial], dass die „extracorporeal membrane oxygenation“ (ECMO) als pumpenbetriebenes venovenöses Verfahren beim schweren Lungenversagen eine lebensrettende Maßnahme ist. Initial als „rescue option“ beim kardialen Versagen nach Kardiotomie etabliert, erfährt der „extracorporeal life support“ (ECLS) zunehmende Verbreitung als pumpenbetriebenes venoarterielles Herz-Kreislauf-Unterstützungsystem im kardiogenen Schock bei Myokardinfarkt, als „Bridging“-Maßnahme zur Transplantation und im Rahmen einer erweiterten Reanimation. Der „pumpless extracorporeal lung assist“ (pECLA) als pumpenloses arteriovenöses Verfahren ist technisch einfacher zu handhaben, garantiert jedoch nur eine suffiziente Decarboxylierung ohne ausreichende Oxygenierung. Daher wird dieses Verfahren insbesondere im Rahmen eines primär hyperkapnischen Lungenversagens mit respiratorischer Acidose angewendet, um eine lungenprotektive Beatmung zu ermöglichen. Enorme technische Enwticklungen und v. a. die extreme Miniaturisierung der extrakorporalen Unterstützungsysteme dürfen jedoch nicht darüber hinwegtäuschen, dass es sich um eine invasive Therapie mit einer hohen Inzidenz von schwerwiegenden Komplikationen handelt. Vor diesem Hintergrund müssen die weite Verbreitung dieser Technologie kritisch hinterfragt und vielmehr die Konzentrierung auf Zentren mit hoher Expertise gefordert werden.
Schlüsselwörter: „Acute respiratory distress syndrome“, „Acute lung injury“, Oxygenierung, Decarboxylierung, Kardiopulmonale Reanimation
Abstract
The use of extracorporeal support systems in cardiac and/or pulmonary failure is an established treatment option. Although scientific evidence is limited there is an increasing amount of data from individual studies, e.g. Conventional Ventilation or ECMO for Severe Adult Respiratory Failure (CESAR) trial 2010, suggesting that extracorporeal membrane oxygenation (ECMO) as a veno-venous pump-driven system is a life-saving procedure in severe respiratory failure. Initially established as a rescue option for postcardiotomy cardiac failure extracorporeal life support (ECLS) as a pump-driven veno-arterial cardiovascular support system is increasingly being used in cardiogenic shock after myocardial infarction, as bridging to transplantation or as part of extended cardiopulmonary resuscitation. The pumpless extracorporeal lung assist (pECLA) as an arterio-venous pumpless system is technically easier to handle but only ensures sufficient decarboxylation and not oxygenation. Therefore, this method is mainly applied in primarily hypercapnic respiratory failure to allow lung protective ventilation. Enormous technical improvements, e.g. extreme miniaturization of the extracorporeal assist devices must not obscure the fact that this therapeutic option represents an invasive procedure frequently associated with major complications. With this in mind a widespread use of this technology cannot be recommended and the use of extracorporeal systems should be restricted to centers with high levels of expertise and experience.
Keywords: Acute respiratory distress syndrome, Acute lung injury, Oxygenation, Decarboxylation, Cardiopulmonary resuscitation
Begriffsbestimmungen
Da es viele verschiedene Begriffe rund um das Thema temporäre Lungen- und Herz-Kreislauf-Ersatzverfahren gibt und diese häufig irreführend sowie uneinheitlich sind, hat die Deutsche Interdisziplinäre Vereinigung für Intensivmedizin (DIVI) sich auf die im Folgenden ausgeführten Empfehlungen geeinigt ([1]; Abb. 1):

Als „extracorporeal membrane oxygenation“ (ECMO) wird die venovenös angeschlossene, pumpenbetriebene Lungenunterstützungstherapie mit Oxygenator bezeichnet. Sie zeichnet sich durch Oxygenierung sowie Decarboxylierung aus dem venösen Blut aus und wird zur Therapie von konservativ nichtbeherrschbarem, hpyoxämischem Lungenversagen eingesetzt. Eine Herz-Kreislauf-Unterstützung ist mit diesem Verfahren aufgrund der Kanülierung nicht möglich.
Abzugrenzen davon ist die „pumpless extracorporeal lung assist“ (pECLA), ein arteriovenös angeschlossenes, nichtpumpenbetriebenes Lungenunterstützungsystem mit einem „Low-resistance“-Oxygenator, das aufgrund der arteriovenösen Blutdruckdifferenz und damit abhängig vom Herzzeitvolumen (HZV) des Patienten eine suffiziente Decarboxylierung, jedoch keine ausreichende Oxygenierung gewährleistet. Somit wird dieses System nahezu ausschließlich beim primär hyperkapnischen Lungenversagen eingesetzt.
Als „extracorporeal life support“ (ECLS) – früher u. a. als venoarterielle ECMO bezeichnet – wird ein venoarteriell angeschlossenes pumpenbetriebenes Herz-Kreislauf-Unterstützungsystem bezeichnet, das nicht nur den Gasaustausch gewährleistet, sondern nahezu das gesamte HZV des Patienten übernehmen kann.
„Extracorporeal membrane oxygenation“
Aufbau
Prinzipiell besteht ein ECMO-System aus folgenden Komponenten (Abb. 2):
extrakorporaler Blutkreislauf mit Entnahme- und Rückgabekanülen und einem in der Regel heparinbeschichteten Schlauchsystem,
Pumpe (in der Regel Zentrifugalpumpe) mit Steuereinheit sowie
Oxygenator mit Wärmetauscher.
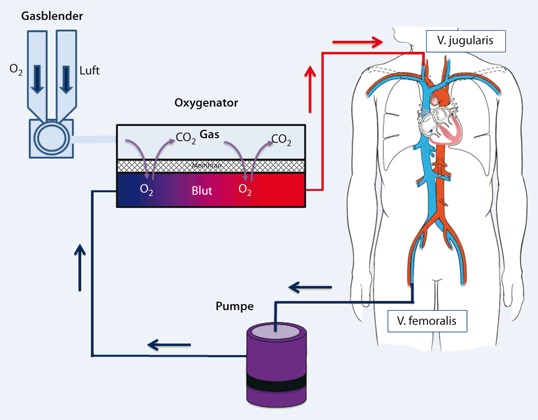
Zur Unterstützung oder auch kompletten Übernahme der Lungenfunktion wird venöses Blut über eine möglichst großlumige Kanüle mithilfe einer aktiven Pumpe aus der V. cava gesaugt und dem Oxygenator zugeführt. Der Oxygenator besteht aus einem gasführenden Hohlfasersystem, das die Diffusion von Sauerstoff (O2) und Kohlendioxid (CO2) in bzw. aus dem Blut erlaubt. Das oxygenierte und decarboxylierte Blut wird dem Patienten über die Rückgabekanüle möglichst in die Nähe des rechten Vorhofs zurückgeführt.
Die derzeit auf dem Markt zur Verfügung stehenden Komplettsysteme (z. B. Maquet Cardiohelp-System, Medos deltastream DP3 ECMO System oder das SORIN SCPC-System) sind sämtlich für den Einsatz von einigen Tagen bis hin zu 2 Wochen zugelassen. Die Systeme verfügen über eine Zentrifugalpumpe, in der durch Rotation von Impellern oder Konen das axial eintretende Blut eine Zentrifugalbeschleunigung erfährt und am Rand des Gehäuses wieder austritt.
Zentrifugalpumpen arbeiten nichtokklusiv. Daher kann es bei stehender Pumpe oder einer zu geringen Drehzahl beim ECLS-System zum Rückfluss vom arteriellen in den venösen Schenkel kommen. Aus diesem Grund müssen die Schläuche bei stehender Pumpe immer abgeklemmt werden. Der Vorteil der Zentrifugalpumpe liegt in der geringeren Blutschädigung. In der Regel werden ECMO-Systeme nichtpulsatil betrieben, Zentrifugalpumpen mit Impellern können jedoch auch pulsatil betrieben werden. Die verfügbaren Systeme sind alle kompakt und mit einem Akku ausgestattet, sodass sie für Transporte geeignet, aber noch nicht alle für alle Arten des Transports zugelassen sind. Die Unterschiede der einzelnen Systeme betreffen insbesondere ihre Beschichtungen: Während einige Systeme bioaktive Heparinbeschichtungen besitzen, sind andere biopassiv mit einer „Physio“ (Phosphorylcholin) beschichtet.
Kanülen und Kanülierung
Die Anlage der zu- und abführenden Kanülen in das venöse Gefäßsystem erfolgt perkutan in Seldinger-Technik, ggf. ultraschallgesteuert. Die Lagekontrolle der ECMO-Kanülen nach ECMO-Anschluss mithilfe der transösophagealen Echokardiographie (TEE) oder radiologisch ist obligat. Bei Verwendung einer Doppellumenkanüle erfolgt die Anlage unter TEE-Kontrolle. Punktionsorte sind bei erwachsenen Patienten mit „acute respiratory distress syndrome“ (ARDS) v. a. die Vv. femoralis und jugularis.
Prinipiziell stehen folgende 3 ECMO-Konfigurationen zur Verfügung:
1. Das Blut wird über die Kanüle in der V. femoralis entnommen und nach Oxygenierung sowie Decarboxylierung dem Körper über die V. jugularis zugeführt.
2. Das Blut wird über eine kurze Kanüle in der V. femoralis entnommen und über eine lange, kontralateral eingebrachte Femoralkanüle zurückgegeben.
Zur Entnahme des Bluts wird in beiden Fällen eine großlumige Kanüle (z. B. 21–23 F) eingesetzt. Die Rückgabe des arterialisierten Bluts erfolgt über eine kleinere Kanüle (z. B. 17–23 F), möglichst zentral in die Nähe des rechten Vorhofs.
3. Seit einiger Zeit existieren auf dem Markt auch „Two-stage“- oder „Multi-stage“-Kanülen (z. B. Avalon Elite Bi-Caval DLC, 13–31 F), die in die V. jugularis interna dextra implantiert werden. Hierbei wird über getrennte Lumina simultan Blut aus den Vv. cava inferior und superior drainiert und direkt in Richtung Trikuspidalklappe zurückgegeben. Die echokardiographische oder angiographische Lagekontrolle der Two-stage-Kanüle ist obligat. Große Vorteile dieser Kanülen liegen neben der geringeren Rezirkulation in der potenziellen Reduktion katheterassoziierter Infektionen sowie der gesteigerten Mobilität des Patienten, da die Punktion der V. femoralis vermieden wird. Insbesondere Patienten mit absehbarer Langzeit-ECMO-Therapie, wie bei chronischen Lungenerkrankungen oder vor Lungentransplantation, können davon profitieren [2].
Ein wesentliches Problem des ECMO-Kreislaufs (Abb. 2) ist das Phänomen der Rezirkulation oder des „shunting“: Liegen die ab- und zuführende Kanülen zu eng beinander, wird ein Teil des zugeführten oxygenierten Blutes unmittelbar wieder abgesaugt. Dies ist insbesondere bei hohen Pumpenflüssen zu beobachten. Dabei scheint eine Rückgabe des Bluts über die V. cava superior gegenüber der V. cava inferior aufgrund der geringeren Rezirkulation (Ansaugen von oxygeniertem Blut) von Vorteil zu sein. Auch bei korrekter Kanülenlage liegt das Shunt-Volumen zwischen 20 und 50%. Eine Bestimmung des Shunt-Volumens ist über die Thermodilution möglich, jedoch in der klinischen Routine nicht etabliert. Daher kommt der Lagekontrolle der Kanülen (Abstand > 15 cm) eine entscheidende Rolle zu. Beträgt der Sauerstoffpartialdruck vor dem Oxygenator < 10% des Sauerstoffpartialdrucks in der arteriellen Kanüle – also hinter dem Oxygenator – ist ebenfalls nicht mit einem erhöhtem Shunt-Volumen zu rechnen [3].
Blut-, Frischgas- und Sauerstofffluss
Der ECMO-Blutfluss ist die hauptsächliche Determinante zur Steuerung der Oxygenierung. Ein ECMO-Blutfluss > 50% des HZV (50–60 ml/kgKG/min) ist notwendig, um einen signifikanten Effekt auf die Oxygenierung des Patienten zu haben. Blutflussraten < 50% des HZV haben keinen wesentlichen Einfluss auf die Oxygenierung, sondern ermöglichen lediglich die Decarboxylierung des Bluts (s. auch Abschn. „‚Pumpless extracorporeal lung assist‘“). Bei hyperdynamischer Kreislaufsituation ist ggf. auch ein Wert > 80–90 ml/kgKG/min für eine suffiziente Oxygenierung nötig.
Die Gasflusssteuerung unterliegt im Wesentlichen den gleichen Regeln, die auch für eine maschinelle Beatmung gelten. Die Steuerung der CO2-Elimination erfolgt hierbei vorwiegend über den Frischgasfluss (1–10 l/min), der über den Membranoxygenator geleitet wird. Je höher der Glasfluss, desto mehr CO2 wird eliminiert. Zur Steuerung des arteriellen Sauerstoffpartialdrucks (paO2) wird die inspiratorische Sauerstofffraktion (FIO2) analog zur Beatmung von 0,21–1,0 eingestellt. Je höher die O2-Konzentration im Frischgaszufluss des Oxygenators eingestellt ist, desto mehr Sauerstoff diffundiert über die Membran des Oxygenators in das Patientenblut.
Ziele und Indikationsbereiche
Aktuell liegt kein allgemeiner Konsensus, sondern lediglich Empfehlungen zum Einsatz der venovenösen ECMO vor. Grundsätzlich liegt das Ziel der ECMO-Behandlung darin, bei Versagen konventioneller Strategien den Gasaustausch zu sichern und/oder einer weiteren ventilatorassoziierten Schädigung der Lungen durch invasive Beatmung mit hohen Beatmungsdrücken und/oder Tidalvolumina vorzubeugen. Somit ist die ECMO-Therapie indiziert bei schwerer Hypoxämie [z. B. paO2-FIO2-Ratio (Horowitz-Index) < 80 mmHg] trotz erhöhtem positiv-endexspiratorischen Druck [“positive end-expiratory pressure“ (PEEP) > 15 cm H2O] bzw. Notwendigkeit exzessiv hoher endinspiratorischer Beatmungsdrücke [z. B. „peak inspiratory pressure“ (PIP) > 35–45 cm H2O] zur Sicherstellung einer ausreichenden Oxygenierung.
Um eine weitere irreversible iatrogene Lungenschädigung zu vermeiden, wird aufgrund der bisherigen Datenlage der frühe Einsatz von extrakorporalen Verfahren – d. h. in den ersten Tagen nach Lungenschädigung – propagiert. Dementsprechend ist die Beatmungsdauer vor ECMO-Implantation einer der stärksten unabhängigen Prädiktoren für Mortalität bei Patienten mit schwerem ARDS [4].
„Acute respiratory distress syndrome“
Aktuelle Datenlage zum ECMO-Einsatz
Zur ECMO-Therapie bei schwerem ARDS liegen insgesamt 3 prospektive randomisierte Studien vor: Die erste Studie (NIH Adult ECMO Trial) wurde 1974–1977 von Zapol et al. [5] an 90 Patienten mit ARDS aus 9 US-Zentren durchgeführt. Die Mortalität betrug in beiden Studiengruppen ca. 90%. Die zweite monozentrisch angelegte Studie an 40 Patienten mit schwerem ARDS (paO2/FIO2 63 mmHg) verglich Patienten mit ECMO-Behandlung (n = 21) und Patienten mit konventioneller Beatmung (n = 19): Das Überleben war in beiden Gruppen vergleichbar (33% vs. 42%, p= 0,08; [6]). Neben der Tatsache, dass es sich bei beiden Studien um historische Daten handelt, verbietet eine Vielzahl von Kritikpunkten [ECMO-Modus (venoarteriell), strenge Antikoagulation mit hoher Inzidenz an Blutungskomplikationen (Transfusionsbedarf 1000–2500 ml/Tag, Blutverlust 1,7 l/Tag), Fehlen einer lungenprotektiven Beatmung auch während ECMO-Therapie (Peak ca. 40 mbar), fehlende Erfahrung in einigen Zentren und lange mittlere Beatmungsdauer vor ECMO-Therapie von 9 Tagen] die Übertragbarkeit der Daten auf die moderne Ära der ECMO-Therapie.
Im Jahr 2009 wurde von Peek et al. [7] die bis dato größte und mit Spannung erwartete ECMO-Studie publiziert, die Conventional Ventilation or ECMO for Severe Adult Respiratory Failure (CESAR) Trial. An dieser prospektiv randomisierten Studie nahmen in den Jahren von 2001 bis 2006 insgesamt 180 ARDS-Patienten teil (Lung Injury Score > 3 oder Hyperkapnie mit dekompensierter respiratorischer Acidose, pH < 7,2). Sie wurden entweder einer konventionellen Beatmungsgruppe in kleineren, nichtspezialisierten Zentren oder einer ECMO-Gruppe im ARDS/ECMO-Zentrum zugeordnet. In der ECMO-Gruppe konnte eine signifikante Verbesserung der Überlebensrate ohne schwere Behinderung nach 6 Monaten nachgewiesen werden. Mehrkosten der ECMO-basierten Behandlung wurden unter Berücksichtigung des besseren Outcome als akzeptabel bewertet. Die Kritikpunkte an der Studie sind vielfältig und lassen sich, wie folgt, zusammenfassen:
- „Intention-to-treat“-Analyse: Nicht alle „ECMO-Patienten“ erhielten auch eine ECMO. Eine ECMO wurde im Studienzentrum dann angelegt, wenn nach Optimierung der Beatmung noch eine kritische Einschränkung der Oxygenierung bestand. Dies war bei 68 von 90 Patienten der Untersuchungsgruppe (76%) der Fall, 24% der Patienten der ECMO-Gruppe wurden nach Optimierung der Behandlung durch Spezialisten wegen erheblicher Besserung des pulmonalen Gasaustauschs nicht mit ECMO versorgt, aber in die Datenanalyse einbezogen.
- Behandlung sämtlicher Patienten der Untersuchungsgruppe in einem spezialisierten ARDS-Zentrum, Behandlung der Kontrollgruppe in vielen verschiedenen kleinen Krankenhäusern.
- Erreichen der statistischen Signifikanz durch „aufgeweichte“ Outcome-Parameter: „Tod oder schwere Beeinträchtigung“. Die statistische Signifikanz des Überlebensvorteils der ECMO-Gruppe wurde nur erreicht, indem zur Variable „Tod“ die Variable „schwere Einschränkung“ hinzugerechnet wurde.
- Unklare, hohe Inzidenz von Leberfunktionsstörungen in der „ECMO-Gruppe“ [15 Patienten mit extrakorporalen Leberersatzverfahren („molecular adsorbents recirculating system“, MARS)].
- Ungenügende (lungenprotektive) Beatmungsstrategie in der Kontrollgruppe. [Nur 70% der Patienten der Kontrollgruppe im Vergleich zu 93% der ECMO-Gruppe erhielten eine konsequente lungenprotektive Beatmung (niedriges Tidalvolumen, adäquat hoher PEEP)]. Unter Berücksichtigung der Ergebnisse des ARDS-Network könnte ohne Mühe argumentiert werden, dass der Unterschied in der Letalität durch die unterschiedliche Beatmungsstrategie und nicht durch die Anwendung der ECMO bedingt ist.
- Keine Angabe über Komplikationen durch das ECMO-Verfahren.
Somit belegt die CESAR Trial zwar, dass die Therapie von ARDS-Patienten in spezialisierten Zentren die Überlebensrate zu erhöhen scheint. Gesicherte Aussagen darüber, ob und in welchem Ausmaß die ECMO an dieser Ergebnisverbesserung beteiligt war, sind jedoch noch nicht möglich. Auch wenn die Frage einer Outcome-Verbesserung aktuell nicht abschließend beantwortet werden kann, sind nicht zuletzt vor dem Hintergrund der positiven Ergebnisse während der Influenza-A-Virus-H1N1-Pandemie die schwere Hypoxämie und/oder die schwere Hyperkapnie sowie die Sicherstellung einer lungenprotektiven Beatmungsstrategie Indikationen für die ECMO-Therapie im Sinne eines Heilversuchs [8].
Definitionen
Das invasive ECMO-Verfahren ist Patienten vorbehalten, die unter einem schweren Lungenversagen leiden. Vor diesem Hintergrund erscheint es notwendig, sich mit der Definition des akuten Atemnotsyndroms (ARDS) auseinanderzusetzen.
Die europäisch-amerikanische Konsensuskonferenz (American-European Consensus Conference, AECC) von 1994 definierte ein ARDS als akut aufgetretene, schwere Oxygenierungsstörung (sog. Oxygenationsindex paO2/FIO2 < 200 mmHg) mit bilateralen Lungeninfiltraten ohne Hinweise auf ein kardial bedingtes Lungenödem [9]. Die „acute lung injury“ (ALI) grenzte sich hierbei einzig durch eine leichtergradige Oxygenierungsstörung (paO2/FIO2 < 300 mmHg) vom ARDS ab. Diese Definition beinhaltet eine Vielzahl von Limitationen: Der zeitliche Verlauf des Auftretens ist nicht definiert; die Respiratoreinstellung, v. a. das eingestellte PEEP-Niveau und die FIO2, werden nicht berücksichtigt. Ein kardiales Lungenödem sollte mithilfe des Pulmonaliskatheters ausgeschlossen werden, allerdings weisen 30% aller Patienten mit ARDS einen Wedge-Druck („pulmonary capillary wedge pressure“, PCWP) > 18 mmHg auf.
Vor diesem Hintergrund wurde 2011 in Berlin eine neue ARDS-Definiton unter Federführung der European Society of Intensive Care Medicine, der American Thoracic Society und der Society of Critical Care Medicine verabschiedet [10]. Diese unterscheidet nicht mehr 2, sondern 3 Schweregrade des ARDS, in Abhängigkeit von der Schwere der Hypoxämie und unter Berücksichtigung der Respiratoreinstellung:
schweres ARDS: paO2/FIO2 ≤ 100 mmHg, bei PEEP ≥ 5 cm H2O,
moderates ARDS: paO2/FIO2= 101–200 mmHg, bei PEEP ≥ 5 cm H2O und
mildes ARDS : paO2/FIO2= 201–300 mmHg, bei PEEP ≥ 5 cm H2O.
Die Bezeichnung „akute Lungenschädigung“ (ALI) für die mildere Verlaufsform entfällt in der neuen Definition. Darüber hinaus wurde der zeitliche Verlauf genauer definiert. Als bildgebende Verfahren neben dem Thoraxröntgen werden insbesondere die Computertomographie betont und die Echokardiographie als Verfahren der ersten Wahl zum Ausschluss eines kardialen Lungenversagens hervorgehoben. Des Weiteren werden für die Definition des schweren ARDS die Lungen-Compliance sowie -Resistance herangezogen (Tab. 1).
| Definition der American-European Consensus Conference [9] | Berlin-Definition [10] | |
|---|---|---|
| Zeitlicher Verlauf | Akuter Beginn | Beginn innerhalb 1 Woche bei bekannter Ursache oder neuer oder verschlimmerter Symptome |
| Thoraxröntgen | Bilaterale Infiltrate | Bilaterale Infiltrate, die sich nicht vollständig durch Pleuraergüsse, Atelektasen oder Rundherde erklären lassen |
| Ursache des Lungenödems | PAWP < 18 mmHg oder alternatives Verfahren zum Ausschluss einer Linksherzinsuffizienz | Respiratorisches Versagen nicht ausschließlich über Herzversagen oder Volumenüberschuss erklärbar. Notwendigkeit weiterer Untersuchungen zum Ausschluss eines hydrostatischen Ödems, falls kein Risikofaktor vorhanden |
| Oxygenierung |
ALI: paO2/FIO2 < 300 mmHg ARDS: paO2/FIO2 < 200 mmHg |
Mildes ARDS : 200 mmHg < paO2/FIO2 ≤ 300 mmHg mit PEEP oder CPAP ≥ 5 cm H2O Moderates ARDS : 100 mmHg < paO2/FIO2 ≤ 200 mmHg mit PEEP ≥ 5 cm H2O Schweres ARDS: paO2/FIO2 ≤ 100 mmHg mit PEEP ≥ 5 cm H2O |
ALI „acute lung injury“, CPAP „continuous positive airway pressure“, PAWP „pulmonary capillary wedge pressure“, PEEP „positive end-expiratory pressure“, p a O 2 /F I O 2 Horowitz-Index.
In einer Metaanalyse von ARDS-Studien mit mehr als 4000 Patienten wurde die Praktikabilität der 3 neuen Kategorien bereits an den signifikant unterschiedlichen Mortalitätsraten (27, 32 und 42%) und Beatmungszeiten (5, 7 und 9 Tage) nachgewiesen.
Benötigen nun alle Patienten mit schwerem ARDS – definiert als Horowitz-Index ≤ 100 mmHg, bei einem PEEP ≥ 5 cm H2O – eine ECMO? Diese Frage muss eindeutig verneint werden.
Neben der Sicherstellung der arteriellen Oxygenierung und Decarboxylierung steht die kausale Therapie der zugrunde liegenden Erkrankung im Vordergrund der ARDS-Therapie. In der Regel handelt es sich dabei um die Sanierung eines infektiösen Fokus durch adäquate antibiotische Therapie oder durch chirurgische Maßnahmen. Die Extracorporeal Life Support Organization (ELSO) sieht die Indikation für eine ECMO-Therapie als gegeben, wenn die zu erwartende Mortalität ohne ECMO-Therapie 80% übersteigt, z. B. bei einer paO2-FIO2-Ratio < 80 mmHg bei einer FIO2 > 0,9 und einem Lung Injury Score (Murray Score) von 3–4.
Neben der kausalen Therapie, wie etwa der antimikrobiellen Therapie im Fall einer Pneumonie, steht eine Reihe von begleitenden Therapieoptionen zur Verfügung, wie etwa lungenprotektive Beatmung, dorsoventrale Wechsellagerung, Flüssigkeitsmanagement oder inhalative Stickstoffmonoxidtherapie [11, 12]. Somit ergeben sich folgende Eckpunkte bei der Indikationsstellung zur ECMO-Therapie:
potenziell reversible Ursache des ARDS,
Identifikation von Patienten mit hoher Mortalität,
- Muray Score > 3,
- paO2-FIO2-Ratio < 100 mmHg,
- PEEP > 15 cm H2O und
- bilaterale Infiltrate,
trotz
protektiver Beatmung, permissiver Hyperkapnie,
Bauchlage,
Optimierung des Volumenhaushalts (Diuretika, Nierenersatzverfahren) und
inhalativer Stickstoffmonoxidgabe.
Nach den Daten der ELSO aus 2011 wurden die registrierten ECMO-Implantationen v. a. bei bakterieller Pneumonie sowie postoperativem oder traumatischem ARDS durchgeführt (Tab. 2). Die durchschnittliche Therapiedauer lag je nach Indikation zwischen 194 und 293 h; die längste Therapiedauer betrug 209 Tage.
| Erkrankung | ECMO-Implantationen | Überleben (%) | |
|---|---|---|---|
| Anzahl (n) | Anteil (%) | ||
| Virale Pneumonie | 107 | 4,4 | 65 |
| Bakterielle Pneumonie | 423 | 17,6 | 59 |
| Aspirationspneumonie | 61 | 2,5 | 61 |
| „Acute respiratory distress syndrome“ (ARDS) | |||
| Postoperativ/traumatisch | 203 | 8,4 | 52 |
| Nichtpostoperativ/-traumatisch | 349 | 14,5 | 48 |
| Akute Lungenschädigung, nicht ARDS | 121 | 5,0 | 55 |
| Andere | 1142 | 47,5 | 52 |
| Gesamt | 2406 | 56 | |
ECMO „extracorporeal membrane oxygenation“, ELSO Extracorporeal Life Support Organization.
Beatmung
Primärziel der Beatmung unter ECMO-Therapie ist die Vermeidung einer weiteren „ventilatorassoziierten Lungenschädigung“ („ventilator-associated lung injury“, VALI). Daher sollte eine maximal-lungenprotektive Beatmung durchgeführt werden. Zugleich sollte eine zeitnahe Spontaneisierung ggf. mit frühzeitiger Tracheotomie des Patienten erfolgen, um unerwünschte Effekte einer prolongierten invasiven Beatmung [ventilatorassoziierte Pneumonie (VAP), Hypotrophie der Atemhilfsmuskulatur etc.] zu reduzieren.
Komplikationen
Auch wenn in den letzten Jahren auf dem Gebiet der extrakorporalen Systeme eine rasante technische Entwicklung stattgefunden hat, sind Komplikationen während der ECMO-Therapie nicht selten. Eine Übersicht über Art und Häufigkeit von Komplikationen unter ECMO-Therapie gibt Tab. 3 (http://www.eslonet.com).
| Komplikationen | Häufigkeit (%) |
|---|---|
| Direkt | |
| Gerinnselbildung im ECMO-System | 17,8 |
| Versagen des Membranoxygenators | 17,5 |
| Kanülenprobleme (Dislokation etc.) | 8,4 |
| Sonstige | 7,9 |
| Indirekt | |
| Nachblutungen | 19 |
| Blutungen im Bereich der Kanülierungsstelle(n) | 17,1 |
| Pulmonale Blutung | 8,1 |
| Gastrointestinale Blutung | 5,1 |
| Intrakranielle Blutung | 3,8 |
| Hämolyse | 6,9 |
| Disseminierte intravasale Gerinnungsstörung | 3,7 |
„Extracorporeal life support“
Aufbau und Kanülierungsformen
Der Aufbau eines „extracorporeal life support“ (ECLS) entspricht prinzipiell dem der ECMO; lediglich die Kanülierung unterscheidet sich: Bei einer ECLS als Herz- oder Herz-Lungen-Ersatz wird venöses Blut aus der V. cava inferior entnommen und arteriell zurückgeführt.
Die ECLS kann sowohl zentral, d. h. im Bereich der thorakalen Aorta und des rechten Vorhofs, als auch peripher im Bereich der A. femoralis oder A. subclavia angeschlossen werden. Insgesamt existieren 3 Kanülierungskonfigurationen, die durch spezifische hämodynamische Verhältnisse und Komplikationen charakterisiert sind. So kann es je nach Art der Kanülierung zu einer mehr oder weniger stark ausgeprägten Mischung von sauerstoffreichem und -armem Blut in der oberen Körperhälfte kommen.
Venöser Abfluss über die V. femoralis, arterieller Zufluss peripher über die A. femoralis
Das Einbringen einer großlumigen Kanüle in das periphere arterielle Gefäßsystem kann zu Perfusionsstörungen distal der Kanüle führen. Zur Prophylaxe kann distal der arteriellen ECLS-Kanüle eine Beinperfusionskanüle (10–12 F) in Seldinger-Technik eingebracht werden. Alternativ besteht die Möglichkeit, den peripheren arteriellen Gefäßzugang chirurgisch mithilfe der Aufnaht einer Gefäßprothese (meist 8 mm) herzustellen.
Das linke Herz sollte unter ECLS-Therapie zwar weitgehend entlastet werden, dennoch leicht auswerfen, um Thrombenbildungen an der ansonsten verschlossenen Aortenklappe zu vermeiden und um den linken Ventrikel zu entleeren. Je nach Ausmaß der linksventrikulären Auswurfleistung resultiert somit eine unterschiedlich stark ausgeprägte Mischperfusion der Körpers (Abb. 3): Auch bei deutlich eingeschränkter eigener kardialer Auswurfleistung findet unter ECLS-Therapie die Koronardurchblutung hauptsächlich über das linksventrikulär ausgeworfene Blut statt. Bei zunehmender Auswurfleistung werden die gesamte obere Körperhälfte über das ausgeworfene Blut, die untere Körperhälfte über das retrograd von der ECLS zurückgeführte Blut perfundiert.

Im Fall eines begleitenden Lungenversagens ist das vom Herzen ausgeworfene Blut schlecht oxygeniert, sodass sowohl die Koronargefäße – mit konsekutiver myokardialer Hypoxie – als auch ggf. die oberen Extremitäten und der Kopf des Patienten einer Sauerstoffunterversorgung unterliegen („Harlekin-Phänomen“). Dies kann dazu führen, dass zwischen rechtem und linkem Arm sowie den unteren Extremitäten die arteriellen Sauerstoff- und Kohlendioxidpartialdrücke und auch die arterielle Sauerstoffsättigung stark differieren können. Da der Ort des höchsten Mischblutanteils aufgrund der anatomischen Situation der rechte Arm ist, sollten sowohl das Monitoring der Sauerstoffsättigung als auch die Blutgasentnahme an dieser Stelle erfolgen, um eine lokale Hypoxämie frühzeitig detektieren zu können.
Des Weiteren kann es – insbesondere bei einer Insuffizienz der Aortenklappe – zu einer massiven Volumenbelastung des linken Ventrikels mit linksventrikulärer Distension kommen. In diesem Fall muss ein „vent“ im linken Ventrikel für Entlastung sorgen, der das System allerdings verkompliziert und es anfälliger für Luftembolien macht. Alternativ kann eine Vorhofseptostomie erfolgen [13].
Venöser Abfluss über eine Zwei- (40/32 F) oder Dreistufenkanüle (29 F) im rechten Vorhofohr, arterieller Zufluss über direkte Kanülierung der Aorta ascendens (18–24 F)
Voraussetzung für dieses Vorgehen ist ein offener Thorax. Es bestehen keine Probleme bezüglich der peripheren Perfusion. Aufgrund der antegraden Flussrichtung des ECLS-Systems bei zentraler Kanülierung kommt es nicht zu einem entgegengesetzten kardialen Blutfluss. Daher kann die Blutentnahme an beiden Armen sowie an den Femoralgefäßen des Patienten erfolgen.
Venöser Abfluss über die V. femoralis, arterieller Zufluss peripher über die A. subcalvia
Die Kanülierung der A. subclavia erfolgt entweder in Seldinger-Technik mit zusätzlicher Armperfusionskanüle, häufiger jedoch chirurgisch. Venös wird die V. femoralis punktiert. Bei diesem Zugang fließt das Blut durch den Truncus brachiocephalicus direkt in den Aortenbogen und generiert somit einen fast physiologischen Fluss. Der rechte Arm des Patienten wird direkt über das ECLS-System versorgt. Zur Blutgasanalyse bieten sich bei dieser Versorgung also Blutentnahme aus dem linken Arm sowie aus den Femoralgefäßen an.
Indikationen
Im Gegensatz zur ECMO hat sich das Verfahren der ECLS außerhalb der Herzchirurgie im Rahmen eines Postkardiotomie-low-output-Syndroms erst in den letzten Jahren etabliert. Daher existieren bisher kaum Empfehlungen zum Einsatz der ECLS [14]. Im Allgemeinen ist die ECLS-Implantation bei Patienten mit therapierefraktärem kardiogenem Schock zu erwägen, wenn diese trotz maximaler konservativer Therapie einschließlich Volumen-, Vasopressor-, Inotropikagabe sowie Intraaortaler-Ballonpumpen(IABP)-Implantation keine ausreichende systemische Perfusion aufbauen [14]. Des Weiteren ist die ECLS unter gewissen Umständen im Rahmen einer erweiterten kardiopulmonalen Reanimation („cardiopulmonary resuscitation“, CPR) zu erwägen.
Die Entscheidung zur ECLS-Implantation muss immer im Team und individuell von Fall zu Fall getroffen werden. Dabei müssen v. a. Patientenalter, Prognose des Patienten, Begleiterkrankungen, Ziel der ECLS-Therapie, neurologischer Status und bereits vorliegende Endorganschäden (Multiorganversagen?) berücksichtigt werden. Folgende Erkrankungen gelten als Grundlage der ECLS-Implantation:
„post-perfusion low-cardiac output“ bzw. „Weaning“-Versagen nach extrakorporaler Zirkulation,
akute Exazerbation einer chronischen Herzinsuffizienz,
akute massive Lungenemboli,
akutes kardiales Versagen nach Intoxikation,
Kühlung von Patienten nach Herz-Kreislauf-Stillstand,
kardiogener Schock bei akutem Myokardinfarkt und
akute Transplantatabstoßung.
Da es sich bei der ECLS nicht um eine dauerhafte Therapieoption, sondern um eine Überbrückungsmaßnahme handelt, kann die ECLS-Therapie aufgrund ihrer Zielsetzung, wie folgt, klassifiziert werden:
„Bridge to recovery“: Überbrückung bis zur Erholung der myokardialen Funktion, v. a. bei Myokarditispatienten.
„Bridge to decision“: In der Akutsituation ist die Entscheidung für eine weiterführende, eskalierende Therapie oft schwierig, z. B. bei unklarer neurologischer Situation nach Reanimation. Die ECLS bietet die Möglichkeit der Stabilisierung in der Akutphase, um Zeit für die weitere Therapieplanung [z. B. „Left-ventricle-assistent-device“(LVAD)-Implantation] zu gewinnen.
„Bridge to bridge“: Die Überbrückung zur Implantation eines kardialen Assist device [LVAD, RCAD, BVAD), um dann eine Herztransplantation anzustreben.
„Bridge to transplantation“: Überbrückung zur Herztransplantation.
Des Weiteren wird in letzter Zeit bei der Versorgung von Patienten mit kardiogenem Schock auf dem Boden eines akuten Koronarsyndroms häufig von „bridge to intervention“ gesprochen. Nach den Daten der ELSO aus 2011 wurden die registrierten ECLS-Implantationen bei über 16-jährigen Patienten v. a. im kardiogenen Schock sowie bei bekannter Kardiomyopathie mit akuter Exazerbation durchgeführt (Tab. 4; http://www.eslonet.com).
| Erkrankung | Anzahl (n) der ECLS-Implantationen | Überleben (%) |
|---|---|---|
| Kongenitales Herzvitium | 144 | 36 |
| Herz-Kreislauf-Stillstand | 84 | 27 |
| Kardiogener Schock | 196 | 39 |
| Kardiomyopathie | 223 | 45 |
| Myokarditis | 64 | 69 |
| Andere | 1015 | 37 |
ECLS „extracorporeal life support“, ELSO Extracorporeal Life Support Organization.
Die durchschnittliche Therapiedauer lag je nach Indikation zwischen 73 und 163 h; die längste Therapiedauer betrug 88 Tage.
Kardiopulmonale Reanimation
In den aktuellen nationalen und internationalen Leitlinien zur CPR wird die ECLS als bevorzugte Methode zur aktiven internen Wiedererwärmung bei hypothermen Patienten mit Atem- und Herz-Kreislauf-Stillstand sowie Patienten nach Intoxikation mit kardiodepressiven Substanzen und konsekutivem Herz-Kreislauf-Versagen empfohlen [15]. Zahlreiche Studien belegen jedoch, dass der Einsatz eines ECLS-Systems unter CPR prinzipiell bei jeder potenziell kurativ behandelbaren Grundkrankheit zu überlegen ist. Anhand kleiner Fallzahlen ist eine Überlebensrate nach Herz-Kreislauf-Stillstand und CPR durch den ECLS-Einsatz von 27% beschrieben, bei Patienten, die sonst keine Therapiemöglichkeit mehr gehabt hätten [16]. Andere Untersuchungen berichten von einer Krankenhausüberlebensrate nach Einsatz eines ECLS-Systems bei CPR von 40–50% [17]. Eine prospektive, randomisierte Studie zum ECLS bei „out-of-hospital cardiac arrest“ ist in Planung (Prague OHCA Study).
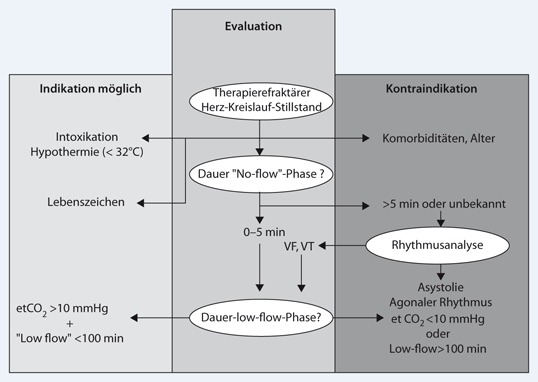
Möglichkeit und Sinnhaftigkeit der ECLS-Implantation während der CPR bleiben individuell im Einzelfall abzuwägen und hängen von der Prognose des Patienten sowie Dauer, Art und Grund der CPR ab. Die ECLS-Implantation erfordert einen hohen logistischen Aufwand sowie ein ECLS-Team im „standby“ (24/7). Ein möglicher Algorithmus zur Evaluation von Patienten unter CPR hinsichtlich der Indikation zur ECLS-Implantation ist in Abb. 4 zu sehen. Ein Ausschlusskriterium ist der hypoxische Herz-Kreislauf-Stillstand.
Erforderliche personelle und technische Voraussetzungen
Moderne ECMO-/ECLS-Systeme sind leicht zu implantieren, hoch effektiv und transportabel. Dennoch dürfen rasante technische Entwicklungen auf dem Gebiet der extrakorporalen Systeme nicht darüber hinwegtäuschen, dass es sich um ein invasives Verfahren handelt, dass viel Expertise und Erfahrung erfordert. Des Weiteren sind Komplikationen während der ECMO-/ECLS-Therapie nicht selten: In einer retrospektiven Analyse der ELSO-Datenbank traten in bis zu 17,5% der Fälle technische Probleme wie z. B. eine Oxygenatordysfunktion auf. Außerdem kommt es unter der Therapie gehäuft zu Blutungskomplikationen (19%) und lebensbedrohenden peripheren sowie auch zentralen Gefäßkomplikationen. Vor diesem Hintergrund muss kritisch beleuchtet werden, dass in jüngster Vergangenheit zunehmend niedergelassene Kardiologen Interesse an ECLS-Systemen gefunden haben, um Patienten bei „perkutaner transluminaler koronarer Hochrisikoangioplastie“ im Notfall unterstützen zu können. Um diesen Entwicklungen gegenzusteuern, haben die Arbeitsgruppe Extrakorporale Zirkulation (EKZ) der Deutschen Gesellschaft für Herz-, Thorax- und Gefäßchirurgie (DGTHG) sowie die Deutsche Gesellschaft für Kardiotechnik (DGfK) ein Positionspapier zur ECLS-Therapie verfasst und empfehlen den Einsatz dieser Systeme nur in Zentren, die über die entsprechende Expertise verfügen, um die Kanüle sicher in Seldinger- und/oder chirurgischer Technik platzieren, Gefäßkomplikationen kathetertechnisch und/oder chirurgisch beheben sowie eine Notfallthorakotomie und den Einsatz der EKZ durchführen zu können. Folgende Mindestanforderungen wurden von den genannten Fachgesellschaften formuliert [10]:
- Verfügbarkeit eines Facharzts für Herzchirurgie (bzw. Herzchirurgen mit Facharztniveau) mit hinreichender Erfahrung in der transkutanen und konventionell chirurgischen Implantation von arteriellen und venösen Kanülen unter Notfallbedingungen,
- Verfügbarkeit eines European Board of Cardiovascular Perfusion (EBCP) zertifizierten Kardiotechnikers mit hinreichender klinischer Erfahrung (bzw. mehr als 500 selbstständig durchgeführten extrakorporalen Zirkulationen),
- Verfügbarkeit einer kompletten apparativen Ausstattung [mobile Herz-Kreislauf-Unterstützungssysteme mit redundantem Back-up-System, diverse arterielle und venöse Kanülen, Operationssieb, Geräte für die Bestimmung von „activated clotting time“ (ACT) und die Blutgasanalyse (BGA) etc.].
„Pumpless extracorporeal lung assist“
Am Klinikum der Universität Regensburg wurde von einer interdisziplinären Arbeitsgruppe ein neues arteriovenöses Lungenunterstützungssystem entwickelt [19]: Der iLA-Membranventilator® wird arteriovenös über die femoralen Gefäße angeschlossen und bewirkt ohne Notwendigkeit einer Blutpumpe eine extrakorporale CO2-Elimination und geringe Oxygenierung des Bluts (Abb. 5).
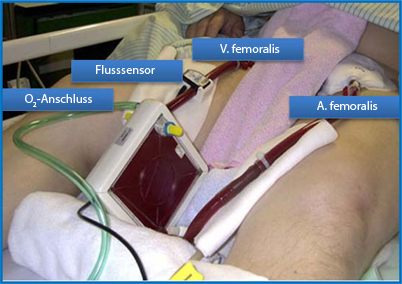
Der Blutfluss wird durch den Druckgradienten zwischen A. und V. femoralis erzeugt (durchschnittliche treibende Druckdifferenz von 60–80 mmHg). Damit wird ein vom HZV-abhängiger Blutfluss von maximal 4,5 l/min generiert; die direkte Einstellung des Blutflusses ist nicht möglich. Es werden ca. 20% des HZV über die Membran geleitet. Für die optimale Funktion der Membran ist ein Blutfluss von ca. 1,0–1,5 l/min erforderlich. Somit ist die Limitation der Methode aus zirkulatorischer Sicht bei einem arteriellen Mitteldruck < 60 mmHg anzusiedeln; ein kardiogener Schock stellt eine Kontraindikation für den Einsatz der pECLA dar. Häufig sind jedoch nach pECLA-Implantation ein Anstieg des HZV und eine Reduktion der Vasopressortherapie aufgrund der Normalisierung des pH-Werts zu beobachten.
Die pECLA zeichnet sich durch eine sehr gute Decarboxylierungsleistung (abhängig von pCO2, Gasfluss, Blutfluss), jedoch nur eine eingeschränkte Oxygenierungsleistung (da arterielles Blut nahezu komplett gesättigt ist, wesentlicher Effekt ist die Reduktion des alveolären pCO2) aus. Deshalb sollte die Methode als unterstützendes Verfahren zur Lungenprotektion, nicht aber als Lungenersatztherapie bei primärem Oxygenierungsversagen eingesetzt werden. Dennoch stellt dieses Verfahren keine Behelfsvariante der ECMO, sondern einen eigenen Therapieansatz dar, der auf CO2-Elimination abzielt und dadurch die Lungenprotektion in der Beatmungsstrategie ermöglicht. Die Hauptindikation zur pECLA-Therapie liegt in der primär hyperkapnischen (respiratorischen) Acidose mit einem pH-Wert < 7,25, die nicht oder nur durch eine lungenschädigende Beatmung (Tidalvolumen > 8 ml/kg Ideal-KG, Spitzendruck > 35 cm H2O, FIO2 > 0,6) zu beseitigen ist.
Auf die Integration eines Wärmetauschers kann wegen zu vernachlässigender Temperaturverluste durch Konvektion verzichtet werden. Das Füllvolumen des gesamten extrakorporalen Systems, einschließlich der Anschlussleitung an die Kanülen, beträgt maximal 250 ml; es kommt zu einer verhältnismäßig geringen Schädigung der korpuskulären Blutbestandteile. Weitere Vorteile liegen in der wesentlich leichteren Anlage und Handhabbarkeit ohne Notwendigkeit eines Kardiotechnikers und der wesentlich geringeren Größe, die sich v. a. bei Transport und Mobilisation des Patienten bemerkbar macht.
Als kritischer Punkt ist jedoch die Kanülierung der A. femoralis anzusehen. Hier ist besondere Sorgfalt darauf zu verwenden, dass es nicht zur unzureichenden Perfusion im Abstromgebiet des arteriell punktierten Gefäßes kommt (Tab. 5).
| „Extracorporeal membrane oxygenation“ | „Pumpless extracorporeal lung assist“ | |
|---|---|---|
| Effekt auf den Gasaustausch |
Oxygenierung ↑↑ Decarboxylierung ↑↑ |
Oxygenierung ↑ Decarboxylierung ↑↑ |
| Kanülierung | Venovenös | Arteriovenös |
| Extrakorporaler Blutfluss (l/min) | Zirka 4 | 1,5–2 |
| Antikoagulation | Heparinisierung | „Low-dose“-Heparin |
| Komplikation | Blutung, Membranleckage, Hämolyse, Rezirkulation | „Low cardiac output“, heparininduzierte Thrombozytopenie Typ II |
| Personeller und technischer Aufwand | Hoch | Gering |
Einen Überblick über die Kontraindikationen zur pECLA-Therapie gibt Tab. 6.
| Kontraindikationen |
|---|
| Eingeschränkte kardiale Pumpfunktion (Herzminutenvolumen < 2,5 ml/min) |
| Therapierefraktäre Hypoxämie |
| Periphere arterielle Verschlusskrankheit |
| Arterieller Gefäßdurchmesser < 5 mm |
| Schwere disseminierte intravasale Gerinnungsstörung |
| Heparininduzierte Thrombozytopenie Typ II |
Entscheidend für den Erfolg der pECLA-Therapie scheint, ähnlich wie bei der ECMO-Therapie, der frühzeitige Einsatz zu sein, um der Lungenschädigung durch eine aggressive Beatmung vorzubeugen: So ist dem „ILA-Registry“ zufolge die Überlebensrate bei Patienten mit „chronic obstructive pulmonary disease“ (COPD) im Fall einer frühzeitigen pECLA-Implantation (< 48 h nach respiratorischer Acidose, pH < 7,25) mit 75% signifikant besser als bei Patienten mit verspäteter ILA-Therapie (http://www.novalung.com). Prospektiv-randomisierte Studien zum Einsatz der pECLA existieren nicht. Die Mortalität lag in den bisher publizierten Fallserien mit 57% (263 von 462 Patienten) unter der erwarteten Sterblichkeit. In allen Studien konnte die suffiziente Decarboxylierung mit konsekutiver Deeskalation der mechanischen Beatmung erreicht werden. Die Inzidenz von lokalen Komplikationen an der arteriellen Kanülierungsstelle konnte im Zeitraum von 2006 bis 2009 von 24,4 auf 11,9% gesenkt werden; es traten keine pECLA-assozierten Todesfälle auf [20].
Ausblick
Aufgrund ständiger technischer Weiterentwicklung, insbesondere im Bereich der Systemminiaturisierung, sind die weitere Zunahme der Implantationszahlen und auch die Ausweitung auf weitere Indikationsgebiete im Bereich der kurz- und längerfristigen Herz-/Lungenunterstützungssysteme zu erwarten.
Im Bereich der ECLS-Therapie hat der bereits stattgefundene Wandel der LVAD-Therapie weg vom „bridging to transplant“ hin zur „Destination“-Therapie zu einer breiteren Anwendung an Patienten, die keine Transplantationskandiaten sind, geführt. Darüber hinaus gibt es zunehmend Bemühungen zur Etablierung von Netzwerken, um Patienten im schwersten kardiogenen Schock oder sogar im Rahmen einer CPR auch jenseits des herzchirurgischen Settings mit einer ECLS zu versorgen und anschließend in ein Zentrum der Maximalversorung mit herzchirurgischer Expertise zu verlegen. Des Weiteren gibt es erste positive Berichte über den Einsatz eines ECLS in der Therapie des septischen Schocks; eine asiatische retrospektive Observationsstudie wird voraussichtlich Ende 2013 vorgestellt.
Die pECLA hat sich in den letzten Jahren weg vom Rescue-Verfahren beim schwersten hyperkapnischen Lungenversagen hin zum Tool zur Vermeidung einer lungenschädigenden Beatmung entwickelt. So wird dieses Verfahren zunehmend beim wachen ansprechbaren Patienten angewendet, um die endotracheale Intubation mit all ihren negativen Effekten zu vermeiden. Ähnliches lässt sich von der ECMO-Therapie berichten: Aufgrund des Wissens um dies lungenschädigenden Effekte einer aggressiven Beatmung wird die Indikation zur ECMO-Therapie immer früher gestellt. Eine prospektive randomisierte Studie zum frühen Einsatz der ECMO – 3–6 h nach Diagnose eines schweren ARDS – befindet sich in der Rekrutierungsphase (Extracorporeal Membrane Oxygenation for Severe Acute Respiratory Distress Syndrome, EOLIA).
Insbesondere die Anwendung einer Doppellumenkanüle ermöglicht den Langzeiteinsatz in wachen und mobilen Patienten, z. B. als Bridging zur Lungentransplantation. Die Ergebnisse einer prospektiven Studie zur ECMO-Therapie in wachen Patienten vor Lungentransplantation werden 2014 erwartet. Zusammengefasst handelt es sich daher bei der extrakorporalen Herz- und/oder Lungenunterstützung um ein Gebiet mit großem Entwicklungspotenzial, das nicht nur zahlenmäßig immer mehr in den Fokus der Herzchirurgen und der Intensivmediziner tritt.
Fazit für die Praxis
Trotz ihres invasiven Charakters finden Herz- und/oder Lungenersatzverfahren aufgrund technischer Fortschritte sowie auch positiver Studienergebnisse und klinischer Erfahrung zunehmend Anwendung. Es ist jedoch eine hohe Inzidenz an Komplikationen unter ECMO-/ECLS-Therapie zu beobachten; Indikationsstellung und v. a. Timing erfordern große Expertise. Vor diesem Hintergrund ist eine Begrenzung dieser Therapieoptionen auf große Zentren mit herzchirurgischer Anbindung zu fordern.
Acknowledgments
Interessenkonflikt
Der korrespondierende Autor gibt für sich und seine Koautoren an, dass kein Interessenkonflikt besteht.
K. Pilarczyk
Kevin Pilarczyk studierte von 2000 bis 2007 Humanmedizin in Gießen, Essen, Rochester(USA) sowie Houston (USA) und ist seit 2007 Assistenzarzt an der Klinik für Thorax- und Kardiovaskuläre Chirurgie des Westdeutschen Herzzentrums Essen. Sein klinischer und wissenschaftlicher Schwerpunkt ist die herzchirurgische Intensivmedizin.
Literatur
- 1.Trummer G, Bein B, Buerke M et al (2013) Einteilung mechanischer Herz-, Lungen und/oder Kreislaufunterstützungssysteme: Eine Empfehlung der Sektion Herz-Kreislauf der Deutschen Interdisziplinären Vereinigung für Intensiv- und Notfallmedizin (DIVI) (im Druck)
- 2.Garcia J Thorac Cardiovasc Surg. 2011;142:755. doi: 10.1016/j.jtcvs.2011.07.029. [DOI] [PubMed] [Google Scholar]
- 3.Locker J Clin Anesth. 2003;15:441. doi: 10.1016/S0952-8180(03)00108-9. [DOI] [PubMed] [Google Scholar]
- 4.Brogan Intensive Care Med. 2009;35:2105. doi: 10.1007/s00134-009-1661-7. [DOI] [PubMed] [Google Scholar]
- 5.Zapol JAMA. 1979;242:2193. doi: 10.1001/jama.1979.03300200023016. [DOI] [PubMed] [Google Scholar]
- 6.Morris Am J Respir Crit Care Med. 1994;149:295. doi: 10.1164/ajrccm.149.2.8306022. [DOI] [PubMed] [Google Scholar]
- 7.Peek Lancet. 2009;374:1351. doi: 10.1016/S0140-6736(09)61069-2. [DOI] [PubMed] [Google Scholar]
- 8.Pham T, Combes A, Rozé H et al (2012) Extracorporeal membrane oxygenation for pandemic influenza A(H1N1) induced acute respiratory distress syndrome. A cohort study and propensity-matched analysis. Am J Respir Crit Care Med. DOI 10.1164/rccm.201205-0815OC [DOI] [PubMed]
- 9.Bernard Am J Respir Crit Care Med. 1994;149:818. doi: 10.1164/ajrccm.149.3.7509706. [DOI] [PubMed] [Google Scholar]
- 10.ARDS JAMA. 2012;307:2526. doi: 10.1001/jama.2012.5669. [DOI] [PubMed] [Google Scholar]
- 11.Kluge Dtsch Med Wochenschr. 2011;136:186. doi: 10.1055/s-0031-1272506. [DOI] [PubMed] [Google Scholar]
- 12.Deja J Int Med Res. 2008;36:211. doi: 10.1177/147323000803600201. [DOI] [PubMed] [Google Scholar]
- 13.Avalli ASAIO J. 2011;57:38. doi: 10.1097/MAT.0b013e3181fe5d0b. [DOI] [PubMed] [Google Scholar]
- 14.Beckmann Eur J Cardiothorac Surg. 2011;40:676. [Google Scholar]
- 15.Hazinski Circulation. 2010;122:250. doi: 10.1161/CIRCULATIONAHA.110.970897. [DOI] [Google Scholar]
- 16.Haneya Resuscitation. 2012;83:1331. doi: 10.1016/j.resuscitation.2012.07.009. [DOI] [PubMed] [Google Scholar]
- 17.Kagawa Resuscitation. 2010;81:968. doi: 10.1016/j.resuscitation.2010.03.037. [DOI] [PubMed] [Google Scholar]
- 18.Conseil Ann Fr Anesth Reanim. 2009;28:182. doi: 10.1016/j.annfar.2008.12.011. [DOI] [PubMed] [Google Scholar]
- 19.Bein Crit Care Med. 2006;34:1372. doi: 10.1097/01.CCM.0000215111.85483.BD. [DOI] [PubMed] [Google Scholar]
- 20.Zimmermann Crit Care. 2009;13:R10. doi: 10.1186/cc7703. [DOI] [PMC free article] [PubMed] [Google Scholar]


