Abb. 2.
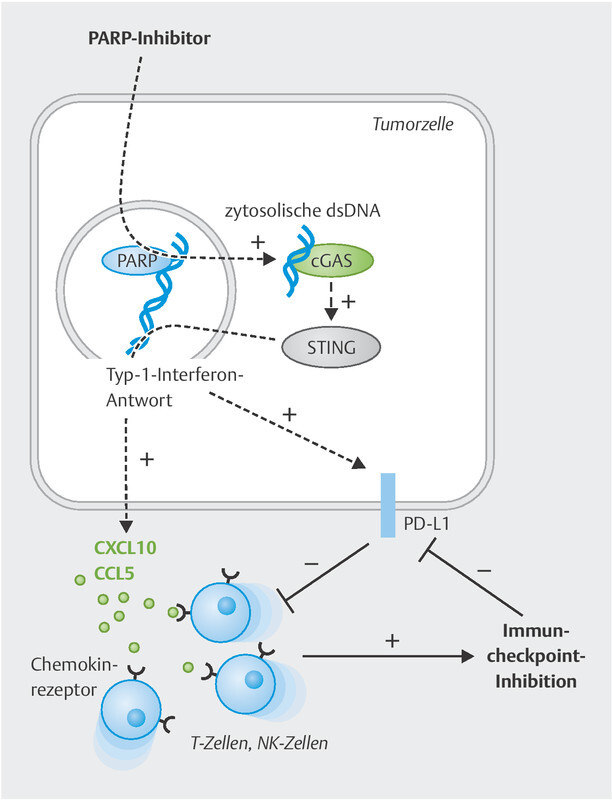
PARPi-vermittelte Tumorzelleffekte, die eine Kombinationstherapie mit einer Immuncheckpoint-Blockade ermöglichen. Inhibition der PARP führt (ähnlich wie ein BRCA1/2 -Funktionsverlust) zu einer Akkumulierung von Fragmenten doppelsträngiger DNA (dsDNA) im Zytosol der Tumorzelle. Hierdurch wird der cGAS/STING-Signalweg aktiviert, der letztlich eine Interferon-Antwort vom Typ I auslöst. Nachgeschaltet werden darüber hinaus u. a. Chemokine (CXCL10, CXCL11, CCL5) freigesetzt, die tumorsuppressive T- und NK-Zellen in den Tumor locken. Daneben wird aber auch die PD-L1-Expression im Tumormikromilieu hochreguliert. Sowohl die Rekrutierung von Immunzellen als auch die PD-L1-Induktion erlauben nun eine wirksame Immuncheckpoint-Blockade.
