Abstract
血管支架置入的介入治疗是心血管狭窄和堵塞普遍采用的治疗方法,但支架的传统制造方法如激光切割等工艺复杂且无法制造分叉支架等复杂结构,而三维(3D)打印技术为复杂结构及个性化血管支架制造提供了新的思路。本文采用3D打印技术和0~10 µm的316L不锈钢粉末材料打印制作了一种新型血管支架,对打印完成的血管支架进行电解抛光以去除支架表面粘附的粉末,并对抛光后的支架进行了球囊扩张及平面压缩实验。结果表明,本文设计的新型结构血管支架可采用3D打印技术制备;电解抛光去除了粘附的粉末,使支架表面粗糙度Ra由1.36 µm降低到了0.82 µm;抛光后的支架在球囊压力下外径由2.42 mm扩张到3.63 mm时的轴向缩短率为4.23%,卸载后径向回弹率为2.48%;支架的径向支撑力为8.32 N。3D打印血管支架可通过电解抛光去除表面粉末改善表面质量,并具有良好的扩张表现及径向支撑性能,为3D打印血管支架的实际应用提供了参考依据。
Keywords: 血管支架, 三维打印, 316L不锈钢, 电解抛光, 球囊扩张
Abstract
The interventional therapy of vascular stent implantation is a popular treatment method for cardiovascular stenosis and blockage. However, traditional stent manufacturing methods such as laser cutting are complex and cannot easily manufacture complex structures such as bifurcated stents, while three-dimensional (3D) printing technology provides a new method for manufacturing stents with complex structure and personalized designs. In this paper, a cardiovascular stent was designed, and printed using selective laser melting technology and 316L stainless steel powder of 0−10 µm size. Electrolytic polishing was performed to improve the surface quality of the printed vascular stent, and the expansion behavior of the polished stent was assessed by balloon inflation. The results showed that the newly designed cardiovascular stent could be manufactured by 3D printing technology. Electrolytic polishing removed the attached powder and reduced the surface roughness Ra from 1.36 µm to 0.82 µm. The axial shortening rate of the polished bracket was 4.23% when the outside diameter was expanded from 2.42 mm to 3.63 mm under the pressure of the balloon, and the radial rebound rate was 2.48% after unloading. The radial force of polished stent was 8.32 N. The 3D printed vascular stent can remove the surface powder through electrolytic polishing to improve the surface quality, and show good dilatation performance and radial support performance, which provides a reference for the practical application of 3D printed vascular stent.
Keywords: Vascular stent, Three-dimensional printing, 316L stainless steel, Electrolytic polishing, Balloon expansion
0. 引言
心血管疾病在我国城镇和乡村居民中引起的死亡占比分别为43.56%和45.91%[1],该病主要由动脉粥样硬化造成,是血液中的脂质聚集、纤维增生、钙质沉积和平滑肌细胞的过度增生导致血管壁增厚变硬,进而造成血管狭窄阻碍了血液的正常流通[2]。血管狭窄治疗方法主要分为药物治疗、外科手术治疗和介入治疗,血管支架置入的介入治疗是目前普遍采用的治疗方法[3]。血管支架的制造方式以预制管激光切割为主,但这种方式无法适配患者千差万别的病症,而且热加工产生的条纹、重铸层、微裂纹、残余拉伸和熔渣等热损伤,会降低支架生物相容性,易造成炎症和再狭窄等并发症[4]。三维(three-dimensional,3D)打印技术可以根据病灶部位特征设计制造专属支架,不需要预制细管及激光切割等复杂工艺,且未利用的材料可二次使用,为血管支架制造提供了新思路。
Veerubhotla等[5]采用3D打印技术制造了数百微米厚的三种水凝胶生物可降解血管支架,且具有足够的机械强度。Wen等[6]和Demir等[7]采用激光选区熔融的3D打印技术分别制造了金属锌和钴铬合金的血管支架,但对于支架力学性能等未做进一步的研究。Finazzi等[3]使用激光选区熔融的3D打印技术制造了钴铬合金支架,进行了支架的电解抛光及后续的球囊扩张实验,支架在球囊压力0~8 bar下扩张没有发生断裂,表现出了良好的扩张性能。陈姗姗等[8]对金属血管支架的临床应用进行了分析,指出316L不锈钢因力学性能优异、易加工及生物相容性好而被广泛用作血管支架材料。刘磊等[9]研究了金属支架激光切割工艺,结果表明采用316L不锈钢材料时,其切割面上粘附的熔渣颗粒容易通过酸洗而去除。
本文设计了一种新型血管支架,选用成本较低且粘附颗粒易去除的316L不锈钢粉末,采用激光选区熔融的3D打印技术制备,通过酸洗后的电解抛光去除表面粘附颗粒,提高表面光洁度,并且进行了球囊扩张实验以评估抛光后支架的扩张性能及径向回弹率和轴向缩短率,以及平面压缩实验以检测支架径向支撑性能。
1. 实验方案
1.1. 血管支架制备
1.1.1. 支架的设计
血管支架通常由支撑环和连接筋两部分组成,支撑环为血管支架在血管内提供径向支撑力,连接筋将相邻的支撑环进行连接且会影响支架柔顺性。血管支架能否在血管内服役,径向支撑力是重要评定因素。本文所设计支架的支撑环采用6个3组支撑单元交错排列的形式,每组支撑单元包含2个高度不同的支撑结构[10-11],支架两端支撑环为等高结构。连接筋采用直筋与弯曲筋沿轴向间隔分布的形式。直筋结构简单,但在支架扩张过程中不易沿轴向变形,从而使支撑环在扩张时引起的支架轴向缩短明显;弯曲筋可以降低支架扩张时的轴向缩短。根据激光选区熔融的3D打印工艺要求:悬垂距离不超过1 mm,倾角不超过45°,桥接距离不超过4 mm[12];同时考虑激光选区熔融技术的打印精度,支架筋宽设计为0.15 mm,壁厚0.15 mm;轴向长度为19.37 mm,外径2.4 mm,支架结构模型如图1所示。
图 1.
Stent structure model diagram
支架结构模型图
1.1.2. 支架的打印
使用金属3D打印机(琛维,AIXWAY Precision 100,德国),采用同心圆扫描策略,使激光束沿着预定的轨迹运动,获得所设计的血管支架。3D打印参数为激光功率200 W、光斑尺寸25 µm、打印速度1 200 mm/s、铺粉厚度10 µm、316L不锈钢粉末粒径0~10 µm。为防止打印过程中的氧化,采用氩气为保护气体。
1.1.3. 金相组织试样制备
对打印完成的血管支架进行镶嵌、研磨、抛光,并做腐蚀处理以观察金相组织。腐蚀液为HF∶HNO3∶H2O=20∶10∶70,腐蚀方式为腐蚀面向上并完全浸入腐蚀液中浸泡30 min,然后用饱和碳酸钠溶液清洗2~3 min以中和酸性,再用无水乙醇清洗,最后用热风吹干[13]。
1.2. 支架的抛光
血管支架的表面质量是支架应用的重要指标,良好的表面质量可以降低支架植入中的再狭窄风险,打印完成的支架表面粘附有粉末颗粒,可以通过电解抛光去除从而降低支架表面粗糙度。其具体步骤如下:
(1)支架酸洗:酸洗可以去除表面杂质和氧化物,且能够活化金属表面以利于抛光过程。酸洗液成分为HF∶HNO3∶H2O=3∶9∶88[14]。实验中将支架浸泡在40 ℃恒温水浴的酸洗液中20 min,然后用去离子水超声清洗5 min,取出自然风干后进行电解抛光。
(2)支架抛光:采用EP-06型电解抛光腐蚀仪对支架进行电解抛光,其装置示意图如图2a所示:支架作为阳极接电源正极,使用钛管作为阴极接电源负极。由于支架是柱状镂空结构,为消除阴阳极形状差异对抛光的影响,使支架抛光更均匀,阴极选用厚度3 mm、内径为82.4 mm钛管。为保证支架和钛管内表面距离为40 mm[15],在钛管上部固定了圆形透明塑料卡片,并将支架固定在钛管轴线上,确保电解抛光时支架轴线位于阴极钛管的中心,钛管长度大于支架长度。电解抛光在70 ℃恒温水浴下进行,抛光液成分为H2SO4∶H3PO4∶H2O=35∶45∶20[16-17],电压10 V,抛光时间15 s。
图 2.
Schematic diagram of experimental device
实验装置示意图
a. 电解抛光;b. 球囊扩张
a. electrolytic polishing; b. balloon expansion
(3)使用扫描电镜(日立HITACHI,SU8200,日本)和3D表面轮廓仪(中图仪器,Sper View W1,中国)对抛光后支架的表面形貌和粗糙度进行分析测量。
1.3. 支架的球囊扩张
使用球囊扩张导管(江苏常美医疗器械有限公司,PB-20E-0420,中国)和压力泵(江苏常美医疗器械有限公司,BI-20A-10,中国)对支架进行扩张,其中球囊工作压力为8 bar,最大耐压为10 bar,球囊最大扩张直径为4 mm,并使用立体显微镜(HW4K,深圳市显微精工科技有限公司,中国)记录支架的扩张过程,其实验装置示意图如图2b所示。支架外径由2.4 mm扩张到3.6 mm左右过程中,球囊内压每增加1 bar,测量一次支架的几何尺寸,包括支架两端及中间直径和支架长度。本研究对三个电解抛光后的支架进行了扩张实验。
1.4. 支架的径向支撑
支架的径向支撑性能是其重要性能指标,测试方法有平面压缩法、V型槽压缩法和径向压缩法。径向压缩法可以直接表达支架外径与所受载荷的关系,但设备复杂且扇形块摩擦影响精度,平面压缩法和V型槽压缩法所需设备简单,成本低精度高,其中平面压缩法更适合用于不同外径、不同结构的支架,同时三种测试方法得到的载荷-位移曲线整体趋于一致[18],因此本试验采用平面压缩法测试支架的径向支撑性能。实验仪器为高精度生物力学试验机(ElectroForce Systems Group,ElectroForce 3200 Series,美国),球囊扩张后的血管支架放置在支撑板上,其中上压板以0.15 mm/min的速率向下压缩,获得支架平面压缩实验的载荷-位移曲线。同时采用激光切割方法制作了本文所设计的支架,进行球囊扩张及后续的平面压缩实验,与3D打印支架的径向支撑性能进行对比。
2. 结果
2.1. 3D打印血管支架
2.1.1. 3D打印血管支架
图3为激光选区熔融技术打印的血管支架,可以看出在无额外支撑结构情况下,血管支架各结构打印完整且无宏观缺陷,支架的外径和内径分别为2.45 mm和2.07 mm,相较于设计尺寸的2.40 mm和2.10 mm,存在0.05 mm和−0.03 mm的偏差。
图 3.
3D printed stent
3D打印血管支架
2.1.2. 打印支架组织
3D打印支架径丝的金相组织如图4所示,可以看出明显熔池在支架内部相互交错重叠;支架径丝无明显缺陷但内部存在气孔,大部分气孔为球型而少部分为不规则形状,通常是能量输入过多或者工艺条件不稳定导致气体被困形成的[19],这些气孔的存在会降低材料强度并影响支架的力学性能[20-21]。
图 4.
Stent metallographic structure
支架金相组织
2.2. 3D打印血管支架电解抛光
血管支架的扫描电镜图如图5所示,可以看出未抛光时支架表面粘附有较多不锈钢粉末颗粒,同时存在明显的金属液凝固的痕迹,主要是采用激光选区熔融的3D打印工艺制备支架时由于金属粉末熔融后凝固产生,这些粘附颗粒和凝固痕迹对支架表面粗糙度产生较大影响。抛光后支架表面粘附的粉末颗粒被完全去除,激光熔融导致的金属液态凝固痕迹也得到了明显改善。支架直筋三维形貌和参数分析如图6所示,支架表面的最大高度差由抛光前12 µm降为抛光后的6 µm,降幅达到50%,且支架表面参数分析曲线趋势由抛光前的峰状波动变为阶梯式,三条分析曲线取平均值得出:支架表面粗糙度Ra由1.36 µm降低到0.82 µm,Rz由6.59 µm降低到2.53 µm。
图 5.
Scanning electron microscopy images of stent
血管支架的扫描电镜图
图 6.

3D topography and parameter analysis of the surface of a straight strut of the stent
支架直筋表面的三维形貌及参数分析
2.3. 支架的扩张性能
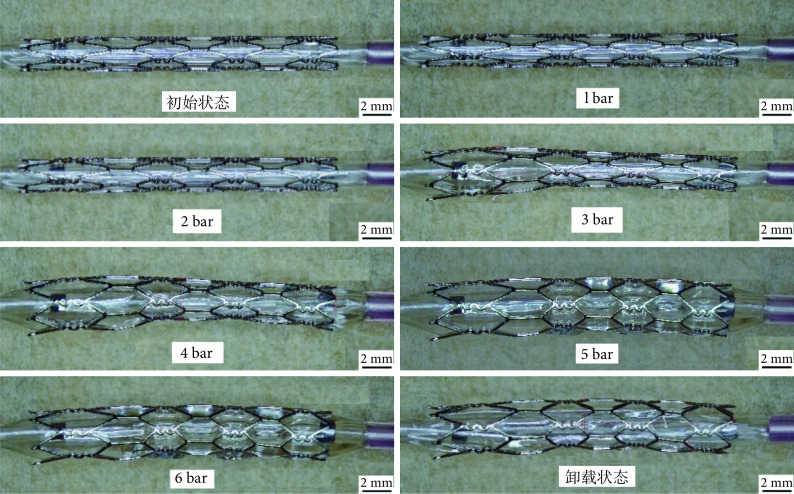
图7为支架球囊扩张过程,图8为支架扩张过程的外径及轴向长度变化曲线。在球囊压力0~2 bar时支架直径和长度均无明显变化;在压力2~3 bar时支架由左端率先开始扩张,中间和右端几乎无扩张,这可能是支架左端的弯曲连接筋在从打印基板取下时发生了形变,导致弯曲筋长度增长从而强度降低;在压力3~4 bar时支架的中间和右端开始扩张且扩张趋势相同;在压力4~5 bar时支架左端扩张趋势趋于平缓,但支架中间和右端扩张速率变大且支架整体直径趋于一致;在达到6 bar时支架外径由原来的2.42 mm扩张到3.63 mm,扩张率接近50%且结构无断裂。球囊压力卸去后,支架外径回弹到3.54 mm,由式(1)得到支架的径向回弹率为2.48%,这有利于支架释放后更好地与血管壁贴合以提高支架的径向支撑性能;支架长度由初始的21.74 mm缩短到卸载后的20.82 mm,由式(2)得到支架的轴向缩短率为4.23%,表明该支架有良好的扩张性能。
图 7.
Expansion of the stent via balloon inflation
支架的球囊扩张图
图 8.
Plot of stent size versus balloon pressure
支架尺寸与球囊压力曲线图
 |
1 |
式中,R为径向回弹率,D为球囊扩张后的支架外径,d为球囊卸载后的支架外径。
 |
2 |
式中, 为轴向缩短率,L为支架初始状态长度,L1为卸载后支架的长度[22]。
为轴向缩短率,L为支架初始状态长度,L1为卸载后支架的长度[22]。
2.4. 支架的径向支撑力
血管支架平面压缩测试的载荷-位移曲线如图9所示,可以看出在压缩过程中,激光切割支架的压缩载荷随着下压量增大而快速增加,而3D打印支架的压缩载荷随着下压量增加,先快速增长而后趋于平缓。取压缩量为支架外径的一半时位移所对应的载荷为支架的径向支撑力[11],3D打印支架的径向支撑力为8.32 N,远小于激光切割支架的径向支撑力19.36 N,这可能是打印支架内部气孔造成的材料强度不足,在后续需要不断优化打印工艺以提高打印支架的强度。
图 9.
Force-displacement curve of stent plane compression
支架平面压缩的载荷-位移曲线
3. 结论
本文采用激光选区熔融的3D打印技术和粉末粒径为0~10 µm的316L不锈钢制备了一种新型血管支架,并进行了电解抛光、球囊扩张及平面压缩实验。得出主要结论如下:
(1)使用0~10 µm的316L不锈钢金属粉末,采用激光选区熔融3D打印技术可以制备新型血管支架,新型支架结构设计合理。
(2)电解抛光可以去除表面粘附粉末颗粒,有效地改善支架的表面质量,支架表面粗糙度Ra由1.36 µm降低到0.82 µm,Rz由6.59 µm降低到2.53 µm。
(3)支架具有良好的性能,初始直径为2.43 mm的支架在6 bar的球囊压力下扩张到3.63 mm而没有发生破坏;卸载后径向回弹率为2.48%,轴向缩短率为4.23%;3D打印支架径向支撑力为8.32 N。
重要声明
利益冲突声明:本文全体作者均声明不存在利益冲突。
作者贡献说明:陈志昂负责论文撰写、实验实施与数据分析等;苗京涛负责血管支架结构设计;汪琪龙负责支架的平板压缩实验;黄素霞负责支架3D打印及性能检测指导;曹晶晶负责支架电化学抛光实验设计及实施指导;李河宗负责支架结构设计、实验方案制订、数据分析指导等;赵利果负责支架结构设计、力学性能评估指导等;袁江永负责支架结构、表面状态及力学性能临床应用可能性评估指导。
Funding Statement
中华人民共和国科学技术部项目(G2021003007L)
Project Fund of the Ministry of Science and Technology of the People’s Republic of China
References
- 1.中国心血管健康与疾病报告编写组 中国心血管健康与疾病报告2019概要. 中华老年病研究电子杂志. 2020;7(4):4–15. [Google Scholar]
- 2.Momiyama Y, Ishzakka N, Adachi H, et al Inflammation, atherosclerosis and coronary artery disease. Clin Med Insights. 2014;8:67–70. doi: 10.4137/CMC.S39423. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 3.Finazzi V, Demir A G, Biffi C A, et al Design and functional testing of a novel balloon-expandable cardiovascular stent in CoCr alloy produced by selective laser melting. J Manuf Processes. 2020;55:161–173. doi: 10.1016/j.jmapro.2020.03.060. [DOI] [Google Scholar]
- 4.Guerra A, Ciurana J 3D-printed bioabsordable polycaprolactone stent: The effect of process parameters on its physical features. Mater Design. 2018;137:430–437. doi: 10.1016/j.matdes.2017.10.045. [DOI] [Google Scholar]
- 5.Veerubhotla K, Lee Y Y, Lee C H Parametric optimization of 3D printed hydrogel-based cardiovascular stent. Pharm Res. 2021;38(5):885–900. doi: 10.1007/s11095-021-03049-1. [DOI] [PubMed] [Google Scholar]
- 6.Wen Peng, Voshage M, Jauer L, et al Laser additive manufacturing of Zn metal parts for biodegradable applications: Processing, formation quality and mechanical properties. Mater Design. 2018;155:36–45. doi: 10.1016/j.matdes.2018.05.057. [DOI] [Google Scholar]
- 7.Demir A G, Previtali B Additive manufacturing of cardiovascular CoCr stents by selective laser melting. Mater Design. 2017;119:338–350. doi: 10.1016/j.matdes.2017.01.091. [DOI] [Google Scholar]
- 8.陈姗姗, 张炳春, 杨柯 医用无镍不锈钢在血管支架领域的研究进展. 中国医疗设备. 2018;33(5):14–17. [Google Scholar]
- 9.刘磊, 李东波, 童一飞, 等 血管支架的激光加工工艺及研究进展. 热加工工艺. 2017;46(5):15–18. [Google Scholar]
- 10.张宏辉, 冯海全, 李治国, 等 镁合金冠脉支架支撑性能分析及其优化. 医用生物力学. 2019;34(1):14–20. [Google Scholar]
- 11.魏云波, 赵丹阳, 王敏杰, 等 高径向支撑性可生物降解聚合物血管支架结构设计与力学性能分析. 中国机械工程. 2020;31(9):1098–1107. [Google Scholar]
- 12.Finazzi V, Demir A G, Biffi C A, et al Design rules for producing cardiovascular stents by selective laser melting: Geometrical constraints and opportunities. Procedia Structur Integr. 2019;15:16–23. doi: 10.1016/j.prostr.2019.07.004. [DOI] [Google Scholar]
- 13.蒋华臻, 房佳汇钰, 陈启生, 等 激光选区熔化成形316l不锈钢工艺、微观组织、力学性能的研究现状. 中国激光. 2022;49(14):309–329. [Google Scholar]
- 14.Kao J K, Lin Shengyao, Chen Y S Surface processing technology for 316LVM stainless steel stents. J Appl Sci Eng. 2018;21(3):343–350. [Google Scholar]
- 15.杨希明, 侯章垒 超薄不锈钢基材连续电解抛光工艺的优化. 电镀与涂饰. 2017;36(13):689–695. [Google Scholar]
- 16.Sojitra P, Engineer C, Kothwala D, et al Electropolishing of 316LVM stainless steel cardiovascular stents: An investigation of material removal, surface roughness and corrosion behaviour. Trends Biomater Artif Organs. 2010;23(3):115–121. [Google Scholar]
- 17.Han Wei, Fang Fengzhou Orientation effect of electropolishing characteristics of 316L stainless steel fabricated by laser powder bed fusion. Front Mech Eng. 2021;16:580–598. doi: 10.1007/s11465-021-0633-7. [DOI] [Google Scholar]
- 18.魏云波, 王敏杰, 赵丹阳, 等 可降解聚合物血管支架体外力学性能测试实验研究. 生物医学工程学杂志. 2019;36(4):604–612. doi: 10.7507/1001-5515.201812009. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 19.季文彬, 徐立奎, 戴士杰, 等 激光选区熔化成型316L不锈钢的工艺参数对硬度与微观组织的影响. 材料导报. 2021;35(22):22125–22131. doi: 10.11896/cldb.20070232. [DOI] [Google Scholar]
- 20.姚讯杰, 王佳玮, 杨雁程, 等 金属构件激光增材制造缺陷产生机理及控制机制探究. 中国激光. 2022;49(14):286–296. [Google Scholar]
- 21.Zhang Bi, Li Yongtao, Bai Qian Defect formation mechanisms in selective laser melting: A review. Chin J Mech Eng. 2017;30:515–527. doi: 10.1007/s10033-017-0121-5. [DOI] [Google Scholar]
- 22.张园园, 颜文涛, 李建军, 等 不同结构的左旋聚乳酸冠脉支架的力学行为研究. 生物医学工程学进展. 2021;42(22):63–67. doi: 10.3969/j.issn.1674-1242.2021.02.001. [DOI] [Google Scholar]