Abstract
体外力学性能测试是评估血管支架安全性和有效性的主要手段,其性能指标具有重要的临床意义。本文对比分析了可降解聚合物血管支架径向支撑性能测试的平面压缩法、V 型槽压缩法和径向压缩法,并研究了压缩速率和压缩周向位置对支撑性能测试结果的影响,采用三点弯曲法研究了压缩速率和压缩周向位置对柔顺性能测试结果的影响。选取最优测试方案,测试了本文在不同外径(1.4、1.7、2.4 mm)下设计的三种支架和生物可降解聚合物血管支架(BVS)(BVS1.1,Abbott Vascular,美国)的支撑性能和柔顺性能。结果表明,三种支撑性能测试方法得到的压缩载荷—压缩位移曲线整体趋势一致,但归一化支撑力差异较大;平面压缩法更适合对不同外径、不同结构血管支架的支撑性能进行对比测试;压缩速率对支撑性能和柔顺性能测试结果无显著影响;压缩周向位置对采用平面压缩法、V 型槽压缩法测试支撑性能和采用三点弯曲法测试柔顺性能有较大影响。综合比较,本文所设计的三种支架相对 BVS 支架其径向支撑性能均有不同程度的提高。本研究对血管支架的力学性能测试具有一定的指导意义和参考价值。
Keywords: 生物可降解聚合物, 血管支架, 体外性能测试, 径向支撑性能, 柔顺性能
Abstract
In vitro experimental test for mechanical properties of a vascular stent is a main method to evaluate its effectiveness and safety, which is of great significance to the clinical applications. In this study, a comparative study of planar, V-groove and radial compression methods for the radial support property test were performed, and the effects of compression rate and circumferential position on the test results were conducted. Based on the three-point bending method, the influences of compression rate and circumferential position on flexibility were also explored. And then a best test proposal was selected to evaluate the radial support property and flexibility of the three self-designed stents and the comparative biodegradable vascular stent (BVS) (BVS1.1, Abbott Vascular, USA) with different outside diameters of 1.4 mm, 1.7 mm and 2.4 mm. The results show that the developing trends of the compression load with the compression displacement measured by the three radial support property test methods are the same, but normalized radial force values are quite different. The planar compression method is more suitable for comparing the radial support properties of stents with different diameters and structures. Compression rate has no obvious effect on the testing results of both the radial support property and flexibility. Compression circumferential position has a great impact on testing radial support property with the planar or V-groove compression methods and testing flexibility with three-point bending method. The radial support properties of all the three self-designed stents are improved at a certain degree compared to that of the BVS stent. The study has better guide significance and reference value for testing mechanical properties of vascular stents.
Keywords: biodegradable polymer, vascular stent, in vitro mechanical test , radial support property, flexibility
引言
体外力学性能测试是获得血管支架力学性能参数的重要方法,也是检验血管支架安全性和有效性的主要手段[1]。可降解聚合物血管支架避免了传统血管支架永久留在体内而导致的晚期支架内再狭窄等问题,是血管支架领域的重要研究方向[2]。但是,目前对可降解聚合物血管支架力学性能测试的研究较少,有关血管支架的力学性能测试大多是针对传统的裸金属支架和药物洗脱支架开展相应研究[3-7]。聚合物材料与金属材料的力学性能差异很大,传统金属血管支架的力学性能测试方法不一定完全适用于可降解聚合物血管支架[8]。由于可降解聚合物血管支架力学性能弱、结构多样,相对传统的裸金属支架和药物洗脱支架,聚合物支架的力学性能测试仍具有一定的挑战性[9]。Grabow 等[8]设计并制备了内径为 2.8 mm,壁厚为 0.3 mm 的聚左旋乳酸/聚—4—羟基丁酸酯血管支架,采用液压径向压缩法对其径向支撑性能进行了测试。测试结果表明,所设计的血管支架具有良好的径向支撑性能。Wang 等[10]采用扇形块径向压缩法和三点弯曲法对外径 3.4 mm,壁厚 0.15 mm 的聚乳酸血管支架的径向支撑性能和柔顺性能进行了测试,测试结果与有限元计算结果具有较好的一致性。Zhao 等[11]、Li 等[12]采用局部压缩法分别测试了所设计的内径为 8 mm,外径约为 9.5 mm 编织型聚二氧六环酮血管支架和内径为 6 mm 的聚乳酸/聚己内酯复合血管支架的径向支撑性能,但是该方法得到的测试结果只能反映支架轴向局部位置的径向支撑性能。通过以上研究可以看出,目前对可降解聚合物血管支架的径向支撑性能和柔顺性能测试已取得一定进展,但是这些研究在测试时仅采用某一特定实验方法和特定实验条件,有关不同测试方法和测试条件对这两个性能测试结果影响的研究尚有待完善。同时,相关研究大多是针对同一血管支架的某一单项性能进行研究,缺少对不同尺寸、不同结构血管支架的多性能指标的综合研究和评价。此外,上述研究所测试血管支架的直径或壁厚远大于实际血管支架尺寸,而实际血管支架的尺寸通常直径小于 3.5 mm,壁厚小于 0.15 mm[13],这一客观差异导致测试结果与实际可降解聚合物血管支架的力学性能存在相应差异。因此,对可降解聚合物血管支架力学性能的测试有待进一步研究。
针对以上问题,本文研究了可降解聚合物血管支架径向支撑性能测试的平面压缩法、V 型槽压缩法和径向压缩法,以及每一方法中压缩速率和压缩周向位置对径向支撑性能测试结果的影响,同时采用三点弯曲法研究了压缩速率和压缩周向位置对柔顺性能测试结果的影响。然后本文选取最优测试方案,对不同外径下本文所设计的三种可降解聚合物血管支架以及雅培公司的生物可降解血管支架(bioresorbable vascular scaffolds,BVS)(BVS1.1,Abbott Vascular,美国)的径向支撑性能和柔顺性能进行了测试。同时,为分析所设计三种血管支架的综合力学性能,通过扩张实验测试了这些血管支架的径向回缩性能和轴向短缩性能。通过以上研究,本文结果或对血管支架的力学性能测试具有一定的指导意义和参考价值。
1. 血管支架力学性能
血管支架的径向回缩性能、轴向短缩性能、径向支撑性能和柔顺性能通常分别由径向回缩率、轴向短缩率、归一化支撑力和弯曲刚度来表征。
1.1. 径向回缩性能
径向回缩性能指从球囊扩张到球囊卸载后,血管支架的直径尺寸变化,通常用径向回缩率表示,其计算公式如式(1)所示[14]:
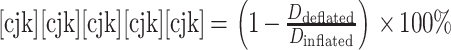 |
1 |
式中 Ddeflated 为球囊卸载后支架的外径,Dinflated 为球囊扩张后支架的外径。
1.2. 轴向短缩性能
轴向短缩性能通常用轴向短缩率表示,指血管支架从非展开状态至扩张到标称直径后长度的变化比,其计算公式如式(2)所示[15]:
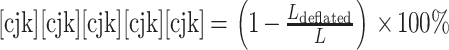 |
2 |
式中 L 为支架非展开状态长度,Ldeflated 为球囊卸载后支架的长度。
1.3. 径向支撑性能
径向支撑性能指血管支架抵抗血管壁收缩的能力。用压缩量为卸载后支架外径的 50% 时所对应的压缩载荷来表示支架的径向支撑性能[16]。根据美国材料与试验协会(American Society for Testing Materials,ASTM)标准 F3067-14[17],为使不同支架的径向支撑性能具有可比性,将力载荷进行归一化处理,其计算公式如式(3)所示:
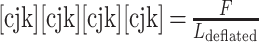 |
3 |
式中
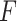 为实测压力值,Ldeflated 为球囊卸载后支架的长度。
为实测压力值,Ldeflated 为球囊卸载后支架的长度。
1.4. 柔顺性能
柔顺性能是指血管支架的轴向弯曲能力,可通过三点弯曲实验获得,用弯曲刚度来量化表征,计算公式如式(4)所示[18]:
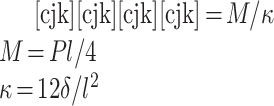 |
4 |
式中 M 为跨中弯矩,
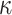 为跨中曲率,P 为压缩载荷,
为跨中曲率,P 为压缩载荷,
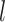 为跨距,
为跨距,
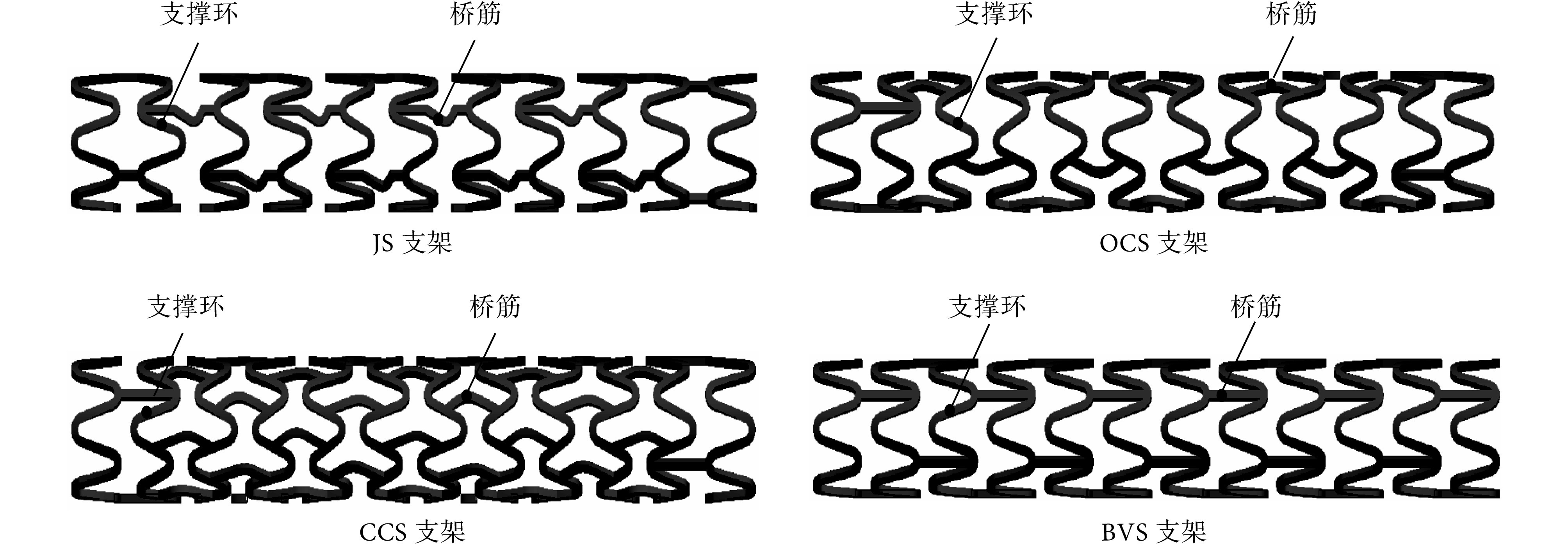
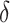 为压缩量。
为压缩量。
2. 实验条件和测试方法
2.1. 可降解聚合物血管支架类型
使用聚乳酸(Ingeo 4032D,NatureWorks LLC,美国)原料,挤出成型外径为 1.4、1.7、2.4 mm 的聚乳酸微管,采用飞秒激光技术雕刻出本文所设计的 J 型支架(J-shaped stent,JS)、开放式 C 型支架(open C-shaped stent,OCS)、密闭式 C 型支架(closed C -shaped stent,CCS)以及对比 BVS 支架(BVS1.1,Abbott Vascular,美国),其结构如图 1 所示。挤出设备为单螺杆挤出机(HPE-100H,Davis-Standard LLC,美国),雕刻设备为激光雕刻机(Starfemoto,Coherent-ROFIN Co. Ltd.,美国)。
图 1.
Models of four vascular stents
四种血管支架模型
聚乳酸微管的壁厚均匀度大于 93%,椭圆度小于 2.1%。激光雕刻后的血管支架筋宽一致性小于 ± 5 μm,无热影响区。不同外径和不同结构血管支架的尺寸如表 1 所示。
表 1. Dimensions of stents with different outside diameters and structures.
不同外径、不同结构血管支架的尺寸
| 支架类型 | 外径/mm | 壁厚/mm | 长度/mm |
| JS 支架 | 1.4 | 0.11 | 9.1 |
| 1.7 | 0.16 | 11.4 | |
| 2.4 | 0.14 | 16.1 | |
| OCS 支架 | 1.4 | 0.11 | 8.8 |
| 1.7 | 0.16 | 11.1 | |
| 2.4 | 0.14 | 15.5 | |
| CCS 支架 | 1.4 | 0.11 | 8.9 |
| 1.7 | 0.16 | 11.2 | |
| 2.4 | 0.14 | 15.7 | |
| BVS 支架 | 1.4 | 0.11 | 9.1 |
| 1.7 | 0.16 | 11.4 | |
| 2.4 | 0.14 | 16.1 |
2.2. 径向回缩性能和轴向短缩性能测试方法
对血管支架进行扩张实验可获得其径向回缩性能和轴向短缩性能,测试方法参见标准 ASTM F2079-09[14]和 ASTM F2081-06[15]。扩张装置为球囊扩张导管(Quantum-Maverick 2 Monorail,Boston Scientific,美国),充压装置为压力泵[LP-P-30S,乐普(北京)医疗器械公司,中国],尺寸测量设备为工具显微镜(VTM-3020F,苏州欧卡精密光学仪器公司,中国),测量精度 ± 0.001 mm。其中,外径为 1.4、1.7、2.4 mm 的血管支架分别用规格为 2.0 × 15、2.5 × 20、3.0 × 25 mm 的球囊扩张导管进行扩张。
2.3. 径向支撑性能测试方法
血管支架径向支撑性能测试方法主要有平面压缩法、V 型槽压缩法和径向压缩法,如图 2 所示。平面压缩法是指将球囊卸载后的血管支架放置于上、下两平面压板之间进行压缩。V 型槽压缩法是在平面压缩法的基础上,对下压板开设 V 型槽结构,测试时将球囊卸载后的血管支架置于 V 型槽内。径向压缩法指通过扇形块对球囊卸载后的支架外表面施加均匀的径向载荷。首先,选取任一外径、任一结构血管支架为研究对象,对比分析这三种测试方法以及每一种方法下压缩速率和压缩周向位置对测试结果的影响。根据前期实验可知,采用不同外径、不同结构血管支架得出的结论一致。因此,本文以外径为 2.4 mm 的 CCS 支架为例展开讨论。然后选用最优的测试方案测试了本文所设计的三种支架和 BVS 支架的支撑性能。每一种测试均应至少对 3 个试样进行测量,并取其算数平均值。
图 2.
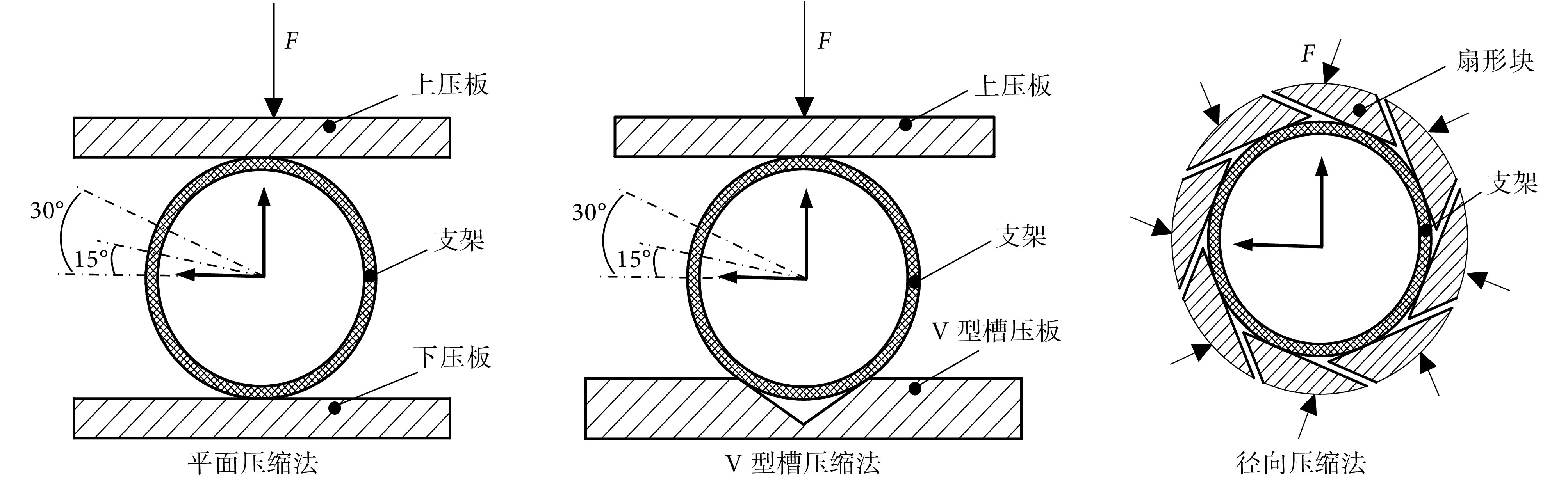
Schematic diagrams of distinct testing methods for radial support property
不同径向支撑性能测试方法示意图
2.3.1. 平面压缩法
实验设备为电脑伺服拉压力材料试验机(HD-B609B-S,东莞市海达仪器有限公司,中国)和平面压缩夹具。具体操作步骤为:
(1)上压板分别以 0.1、0.3、0.5、1.0 mm/min 的速率对支架进行压缩,得到不同压缩速率下压缩载荷−压缩位移曲线。
(2)根据步骤(1)的测试结果,选取最优的压缩速率,分别对支架周向 0°、15°、30° 进行压缩,如图 2 所示,得到不同压缩周向位置下压缩载荷−压缩位移曲线。
2.3.2. V 型槽压缩法
实验设备为电脑伺服拉压力材料试验机(HD-B609B-S,东莞市海达仪器有限公司,中国)和 V 型槽压缩夹具。具体操作步骤为:
(1)上压板分别以 0.1、0.3、0.5、1.0 mm/min 的速率对支架进行压缩,得到不同压缩速率下压缩载荷−压缩位移曲线。
(2)根据步骤(1)的测试结果,选取最优的压缩速率,分别对支架周向 0°、15°、30° 进行压缩,如图 2 所示,得到不同压缩周向位置下压缩载荷−压缩位移曲线。
2.3.3. 径向压缩法
实验设备为径向压握机(TTR2,Blockwise Engineering LLC,美国)。具体操作步骤为:扇形块分别以 0.05、0.15、0.25、0.50 mm/min 的速率对支架进行压缩,得到压缩载荷−外径曲线。因扇形块在压握过程中存在自摩擦,测试前应以相应的测试速率空运行一次,获取基础摩擦力曲线,支架的真实压缩载荷为实测值减去基础摩擦力。
对比三种测试方法,平面压缩法和 V 型槽压缩法所需设备简单、成本低且精度高,同时能够反映出支架不同周向位置抗压能力的差异,然而这两种方法只能侧面反映支架的支撑性能。其中,对于 V 型槽压缩法,因不同外径的支架与 V 型槽的接触角和嵌入 V 型槽的深度不同,因此无法对不同外径支架的支撑性能进行比较测试。而径向压缩法可以直接表达出支架的外径与所受径向载荷的关系,也可以实现对不同外径支架的支撑性能进行比较测试,但是不能体现出周向位置抗压能力的差异。此外,径向压缩法的测试设备结构复杂,扇形块间的自摩擦和支架与扇形块间的摩擦对测试结果均有一定影响,对于支撑性能较弱的支架甚至不能满足测试要求[17, 19]。
2.4. 柔顺性能测试方法
实验设备为电脑伺服拉压力材料试验机(HD-B609B-S,东莞市海达仪器有限公司,中国)和三点弯曲夹具。选取任一外径、任一结构血管支架为研究对象,分析压缩速率和压缩周向位置对测试结果的影响。根据前期实验可知,采用不同外径、不同结构血管支架得出的结论一致。因此,本文仍以外径为 2.4 mm 的 CCS 支架为例展开讨论。具体操作步骤为:
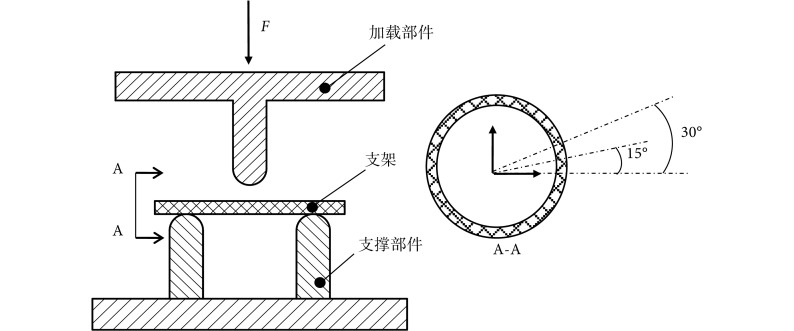
(1)将扩张后的支架放置于支撑部件上,如图 3 所示。加载部件分别以 0.1、0.3、0.5、1.0 mm/min 的速率对支架进行压缩,得到不同压缩速率下跨中弯矩—跨中曲率曲线。
图 3.
Schematic diagram of testing flexibility
柔顺性能测试示意图
(2)根据步骤(1)的测试结果,选取最优压缩速率,分别对支架周向 0°、15°、30° 进行压缩,得到不同压缩周向位置下跨中弯矩—跨中曲率曲线,如图 3 所示的 A-A 向视图。
(3)选取最优的测试方案,对不同外径下本文所设计的三种支架和 BVS 支架的柔顺性能进行测试。
因不同外径支架的长度差异较大,测试时原始外径为 1.4、1.7、2.4 mm 的支架对应的跨距分别为 4.0、6.0、8.0 mm。每一种测试均应至少对 3 个试样进行测量,并取其算数平均值。
3. 实验结果和讨论
3.1. 径向回缩性能和轴向短缩性能实验
根据支架扩张实验,可以得到不同外径下 JS 支架、OCS 支架、CCS 支架和 BVS 支架的径向回缩率和轴向短缩率,如表 2 所示。
表 2. Radial recoil and axial foreshortening of stents with diffe rent outside diameters and structures.
不同外径、不同结构支架的径向回缩率和轴向短缩率
| 支架类型 | 外径/mm | 径向回缩率 | 轴向短缩率 | 扩张比 |
| JS 支架 | 1.4 | 7.8% ± 0.5% | – 1.7% ± 0.2% | 69% |
| 1.7 | 7.5% ± 0.5% | – 1.8% ± 0.3% | 81% | |
| 2.4 | 8.5% ± 0.4% | – 1.4% ± 0.4% | 39% | |
| OCS 支架 | 1.4 | 7.3% ± 0.4% | – 2.3% ± 0.3% | 69% |
| 1.7 | 7.1% ± 0.7% | – 2.5% ± 0.3% | 81% | |
| 2.4 | 8.3% ± 0.4% | – 2.1% ± 0.2% | 39% | |
| CCS 支架 | 1.4 | 7.3% ± 0.3% | – 2.3% ± 0.2% | 69% |
| 1.7 | 7.0% ± 0.4% | – 2.5% ± 0.3% | 81% | |
| 2.4 | 7.9% ± 0.5% | – 2.2% ± 0.3% | 39% | |
| BVS 支架 | 1.4 | 10.1% ± 0.6% | 1.6% ± 0.2% | 69% |
| 1.7 | 9.8% ± 0.6% | 1.8% ± 0.2% | 81% | |
| 2.4 | 10.6% ± 0.5% | 1.5% ± 0.3% | 39% |
3.1.1. 径向回缩性能
如表 2 所示,同一外径下,本文所设计三种支架的径向回缩率近似相同,相对 BVS 支架降低了 20% 以上。同一结构、不同外径时,外径为 1.7 mm 时支架的径向回缩率最小,外径为 2.4 mm 时最大,其原因是不同外径支架在膨胀过程中扩张比不同。外径为 1.4、1.7、2.4 mm 的支架分别用规格为 2.0 × 15、2.5 × 20、3.0 × 25 mm 的球囊导管扩张,则扩张比分别为 69%、81%、39%,如表 2 所示。其中,外径为 1.7 mm 的支架,扩张比最大,支架发生塑性变形的区域最大、弹性变形的区域最小,因此支架在球囊卸载后,发生因弹性变形引起的径向回缩最小,从而径向回缩率最小。相反,外径为 2.4 mm 的支架,扩张比最小,因此径向回缩率最大。
3.1.2. 轴向短缩性能
如表 2 所示,同一外径下 BVS 支架的轴向短缩率最大,本文所设计的三种支架的轴向短缩率为负值,说明其非但没有发生轴向缩短且有所伸长。同一结构、不同外径时,外径为 1.7 mm 时支架轴向变化量(伸长或短缩)最大,外径为 2.4 mm 时最小。其原因是扩张比越大,球囊扩张后支架径向变形越大,球囊卸载后径向回缩越小,导致支架最终的径向变形越大,即轴向变形越严重。
3.2. 径向支撑性能实验
3.2.1. 平面压缩法实验
(1)压缩速率对测试结果的影响
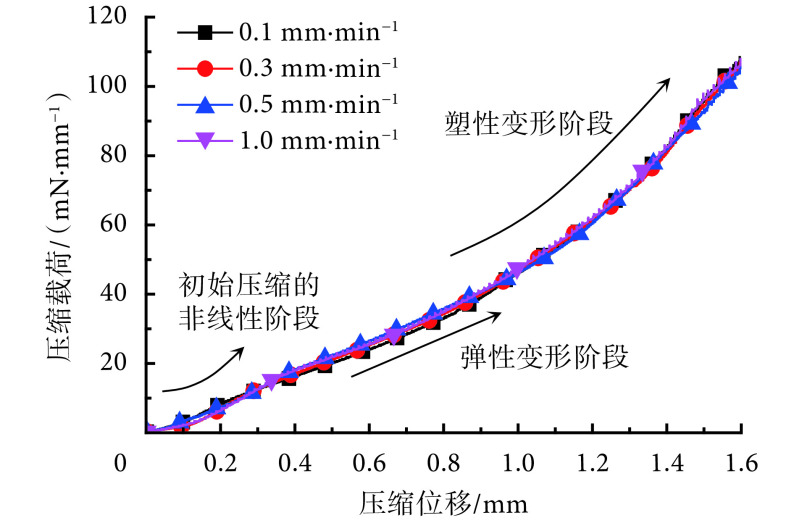
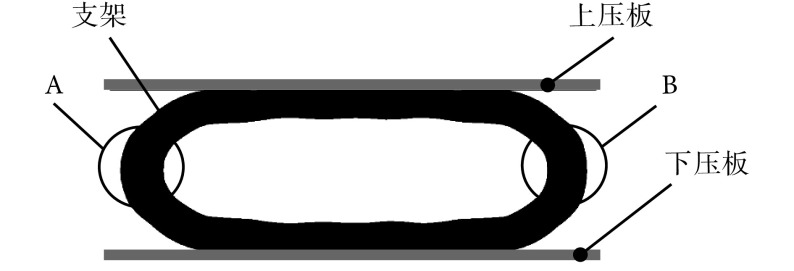
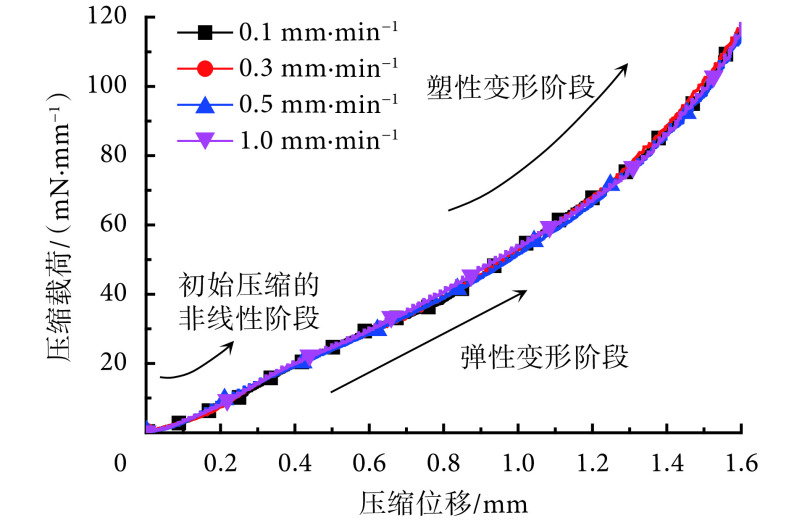
不同压缩速率下压缩载荷—压缩位移曲线如图 4 所示。支架在压缩过程中主要经历了三个阶段:① 初始压缩的非线性阶段,该阶段支架与上压板尚未完全接触;② 弹性变形阶段,此时支架与上压板已完全接触,压缩载荷随着压缩量近似呈线性增长;③ 塑性变形阶段,随着变形量继续增大,支架开始发生塑性变形,压缩载荷呈非线性增长,且增长速率逐渐提高。增长速率提高的原因一方面是在塑性变形过程中,支架出现应变强化现象,另一方面是当支架变形量较大时,支架局部位置 A、B 的筋相互接触阻碍其继续变形,如图 5 所示。根据公式(3)可知,不同压缩速率所测得的平均归一化支撑力为(89.90 ± 0.82)mN/mm,显然,压缩速率对支撑性能无显著影响。但是压缩速率不能过大,否则移动部件惯性会导致测试曲线波动较大;同时压缩速率也不能过小,以避免静摩擦引起的粘结,同时可以提高实验效率[17]。根据实验结果以及前期实验的探索,压缩速率在 0.1~0.3 mm/min 之间为宜。
图 4.
Compressive load- displacement curves at different com pression rates using planar compression method
平面压缩法中不同压缩速率下压缩载荷—压缩位移曲线
图 5.
Vascular stent after deformation
变形后的血管支架
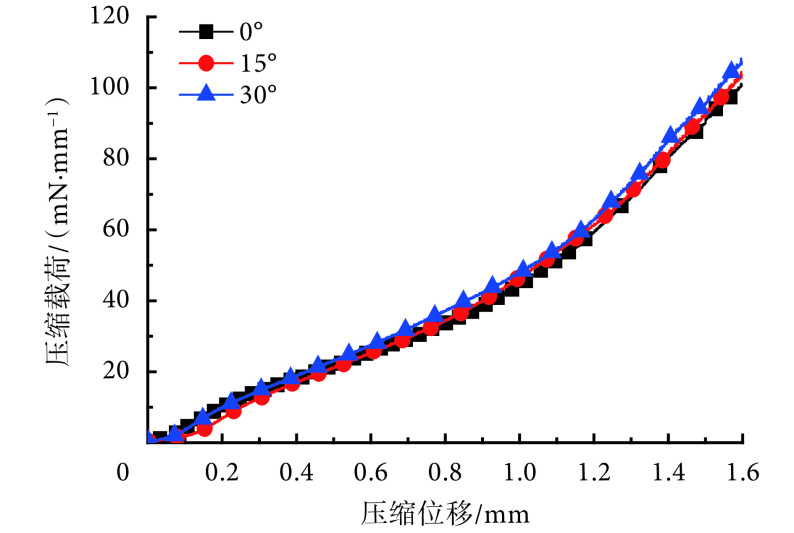
(2)压缩周向位置对测试结果的影响
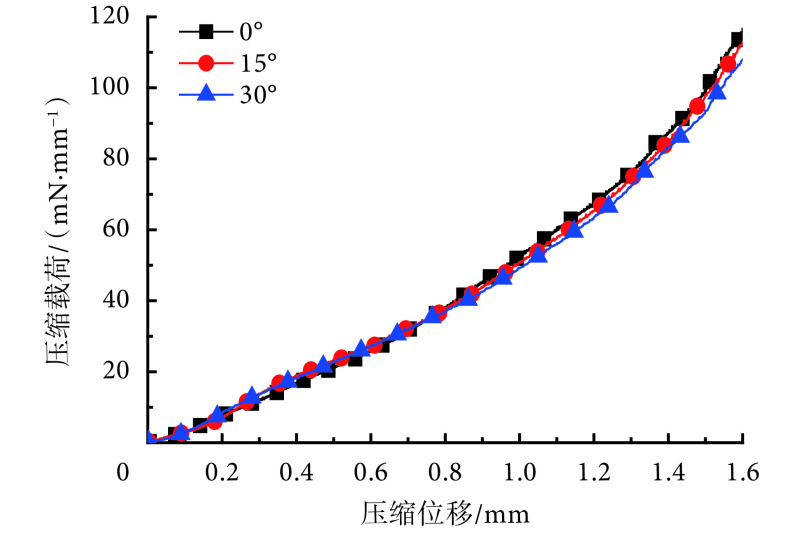
不同压缩周向位置下,压缩载荷—压缩位移曲线如图 6 所示。因支架的周向结构不同,支架对上压板的作用力不同,因此不同压缩周向位置得到的曲线有所差异,但整体趋势相同。根据公式(3)可知,周向位置为 0°、15°、30° 时,所对应的归一化支撑力分别为(84.67 ± 0.85)、(87.40 ± 0.76)、(95.05 ± 0.82)mN/mm,最大值与平均值相差 8% 以上,因此在测试时应对不同周向位置进行压缩。为体现支架周向结构差异对径向支撑性能的影响,本文用极差反映归一化支撑力的波动范围,采用置信度为 0.95 的置信区间作为支架实际归一化支撑力,如式(5)、(6)所示。则该支架的归一化支撑力为(89.04 ± 5.14)mN/mm,极差为 12.09 mN/mm。
图 6.
Compressive load-displacement curves at different com pression circumferential positions using planar compre ssion method
平面压缩法中不同压缩周向位置下压缩载荷—压缩位 移曲线
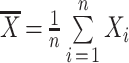 |
5 |
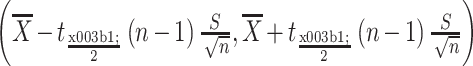 |
6 |
式中,
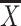 为归一化支撑力的样本均值,
为归一化支撑力的样本均值,
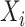 为每次测量支架的归一化支撑力,
为每次测量支架的归一化支撑力,
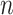 为测量次数,
为测量次数,
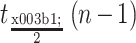 为自由度为
为自由度为
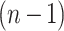 时,学生 t 检验中分布的
时,学生 t 检验中分布的
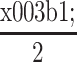 分位数,
分位数,
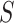 为样本标准差。
为样本标准差。
3.2.2. V 型槽压缩法实验
(1)压缩速率对测试结果的影响
不同压缩速率下,压缩载荷—压缩位移曲线如图 7 所示。与平面压缩法测试类似,支架也经历了初始压缩的非线性阶段、弹性变形阶段和塑性变形阶段。根据公式(3)可知,不同压缩速率所测得的平均归一化支撑力为(102.61 ± 0.82)mN/mm,可见压缩速率对测试结果无显著影响。但是如前所述,压缩速率不宜过大或过小,根据实验,压缩速率在 0.1~0.3 mm/min 之间为宜。
图 7.
Compressive load- displacement curves at different compression rates using V-groove compression method
V 型槽压缩法中不同压缩速率下压缩载荷—压缩位移 曲线
(2)压缩周向位置对测试结果的影响
不同压缩周向位置下,压缩载荷—压缩位移曲线如图 8 所示。根据公式(3)可知,压缩周向位置为 0°、15°、30° 所对应的归一化支撑力分别为(107.47 ± 0.82)、(101.73 ± 0.95)、(97.60 ± 0.84)mN/mm,最大值与平均值相差 6% 以上,可见压缩周向位置对测试结果有较明显的影响,在测试时应对不同周向位置进行压缩。该支架置信度为 0.95 的归一化支撑力为(102.24 ± 4.73)mN/mm,极差为 11.52 mN/mm。相对平面压缩法,V 型槽法测得的归一化支撑力较大,其原因是支架在 V 型槽两斜面的作用下不易发生变形。
图 8.
Compressive load- displacement curves at different com pression circumferential positions using V-groove compre ssion method
V 型槽压缩法中不同周向位置下压缩载荷—压缩位移 曲线
3.2.3. 径向压缩法实验
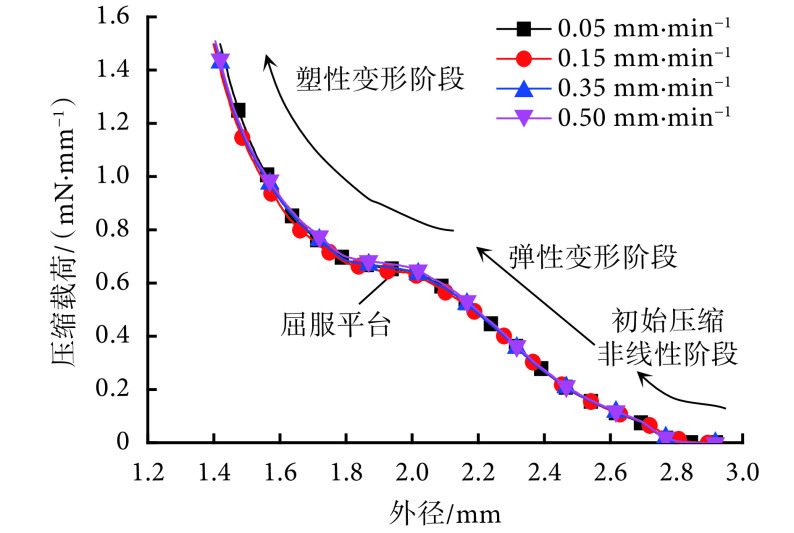
不同压缩速率下,压缩载荷—外径曲线如图 9 所示。支架也经历了初始压缩的非线性阶段、弹性变形阶段和塑性变形阶段。与其它前两种方法相比,支架出现了明显的屈服平台,其原因是支架外表面受力均匀,随着压缩量的增大,支撑环几乎同时发生塑性变形。根据公式(3)可知,不同压缩速率所测得的平均归一化支撑力为(1.30 ± 0.05)N/mm,可见压缩速率对测试结果没有显著影响。但是,压缩速率同样不宜过大或过小,根据实验,压缩速率在 0.15~0.25 mm/min 之间为宜。
图 9.
Compressive load- outside diameter curves at different compression rates using radial compression method
径向压缩法中不同压缩速率下压缩载荷—外径曲线
综合考虑三种测试方法的优缺点,平面压缩法更适合对不同外径、不同结构的聚合物血管支架的支撑性能进行对比测试。因此采用该方法测试了不同外径下本文所设计的三种支架和 BVS 支架的支撑性能。采用压缩速率为 0.3 mm/min,对不同周向位置进行压缩,以 0.95 的置信度来估算归一化支撑力,同时用极差反映其波动范围,最终得到不同外径、不同结构血管支架的归一化支撑力如表 3 所示。
表 3. Radial force of stents with different outside diameters and structures.
不同外径、不同结构血管支架的归一化支撑力
| 支架类型 | 外径/
mm |
归一化支撑力/
(mN·mm−1) |
极差/
(mN·mm−1) |
| JS 支架 | 1.4 | 75.28 ± 4.04 | 9.85 |
| 1.7 | 114.28 ± 6.96 | 14.01 | |
| 2.4 | 71.82 ± 6.30 | 14.19 | |
| OCS 支架 | 1.4 | 87.22 ± 3.14 | 8.21 |
| 1.7 | 134.31 ± 5.94 | 13.78 | |
| 2.4 | 84.79 ± 5.66 | 14.46 | |
| CCS 支架 | 1.4 | 95.12 ± 3.02 | 7.52 |
| 1.7 | 145.18 ± 5.70 | 12.23 | |
| 2.4 | 89.94 ± 5.14 | 12.09 | |
| BVS 支架 | 1.4 | 66.10 ± 3.96 | 9.64 |
| 1.7 | 103.01 ± 6.80 | 13.98 | |
| 2.4 | 63.38 ± 6.49 | 14.01 |
在同一外径下,本文所设计三种支架的归一化支撑力相对 BVS 支架均有不同程度提高,尤其是 CCS 支架,提高了 40% 以上,其主要原因是本文所设计的三种支架均采用了不等高支撑环结构[20],该结构有利于提高支架的支撑性能。对于同一结构、不同外径的情况,支架的归一化支撑力在外径为 1.7 mm 时最大,外径为 2.4 mm 时最小。其原因是外径为 1.7 mm 时,扩张比最大,扩张比越大,支撑单元夹角越大,其抵抗变形能力越强。
3.3. 柔顺性能实验
3.3.1. 压缩速率对测试结果的影响
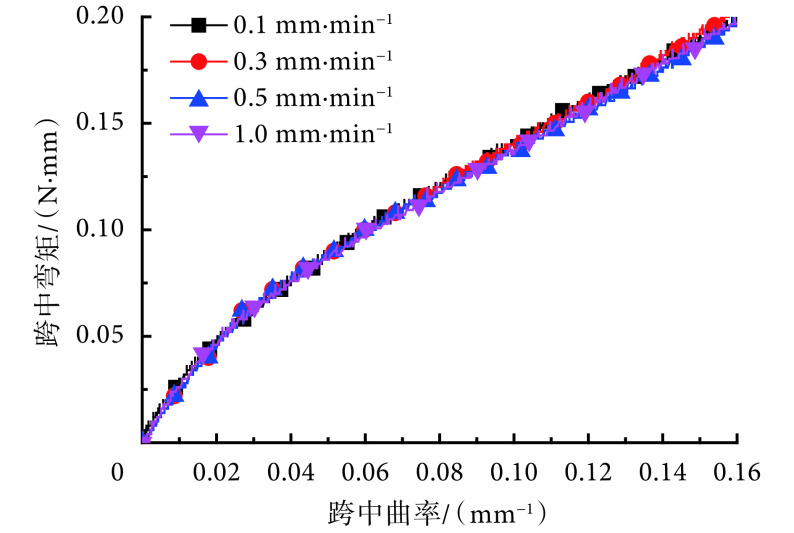
不同压缩速率下,跨中弯矩—跨中曲率曲线如图 10 所示。在压缩的初始阶段,测试曲线近似为线性,且几乎重合。随着支架的进一步弯曲,曲线之间略有差异,其原因是支架相邻支撑环之间存在间隙,当间隙滑过支撑部件时会产生一定的波动和沿水平面的滑动。根据公式(4)可知,弯曲刚度为测试曲线的斜率,取压缩初始阶段的斜率作为支架的弯曲刚度[21],则 4 种压缩速率下的平均弯曲刚度为(2.11 ± 0.07)N/mm2,可以看出,压缩速率对弯曲刚度无显著影响,但是压缩速率过大会导致曲线波动较大,因此压缩速率不宜过高。根据实验,压缩速率在 0.1~0.3 mm/min 之间为宜。
图 10.
Midspan bending moment-curvature curves at different compression rates using three-point bending method
三点弯曲法中不同压缩速率下跨中弯矩—跨中曲率曲线
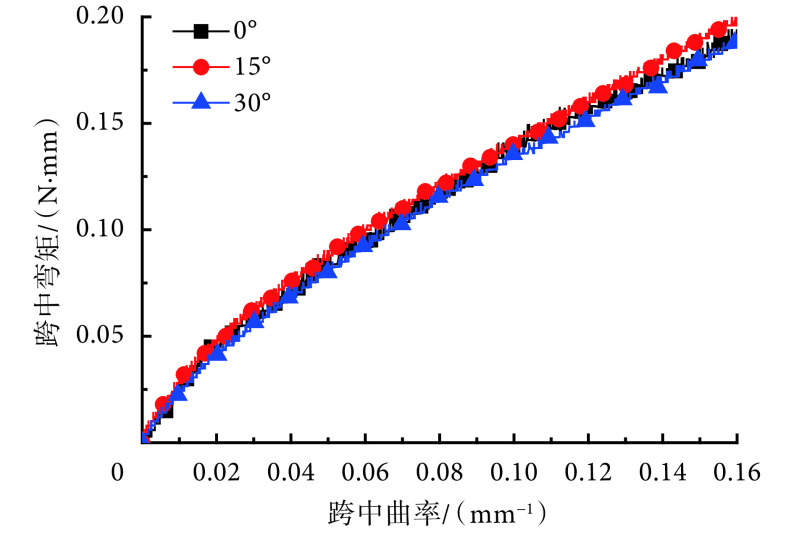
3.3.2. 压缩周向位置对测试结果的影响
不同压缩周向位置下,跨中弯矩—跨中曲率曲线如图 11 所示。根据公式(4)可知,压缩周向位置为 0°、15°、30° 时的弯曲刚度分别为(2.07 ± 0.06)、(2.35 ± 0.07)、(1.95 ± 0.07)N/mm2,弯曲刚度最大值与平均值相差 14% 以上,因此测试时应对不同周向位置进行压缩。仍采用置信度为 0.95 估计弯曲刚度,用极差反应弯曲刚度的波动范围,则该支架的弯曲刚度为(2.12 ± 0.20)N/mm2,极差为 0.55 N/mm2。
图 11.
Midspan bending moment-curvature curves at different compression circumferential positions using three- point bending method
三点弯曲法中不同周向位置下跨中弯矩—跨中曲率曲线
根据上述实验,选取压缩速率为 0.1 mm/min,对支架不同周向位置进行压缩,以 0.95 的置信度估算弯曲刚度,用极差反映支架弯曲刚度的波动范围。最终得到不同外径、不同结构血管支架的弯曲刚度如表 4 所示。可以看出,同一外径下,OCS 支架、JS 支架与 BVS 支架的弯曲刚度相当,CCS 支架的弯曲刚度较大。由于不同外径支架所用的跨距不同,则不同外径支架的弯曲刚度不具可比性。
表 4. Bending stiffness of stents with different outside diame ters and structures.
不同外径、不同结构血管支架的弯曲刚度
| 支架类型 | 外径/
mm |
弯曲刚度/
(N·mm−2) |
极差/
(N·mm−2) |
| JS 支架 | 1.4 | 0.05 ± 0.01 | 0.03 |
| 1.7 | 0.22 ± 0.04 | 0.06 | |
| 2.4 | 0.63 ± 0.09 | 0.16 | |
| OCS 支架 | 1.4 | 0.05 ± 0.01 | 0.04 |
| 1.7 | 0.21 ± 0.03 | 0.06 | |
| 2.4 | 0.63 ± 0.08 | 0.15 | |
| CCS 支架 | 1.4 | 0.25 ± 0.10 | 0.12 |
| 1.7 | 1.24 ± 0.15 | 0.32 | |
| 2.4 | 2.12 ± 0.20 | 0.55 | |
| BVS 支架 | 1.4 | 0.05 ± 0.01 | 0.04 |
| 1.7 | 0.22 ± 0.04 | 0.07 | |
| 2.4 | 0.62 ± 0.08 | 0.15 |
综合分析本文所设计三种支架的力学性能,CCS 支架和 OCS 支架具有较高的径向支撑性能,且径向回缩性能和轴向短缩性能也均优于 BVS 支架。虽然 CCS 支架的弯曲刚度较大,但仍远低于常用的商业支架[9-10]。因此比较结果显示,OCS 支架和 CCS 支架综合力学性能更好。
4. 结论
本文对比分析了可降解聚合物血管支架径向支撑性能测试的平面压缩法、V 型槽压缩法和径向压缩法以及每一种方法下压缩速率和压缩周向位置对径向支撑性能测试结果的影响,采用三点弯曲法研究了压缩速率和压缩周向位置对柔顺性能测试结果的影响。选取最优测试方案,测试了本文所设计的三种可降解聚合物血管支架和 BVS 支架的径向支撑性能、柔顺性能、径向回缩性能和轴向短缩性能,并得出以下主要结论:
(1)采用平面压缩法、V 型槽压缩法和径向压缩法对血管支架进行压缩时,支架均经历了初始压缩的非线性阶段、弹性变形阶段和塑性变形阶段,三种方法得到的压缩载荷—压缩位移(或外径)曲线整体趋势一致,但是归一化支撑力差异较大。其中平面压缩法因具有能够反映出血管支架不同周向位置抗压能力的差异等优点,更适合对不同外径、不同结构血管支架的径向支撑性能进行对比测试。
(2)压缩速率对径向支撑性能和柔顺性能测试结果并无显著影响。压缩周向位置对采用平面压缩法和 V 型槽压缩法测试径向支撑性能和采用三点弯曲法测试柔顺性能有较大影响,测试时应对不同周向位置进行压缩,测试结果应给出具有一定置信度的力学性能参数置信区间,并通过极差来反映力学性能的最大波动范围。
(3)本文所设计的三种血管支架相对 BVS 支架其径向支撑性能均有不同程度的提高,尤其是 CCS 支架,提高 40% 以上。JS 支架和 OCS 支架与 BVS 支架的柔顺性能相当,CCS 支架弯曲刚度较大。本文所设计三种支架的径向回缩率相对 BVS 支架降低了 20% 以上,且均未发生轴向短缩。同一结构不同外径下,支架的径向支撑性能、径向回缩性能和轴向短缩性能主要跟支架扩张比有关,扩张比越大,径向支撑性能和径向回缩性能越好,但是轴向短缩或伸长越严重。
利益冲突声明:本文全体作者均声明不存在利益冲突。
Funding Statement
国家自然科学基金项目(51675079,11502044);中央高校基本业务费(DUT17RC(3)104)
References
- 1.邹秋华, 林婧, 关国平, 等 一体化编织型血管覆膜支架的压缩性能. 东华大学学报: 自然科学版. 2017;43(1):27–30, 87. [Google Scholar]
- 2.魏雨, 张景迅, 范娟娟, 等 心血管支架表面改性及应用. 生物医学工程学杂志. 2016;33(3):593–597, 608. doi: 10.7507/1001-5515.20160099. [DOI] [PubMed] [Google Scholar]
- 3.Zou Qiuhua, Xue Wen, Lin Jing, et al Mechanical characteristics of novel polyester/NiTi wires braided composite stent for the medical application. Results in Physics. 2016;6:440–446. doi: 10.1016/j.rinp.2016.07.007. [DOI] [Google Scholar]
- 4.Hermawan H, Mantovani D Process of prototyping coronary stents from biodegradable Fe-Mn alloys. Acta Biomater. 2013;9(10):8585–8592. doi: 10.1016/j.actbio.2013.04.027. [DOI] [PubMed] [Google Scholar]
- 5.Isayama H, Nakai Y, Toyokawa Y, et al Measurement of radial and axial forces of biliary self-expandable metallic stents. Gastrointest Endosc. 2009;70(1):37–44. doi: 10.1016/j.gie.2008.09.032. [DOI] [PubMed] [Google Scholar]
- 6.Hirdes M M, Vleggaar F P, de Beule M A In vitro evaluation of the radial and axial force of self-expanding esophageal stents . Endoscopy. 2013;45(12):997–1005. doi: 10.1055/s-00000012. [DOI] [PubMed] [Google Scholar]
- 7.Schmidt W, Lanzer P, Behrens P, et al A comparison of the mechanical performance characteristics of seven drug‐eluting stent systems. Catheter Cardiovasc Interv. 2009;73(3):350–360. doi: 10.1002/ccd.v73:3. [DOI] [PubMed] [Google Scholar]
- 8.Grabow N, Bünger C M, Schultze C, et al A biodegradable slotted tube stent based on poly(L-lactide) and poly(4-hydroxybutyrate) for rapid balloon-expansion. Ann Biomed Eng. 2007;35(12):2031–2038. doi: 10.1007/s10439-007-9376-9. [DOI] [PubMed] [Google Scholar]
- 9.Schmidt W, Behrens P, Brandt-Wunderlich C, et al In vitro performance investigation of bioresorbable scaffolds-standard tests for vascular stents and beyond . Cardiovasc Revasc Med. 2016;17(6):375–383. doi: 10.1016/j.carrev.2016.05.001. [DOI] [PubMed] [Google Scholar]
- 10.Wang Qian, Fang Gang, Zhao Yinghong, et al Computational and experimental investigation into mechanical performances of Poly-L-Lactide Acid (PLLA) coronary stents. J Mech Behav Biomed Mater. 2017;65:415–427. doi: 10.1016/j.jmbbm.2016.08.033. [DOI] [PubMed] [Google Scholar]
- 11.Zhao Fan, Xue Wen, Wang Fujun, et al A new approach to improve the local compressive properties of PPDO self-expandable stent. J Mech Behav Biomed Mater. 2017;68:318–326. doi: 10.1016/j.jmbbm.2017.02.015. [DOI] [PubMed] [Google Scholar]
- 12.Li Chaojing, Wang Fujun, Chen Peifeng, et al Preventing collapsing of vascular scaffolds: the mechanical behavior of PLA/PCL composite structure prostheses during in vitro degradation . J Mech Behav Biomed Mater. 2017;75:455–462. doi: 10.1016/j.jmbbm.2017.08.015. [DOI] [PubMed] [Google Scholar]
- 13.Brie D, Penson P, Serban M C, et al. Bioresorbable scaffold-a magic bullet for the treatment of coronary artery disease?. Int J Cardiol, 2016, 215: 47-59.
- 14.李婧, 彭坤, 崔新阳, 等 位姿对支架虚拟释放结果影响的数值模拟研究. 生物医学工程学杂志. 2018;35(02):214–218, 228. doi: 10.7507/1001-5515.201703013. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 15.ASTM International F2081-06 Standard guide for characterization and presentation of the dimensional attributes of vascular stents. West Conshohocken, PA: ASTM International press. 2013:1–3. [Google Scholar]
- 16.Pauck R G, Reddy B D Computational analysis of the radial mechanical performance of PLLA coronary artery stents. Med Eng Phys. 2015;37(1):7–12. doi: 10.1016/j.medengphy.2014.09.014. [DOI] [PubMed] [Google Scholar]
- 17.ASTM International F3067-14 Guide for radial loading of balloon expandable and self expanding vascular stents. West Conshohocken, PA: ASTM International Press. 2014 [Google Scholar]
- 18.ASTM International F2606-08 Three-point bending of balloon expandable vascular stents and stent systems. West Conshohocken, PA: ASTM International Press. 2014 [Google Scholar]
- 19.刘倩, 雷丽萍, 曾攀, 等 血管支架径向支撑能力的数值模拟和实验研究. 中国医疗器械杂志. 2010;34(3):175–179. doi: 10.3969/j.issn.1671-7104.2010.03.006. [DOI] [PubMed] [Google Scholar]
- 20.王敏杰, 赵丹阳, 魏云波, 等. 一种注塑成型的生物可降解聚合物血管支架. 大连理工大学. 2018. ZL201710149983.9.
- 21.Shen Xiang, Deng Yongquan, Ji Song, et al Flexibility behavior of coronary stents: the role of linker investigated with numerical simulation. J Mech Med Biol. 2017;17(8):1750112. doi: 10.1142/S0219519417501123. [DOI] [Google Scholar]