Abstract
El asma es una de las enfermedades crónicas más prevalentes en España. La Sociedad Española de Alergología e Inmunología Clínica (SEAIC), la Sociedad Española de Médicos de Atención Primaria (SEMERGEN), la Sociedad Española de Medicina Familiar y Comunitaria (semFYC), la Sociedad Española de Médicos Generales y de Familia (SEMG) y la Sociedad Española de Neumología y Cirugía Torácica (SEPAR) consensuaron en 2019 un documento donde se establecieron criterios de derivación y pautas de actuación en el diagnóstico, control y seguimiento del paciente asmático con el fin de facilitar la continuidad asistencial y una mejor atención en cada ámbito. Las nuevas circunstancias motivadas por la pandemia covid-19 y nuevas evidencias científicas en algunos aspectos han llevado a actualizar algunas de las recomendaciones de la anterior edición, adaptándolas a la nueva situación asistencial.
Palabras clave: Asma, Derivación, Atención especializada, Atención primaria, Continuidad asistencial
Abstract
Asthma is one of the most prevalent chronic diseases in Spain. In 2019, the Spanish Society of Allergology and Clinical Immunology (SEAIC), the Spanish Society of Primary Care Physicians (SEMERGEN), the Spanish Society of Family and Community Medicine (semFYC), the Spanish Society of General and Family Physicians (SEMG) and the Spanish Society of Pulmonology and Thoracic Surgery (SEPAR) drafted a document laying down the criteria for referral and action guidelines in the diagnosis, control and monitoring of the asthmatic patient to facilitate ongoing care and improved attention in every setting. The new circumstances derived from the Covid-19 pandemic have demanded that some of the recommendations of the previous edition be updated and adapted to the new healthcare situation.
Keywords: Asthma, Referral, Specialized care, Primary care, Continuity of care
Introducción
El asma es una de las enfermedades crónicas más prevalentes en España, ya que afecta a más del 10% de la población infantil y más del 5% de la población adulta1. Con los tratamientos actualmente disponibles, la mayor parte de los pacientes podrían alcanzar el control de la enfermedad, sin sufrir alteraciones significativas en sus actividades ordinarias, aunque habitualmente no se logra este control debido a factores como la falta de diagnóstico y seguimiento y/o la falta de adhesión terapéutica. En 2019 la Sociedad Española de Alergología e Inmunología Clínica (SEAIC), la Sociedad Española de Médicos de Atención Primaria (SEMERGEN), la Sociedad Española de Medicina Familiar y Comunitaria (semFYC), la Sociedad Española de Médicos Generales y de Familia (SEMG) y la Sociedad Española de Neumología y Cirugía Torácica (SEPAR) elaboraron un documento de consenso2 donde se establecieron los criterios de derivación, pautas de actuación en el diagnóstico, control y seguimiento del paciente asmático entre los diferentes profesionales y niveles asistenciales implicados en la atención al paciente con asma. Las nuevas circunstancias motivadas por la pandemia covid-19 obligan a matizar algunas de las recomendaciones de la anterior edición, adaptándolas a la nueva situación asistencial y a la necesidad de garantizar tanto los derechos de los pacientes a ser evaluados de acuerdo con los criterios de calidad adecuados como la seguridad de los mismos y de los trabajadores sanitarios. En esta versión se ha sumado el Grupo de Respiratorio de Atención Primaria (GRAP), incorporando la visión de enfermería como elemento esencial en la atención del paciente con asma.
Valoración diagnóstica inicial ante sospecha de asma
Sospecha clínica
Ante un paciente que acude a consulta de Atención Primaria (AP) por un cuadro clínico sospechoso de asma (tos, disnea, sibilancias y opresión torácica) sin diagnóstico previo, recomendamos seguir la sistemática de estudio que se expone en la figura 1. En primer lugar, se aconseja realizar una anamnesis en profundidad y una exploración física adecuada. La anamnesis contemplará, además de preguntas clave (tabla 1), el inicio de los síntomas y la presencia de rinosinusitis crónica con o sin pólipos, rinitis alérgica, dermatitis y la historia familiar de asma o atopia, dado que aumentan la probabilidad diagnóstica de asma. El resultado de ambas permitirá, en la mayor parte de los casos, dirigir correctamente la actitud a seguir o las pruebas complementarias a realizar.
Figura 1.
Algoritmo ante un caso de sospecha de asma.
Tabla 1.
Preguntas clave en el diagnóstico del paciente asmático
| ¿Ha notado alguna vez «pitos» en el pecho? |
| ¿Ha presentado tos, sobre todo por las noches? |
| ¿Ha tenido estos síntomas o dificultad al respirar en algunas épocas concretas del año, en contacto con determinados animales, plantas, tabaco, en su trabajo o después de hacer ejercicio físico? |
| ¿Los resfriados le han durado más de 10 días o le han «bajado al pecho»? |
| ¿Estos síntomas han mejorado con medicamentos inhalados? |
| ¿Usted tiene algún tipo de alergia o algún familiar con asma o alergia? |
El algoritmo propuesto en la figura 1 pretende mostrar las posibles formas de actuación ante un caso de sospecha de asma. Su desarrollo se basa en dos supuestos: 1) Paciente con sospecha de asma que precisa tratamiento inmediato (su situación clínica imposibilita realizar pruebas complementarias) y confirmación diagnóstica posterior. 2) Paciente con sospecha de asma que permite realizar pruebas diagnósticas antes de iniciar tratamiento.
Diagnóstico de asma, pruebas complementarias
Pruebas de función pulmonar
A todo paciente con sospecha clínica de asma se le debe realizar una espirometría con prueba broncodilatadora (PBD), aunque una espirometría normal no excluye el diagnóstico2.
Para la realización de la PBD se recomienda administrar 4 inhalaciones sucesivas de 100 μg de salbutamol mediante un inhalador presurizado con cámara espaciadora, o su equivalente de terbutalina (2 inhalaciones), a intervalos de 30 segundos tras cada aplicación. Debe realizarse una espirometría en situación basal y tras 15 minutos para los agonistas ß2-adrenérgicos. En el caso de no poder usar betagonistas de acción corta (SABA) se podría utilizar bromuro de ipratropio3, (8 inhalaciones de 20 μg, dosis total 160 μg, mediante cartucho presurizado con cámara, realizando la espirometría posterior a los 30-40 minutos). En sujetos adultos, se considera respuesta positiva (o broncodilatación significativa) un aumento del volumen espiratorio forzado en el primer segundo (FEV1) ≥ 12% y ≥ 200 ml respecto al valor basal.
Algunas de las técnicas de examen de las vías respiratorias son procedimientos que, por la emisión de aerosoles, pueden transmitir enfermedades infecciosas, tanto a los pacientes como a los profesionales que las realizan. Por ello, en épocas que coincidan con pico de pandemia por SARS-CoV-2 u otros virus respiratorios, la realización de la espirometría debería limitarse a aquellas pruebas que el clínico considere imprescindibles. En los momentos de post-pico de la pandemia o en caso de pacientes con sospecha de infección respiratoria, la espirometría debe realizarse con unas medidas extraordinarias de asepsia por el riesgo de transmisión de aerosoles. Se cuidará especialmente la protección del profesional sanitario que realiza la prueba, así como la desinfección del aparataje y las superficies con las que el paciente haya podido estar en contacto. Cuando la incidencia de dicha infección en la población sea muy baja, se podría considerar volver a los estándares habituales, pero siempre con la precaución de estar muy alerta a la situación cambiante en la que se puede mover el escenario epidemiológico. Se recomienda realizar la espirometría en una habitación separada, con una superficie mínima de 2,5 m2. Será ocupada por un único paciente cada vez, sin acompañante y con tiempos de ventilación entre paciente y paciente4. Así mismo, en el caso de que la espirometría no pueda realizarse en condiciones de seguridad, se puede valorar derivar al paciente a un centro que sí disponga de tales medidas.
La medición de la variabilidad del flujo espiratorio máximo (FEM) constituye una técnica segura de diagnóstico de asma en el contexto de pandemia por virus respiratorios, por lo que esta opción se considera de elección para el diagnóstico extrahospitalario de pacientes con sospecha de asma en dicha situación. Además, al recogerse con datos numéricos y gráficas, fácilmente exportables a plataformas digitales, resulta más ventajoso en el marco de las nuevas prácticas clínicas de telemedicina5. En el contexto de pandemia, las técnicas que requieran nebulizaciones deben limitarse a lo clínicamente imprescindible. En cualquier caso, se aconseja la realización con dosímetro ya que reduce el riesgo de flujo espiratorio, así como valorar la posibilidad de realizar pruebas que descarten infección activa.
Medidas de inflamación y estudio alergológico
La medición de la fracción exhalada de óxido nítrico (FENO) evalúa de forma no invasiva la inflamación eosinofílica de las vías respiratorias. Un valor ≥ 40 partes por billón puede ser útil para el diagnóstico de asma. Sin embargo, un valor normal de FENO no excluye el diagnóstico, especialmente en personas no atópicas6.
En un entorno fuera de una situación de pandemia, la medición de la FENO puede ser una herramienta muy útil en el diagnóstico de los pacientes con asma. En general, no es necesario, con la mayoría de los dispositivos actuales, que el profesional se sitúe muy próximo al paciente e incluso algunos permiten su conexión remota a ordenador con volcado inmediato de los datos. En el mantenimiento de los aparatos es obligatorio el uso de filtros antibacterianos y antivirales.
La presencia de atopia, considerada como la presencia de sensibilización alérgica, aumenta la probabilidad de que un paciente con síntomas respiratorios presente un asma alérgica, aunque no es específico de asma y no está presente en todos los fenotipos de la enfermedad.
Tratamiento y control del asma
Tratamiento del asma
Los objetivos del tratamiento del asma son, por un lado, alcanzar un buen control de síntomas y unos niveles normales de actividad (control actual) y, por otro, minimizar la mortalidad, las exacerbaciones, la obstrucción crónica al flujo aéreo y los efectos adversos (riesgo futuro)1, 7.
Es aconsejable establecer un plan de tratamiento consensuado entre médico y paciente1, 7, 8. El inicio del tratamiento del asma dependerá de la gravedad, definida por la presencia y la frecuencia de síntomas diurnos y nocturnos, la necesidad de medicación de rescate, las limitaciones de la actividad, la función pulmonar y las exacerbaciones. El tratamiento de mantenimiento se evaluará de forma cíclica y vendrá determinado por el grado de control del asma.
Para los pacientes en tratamiento, la gravedad se determina en función de los requerimientos mínimos de medicación para mantener el control1, 9. Así pues, gravedad y grado de control serán determinantes para tomar decisiones sobre el tratamiento de mantenimiento y el ajuste de dosis escalonado que propone la Guía Española para el Manejo del Asma (GEMA 5.1)1.
Los glucocorticoides inhalados (GCI) constituyen el tratamiento de mantenimiento más efectivo para el asma persistente, al controlar síntomas y disminuir el riesgo de exacerbaciones10, 11, 12, 13. Aunque en los primeros escalones de tratamiento pueden administrarse los GCI como única medicación de mantenimiento, en general se administran en combinación con un LABA (salmeterol, formoterol o vilanterol) inhalado, preferiblemente en un mismo dispositivo. El uso de esta combinación en el asma moderada ha demostrado una mejor respuesta en reducción de síntomas, mejoría en la función pulmonar, reducción de las exacerbaciones y del uso de medicación de alivio que aumentando la dosis de GCI1. Estudios recientes indican que la combinación budesónida/formoterol en un solo inhalador a demanda, en comparación con la del tratamiento continuo con GCI en el asma persistente leve e incluso con asma moderada, no fue inferior en la prevención de exacerbaciones (que fueron similarmente bajas); sin embargo, resultó inferior en el mantenimiento del control y en el incremento de la función pulmonar14, 15, 16, 17.
En su elección debemos tener en cuenta las dosis equipotentes entre ellos, su índice terapéutico y el tipo de dispositivo, teniendo en cuenta las preferencias y experiencia previa de cada paciente. En caso de necesitar diferentes principios activos, se recomienda unificar en el mismo dispositivo o al menos utilizar aquellos con mecanismo de dispensación parecido18.
Un objetivo que señala GEMA 5.1 es cambiar la inercia terapéutica; en ese sentido, si el asma permanece estable al menos 3 meses, podemos valorar bajar de escalón terapéutico (step down) con el fin de determinar las necesidades terapéuticas mínimas para mantener el control1, 19.
En casos individualizados en los que el asma permanezca bien controlada con la dosis mínima de GCI durante al menos un año, y siempre que no existan otros factores de riesgo, podría realizarse un ensayo de retirada de GCI bajo estricto control clínico, funcional e inflamatorio, reintroduciéndolo en caso de empeoramiento7, 8.
La inmunoterapia con extractos alergénicos por vía subcutánea o sublingual es un tratamiento eficaz en el asma alérgica bien controlada (escalones 1-4 de GEMA 5.1), siempre que se demuestre una sensibilización mediada por IgE a un alérgeno clínicamente relevante y se utilicen extractos bien caracterizados y estandarizados.
Nuevos tratamientos para el asma grave no controlada a recomendar en Atención Especializada
Tratamientos biológicos
Están indicados en algunos casos de asma grave no controlada de tipo T2, alérgica y/o eosinofílica con mala respuesta, a pesar de un tratamiento correcto y continuado. Actúan por dos mecanismos principales; como anticuerpos anti-IgE (omalizumab) o como anticuerpos inhibidores de diversas interleucinas implicadas en la fisiopatología del asma como la interleucina-5 (IL-5) (mepolizumab, reslizumab), el receptor de la IL-5 (benralizumab), o el receptor para la IL4 e IL13 (dupilumab)1. Los principales beneficios son la reducción de exacerbaciones y de la utilización de esteroides sistémicos, así como la mejora del control de la enfermedad, la calidad de vida y la función pulmonar en la mayoría de los pacientes.
Macrólidos
Algún estudio ha demostrado reducción de las exacerbaciones tras la administración prolongada de azitromicina20. El reciente estudio AMAZES demuestra una reducción significativa en el número de exacerbaciones y una mejora de la calidad de vida con dosis de 500 mg de azitromicina 3 veces por semana durante 48 semanas, independientemente del fenotipo inflamatorio de los pacientes21 aunque, debido a los potenciales efectos secundarios (auditivos, cardiológicos, aumento de micobacterias atípicas y de las resistencias microbiológicas) su uso debe ser restringido e individualizado.
Termoplastia endobronquial
Es un procedimiento broncoscópico que reduce la capa muscular lisa bronquial mediante la aplicación de calor por radiofrecuencia. Aunque su indicación es muy limitada, podría considerarse en asma grave no controlada (AGNC) con limitación crónica al flujo aéreo (FEV1 entre 50-80% y sin hipersecreción bronquial), y fenotipos no subsidiarios de tratamiento con biológicos, o en los que estos hayan fracasado22, 23.
Evaluación del control del asma
La percepción de control del asma varía entre pacientes y profesionales sanitarios24. Aunque los pacientes suelen pensar que su asma está bien controlada cuando el uso de agonistas ß2-adrenérgicos de acción corta (SABA) a demanda logra revertir sus síntomas4, 25, es necesario explicarles que el asma está bien controlada cuando en el último mes solo hayan presentado síntomas diurnos o necesidad de medicación de rescate menos de 2 días, ningún síntoma nocturno, mantengan una función pulmonar normal y no hayan tenido ni exacerbaciones ni limitación de sus actividades habituales.
La visita de seguimiento es la herramienta fundamental para evaluar el control de la enfermedad, en la cual se valorará el control clínico y los factores de riesgo de presentar exacerbaciones (tabla 2). El control debe evaluarse en cada visita médica. El grado de control determinará las decisiones sobre el tratamiento de mantenimiento y el ajuste de dosis, según los pasos o escalones terapéuticos que muestran las guías de práctica clínica1, 7.
Tabla 2.
Evaluación del control y de los factores de riesgo de exacerbaciones del asma
| En el último mes ha presentado | Sí | No | Control | |
|---|---|---|---|---|
| Control clínico | ¿Síntomas asmáticos diurnos > 2 veces/mes? |
Todos NO: Asma bien controlada |
||
| ¿Algún síntoma o despertar nocturno debido al asma? | ||||
| ¿Necesidad de medicación de rescate (SABA) > 2 veces/mes? | ||||
| ¿Alguna limitación de la actividad debida al asma? | ||||
| ¿Alguna exacerbación grave del asma en el último año? |
||||
| FEV1 y/o FEM < 80% del teórico/mejor valor personal? | ||||
| Factores de riesgo de exacerbaciones | Mal control actual | ACT < 20 o ACQ > 1,5 | ||
| Exacerbaciones previas | ≥ 1 exacerbación grave en el último año o historia de asma casi mortal | |||
| Derivados del tratamiento | Mala adhesión y técnica de inhalación incorrecta | |||
| Sobreuso SABA: ≥ 3 inhaladores al año (≥ 2 inhalaciones al día) | ||||
| No utilización de esteroide inhalado | ||||
| Utilización de corticoides sistémicos o altas dosis de GCI | ||||
| Comorbilidades | Rinosinusitis, poliposis nasal, reflujo gastroesofágico, obesidad, alergia alimentaria, trastornos psicológicos, embarazo | |||
| Exposición ambiental y otros agravantes | Tabaco y otros tóxicos inhalados (marihuana, cocaína), alérgenos, factores ocupacionales, etc. Problemas socioeconómicos |
|||
| Función pulmonar | FEV1 basal < 60% pred, reversibilidad con el broncodilatador. | |||
ACQ: Asthma Control Questionnaire; ACT: Asthma Control Test; FEM: flujo espiratorio máximo; FEV1: volumen espiratorio forzado en el primer segundo; GCI: glucocorticoides inhalados; SABA: agonistas β2-adrenérgicos de acción corta.
Fuente: Adaptada de GINA 2020 (www.ginasthma.org) y GEMA 5.0 (www.gemasma.com).
Seguimiento de los pacientes con asma
El seguimiento del asma (entendido como las consultas que se realizan tras el diagnóstico y primer tratamiento) es esencial para el control de la enfermedad y para la educación del paciente. Para optimizar su eficacia deben estar protocolizadas y abarcar aspectos de control actual y riesgo futuro. Se recomienda realizar una evaluación sistemática del paciente como refleja la tabla 3. Seguir un esquema adecuado es especialmente importante cuando la consulta de seguimiento se realiza mediante teleasistencia, en la que la comunicación puede ser más complicada. Por ello, sería recomendable una mínima formación previa en nuevas habilidades para la comunicación con el paciente con el uso de teleasistencia. En pacientes que reúnan criterios para la teleasistencia (tabla 4), la visita de seguimiento se centrará en los aspectos resumidos en la tabla 5:
-
-
Se deberá llevar a cabo un interrogatorio estructurado de síntomas (tabla 6) o telefónicamente un test de control del asma (ACT) (recogiendo la puntuación total y de cada ítem) incluyendo el registro de exacerbaciones.
-
-
El interrogatorio acerca del uso de SABA debe acompañarse de la comprobación de su retirada de farmacia en los sistemas de atención sanitaria que lo permitan. Ante sospecha de sobreuso de SABA deben cuantificarse los envases retirados mensualmente de la oficina de farmacia desde la consulta previa.
-
-
Preguntar sobre control de comorbilidades, exposición a factores desencadenantes, especialmente agentes irritantes (tabaquismo y otros) y los alérgenos a los que el paciente está sensibilizado.
-
-
Valoración de la adhesión terapéutica de fármacos de mantenimiento y la correcta realización de la técnica de inhalación, aspectos donde la consulta de enfermería juega un papel primordial18. En un escenario de consultas telefónicas, es de gran importancia que enfermería disponga de medios adecuados tanto para valorar y mejorar la adhesión terapéutica como para optimizar la revisión y educación terapéutica del paciente, incidiendo en el uso correcto de dispositivos de inhalación. Son especialmente interesantes equipos que permitan recomendar herramientas audiovisuales que faciliten la realización de técnicas de inhalación a pacientes con habilidades digitales. De igual modo se recomienda la aplicación de cuestionarios validados como el Test de Adhesión a Inhaladores (TAI), que permite discriminar el tipo de incumplimiento terapéutico. El uso de las nuevas tecnologías también debe aplicarse a la educación del paciente: el desarrollo de apps y otros materiales educativos que deben facilitar la realización de una adecuada educación sin hacer imprescindible la consulta presencial.
-
-
Valoración funcional: la espirometría es la prueba de función pulmonar más útil en el seguimiento del paciente asmático. En situaciones de pandemia se recomienda tomar las medidas de protección para evitar el contagio del personal sanitario, como adaptar cuidadosamente el medio en el que se realizan a las normas recomendadas por las sociedades científicas o la realización de pruebas rápidas de antígenos a los pacientes previamente a la realización de la prueba. En estas circunstancias son de gran utilidad, para valorar el control y la evolución del asma, instruir al paciente en el uso del medidor de FEM para conseguir un buen manejo en el autocontrol. En caso de deterioro clínico o de función pulmonar es aconsejable realizar una consulta presencial y valorar la necesidad de pruebas complementarias.
Tabla 3.
Evaluación sistemática en el seguimiento del asma
| Evaluación | Indicadores | Acción | Recomendación |
|---|---|---|---|
| Gravedad | GCI a altas dosis + segundo controlador | Comprobar adhesión | Educación |
| Control de síntomas | ACT: Mal control: < 16 Parcialmente controlado: entre 19 y 16 |
TAI: Cumplidor Incumplidor |
Confirmar asma Educación |
| Exacerbaciones graves | ≥ 2/año previo Ingresos en Urgencias | Adhesión al tratamiento Desencadenantes AINE, ß-bloqueantes |
Educación Evitación |
| Función pulmonar | Espirometría FEV1/FVC < 0,70 FEV1 – post-BD < 80% Declive rápido |
Rx/TC Historia tabáquica |
Valorar: ACO/EPOC/BQ |
| Tratamiento | Escalón ≥ 5 GEMA Efectos adversos |
Adherencia CO, ß-2 agonistas |
Alternativas terapéuticas en AE (biológicos, macrólidos, termoplastia) |
| Desencadenantes | Ambientales Ocupacionales Ejercicio EREA β-bloqueantes |
Eosinofilia, IgE FEM FEM, espirometría. Interrogar por patologia nasosinusal Colirios |
Evitación Investigación ß-2 agonistas Evitación/alternativas Alternativas |
| Comorbilidad | Rinitis/rinosinusitis Poliposis nasal Obesidad SAHS ERGE |
Cuestionarios TC, fibroendoscopia nasal IMC STOP-BANG IBP empírico |
Corticoide nasal ORL en caso de cirugía Dieta endocrinólogo Poligrafía IBP, digestivo |
ACO: solapamiento de asma y EPOC; ACT: test de control del asma; AE: Atención Especializada; AINE: antiinflamatorios no esteroideos; BQ: bronquiectasias; CO: corticoides orales; EPOC: enfermedad pulmonar obstructiva crónica; EREA: enfermedad respiratoria exacerbada por aspirina y otros AINE; ERGE: enfermedad por reflujo gastroesofágico; FEM: flujo espiratorio máximo; FEV1: volumen espiratorio forzado en el primer segundo; FVC: capacidad vital forzada; GCI: glucocorticoide inhalado; GEMA: Guía española para el manejo del asma; IBP: inhibidores de la bomba de protons; IgE: inmunoglobulina E; IMC: índice demasa corporal; post-BD: post-broncodilatación; Rx: radiografía; SAHS: síndrome de apnea-hipopnea del sueño; TAI: test de adherencia a inhaladores; TC: tomografía computarizada.
Tabla 4.
Criterios de inclusión y exclusión para teleasistencia
| Criterios de inclusión |
| Conformidad para participar en consulta telefónica |
| Plenas facultades mentales |
| Disponibilidad y familiaridad en el uso de teléfono móvil, tableta u ordenador personal y aplicaciones informáticas |
| Paciente en seguimiento previo en consulta presencial |
| Criterios de exclusión |
| Ausencia de consentimiento verbal o escrito |
| Diagnóstico de asma no confirmado por pruebas objetivas |
| Imposibilidad física o cognitiva que impida la teleconferencia |
| Inestabilidad clínica que requiera exploración física o pruebas complementarias |
| Sospecha de exacerbación respiratoria moderada-grave |
| No respuesta a tratamientos pautados |
| Dudas por parte el médico o del paciente |
Tabla 5.
Consulta telefónica de seguimiento. Contenido
| Medición control de síntomas mediante encuesta clínica y cuestionario validado (ACT) |
| Exacerbaciones: cuantificación y gravedad |
| Cumplimiento (TAI, retirada en receta electrónica) |
| Comorbilidades |
| Desencadenantes y agravantes |
| Ajuste tratamiento |
| Solicitud de pruebas diagnósticas |
| Fijar próxima cita telemática o presencial |
ACT: test de control del asma; TAI: test de adherencia a inhaladores.
Tabla 6.
Control de los síntomas y de la función pulmonar
| Control de los síntomas1: |
| ¿Ha tenido síntomas diurnos de asma (número de veces/mes)? |
| ¿Ha tenido síntomas nocturnos/despertares por asma (número de noches/mes)? |
| ¿Le ha impedido el asma realizar sus actividades diarias (sí/no)? |
| ¿Precisó medicación de rescate (veces/mes)? |
| ¿Ha tenido crisis de asma que precisaron ciclo de corticoides orales, visitas a Urgencias o ingresos? |
| Cuestionario ACT |
| Función pulmonar* (según disponibilidad en AP) |
ACT: test de control del asma; AP: Atención Primaria.
La prueba ideal para medición de la función pulmonar es la espirometría con prueba broncodilatadora, pero en aquellos casos que no exista disponibilidad sería aconsejable realizar como mínimo una medición del FEM. Se aconseja al inicio del diagnóstico/tratamiento, a los 3-6 meses y luego periódicamente como mínimo una vez al año.
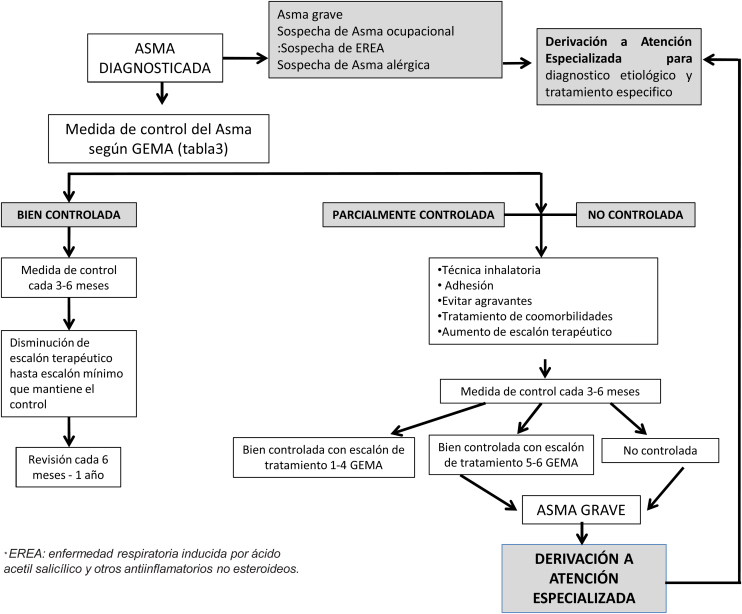
En ausencia de evidencia científica nuestro objetivo es consensuar unas pautas de seguimiento del asma en coordinación AP-Atención Especializada (AE) (fig. 2).
Figura 2.
Algoritmo de seguimiento del asma.
Las circunstancias actuales generan nuevas estrategias asistenciales basadas en las nuevas tecnologías que deberán ser una herramienta habitual en nuestra actividad y un excelente apoyo, si bien, en muchos aspectos, requieren una formación para la adquisición de habilidades específicas. El profesional sanitario debe jugar un papel protagonista en el diseño de las nuevas soluciones que permitan una consulta segura y de calidad.
Conflicto de intereses
José Ángel Carretero Gracia declara que en los últimos tres años ha recibido honorarios por impartir o recibir formación continuada y para proyectos científicos y de investigación procedentes de Boehringer Ingelheim, GlaxoSminthKline, Menarini, Novartis, TEVA y la fundación Pneumaragon de la Sociedad Aragonesa de Aparato Respiratorio. Fernando Rodríguez Fernández declara que en los últimos años ha recibido honorarios por asesor o consultor científico e impartir conferencias y sesiones patrocinadas para Astra/Zeneca, GSK, Mundipharma, Novartis y Sanofi. José Tomás Gómez Sáenz declara que los últimos tres años ha recibido honorarios por escribir monografías o impartir cursos y conferencias patrocinadas por sociedades científicas, GlaxoSmithKline, Menarini, BIAL, Boehringer-Ingelheim y Rovi. Jesús Molina declara que los últimos tres años ha recibido honorarios por impartir conferencias patrocinadas por Astra/Zeneca, Boehringer-Ingelheim, GlaxoSmithKline, Menarini, y Roche. Recibió financiación para proyectos de investigación de diferentes agencias gubernamentales, de sociedades científicas, así como de Boehringer-Ingelheim. Fernando Gómez Ruiz declara que en los últimos tres años ha recibido honorarios por impartir conferencias, cursos o asesoramiento científico de laboratorios Pfizer SL, Mundipharma, GSK y Lilly. Valentín López Carrasco declara que en los últimos años ha recibido honorarios en conceptos de docencia por parte de los siguientes laboratorios: Novartis, TEVA, GSK, Astra/Zeneca y Chiesi. Ana María Uréndez Ruiz declara que no tiene conflicto de intereses. David Díaz Pérez declara que no tiene conflictos de intereses. Marina Blanco Aparicio declara que los últimos tres años ha recibido honorarios por impartir conferencias, cursos, participar en monografías y normativas o asesoramiento científico de AstraZeneca, Sanofi, Esteve, GSK, Menarini, Novartis, TEVA y Sanofi. Javier Domínguez Ortega declara que en los últimos tres años ha recibido honorarios por asesor o consultor científico e impartir conferencias y sesiones patrocinadas para ALK-Abello, Astra/Zeneca, Chiesi, GSK, Mundipharma, Novartis, Sanofi y TEVA. Antonio Hidalgo Requena declara que en los últimos cinco años ha recibido honorarios por concepto de docencia, investigación, consultas y asistencia a congresos por parte de laboratorios Esteve, Astra/ Zeneca, GSK, Boheringuer Inguelheim, Menarini, Novartis, Pfizer, Mundifarma, TEVA, Rovi, Faes farma. Sara Núñez declara que los últimos tres años ha recibido honorarios por escribir monografías o impartir cursos y conferencias patrocinadas por sociedades científicas, GlaxoSmithKline, Pfizer y Rovi. Recibió financiación para proyectos de investigación de diferentes agencias gubernamentales y de sociedades científicas. Juan Antonio Trigueros declara que en los últimos tres años ha recibido honorarios en concepto de docencia, investigación y asesoramiento por Astra/Zeneca, GlaxoSmithKline, Menarini, Mundipharma, TEVA, Pfizer, y Chiesi. Francisco Javier Álvarez declara que en los últimos tres años ha recibido honorarios por impartir conferencias, cursos, escribir monografías o asesoramiento científico de ALK-Abello, Astra/Zeneca, Bial, Boheringer Ingelheim, Chiesi, Esteve, GSK, Menarini, Mundipharma, Novartis, TEVA y Sanofi. Julio Delgado declara que en los últimos tres años ha recibido honorarios por impartir conferencias, o asesoramiento científico para GSK, ALK-Abello, Astra/Zeneca, Chiesi, Mundipharma, Sanofi y TEVA.
Bibliografía
- 1.Guía Española para el Manejo del Asma (GEMA 5.1). Disponible en http://www.gemasma.com
- 2.Blanco Aparicio M., Delgado Romero J., Molina París J., Tomás Gómez J., Gómez Ruiz F., Álvarez Gutiérrez F.J., et al. Referral Criteria for Asthma: Consensus Document. J Investig Allergol Clin Immunol. 2019;29:422–430. doi: 10.18176/jiaci.0393. [DOI] [PubMed] [Google Scholar]
- 3.Cimas J.C.E., Fernández A., Gonzalvez J., Lobo M.A., Mascarós E., Molina J., et al. Sociedad Española de Medicina de Familia y Comunitaria; 2016. Guía de procedimiento para la Espirometría en Atención Primaria. [Google Scholar]
- 4.Olaguibel J.M., Alobid I., Alvarez Puebla M., Crespo-Lessmann A., Dominguez Ortega J., Garcia-Rio F., et al. Functional Examination of the Upper and Lower Airways in Asthma and Respiratory Allergic Diseases: Considerations in the Post-SARS-CoV-2 Era. J Investig Allergol Clin Immunol. 2021;31:17–35. doi: 10.18176/jiaci.0625. [DOI] [PubMed] [Google Scholar]
- 5.Núñez S., Álvarez F.J., Delgado J., Gómez F., Hidalgo A. Criterios de derivación de asma: nuevas perspectivas tras la pandemia de covid-19. Med Gen Fam. 2020;9:264–266. [Google Scholar]
- 6.Olaguibel A., Oleaga M., Iraola A., Cortaberria R., Corcuera A., Alvarez-Puebla M.J., et al. Exhaled Nitric Oxide (eNO) Measurements With the New evernoa Device Are Valid and Reproducible Through an Extended Range of eNO Levels. J Investig Allergol Clin Immunol. 2020;30:147–149. doi: 10.18176/jiaci.0465. [DOI] [PubMed] [Google Scholar]
- 7.Global Initiative for Asthma Global Strategy for Asthma Management and Prevention. 2021 Disponible en www.ginasthma.org. [Google Scholar]
- 8.SING 153. British guideline on the management of asthma 2016. https://www.brit-thoracic.org.uk/docu-ment-library/clinical-information/asthma/btssign-asthma-guideline-2016
- 9.Taylor D.R., Bateman E.D., Boulet L.P., Boushey H.A., Busse W.W., Casale T.B., et al. A new perspective on concepts of asthma severity and control. Eur Respir J. 2008;32:545–554. doi: 10.1183/09031936.00155307. [DOI] [PubMed] [Google Scholar]
- 10.Reddel H.K., Belousova E.G., Marks G.B., Jenkins C.R. Does continuous use of inhaled corticosteroids improve outcomes in mild asthma? A double-blind randomised controlled trial. Prim Care Respir J. 2008;17:39–45. doi: 10.3132/pcrj.2008.00014. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 11.Pauwels R.A., Pedersen S., Busse W.W., Tan W.C., Chen Y.Z., Ohlsson S.V., et al. Early intervention with budesonide in mild persistent asthma: a randomised, double-blind trial. Lancet. 2003;361:1071–1076. doi: 10.1016/S0140-6736(03)12891-7. [DOI] [PubMed] [Google Scholar]
- 12.O’Byrne P.M., Bisgaard H., Godard P.P., Pistolesi M., Palmqvist M., Zhu Y., et al. Budesonide/formoterol combination therapy as both maintenance and reliever medication in asthma. Am J Respir Crit Care Med. 2005;171:129–136. doi: 10.1164/rccm.200407-884OC. [DOI] [PubMed] [Google Scholar]
- 13.Suissa S., Ernst P. Inhaled corticosteroids: impact on asthma morbidity and mortality. J Allergy Clin Immunol. 2001;107:937–944. doi: 10.1067/mai.2001.115653. [DOI] [PubMed] [Google Scholar]
- 14.O’Byrne P.M., FitzGerald J.M., Bateman E.D., Barnes P.J., Zhong N., Keen C., et al. Inhaled Combined Budesonide-Formoterol as Needed in Mild Asthma. N Engl J Med. 2018;378:1865–1876. doi: 10.1056/NEJMoa1715274. [DOI] [PubMed] [Google Scholar]
- 15.Bateman E.D., Reddel H.K., O’Byrne P.M., Barnes P.J., Zhong N., Keen C., et al. As-Needed Budesonide-Formoterol versus Maintenance Budesonide in Mild Asthma. N Engl J Med. 2018;378:1877–1887. doi: 10.1056/NEJMoa1715275. [DOI] [PubMed] [Google Scholar]
- 16.Beasley R., Holliday M., Reddel H.K., Braithwaite I., Ebmeier S., Hancox R.J., et al. Controlled Trial of Budesonide-Formoterol as Needed for Mild Asthma. N Engl J Med. 2019;380:2020–2030. doi: 10.1056/NEJMoa1901963. [DOI] [PubMed] [Google Scholar]
- 17.Hardy J., Baggott C., Fingleton J., Reddel H.K., Hancox R.J., Harwood M., et al. Budesonide-formoterol reliever therapy versus maintenance budesonide plus terbutaline reliever therapy in adults with mild to moderate asthma (PRACTICAL): a 52-week, open-label, multicentre, superiority, randomised controlled trial. Lancet. 2019;394:919–928. doi: 10.1016/S0140-6736(19)31948-8. [DOI] [PubMed] [Google Scholar]
- 18.Vaquero-Lozano P.L.-G.I., Giner-Donaire J., Gómez-Neira M.d.C, Serra-Batlles J., García-García R., Álvarez Gutiérrez F.J., et al. Documento consenso de enfermería en asma 2020. Open Respir Arch. 2021;3:100079. doi: 10.1016/j.opresp.2020.100079. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 19.Bateman E.D., Jacques L., Goldfrad C., Atienza T., Mihaescu T., Duggan M. Asthma control can be maintained when fluticasone propionate/salmeterol in a single inhaler is stepped down. J Allergy Clin Immunol. 2006;117:563–570. doi: 10.1016/j.jaci.2005.11.036. [DOI] [PubMed] [Google Scholar]
- 20.Brusselle G.G., Vanderstichele C., Jordens P., Deman R., Slabbynck H., Ringoet V., et al. Azithromycin for prevention of exacerbations in severe asthma (AZISAST): a multicentre randomised double-blind placebo-controlled trial. Thorax. 2013;68:322–329. doi: 10.1136/thoraxjnl-2012-202698. [DOI] [PubMed] [Google Scholar]
- 21.Gibson P.G., Yang I.A., Upham J.W., Reynolds P.N., Hodge S., James A.L., et al. Effect of azithromycin on asthma exacerbations and quality of life in adults with persistent uncontrolled asthma (AMAZES): a randomised, double-blind, placebo-controlled trial. Lancet. 2017;390:659–668. doi: 10.1016/S0140-6736(17)31281-3. [DOI] [PubMed] [Google Scholar]
- 22.Torrego A., Sola I., Munoz A.M., Roque I.F.M., Yepes-Nunez J.J., Alonso-Coello P., et al. Bronchial thermoplasty for moderate or severe persistent asthma in adults. Cochrane Database Syst Rev. 2014;(3) doi: 10.1002/14651858.CD009910.pub2. CD009910. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 23.Blanco Aparicio M.A.G.F., Casas Maldonado F. Thermoplasty in the Spotlight. Arch Bronconeumol. 2020;56:269–270. doi: 10.1016/j.arbres.2019.07.016. [DOI] [PubMed] [Google Scholar]
- 24.Olaguibel J.M., Quirce S., Julia B., Fernandez C., Fortuna A.M., Molina J., et al. Measurement of asthma control according to Global Initiative for Asthma guidelines: a comparison with the Asthma Control Questionnaire. Respir Res. 2012;13:50. doi: 10.1186/1465-9921-13-50. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 25.Sastre J., Fabbri L.M., Price D., Wahn H.U., Bousquet J., Fish J.E., et al. Insights, attitudes, and perceptions about asthma and its treatment: a multinational survey of patients from Europe and Canada. World Allergy Organ J. 2016;9:13. doi: 10.1186/s40413-016-0105-4. [DOI] [PMC free article] [PubMed] [Google Scholar]