Abstract
目的
比较单纯食管超声心动图(TEE)引导与X射线引导经皮房间隔缺损(ASD)封堵术治疗ASD患儿的疗效差异。
方法
回顾性分析2017年1月至2018年3月浙江大学医学院附属儿童医院行单纯TEE引导经皮ASD封堵术患儿(TEE组,120例)和行X射线引导经皮ASD封堵术患儿(X射线组,125例)的资料。比较两组的手术实施情况、术后疗效和术后并发症发生情况等资料。
结果
TEE组和X射线组均顺利完成ASD封堵术。TEE组手术时间为(20±14)min,X射线组为(29±11)min,差异有统计学意义( t=-7.939, P < 0.05);TEE组ASD直径为(11±4)mm,大于X射线组[(9±4)mm, t=2.512, P < 0.05],但两组在术中使用的封堵器直径和外鞘直径差异无统计学意义(均 P>0.05)。两组患儿术后均无残余分流、封堵器脱落或移位,未发生严重心律失常、心包积液。术后发热、咳嗽、腹泻的发生率两组间差异无统计学意义(均 P>0.05)。
结论
单纯TEE引导经皮ASD封堵术与X射线引导经皮ASD封堵术疗效相近,但前者避免了射线辐射、手术时间短、对ASD的直径评估更精确,且无需使用大型数字减影设备,适宜推广和普及。
Abstract
Objective
To compare the efficacy of percutaneous atrial septal defect (ASD) closure guided by transesophageal echocardiography (TEE) or guided by fluoroscopy in pediatric patients.
Methods
Medical records of patients who underwent percutaneous ASD closure in the Children's Hospital, Zhejiang University School of Medicine from January 2017 to March 2018 were reviewed. There were 120 patients whose procedures were guided by TEE (TEE group), and 125 patients who had their procedures guided by fluoroscopy (fluoroscopy group). The performance of surgery, efficacy and postoperative complications were compared between two groups.
Results
Percutaneous ASD closure was successful in all patients. The operation time was shorter in the TEE group than that in fluoroscopy group[(20±14) min vs. (29±11) min, t=-7.939, P < 0.05]. The size of the defect was larger in the TEE group than that of fluoroscopy group[(11±4) mm vs. (9±4) mm, t=2.512, P < 0.05], but there was no significant difference in the sizes of occluder and occluder sheath between two groups (all P>0.05). No residual shunt, occluder shedding or displacement, severe arrhythmia or pericardial effusion were observed in either group. The incidence rates of fever, cough and diarrhea were not statistically different between two groups (all P>0.05).
Conclusion
There was no significant difference in the outcome of percutaneous ASD closure guided by TEE or by fluoroscopy, but the procedure guided by TEE may reduce the operation time and can evaluate the size of ASD more accurately without involving radiation exposure, contrast agents use and large digital subtraction equipment.
Keywords: Heart septal defects, atrial/surgery; Heart septal defects, atrial/ultrasonography; Echocardiography, transesophageal; Fluoroscopy; Child; Treatment outcome
先天性心脏病是导致流产、死胎和婴幼儿死亡、致残的主要原因之一,其发生率居我国出生缺陷的首位,是目前我国5岁以下儿童死亡的首要原因。房间隔缺损(atrial septal defect,ASD)是临床最常见的先天性心脏病之一,可导致反复呼吸道感染和生长发育落后,早期诊断和治疗可以避免严重并发症的发生。
ASD的治疗方法多样,主要包括心内直视下ASD修补术和ASD封堵术。心内直视下ASD修补术是一种高度侵入性的方法,不仅需要心肺分流术、开胸或胸骨切开,而且手术时间长,并发症发生率高。X射线引导经皮ASD封堵术因手术成功率高、患儿术后恢复快、术后并发症少、创伤小等优点,已成为治疗先天性ASD的一种常规术式。但X射线对儿童健康的影响不容忽视。近年来,随着ASD封堵技术的迅速发展和儿童超声技术的逐渐成熟,食管超声心动图(transesophageal echocardiography,TEE)引导经皮ASD封堵术开始逐步发展并应用于先天性ASD患儿的治疗。本研究回顾性分析2017年1月至2018年3月在浙江大学医学院附属儿童医院行单纯TEE引导经皮ASD封堵术和X射线引导经皮ASD封堵术患儿的资料,比较两种治疗方法的疗效。
选择2017年1月至2018年3月浙江大学医学院附属儿童医院行单纯TEE引导经皮ASD封堵术患儿(TEE组)120例和X射线引导经皮ASD封堵术患儿(X射线组)125例。所有患儿术前根据病史、临床症状和体征,胸部X射线、心电图及经胸超声心动图(TTE)检查结果确诊为继发孔型ASD,并为单孔ASD,缺损边缘至冠状静脉窦,上、下腔静脉及肺静脉的距离5 mm及以上,至二尖瓣距离7 mm及以上。所有患儿无中重度肺动脉高压、感染性疾病、其他心脏疾病等手术禁忌证。本研究方案经医院伦理委员会审批通过,并获患儿监护人书面知情同意。
TEE组中,男性38例,女性82例,年龄(67±39)个月,体质量为(20±12)kg;X射线组中,男性49例,女性76例,年龄(61±38)个月,体质量为(20±9)kg。TEE组ASD直径为(11±4)mm,大于X射线组[(9±4)mm, P < 0.05],但两组ASD与上腔静脉、下腔静脉、二尖瓣和心房顶的距离,以及房间隔长度差异均无统计学意义(均 P>0.05),见 表 1。
表1 两组患儿基线资料比较
Table 1 Baseline characteristics of two groups
|
( x ± s) | ||||||||||
|
组别 |
n |
男性/女性( n) |
月龄(月) |
体质量(kg) |
ASD直径(mm) |
ASD与SVC距离(mm) |
ASD与IVC距离(mm) |
ASD与MV距离(mm) |
ASD与心房顶距离(mm) |
房间隔长度(mm) |
|
TEE组 |
120 |
38/82 |
67±39 |
20±12 |
11±4 |
13±4 |
13±4 |
12±4 |
12±4 |
38±6 |
|
X射线组 |
125 |
49/76 |
61±38 |
20±9 |
9±4 |
13±4 |
14±4 |
11±4 |
12±3 |
38±6 |
|
t/ χ 2值 |
— |
1.517 |
1.167 |
-0.456 |
2.512 |
-0.167 |
-1.146 |
1.150 |
-0.441 |
0.274 |
|
P值 |
- |
>0.05 |
>0.05 |
>0.05 |
< 0.05 |
>0.05 |
>0.05 |
>0.05 |
>0.05 |
>0.05 |
“—”无相关数据.TEE:食管超声心动图;ASD:房间隔缺损;SVC:上腔静脉;IVC:下腔静脉;MV:二尖瓣.
由手术医生、超声科医生、麻醉科医生和巡回护士组成团队进行手术。患儿经静脉-吸入(经鼻气管插管)复合麻醉(咪达唑仑0.1~0.2 mg/kg,丙泊酚2 mg/kg,罗库溴铵0.9 mg/kg,芬太尼5~10 μg/kg)。通常选择TEE下心房两腔心切面、大动脉短轴切面、四腔心切面等对ASD进行评估。所有患儿均选用国产ASD封堵器[先健科技(深圳)有限公司和上海形状记忆合金材料有限公司]。测量右锁骨中线第3肋间至静脉穿刺点距离,并于术中在导管及导丝上标记该工作距离。常规穿刺右侧股静脉,置入动脉鞘管,静脉注射肝素80~100 U/kg。经动脉鞘管送入5-6F多功能导管和加硬导丝,将导管和导丝一起向前推送,切忌暴力推送导管。经股静脉途径者可以在剑突下切面显示下腔静脉,监测导管和导丝通过情况。导管和导丝插入体内到达工作距离后,退出导丝,轻轻旋转导管,超声于两腔心切面即可发现导管。在超声引导下调整导管方向,将导管送过ASD进入左心房。沿导管插入导丝,插入深度不能超过工作距离5~7 cm,同时必须严格超声监测,切勿插入过深损伤左心房。保留导丝,退出导管,同时标记导管插入的深度。退出动脉鞘管后,沿加硬导丝将输送鞘送至左心房,其送入体内的深度与前述导管送入体内的深度一致。退出导丝及输送鞘内芯的同时轻轻推送外鞘管,保持输送鞘管头端在左心房内的位置不变。按超声测量的ASD最大缺损直径加4~6 mm选择封堵器,同时测量房间隔总长度,以便判断封堵器是否能充分展开,ASD直径较大或缺损边缘较薄时封堵器可增加至8~10 mm。在超声监测下送入ASD封堵器进行封堵,安装及推送封堵器过程中要严格排气,推送时应将系统尾部浸没于等渗氯化钠溶液中,以免推送过程中因负压抽吸导致进气。封堵器安置成功后,在主动脉短轴切面、心尖四腔心切面、两腔心(经鼻气管插管)切面、剑突下切面等超声确认封堵器对二尖瓣、肺静脉及冠状静脉窦等周围组织无影响,位置及形态良好后释放封堵器。拔出长鞘,压迫或缝合穿刺点后加压绷带包扎。手术过程中的超声影像见 图 1。
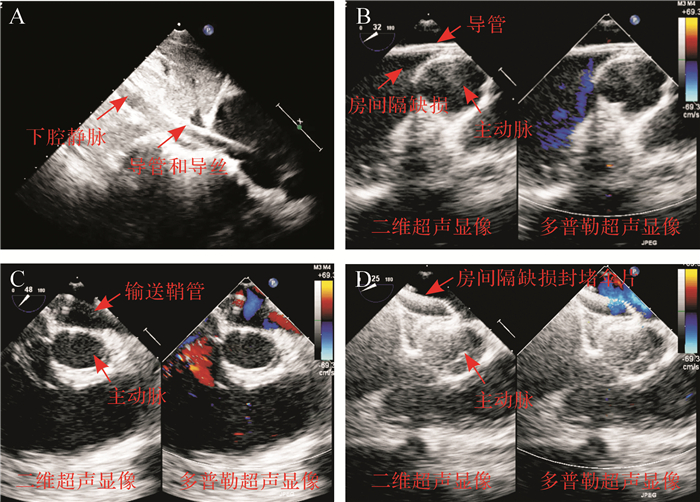
年龄大于12岁且能够配合手术的患儿使用利多卡因局部麻醉; 不能配合手术的患儿行吸入麻醉加骶管麻醉。吸入麻醉药物为咪达唑仑0.1~ 0.2 mg/kg、丙泊酚2 mg/kg、喷他佐辛0.3 mg/kg,骶管麻醉按照利多卡因“高剂量低浓度、总量不超过10 mg/kg”的原则,体质量为10~15 kg的患儿使用浓度为0.67%的利多卡因,15~25 kg的患儿使用浓度为0.8%的利多卡因。术前通过TTE评估ASD的直径和边缘条件,所有患儿均选用国产ASD封堵器[先健科技(深圳)有限公司和上海形状记忆合金材料有限公司]。常规穿刺右侧股静脉,置入动脉鞘管,静脉注射肝素80~100 U/kg。在X射线引导经动脉鞘管送入5-6F多功能导管及加硬导丝,通过ASD进入肺静脉,交换导丝后置入输送鞘,沿输送鞘将封堵器送入左心房,释放左房盘后回撤递送系统使左房盘与房间隔相贴,回撤外鞘以释放封堵器腰部和右房盘,完成推拉试验。TTE多切面观察,对封堵器位置,残余分流,各瓣膜情况,有无心包积液,封堵器与冠状静脉窦、上下腔静脉及肺静脉的关系等进行评估。确定封堵成功后在X射线引导下释放封堵器,拔出长鞘,压迫或缝合穿刺点后,加压绷带包扎。
两种术式操作过程中均密切注意患儿血压有无波动,心电图有无传导阻滞、T波改变等心律失常等,如有异常,暂停手术,待恢复后继续手术。记录封堵器直径、外鞘直径和手术时间(肝素化到输送系统退出的时间)。两种术式的操作人员均获得国家心血管疾病介入诊疗医师资质,操作能力和水平达到均质化要求。
所有患儿术前完善相关检查,并于术前24 h或手术当日静脉应用抗菌药物。术后肝素抗凝24 h,静脉应用抗菌药物24 h;对所有患儿进行心电监测,24 h内复查超声心动图、胸部X射线检查、心电图,观察1~2 d情况良好后出院。所有患儿术后口服阿司匹林6个月,剂量为每日3~5 mg/kg。术后第1、3、6、12个月及每年随访,复查心电图和超声心动图,必要时行胸部X射线检查。
所有数据采用SPSS 20.0软件分析。计量资料以均数±标准差( x ± s)表示,组间比较采用 t检验;计量数据采用例数和百分率[ n(%)]表示,组间比较采用 χ 2检验或精确概率检验法。 P<0.05为差异有统计学意义。
两组患儿均顺利完成手术。TEE组的手术时间为(20±14)min,较X射线组[(29±11)min]缩短,差异有统计学意义( t=-7.939, P<0.05);TEE组使用的封堵器直径为(15±4)mm,X射线组为(14±4)mm,差异无统计学意义( t=1.031, P>0.05);TEE组使用的外鞘直径为(8.9±1.7)mm,X射线组为(8.9±1.0)mm,差异无统计学意义( t=0.058, P>0.05)。
TEE组和X射线组分别有4例(3.3%)和7例(5.6%)患儿术后出现发热,复查血常规,均未见白细胞、中性粒细胞或淋巴细胞百分比等指标明显增高,予对症治疗后好转;TEE组和X射线组分别有4例(3.3%)和5例(4.0%)患儿术后出现咳嗽,行胸部X射线检查均未见下呼吸道感染征象,予雾化治疗后好转;TEE组和X射线组各有1例患儿术后出现腹泻(0.83%和0.80%),行消化道病毒检测均未见阳性,对症治疗后好转。两组术后发热、咳嗽、腹泻的发生率差异均无统计学意义(均 P>0.05)。两组患儿术后复查心脏超声、心电图和胸部X射线检查均无严重心律失常、残余分流、封堵器脱落或移位、心包积液等。两组均无下肢活动障碍、溶血等并发症发生。
随着小儿先天性心脏病治疗技术的发展和成熟,ASD的治疗方法也趋于多样化,主要包括器械封堵术和心内直视下ASD修补术。传统的器械封堵术主要是经皮X射线引导ASD封堵术,该手术方式因创伤小、手术时间短、术后恢复快 [ 1- 2] ,在一定范围内替代了心内直视下ASD修补术。但是,射线可能会影响患儿骨髓、生殖器及甲状腺等器官的功能,亦对医务人员身体造成一定程度的损害 [ 3- 6] 。2004年,Kardon等 [ 7] 提出了TEE引导经皮ASD封堵术。近年来,TEE引导经皮ASD封堵术临床应用逐渐增多 [ 8- 9] 。TEE引导经皮ASD封堵术既保留了X射线引导经皮ASD封堵术安全、美观的优点,又可以避免儿童辐射损伤、造影剂过敏、肾功能损伤等风险,以及医务人员长期辐射暴露导致的损伤和穿着铅衣而带来的高强度劳动 [ 10- 11] 。本文回顾性分析浙江大学医学院附属儿童医院实施X射线引导经皮ASD封堵术和单纯TEE引导经皮ASD封堵术的临床资料,比较两种手术方法的疗效差异,总结单纯TEE引导经皮ASD封堵术实施的可行性及其中的操作要点。
本文资料显示,所有患儿均成功实施了ASD封堵术,X射线引导经皮ASD封堵术与单纯TEE引导经皮ASD封堵术疗效相似,且两组患儿均未出现严重心律失常、残余分流、封堵器脱落或移位和心包积液等特异性的术后并发症。两组术后均有患儿出现发热、咳嗽、腹泻等症状。本文资料术后出现发热的患儿血常规均未见明显异常,可以在一定程度上排除感染的可能,考虑术后应激反应和麻醉药物不良反应可能性较大。咳嗽症状可能与术前社区呼吸道感染、手术温度变化引起上呼吸道应激等有关。由于TEE组采用气管插管,术后咽喉和气管损伤水肿引起咳嗽的概率较高。两组出现腹泻的患儿其感染指标均阴性,考虑可能与手术应激、麻醉后肠道功能紊乱有关。
根据本文资料,除避免了放射辐射外,单纯TEE引导经皮ASD封堵术还具有以下优点:
首先,TEE组的手术时间较X射线组短,分析原因主要有:①TEE的图像更清晰,能够更精确地评估ASD的大小和位置,有利于快速选择合适的封堵器一次性封堵成功;②X射线组须将多功能导管置入左右肺静脉中,输送鞘要到达肺静脉后再回撤,而TEE组在多功能导管穿过ASD后即可通过交换导丝引导输送鞘通过ASD,快者仅6 min即可完成封堵操作;③X射线数字减影设备对心内解剖结构显影不精确,在封堵过程中须旋转机头和搬运超声机器反复评估,延长了手术时间。
其次,单纯TEE引导经皮ASD封堵术在实施过程中可以更为精确地对ASD的大小进行评估,从而选择合适的封堵器。Baruteau等 [ 12] 认为无论是TEE还是TTE都能很好地进行ASD的测量、伞片释放等操作步骤,但TEE能更清晰更精确地评估ASD的大小 [ 13] 。本文资料显示,TEE组术前ASD直径大于X射线组,但两组的封堵器和输送外鞘的直径差异无统计学意义,提示相同大小的封堵器和输送外鞘在TEE的评估下可以在更大的ASD上使用。对于左右心房容积不大、房间隔长度不足等临界条件的患儿,使用相对更小的封堵器和更细的输送鞘可以减少股静脉损伤、主动脉心房瘘等并发症的发生。
此外,单纯TEE引导经皮ASD封堵术不需要大型数字减影设备,可在外科手术室进行操作,一旦术中发现ASD不适合经皮封堵或者经皮封堵失败,可立即转为TEE引导经胸封堵术或者心内直视下修补术,最快速度实现术中响应,最大限度保证患儿术中安全。
但是,单纯TEE引导经皮ASD封堵术在实施过程中仍具有一定的局限性。首先,其操作过程中导管、导丝、鞘管路径的整体观不如X射线引导ASD封堵术。因此,初学者在进行手术时可能会出现导管和导丝进入下腔静脉分支等血管、导管打折、血管破裂、左房破裂等不良事件。根据我们的经验,可以通过以下三个方法来避免这些不良事件的发生:①股静脉置管后,超声探头以股静脉为起点,随着导管和导丝的进入连续扫描,引导导管和导丝的前行方向;②术前测量股静脉到胸骨2、3肋间的距离,并在导管、鞘管和导丝上做好标记;③如有导管和导丝进入分支血管,及时退出后轻缓旋转调整导管头部方向后再前行,遇到阻力切勿盲目前行,到达左心房后避免进入左心耳。
综上所述,单纯TEE引导经皮ASD封堵术与X射线引导经皮ASD封堵术在疗效上无显著差异,但单纯TEE引导经皮ASD封堵术避免了射线辐射,手术时间短,对ASD的直径评估更精确,且无需使用大型数字减影设备,更适宜推广和普及。
Funding Statement
浙江省科技厅国际科技合作项目(2016C54006);浙江省卫生高层次人才培养工程(2016-6)
References
- 1.DU Z D, HIJAZI Z M, KLEINMAN C S, et al. Comparison between transcatheter and surgical closure of secundum atrial septal defect in children and adults:results of a multicenter nonrandomized trial. J Am Coll Cardiol. 2002;39(11):1836–1844. doi: 10.1016/S0735-1097(02)01862-4. [DU Z D, HIJAZI Z M, KLEINMAN C S, et al. Comparison between transcatheter and surgical closure of secundum atrial septal defect in children and adults:results of a multicenter nonrandomized trial[J]. J Am Coll Cardiol, 2002, 39(11):1836-1844.] [DOI] [PubMed] [Google Scholar]
- 2.MOORE J, HEGDE S, EL-SAID H, et al. Transcatheter device closure of atrial septal defects:a safety review. JACC Cardiovasc Interv. 2013;6(5):433–442. doi: 10.1016/j.jcin.2013.02.005. [MOORE J, HEGDE S, EL-SAID H, et al. Transcatheter device closure of atrial septal defects:a safety review[J]. JACC Cardiovasc Interv, 2013, 6(5):433-442.] [DOI] [PubMed] [Google Scholar]
- 3.KLEINERMAN R A. Cancer risks following diagnostic and therapeutic radiation exposure in children. http://d.old.wanfangdata.com.cn/NSTLQK/10.1007-s00247-006-0191-5/ Pediatr Radiol. 2006;36(Suppl 2):121–125. doi: 10.1007/s00247-006-0191-5. [KLEINERMAN R A. Cancer risks following diagnostic and therapeutic radiation exposure in children[J]. Pediatr Radiol, 2006, 36 Suppl 2:121-125.] [DOI] [PMC free article] [PubMed] [Google Scholar]
- 4.National Research Council(US) Board on Radiation Effects Research. Health risks from exposure to low levels of ionizing radiation: BEIR Ⅶ Phase 2[C]. Washington, D.C.: National Academies Press, 2006. . [PubMed]
- 5.WAGDI P, RITTER M. Patient radiation dose during percutaneous interventional closure of interatrial communications. J Cardiol. 2009;53(3):368–373. doi: 10.1016/j.jjcc.2009.01.001. [WAGDI P, RITTER M. Patient radiation dose during percutaneous interventional closure of interatrial communications[J]. J Cardiol, 2009, 53(3):368-373.] [DOI] [PubMed] [Google Scholar]
- 6.YAKOUMAKIS E N, GIALOUSIS G I, PAPADOPOULOU D, et al. Estimation of children's radiation dose from cardiac catheterisations, performed for the diagnosis or the treatment of a congenital heart disease using TLD dosimetry and Monte Carlo simulation. J Radiol Prot. 2009;29(2):251–261. doi: 10.1088/0952-4746/29/2/011. [YAKOUMAKIS E N, GIALOUSIS G I, PAPADOPOULOU D, et al. Estimation of children's radiation dose from cardiac catheterisations, performed for the diagnosis or the treatment of a congenital heart disease using TLD dosimetry and Monte Carlo simulation[J]. J Radiol Prot, 2009, 29(2):251-261.] [DOI] [PubMed] [Google Scholar]
- 7.KARDON R E, SOKOLOSKI M C, LEVI D S, et al. Transthoracic echocardiographic guidance of transcatheter atrial septal defect closure. Am J Cardiol. 2004;94(2):256–260. doi: 10.1016/j.amjcard.2004.03.080. [KARDON R E, SOKOLOSKI M C, LEVI D S, et al. Transthoracic echocardiographic guidance of transcatheter atrial septal defect closure[J]. Am J Cardiol, 2004, 94(2):256-260.] [DOI] [PubMed] [Google Scholar]
- 8.HONGXIN L, ZHANG N, WENBIN G, et al. Peratrial device closure of perimembranous ventricular septal defects through a right parasternal approach. Ann Thorac Surg. 2014;98(2):668–674. doi: 10.1016/j.athoracsur.2014.03.029. [HONGXIN L, ZHANG N, WENBIN G, et al. Peratrial device closure of perimembranous ventricular septal defects through a right parasternal approach[J]. Ann Thorac Surg, 2014, 98(2):668-674.] [DOI] [PubMed] [Google Scholar]
- 9.卢 衡, 陈 良万, 张 贵灿, et al. 超声心动图引导下经皮房间隔缺损封堵术的临床评估. http://d.old.wanfangdata.com.cn/Periodical/hnykdx201506012. 中南大学学报:医学版. 2015;40(6):646–650. doi: 10.11817/j.issn.1672-7347.2015.06.012. [卢衡, 陈良万, 张贵灿, 等.超声心动图引导下经皮房间隔缺损封堵术的临床评估[J].中南大学学报:医学版, 2015, 40(6):646-650.] [DOI] [PubMed] [Google Scholar]
- 10.潘 湘斌, 逄 坤静, 胡 盛寿, et al. 经食管超声心动图引导下介入治疗房间隔缺损幼儿的有效性和安全性. 中华心血管病杂志. 2013;41(9):744–746. doi: 10.3760/cma.j.issn.0253-3758.2013.09.005. [潘湘斌, 逄坤静, 胡盛寿, 等.经食管超声心动图引导下介入治疗房间隔缺损幼儿的有效性和安全性[J].中华心血管病杂志, 2013, 41(9):744-746.] [DOI] [PubMed] [Google Scholar]
- 11.EWERT P, BERGER F, DAEHNERT I, et al. Transcatheter closure of atrial septal defects without fluoroscopy:feasibility of a new method. Circulation. 2000;101(8):847–849. doi: 10.1161/01.CIR.101.8.847. [EWERT P, BERGER F, DAEHNERT I, et al. Transcatheter closure of atrial septal defects without fluoroscopy:feasibility of a new method[J]. Circulation, 2000, 101(8):847-849.] [DOI] [PubMed] [Google Scholar]
- 12.BARUTEAU A E, HASCOËT S, FRAISSE A. Transthoracic echocardiography is a safe alternative for assessment and guidance of transcatheter closure of secundum atrial septal defect in children. J Thorac Dis. 2017;9(5):1247–1256. doi: 10.21037/jtd. [BARUTEAU A E, HASCOËT S, FRAISSE A. Transthoracic echocardiography is a safe alternative for assessment and guidance of transcatheter closure of secundum atrial septal defect in children[J]. J Thorac Dis, 2017, 9(5):1247-1256.] [DOI] [PMC free article] [PubMed] [Google Scholar]
- 13.ZHANG G C, CHEN Q, CAO H, et al. Minimally invasive perventricular device closure of ventricular septal defect in infants under transthoracic echocardiograhic guidance: feasibility and comparison with transesophageal echocardiography[J/OL]. Cardiovasc Ultrasound, 2013, 11: 8. . [DOI] [PMC free article] [PubMed]


