Abstract
目的
设计制备三种瑞戈非尼环糊精包合物,以改善瑞戈非尼的溶解度、溶出度和生物利用度。
方法
采用重结晶、饱和水溶液等方法对瑞戈非尼—环糊精包合物的制备方法进行研究,通过傅里叶红外光谱、热重分析、X射线粉末衍射、核磁共振、核欧佛豪瑟效应频谱等方法对瑞戈非尼—环糊精包合物进行结构分析。并采用SW620结肠癌细胞荷瘤裸鼠模型考察其体内抑瘤效果。
结果
瑞戈非尼被环糊精包合后溶解性能明显改善,溶出度从大到小依次为:瑞戈非尼-β-环糊精包合物 > 瑞戈非尼—羟丙基-β-环糊精 > 瑞戈非尼-γ-环糊精包合物。优选包合及溶出效果最好的瑞戈非尼-β-环糊精包合物进行裸鼠体内抑瘤试验,结果表明,瑞戈非尼-β-环糊精包合物抑瘤效果比瑞戈非尼明显提高。
结论
难溶性药物瑞戈非尼被环糊精包合后其溶解度和溶出度改善,从而提高瑞戈非尼的生物利用度。
Abstract
Objective
In order to improve the drug's solubility, dissolution and bioavailability, RG-β-CD, RG-γ-CD and RG-Hp-β-CD were prepared by co-crystallization between Regorafenib (RG) and β-cyclodextrin (β-CD), γ-cyclodextrin (γ-CD) and Hydroxypropyl-β-cyclodextrin (Hp-β-CD).
Methods
Three inclusion complexes were prepared by recrystallization and solvent evaporation methods and characterized by fourier transform infrared spectroscopy (FT-IR), thermal analysis (TG), differential scanning calorimetry (DSC), powder X-ray diffraction (PXRD), 1H nuclear magnetic resonance ( 1H-NMR), nuclear overhauser effect spectroscopy (NOESY). In vivo experiments, tumor suppression assay were made with SW620 colon cancer cell.
Results
The ability of solubility and dissolution were improved after inclusion with three kinds of cyclodextrins. The regorafenib-β-cyclodextrin inclusionis proved to have the best stability. The less enhanced was regorafenib-γ-cycl-odextrin inclusion. The best dissolution of regorafenib-β-cyclodextrin inclusion complex was to bring as the tumor suppression assay, the result shows that regorafenib inclusion with β-cyclodextrin is better than regorafenib itself.
Conclusion
The bioavailability of regorafenib by inclusion with cyclodextrin can enhance due to the solubility enhancement of RG, which can provide an effective method for improving solubility and dissolution of insoluble drug in clinical medication.
Keywords: Protein kinase inhibitors, Beta-cyclodextrins, Drug compounding, Antineoplastic agents, Solubility, Biological availability
瑞戈非尼(regorafenib,RG)是一种新型的口服多靶点络氨酸激酶抑制剂,可以有效阻断促进肿瘤血管生成的多个蛋白激酶,同时破坏肿瘤生长所需要的微环境,具有良好的抗肿瘤活性 [ 1- 4] 。2013年2月,美国食品药品监督管理局(FDA)批准其用于治疗先前接受过伊马替尼和舒尼替尼治疗的局部晚期、不能手术切除或转移性胃肠道间质瘤患者 [ 5- 8] 。
然而,瑞戈非尼属于生物药剂学分类系统(BCS)Ⅱ类药物 [ 9] ,溶解度低,影响其生物利用度和临床疗效。目前常用能提高药物溶解度的包合技术采用具有空穴结构的分子包合药物形成包合物,这种包合物由主体分子和客体分子组成。药物被包合后,溶解度增大,稳定性提高 [ 10- 12] 。近年来,环糊精(cyclodextrin,CD)作为包合材料在超分子化学领域起着相当重要的作用 [ 13- 15] 。CD的分子是由六个或者六个以上葡萄糖通过α-1, 4糖苷键连接而成的环状低聚糖,每个葡萄糖单元都是椅式构象。常见的β-CD和γ-CD是已知效果最好的包合材料,分别含有七个、八个葡萄糖单元,羟丙基-β-环糊精(Hp-β-CD)是β-CD部分葡萄糖的6-位羟基与1, 2-环氧丙烷发生醚化反应引入6-(2, -羟丙基)的产物,其口服后基本全部以原形代谢排出体外,几乎不参与生物体内代谢,也不蓄积。
本研究采用β-CD、γ-CD、Hp-β-CD对瑞戈非尼进行包合,探究形成的包合物对药物溶解度、溶出度和生物利用度的影响,为提高瑞戈非尼药效提供一个新的途径。
瑞戈非尼(纯度大于99%)由浙江京新药业股份有限公司提供;β-CD(纯度大于99%)购自上海伯奥生物科技有限公司);γ-CD(纯度大于99%)购自上海麦克林生化科技有限公司)。十二烷基硫酸钠(SDS)购自国药集团化学试剂有限公司;DMEM培养基购自赛默飞世尔生物化学制品(北京)有限公司;Gibco胎牛血清、Gibco胰蛋白酶EDTA溶液购自美国Thermo Fisher Scientific公司;二甲基亚砜(DMSO)购自西格玛奥德里奇(上海)贸易有限公司;其它试剂均为分析纯。SW620细胞株购自中国科学院上海生科院细胞资源中心。BALB/c裸鼠(体质量16~18 g)购自浙江省医学科学院。
多晶X射线衍射仪(Rigaku D/Max-2550) 为日本理学公司产品;差示扫描量热仪(DSC Q100) 和热重分析仪(TA SDT Q600) 为美国TA公司产品;傅里叶红外光谱仪(VECTOR-22) 为德国Bruker公司产品;核磁共振光谱仪(Bruker Advance Ⅲ500MH Z)为德国Bruker公司产品;紫外分光光度计(U-3400) 为日本日立公司产品。
称取β-CD1.134 g(1 mmol)和RG 0.482 g(1 mmol)至圆底烧瓶中,加70%的乙醇40 mL放入水浴锅中边搅拌边加热到85 ℃,溶清后继续搅拌8~24 h,然后取出室温(15~30 ℃)放置,静置析晶8~10 h,直至析晶完全,抽滤,烘干(25 ℃真空干燥),即得RG-β-CD包合物。RG-γ-CD、RG-Hp-β-CD制备方法同上。
RG及RG包合物研磨过300目筛,平铺在测试板凹槽内,压平,置于多晶X射线衍射仪上测定。采用CuKα辐射(λ=1.540 59 Å),电压40 kV,电流250 mA,扫描范围是3.0~40.0°(2θ),步宽为0.02°,DS=SS=1°,RS=0.15 mm,扫描速度5°/min。所得数据用MDI-Jade version 6.5软件处理。
精密称取1~3 mg样品放入铝盘中,测试条件为:氮气速度为50 mL/min,升温速度为10 ℃/min,温度范围为30 ℃~400 ℃。对RG及RG-CD包合物样品进行差示扫描量热分析。5 mg样品在氮气流(流速=120 mL/min)中,以10 ℃/min升温速度从30 ℃升到400 ℃,进行热重分析。
分别取RG、RG-CD包合物共4个粉末样品适量,与溴化钾混合均匀,将混合物研细之后压成片,在4000~400 cm -1范围内测其红外光谱。
RG、β-CD、γ-CD、HP-β-CD以及其包合物均以氘代二甲基亚砜(DMSO-d 6)为溶剂,充分溶解后装入核磁共振管中,室温下用核磁共振光谱仪进行测定。
RG粉末20 mg(0.041 mmol)溶于10 mL甲醇后转移至50 mL容量瓶中,用甲醇定容至刻度线。分别取0.1、0.2、0.3、0.4、0.5 mL溶液,用含0.2% SDS表面活性剂的水溶液定容至25 mL。220~400 nm全波长扫描,得到特征吸收谱线波长,在此波长处测定不同浓度的吸光度值,每个样品平行测定三次。由浓度和吸光度值绘制RG在水中的标准曲线。同样的方法分别测定RG在酸碱度值为1.2酸性溶液(含0.2%十二烷基硫酸钠)和酸碱度值为6.8磷酸缓冲溶液(含0.2%十二烷基硫酸钠)以及RG包合物在以上介质中的标准曲线。
制备得到的RG-β-CD包合物粉末16.1 mg用含0.2% SDS表面活性剂的水溶液溶解后转移于50 mL容量瓶中,用含0.2% SDS表面活性剂的水溶液定容,取1 mL溶液定容至10 mL的容量瓶中,在1.4.1项测得的特征吸收波长处测定吸光度值(在特征波长处三种CD均无吸收),每个样品平行测定三次。同样的方法测定RG-γ-CD包合物和RG-HP-β-CD包合物的包合率。
取RG(0.5g)三份分别加入500 mL水、酸碱度值1.2酸性溶液和酸碱度值6.8磷酸缓冲溶液中,置水浴锅中,37 ℃,100 r/min转速下振荡,每隔一定时间时取样5 mL,过0.45 μm的微孔滤膜至离心管中,每次取样完成后加等温等量的溶出溶剂。为使测定得到的吸光度值在规定范围内,取样得到的澄清溶液用相应的溶剂稀释一定的倍数,再行测定。每个样品平行测定三次。同样的方法测定含等量药物的RG-β-CD包合物、RG-γ-CD包合物和RG-HP-β-CD包合物粉末在以上溶剂中的溶出曲线。
取BALB/c裸鼠(16~18 g)15只,用SW620结肠癌细胞株荷瘤,无菌条件下于裸鼠左下腹皮下一次性接种SW620细胞6×10 6个/100 μL。待肿瘤长至100 mm 3左右时,随机分为三组,分别为肿瘤对照组、RG对照组和RG-β-CD组,各组每周一、三、五分别PBS、RG和RG-β-CD口服给药,RG和RG-β-CD均用生理盐水配成250 μg/mL和1000 μg/mL(相当于250 mg/mL RG), 每只裸鼠口服80 μg/200 μL。连续给药3周,观察裸鼠的肿瘤生长和裸鼠的生存情况。
实验所得的数据采用SPSS11(for Windows)统计分析软件包进行统计分析,行方差齐性检验,多个样本间比较采用单因素方差分析,两组间比较采用Bonferronit检验, P < 0.05为差异具有统计学意义。
RG在衍射角2θ为7.25°、13.40°、14.54°处有强的特征衍射峰;β-CD在2θ为4.52°、9.03°、12.49°有强的特征衍射峰;包合物的衍射图谱中瑞戈非尼的特征衍射峰消失,在2θ为6.04°、7.15°、10.02°、12.15°处有强的衍射峰。γ-CD在衍射角2θ为5.05°、6.14°、10.12°处有特征衍射峰;包合物的衍射图谱中RG的特征峰消失,在2θ为5.21°、7.39°、10.50°、14.20°处有特征衍射峰,说明形成了新的物相。HP-β-CD的X-射线衍射图无明显的特征衍射峰,说明其为无定形;包合物的衍射图谱中RG的特征峰消失,同样有两个无定形的包,说明可能形成了新的物相,但是否形成包合物将在下面的表征中进行验证。RG、CD与RG包合物的X射线衍射图见 图 1。

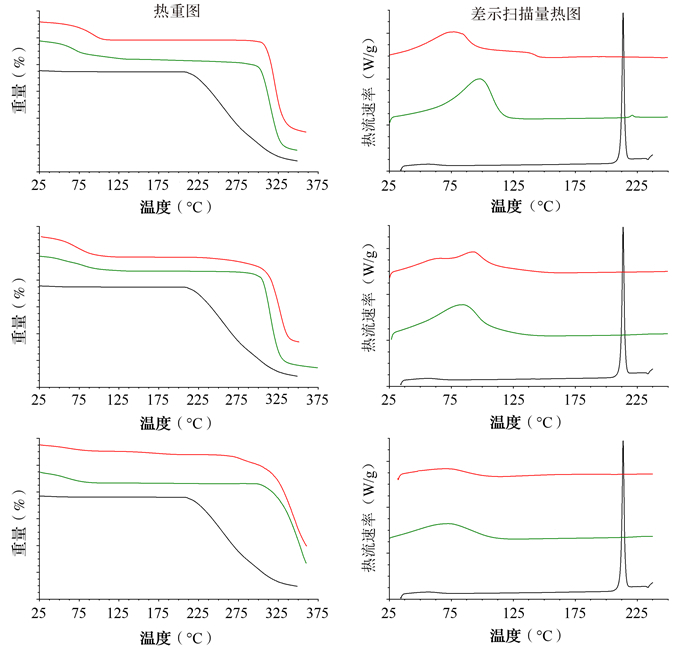
从热重图中可以看出,RG没有失水峰,RG的三种环糊精包合物在分解前不断失水,且在300 ℃左右开始熔融分解,与RG有很大差别,说明CD已基本包合RG,提高了药物的耐热分解能力。
由差示扫描量热图可知,在RG的三个CD包合物的曲线中,均形成了新的吸热峰(RG-β-CD包合物的76.8 ℃、131.9 ℃两个吸热峰,RG-γ-CD包合物的63.9 ℃、92.7 ℃两个吸热峰和RG-HP-β-CD包合物的69.7 ℃吸热峰),已无RG(213.7 ℃)的熔点峰和熔融分解峰,说明RG已被环糊精包合,形成了新的物质。RG与RG-CD包合物的热重和差示扫描量热图见 图 2。
以RG-β-CD包合物为例,RG在3350 cm -1处有-NH 2伸缩振动强峰,3142 cm -1、3076 cm -1为C-H吸收峰,1721 cm -1处C=O伸缩振动,1658 cm -1、1546 cm -1、1486 cm -1为苯环的强吸收峰;β-CD在3440 cm -1附近为-OH的伸缩振动吸收峰,2922 cm -1附近为-CH 2的反对称伸缩振动吸收峰,1416 cm -1附近显示-CH 2的弯曲振动吸收峰,1641 cm -1处-COOH中C=O键的吸收峰;在包合物的红外光谱中,RG部分特征峰(1720 cm -1处的C=O伸缩振动峰)消失或较弱,而β-环糊精中C-O伸缩振动,-OH伸缩振动峰均向高频位移了几个到十几个单位,1641 cm -1处的C=O吸收峰消失, 可以推断β-CD对RG有包合作用,且只有部分基团被包裹于β-CD及其衍生物的空腔中。RG、CD和RG-CD包合物的红外图谱见 图 3。

以RG-β-CD包合物为例,β-CD中H-1、H-3、H-4和H-5的化学位移分别位于4.83 ppm、3.63 ppm、3.35 ppm和3.55 ppm;RG-β-CD包合物中H-3、H-5的化学位移分别为3.60 ppm和3.58 ppm,H-1、H-4为4.83 ppm和3.37 ppm,H-3和H-5处于环糊精空腔内部,H-1和H-4处于空腔外部。由这两条曲线可知,RG从宽边进入与H-5相连接,说明RG和β-CD形成了包合物。同理可推断形成了RG-γ-CD和RG-HP-β-CD包合物。RG、β-CD、γ-CD和HP-β-CD及与RG包合物的核磁共振H谱见 图 4。

NOESY是通过NOE效应来建立核与核之间联系的,NOESY的交叉峰表明两个质子之间有足够强的NOE效应,通常两个质子之间的距离不大于5Å时才可能检测到NOE效应。另外,由交叉峰强度还可得出核与核之间的距离。RG-γ-CD包合物和RG-HP-β-CD包合物的核欧佛豪瑟效应频谱见 图 5。
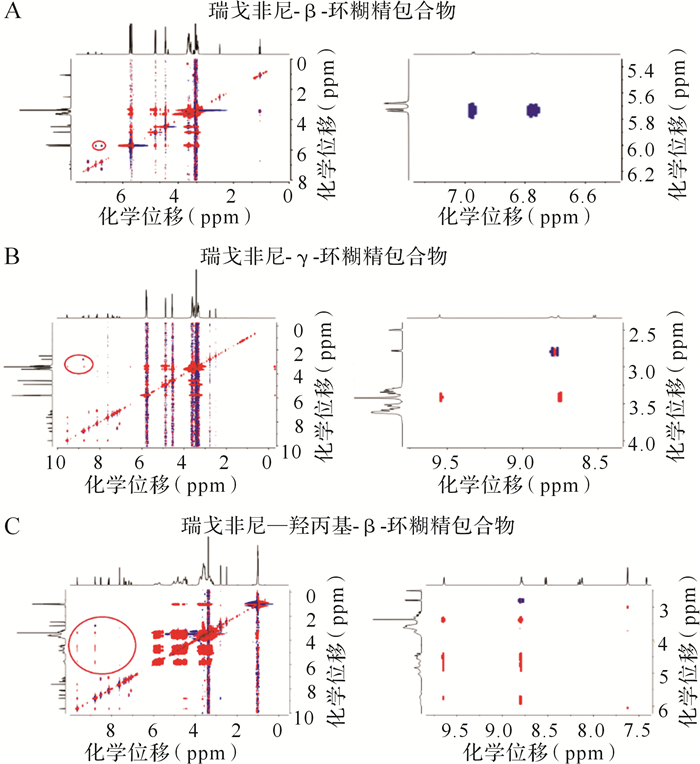
图 5A是RG-β-CD包合物的NOESY图,在化学位移5.8~6.2 ppm处环糊精的质子峰与RG的三氟甲基上的质子有重合,说明RG的三氟甲基连接的芳环上的氢与环糊精的氢有相关,其余RG的氢峰全部消失,因此可推断RG除了三氟甲基芳香环的一端露出β-CD外,剩余一段套入环糊精的空腔中,由于环糊精中含水量较多,RG是以稳定的一水合物晶型的形式存在并套入,可推测形成如 图 6的结构。
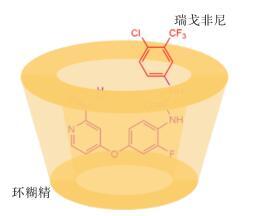
图 5B是RG-γ-CD包合物的NOESY图。图中γ-CD在化学位移2.4~3.4 ppm处的质子峰与RG酰胺基团上的甲基峰和尿基上的氨基峰有重合,又γ-CD形成的空腔直径较大,RG分子可以自由进出其空腔中,说明RG整个分子套入环糊精空腔中并在一定条件下可释放。
图 5C是RG-HP-β-CD包合物的NOESY图。图中HP-β-CD在化学位移3.0~5.0 ppm处的质子峰与RG酰胺基团上的甲基氢,尿基上的氨基氢和芳香环上的芳环氢的质子峰均有重合,说明几乎RG整个分子都套入环糊精的空腔中,与γ-CD情况类似,瑞戈非尼分子可自由进出环糊精空腔,说明RG整个分子套入环糊精空腔中并在一定条件下可释放。
RG-β-CD包合物、RG-γ-CD包合物和RG-HP-β-CD包合物的包合率分别为86.0%、83.7%和85.2%。可以看出三种包合物的包合率均较高,其中RG-β-CD包合物的包合率最高,包合效果最好。
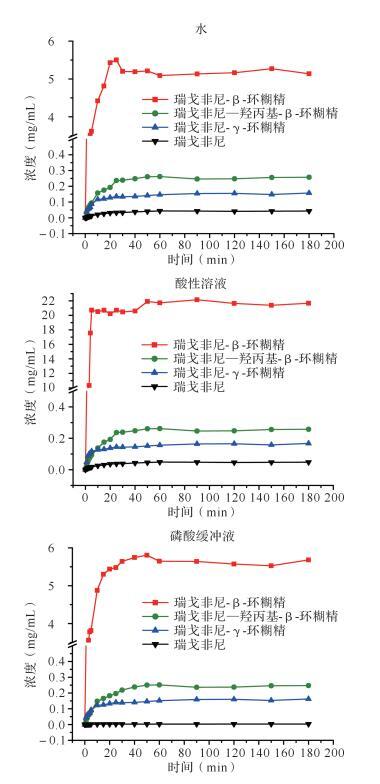
RG-β-CD在三种溶出介质中的最大溶出浓度分别约为5.5 mg/mL、22.6 mg/mL和5.9 mg/mL;而RG-Hp-β-CD的溶出度其次,其最大溶出浓度分别约为0.15 mg/mL、0.24 mg/mL和0.16 mg/mL;RG-γ-CD的溶出度提高最少,其最大溶出浓度分别约为0.25 mg/mL、0.34 mg/mL和0.15 mg/mL。在水中的最大溶出浓度三种包合物与RG比较,分别提高到3倍、5倍、100倍。虽然RG被γ-CD包合时溶出度提高最少,但与RG药物比较,溶解度仍增加不少。RG及其包合物分别在水、酸性溶液(酸碱度值1.2) 和磷酸缓冲溶液(酸碱度值6.8) 中的体外溶出速率见 图 7。由此可知,RG被环糊精包合后能显著增加溶出度,并且RG-β-CD在三种溶出介质中的溶出度是最好的。
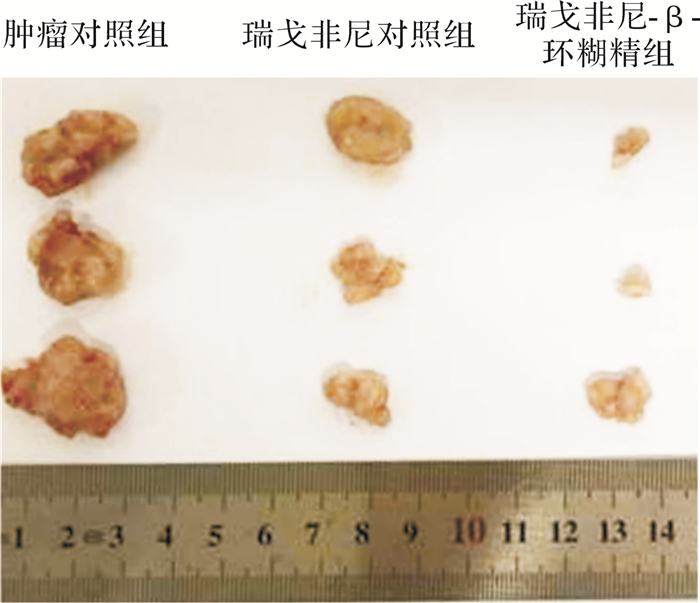
肿瘤生长抑制曲线显示,在口服给药后,肿瘤对照组和RG对照组肿瘤体积都随着时间的增加而逐渐增大。而RG-β-CD组肿瘤生长明显抑制。肿瘤抑制试验结果显示,三组裸鼠分别口服给药21 d后,肿瘤对照组的肿瘤体积最大,RG对照组次之,RG-β-CD组肿瘤最小,实验结果分别见 图 8和 图 9。抑瘤实验结果说明RG-β-CD组比纯药RG组的抑瘤效果好。

同时在肿瘤抑制试验中,三组裸鼠体质量均维持在22 g左右,没有明显变化,见 图 10,说明药物对裸鼠的毒副作用均小。

目前,国外对药物—环糊精超分子体,特别是药物-β-CD衍生物的应用进行了大量研究。已有多种CD包合技术药物产品上市,如前列地尔、斯皮仁诺、卓乐定胶囊等。国内也在积极开发利用这一类型辅料及其衍生物。我国由于受产酶细菌及分离技术等的限制,国内工业生产和应用的仅为β-CD一种,主要集中在中药挥发性成分CD包合物的制备。中药挥发油经与CD包合成包合物后,稳定性大大增加,对保留挥发油及其挥发性成分有突出作用,对提高中成药产品质量和临床疗效、提高产品科技含量有重要意义。
本研究采用β-CD、γ-CD、羟丙基-β-CD对瑞戈非尼进行包合,制备出三种CD包合物,且包合比例均为1:1。X射线衍射分析、热重分析、红外光谱、核磁共振等分析结果表明,已成功制备得到RG的三种包合物。
从RG与CD的结合情况分析,RG分子套入CD空腔,但CD空腔的大小对包合物的形成及其稳定性有重要影响。随着CD空腔大小的增大,RG套入环糊精的结构增大,形成了CD和药物的不同构型,这是由CD空腔大小和药物的分子构型决定的。其中,β-CD包合了RG的一部分,γ-CD和羟丙基-β-CD包合了整个RG分子,并能较好地游离出。β-CD的腔大小与RG分子匹配较好,因此制备RG-β-CD时需要的作用时间较长,但制备得到的包合物更稳定。γ-CD腔体较大,RG分子在其中可自由进出,因此虽然制备较容易,但制备得到的RG-γ-CD包合物不稳定。因此,CD空腔大小对包合物的形成至关重要,这对如何选择环糊精包合药物具有到重要的借鉴作用。
固有溶出速率是指在恒定温度下,药物与溶出介质在恒定的接触面积下的溶出速率 [ 16] 。通常所说的溶解度则是另一个概念,是指在给定的温度下溶出过程的平衡状态,在此状态下,药物未溶解的固相部分与在饱和溶液中的已溶解的部分达到平衡。与平衡溶解度相比,固有溶出速率更接近固体口服制剂在体内溶出的情况。测定固有溶出速率有助于选取具有合适药物释放行为的固体形态。在包合物溶解度、溶出度研究中,RG被CD包合后能显著提高其溶解度和溶出度,其中RG-β-CD包合物在三种溶出介质中的溶解度和溶出度是最好的,这也与包合物的结构分析结果一致。鉴于RG-β-CD包合物良好的药物释放行为,接下来我们考察了RG-β-CD包合物对荷瘤裸鼠肿瘤生长的抑制能力。
RG-β-CD裸鼠体内抑瘤实验表明,RG-β-CD组抑瘤效果明显好于RG对照组和肿瘤对照组。首先包合物在通过口服进入体内后,可以较好地避免肝脏的首过效应;其次由于体内含有较丰富的酶,可对环糊精进行降解。包合物中的CD被酶降解后,药物RG释放,进入血液中的药物增多,血药浓度增大。因此,RG-β-CD的生物利用度明显高于RG,抑瘤效果增强。
综上所述,通过对瑞戈非尼和CD包合物的筛选,我们制得了三种RG与CD包合物,相比于RG,三种包合物的溶解度和溶出度明显增加,其中RG-β-CD包合物增加最显著,这为RG的进一步应用提供了重要参考。同时药物与CD形成包合物的方法也为改善难溶性药物的溶解度和生物利用度提供了一种非常有效的方法。
Funding Statement
国家自然科学基金(21374098)
References
- 1.WILHELM S M, DUMAS J, ADNANE L, et al. Regorafenib (BAY 73-4506): a new oral multikinase inhibitor of angiogenic, stromal and oncogenic receptor tyrosine kinases with potent preclinical antitumor activity. Int J Cancer. 2011;129(1):245–255. doi: 10.1002/ijc.v129.1. [WILHELM S M, DUMAS J, ADNANE L, et al. Regorafenib (BAY 73-4506): a new oral multikinase inhibitor of angiogenic, stromal and oncogenic receptor tyrosine kinases with potent preclinical antitumor activity [J]. Int J Cancer, 2011, 129(1):245-255.] [DOI] [PubMed] [Google Scholar]
- 2.GROTHEY A, VAN CUTSEM E, SOBRERO A, et al. Regorafenib monotherapy for previously treated metastatic colorectal cancer (CORRECT): an international, multicentre, randomised, placebo-controlled, phase 3 trial. Lancet. 2013;381(9863):303–312. doi: 10.1016/S0140-6736(12)61900-X. [GROTHEY A, VAN CUTSEM E, SOBRERO A, et al. Regorafenib monotherapy for previously treated metastatic colorectal cancer (CORRECT): an international, multicentre, randomised, placebo-controlled, phase 3 trial [J]. Lancet, 2013, 381(9863):303-312.] [DOI] [PubMed] [Google Scholar]
- 3.李 进. 新型口服多激酶抑制剂瑞戈非尼治疗癌症的研究进展. http://www.cnki.com.cn/Article/CJFDTOTAL-LCZL201405001.htm. 临床肿瘤学杂志. 2014;19(5):385–390. [李进.新型口服多激酶抑制剂瑞戈非尼治疗癌症的研究进展[J].临床肿瘤学杂志, 2014, 19(5):385-390.] [Google Scholar]
- 4.STRUMBERG D, SCHEULEN M, SCHULTHEIS B, et al. Regorafenib (BAY 73-4506) in advanced colorectal cancer: a phase Ⅰ study. Br J Cancer. 2012;106(11):1722–1727. doi: 10.1038/bjc.2012.153. [STRUMBERG D, SCHEULEN M, SCHULTHEIS B, et al. Regorafenib (BAY 73-4506) in advanced colorectal cancer: a phase Ⅰ study [J]. Br J Cancer, 2012, 106(11):1722-1727.] [DOI] [PMC free article] [PubMed] [Google Scholar]
- 5.DIRK S, BEATE S. Regorafenib for cancer. Expert Opin Inv Drugs. 2012;21(6):879–889. doi: 10.1517/13543784.2012.684752. [DIRK S, BEATE S. Regorafenib for cancer [J]. Expert Opin Inv Drugs, 2012, 21(6):879-889.] [DOI] [PubMed] [Google Scholar]
- 6.KLAUS M, ANNETTE F, SIMONE S, et al. A phase Ⅰ dose-escalation study of regorafenib (bay 73 -4506), an inhibitor of oncogenic, angiogenic, and stromal kinases, in patients with advanced solid tumors. Clin Cancer Res. 2012;18(9):2658–2667. doi: 10.1158/1078-0432.CCR-11-1900. [KLAUS M, ANNETTE F, SIMONE S, et al. A phase Ⅰ dose-escalation study of regorafenib (bay 73 -4506), an inhibitor of oncogenic, angiogenic, and stromal kinases, in patients with advanced solid tumors [J]. Clin Cancer Res, 2012, 18(9):2658-2667.] [DOI] [PubMed] [Google Scholar]
- 7.刘 正平, 刘 军田, 王 明森, et al. 瑞戈非尼固体分散体的制备及体外溶出度考察. http://www.cnki.com.cn/Article/CJFDTOTAL-SDYG201509011.htm. 药学研究. 2015;34(9):524–526. [刘正平, 刘军田, 王明森, 等.瑞戈非尼固体分散体的制备及体外溶出度考察[J].药学研究, 2015, 34(9):524-526.] [Google Scholar]
- 8.JOENSUU H. Adjuvant treatment of GIST: patient selection and treatment strategies. Nat Rev Oncol. 2012;9(6):351–358. doi: 10.1038/nrclinonc.2012.74. [JOENSUU H. Adjuvant treatment of GIST: patient selection and treatment strategies [J]. Nat Rev Oncol, 2012, 9(6):351-358.] [DOI] [PubMed] [Google Scholar]
- 9.DAS B, BARUAH J B. Assemblies of cytosine within H-bonded net-work of adipic acid and citric acid. J Mot Struct. 2011;1001(1-3):134–138. doi: 10.1016/j.molstruc.2011.06.029. [DAS B, BARUAH J B. Assemblies of cytosine within H-bonded net-work of adipic acid and citric acid [J]. J Mot Struct, 2011, 1001(1-3):134-138.] [DOI] [Google Scholar]
- 10.VANDELLI M, SALVIOLI G, MUCCI A, et al. 2-hydroxypropyl-β-cyclodextrin complexation with ursodeoxycholic acid. Int J Pharm. 1995;118(1):77–83. doi: 10.1016/0378-5173(94)00342-3. [VANDELLI M, SALVIOLI G, MUCCI A, et al. 2-hydroxypropyl-β-cyclodextrin complexation with ursodeoxycholic acid [J]. Int J Pharm, 1995, 118(1):77-83.] [DOI] [Google Scholar]
- 11.TAKAYAMA K, NAMBU N, NAGAI T. Dissolution kinetics for coprecipitates of indomethacin with polyvinylpyrrolidone. Chem Pharm Bull. 1980;28(11):3304–3309. doi: 10.1248/cpb.28.3304. [TAKAYAMA K, NAMBU N, NAGAI T. Dissolution kinetics for coprecipitates of indomethacin with polyvinylpyrrolidone [J]. Chem Pharm Bull, 1980, 28(11):3304-3309.] [DOI] [Google Scholar]
- 12.ARCHONTAKI H A, VERTZONI M V, ATHANASSIOU-MALAKI M H. Study on the inclusion complexes of bromazepam with β-and β-hydroxypropyl-cyclodextrins. J Pharm Biomed Anal. 2002;28(3-4):761–769. doi: 10.1016/S0731-7085(01)00679-3. [ARCHONTAKI H A, VERTZONI M V, ATHANASSIOU-MALAKI M H. Study on the inclusion complexes of bromazepam with β-and β-hydroxypropyl-cyclodextrins [J]. J Pharm Biomed Anal, 2002, 28(3-4):761-769.] [DOI] [PubMed] [Google Scholar]
- 13.RIEKES M K, TAGLIARI M P, GRANADA A, et al. Enhanced solubility and dissolution rate of amiodarone by complexation with β-cyclodextrin through different methods. Mater Sci Eng C. 2010;30(7):1008–1013. doi: 10.1016/j.msec.2010.05.001. [RIEKES M K, TAGLIARI M P, GRANADA A, et al. Enhanced solubility and dissolution rate of amiodarone by complexation with β-cyclodextrin through different methods [J]. Mater Sci Eng C, 2010, 30(7):1008-1013.] [DOI] [Google Scholar]
- 14.GE X, HUANG G, TIAN S, et al. Complexation of carbendazim with hydroxypropyl-β-cyclodextrin to improve solubility and fungicidal activity. Carbohyd Polym. 2012;89(1):208–212. doi: 10.1016/j.carbpol.2012.02.072. [GE X, HUANG G, TIAN S, et al. Complexation of carbendazim with hydroxypropyl-β-cyclodextrin to improve solubility and fungicidal activity [J]. Carbohyd Polym, 2012, 89(1):208-212.] [DOI] [PubMed] [Google Scholar]
- 15.GIDWAM B, VYAS A. Synthesis, characterization and application of epichlorohydrin-β-cyclodextrin polymer. Coll SurfaceB Biointerfaces. 2014;114:130–137. doi: 10.1016/j.colsurfb.2013.09.035. [GIDWAM B, VYAS A. Synthesis, characterization and application of epichlorohydrin-β-cyclodextrin polymer [J]. Coll SurfaceB Biointerfaces, 2014, 114:130-137.] [DOI] [PubMed] [Google Scholar]
- 16.高 缘, 祖 卉, 张 建军. 药物共晶研究进展. http://www.cnki.com.cn/Article/CJFDTOTAL-HXJZ201005007.htm. 化学进展. 2010;22(5):829–836. [高缘, 祖卉, 张建军.药物共晶研究进展[J].化学进展, 2010, 22(5):829-836.] [Google Scholar]


