Resumen
Introducción:
la cobertura de detección de cáncer de mama en México es limitada. Es necesario configurar al sistema de salud mexicano para hacerlo capaz de producir más mastografías, sin dejar de lado la calidad y la oportunidad diagnóstica.
Objetivo:
proyectar la capacidad de cobertura de los programas de detección oportuna de cáncer de mama en México en función de los mastógrafos disponibles en las instituciones públicas del país.
Material y métodos:
se hizo un estudio exploratorio correlacionando la cantidad de mastógrafos del sector público con las mujeres entre 40 y 69 años quienes son el objetivo de los programas de tamizaje en México. El análisis consistió en calcular la población blanco-cubierta, a nivel nacional y por estado, asumiendo que cada mastógrafo pudiera ejecutar 6336 estudios de tamizaje al año. Todos los cálculos se realizaron con la información del año 2020 por ser los datos más actuales en materia de densidad poblacional.
Resultados:
se determinó que se cuenta con el número de mastógrafos suficiente como para elevar la oferta de estudios de tamizaje al 50% a nivel nacional. Incluso hay estados cuya capacidad de cobertura se proyecta por arriba del 70%. Algunos de ellos son Ciudad de México, Colima, Durango, Quintana Roo, Zacatecas, Baja California Sur y Coahuila. También se observó que la distribución de estos equipos no es equitativa, habiendo estados con grandes necesidades de inversión en equipo y, por ende, en estrategias de tamización para cáncer de mama.
Conclusiones:
nuestros datos demuestran que es posible incrementar la cobertura de los programas de detección oportuna de cáncer de mama en México, aunque es necesario mejorar las capacidades gerenciales de nuestros programas para que estos impacten en la cobertura, pero también en la calidad.
Palabras clave: Neoplasias de la Mama, Mamografía, México
Abstract
Background:
Breast cancer screening coverage in Mexico is limited. It is necessary to configure the Mexican health system to make it capable of producing more mammograms, without neglecting quality and diagnostic opportunity.
Objective:
To project the coverage of breast cancer screening programs according to the mammographs availability in the Mexican Health System.
Material and methods:
An exploratory study was conducted correlating the number mammographs available in the Mexican Health System with women between 40 and 69 who are the target of screening programs in Mexico. The analysis consisted of calculating the coverage of breast cancer screening programs if each mammograph could perform 6336 screening mammograms per year. All the calculations were made with the information of the year 2020 as the most current data in terms of population density.
Results:
It was determined that the number of mammographs is enough to raise the offer of screening studies to ≈50% at the national level. There are even states whose coverage capacity is projected above 70%. Some of them are Mexico City, Colima, Durango, Quintana Roo, Zacatecas, Baja California Sur and Coahuila. Also, it was observed that the distribution of mammographs is not equitable in the national territory, suggesting investment both in equipment and in screening strategies for breast cancer.
Conclusions:
Our data show that it is possible to advance in preventing breast cancer in Mexico, although the improvement of the management capacities of the Mexican Health System is required to improve both the coverage and quality of the breast cancer screening programs.
Keywords: Breast Neoplasms, Mammography, Mexico
Introducción
La cobertura de detección de cáncer de mama en México es limitada. Lo anterior se debe, principalmente, a las barreras en el acceso a los servicios, las cuales se asocian a la falta de equipo médico y de personal capacitado, así como a la insuficiencia de programas permanentes de tamizaje con mastografía.1,2 También se reconoce que hay barreras por el lado de la demanda, como la baja percepción del riesgo y las actitudes negativas hacía el diagnóstico y el pronóstico del cáncer.3
En múltiples foros se ha recomendado que, para incrementar la cobertura, es necesario configurar al sistema de salud mexicano, volviéndolo capaz de producir más mastografías, sin dejar de lado la calidad y la oportunidad diagnóstica.4,5,6 A este respecto, la Organización Mundial de la Salud (OMS) se ha manifestado a favor de reducir la mortalidad mundial por cáncer de mama; incentivando, sobre todo a los países con economías limitadas, a que reconozcan la carga de esta enfermedad y a que dispongan de todos sus recursos para mitigar su impacto negativo.7,8
No hay duda de que el cáncer de mama en México representa una pesada carga de muertes prematuras en mujeres. También es la principal causa de años de vida ajustados por discapacidad (AVISAs) perdidos por cáncer.9,10 Sobre el aprovechamiento de los recursos, poco se ha estudiado qué tan eficientes son las instituciones públicas de nuestro país para producir mastografías, aunque de manera indirecta se ha asumido la ineficiencia en la provisión de estos servicios por múltiples causas, incluyendo la subutilización de los equipos.11,12
El presente estudio busca proyectar la “plausible” capacidad de cobertura de los programas de detección oportuna de cáncer de mama en México en función de los mastógrafos disponibles en las instituciones públicas del país. Nuestro objetivo es aportar cifras sobre la eficiencia técnica de acuerdo con la capacidad instalada, con el fin de influir en las políticas adoptadas para el control del cáncer de mama en México.
Material y Métodos
Disponibilidad de recursos y factibilidad para alcanzar la cobertura.
Se ofrece un estudio descriptivo, longitudinal, observacional y analítico, en el que se integró la información relacionada la disponibilidad de mastógrafos y su productividad, en las instituciones del sector público a nivel nacional, incluyendo a las siguientes:
A. Instituto Mexicano del Seguro Social (IMSS)
B. Secretaría de Salud (SSA)
C. Instituto de Seguridad y Servicios Sociales de los Trabajadores del Estado (ISSSTE)
D. Secretaría de Marina (SEMAR)
E. Petróleos Mexicanos (PEMEX)
F. Secretaría de la Defensa Nacional (SEDENA)
G. Mastógrafos municipales
Para proyectar la cobertura por estado, se aplicó la fórmula presentada en el trabajo de da Cunha y colaboradores13 con la que se expone la cantidad de estudios anuales que se pudieran hacer con un mastógrafo trabajando en el tamizaje, durante un turno:
Fórmula 1. Fórmual 1.

La cantidad de mastografías estimadas con base en los equipos disponibles se correlacionó con las mujeres del grupo programático con base en los datos de densidad poblacional del 2020, por ser los últimos disponibles por parte del Instituto Nacional de Estadística y Geografía (INEGI).14 Mientras tanto, la cantidad de mastógrafos fue obtenida de la Dirección General de Información en Salud (DGIS).15
Es importante aclarar que, para proyectar el porcentaje de cobertura, la población blanco o grupo programático (mujeres entre 40 y 69 años) de cada entidad federativa fue dividida a la mitad, ya que la recomendación en cuanto a la estrategia de tamización para cáncer de mama en México es que ésta se aplique de forma bienal.16
Evaluación de la estabilidad en el número de mastógrafos a lo largo de un periodo como control de calidad de los datos.
La estrategia para medir la estabilidad en el registro de los mastógrafos fue la de aplicar la fórmula de cálculo de incremento porcentual. Tal estrategia se desarrolló basándonos en la metodología de control de inventarios descrita en el documento “Introducción a la gestión de inventarios de equipo médico” de la OMS en donde se menciona que una lista determinada de equipo puede compararse con el inventario actual para detectar las deficiencias y/o excesos en el equipo médico, e identificar las fuentes de variación que tengan implicaciones en los resultados.17
La fórmula utilizada para nuestros cálculos fue la siguiente:
Fórmula 2. Fórmual 2.

Las variaciones, que son trazadas en gráficos de control, corresponden al periodo 2015-2021, y se describen a nivel nacional, por entidad federativa y por institución. Se reitera que los objetivos de esta acción fue encontrar, mostrar y discutir todas las posibles fuentes de variación en el registro de los mastógrafos disponibles en México. En ningún momento se planeó hacer un análisis sobre la agudeza de los inventarios de equipo médico.
Resultados
Como se aprecia en el cuadro I, en el 2020 se registraron 765 mastógrafos. La mayor cantidad la tuvieron en las entidades con la mayor densidad población como son Ciudad de México (108), Estado de México (51), Guanajuato (38), Jalisco (46) y Nuevo León (44). Por su parte, las entidades que contaron con menos unidades fueron Morelos (5), Nayarit (6), Aguascalientes (7), Colima (7), Tlaxcala (7) y Campeche (8).
Cuadro I. Mujeres entre 40 y 69 años del año 2020 y mastógrafos reportados en los diferentes estados en el periodo 2015-2021.
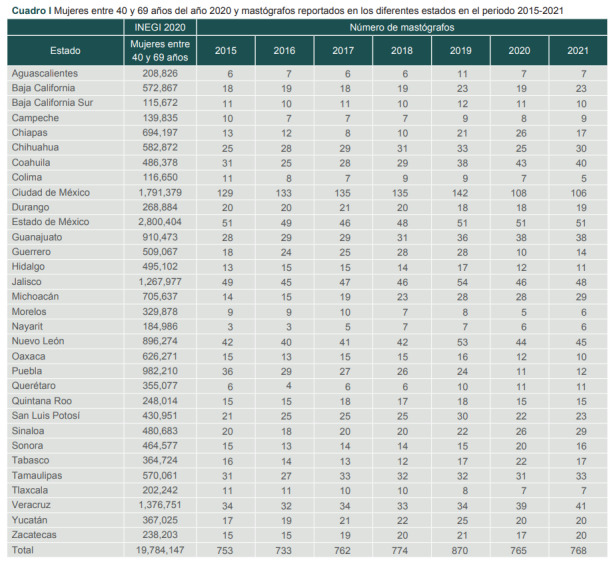
En este mismo cuadro, se aprecia que el número de mujeres entre 40 y 69 años fue de 19 784 147. Por lo anteriormente explicado respecto a las recomendaciones para la prevención y seguimiento del cáncer de mama,16 la población blanco usada en nuestros cálculos fueron 9 892 374 mujeres.
Con base en la productividad de 6336 estudios de tamizaje anuales por equipo disponible, se calculó el porcentaje de cobertura “asequible” a nivel nacional. El ejercicio consistió en multiplicar la productividad, por el número de mastógrafos disponibles para el 2020 (6336 mastografías por año x 765 mastógrafos). Así, se obtuvo un total de 4,847,040 estudios mastográficos. Esto quiere decir que la cobertura alcanzada pudo ser del 49% ([4,847,040/ 9,892,374] x 100).
El siguiente paso fue demostrar la posibilidad de eficientizar los programas de detección oportuna de cáncer de mama en cada entidad federativa. Como ejemplo se presenta el caso de Coahuila toda vez que es uno de los estados con las mayores expectativas de crecimiento en estos programas (figura 1). Las estadísticas arrojan una población blanco de 486,384. Esto quiere decir que la productividad real para alcanzar el 100% de cobertura debería ser de 243,192 (486,384/2) estudios anuales. Dicha productividad se representó en un gráfico de frecuencias en el que las candidatas al tamizaje fueron divididas entre 12 meses, dando un total de 20 266 mujeres por mes. Estas mujeres están representadas en la primera barra, mientras que las barras subsecuentes son el cúmulo de las frecuencias anteriores.
Figura 1. Gráfica de frecuencia acumulada en la que se representa el porcentaje de cobertura que pudiera alcanzarse en el estado de Coahuila, en función de los mastógrafos del sector público.
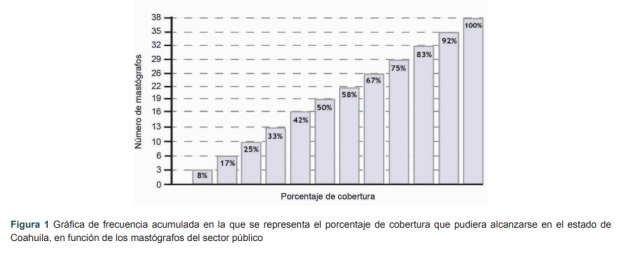
El presente ejercicio demuestra que si, en el 2020 en Coahuila, se hubieran tamizado a 20,266 mujeres, el porcentaje de cobertura alcanzado hubiera sido del 8% ([20,266/243,192] x 100). Para esto, son necesarios, como mínimo, 3 mastógrafos trabajando un turno, todo el año, en programas de detección oportuna de cáncer de mama (6336 mastografías x 3 mastógrafos = 19,008 mastografías). Así, se representa la capacidad de detección en orden creciente, en función de los mastógrafos disponibles. Como se puede observar, la cobertura de este estado potencialmente pudo ser del 100%, con los 43 mastógrafos que hubo disponibles en el sector público durante el 2020.
En el cuadro II, se exponen los resultados que arroja este mismo ejercicio para el resto de las entidades federativas. También se muestran los mastógrafos necesarios para alcanzar o rebasar el 70% de cobertura, lo cuales se pueden contrastar con la capacidad instalada en la actualidad.
Cuadro II. Porcentaje de cobertura por entidad federativa en función de la capacidad instalada y de la población programática.
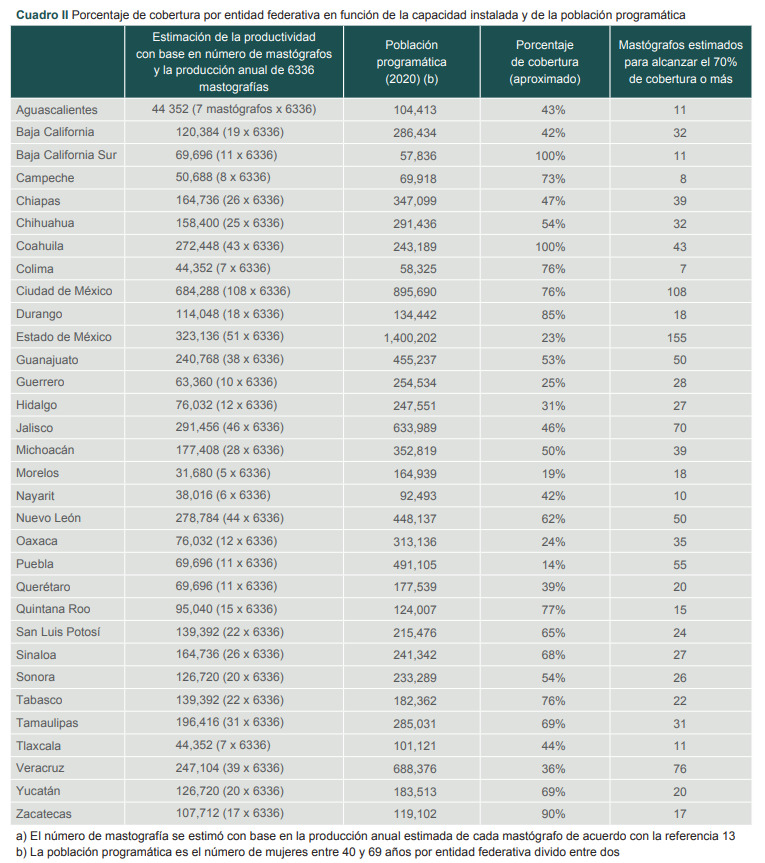
a) El número de mastografía se estimó con base en la producción anual estimada de cada mastógrafo de acuerdo con la referencia 13
b) La población programática es el número de mujeres entre 40 y 69 años por entidad federativa divido entre dos.
En cuanto a la estabilidad en los registros de mastógrafos, la figura 2A muestra variaciones importantes a nivel nacional entre el 2015 y el 2021. Estas se traducen en incrementos sostenidos en los años 2017 y 2018, progresando significativamente en el 2019. Las entidades federativas con crecimientos importantes en el registro de mastógrafos entre el 2018 y el 2019 fueron Chiapas (110%), Aguascalientes (83%), Querétaro (67%), Tabasco (42%) y Coahuila (31%). Por otro lado, hubo un presunto subregistro en el año de la pandemia (2020), donde los reportes negativos más importantes se presentaron en los estados de Guerrero (-64%), Puebla (-54%), Morelos (-37%) y Aguascalientes (-36%).
Figura 2. Cambios en el número de mastógrafos reportados, en el sector público, en el periodo 2015-2021. En el inciso A se muestran los cambios porcentuales que fueron calculadas a nivel nacional, mientras que en el inciso B se representan por estado. Morelos, Puebla y Guerrero mostraron las tendencias negativas más importantes en cuanto al subregistro y/o déficit de mastógrafos.
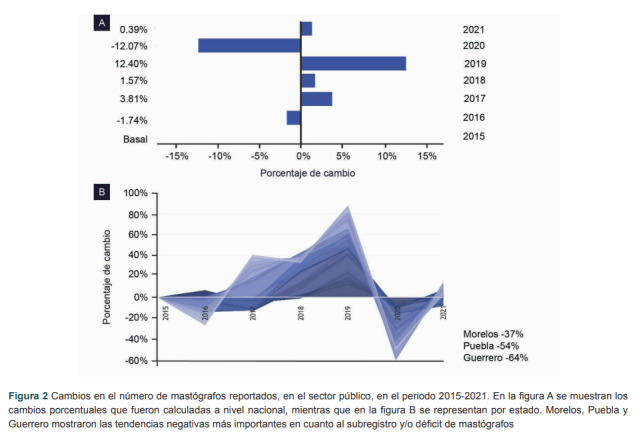
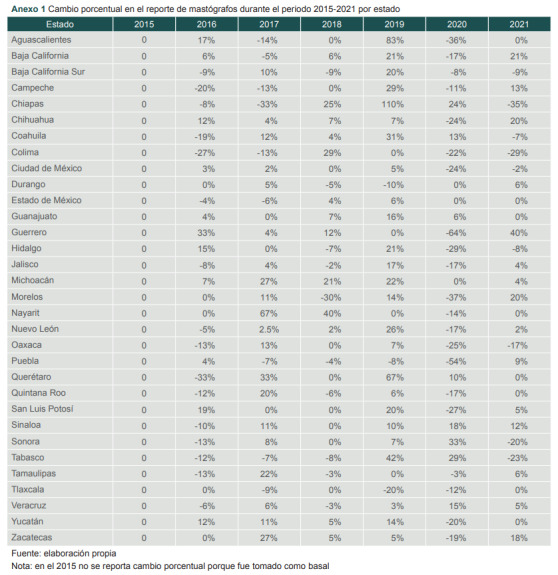
En la figura 2B se puede apreciar el hipotético “subregistro” por entidad federativa, el cual se hace patente ya que esta alternancia es la más marcada del periodo estudiado. Para corroborar esta información, se sugiere que se revise el anexo 1.
Anexo 1. Cambio porcentual en el reporte de mastógrafos durante el periodo 2015-2021 por estado.
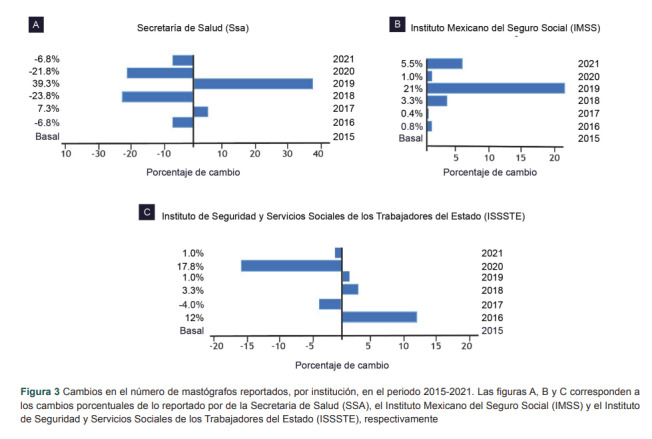
Finalmente, en la figura 3 se presentan los cambios en el registro de mastógrafos en las principales instituciones públicas de salud en México. De acuerdo con nuestros resultados, la institución más aventajada en el 2019 fue la SSA, con un incremento del 39.9%. Sin embargo, en el 2020, ésta demostró una importante caída en sus registros (figura 3A). Por el contrario, en el IMSS, hubo una ganancia importante en el número de mastógrafos en el 2019, la cual se mantuvo en el 2020 (figura 3B). Finalmente, en el ISSSTE, se observa un fenómeno similar a lo ocurrido en la SSA. Es decir, también hubo una “aparente” deficiencia en la documentación de mastógrafos en el año de la pandemia (figura 3C).
Figura 3. Cambios en el número de mastógrafos reportados, por institución, en el periodo 2015-2021. Los incisos A, B y C corresponden a los cambios porcentuales de lo reportado por de la Secretaria de Salud (SSA), el Instituto Mexicano del Seguro Social (IMSS) y el Instituto de Seguridad y Servicios Sociales de los Trabajadores del Estado (ISSSTE), respectivamente.
En el anexo 2 se puede observar la cantidad de mastógrafos reportados año con año (entre el 2015 y el 2021) en las instituciones reportadas en la figura 4, pero también en otras instituciones del sector público como la SEDENA, la SEMAR, PEMEX, entre otras.
Anexo 2. Reporte de mastógrafos por institución en el periodo 2015-2021 y los cambios porcentuales en el periodo.
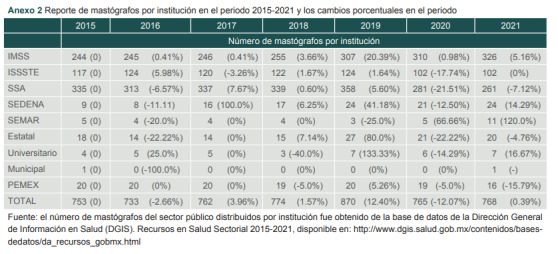
Fuente: el número de mastógrafos del sector público distribuidos por institución fue obtenido de la base de datos de la Dirección General de Información en Salud (DGIS). Recursos en Salud Sectorial 2015-2021, disponible en: http://www.dgis.salud.gob.mx/contenidos/basesdedatos/da_recursos_gobmx.htm
Discusión
En el presente trabajo se muestra que México cuenta con la cantidad suficiente de mastógrafos como para elevar la oferta de mastografías en ≈50% a nivel nacional, lo que sugiere que detrás del ≈20% de cobertura asiduamente reportado,1,2 está la subutilización de los equipos menoscabando los programas de detección de cáncer de mama. De acuerdo con nuestros resultados, los estados que pudieran tener las mejores capacidades de producción de mastografía son Coahuila, Baja California Sur, Zacatecas, Quintana Roo, Durango, Colima y Ciudad de México. Por otro lado, están los estados pocos equipos en función de su demanda. Algunos de estos son Puebla, Morelos, Estado de México, Oaxaca y Guerrero.
No hay duda de que los programas de tamizaje con mastografías son la única manera de disminuir la mortalidad por cáncer de mama, siempre y cuando se ejecuten de forma organizada y con calidad. Lo ideal es que éstos cubran al 70% de una población blanco para disminuir el ritmo de mortalidad en 35%.18,19
Desafortunadamente, México no se encuentra en la lista de países con programas de tamizaje con mastografía organizados y de calidad. La situación es que “aparentemente” los limitados ingresos de nuestro sistema de salud no podrían sostener un modelo de detección de cáncer de mama que es costoso por depender de equipo médico de alta tecnología y de personal altamente capacitado. Mucho menos se puede pensar en inversiones para garantizar la sostenibilidad de los equipos y, por ende, la de los programas de tamizaje.20,21 Lo anterior no nulifica la lucha contra el cáncer de mama en nuestro país. Ésta existe, pero responde a programas de estructura oportunista, lo que le confiere debilidades en su sistema de gestión, control de calidad y seguimiento de las pacientes.22
Si bien para los estados como las capacidades de cobertura más bajas se requiere de una inversión económica para la adquisición de mastógrafos como lo demuestran nuestros resultados, es conveniente que, de darse, ésta sea estratificada. Es decir, los recursos materiales y humanos deben incorporarse poco a poco, pero sin interrupción, de tal manera que continuamente se evalúe la competitividad de los programas como una medida de protección de las finanzas del sistema de salud.23
Es importante enfatizar en que la estratificación de los recursos y el pilotaje de los modelos de programas de detección oportuna de cáncer de mama no solo se sugieren para los estados con baja capacidad de oferta. Sino también para aquellos que tienen aforos altos, pero deficiencias en la percepción global de la lucha contra el cáncer de mama. La razón es simple: cuáles son los beneficios de invertir en infraestructura y/o de aumentar la oferta de mastografías si no hay mecanismos de control para esta neoplasia, como la realización de biopsias. Es para todos claro que la lucha contra el cáncer de mama no termina con la detección, sino que implica acciones para hacer diagnósticos tempranos y garantizar el tratamiento.2,12
Nuestro ejemplo más cercano de un programa que se preocupa de manera integral por las mujeres con cáncer de mama es el modelo de un día que se aplica en Instituto Nacional de Cancerología (INCan) desde hace más de 5 años. El desarrollo de este modelo de programa gira en términos del acceso a servicios adicionales a la mastografía (como ultrasonido y proyecciones adicionales) que garantizan el diagnóstico por imagen en un día. Al mismo tiempo, nuestro modelo acelera la biopsia de los casos que lo ameritan, así como el análisis patológico. Estas acciones optimizan el tiempo y crean flujos de trabajo más ágiles tanto en el INCan como en el resto de las Instituciones en donde las mujeres son tratadas.7 Con el modelo de un día se han abatido estrategias obsoletas y sistema que injustificadamente dejan a las mujeres sin diagnóstico y tratamiento oportuno.24
Retomando las causas de la subutilización de los mastógrafos en México, una de ellas podría ser su modesta migración a tecnología digital. Por ejemplo, en el 2015, el Centro Nacional de Excelencia Tecnológica en Salud (CENETEC) reportó que, de un total de 882 mastógrafos del sector público del país, el 60% eran analógicos. Si bien esta tecnología es suficiente para el tamizaje de cáncer de mama, su reemplazo por técnicas digitales es irrebatible. Lo anterior se debe, en parte, a la obsolescencia de algunos materiales que ocupan los mastógrafos analógicos, como las placas para revelado. Los digitales, por su parte, cuentan con herramientas para mejorar la calidad de la imagen, lo que los hace más sensibles y precisos, con el consecuente impacto positivo en la productividad.25
Ahora bien, hay otros factores que no están relacionados directamente con la subutilización de los mastógrafos, pero que limitan su operación efectiva. Tal es el caso de las deficiencias en la calidad de la imagen y la falta de médicos y técnicos radiólogos capacitados.26 Para abatir las deficiencias en los temas que competen a la calidad de la imagen, en Canadá, Estados Unidos, algunos países de Europa y América Latina, se han instituido programas sólidos de certificación.27,28,29 Basándonos en el programa descrito por Fleitas y colaboradores,29 en México también se han ejecutado acciones para mejorar la calidad de los estudios de detección, entre las que destaca el programa voluntario de verificación llamado “Reconocimiento INCan”.30
Además, en materia de capacitación, el INCan cuenta con dos cursos dirigidos a técnicos y a médicos radiólogos, los cuales proveen capacitación continua en la toma y en la interpretación de las mastografías de tamizaje. Ambos cursos surgieron en el 2014 bajo la premisa de que de nada sirve tener equipos de la más amplia gama tecnológica sino se cuenta con el personal capacitado para operarlos de manera correcta. Con las estadísticas obtenidas de nuestros cursos, y de otros que hay disponibles a nivel nacional, será un objetivo de trabajos futuros asociar a la población blanco con la capacidad instalada, pero también con el personal que cuenta con los estándares más altos en cuanto a capacitación para realizar la labor de tamización para cáncer de mama.
El presente estudio tiene varias limitaciones como el hecho de que en los cálculos no se contemplan variables como problemas culturales, estado de calidad de los equipos, obtención de imágenes según controles estandarizados, etc. Somos conscientes de que la relación entre número de mastógrafos y cobertura no puede ser lineal. Sin embargo, por el momento no es posible añadir más variables a la ecuación ya que, hasta nuestro conocimiento, no existe tal información en México. En este sentido, más que una limitante, se presenta un área de oportunidad que pudiera conducir a un registro nacional con datos que permitan hacer análisis más sofisticados.
Otro aspecto restrictivo para nuestro análisis fue el presunto subregistro de mastógrafos en el año 2020. Sobre este punto se observó que la pérdida global fue de ≈12%. Aunque esta cifra puede parecer modesta, hubo estados que contribuyeron sustancialmente con este fenómeno, con desplomes de más del 50%. Es importante mencionar que las instituciones en la que se observó con mayor agudeza el subregistro de mastógrafos fueron la SSA y el ISSSTE, mientras que las cifras del IMSS se mantuvieron constantes, lo que es un indicio de congruencia, pero no de subregistro. Una de las causas de las divergencias antes mencionadas es que los mastógrafos se perdieron por obsolescencia. No obstante, se considera que el trasfondo fue el cierre de servicios no esenciales, la reconversión hospitalaria y la falta de personal; todo en relación con el COVID-19. Insistimos con las autoridades dedicadas a recopilar la información relacionada con el equipo médico, que avalen su incorporación oportuna con el fin de apoyar los planes de desarrollo nacional y subnacional en materia de programas de detección oportuna de cáncer de mama.
El resultado más importante de nuestro trabajo es que se demuestra que en varios estados cuentan con la capacidad necesaria para aumentar las metas de cobertura con cifras tan altas como el 70%. También se evidencian los mastógrafos que podrían garantizar el crecimiento de los programas de prevención de cáncer de mama en los estados más comprometidos en materia de tamizaje. Aunque hace falta invertir en mastógrafos, también es necesario revisar procesos para garantizar el uso eficaz y eficiente del equipo médico disponible. Algunos de estos son la capacitación continua de médicos y técnicos radiólogos. Finalmente, hay que tener en cuenta que, si las limitaciones en la confirmación diagnóstica y el acceso a tratamiento continúan sin modificación, nunca se logrará el objetivo final de la tamización para cáncer de mama que es la reducción de muertes por esta neoplasia por más mastógrafos que se adquieran.
Conclusiones
La maniobra presentada en este trabajo permitió estimar “parcialmente” el desempeño que los mastógrafos del sector público mexicano pudieran tener en las actividades de detección oportuna de cáncer de mama. Se evidencia que invertir tanto en equipo médico como en su mantenimiento, es un área de oportunidad para revertir la inequidad en cuanto a las metas de cobertura a nivel nacional. Lo anterior sumado a mecanismos que garanticen que los mastógrafos trabajen a su máxima capacidad para eludir pérdidas productivas. Es necesario cambiar la idea de que el tamizaje con mastografía no puede ser sostenible y organizado. Se puede alcanzar al mejorar nuestro estilo de desarrollo de programas de detección oportuna de cáncer de mama con la inclusión de los mastógrafos en medios provistos de calidad.
Notas
los autores han completado y enviado la forma traducida al español de la declaración de conflictos potenciales de interés del Comité Internacional de Editores de Revistas Médicas, y no fue reportado alguno que tuviera relación con este artículo.
No se contó con ningún tipo de financiamiento para la realización de este trabajo.
Referencias
- 1.Nigenda G, Caballero M, González-Robledo L. Barreras de acceso al diagnóstico temprano del cáncer de mama en el Distrito Federal y en Oaxaca. Salud Publica Mex. 2009;51(Suppl 2):254–262. [PubMed] [Google Scholar]
- 2.Uscanga-Sánchez S, Torres-Mejía G, Ángeles-Llerenas A, et al. Indicadores del proceso de tamizaje de cáncer de mama en México: un estudio de caso. Salud Publica Mex. 2014;56(5):528–537. [PubMed] [Google Scholar]
- 3.Espinosa-de Los Monteros K, Gallo LC. The relevance of fatalism in the study of Latinas' cancer screening behavior: a systematic review of the literature. Int J Behav Med. 2011;18(4):310–318. doi: 10.1007/s12529-010-9119-4. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 4.Secretaría de Salud. Sector Salud Trabaja en Estrategias para Detección Oportuna de Cáncer de Mama. Secretaría de Salud; México: 2022. [Google Scholar]
- 5.Chávarri-Guerra Y, Villarreal-Garza C, Liedke PE, et al. Breast cancer in Mexico: a growing challenge to health and the health system. Lancet Oncol. 2012;13(8):e335–e343. doi: 10.1016/S1470-2045(12)70246-2. [DOI] [PubMed] [Google Scholar]
- 6.Ginsburg O, Yip CH, Brooks A, et al. Breast cancer early detection: A phased approach to implementation. Cancer. 2020;126(Suppl 10):2379–2393. doi: 10.1002/cncr.32887. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 7.Organización Panamericana de la Salud. Cáncer de Mama. Organización Mundial de la Salud; 2022. [citado 2023 julio 12]. Disponible en: https://www.paho.org/es/temas/cancer-mama . [Google Scholar]
- 8.Barrios CH, Werutsky G, Mohar A, et al. Cancer control in Latin America and the Caribbean: recent advances and opportunities to move forward. Lancet Oncol. 2021;22(11):e474–e487. doi: 10.1016/S1470-2045(21)00504-1. [DOI] [PubMed] [Google Scholar]
- 9.Mohar-Betancourt A, Reynoso-Noverón N, Armas-Texta D, et al. Cancer Trends in Mexico: Essential Data for the Creation and Follow-Up of Public Policies. J Glob Oncol. 2017;3(6):740–748. doi: 10.1200/JGO.2016.007476. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 10.Knaul FM, Nigenda G, Lozano R, et al. Breast cancer in Mexico: a pressing priority. Reprod Health Matters. 2008;(32):113–123. doi: 10.1016/S0968-8080(08)32414-8. [DOI] [PubMed] [Google Scholar]
- 11.Mohar A, Bargalló E, Ramírez MT, et al. Recursos disponibles para el tratamiento del cáncer de mama en México. Salud Publica Mex. 2009;51(Suppl 2):s263–s269. [PubMed] [Google Scholar]
- 12.Orozco-Núñez E, Alcalde-Rabanal J, Navarro J, et al. Eficiencia de los procesos administrativos para la gestión del Fondo de Protección contra Gastos Catastróficos en México. Salud Publica Mex. 2016;58(5):543–552. doi: 10.21149/spm.v58i5.8244. [DOI] [PubMed] [Google Scholar]
- 13.da Cunha GN, Vianna CMM, Mosegui GBG, et al. Rastreamento do câncer de mama: modelo de melhoria do acesso pelo uso de mamógrafos. Rev Panam Salud Publica. 2019;43:e19. doi: 10.26633/RPSP.2019.19. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 14.Instituto Nacional de Estadística y Geografía. Población total por entidad federativa y grupo quinquenal de edad según sexo, serie de años censales de 1990 a 2020. Instituto Nacional de Estadística y Geografía; México: 2020. Disponible en: https://www.inegi.org.mx/app/tabulados/interactivos/?px=Poblacion_01&bd=Poblacion . [Google Scholar]
- 15.Dirección General de Información en Salud. Recursos de Salud. Datos Abiertos. Dirección General de Información en Salud; México: 2023. Disponible en: http://www.dgis.salud.gob.mx/contenidos/basesdedatos/da_recursos_gobmx.html . [Google Scholar]
- 16.Norma Oficial Mexicana NOM-041-SSA2-2011, Para la prevención, diagnóstico, tratamiento, control y vigilancia epidemiológica del cáncer de mama. Secretaría de Gobernación; México: 2011. Disponible en: https://dof.gob.mx/nota_detalle.php?codigo=5194157&fecha=09/06/2011#gsc.tab=0 . [Google Scholar]
- 17.Organización Mundial de la Salud. Introducción a la gestión de inventarios de equipo médico. Organización Mundial de la Salud; 2011. Disponible en: https://www.who.int/es/publications/i/item/9789241501392 . [Google Scholar]
- 18.Organización Mundial de la Salud. WHO Position Paper on Mammography Screening. Organización Mundial de la Salud; Ginebra: 2014. Disponible en: https://www.ncbi.nlm.nih.gov/books/NBK269546/ [Google Scholar]
- 19.Youlden DR, Cramb SM, Dunn NA, et al. The descriptive epidemiology of female breast cancer: an international comparison of screening, incidence, survival and mortality. Cancer Epidemiol. 2012;36(3):237–248. doi: 10.1016/j.canep.2012.02.007. [DOI] [PubMed] [Google Scholar]
- 20.Torres-Mejía G, Ortega-Olvera C, Ángeles-Llerenas A, et al. Patrones de utilización de programas de prevención y diagnóstico temprano de cáncer en la mujer. Salud Publica Mex. 2013;55(Suppl 2):S241–S248. [PubMed] [Google Scholar]
- 21.Martínez-Montañez OG, Uribe-Zúñiga P, Hernández-Avila M. Políticas públicas para la detección del cáncer de mama en México. Salud Publica Mex. 2009;51(Suppl 2):s350–s360. doi: 10.1590/s0036-36342009000800028. [DOI] [PubMed] [Google Scholar]
- 22.Rodríguez-Cuevas S, Guisa-Hohenstein F, Labastida-Almendaro S. First breast cancer mammography screening program in Mexico: initial results 2005-2006. Breast J. 2009;15(6):623–631. doi: 10.1111/j.1524-4741.2009.00811.x. [DOI] [PubMed] [Google Scholar]
- 23.Organización Panamericana de la Salud. Planificación: panificación de programas integrales contra el cáncer de mama: un llamado a la acción. The Breast Healt Global Initiative; Ginebra: 2015. Disponible en: https://www.paho.org/es/node/55272 . [Google Scholar]
- 24.Sollozo-Dupont I, Galván-Espinoza HA, Castillo-López JP, et al. Impacto de la pandemia de Covid-19 en el tamizaje de cáncer de mama y algunas estrategias para actuar pronto y seguro. Salud Publica Mex. 2022;64(3):333–339. doi: 10.21149/13412. [DOI] [PubMed] [Google Scholar]
- 25.Song SY, Park B, Hong S, et al. Comparison of Digital and Screen-Film Mammography for Breast-Cancer Screening: A Systematic Review and Meta-Analysis. J Breast Cancer. 2019;22(2):311–325. doi: 10.4048/jbc.2019.22.e24. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 26.Brandan ME, Ruiz-Trejo C, Verdejo-Silva M, et al. Evaluation of equipment performance, patient dose, imaging quality, and diagnostic coincidence in five Mexico City mammography services. Arch Med Res. 2004;35(1):24–30. doi: 10.1016/j.arcmed.2003.06.008. [DOI] [PubMed] [Google Scholar]
- 27.Blanco S, Andisco D, Jiménez P, et al. Calidad de la mamografía y tamizaje del cáncer de mama en Argentina. Rev Panam Salud Publica. 2019;43:e63. doi: 10.26633/RPSP.2019.63. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 28.Organización Panamericana de la Salud. Garantía de calidad de los servicios de mamografía: Normas básicas para América Latina y el Caribe. Organización Mundial de la Salud Oficina Regional para las Américas; Washington: 2016. p. 48 p. Disponible en: https://notablesdelaciencia.conicet.gov.ar/bitstream/handle/11336/108213/CONICE 8 T_Digital_Nro.75579e5c-69ab-493b-91f1 9 fb4bc7fbf5e6_A.pdf?sequence=2&isAllowed=y . [Google Scholar]
- 29.Fleitas I, Caspani CC, Borrás C, et al. La calidad de los servicios de radiología en cinco países latinoamericanos. Rev Panam Salud Publica. 2006;20(2-3):113–124. doi: 10.1590/s1020-49892006000800008. [DOI] [PubMed] [Google Scholar]
- 30.Villaseñor-Navarro Y. Un llamado a mejorar la calidad de los servicios de tamizaje con mastografía: hablando del programa Reconocimiento INCan. Salud Publica Mex. 2021;63(3):336. doi: 10.21149/12135. [DOI] [PubMed] [Google Scholar]


