Abstract
Introducción.
El fingolimod es un agonista del receptor de esfingosina-1-fosfato utilizado para el tratamiento de la esclerosis múltiple (EM). Nuestro objetivo era evaluar los resultados del fingolimod en la calidad de vida de los pacientes con EM recurrente-remitente tras dos años de tratamiento en este estudio de la vida real.
Pacientes y métodos.
Se trata de un estudio observacional prospectivo de dos años de duración realizado en Bulgaria en pacientes con EM recurrente-remitente tratados con fingolimod. Se evaluó la calidad de vida mediante la versión en búlgaro de la escala Multiple Sclerosis Quality of Life-54 (MSQoL-54). El criterio de valoración principal fue el cambio respecto al valor inicial en la puntuación en la MSQoL-54 tras dos años de tratamiento. Los criterios de valoración secundarios fueron el cambio respecto al valor inicial en la puntuación en la MSQoL-54 tras un año de tratamiento, además de la evaluación del nivel de depresión mediante la puntuación de la escala de puntuación de la depresión de Hamilton (HAM-D17).
Resultados.
En el estudio se incluyó a 87 pacientes elegibles con una edad media de 38,7 ± 8,45 años. La mediana de la puntuación en la Expanded Disability Status Scale (EDSS) fue de 3,5 puntos. Se halló una mejora estadísticamente significativa en 10 subescalas en el mes 12 y en siete subescalas en el mes 24. La puntuación combinada de salud mental aumentó de 64 ± 16,69 puntos a 67,5 ± 15,94 puntos en el mes 24 (p = 0,012). La puntuación combinada de salud física aumentó de 61,7 ± 17,61 a 66,3 ± 16,7 (p = 0,001). El nivel de depresión medido por la HAM-D17 disminuyó considerablemente en el mes 12 y en el mes 24. La puntuación de la EDSS disminuyó o se mantuvo estable en más de la mitad de los pacientes (61,6%). Detectamos una mejor calidad de vida en los pacientes con una puntuación más baja en la EDSS.
Conclusiones.
Las puntuaciones de calidad de vida y el nivel de depresión mejoraron en los pacientes con EM recurrente-remitente tratados con fingolimod durante dos años en un entorno real.
Palabras clave: Calidad de vida, Depresión, Disfunción sexual, Esclerosis múltiple, Fingolimod, Trastornos del movimiento
Introducción
La esclerosis múltiple (EM) es una enfermedad desmielinizante de origen inmunitario crónica que puede ser potencialmente incapacitante del sistema nervioso central humano [1]. En Europa, la tasa media estimada de incidencia anual de la EM es de 4,3 casos por cada 100.000 [2]. Los datos del Fondo Búlgaro de Seguros de Enfermedad muestran que, en Bulgaria, se trata a unos 1.500 pacientes con EM, pero, según los datos de la Sociedad Búlgara de Trastornos del Movimiento y Esclerosis Múltiple, se calcula que el número de pacientes búlgaros con EM es de unos 3.600 [3].
Normalmente, durante el curso de la enfermedad de la EM recurrente-remitente pueden observarse episodios agudos recurrentes (recaídas) de síntomas neurológicos, seguidos de una recuperación completa o parcial. El 50% aproximadamente de estos pacientes evoluciona hacia la EM secundaria progresiva en un plazo de 10 años, y el 90%, en un plazo de 25 años. Aparte de estas formas inicialmente recurrentes de la EM, entre el 10 y el 15% de los pacientes presentan EM primaria progresiva, que se caracteriza por un deterioro constante del trastorno sin experiencia previa de recaídas [4].
Los estudios que evalúan los efectos terapéuticos de los tratamientos para la EM se suelen centrar casi siempre en ralentizar la progresión de la discapacidad física, reducir la tasa de recaídas y reducir la actividad de la enfermedad observada con resonancias magnéticas [5], basándose sobre todo en resultados cuantitativos. Hay muchos datos que demuestran que los tratamientos modificadores de la enfermedad para las formas recidivantes de EM reducen considerablemente la tasa anualizada de recaídas y el número de lesiones focales realzadas con gadolinio en la resonancia magnética y, además, tienen un impacto moderado en la progresión de la discapacidad. Sin embargo, las personas con EM suelen valorar aspectos más amplios, como la salud general, la salud mental y la depresión, como determinantes importantes de su calidad de vida general relacionada con la salud [6]. En las personas con EM, la calidad de vida general relacionada con la salud se deteriora considerablemente a medida que la enfermedad va progresando. La disfunción sexual es un síntoma común, pero a menudo ignorado, de la EM [7]. La prevalencia estimada de las preocupaciones de origen sexual en la población con EM oscila entre el 40 y el 80%, pero hay relativamente pocas investigaciones que hayan evaluado las consecuencias de la disfunción sexual en la calidad de vida en comparación con otros síntomas comunes de la EM [8].
El fingolimod, un agonista del receptor de la esfingosina-1-fosfato, es el primer tratamiento para la EM por vía oral de alta eficacia que ha demostrado efectos coherentes en las cuatro medidas clave de la actividad de la enfermedad frente al placebo y a un comparador activo [9,10].
En un análisis provisional de un programa suizo de seguimiento de la vigilancia (SWISSASCENT) que incluía datos de 100 pacientes con fingolimod, se observó una mejora significativa de la calidad de vida durante el tratamiento con fingolimod, así como de la satisfacción con el tratamiento, en todos los dominios del cuestionario de satisfacción con el tratamiento para medicamentos-9 tras el cambio de otros tratamientos modificadores de la enfermedad a fingolimod [11]. El estudio Evaluate Patient OutComes de fase IV (realizado en Estados Unidos y Canadá) tenía como objetivo demostrar la hipótesis de que el cambio terapéutico a fingolimod por vía oral mejora los resultados comunicados por los pacientes en comparación con el tratamiento modificador de la enfermedad estándar en pacientes con esclerosis múltiple recurrente; y también se evaluaron su seguridad y tolerabilidad. En cuanto a los criterios de valoración secundarios, se utilizó el inventario de la depresión de Beck-II para la depresión y el cuestionario de salud SF-36 para la calidad de vida [12].
Tal y como se ha descrito previamente, los estudios que evaluaron los efectos terapéuticos de los tratamientos para la EM suelen centrarse en reducir la tasa de recaídas, ralentizar la progresión de la discapacidad física y reducir la actividad de la enfermedad observada con resonancias magnéticas. Las personas con EM suelen experimentar otros problemas y síntomas en su día a día que afectan a su calidad de vida general relacionada con la salud.
Pacientes y métodos
Diseño del estudio y pacientes
Es un estudio prospectivo, no intervencionista y observacional para recopilar datos de pacientes con EM recurrente-remitente sometidos a tratamiento con fingolimod (como parte de su tratamiento clínico habitual) sobre la calidad de vida general, la Expanded Disability Status Scale (EDSS), los resultados comunicados por los pacientes y según la práctica clínica habitual. El estudio tenía como objetivo inscribir a 96 pacientes. Se hizo un seguimiento de todos los pacientes de hasta 24 meses. Los pacientes recibieron atención médica estándar durante el estudio, sin que se les realizaran pruebas de laboratorio ni procedimientos médicos adicionales; sólo se evaluaron los resultados comunicados por los mismos pacientes. Las evaluaciones se realizaron al inicio (1 día), en el mes 12 y en el mes 24.
Los pacientes elegibles tenían entre 18 y 60 años, con un diagnóstico de EM recurrente-remitente definido según los criterios de McDonald (2010) y una puntuación de 0-5,5 en la EDSS, y sólo se observó a pacientes con actividad de la enfermedad durante los 12 meses previos a la selección. Otro criterio de inclusión adicional fue haber participado previamente en un tratamiento con un tratamiento modificador de la enfermedad (interferón β-1a o 1b, o bien acetato de glatiramer) antes del tratamiento con fingolimod. Uno de los criterios de exclusión fue tener un trastorno psiquiátrico mayor preexistente o tratamiento antidepresivo en el mes previo a la inscripción. A todos los pacientes se les proporcionó un consentimiento informado por escrito antes de la inscripción.
Recogida de datos
Se evaluó la calidad de vida relacionada con la salud mediante la versión validada en búlgaro del cuestionario MSQOL-54, que consta de 12 subescalas junto con dos puntuaciones de resumen, así como dos mediciones más de un solo ítem. Las subescalas son: función física, limitaciones de la tarea (físicas), limitaciones de la tarea (emocionales), dolor, bienestar emocional, energía, percepciones de salud, función social, función cognitiva, malestar por la salud, calidad de vida general y función sexual. Las puntuaciones resumidas son el resumen combinado de salud física y el resumen combinado de salud mental. Las medidas de un solo ítem son la satisfacción con la función sexual y el cambio en la salud. Las puntuaciones más altas indican una mejor calidad de vida. Este cuestionario se rellenó al inicio, en el mes 12 y en el mes 24 tras el inicio del tratamiento.
La depresión se midió con la escala de puntuación de la depresión de Hamilton (HAM-D17). Esta es una escala que evalúa la depresión, ampliamente utilizada y administrada por clínicos. Se utilizó la versión corta de la prueba, de 17 ítems, para evaluar la gravedad y el cambio en los síntomas depresivos. La puntuación oscila entre 0 y 25, y las puntuaciones más bajas indican una depresión más leve.
La EDSS es la escala más utilizada para medir la discapacidad de los pacientes diagnosticados con EM. Una puntuación en la EDSS superior representa un mayor deterioro neurológico.
Otros datos que se recopilaron fueron la medicación concomitante, el número y la frecuencia de las recaídas, las hospitalizaciones previas y la aparición de acontecimientos adversos durante el estudio.
Métodos estadísticos
Se evaluaron dos poblaciones del estudio: la población para la seguridad se definió como todos los pacientes inscritos que recibieron la medicación del estudio y la población para la eficacia se definió como todos los pacientes de la población para la seguridad que tuvieron al menos un valor válido de datos de la eficacia posterior al inicio.
El criterio de valoración principal del estudio fue el cambio desde el inicio en la puntuación del MSQOL-54 hasta el mes 24 del tratamiento con fingolimod comparado mediante una prueba de la t de muestras emparejadas; en caso contrario, se aplicó la prueba no paramétrica de Wilcoxon. Los criterios de valoración secundarios del estudio (cambios en la puntuación del MSQOL-54 desde el inicio y tras 12 meses de tratamiento con fingolimod, cambios en la puntuación de la función sexual de las escalas relevantes del MSQOL-54, cambios en la puntuación de la HAM-D17, cambios en la puntuación de la EDSS) se analizaron de forma similar al criterio de valoración principal.
Se realizaron análisis de subgrupos por edad en el momento de la inscripción (<40 años; ≥40 años), según la puntuación en la EDSS al inicio (<3 puntos; ≥3 puntos) y por sexo (hombre; mujer). Las asociaciones entre las variables cuantitativas (la edad en el momento de la inscripción, la puntuación inicial en la EDSS) y los resultados de la calidad de vida se midieron mediante la correlación de Spearman.
El nivel de significación estadística se estableció en p < 0,05. Todos los análisis se realizaron con el paquete IBM SPSS Statistics® (versión 26).
Aprobación del protocolo estándar, registros y consentimientos de pacientes
Se obtuvo la aprobación del Comité Ético de Ensayos Multicéntricos de Bulgaria. El número de confirmación es el KI-148/25.11.2015.
Se obtuvo el consentimiento informado por escrito de todos los participantes en el estudio. Tanto la Agencia Búlgara del Medicamento (NIS-0001/ 27.01.2016) como el Comité Ético para Ensayos Multicéntricos (KI-148/25.11.2015) aprobaron el formulario de consentimiento informado.
Resultados
Distribución y características iniciales de los pacientes
En el estudio se inscribieron 93 pacientes con EM, y 87 pacientes tenían al menos un valor válido de datos posteriores al inicio. En la población para la eficacia, había 41 (47,1%) varones y 46 (52,9%) mujeres, y la edad media ± desviación estándar era de 38,7 ± 8,45 años. La mayoría de los pacientes notificó dos recaídas y dos hospitalizaciones al año al inicio del estudio, y la mediana de la puntuación en la EDSS fue de 3,5 puntos (con un rango de 2 a 4,5). En la tabla I se describen las características iniciales detalladas.
Tabla I.
Características demográficas y de la enfermedad iniciales en la población para la eficacia.
| Total (n = 87) | |
|---|---|
| Edad, media (DE), años | 38,7 (8,45) |
|
| |
| Mujeres, n (%) | 46 (52,9%) |
|
| |
| Puntuación en la EDSS, media (intervalo) | 3,2 (2-4,5) |
|
| |
| Número de recaídas al año, n (%) | |
|
| |
| 1 | 8 (9,4%) |
|
| |
| 2 | 73 (85,9%) |
|
| |
| 3 | 4 (4,7%) |
|
| |
| Número de hospitalizaciones al año, n (%) | |
|
| |
| 1 | 9 (10,8%) |
|
| |
| 2 | 71 (85,5%) |
|
| |
| 3 | 3 (3,6%) |
DE: desviación estándar; EDSS: Expanded Disability Status Scale.
Calidad de vida a los 12 meses de tratamiento con fingolimod
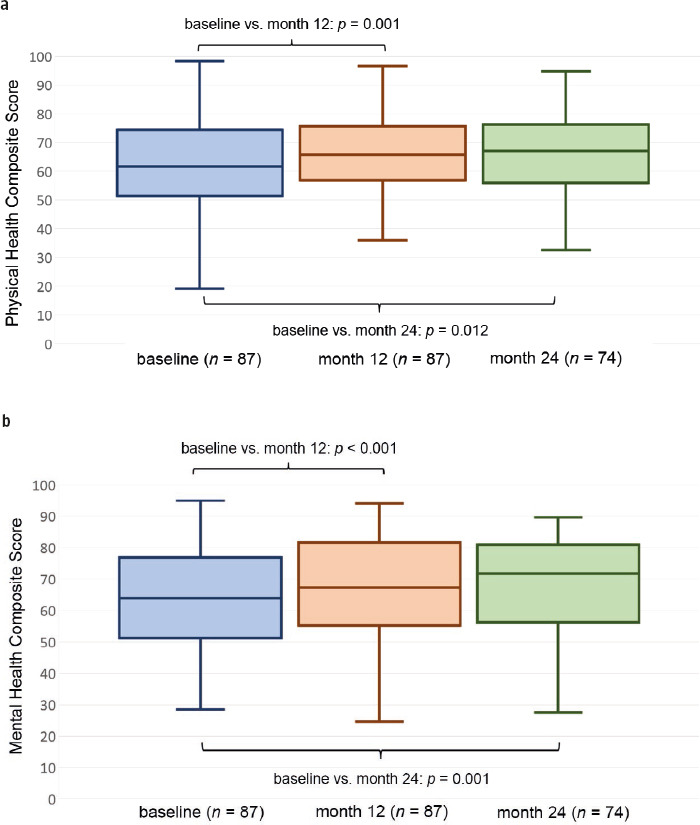
La puntuación combinada de salud mental fue de 63,2 ± 16,11 al inicio y de 66,6 ± 16,98 en el mes 12, lo que supuso un cambio medio estadísticamente significativo con respecto al inicio (p = 0,001). La puntuación del componente físico fue de 61,2 ± 16,98 al inicio y de 66,5 ± 15,46 en el mes 12, y este cambio fue estadísticamente significativo (p < 0,001). Del mismo modo, se observó un cambio estadísticamente significativo a los 12 meses de tratamiento en la puntuación de salud física en las subescalas, las limitaciones de la tarea debido a problemas físicos, las limitaciones de la tarea debido a problemas emocionales, el dolor, el bienestar emocional, la función social, el malestar por la salud, los cambios en la salud y la satisfacción con la función sexual (Tabla II; Fig. 1a y b).
Tabla II.
Puntuaciones combinadas medias de salud física en la MSQoL-54, puntuaciones combinadas de salud mental, puntuaciones en la HAM-D17 y puntuaciones en la EDSS por visitas.
| n | Media (DE) | |
|---|---|---|
| PCS en el MSQoL-54 | ||
| Inicio | 87 | 61,16 (16,98) |
|
| ||
| Mes 12 | 87 | 65,51 (15,46) |
|
| ||
| Mes 24 | 74 | 66,32 (16,7) |
|
| ||
| MCS en el MSQoL-54 | ||
|
| ||
| Inicio | 87 | 63,17 (16,11) |
|
| ||
| Mes 12 | 87 | 66,6 (16,98) |
|
| ||
| Mes 24 | 74 | 67,55 (15,94) |
|
| ||
| HAM-D17 | ||
|
| ||
| Inicio | 87 | 4,93 (4,41) |
|
| ||
| Mes 12 | 87 | 3,97 (2,86) |
|
| ||
| Mes 24 | 75 | 3,41 (2,57) |
|
| ||
| EDSS | ||
|
| ||
| Inicio | 87 | 3,19 (0,744) |
|
| ||
| Mes 12 | 87 | 3,24 (0,758) |
|
| ||
| Mes 24 | 73 | 3,29 (0,845) |
DE: desviación estándar; EDSS: Expanded Disability Status Scale; HAM-D17: escala de puntuación de la depresión de Hamilton; MCS: puntuación combinada de salud mental; MSQoL-54: Multiple Sclerosis Quality of Life-54; PCS: puntuación combinada de salud física.
Figura 1.
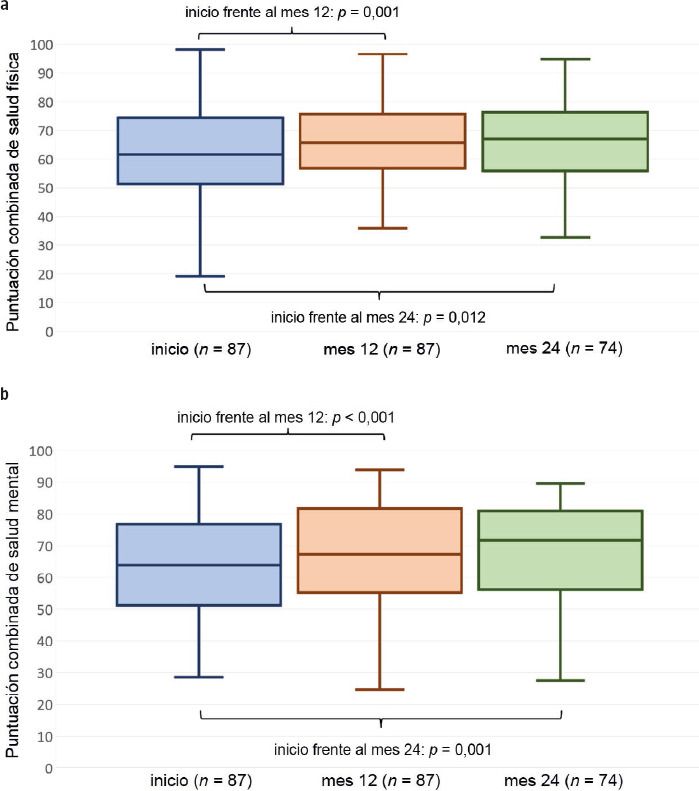
a) Puntuación combinada de salud física; b) Puntuación combinada de salud mental.
Calidad de vida a los 24 meses de tratamiento con fingolimod
La puntuación combinada de salud mental fue de 64 ± 16,69 al inicio y de 67,5 ± 15,94 en el mes 24, lo que supuso un cambio medio estadísticamente significativo con respecto al inicio (p = 0,012). La puntuación combinada de salud física fue de 61,7 ± 17,61 al inicio y de 66,3 ± 16,7 en el mes 24, y este cambio fue estadísticamente significativo (p = 0,001). Del mismo modo, se observaron cambios estadísticamente significativos a los 24 meses de tratamiento en la puntuación de salud física, las limitaciones de la tarea debidas a problemas físicos, el dolor, la energía y el cambio en las subescalas de salud (Tabla II; Fig. 1a y b).
Depresión y funcionamiento sexual
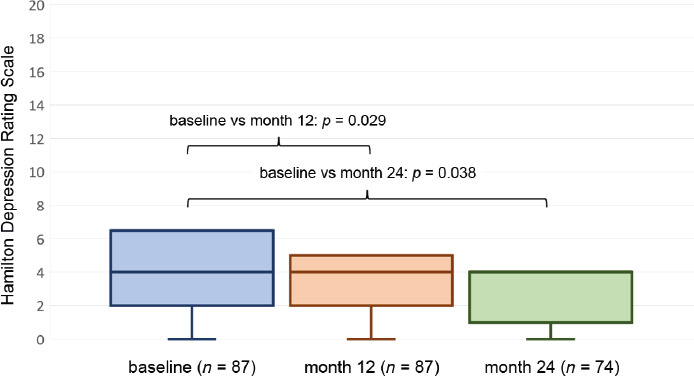
La puntuación media en la HAM-D17 ± desviación estándar fue de 4,93 ± 4,41 al inicio y 3,97 ± 2,86 en el mes 12, y este cambio sí fue estadísticamente significativo (p = 0,029). Del mismo modo, se observó una disminución estadísticamente significativa (p = 0,038) entre el valor medio inicial (4,76 ± 4,5) y el valor del mes 24 (3,41 ± 2,57) (Tabla II; Fig. 2).
Figura 2.
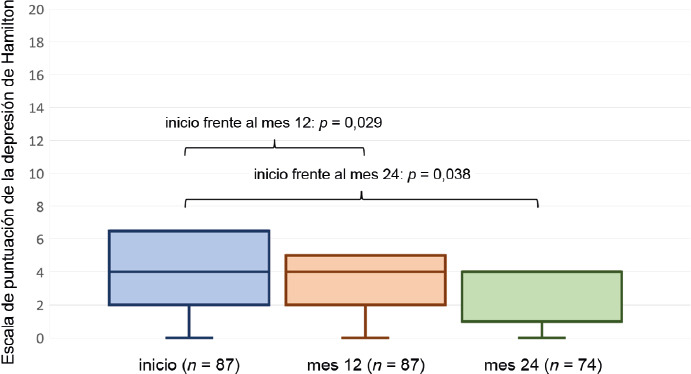
Escala de puntuación de la depresión de Hamilton.
En la comparación entre el valor inicial y el mes 12 encontramos una mejora estadísticamente significativa en la subescala de satisfacción con la función sexual. Dicho valor aumentó desde la media de 66,6 ± 30,54 a 70,9 ± 27,40 puntos (p = 0,028), pero el cambio en la subescala de función sexual no fue significativo (p = 0,184). En la comparación entre el inicio y el mes 24, no encontramos diferencias estadísticamente significativas (escala de la función sexual, p = 0,35; escala de satisfacción con la función sexual, p = 0,424).
Expanded Disability Status Scale
La puntuación media en la EDSS aumentó de 3,19 ± 0,744 a 3,24 ± 0,758 puntos en el mes 12, aunque este aumento no fue estadísticamente significativo (p = 0,302). En la comparación entre el valor inicial y el mes 24, la puntuación en la EDSS aumentó a 3,29 ± 0,845 (p = 0,013). A los 24 meses, se observó una disminución en la puntuación de la EDSS en nueve pacientes (12,3%), se detectó un aumento en 28 pacientes (38,4%) y se registró una puntuación estable en la EDSS en 36 pacientes (49,3%) (Tabla II).
Análisis de subgrupos
En el análisis de subgrupos se observó que la satisfacción con la mejora de la función sexual era superior en las mujeres que en los hombres (p = 0,028; el cambio respecto al valor inicial es de 9,38 puntos y de –3,21 puntos, respectivamente) en el mes 24.
Además, observamos una diferencia estadísticamente significativa entre los pacientes estratificados por edad en la subescala de satisfacción con la función sexual (p = 0,042). Se detectó una mejora en el grupo de pacientes menores de 40 años (cambio medio con respecto al valor inicial en comparación con la puntuación en el mes 24: 9,03 puntos), mientras que en el grupo de pacientes mayores de 40 años se observó un descenso (cambio medio respecto al valor inicial en el mes 24: –4,39 puntos).
Al investigar los objetivos del estudio con subgrupos caracterizados por los puntos en la EDSS al inicio se encontraron mejoras importantes en nueve subescalas en el mes 12 y en 12 subescalas en el mes 24 en la escala Multiple Sclerosis Quality of Life-54 (MSQoL-54). Todos los resultados destacables fueron superiores en el subgrupo de <3 puntos de la EDSS.
Seguridad
Cinco pacientes (el 5,4% de los pacientes inscritos) que recibieron al menos un tratamiento con fingolimod notificaron acontecimientos adversos. Se notificaron un total de 16 acontecimientos y la gran mayoría se registraron como acontecimientos adversos graves (15 acontecimientos en cuatro pacientes). El principal acontecimiento adverso de esta categoría fue la recaída de la EM. Todos los acontecimientos adversos graves estuvieron relacionados con la recaída de la EM.
No hubo ninguna sospecha de que los acontecimientos adversos estuvieran relacionados con el fármaco del estudio. Todos los pacientes afectados se recuperaron completamente de todos los acontecimientos.
Discusión
El objetivo de este estudio era reunir pruebas de la vida real de la cohorte búlgara de pacientes con EM recurrente-remitente y observar el uso de fingolimod como opción de tratamiento una vez que ha fracasado el tratamiento modificador de la enfermedad de primera línea sin andar probando diferentes tratamientos modificadores de la enfermedad de primera línea que no aportaran valor añadido al control de la enfermedad por parte del paciente (la primera opción de la segunda línea).
Como sólo hay un número relativamente reducido de investigaciones que evalúan la depresión, la disfunción sexual y otros resultados comunicados por los pacientes en la población con EM, este estudio aporta conocimientos sobre los efectos que tienen estos síntomas, normalmente ignorados, en la calidad de vida general de los pacientes con EM, proporciona datos prospectivos de dos años sobre los efectos terapéuticos habituales en términos de control de los síntomas y evalúa la influencia en la mejora de la calidad de vida.
Observamos una mejora significativa en la calidad de vida evaluada mediante la escala MSQoL-54, tanto en el mes 12 como en el 24. Nuestros resultados respaldan una observación previa de que los tratamientos de segunda línea pueden tener un mayor impacto en la calidad de vida de los pacientes que los tratamientos de primera línea [13].
Es bien sabido que las puntuaciones de calidad de vida general relacionada con la salud se correlacionan con los resultados de salud en la EM (por ejemplo, la EDSS) y que una mala calidad de vida es un factor predictivo de discapacidad a largo plazo [13]. Esta observación previa se ve respaldada por nuestros hallazgos, que indican que se observaron puntuaciones más altas en varias subescalas de la MSQOL-54 en pacientes con <3 puntos en la EDSS al inicio.
La depresión es un problema importante en los pacientes con EM y su prevalencia a lo largo de la vida puede alcanzar hasta el 50% [14]. En nuestro estudio se aplicó la puntuación de la HAM-D17 para evaluar los niveles de depresión de los pacientes y vimos una mejora significativa. En consonancia con nuestro resultado, otro estudio notificó que el tratamiento con fingolimod se asociaba a una mejora de los síntomas depresivos en pacientes con EM que habían estado recibiendo otro tratamiento distinto antes [15].
Aunque se observó un aumento estadísticamente significativo en la visita a los 24 meses en la puntuación de la EDSS, en la mayoría de los pacientes se observó una puntuación en la EDSS estable o menor, un patrón que también se observó en otro estudio [16].
Nuestro estudio tiene varias limitaciones importantes y algunas de ellas se derivan de su diseño como estudio observacional. Otra de las limitaciones es que en el estudio no se recogieron los resultados de los análisis de laboratorio ni los registros de las exploraciones médicas, por lo que muchos patrones específicos de los pacientes quedan sin explorar. Esta misma limitación puede ser consecuencia de que se notificaron muy pocos efectos secundarios en comparación con otros estudios. Por último, cabe destacar que el pequeño tamaño de la muestra podría influir en nuestros resultados.
En resumen, recopilamos datos de la vida real, y este estudio no intervencionista proporciona información útil para seguir mejorando la atención a los pacientes con EM.
Agradecimientos:
Los autores agradecen a AdWare Research, Hungría, su apoyo en la redacción médica, que fue financiada por Novartis Bulgaria (Sofía), de acuerdo con las últimas directrices de buenas prácticas de publicación.
Funding Statement
Financiación: El estudio está patrocinado por Novartis Bulgaria.