Abstract
Introducción.
La enfermedad de Parkinson (EP) es una enfermedad neurodegenerativa progresiva relacionada con la edad que requiere nuevas alternativas terapéuticas. La safinamida, un nuevo tratamiento add-on a la levodopa, afecta positivamente a las fluctuaciones de esta enfermedad al modular los sistemas dopaminérgico y glutamatérgico. Para investigar más a fondo el uso de la safinamida en la práctica clínica rutinaria europea, el presente análisis post hoc tiene como objetivo comprender el perfil de seguridad de la safinamida dentro de la población española del estudio.
Pacientes y métodos.
Se evaluó a 511 pacientes españoles con EP al inicio, cuatro (±1), ocho (±1) y 12 (±1) meses después de iniciar el tratamiento con safinamida. Se utilizaron la puntuación total de la escala unificada de puntuación de la enfermedad de Parkinson (UPDRS) y la puntuación de la UPDRS III, durante el tiempo en on para medir la gravedad general de la EP y las complicaciones motoras, respectivamente, mientras que la gravedad de los acontecimientos adversos se evaluó siguiendo los criterios de los investigadores.
Resultados.
La safinamida mostró un perfil de seguridad favorable en la población española del estudio, aunque la prescripción a pacientes con enfermedades psiquiátricas y el uso para indicaciones no autorizadas fueron más frecuentes que en la población europea del estudio. En España se observaron mejoras clínicamente significativas en las puntuaciones de la UPDRS cuando se utilizó la safinamida como único tratamiento add-on a la levodopa (el 57,4 y el 53,7% de los pacientes) y cuando se venía de administrar rasagilina (el 55,1% de los pacientes). Las complicaciones motoras se redujeron del 83,2 al 63,3% tras el período de estudio. No se detectaron mayores problemas de seguridad en ningún subgrupo de pacientes, aunque los pacientes con deterioro cognitivo mostraron una frecuencia algo superior de acontecimientos adversos.
Conclusiones.
Este subanálisis respalda el uso de la safinamida como opción segura y eficaz para el tratamiento de las fluctuaciones motoras en diferentes subgrupos de pacientes tratados con levodopa. Sin embargo, la safinamida debe utilizarse con precaución en pacientes con deterioro cognitivo.
Palabras clave: Complicaciones motoras, Complicaciones no motoras, Discinesias, Enfermedad de Parkinson, Levodopa, Safinamida
Introducción
La enfermedad de Parkinson (EP) es el trastorno neurológico que más rápido está aumentando actualmente en el mundo [1]; afecta sobre todo a personas de entre 85 y 89 años, y se prevé que imponga una carga socioeconómica cada vez mayor a las sociedades envejecidas [2-5]. La EP se caracteriza por la degeneración progresiva de las neuronas dopaminérgicas nigroestriadas y el agotamiento de la dopamina en el cuerpo estriado dorsal, lo cual provoca los íntomas motores y no motores característicos [2,6].
Los medicamentos actuales para la EP ayudan a mejorar los déficits motores asociados a la enfermedad, ya que aumentan la actividad dopaminérgica dentro del cuerpo estriado dorsal [7,8]. Debido a su eficacia y tolerabilidad en las primeras fases de la enfermedad, la levodopa, precursora de la dopamina, es la piedra angular del tratamiento de la EP. Sin embargo, los niveles de levodopa en el cerebro empezarán a fluctuar cada vez más, alternando la reaparición de los síntomas (wearing off) con discinesias de dosis máxima asociadas a concentraciones de levodopa más elevadas [7-10]. Esta situación va empeorando progresivamente con el tiempo [7,11-13]. Aunque existen tratamientos complementarios para superar las fluctuaciones, sigue habiendo una necesidad no cubierta del tratamiento óptimo para la EP [7,14].
La safinamida es un tratamiento add-on a levodopa que ha demostrado su eficacia en el control de las fluctuaciones motoras relacionadas con la EP [14-17]. Ejerce un doble mecanismo de acción único, que comprende la inhibición selectiva y reversible de la monoaminooxidasa B y la reducción de la transmisión glutamatérgica hiperactiva, lo que representa una ventaja clínica importante que puede ser eficaz a la hora de aliviar las fluctuaciones motoras y mejorar las discinesias inducidas por la levodopa [7,16,18-24]. Un grupo de expertos españoles llegó a un consenso sobre los beneficios asociados a la safinamida en el tratamiento de pacientes con EP con fluctuaciones de leves a moderadas, e incluso avanzadas [25].
Conforme a la recomendación de la Agencia Europea de Medicamentos sobre la recopilación de datos de apoyo de la vida real [26], se llevó a cabo un estudio observacional del uso de fármacos denominado SYNAPSES (StudY to observe safiNAmide safety profile and pattern of use in clinical Practice during the firSt post-commErcialization phaSe, Estudio para observar el perfil de seguridad de la safinamida y el patrón de uso en la práctica clínica durante la primera fase poscomercialización) para describir los patrones de tratamiento y la aparición de acontecimientos adversos en pacientes con EP tratados con safinamida en condiciones de la vida real, incluidas poblaciones especiales de pacientes: pacientes mayores de 75 años, con comorbilidades relevantes o con enfermedades psiquiátricas concomitantes [27].
Los objetivos principal y secundario del presente análisis post hoc fueron analizar el perfil de seguridad de la safinamida en la población española del estudio en comparación con el conjunto de datos europeo y abordar si el tratamiento con safinamida puede mejorar las complicaciones motoras en subgrupos específicos de pacientes, respectivamente. Además, se analizó la evolución longitudinal de diferentes fluctuaciones motoras.
Pacientes y métodos
Diseño del estudio
El informe actual es un análisis post hoc de los participantes españoles del estudio SYNAPSES (número de registro EU PAS EUPAS-13745), un estudio de cohortes observacional, multinacional, multicéntrico, retrospectivo-prospectivo en el que se hizo un seguimiento de los pacientes con diagnóstico confirmado de EP idiopática durante 12 meses tras iniciar el tratamiento con safinamida (valor inicial) [27]. Este estudio fue aprobado por las autoridades sanitarias e institucionales locales y europeas, y cumplió con sus requisitos (véase el informe principal).
En el informe del estudio principal se describe detalladamente el protocolo del estudio [27]. En resumen, en la evaluación final se inscribió a 511 de los 532 pacientes españoles de 38 centros de neurología y geriatría especializados en el tratamiento de la EP, tras haber cumplido los criterios de inclusión establecidos (véase el informe principal). A lo largo de 24 meses se fue inscribiendo a los pacientes que cumplieron los requisitos en orden consecutivo sin aleatorización [27]. La decisión de iniciar el tratamiento con safinamida se tomó basándose únicamente en la evaluación clínica y tuvo que tomarse antes de la inclusión de los pacientes en el estudio.
Se evaluó a los pacientes al inicio y cuatro (±1), ocho (±1) y 12 (±1) meses después [27]. Los datos se recopilaron de forma prospectiva o retrospectiva en función del momento de la inscripción.
Mediciones
Las comorbilidades concomitantes relevantes, así como la gravedad de los acontecimientos adversos y su relación con el tratamiento con safinamida, se determinaron según el juicio clínico de los investigadores participantes. Se utilizaron la puntuación total de la escala unificada de puntuación de la enfermedad de Parkinson (UPDRS) [28] y la puntuación de la UPDRS III, durante el tiempo en on para medir la gravedad general de la EP y las complicaciones motoras, respectivamente, en los pacientes tratados con safinamida al inicio y durante cada visita de seguimiento. También se analizaron subgrupos específicos: pacientes que habían sido tratados previamente con rasagilina, altas dosis de levodopa o que tenían safinamida como único tratamiento add-on al inicio del período de observación. En cada paciente, se calculó la dosis diaria equivalente de levodopa total al inicio del estudio como la suma de las dosis equivalentes de levodopa en todas las medicaciones en curso siguiendo el cálculo de las dosis equivalentes de levodopa conforme a los factores de conversión predefinidos (Tabla I) [29].
Tabla I.
Factores de conversión para calcular las dosis equivalentes de levodopa para los medicamentos comúnmente utilizados en la EP [29].
| Factor de conversión | |
|---|---|
| Duodopa | DD × 1,11 |
|
| |
| Duodopa (gel de levodopa/carbidopa) | DD × 1,11 |
|
| |
| Levodopa/carbidopa retardada | DD × 0,5 |
|
| |
| Madopar® retardado | DD × 0,5 |
|
| |
| Sinemet® plus retardado | DD × 0,5 |
|
| |
| Sinemet® retardado | DD × 0,5 |
|
| |
| Levodopa/carbidopa | DD × 1 |
|
| |
| Madopar® | DD × 1 |
|
| |
| Sinemet® | DD × 1 |
|
| |
| Stalevo® | DD × 1 |
DD: dosis diaria de un medicamento que contiene levodopa.
Métodos estadísticos
Debido a la naturaleza observacional de este estudio de datos de la vida real, nuestro objetivo sólo era obtener información sobre el uso clínico cotidiano de la safinamida y no buscar significancias estadísticas entre las distintas condiciones. Para más información sobre los análisis estadísticos de SYNAPSES, consulte el informe principal [27]. Los pacientes con valores faltantes no se excluyeron del análisis ni se sustituyeron sus datos. Las variables categóricas se describen mediante frecuencias absolutas y relativas, mientras que las variables continuas y discretas se expresan como medias y desviaciones estándar.
Resultados
Datos españoles y europeos
Comparación del perfil de los pacientes
Los datos demográficos obtenidos del estudio principal SYNAPSES (datos europeos) [27] y del presente análisis post hoc español (datos españoles) son muy similares, como cabía esperar (Tabla II). Sin embargo, observamos ciertas diferencias menores, pero significativas, entre las dos poblaciones de pacientes que pueden tener más implicaciones. Los pacientes con diagnóstico de parkinsonismo atípico habían sido tratados ligeramente más a menudo con safinamida entre la población española del estudio (1,8%) en comparación con la población europea (0,8%). Además, en España observamos una tendencia a prescribir safinamida a los pacientes con EP menos avanzada. Una mayor proporción de los participantes españoles del estudio estaban en los estadios 1 y 2 de Hoehn & Yahr (66,2%) al inicio del estudio, mientras que la proporción correspondiente de los pacientes europeos fue del 56,2%.
Tabla II.
Datos demográficos. Comparación de los perfiles de los pacientes en el estudio principal SYNAPSES (Europa) y el análisis post hoc de la población española del estudio (España).
| Número total de pacientes evaluables | Pacientes > 75 años | Pacientes con comorbilidades relevantes | Pacientes con enfermedades psiquiátricas | ||||||
|---|---|---|---|---|---|---|---|---|---|
|
|
|
|
|
||||||
| España n = 511 (100%) | Europa n = 1558 (100%) | España n = 131 (25,6%) | Europa n = 391 (25,1%) | España n = 373 (73,0%) | Europa n = 1103 (70,8%) | España n = 249 (48,7%) | Europa n = 661 (42,4%) | ||
| Sexo (n, %) | Hombre | 289 (56,6%) | 961 (61,7%) | 59 (45,0%) | 221 (56,5%) | 200 (53,6%) | 665 (60,3%) | 119 (47,8%) | 356 (53,9%) |
|
|
|
|
|
||||||
| Mujer | 222 (43,4%) | 597 (38,3%) | 72 (55,0%) | 170 (43,5%) | 173 (46,4%) | 438 (39,7%) | 130 (52,2%) | 305 (46,1%) | |
|
|
|
|
|
||||||
| Edad en la inscripción (años: DE ± media) | 68 ± 10,3 | 68,4 ± 9,7 | 79,9 ± 3,0 | 79,7 ± 3,1 | 70 ± 9,1 | 70,0 ± 8,7 | 68,7 ± 9,9 | 68,3 ± 9,4 | |
|
|
|
|
|
||||||
| Raza (n, %) | Caucásica | 507 (99,2%) | 1543 (99,0%) | 131 (100%) | 389 (99,5%) | 369 (98,9%) | 1094 (99,2%) | 247 (99,2%) | 658 (99,5%) |
|
|
|
|
|
||||||
| Otra | 4 (0,8%) | 15 (1,0%) | 0 (0,0%) | 2 (0,5%) | 4 (1,1%) | 9 (0,8%) | 2 (0,8%) | 3 (0,5%) | |
|
|
|
|
|
||||||
| Diagnóstico (n, %) | EP idiopática | 500 (97,8%) | 1542 (99,0%) | 129 (98,5%) | 389 (99,5%) | 367 (98,4%) | 1094 (99,2%) | 243 (97,6%) | 653 (98,8%) |
|
|
|
|
|
||||||
| Parkinsonismo atípico | 9 (1,8%) | 12 (0,8%) | 2 (1,5%) | 2 (0,5%) | 5 (1,3%) | 7 (0,6%) | 5 (2,0%) | 6 (0,9%) | |
|
|
|
|
|
||||||
| EP infantil | 2 (0,4%) | 4 (0,3%) | 0 (0,0%) | 0 (0,0%) | 1 (0,3%) | 2 (0,2%) | 1 (0,4%) | 2 (0,3%) | |
|
|
|
|
|
||||||
| Tiempo transcurrido desde el diagnóstico (años: DE ± media) | 8,1 ± 5,6 | 7,9 ± 5,3 | 8,1 ± 5,2 | 7,9 ± 5,3 | 8,0 ± 5,5 | 7,8 ± 5,3 | 8,9 ± 6,1 | 8,4 ± 5,5 | |
|
|
|
|
|
||||||
| Tiempo transcurrido desde el inicio de los síntomas (años: DE ± media) | 8,9 ± 5,5 | 8,8 ± 5,5 | 8,8 ± 4,9 | 8,9 ± 5,5 | 8,8 ± 5,3 | 8,7 ± 5,4 | 9,5 ± 6,1 | 9,3 ± 5,5 | |
|
|
|
|
|
||||||
| Edad al inicio de los síntomas (años: DE ± media) | 58,6 ± 11,5 | 59,3 ± 11,0 | 71,2 ± 5,5 | 70,9 ± 6,5 | 60,9 ± 10,2 | 61,0 ± 10,1 | 58,8 ± 11,5 | 58,8 ± 10,7 | |
| Estadio Hoehn & Yahr (n, %) | 1 | 20 (4,2%) | 82 (5,3%) | 1 (0,8%) | 5 (1,3%) | 16 (4,5%) | 45 (4,1%) | 6 (2,5%) | 21 (3,1%) |
|
|
|
|
|
||||||
| 2 | 295 (62,0%) | 793 (50,9%) | 58 (48,7%) | 143 (36,6%) | 206 (58,4%) | 550 49,9%) | 129 (54,4%) | 307 (46,4%) | |
|
|
|
|
|
||||||
| 3 | 139 (29,2%) | 421 (27,1%) | 52 (43,7%) | 144 (36,9%) | 114 (32,3%) | 325 (29,5%) | 85 (35,9%) | 215 (32,5%) | |
|
|
|
|
|
||||||
| 4 | 21 (4,4%) | 88 (5,6%) | 8 (6,7%) | 40 (10,2%) | 16 (4,5%) | 70 (6,3%) | 17 (7,2%) | 63 (9,5%) | |
|
|
|
|
|
||||||
| 5 | 1 (0,2%) | 6 (0,4%) | 0 (0,0%) | 4 (1,0%) | 1 (0,3%) | 5 (0,5%) | 0 (0,0%) | 4 (0,6%) | |
Los porcentajes (%) se calculan por columnas. DE: desviación estándar; EP: enfermedad de Parkinson; n: número de pacientes.
Una observación de posible relevancia clínica fue que, en España, hubo más pacientes (un 30,9%) cuyo tratamiento con safinamida no se ajustaba a su indicación (es decir, un uso para indicaciones no autorizadas). En la población europea del estudio, sólo el 16,9% de los pacientes tomó safinamida para indicaciones no autorizadas (Tabla III). Esta diferencia se debió principalmente a la prescripción más frecuente de safinamida a pacientes sin fluctuaciones motoras (el 16,8 frente al 8,8%) y al inicio del tratamiento con dosis distintas de 50 mg/día (el 14,5 frente al 7,6%) en España, donde hay tendencia a prescribir safinamida en fases más tempranas, como el estado en on subóptimo.
Tabla III.
Frecuencia de uso para indicaciones no autorizadas de la safinamida entre las poblaciones española y europea del estudio al inicio del tratamiento.
| Categoría de uso para indicaciones no autorizadas | España (n, %) | Europa (n, %) |
|---|---|---|
| Cualquiera | 158 (30,9%) | 233 (16,9%) |
|
| ||
| Pacientes sin fluctuaciones motoras al inicio del tratamiento | 86 (16,8%) | 121 (8,8%) |
|
| ||
| Pacientes que comienzan la safinamida con una dosis distinta de 50 mg/día | 74 (14,5%) | 105 (7,6%) |
|
| ||
| Pacientes sin levodopa además de safinamida | 14 (2,7%) | 21 (1,5%) |
|
| ||
| Pacientes con un diagnóstico distinto a la EP idiopática | 11 (2,2%) | 16 (1,2%) |
|
| ||
| Pacientes tratados concomitantemente con otros inhibidores de la MAO | 7 (1,4%) | 11 (0,8%) |
Los porcentajes (%) se calculan a partir de los pacientes evaluables. EP: enfermedad de Parkinson; MAO: monoaminooxidasa; n: número de pacientes.
Dentro de las poblaciones especiales de pacientes, no observamos diferencias en la proporción de pacientes mayores de 75 años o de pacientes con comorbilidades relevantes al inicio del estudio (Tabla II). Curiosamente, sin embargo, un mayor porcentaje de los pacientes españoles parecía padecer enfermedades psiquiátricas concomitantes preexistentes (48,7%), sobre todo ansiedad (21,7%) y depresión (31,3%), en comparación con la muestra europea (42,4%). La psicosis sólo era prevalente en el 2,2% de la población española del estudio. Además, entre los pacientes españoles hubo alteraciones del sueño con más frecuencia (el 49,5 frente al 45,2%) y fatiga con menos frecuencia (el 19,4 frente al 25,5%) (Fig. 1a). En cuanto a los síntomas motores, los pacientes españoles tendían a padecer temblores (66,9%) con una frecuencia levemente superior en comparación con los participantes europeos (58,3%) antes de iniciar el tratamiento con safinamida.
Figura 1.

Prevalencia de síntomas motores y no motores (a) y uso de tratamientos concomitantes para la EP y psiquiátricos (b) al inicio del estudio en las poblaciones española y europea. Los porcentajes se calculan a partir del número total de pacientes evaluables. Un paciente puede tener más de un síntoma motor/no motor o medicación concomitante. España: n = 511; Europa: n = 1.558. COMT: catecol-O-metiltransferasa; EP: enfermedad de Parkinson; MAO-B: monoaminooxidasa B.
Conforme a la mayor prevalencia de comorbilidades psiquiátricas (incluidas las enfermedades psiquiátricas evaluadas como diagnóstico por los neurólogos y los síntomas psiquiátricos comunicados por los pacientes y evaluados por los clínicos), los pacientes españoles tomaron más fármacos psiquiátricos (como antidepresivos y otros tratamientos psiquiátricos) al inicio del estudio en comparación con la muestra europea (Fig. 1b). No se observaron diferencias importantes en el uso de tratamientos para la EP entre las poblaciones del estudio española y europea.
Población española
Efectos en las puntuaciones de la UPDRS
Observamos una reducción media de 1,6 puntos en la puntuación total de la UPDRS (subescalas I, II y III) y de 1,5 puntos en la puntuación de la UPDRS, parte III (examen motor), desde el inicio hasta los 12 meses de seguimiento entre todos los participantes españoles del estudio durante el tiempo en on (Tabla IV). Esto corrobora aún más la estabilidad de la gravedad de la enfermedad comunicada anteriormente a lo largo del tiempo, con mejoras aparentes de los síntomas motores tras el inicio del tratamiento con safinamida [27].
Tabla IV.
Puntuaciones de la UPDRS durante el período de observación en los participantes españoles del estudio (media ± DE).
| Valor inicial | 4 meses | 8 meses | 12 meses | |
|---|---|---|---|---|
| Parte I: actividad mental, comportamiento y estado de ánimo: 0-16 puntos | 2,2 ± 2,2 | 2,1 ± 2,2 | 1,9 ± 2,0 | 2,0 ± 2,2 |
|
| ||||
| Parte II: actividades de la vida cotidiana: 0-52 puntos | 11,6 ± 6,4 | 11,4 ± 6,3 | 11,0 ± 6,5 | 11,6 ± 6,8 |
|
| ||||
| Parte III: examen motor: 0-108 puntos | 26,8 ± 12,1 | 24,8 ± 12,0 | 24,8 ± 12,3 | 25,3 ± 13,0 |
|
| ||||
| Parte IV: complicaciones del tratamiento (en la última semana): 0-23 puntos | 4,0 ± 2,9 | 3,8 ± 2,6 | 3,6 ± 2,8 | 3,7 ± 2,7 |
|
| ||||
| Puntuación total (subescalas I, II y III): 0-176 puntos | 40,5 ± 17,8 | 38,8 ± 17,7 | 37,8 ± 17,8 | 38,9 ± 19,1 |
|
| ||||
| Puntuación total (subescalas I, II, III y IV): 0-199 puntos | 44,3 ± 18,6 | 42,4 ± 18,5 | 41,6 ± 18,9 | 43,0 ± 20,3 |
DE: desviación estándar; UPDRS: escala unificada de puntuación de la enfermedad de Parkinson.
Para abordar el uso de la safinamida en determinados subgrupos de pacientes, analizamos cómo respondían al tratamiento add-on con safinamida los pacientes tratados previamente con rasagilina, una dosis alta de levodopa (>400 mg) o safinamida como único tratamiento add-on al inicio del estudio (Fig. 2). La proporción de pacientes con una mejoría clínicamente relevante desde el inicio hasta los 12 meses de seguimiento (pacientes que respondieron) se definió en función de los criterios desarrollados por Shulman et al: se consideró clínicamente relevante una diferencia de más de 4,3 puntos en la puntuación total de la UPDRS y de más de 2,5 puntos en la puntuación de la parte III de la UPDRS [30].
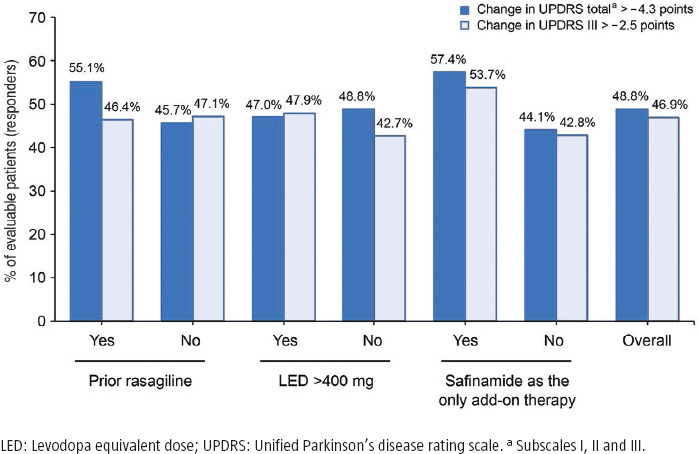
Figura 2.

Evolución de las puntuaciones de la UPDRS desde el inicio hasta el seguimiento de 12 meses en la población española del estudio. Se muestra el porcentaje de pacientes evaluables clasificados como ‘que respondieron’ según los criterios de Schulman (reducción de la UPDRS total > 4,3, barras oscuras; o UPDRS III > 2,5, barras claras) por separado para todos los pacientes evaluables (general) y las categorías de pacientes tratados previamente con rasagilina (rasagilina previa), que tenían una LED > 400 mg al inicio o que tenían safinamida como único tratamiento complementario al inicio. n = 163-207 (no se evaluó la UPDRS en todos los pacientes). Un paciente puede pertenecer a más de una categoría.
Cabe destacar que observamos que el 57,4 y el 53,7% de los pacientes que recibieron safinamida como único tratamiento add-on redujeron la puntuación total de la UPDRS en más de 4,3 puntos y la puntuación de la UPDRS III en más de 2,5 puntos, respectivamente (Fig. 2). Solo el 44,1% de los pacientes con tratamientos complementarios adicionales redujo la puntuación total de la UPDRS en más de 4,3 puntos y el 42,8% redujo la puntuación de la UPDRS III en más de 2,5 puntos. Así, la mejoría clínicamente relevante parecía más común entre los pacientes que recibieron safinamida como único tratamiento add-on, en comparación con quienes también utilizaban otros tratamientos complementarios. Igual de interesante es que el 55,1% de los pacientes tratados previamente con rasagilina, pero que cambiaron a safinamida, respondió al nuevo tratamiento con una mejora clínicamente relevante en la puntuación total de la UPDRS.
Tras 12 meses de tratamiento con safinamida, no observamos grandes diferencias en la mejoría clínicamente relevante entre los grupos de pacientes que recibieron dosis altas o bajas de levodopa al inicio (Fig. 2). Sin embargo, sí parecía haber una tendencia de mayor reducción media tanto en las puntuaciones de la UPDRS III como en las de la UPDRS totales en los pacientes tratados con dosis bajas de levodopa (≤400 mg) (media ± desviación estándar: –2,6 ± 9,1 y –2,3 ± 12,7, respectivamente) en comparación con los pacientes tratados con dosis más altas (>400 mg) (media ± desviación estándar: –0,7 ± 9,6 y –1,3 ± 11,7, respectivamente) (datos no mostrados).
Efectos sobre las complicaciones motoras
A pesar de que la safinamida se tomó con mayor frecuencia para indicaciones no autorizadas entre los participantes españoles, el número de pacientes con complicación motora se redujo del 83,2 al 63,3% tras un año de tratamiento con safinamida (Fig. 3). Las mejoras más pronunciadas se observaron en el período de wearing off de la respuesta, que se redujo del 62,2 al 47,8%, y en las discinesias, que se redujeron del 39,1 al 28,9%.
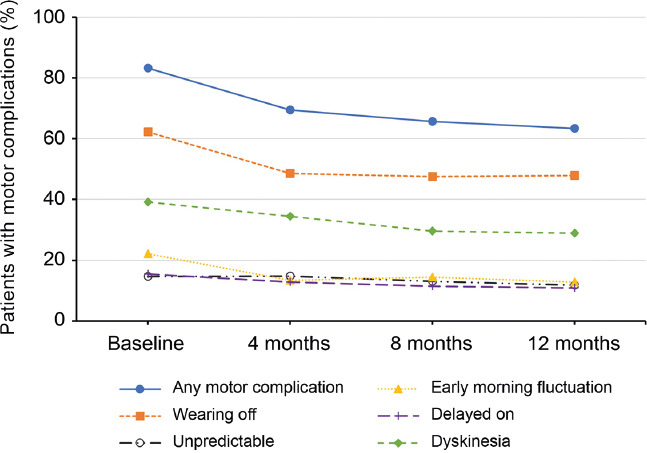
Figura 3.
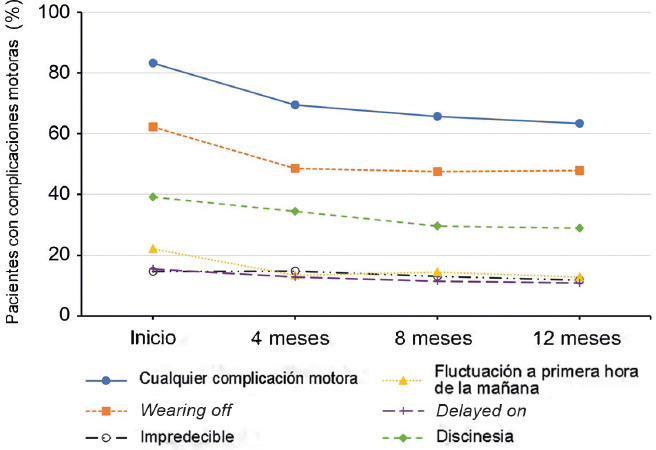
Proporción de pacientes con diferentes complicaciones motoras en la población española del estudio durante el seguimiento. Los porcentajes se calcularon por separado de todos los pacientes evaluables en cada uno de los puntos temporales de observación. Un paciente puede tener más de una complicación motora. Valor inicial: n = 511; a los 4 meses: n = 454; a los 8 meses: n = 436; a los 12 meses: n = 439.
Como era de esperar, se observó un mayor porcentaje de pacientes con complicaciones motoras, sobre todo wearing off de la respuesta y discinesias, entre quienes recibían >400 mg de dosis diaria de levodopa al inicio del tratamiento que entre quienes recibían dosis más bajas (Fig. 4a). Es importante destacar que, en ambas categorías, el tratamiento con safinamida redujo el número de pacientes con complicaciones motoras durante el período de seguimiento de 12 meses. La safinamida como único tratamiento add-on pareció reducir la proporción de pacientes con alguna complicación motora en mayor medida que cuando se combinó con otros tratamientos complementarios (Fig. 4b).
Figura 4.

Proporción de los participantes españoles del estudio con diferentes complicaciones motoras al inicio y a los 12 meses de seguimiento. Se muestran los porcentajes de pacientes con complicaciones por separado para los tratados con levodopa ≤ 400 mg o > 400 mg al inicio (a) y los que tenían safinamida como único tratamiento complementario o en combinación con otros tratamientos complementarios al inicio (b). Un paciente puede tener más de una complicación motora. n = 497 (al inicio). LED: dosis equivalente de levodopa.
Seguridad
En España se notificaron con mayor frecuencia los acontecimientos adversos y las reacciones adversas a los medicamentos (54,8 y 32,9% de los participantes, respectivamente) durante el período de observación, en comparación con el conjunto de datos europeo (45,8 y 27,7%, respectivamente, datos no mostrados). El factor que más contribuyó a las diferencias en los acontecimientos adversos fue la incidencia de trastornos del sistema nervioso (el 39,4 frente al 33,4%, conjuntos de datos españoles y europeos, respectivamente, datos no mostrados). Sin embargo, es interesante señalar que se produjeron menos acontecimientos adversos graves y reacciones adversas graves a medicamentos a pesar del uso más frecuente de la safinamida para indicaciones no autorizadas entre la población española del estudio (acontecimientos adversos graves: el 7,4 frente al 9,2%; y reacciones adversas graves a medicamentos: el 1,6 frente al 2,3% de los participantes, datos no mostrados). En la misma línea, los acontecimientos adversos se caracterizaron con mayor frecuencia como leves entre los pacientes españoles (69,3%) en comparación con los participantes europeos (61,9%).
La tendencia a utilizar con más frecuencia la safinamida para indicaciones no autorizadas en España no dio lugar a mayores inquietudes de seguridad en ninguno de las poblaciones especiales de pacientes. Las tasas de acontecimientos adversos graves o reacciones adversas graves a medicamentos notificados (al menos uno) en pacientes mayores de 75 años, con comorbilidades relevantes o con enfermedades psiquiátricas concomitantes, parecieron ser incluso ligeramente inferiores en España en comparación con los datos europeos. Cabe destacar que no se detectaron diferencias significativas en la frecuencia de los acontecimientos adversos, acontecimientos adversos graves, reacciones adversas a los medicamentos o reacciones adversas graves a medicamentos notificados entre el uso para indicaciones no autorizadas y autorizadas de la safinamida en la población española (Fig. 5). Esto respalda el perfil de seguridad favorable de la safinamida incluso entre los pacientes que hicieron un uso para indicaciones no autorizadas. No obstante, debe evaluarse la prescripción de safinamida a pacientes con deterioro cognitivo, ya que hay cierta tendencia a experimentar una frecuencia ligeramente superior de acontecimientos adversos (el 60 frente al 56,5%), acontecimientos adversos graves (el 10,9 frente al 7,9%), reacciones adversas a los medicamentos (el 36,4 frente al 31,6%) y reacciones adversas graves a medicamentos (el 1,8 frente al 1,1%) en comparación con los pacientes cognitivamente normales.
Figura 5.

Proporción de los participantes españoles del estudio que notificaron al menos un acontecimiento adverso (AA), reacción adversa al fármaco (RAM), acontecimiento adverso grave (AAG) o reacción adversa grave al fármaco (RAGM) durante el período de observación. Los porcentajes se calcularon por separado para los pacientes que tomaron safinamida de acuerdo con el resumen de características del producto (uso autorizado, barras abiertas) y para quienes la tomaron para indicaciones no autorizadas (barras claras). Uso para indicaciones autorizadas: n = 353; uso para indicaciones no autorizadas: n = 158.
Discusión
Se realizó un análisis post hoc para explorar si la safinamida tenía un perfil de seguridad favorable también en la población española del estudio, en la que el fármaco se prescribía con más frecuencia a pacientes con enfermedades psiquiátricas y en la que era más común su uso para indicaciones no autorizadas en comparación con la población europea del estudio. A pesar de que los acontecimientos adversos y las reacciones adversas a los medicamentos se notificaron con mayor frecuencia durante el período de observación, los acontecimientos adversos graves y las reacciones adversas graves a medicamentos parecieron ser menos frecuentes en la población española del estudio. Los acontecimientos adversos también parecieron ser más leves entre los pacientes españoles. Cabe destacar que no se detectaron diferencias significativas en la frecuencia de los acontecimientos adversos, acontecimientos adversos graves, reacciones adversas a los medicamentos o reacciones adversas graves a medicamentos notificados entre el uso para indicaciones no autorizadas y autorizadas de la safinamida. Además, el uso frecuente de la safinamida para indicaciones no autorizadas por parte de la población española no dio lugar a un aumento de las inquietudes de seguridad en ninguna de las poblaciones especiales de pacientes.
Para mayor detalle, también se evaluó si algunos subgrupos específicos de pacientes podrían beneficiarse del tratamiento con safinamida al obtener una mejora clínicamente relevante en las puntuaciones de la UPDRS. Los pacientes tratados previamente con rasagilina se beneficiaron del tratamiento con safinamida con mayor frecuencia en cuanto a la puntuación total de la UPDRS en comparación con quienes no habían tomado rasagilina anteriormente. La safinamida también demostró ser eficaz independientemente de la dosis diaria de levodopa. La safinamida como único tratamiento add-on pareció reducir la proporción de pacientes con fluctuación motora en mayor medida que la administración concomitante con otros tratamientos complementarios. Estas observaciones respaldan el valor de la safinamida como tratamiento add-on inicial y pueden justificar una mayor consideración a la hora de modificar las futuras guías terapéuticas de la EP.
Análisis de los conjuntos de datos españoles y europeos
En un consenso Delphi europeo se encuestó a un panel de especialistas en trastornos del movimiento de toda Europa sobre los resultados de la safinamida en la EP [31]. Se logró un fuerte consenso en todas las afirmaciones relativas a la eficacia de la safinamida sobre los síntomas motores, las fluctuaciones motoras, la calidad de vida y la seguridad. Por otro lado, se alcanzó un consenso positivo para los síntomas no motores, pero hubo falta de acuerdo sobre la eficacia de la safinamida para mejorar la cognición y las funciones urinaria y sexual. Del mismo modo, no se llegó a ningún acuerdo sobre la tolerabilidad del compuesto en pacientes con alucinaciones o en relación con la hipotensión ortostática. En cuanto a las poblaciones objetivo, los panelistas coincidieron en que la safinamida es una opción terapéutica válida en las fases tempranas de las fluctuaciones y en pacientes con EP avanzada [31].
En el presente estudio, cuando se analizaron los conjuntos de datos españoles y europeos, no se apreciaron diferencias destacables en las medicaciones concomitantes entre las dos poblaciones de estudio, lo cual es indicativo de la coherencia en el uso de los tratamientos para la EP en toda Europa y de acuerdo con el consenso Delphi europeo [27,31]. Sin embargo, se detectaron algunos aspectos con potencial relevancia clínica en la población española: mayor prescripción de la safinamida para indicaciones no autorizadas, y mayor proporción de pacientes que sufrían enfermedades psiquiátricas concomitantes y que recibían una mayor cantidad de medicación psiquiátrica.
Efecto de la safinamida en las puntuaciones de la UPDRS y las complicaciones motoras
Se ha demostrado ampliamente que la safinamida como tratamiento complementario logra controlar adecuadamente las complicaciones motoras [31-37], ya que reduce el tiempo en off y las dosis necesarias de levodopa (<400 mg) [31,33,35], lo cual se asocia a un menor riesgo de discinesias problemáticas de la dosis máxima y wearing off, así como a un control clínico satisfactorio de la EP [38-40]. En este análisis, el uso de la safinamida mostró un mayor beneficio clínico (reducción media de las puntuaciones de la UPDRS y de la cantidad de complicaciones motoras) cuando se inició junto con dosis bajas de levodopa y a pesar de un uso superior para indicaciones no autorizadas. Además, se observó una reducción media de las puntuaciones de la UPDRS superior en los pacientes que experimentaron un beneficio clínicamente relevante de la safinamida y tenían dosis equivalentes de levodopa ≤400 mg. Por eso, las futuras investigaciones que aborden los diagnósticos diferenciales y/o los informes de observación clínica para identificar a los pacientes que podrían obtener el mayor beneficio de la safinamida como tratamiento add-on podrían ayudar a explotar todo su potencial terapéutico.
Cambio tras recibir rasagilina
Es bastante habitual que los pacientes con EP que se están tratando con levodopa empiecen a experimentar fluctuaciones en el alivio de sus síntomas [40-42]. Para abordar este tema, el uso de inhibidores de la monoaminooxidasa B ha demostrado ser un complemento útil de la levodopa en pacientes que sufren fluctuaciones motoras [41,43,44]. La rasagilina pertenece a un grupo de fármacos que aumentan la biodisponibilidad de la dopamina al impedir de forma irreversible su metabolismo dependiente de la monoaminooxidasa [41,45]. Ciertos estudios anteriores han sugerido que los pacientes con EP podrían beneficiarse del cambio a la safinamida, no sólo quienes estaban recibiendo rasagilina, sino también quienes recibían otros inhibidores de la monoaminooxidasa B [32,33,41,46], debido a una mejora destacable de las fluctuaciones motoras y los síntomas motores, que se refleja en una puntuación inferior en el cuestionario WOQ-19 [32,41]. Más concretamente, las dosis altas de safinamida tuvieron una eficacia mayor que la rasagilina sobre el tiempo en off diario, las fluctuaciones y la discinesia, y pueden reducir las dosis necesarias de levodopa cuando se utilizan de forma concomitante [33,41,47]. En el presente subanálisis, el 55,1% de pacientes que estaban en tratamiento previo con rasagilina y cambiaron a safinamida respondieron al nuevo tratamiento de forma clínicamente relevante y mejoraron la puntuación total de la UPDRS, lo que sugiere un beneficio añadido del cambio de rasagilina a safinamida.
Perfil de seguridad de la safinamida en la población española
La seguridad de la safinamida se ha evaluado en múltiples estudios en diferentes contextos [31,36,47-50]. Algunos estudios se han centrado en su uso en pacientes de más de 75 años [48,49], en los que la safinamida resultó ser segura, eficaz y bien tolerada en dosis de 50-100 mg, de acuerdo con el consenso Delphi europeo [31,48]. Otros estudios, como el SADness-PD, confirmaron la eficacia y seguridad de la safinamida en pacientes con tratamiento antidepresivo, que es una medicación concomitante común en la EP [50]. Cabe destacar que la coadministración de safinamida con antidepresivos sigue siendo bien tolerada y resulta útil para tratar los síntomas y complicaciones motores [49-51].
En el presente estudio, aunque los acontecimientos adversos y las reacciones adversas a los medicamentos los notificaron con mayor frecuencia los pacientes españoles que los europeos, éstos fueron más leves y menos graves en la población española del estudio. Más concretamente, se reveló que el uso de safinamida para indicaciones no autorizadas era mayor en España, sobre todo debido a la frecuente prescripción de safinamida a pacientes sin fluctuaciones motoras y al inicio del tratamiento con dosis distintas de 50 mg/día. Sin embargo, no se detectaron diferencias significativas en la frecuencia de los acontecimientos adversos, acontecimientos adversos graves, reacciones adversas a los medicamentos o reacciones adversas graves a medicamentos notificados en general ni en ninguna de las poblaciones especiales, en comparación con el uso adecuado de safinamida, lo cual confirma el perfil de seguridad favorable de la safinamida incluso cuando se prescribe fuera de su indicación aprobada.
En cuanto a los pacientes con deterioro cognitivo, el uso de safinamida provocó una frecuencia levemente superior de acontecimientos adversos y reacciones adversas, lo que concuerda con el informe de un estudio en el que el 20% de los pacientes que abandonaron la safinamida debido a acontecimientos adversos presentaban deterioro cognitivo al inicio del estudio [47]. No obstante, el 89% de los panelistas del consenso Delphi europeo respaldó el perfil general de seguridad de la safinamida como tratamiento add-on para los pacientes con deterioro cognitivo [31], lo que sugiere que el mayor riesgo de acontecimientos adversos en esta población especial podría estar asociado a un estado de salud más frágil y no a la tolerabilidad a la safinamida. Otro punto que se debe considerar es la falta de información sobre el número de pacientes con deterioro cognitivo a los que se prescribió safinamida en el conjunto de datos europeo. La mayor frecuencia de acontecimientos adversos y reacciones adversas a los medicamentos podría atribuirse a que se prescribe con más frecuencia en España.
Limitaciones del subanálisis
Podría considerarse deficiente la comparación directa entre las poblaciones del estudio española y europea, ya que el conjunto de datos español estaba incluido en el conjunto de datos europeo. Aunque podría alegarse el enmascaramiento de diferencias interesantes, los análisis del estudio SYNAPSES dejaron claro que la safinamida presentaba un perfil de seguridad general favorable, incluso tras observar un mayor uso para indicaciones no autorizadas y problemas psiquiátricos entre los pacientes españoles con EP. Sin embargo, estas diferencias en la práctica clínica merecen una investigación más detallada y cuidadosa que lleve a la confirmación del perfil de seguridad de la safinamida en la población española del estudio.
Para terminar, la recogida de datos entre los distintos centros de inclusión presentó algunas incoherencias; por eso, algunos conjuntos de datos pueden haberse percibido como incompletos debido a la retirada de pacientes, cuando se debió a la falta de una metodología normalizada para adquirir la información relacionada con el tratamiento.
Conclusiones
El presente análisis post hoc confirma que la población española del estudio observacional SYNAPSES respondió a la safinamida como tratamiento add-on de forma similar a la población europea general del estudio. Curiosamente, aunque se observaron ciertas diferencias en la práctica clínica entre los países europeos participantes (como un mayor uso de la safinamida para usos no autorizados en España), no se observó ninguna consecuencia en el buen perfil de seguridad y tolerabilidad del fármaco. Asimismo, cuando se utilizó como tratamiento add-on para tratar a pacientes con EP fluctuante o a cualquiera de los grupos de interés predefinidos, se observaron beneficios similares en torno a las complicaciones motoras y las puntuaciones motoras con resultados clínicamente relevantes a largo plazo. Sin embargo, las leves diferencias registradas en los sujetos con deterioro cognitivo en cuanto a los efectos secundarios sugieren que, en esta subpoblación, la safinamida debe utilizarse con precaución. En resumen, nuestros resultados respaldan aún más el uso de la safinamida como opción segura y eficaz para el tratamiento de las fluctuaciones motoras en pacientes tratados con levodopa.
Agradecimientos:
Los autores desean dar las gracias a los investigadores y pacientes que participaron en el ensayo SYNAPSES. CDM Barcelona (España) se encargó de la redacción médica profesional y la ayuda editorial financiada por Zambon España. Zambon España financió la publicación de este artículo. Ninguno de los autores recibió ninguna remuneración económica.
Funding Statement
Financiación: El estudio europeo fue financiado por Zambon S.p.A. El subanálisis español fue financiado por Zambon España.