Abstract
目的
探讨自稳式人工椎体(artificial vertebral body,AVB)在颈前路椎体次全切除内固定融合手术(anterior cervical corpectomy and fusion,ACCF)中的短期应用效果。
方法
遵循牛津IDEAL(Idea, Development, Exploration, Assessment, and Long-term Follow-up)方法学原则,采用单臂探索型研究的方法,纳入脊髓型颈椎病患者进行回顾性分析。所有患者均接受单节段ACCF手术,术中植入3D打印自稳式AVB,术后规律随访。采用日本骨科协会(Japanese Orthopedics Association,JOA)脊髓损害评分表评估手术前后神经功能改善情况,依据术后6个月的影像学测量数据评估融合情况。
结果
共纳入11例病例,随访时间均超过6个月,手术时的平均年龄(57.2±10.2)岁,平均手术时间(76.1±23.1) min,中位出血量150(100, 200) mL。术后无吞咽困难、血肿形成、神经功能损伤加重等并发症出现。至末次随访,JOA评分由术前的13.2±2.2恢复至末次随访时的16.3±0.8,恢复率为85.9%。假体平均沉降距离为(1.2±1.1) mm,1例假体出现超出3 mm的严重沉降(9.1%)。颈椎前凸角度较术前显著改变(P=0.013)。至术后6个月时,所有病例均实现融合。
结论
自稳式AVB在单节段ACCF中的短期应用效果良好,融合率高,具有零切迹的优势,并发症少。
Keywords: 人工椎体, 自稳式, 零切迹, 3D打印, 脊髓型颈椎病
Abstract
Objective
To explore the short-term outcomes of 3D-printing stand-alone artificial vertebral body (AVB) in the surgical procedure of anterior cervical corpectomy and fusion (ACCF).
Methods
Following the proposal of IDEAL (idea, development, exploration, assessment, and long-term follow-up) framework, we designed and conducted this single-armed, retrospective cohort study. The patients with cervical spondylotic myelopathy were recruited, and these patients exclusively received the surgical procedure of single-level ACCF in our single center. After the process of corpectomy, the size was tailored using different trials and the most suitable stand-alone AVB was then implanted. This AVB was manufactured by the fashion of 3D-printing. Two pairs of screws were inserted in an inclined way into the adjacent vertebral bodies, to stabilize the AVB. The participants were regularly followed-up after the operation. Their clinical data were thoroughly reviewed. We assessed the neurological status according to Japanese Orthopedic Association (JOA) scale. We determined the fusion based on imaging examination six months after the operation. The recorded clinical data were analyzed using specific software and they presented in suitable styles. Paired t test was employed in comparison analysis.
Results
In total, there were eleven patients being recruited eventually. The patients were all followed up over six months after the operation. The mean age of the cohort was (57.2±10.2) years. The mean operation time was (76.1±23.1) min and the median bleeding volume was 150 (100, 200) mL. The postoperative course was uneventful for all the cases. Dysphagia, emergent hematoma, and deterioration of neurological function did not occur. Mean JOA scores were 13.2±2.2 before the operation and 16.3±0.8 at the final follow-up, which were significantly different (P < 0.001). The mean recovery rate of neurological function was 85.9%. By comparing the imaging examinations postoperatively and six months after the operation, we found that the average subsidence length was (1.2±1.1) mm, and that there was only one cases (9.1%) of the severe subsidence (>3 mm). We observed significant improvement of cervical lordosis after the operation (P=0.013). All the cases obtained solid fusion.
Conclusion
3D-printing stand-alone AVB presented favorable short-term outcome in one-level ACCF in this study. The fusion rate of this zero-profile prosthesis was satisfactory and the complication rate was relatively low.
Keywords: Artificial vertebral body, Stand-alone, Zero-profile, 3D-printing, Cervical spondylotic myelopathy
脊髓型颈椎病(cervical spondylotic myelopathy, CSM)为常见病,在45~60岁人群中发病率高达20%[1]。手术为CSM主要的治疗方式,依据入路不同,手术方案分为颈后路手术、颈前路手术和联合入路手术[2]。颈前路椎体次全切除减压融合手术(anterior cervical corpectomy and fusion,ACCF)是处理短节段、局限性椎管狭窄的有效方案之一,通过切除脊髓前方的椎体,实现局部“椎管扩大”,疗效确切。ACCF具有切口小、微创化、恢复快、住院时间短、并发症少等优点。椎体切除后的固定重建方式为钛笼(titanium mesh cage,TMC)植入加以钉板系统进行固定。既往研究发现,ACCF手术可提供良好的短期和长期稳定性,改善疼痛、神经功能障碍等症状[3-8]。尽管颈前路手术创伤较小,术后仍会出现颈部疼痛、吞咽困难、血肿形成甚至是植入物失败等并发症[8-9]。Lin等[10]进行病例比较发现,ACCF的植入物相关并发症发生率为9.5%,高于颈前路椎间盘切除内固定融合术。降低颈前路术后并发症的方案包括术前进行气管锻炼、术中仔细止血、缩短手术时间以及应用光滑的薄钛板或者“零切迹”植入物[11]。与常规的钉板内固定相比,单节段零切迹的椎间融合器固定融合效果相似,而颈部不适、吞咽困难的发生率显著降低[12-13]。对于ACCF而言,由于术中切除大部分椎体,对于脊柱稳定性的破坏更大,其内固定重建的要求更高,因此,在临床实践中更倾向于采取TMC加钉板系统的方式。检索国内外文献,采用单一的钛笼或人工椎体进行前柱重建的报告较少见[14],仅见Tohamy等[14]报告ACCF中单独应用可撑开假体,31例患者无一出现明显的假体沉降和颈椎曲度的丢失。
目前,3D打印技术在脊柱植入物领域大量应用[15-16]。本课题组研发一款自稳式人工椎体(artificial vertebral body,AVB),采用3D打印的工艺制备,此假体具备内嵌式的钉道及锁定结构,植入体内后不需要额外的钉板固定,实现了自稳定、零切迹效果,先期的力学分析以及动物实验结果显示,该假体具备良好的力学性能和骨融合性能[17]。本研究旨在探索3D打印自稳式AVB在临床中应用的有效性和安全性,报告其短期临床效果。
1. 资料与方法
1.1. 假体设计与制备
假体外观呈圆柱状,后方设计弧形凹槽以适应椎管形状,头尾两端分别设计内嵌的斜形钉道(图 1)。假体材质为Ti6Al4V,采用电子束熔融层叠工艺进行制备(Arcam EBM系统,Arcam公司,瑞典),详细的制备方案见Yang等[17]报道。假体的孔径为(600±200) μm,孔隙率约为70%。自稳式AVB的抗压强度和杨氏模量分别为27.6 MPa和14.2 GPa。参考颈椎正常前凸曲度以及椎体终板角度,设置假体端面倾斜角为0°、4°和8°,以便假体与终板良好的贴附。AVB的直径有12 mm、14 mm两种规格,长度20~30 mm规格以供术中选择。
图 1.
自稳式颈椎人工椎体
Stand-alone artificial vertebral body for the cervical spine
1.2. 病例选择
本研究为单臂、回顾性队列研究,选择北京大学第三医院骨科2021年11月—2022年9月的患者病例资料进行回顾性分析和随访。本研究开始前已经北京大学第三医院医学科学伦理委员会审查批准(16-09-QX-GK)。
纳入标准:(1)CSM患者;(2)脊柱退变或后纵韧带骨化等造成局限性椎管狭窄;(3)接受单节段ACCF手术,术中植入自稳式AVB;(4)术后随访6个月及以上。
排除标准:(1)既往颈椎手术者;(2)骨质疏松患者;(3)多节段ACCF或联合后路手术者;(4)随访资料不全者。遵循临床研究的牛津IDEAL(Idea, Development, Exploration, Assessment, and Long-term Follow-up)方法学原则,共有11例患者纳入本单臂探索性研究。
1.3. 手术方法
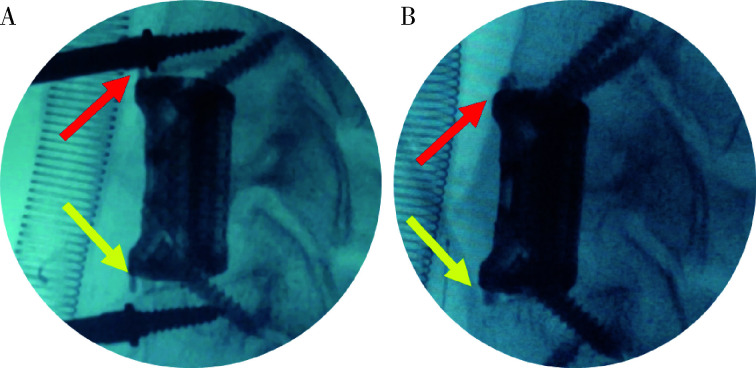
采用全身麻醉,取仰卧位,颈部及肩部垫高使颈椎呈过度后伸状态。采用颈前路横切口,完成术区显露后安装Kasper撑开器。咬除椎体前方突出之骨赘,刮除头、尾侧椎间盘,使用尖嘴咬骨钳或超声骨刀完成椎体的次全切除。止血后逐次放入试体以确定型号。植入合适假体(北京爱康宜城医疗器械有限公司),头尾侧分别斜形拧入1枚螺钉,透视检验假体位置(图 2)。位置满意后方可拧入另1枚螺钉,并锁紧。
图 2.
术中透视图像显示假体的加压作用
Fluoroscopy images during operation show the effect of compressing
A, little space presented between implant and endplates after nailing one screw; B, implant-endplate disappeared, and good attachment was achieved.
1.4. 随访
术后3个月、6个月和12个月进行随访,随访地点为北京大学第三医院门诊,随访内容包括临床症状评估、影像学检查以及患者自评量表。症状评估内容包括疼痛情况、神经功能情况、咽喉不适及吞咽情况。影像学检查包括颈椎正侧位X线片、颈椎侧位过伸过屈位X线片、CT检查以及MRI检查。患者自评量表为颈椎功能障碍指数(neck disability index,NDI)量表。
1.5. 临床资料评估
手术相关数据:包括手术时间、出血量以及围术期并发症。
临床症状数据:采用视觉模拟评分(visual analogue scale,VAS)评估疼痛情况,采用日本骨科协会(Japanese Orthopedics Association,JOA)脊髓损伤评分表(17分法)评估神经功能情况。吞咽困难的评估采用Bazaz方案[18],以严重程度分为无、轻度、中度、重度。
1.6. 影像学资料评估
依据术后6个月影像学检查评估融合情况[19]。评估内容包括假体-骨界面骨小梁长入情况、假体周围透亮影、AVB/螺钉是否移位。测量指标包括头尾端临近椎体间高度,以高度丢失情况来反映假体沉降情况,≥3 mm表示严重沉降;C2、C7下终板间角度,以表示颈椎曲度;测量颈椎过伸过屈位X线片上头尾侧椎体的骨性终板间角度的变化。以影像学所见AVB无松动和移位、假体-骨界面骨小梁长入、动力位头尾侧终板角度变化<4°定义为稳定状态,否则定义为不稳定状态[20]。当X线片无法判断时,则依据CT检查判断[21]。
1.7. 统计学分析
使用SPSS 20.0软件,采用Lilliefors检验评估计量资料的数据分布情况,符合正态分布者,数据描述为均数±标准差,不符合正态分布者,数据描述为M(min, max)。计量参数以n(%)表示。采用配对t检验比较治疗前后的效果,检验水准α值取单侧0.05。
2. 结果
2.1. 一般资料
共纳入11例患者,男性7例,女性4例,平均年龄(57.2±10.2)岁(表 1)。纳入病例的T值均≥-1(双能X线吸收法)。所有患者均接受单节段的ACCF手术,术中植入自稳式AVB。平均手术时间(76.1±23.1) min,中位出血量150(100, 200) mL。术后无血肿形成、神经功能加重等并发症出现。
表 1.
入组病例的临床资料
Clinical features of the recruited patients
| Items | Values |
| BMI, body mass index. | |
| Age/years,x±s | 57.2±10.7 |
| Gender,male/female | 7/4 |
| BMI/(kg/m2),x±s | 24.6±2.7 |
| Operative segment, n(%) | |
| C3 | 1(9.1) |
| C4 | 1 (9.1) |
| C5 | 7 (63.6) |
| C6 | 2 (18.2) |
| Operative time/min,x±s | 76.1±23.1 |
| Blood loss/mL, M(min, max) | 150 (100, 200) |
| Height loss of adjacent vertebra/mm,x±s | 1.17±1.18 |
| Severe subsidence, n(%) | 1 (9.1) |
| Solid fusion, n(%) | 11 (100) |
| Neurological recovery rate/%,x±s | 85.9±13.2 |
2.2. 临床指标变化
JOA评分由术前13.2±2.2恢复至末次随访时的16.3±0.8,差异有统计学意义(P < 0.001,表 2)。至术后6个月时,神经功能恢复率为85.9%。术后3例患者短期出现轻度咽部不适,至末次随访时均已消失;无中重度吞咽困难出现。NDI评分由术前14.2±5.2末次随访时恢复至3.4±2.1,差异有统计学意义(P < 0.001)。
表 2.
患者手术前后临床症状、颈椎曲度的变化
Changes of clinical symptoms and cervical lordosis after the operation
| Items | Preoperatively | Final follow-up | P value |
| x±s,JOA,Japanese Orthopedic Association; NDI, neck disability index. | |||
| Neck pain | 3.3±2.5 | 0.64±1.12 | 0.001 |
| JOA scores | 13.2±2.2 | 16.3±0.8 | < 0.001 |
| NDI scores | 14.2±5.2 | 3.4±2.1 | < 0.001 |
| Global lordosis angle/(°) | 10.6±9.6 | 17.0±15.4 | 0.013 |
影像学评估结果:至术后6个月时,所有病例均实现了骨性融合。假体平均沉降距离为(1.2±1.1) mm;1例假体出现超出3 mm的严重沉降(9.1%),至末次随访已实现融合。颈椎前凸角度术前为10.6°±9.6°,术后为17.0°±15.4°,较术前显著改变(P=0.013)。
2.3. 典型病例
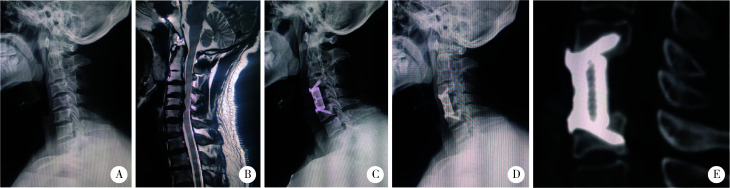
患者男,37岁,因双手麻木、不灵活于2021年12月入院。查体双手握力降低、Hoffman征(+)。术前X线片提示颈椎曲度变直、部分椎体缘及小关节增生硬化(图 3A),MRI提示多节段椎间盘突出,以C4/5、C5/6为主(图 3B)。术前诊断CSM明确,有手术指征。手术方案为颈5椎体次全切除、自稳式3D打印AVB植入。术后症状缓解满意,影像学检查显示假体位置满意,假体无沉降(图 3C、D、E),实现了骨性融合。
图 3.
典型病例显示假体实现了可靠的骨性融合
Illustrative case presents firm bony fusion at the final follow-up
A, decreased lordosis curve on lateral X-ray; B, multi-level disc herniation on magnetic resonance imaging; C, lateral X-ray before discharge; D, lateral X-ray at the final follow-up; E, sagittal reconstruction film of CT scan at the final follow-up.
3. 讨论
内固定效果直接影响ACCF手术的疗效,TMC/钉板是目前常用的固定重建方案,但仍有一定缺陷,如TMC与终板角度不适配造成严重塌陷、钛板切迹较高造成吞咽困难等[18, 22]。本研究采用3D打印技术制备设计自稳式、“零切迹”的人工椎体,术后6个月的应用效果良好,具有较高的推广价值。
3.1. 自稳式AVB的骨融合性能与TMC/钉板相似
先期研究表明[17],自稳式假体采用立体微孔设计,其微观结构模拟正常骨小梁结构,具有一定程度的生物活性,通过诱导骨长入提升融合性能。假体两端设计有不同斜面,以适应椎体终板角度。假体的固定结构为两端内嵌的斜向钉道,末端设计有独特的锁定结构。术中拧入螺钉后,通过“拉力钉”原理产生瞬时加压作用,以便假体-终板界面更好地贴附(图 2);螺钉拧入后,头尾侧螺钉呈现“八”字形态,可阻止假体向前方的移位,这些优势是传统TMC/钉板系统所不具备的。良好的贴附使得上方的载重经终板均匀的传导,避免出现终板因不均匀受力出现破裂,导致假体塌陷甚至松动移位[23]。Chen等[24]统计单中心300例ACCF病例,发现严重钛笼沉降发生率为19.0%。假体的严重沉降可导致持续颈痛、植入物松动和移位,甚至影响神经功能恢复[18]。本组病例术后随访,自稳式假体严重沉降的发生率为9.1%,优于传统TMC[23-25]。本研究显示,患者的颈椎前凸曲度得到部分恢复(表 2),假体融合率达到100%。与常规TMC比较,自稳式假体具备相似的融合性能[26]。
3.2. 自稳式假体的临床效果
本研究显示自稳式假体术后短期内JOA评分改善率达85.9%,与传统的ACCF手术的临床效果相当[3-8, 25]。手术操作方便,节省置板时间,并不增加手术时间及出血量,术后无需延长颈托的固定时间,主要并发症方面,自稳式假体组并未出现血肿形成、感染、食管瘘等严重并发症。Riley等[27]统计多中心病例,发现术后3个月仍有29.8%的患者报告不同程度的吞咽困难,其中21.3%的患者术后2年仍有症状。由于零切迹的设计,手术后食管后方并无异物挤压、摩擦,因此术后咽部不适、吞咽困难等情况较少。本研究自稳式假体组术后3例出现轻度的咽部异物感,但很快便得以缓解,考虑与气管插管、术中牵拉食管等相关[18],而并非假体刺激所致。
3.3. 自稳式假体优势分析与应用前景
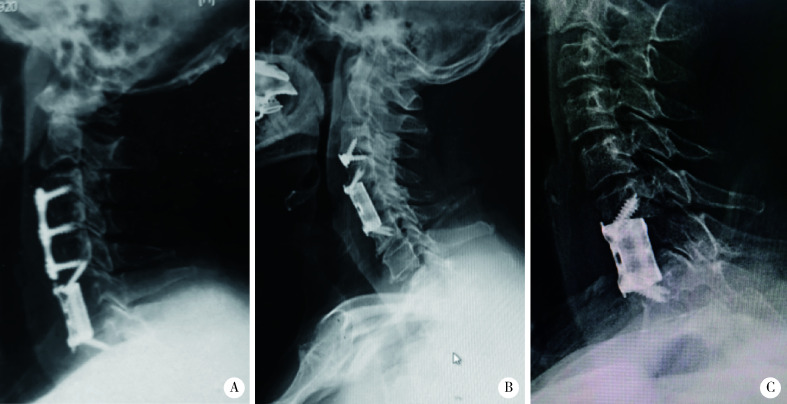
本研究证实,自稳式AVB在单节段ACCF具有较好的应用效果。传统TMC在CSM治疗中具有长期的应用经验,制备简单,成本低廉,并可通过内部填塞自体颗粒骨、异体骨或者活性骨成分增加骨性融合概率,但其缺点是两端与骨性终板贴附面小,压强集中,易造成终板骨折、塌陷,不具备自稳特点,需与钉板系统配合,术后即刻稳定性差,术后3个月内需佩戴围领、支具辅助固定。自稳式AVB相较于常规的TMC/钉板固定系统,具有自稳定优势,不影响椎前的食管、气管组织,终板贴附面大,不易造成终板骨折、假体塌陷,术后即刻稳定性好,术后仅需佩戴围领2周。在颈椎术后邻椎病的治疗中,自稳式AVB可不拆除原有的钉板系统,从而缩短手术时间、缩小操作范围、降低手术难度(图 4A)。与Zero-P等椎间融合器联合应用,可实现多节段颈椎前路的零切迹效果(图 4B)。此外,自稳式假体内部模拟正常骨小梁结构,无需填充,可应用于椎体肿瘤、感染等病例中(图 4C)。
图 4.
自稳式假体可广泛应用于邻椎病、多节段病变及脊柱肿瘤手术
Wide application of stand-alone artificial vertebral body in adjacent vertebral disease, multilevel surgery and spinal tumor surgery
A, surgery of adjacent vertebral disease; B, combination with a Zero-P cage; C, application in spinal metastatic cases.
3.4. 研究的局限性
本研究存在一定的局限性,首先,本研究为单臂、回顾性队列研究,证据等级较低;其次,本研究纳入样本量较小,统计分析结果需谨慎参考。自稳式AVB在颈椎中应用时间尚短,其应用价值和相对优势尚需大规模临床病例研究验证。
综上所述,自稳式AVB在单节段ACCF手术中的短期应用效果良好,与传统TMC相比,术后假体塌陷、咽部不适发生率低,有着良好的应用前景,但其长期应用效果仍需大规模的前瞻性病例研究来验证。
Funding Statement
北京大学第三医院临床重点孵育项目(BYSYZD2022023)
Supported by Institutional Clinical Research Incubating Projects of Peking University Third Hospital (BYSYZD2022023)
Footnotes
利益冲突 所有作者均声明不存在利益冲突。
作者贡献声明 胡攀攀:撰写论文;李彦、刘啸、唐彦超、李梓赫:修改论文;刘忠军:设计研究方案和修改论文。
References
- 1.Lv Y, Tian W, Chen D, et al. The prevalence and associated factors of symptomatic cervical spondylosis in Chinese adults: A community-based cross-sectional study. BMC Musculoskelet Disord. 2018;19(1):325. doi: 10.1186/s12891-018-2234-0. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 2.Bakhsheshian J, Mehta VA, Liu JC. Current diagnosis and management of cervical spondylotic myelopathy. Global Spine J. 2017;7(6):572–586. doi: 10.1177/2192568217699208. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 3.蔡 钦林. 颈椎病的手术治疗(一) 中国脊柱脊髓杂志. 1996;(2):42–45. [Google Scholar]
- 4.Böhler J, Gaudernak T. Anterior plate stabilization for fracture-dislocations of the lower cervical spine. J Trauma. 1980;20(3):203–205. doi: 10.1097/00005373-198003000-00002. [DOI] [PubMed] [Google Scholar]
- 5.Orozco-Declos R, Llovet-Tapies J. Osteosintesis en las fracturas del raquis cervical: Nota técnica. Rev Ortop Traumatol. 1970;14:285–288. [Google Scholar]
- 6.袁 文, 贾 连顺, 倪 斌. 前路椎体次全切除减压及带锁钢板固定治疗脊髓型颈椎病. 中华外科杂志. 2000;38(3):182–184. [Google Scholar]
- 7.毛 志国, 袁 文, 贾 连顺, et al. 钛质网笼内植物加前路带锁钢板对颈椎稳定性的生物力学评价. 中国脊柱脊髓杂志. 2001;11(6):355–357. doi: 10.3969/j.issn.1004-406X.2001.06.010. [DOI] [Google Scholar]
- 8.Qin R, Chen X, Zhou P, et al. Anterior cervical corpectomy and fusion versus posterior laminoplasty for the treatment of oppressive myelopathy owing to cervical ossification of posterior longitudinal ligament: A meta-analysis. Eur Spine J. 2018;27(6):1375–1387. doi: 10.1007/s00586-017-5451-6. [DOI] [PubMed] [Google Scholar]
- 9.Wang T, Tian XM, Liu SK, et al. Prevalence of complications after surgery in treatment for cervical compressive myelopathy: A meta-analysis for last decade. Medicine (Baltimore) 2017;96(12):e6421. doi: 10.1097/MD.0000000000006421. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 10.Lin Q, Zhou X, Wang X, et al. A comparison of anterior cervical discectomy and corpectomy in patients with multilevel cervical spondylotic myelopathy. Eur Spine J. 2012;21(3):474–481. doi: 10.1007/s00586-011-1961-9. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 11.Joaquim AF, Murar J, Savage JW, et al. Dysphagia after anterior cervical spine surgery: A systematic review of potential preventative measures. Spine J. 2014;14(9):2246–2260. doi: 10.1016/j.spinee.2014.03.030. [DOI] [PubMed] [Google Scholar]
- 12.Barbagallo GM, Romano D, Certo F, et al. Zero-P: A new zero-profile cage-plate device for single and multilevel ACDF. A single institution series with four years maximum follow-up and review of the literature on zero-profile devices. Eur Spine J. 2013;22(Suppl 6):S868–S878. doi: 10.1007/s00586-013-3005-0. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 13.Njoku I Jr, Alimi M, Leng LZ, et al. Anterior cervical discectomy and fusion with a zero-profile integrated plate and spacer device: A clinical and radiological study. J Neurosurg Spine. 2014;21(4):529–537. doi: 10.3171/2014.6.SPINE12951. [DOI] [PubMed] [Google Scholar]
- 14.Tohamy MH, Osterhoff G, Abdelgawaad AS, et al. Anterior cervical corpectomy and fusion with stand-alone cages in patients with multilevel degenerative cervical spine disease is safe. BMC Musculoskelet Disord. 2022;23(1):20. doi: 10.1186/s12891-021-04883-5. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 15.Zhou H, Liu S, Li Z, et al. 3D-printed vertebral body for anterior spinal reconstruction in patients with thoracolumbar spinal tumors. J Neurosurg Spine. 2022;25:1–9. doi: 10.3171/2022.1.SPINE21900. [DOI] [PubMed] [Google Scholar]
- 16.Hu P, Du S, Wei F, et al. Reconstruction after resection of C2 vertebral tumors: A comparative study of 3D-printed vertebral body versus titanium mesh. Front Oncol. 2022;12:1065303. doi: 10.3389/fonc.2022.1065303. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 17.Yang J, Cai H, Liu Z, et al. In vivo study of a self-stabilizing artificial vertebral body fabricated by electron beam melting. Spine (Phila Pa 1976) 2014;39(8):E486–E492. doi: 10.1097/BRS.0000000000000211. [DOI] [PubMed] [Google Scholar]
- 18.Bazaz R, Lee MJ, Yoo JU. Incidence of dysphagia after anterior cervical spine surgery: A prospective study. Spine (Phila Pa 1976) 2002;27(22):2453–2458. doi: 10.1097/00007632-200211150-00007. [DOI] [PubMed] [Google Scholar]
- 19.Kanayama M, Hashimoto T, Shigenobu K, et al. Pitfalls of anterior cervical fusion using titanium mesh and local autograft. J Spinal Disord Tech. 2003;16(6):513–518. doi: 10.1097/00024720-200312000-00005. [DOI] [PubMed] [Google Scholar]
- 20.Wei F, Xu N, Li Z, et al. A prospective randomized cohort study on 3D-printed artificial vertebral body in single-level anterior cervical corpectomy for cervical spondylotic myelopathy. Ann Transl Med. 2020;8(17):1070. doi: 10.21037/atm-19-4719. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 21.Liu Y, Qi M, Chen H, et al. Comparative analysis of complications of different reconstructive techniques following anterior decompression for multilevel cervical spondylotic myelopathy. Eur Spine J. 2012;21(12):2428–2435. doi: 10.1007/s00586-012-2323-y. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 22.Ji C, Yu S, Yan N, et al. Risk factors for subsidence of titanium mesh cage following single-level anterior cervical corpectomy and fusion. BMC Musculoskelet Disord. 2020;21(1):32. doi: 10.1186/s12891-019-3036-8. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 23.Mohammad-Shahi MH, Nikolaou VS, Giannitsios D, et al. The effect of angular mismatch between vertebral endplate and vertebral body replacement endplate on implant subsidence. J Spinal Disord Tech. 2013;26(5):268–273. doi: 10.1097/BSD.0b013e3182425eab. [DOI] [PubMed] [Google Scholar]
- 24.Chen Y, Chen D, Guo Y, et al. Subsidence of titanium mesh cage: A study based on 300 cases. J Spinal Disord Tech. 2008;21(7):489–492. doi: 10.1097/BSD.0b013e318158de22. [DOI] [PubMed] [Google Scholar]
- 25.Cheng H, Luo G, Xu D, et al. Comparison of radiological and clinical outcomes of 3D-printed artificial vertebral body with titanium mesh cage in single-level anterior cervical corpectomy and fusion: A meta-analysis. Front Surg. 2023;9:1077551. doi: 10.3389/fsurg.2022.1077551. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 26.Jiang SD, Jiang LS, Dai LY. Anterior cervical discectomy and fusion versus anterior cervical corpectomy and fusion for multilevel cervical spondylosis: A systematic review. Arch Orthop Trauma Surg. 2012;132(2):155–161. doi: 10.1007/s00402-011-1402-6. [DOI] [PubMed] [Google Scholar]
- 27.Riley LH 3rd, Skolasky RL, Albert TJ, et al. Dysphagia after anterior cervical decompression and fusion: prevalence and risk factors from a longitudinal cohort study. Spine (Phila Pa 1976) 2005;30(22):2564–2569. doi: 10.1097/01.brs.0000186317.86379.02. [DOI] [PubMed] [Google Scholar]