Abstract
目的
随着围生和新生儿重症医学的发展,极早早产儿的存活率逐年升高,但其支气管肺发育不良(bronchopulmonary dysplasia,BPD)的发病率仍逐年升高,并严重影响极早早产儿的生存预后。如何有效地防治BPD已成为新生儿科医生的关注热点。本研究分析极早早产儿BPD的临床特征,旨在为极早早产儿BPD的防治措施提供参考。
方法
回顾性纳入中南大学湘雅二医院儿科新生儿专科收治的472例极早早产儿,根据最终是否诊断为BPD分为BPD组(n=147)和非BPD组(n=325)。收集2组患儿的基本情况、母孕期资料、实验室检查结果、营养支持情况、呼吸支持模式和持续时间、各系统并发症,并比较2组患儿的临床特征。
结果
BPD组的出生胎龄、头围、体重及身长均小于、低于或短于非BPD组(均P<0.05),1 min及5 min Apgar评分、平均体重增长速度均低于非BPD组(均P<0.05);男婴、极低出生体重(very low birth weight,VLBW)及超低出生体重(extremely low birth weight,ELBW)比例均高于非BPD组(均P<0.05);BPD组患儿母亲宫颈机能不全发生率和胚胎移植技术使用率均高于非BPD组,产前激素使用率低于非BPD组(均P<0.05);BPD组患儿痰培养阳性率高于非BPD组(P<0.05),白细胞计数、中性粒细胞比值及降钙素原均高于非BPD组(均P<0.05);BPD组患儿禁食时间、微量喂养时间、全肠外营养(total parenteral nutrition,TPN)及部分肠外营养(partial parenteral nutrition,PPN)时间均长于非BPD组(P<0.05);BPD组患儿鼻导管吸氧和机械通气使用时间长于非BPD组,出生后第1、3、7、14、21、28天机械通气使用率均高于非BPD组(均P<0.05);BPD组呼吸窘迫综合征、呼吸暂停、呼吸衰竭、肺炎、肺出血、胸腔积液、持续肺动脉高压、有血流动力学意义的动脉导管未闭、巨细胞病毒感染、新生儿坏死性小肠结肠炎、胆汁淤积、贫血、病理性黄疸、血液系统异常、甲状腺功能减低、早产儿视网膜病变,以及内环境紊乱发病率均高于非BPD组(均P<0.05)。
结论
患有BPD的极早早产儿在基本情况、母孕期病史、炎症指标水平、营养支持、呼吸支持、合并症及并发症发生率方面与未患BPD的极早早产儿均存在明显差异。确保胎儿正常发育,减轻极早早产儿的炎症反应,尽早建立肠内营养,缩短机械通气时间,降低合并症及并发症的发生率有利于降低极早早产儿BPD发生率及改善BPD远期预后。
Keywords: 极早早产儿, 支气管肺发育不良, 临床特征
Abstract
Objective
With the development of perinatal and neonatal intensive care medicine, the survival rate of very premature infants increases year by year. However, the incidence of bronchopulmonary dysplasia (BPD) increases year by year, which seriously affects the survival prognosis of very premature infants. How to prevent and treat BPD effectively has become the focus of neonatologists. This study aims to provide ideas for the prevention and treatment of BPD in very preterm infants via analyzing the clinical characteristics of BPD.
Methods
A total of 472 cases of very premature infants admitted to the Divison of Neonatology, Department of Pediatrics at the Second Xiangya Hospital of Central South University were retrospectively selected and assigned into a BPD group (n=147) and a non-BPD group (n=325) according to the diagnosis of BPD. Clinical data of each group were collected to find out the clinical characteristics of BPD in very preterm infants. Basic information, maternal pregnancy data, laboratory findings, nutritional support, respiratory support patterns and duration, and systemic complications were included.
Results
Compared with the non-BPD group, gestational age, birth weight, head circumference and body length in the BPD group were lower, the Apgar score in 1st min and 5th min and average body weight growth rate were lower (all P<0.05); the ratios of male, very low birth weight (VLBW), and extremely low birth weight (ELBW) in the BPD group were higher than those in the non-BPD group (all P<0.5); the incidence of maternal cervical insufficiency and the rate of using embryo transfer technology in the BPD group were higher than those in the non-BPD group, and the rate of using prenatal hormone in the BPD group was lower than that in the non-BPD group (all P<0.05). The positive rate of sputum culture in the BPD group was higher than that in the non-BPD group (P<0.05), and the white blood cell count, neutrophil ratio, and procalcitonin in the BPD group were higher than those in the non-BPD group (all P<0.05). The period of fasting, minimal feeding, total parenteral nutrition (TPN), and partial parenteral nutrition (PPN) in the BPD group were longer than those in the non-BPD group (all P<0.05). The duration of nasal catheter oxygen inhalation and mechanical ventilation in the BPD group was longer than that in the non-BPD group, and the rates of mechanical ventilation at Day 1, 3, 7, 14, 21 and 28 after birth were higher than those in the non-BPD group (all P<0.05). The incidence of respiratory distress syndrome, apnea of prematurity, respiratory failure, pneumonia, pulmonary hemorrhage, pleural effusion, persistent pulmonary hypertension, hemodynamic patent ductus arteriosus, cytomegalovirus infection, neonatal necrotic enterocolitis, cholestasis, anemia, abnormal blood system, hypothyroidism, retinopathy of prematurity, and internal environment disorders in the BPD group were significantly higher than those in non-BPD group (all P<0.05).
Conclusion
There are significant differences between very premature infants with BPD and those without BPD in general information, maternal history, inflammatory indicators, nutritional support, respiratory support, comorbidities and complication rates. To ensure normal fetal development, reducing the inflammatory reaction of very premature infants, establishing enteral nutrition as early as possible, shortening the time of mechanical ventilation, and reducing the occurrence of complications are beneficial to decrease the incidence of BPD in very premature infants and improve the long-term prognosis of BPD.
Keywords: very preterm infants, bronchopulmonary dysplasia, clinical characteristics
支气管肺发育不良(bronchopulmonary dysplasia,BPD)是婴幼儿最常见的慢性肺部疾病,也是其神经发育障碍、长期肺部并发症和死亡的主要原因[1]。随着医学的不断发展和进步,早产儿的存活率显著提高,但BPD的患病率也随之升高,对早产儿的生存质量产生了严重影响[2]。其社会影响和经济影响需要从受损的儿童健康、生活质量、家庭压力、经济困难、社会医疗成本几方面来共同衡量[3-4]。由于大多数早产儿通过使用产前皮质类固醇、先进的新生儿诊疗护理技术、有效的呼吸支持设备和肺表面活性剂替代治疗能得以生存[5],BPD的临床特征在过去50年中已发生了很大改变。同时由于我国早产儿出生胎龄主要集中在28~32周,也就是极早早产儿,因此国外的BPD特征并不适用于国内早产儿人群。本研究收集472例极早早产儿的临床资料,对比分析非BPD患儿和BPD患儿的临床特点,为极早早产儿BPD的防治措施提供参考。
1. 资料与方法
1.1. 一般资料
选取中南大学湘雅二医院儿科新生儿专科2016年1月1日至2020年11月30日收治的472例极早早产儿作为研究对象,所有患儿根据2018年修订的诊断标准[6]进行诊断并分组。根据是否存在BPD将极早早产儿分为2组,其中BPD组147例,非BPD组325例。纳入标准:1)同院产科分娩并于生后24 h内入住新生儿专科;2)患儿出生胎龄<32周;3)住院时间>28 d。排除标准:1)严重先天畸形(如神经管缺陷、脑发育畸形、复杂紫绀型先天性心脏病、消化道畸形、食管/肛门闭锁、膈疝等);2)患有先天性遗传病或先天性代谢性疾病(如21-三体综合征、特纳综合征、苯丙酮尿症、肝豆状核变性等);3)肺或肺血管先天性发育不良;4)14日龄内死亡、在14日龄至矫正胎龄36周中非因持续性实质性肺部疾病和呼吸衰竭死亡;5)意外出院(如因经济状况或其他原因放弃治疗),或因其他疾病需手术治疗(如坏死性小肠结肠炎、脑出血等)中途转至其他医院;6)重要数据不完整者。
本研究通过中南大学湘雅二医院伦理委员会批准[审批号:(2020)临研第076号]。
1.2. 方法
回顾性收集、整理极早早产儿的病历资料,包括:1)极早早产儿基本情况;2)母亲围生期资料;3)实验室检查结果;4)营养支持情况[肠内营养(enteral nutrition,EN)、肠外营养(parenteral nutrition,PN)及每周摄入各营养素情况];5)呼吸支持模式及持续时间(第1、3、7、14、21、28天呼吸支持模式及呼吸机参数);6)住院期间各系统临床结局。
1.3. 统计学处理
采用 SPSS(Version 25.0,IBM)统计学软件对数据进行分析,符合正态分布且方差齐性的计量资料以均数±标准差( ±s)表示,组间差异分析采用独立样本t检验;不符合正态分布或方差不齐的计量资料以中位数(第1四分位数,第3四分位数)[M(P 25, P 75)]表示,组间差异分析采用Mann-Whitney U检验;计数资料用例数(百分比)[例(%)]表示,组间差异分析采用χ²检验。P<0.05为差异有统计学意义。
2. 结 果
2.1. 一般情况
本研究共纳入极早早产儿472例,其中男247例,女225例;BPD组147例,非BPD组325例,BPD发病率为31.1%。BPD组的出生胎龄、头围、体重及身长均小于、低于或短于非BPD组(P<0.05)。BPD组1 min及5 min Apgar评分、平均体重增长速度低于非BPD组(均P<0.05)。BPD组男婴、极低出生体重(very low birth weight,VLBW)、超低出生体重(extremely low birth weight,ELBW)比例高于非BPD组(均P<0.05)。但2组小于胎龄儿(small for gestational age,SGA)发生率、生理性体重下降百分数差异无统计学意义(均P>0.05,表1)。
表1.
非BPD组与BPD组患儿基本情况比较
Table 1 Comparison of general characteristics in the non-BPD group and the BPD group
| 组别 | n | 性别(男)/[例(%)] | 出生胎龄/周 | 出生体重/g | 出生头围/cm | 出生身长/cm | VLBW/[例(%)] |
|---|---|---|---|---|---|---|---|
| 非BPD组 | 325 | 160(49.2) | 30.34±1.19 | 1 451.19±281.35 | 27.51±1.83 | 38.76±3.01 | 185(56.9) |
| BPD组 | 147 | 87(59.2) | 28.13±1.84 | 1 071.37±276.30 | 25.20±2.00 | 35.12±3.19 | 136(92.5) |
| t/χ 2 | 4.29 | 15.76 | 14.31 | 12.73 | 13.41 | 68.92 | |
| P | 0.038 | <0.001 | <0.001 | <0.001 | <0.001 | <0.001 |
| 组别 | ELBW/[例(%)] | SGA/[例(%)] | 1 min Apgar评分 | 5 min Apgar评分 | 体重下降/% | 平均体重增长/(g·kg-1·d-1) |
|---|---|---|---|---|---|---|
| 非BPD组 | 16(4.9) | 11(3.4) | 7.27±1.45 | 8.85±0.92 | 9.54±4.15 | 16.17±2.86 |
| BPD组 | 65(44.2) | 11(7.5) | 5.84±1.71 | 7.80±1.33 | 10.11±4.29 | 14.26±2.71 |
| t/χ 2 | 106.51 | 3.27 | 9.68 | 10.07 | -1.26 | 6.21 |
| P | <0.001 | 0.071 | <0.001 | <0.001 | 0.209 | <0.001 |
BPD:支气管肺发育不良;VLBW:极低出生体重;ELBW:超低出生体重;SGA:小于胎龄儿;Apgar 1 min:1 min阿普加评分;Apgar 5 min:5 min阿普加评分。
2.2. 母孕期资料
BPD组患儿母亲宫颈机能不全发生率及胚胎移植技术使用率均高于非BPD组(均P<0.05),产前激素使用率低于非BPD组(P<0.05)。但在母亲年龄、妊娠期疾病发生率方面2组比较差异均无统计学意义(均 P>0.05,表2)。
表2.
非BPD组与BPD组围产期资料比较
Table 2 Comparison of perinatal conditions in the non-BPD group and the BPD group
| 组别 | n | 母亲年龄/岁 |
试管婴儿/ [例(%)] |
产前使用激素/[例(%)] | 宫颈机能不全/[例(%)] | 羊水污染/[例(%)] | 绒毛膜羊膜炎/[例(%)] |
胎膜早破/ [例(%)] |
|---|---|---|---|---|---|---|---|---|
| 非BPD组 | 325 | 31.08±5.07 | 76(23.4) | 272(83.7) | 21(6.5) | 5(1.5) | 9(2.8) | 152(46.8) |
| BPD组 | 147 | 30.71±4.72 | 48(32.7) | 102(69.4) | 19(12.9) | 7(4.8) | 10(6.8) | 63(42.9) |
| t/χ 2 | 0.775 | 4.546 | 12.123 | 5.187 | 9.84 | 3.674 | 0.598 | |
| P | 0.439 | 0.033 | <0.001 | 0.023 | 0.080 | 0.055 | 0.439 |
| 组别 | 生殖道感染/[例(%)] | 胆汁淤积/[例(%)] | 妊娠高血压/[例(%)] |
贫血/ [例(%)] |
妊娠糖尿病/[例(%)] | 胎盘异常/[例(%)] | 脐带异常/[例(%)] | 胎儿窘迫/[例(%)] |
|---|---|---|---|---|---|---|---|---|
| 非BPD组 | 81(24.9) | 25(7.7) | 65(20.0) | 47(14.5) | 91(28.0) | 70(21.5) | 55(16.9) | 15(4.6) |
| BPD组 | 35(23.8) | 7(4.8) | 30(20.4) | 28(19.0) | 44(29.9) | 32(21.8) | 21(14.3) | 6(4.1) |
| t/χ 2 | 0.108 | 1.844 | 0.024 | 1.531 | 0.120 | 0.004 | 0.652 | 0.612 |
| P | 0.743 | 0.174 | 0.877 | 0.216 | 0.729 | 0.949 | 0.419 | 0.408 |
BPD:支气管肺发育不良。
2.3. 实验室检查结果
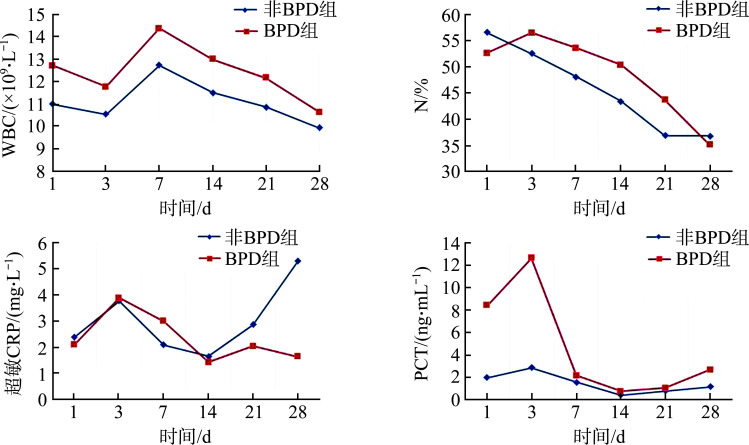
BPD组患儿白细胞计数在第7、14、21天均高于非BPD组(均P<0.05),中性粒细胞比值在第3、7、14、21天均高于非BPD组(均P<0.05),降钙素原(procalcitonin,PCT)在第1、3天均明显高于非BPD组(均P<0.05,图1)。
图1.
生后1~28 d炎症指标变化趋势
Figure 1 Changing trend of routine inflammation index from 1st to 28th postnatal day WBC: White blood cell; N: Neutrophil; CRP: C-reaction protein; PCT: Procalcitonin; BPD: Bronchopulmonary dysplasia.
BPD组患儿痰培养阳性率高于非BPD组(P<0.05)。胃液培养与血培养阳性率2组比较差异无统计学意义(P>0.05,表3)。
表3.
非BPD组与BPD组实验室检查比较
Table 3 Comparison of routine laboratory examination in the non-BPD group and the BPD group
| 组别 | n | 痰培养 | 胃液培养 |
血培养阳性/ [例(%)] |
||
|---|---|---|---|---|---|---|
| 未做/[例(%)] | 阳性/[例(%)] | 未做/[例(%)] | 阳性/[例(%)] | |||
| 非BPD组 | 325 | 109(33.5) | 56(17.2) | 163(50.2) | 24(7.4) | 29(8.9) |
| BPD组 | 147 | 14(9.5) | 78(53.1) | 75(50.1) | 10(6.8) | 16(10.9) |
| χ 2 | 60.386 | 0.095 | 0.345 | |||
| P | <0.001 | 0.954 | 0.557 | |||
BPD:支气管肺发育不良。
2.4. 营养支持情况
BPD组患儿开奶时间晚于非BPD组(P<0.05),BPD组患儿禁食时间、微量喂养时间、全肠外营养(total parenteral nutrition,TPN)及部分肠外营养(partial parenteral nutrition,PPN)时间长于非BPD组(P<0.05)。BPD组开奶奶量小于非BPD组(P<0.05,表4)。
表4.
非BPD组与BPD组营养支持情况比较( ±s)
Table 4 Comparison of nutritional supports in the non-BPD group and the BPD group ( ±s)
| 组别 | n | 开奶时间/h | 开奶奶量/[mL·kg-1·d-1] | 总禁食时间/d | 微量喂养/d |
|---|---|---|---|---|---|
| 非BPD组 | 325 | 32.66±21.49 | 11.28±3.90 | 1.97±0.29 | 3.97±3.70 |
| BPD组 | 147 | 64.74±27.56 | 9.85±4.09 | 5.75±1.30 | 6.12±5.29 |
| t/χ 2 | -4.071 | 3.318 | -7.919 | -4.679 | |
| P | <0.001 | 0.001 | <0.001 | <0.001 |
| 组别 | 平均加奶速度/(mL·kg-1·d-1) | 达全EN日龄/d | TPN时间/d | PPN时间/d |
|---|---|---|---|---|
| 非BPD组 | 11.40±3.60 | 28.23±10.76 | 1.96±0.29 | 29.18±11.82 |
| BPD组 | 10.15±3.02 | 44.47±17.29 | 5.75±1.30 | 42.83±16.84 |
| t/χ 2 | 3.354 | -11.504 | -7.949 | -9.339 |
| P | 0.001 | <0.001 | <0.001 | <0.001 |
BPD:支气管肺发育不良;EN:肠内营养;TPN:全肠外营养;PPN:部分肠外营养。
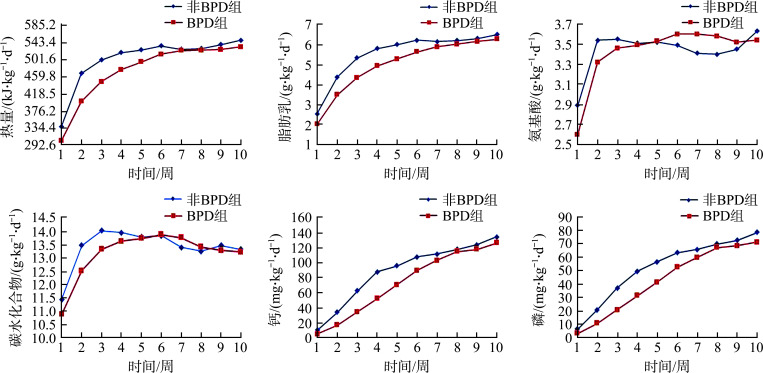
BPD组患儿出生后前6周热量及脂肪乳、钙、磷摄入量均低于非BPD组患儿(均P<0.05)。BPD组患儿出生后前2周氨基酸及碳水摄入量均低于非BPD组患儿(均P<0.05,图2)。
图2.
1~10周营养摄入情况
Figure 2 Weekly nutrient intake in two groups from 1st to 10th postnatal week BPD: Bronchopulmonary dysplasia.
2.5. 呼吸支持情况
BPD组患儿鼻导管吸氧、机械通气使用时间均长于非BPD组(均P<0.05,表5)。
表5.
在非BPD组与BPD组呼吸支持模式比较( ±s)
Table 5 Comparison of respiratory support patterns in the BPD group and the non-BPD group ( ±s)
| 组别 | n | 用氧时间/d | 鼻导管吸氧时间/d | nCPAP时间/d | 无创常频时间/d | 有创常频时间/d | 有创高频时间/d |
|---|---|---|---|---|---|---|---|
| 非BPD组 | 325 | 18.96±14.58 | 12.89±11.25 | 1.08±0.62 | 3.85±2.64 | 0.82±0.28 | 0.34±0.17 |
| BPD组 | 147 | 67.89±23.03 | 38.38±15.42 | 2.14±1.35 | 13.46±10.75 | 10.28±5.33 | 4.05±2.35 |
| t/χ 2 | -25.762 | -18.606 | -2.822 | -11.798 | -10.055 | -5.851 | |
| P | <0.001 | <0.001 | 0.005 | <0.001 | <0.001 | <0.001 |
nCPAP:经鼻持续气道正压通气。
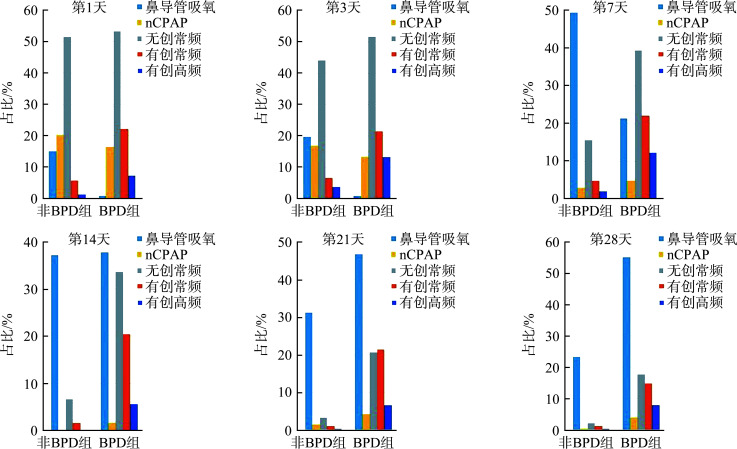
BPD组患儿生后第1、3、7、14、21、28天机械通气使用率均高于非BPD组(图3)。
图3.
1~28 d呼吸支持比较
Figure 3 Comparison of respiratory support on day 1 to 28 nCPAP: Nasal continuous positive airway pressure; BPD: Bronchopulmonary dysplasia.
2.6. 合并症及并发症
BPD组呼吸系统疾病、循环系统疾病、消化系统疾病、血液系统疾病、感染性疾病、甲状腺功能减低、早产儿视网膜病变(retinopathy of prematurity,ROP)、内环境紊乱发病率均高于非BPD组(均P<0.05)。新生儿脑病(胎龄≥35周的新生儿发生的以意识状态改变、肌张力或反射异常、惊厥等为特点的一组急性神经功能障碍的总称)、脑室内出血(intraventricular hemorrhage,IVH)、脑室周围白质软化发生率2组差异均无统计学意义(均P>0.05,表6)。
表6.
非BPD组与BPD组的并发症比较
Table 6 Comparison of complications in the BPD group and the non-BPD group
| 组别 | n | RDS/[例(%)] |
AOP/ [例(%)] |
呼吸衰竭/ [例(%)] |
肺炎/[例(%)] |
肺出血/ [例(%)] |
胸腔积液/[例(%)] |
PPHN/ [例(%)] |
|---|---|---|---|---|---|---|---|---|
| 非BPD组 | 325 | 246(75.7) | 113(34.8) | 253(77.8) | 280(86.2) | 6(1.8) | 2(0.6) | 6(1.8) |
| BPD组 | 147 | 145(98.6) | 72(49.0) | 147(100) | 141(95.9) | 26(17.7) | 11(7.5) | 14(9.5) |
| χ 2 | 32.857 | 8.576 | 38.428 | 10.414 | 40.188 | 17.824 | 14.704 | |
| P | <0.001 | 0.003 | <0.001 | 0.001 | <0.001 | <0.001 | <0.001 |
| 组别 |
hsPDA/ [例(%)] |
CMV感染/ [例(%)] |
NEC/ [例(%)] |
胆汁淤积/ [例(%)] |
新生儿脑病/[例(%)] |
IVH/ [例(%)] |
脑室周围白质软化/[例(%)] |
甲状腺功能减低/ [例(%)] |
|---|---|---|---|---|---|---|---|---|
| 非BPD组 | 16(4.9) | 20(6.2) | 7(2.2) | 13(4.0) | 323(99.4) | 191(58.8) | 2(0.6) | 2(0.6) |
| BPD组 | 26(17.7) | 25(17.0) | 22(15.0) | 20(13.6) | 147(100) | 96(65.3) | 2(1.4) | 12(8.2) |
| χ 2 | 20.342 | 13.823 | 28.813 | 14.361 | 0.908 | 1.815 | 0.669 | 20.035 |
| P | <0.001 | <0.001 | <0.001 | <0.001 | 0.341 | 0.178 | 0.413 | <0.001 |
| 组别 |
贫血/ [例(%)] |
病理性黄疸/ [例(%)] |
血小板减少症/[例(%)] | 白细胞减少症/[例(%)] |
凝血功能 异常/[例(%)] |
ROP | ||
|---|---|---|---|---|---|---|---|---|
| 复查即可/[例(%)] | 注射VEGF手术/[例(%)] | 激光手术/[例(%)] | ||||||
| 非BPD组 | 285(87.7) | 294(90.5) | 26(8.0) | 17(5.2) | 51(15.7) | 48(14.8) | 6(1.8) | 0(0.0) |
| BPD组 | 143(97.3) | 143(97.3) | 40(27.2) | 23(15.6) | 46(31.3) | 52(35.4) | 7(4.8) | 4(2.7) |
| χ 2 | 11.005 | 6.852 | 31.058 | 14.157 | 15.087 | 37.386 | ||
| P | 0.001 | 0.009 | <0.001 | 0.001 | <0.001 | <0.001 | ||
| 组别 | 低蛋白血症/[例(%)] | 氮质血症/[例(%)] | 代谢性酸中毒/[例(%)] | 代谢性碱中毒/[例(%)] |
高血糖/ [例(%)] |
低血糖/ [例(%)] |
低钙血症/[例(%)] | 低镁血症/[例(%)] | 低磷血症/[例(%)] |
|---|---|---|---|---|---|---|---|---|---|
| 非BPD组 | 92(28.3) | 99(30.5) | 67(20.6) | 1(0.3) | 40(12.3) | 75(23.1) | 129(39.7) | 16(4.9) | 9(2.8) |
| BPD组 | 70(48.3) | 88(59.9) | 46(31.3) | 4(2.7) | 67(45.6) | 48(32.7) | 95(64.6) | 29(19.7) | 11(7.5) |
| χ 2 | 16.745 | 36.578 | 6.337 | 5.625 | 63.912 | 4.817 | 25.235 | 25.772 | 5.543 |
| P | <0.001 | <0.001 | 0.012 | 0.018 | <0.001 | 0.028 | <0.001 | <0.001 | 0.019 |
新生儿脑病;RDS:呼吸窘迫综合征;AOP:早产儿呼吸暂停;PPHN:持续肺动脉高压;hsPDA:有血流动力学意义的动脉导管未闭;CMV:巨细胞病毒;NEC:新生儿坏死性小肠结肠炎;IVH:脑室内出血;ROP:早产儿视网膜病变;VEGF:血管内皮生长因子。
3. 讨 论
随着新生儿科医生对BPD认识的逐渐加深,BPD的防治取得了一定的成效,但其发病率仍持续升高。多中心研究[7]表明,我国2017年极早早产儿的BPD发病率为28.5%。本研究根据美国国立儿童健康与人类发育研究所(National Institute of Child Health and Human Development,NICHD)2018年诊断标准,得出极早早产儿BPD发病率为31.1%。极早早产儿BPD发病率的升高可能导致该人群临床特点发生变化。本研究显示BPD组患儿母亲胚胎移植技术使用率高于非BPD组,产前激素使用率则低于非BPD组。医学技术的发展及对疾病的认知,一方面解决了部分不孕难题,并预防了部分BPD的发生;另一方面却增加了BPD的发生风险。这可能是极早早产儿临床特点变化的部分原因。
BPD的发生是肺发育可塑性、损伤和异常修复共同作用的结果[3]。
本研究显示:BPD组的出生胎龄、头围、体重、身长均小于、低于或短于非BPD组,且BPD组VLBW、ELBW比例更高。这与BPD的发生、发展相吻合。人类肺发育分为5个阶段[8],极早早产儿肺发育处于小管期至囊泡期,此期是肺组织从不具有气体交换功能到有潜在交换功能的过渡期。若在此期早产,肺组织将受到不成熟及初始肺损伤的双重挑战,出生胎龄及出生体重越小,肺发育越不成熟,初始肺损伤程度越重,BPD越容易发生。
目前认为宫内感染及出生后感染在BPD发病中起重要作用。本研究显示母亲羊水污染发生率、绒毛膜羊膜炎、胎膜早破、生殖道感染2组发生率差异无统计学意义,这与李文丽等[9]研究结果一致。但也有研究[10]表明绒毛膜羊膜炎、胎盘感染或不正常的定植会引发并加重BPD的发展。国内对此问题并未有统一结论,但感染和炎症在BPD发病机制中的作用已引起人们的广泛关注[11]。本研究显示:BPD组患儿炎症指标明显高于非BPD组患儿。BPD组患儿痰液培养阳性率更高,且多为革兰氏阴性杆菌,如肺炎克雷伯菌、流感嗜血杆菌等,这与既往研究[12]一致。故应积极治疗原发感染,预防呼吸机相关性肺炎等医院感染发生,避免肺部继续损伤。
在本研究中,BPD组患儿机械通气使用时间较长,且接受有创机械通气的患儿发展为BPD的比例更高,提示呼吸支持模式的选择及其持续时间是BPD发生、发展的重要预测指标。早产儿出生后前2周会出现3种肺部疾病模式[13-19]:第1种模式,婴儿的肺部疾病极少并逐渐康复;第2种模式为早期持续性肺部恶化(early persistent pulmonary deterioration,EPPD),从出生开始就需要大量和长期的呼吸支持;第3种模式,出生后第1周内肺部疾病最初得到改善,随后出现肺部恶化,需要机械通气,并且用氧浓度升高。近50%的肺部恶化患儿和近70%的EPPD患儿病情最后会进展为BPD[20]。极早早产儿往往出现第3种模式,需要频繁的呼吸支持,同时也是对肺部的继续损伤。为了减少BPD的发生,建议选用适宜且安全的呼吸支持模式帮助患儿过渡。
肺发育、损伤、修复都与营养息息相关,早期营养供给不足是BPD发生的重要影响因素,与其发生、发展和最终临床结局密切相关,优化营养支持可降低BPD发生率和减轻其严重程度,对促进患儿肺发育和神经系统预后至关重要[21]。本研究早产儿入院时均统一采取积极的营养策略[22],但与非BPD组相比,BPD组患儿受多方面因素的影响,其禁食时间、微量喂养时间、TPN及PPN时间更长。早期的低能量喂养可导致肺泡数量减少[23],从而增加BPD的发生风险。中国《早产儿支气管肺发育不良营养管理专家共识》[24]关于能量摄入的推荐如下:潜在BPD患儿在出生后1周能量需达334~418 kJ/(kg·d),4周内逐渐增至502~627 kJ/(kg·d),以降低BPD的发生风险。本研究结果显示BPD组患儿出生后1周摄入能量仅为(301.55±46.44) kJ/(kg·d),出生后4周为(474.68±93.72) kJ/(kg·d),低于上述专家共识推荐的标准。黄希等[25]研究表明ELBW患儿喂养不耐受发生率为88.89%。因此,极早早产儿通常难以满足积极的营养策略。早产儿出生后早期液体超负荷是BPD的危险因素[26],临床医师应谨慎协调患儿液体摄入量与营养摄入之间的关系,尽量避免患儿早期发生营养不良。早期积极进行营养支持、仔细调整肠外营养及适当地进行肠内喂养可能会加快BPD早产儿的生长,并促进其神经功能的更好发育[27],从而改善BPD的预后。
本研究中BPD组患儿呼吸窘迫综合征(respiratory distress syndrome,RDS)、早产儿呼吸暂停(apnea of prematurity,AOP)、呼吸衰竭、肺炎、肺出血、气胸、胸腔积液、持续肺动脉高压(persistent pulmonary hypertension,PPHN)、有血流动力学意义的动脉导管未闭(hemodynamic patent ductus arteriosus,hsPDA)[28]、巨细胞病毒(cytomegalovirus,CMV)感染、新生儿坏死性小肠结肠炎(neonatal necrotic enterocolitis,NEC)、贫血、ROP,以及酸碱电解质紊乱发病率更高,RDS、AOP、肺出血、气胸等可延长极早早产儿呼吸支持时间,从而造成早期肺损伤及肺修复的反复发生,使极早早产儿的肺部疾病模式向第3种模式转变,最终导致BPD的发生。肺炎、CMV感染、NEC带来的全身炎症反应影响肺血管的通透性,从而阻止早产儿肺的肺泡化。同时,发生NEC需禁食或减少喂养处理,致使患儿营养摄入不足,可导致BPD的发生。PPHN及hsPDA引起的肺循环血量增加也可增加极早早产儿BPD的易感性。但BPD与非BPD患儿的新生儿脑病[29]、脑室内出血、脑室周围白质软化等神经系统并发症发生率无明显差异,这可能与患儿所在科室的营养策略有关,早期积极营养支持、仔细调整的肠外营养及个体化精细管理为降低神经系统并发症发生率起到了积极作用。
本研究为单中心回顾性分析,后续研究可在不同地区选择不同级别的医院进行多中心、大样本的研究,或进行动物实验及实验室的基础研究,获得更严谨的数据,以更准确地了解极早早产儿BPD的特点。
综上所述,患有BPD的极早早产儿在一般情况、母孕期病史、炎症指标水平、营养支持、呼吸支持、合并症及并发症发生率等方面与正常极早早产儿存在显著差异。确保胎儿正常发育,减轻极早早产儿的炎症反应,尽早建立肠内营养,缩短机械通气时间,减少合并症及并发症的发生有利于降低极早早产儿BPD发生率及改善BPD的远期预后。
基金资助
中南大学湘雅临床大数据系统建设项目(No.56)。
This work was supported by the Xiangya Clinical Big Data System Construction Project, China (No.56).
利益冲突声明
作者声称无任何利益冲突。
作者贡献
杨勇晖 研究设计,数据分析,论文撰写与修改;贺晓日 研究设计,论文指导及修改;张雪菲 数据采集;陈平洋 论文指导。所有作者阅读并同意最终的文本。
原文网址
http://xbyxb.csu.edu.cn/xbwk/fileup/PDF/2023101592.pdf
参考文献
- 1. Leigh RM, Pham A, Rao SS, et al. Machine learning for prediction of bronchopulmonary dysplasia-free survival among very preterm infants[J]. BMC Pediatr, 2022, 22(1): 542. 10.1186/s12887-022-03602-w. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 2. 高旭, 朱梦茹, 焦冬香. 不同程度支气管肺发育不良早产儿的临床特征[J]. 临床医学研究与实践, 2023, 8(3): 83-85. 10.19347/j.cnki.2096-1413.202303023. [DOI] [Google Scholar]; GAO Xu, ZHU Mengru, JIAO Dongxiang. Clinical characteristics of premature infants with different degree of bronchopulmonary dysplasia[J]. Clinical Research and Practice, 2023, 8(3): 83-85. 10.19347/j.cnki.2096-1413.202303023. [DOI] [Google Scholar]
- 3. Thébaud B, Goss KN, Laughon M, et al. Bronchopulmonary dysplasia[J]. Nat Rev Dis Primers, 2019, 5: 78. 10.1038/s41572-019-0127-7. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 4. Greenberg RG, Gayam S, Savage D, et al. Furosemide exposure and prevention of bronchopulmonary dysplasia in premature infants[J/OL]. J Pediatr, 2019, 208: 134-140. e2[2023-05-01]. 10.1016/j.jpeds.2018.11.043 [DOI] [PMC free article] [PubMed] [Google Scholar]
- 5. Dankhara N, Holla I, Ramarao S, et al. Bronchopulmonary dysplasia: Pathogenesis and pathophysiology[J]. J Clin Med, 2023, 12(13): 4207. 10.3390/jcm12134207. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 6. Higgins RD, Jobe AH, Koso-Thomas M, et al. Bronchopulmonary dysplasia: executive summary of a workshop[J]. JPediatr, 2018, 197: 300-308. 10.1016/j.jpeds.2018.01.043. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 7. 江苏省新生儿重症监护病房母乳质量改进临床研究协作组 . 多中心回顾性分析极低及超低出生体重儿支气管肺发育不良的临床特点及高危因素[J]. 中华儿科杂志, 2019, 57(1): 33-39. 10.3760/cma.j.issn.0578-1310.2019.01.009. [DOI] [Google Scholar]; Breast Milk Improvement in NICU Clinical Research Collaboration Group of Jiangsu Province . Clinical characteristics and risk factors of very low birth weight and extremely low birth weight infants with bronchopulmonary dysplasia: multicenter retrospective analysis[J]. Chinese Journal of Pediatrics, 2019, 57(1): 33-39. 10.3760/cma.j.issn.0578-1310.2019.01.009. [DOI] [PubMed] [Google Scholar]
- 8. 常立文, 李文斌. 胎儿和新生儿肺发育 [J]. 实用儿科临床杂志, 2011, 26(14): 1065-1067. 10.3969/j.issn.1003-515X.2011.14.001. [DOI] [Google Scholar]; CHANG Liwen, LI Wenbin. Fetal and neonatal lung development[J]. Chinese Journal of Applied Clinical Pediatrics, 2011, 26(14): 1065-1067. 10.3969/j.issn.1003-515X.2011.14.001. [DOI] [Google Scholar]
- 9. 李文丽, 徐发林, 牛铭, 等. 不同程度支气管肺发育不良早产儿的临床特征及预后分析[J]. 中国当代儿科杂志, 2018, 20(4): 261-266. 10.7499/j.issn.1008-8830.2018.04.002. [DOI] [PMC free article] [PubMed] [Google Scholar]; LI Wenli, XU Falin, NIU Ming, et al. Clinical features and prognosis of preterm infants with varying degrees of bronchopulmonary dysplasia[J]. Chinese Journal of Contemporary Pediatrics, 2018, 20(4): 261-266. 10.7499/j.issn.1008-8830.2018.04.002. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 10. Hundscheid TM, Huizing MJ, Villamor E, et al. Association of funisitis with short-term outcomes of prematurity: a frequentist and bayesian Meta-analysis[J]. Antioxidants (Basel), 2023, 12(2): 534. 10.3390/antiox12020534. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 11. Ou W, Lei K, Wang H, et al. Development of a blood proteins-based model for bronchopulmonary dysplasia prediction in premature infants[J]. BMC Pediatr, 2023, 23(1): 304. 10.1186/s12887-023-04065-3. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 12. 任艳丽, 孔祥永, 杜志方, 等. 不同程度支气管肺发育不良早产儿的临床及影像学特点[J]. 中国当代儿科杂志, 2015, 17(5): 440-444. 10.7499/j.issn.1008-8830.2015.05.005. [DOI] [PubMed] [Google Scholar]; REN Yanli, KONG Xiangyong, DU Zhifang, et al. Clinical and imaging features of premature infants with different degrees of bronchopulmonary dysplasia[J]. Chinese Journal of Contemporary Pediatrics, 2015, 17(5): 440-444. 10.7499/j.issn.1008-8830.2015.05.005. [DOI] [PubMed] [Google Scholar]
- 13. Laughon M, Bose C, Allred EN, et al. Antecedents of chronic lung disease following three patterns of early respiratory disease in preterm infants[J]. Arch Dis Child Fetal Neonatal Ed, 2011, 96(2): F114-F120. 10.1136/adc.2010.182865. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 14. Dylag AM, Kopin HG, O’Reilly MA, et al. Early neonatal oxygen exposure predicts pulmonary morbidity and functional deficits at 1 year[J/OL]. J Pediatr, 2020, 223: 20-28. e2[2023-05-01]. 10.1016/j.jpeds.2020.04.042. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 15. Panickar J, Scholefield H, Kumar Y, et al. Atypical chronic lung disease in preterm infants[J]. J Perinat Med, 2004, 32(2): 162-167. 10.1515/JPM.2004.029. [DOI] [PubMed] [Google Scholar]
- 16. Choi CW, Kim BI, Koh YY, et al. Clinical characteristics of chronic lung disease without preceding respiratory distress syndrome in preterm infants[J]. Pediatr Int, 2005, 47(1): 72-79. 10.1111/j.1442-200x.2004.01996.x. [DOI] [PubMed] [Google Scholar]
- 17. Choi CW, Kim BI, Park JD, et al. Risk factors for the different types of chronic lung diseases of prematurity according to the preceding respiratory distress syndrome[J]. Pediatr Int, 2005, 47(4): 417-423. 10.1111/j.1442-200x.2005.02081.x. [DOI] [PubMed] [Google Scholar]
- 18. Streubel AH, Donohue PK, Aucott SW. The epidemiology of atypical chronic lung disease in extremely low birth weight infants[J]. J Perinatol, 2008, 28(2): 141-148. 10.1038/sj.jp.7211894. [DOI] [PubMed] [Google Scholar]
- 19. Nobile S, Marchionni P, Vento G, et al. New insights on early patterns of respiratory disease among extremely low gestational age newborns[J]. Neonatology, 2017, 112(1): 53-59. 10.1159/000456706. [DOI] [PubMed] [Google Scholar]
- 20. Laughon M, Allred EN, Bose C, et al. Patterns of respiratory disease during the first 2 postnatal weeks in extremely premature infants[J]. Pediatrics, 2009, 123(4): 1124-1131. 10.1542/peds.2008-0862. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 21. Lignelli E, Palumbo F, Myti D, et al. Recent advances in our understanding of the mechanisms of lung alveolarization and bronchopulmonary dysplasia[J]. Am J Physiol Lung Cell Mol Physiol, 2019, 317(6): L832-L887. 10.1152/ajplung.00369.2019. [DOI] [PubMed] [Google Scholar]
- 22. 蔡威, 汤庆娅, 王莹, 等. 中国新生儿营养支持临床应用指南[J]. 临床儿科杂志, 2013, 31(12): 1177-1182. 10.3969/j.issn.1000-3606.2013.11.020. [DOI] [Google Scholar]; CAI Wei, TANG Qingya, WANG Ying, et al. Guidelines for clinical application of neonatal nutritional support in China[J]. Journal of Clinical Pediatrics, 2013, 31(12): 1177-1182. 10.3969/j.issn.1000-3606.2013.11.020. [DOI] [Google Scholar]
- 23. Karatza AA, Gkentzi D, Varvarigou A. Nutrition of infants with bronchopulmonary dysplasia before and after discharge from the neonatal intensive care unit[J]. Nutrients, 2022, 14(16): 3311. 10.3390/nu14163311. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 24. 张蓉, 林新祝, 常艳美, 等. 早产儿支气管肺发育不良营养管理专家共识[J]. 中国当代儿科杂志, 2020, 22(8): 805-814. 10.7499/j.issn.1008-8830.2005080. [DOI] [PMC free article] [PubMed] [Google Scholar]; ZHANG Rong, LIN Xinzhu, CHANG Yanmei, et al. Expert consensus on nutritional management of preterm infants with bronchopulmonary dysplasia[J]. Chinese Journal of Contemporary Pediatrics, 2020, 22(8): 805-814. 10.7499/j.issn.1008-8830.2005080. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 25. 黄希, 陈琼, 彭文涛. 早产儿喂养不耐受的临床特征及其危险因素[J]. 中南大学学报(医学版), 2018, 43(7): 797-804. 10.11817/j.issn.1672-7347.2018.07.016. [DOI] [PubMed] [Google Scholar]; HUANG Xi, CHEN Qiong, PENG Wentao. Clinical characteristics and risk factors for feeding intolerance in preterm infants [J]. Journal of Central South University. Medical Science, 2018, 43(7): 797-804. 10.11817/j.issn.1672-7347.2018.07.016. [DOI] [PubMed] [Google Scholar]
- 26. 徐儒政,孙斌,赵乃琤. 早期肠外营养与早产儿支气管肺发育不良发生的关系[J]. 中国当代儿科杂志, 2023, 25(4): 362-367. https:// 10.7499/j.issn.1008-8830.2210128 [DOI] [PMC free article] [PubMed] [Google Scholar]; XU Ruzheng, SUN Bin, ZHAO Naicheng. Association between early parenteral nutrition and the development of bronchopulmonary dysplasia in preterm infants[J]. Chinese Journal of Contemporary Pediatrics, 2023, 25(4): 362–367. 10.7499/j.issn.1008-8830.2210128. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 27. Dani C, Poggi C. Nutrition and bronchopulmonary dysplasia [J]. The Journal of Maternal-Fetal & Neonatal Medicine, 2012, 25(S3): 37-40. 10.3109/14767058.2012.712314. [DOI] [PubMed] [Google Scholar]
- 28. Dudley S, SenShawn, Hanson A, et al. The role of furosemide and fluid management for a hemodynamically significant patent ductus arteriosus in premature infants[J]. J Perinatol, 2022, 42(12): 1703-1707. 10.1038/s41372-022-01450-1. [DOI] [PubMed] [Google Scholar]
- 29. 黄秀清, 程国强. 新生儿脑病: 多病因识别 [J]. 中国小儿急救医学, 2021, 28(8): 649-653. 10.3760/cma.j.issn.1673-4912.2021.08.002. [DOI] [Google Scholar]; HUANG Xiuqing, CHENG Guoqiang. Neonatal encephalopathy: identification of multiple causes [J]. Chinese Pediatric Emergency Medicine, 2021, 28(8): 649-653. 10.3760/cma.j.issn.1673-4912.2021.08.002. [DOI] [Google Scholar]