Abstract
宫腔粘连(intrauterine adhesion,IUA)是由于子宫内膜基底层受损导致内膜纤维化形成粘连,以致宫腔部分或全部闭塞,从而导致月经异常、不孕或反复流产。近年来IUA患病率呈上升趋势,且中重度IUA的高复发率使IUA治疗更具挑战性。医源性子宫内膜损伤是IUA的主要病因,但在临床上接受过类似宫腔操作的患者中,IUA发病与否以及IUA的严重程度也不尽相同,因此IUA的发生可能存在其他的协同作用因素。IUA发病机制与生殖道微生物群存在一定的关联性,在许多IUA患者中都观察到阴道内乳杆菌等益生菌显著减少,加德纳菌和普雷沃氏菌等病原菌过度生长。生殖道微生物群能通过影响免疫功能和代谢来参与IUA的发生和发展。
Keywords: 宫腔粘连, 生殖道微生物群, 免疫反应, 细胞因子
Abstract
Intrauterine adhesion (IUA) is caused by damage of the basal layer of endometrium, which leads to fibrosis of the endometrium and the formation of adhesion, resulting in partial or complete occlusion of the uterine cavity, abnormal menstruation, infertility or recurrent miscarriage. The prevalence of IUA in women has been increasing in recent years, and the high recurrence rate of moderate to severe IUA makes IUA treatment more challenging. Iatrogenic endometrial injury is the main cause of IUA. However, the incidence of IUA and the severity of IUA vary among patients who have received similar uterine operations, suggesting that there may be other synergistic factors in the development of IUA. There is a certain correlation between the pathogenesis and the microbiota of the gential tract. In many IUA patients, it has been observed that the probiotics such as Lactobacillus in the vagina is significant reduced, and the pathogenic bacteria such as Gardnerella and Prevotella are excessive growth. The reproductive tract microbiota can be involved in the development and progression of IUA via impacting immune function and metabolism.
Keywords: intrauterine adhesion, reproductive tract microbiota, immune response, cytokine
宫腔粘连(intrauterine adhesion,IUA)又称Asherman综合征,是一种获得性子宫疾病,其特征是宫腔内形成瘢痕组织。在许多情况下,瘢痕组织会导致对立子宫内膜的粘连。当受损子宫内膜表面出现纤维和炎性渗出时,粘连开始形成且逐渐发展为更加致密的纤维带,最终演变成大量粘连。IUA可导致宫腔部分或全部闭塞、影响子宫内膜血流与容受性、缩小胚胎着床面积而不利于胚胎生长。IUA的常见临床表现包括月经过少、闭经、反复流产和继发性不孕等[1]。近年来IUA患病率呈上升趋势,且IUA的高复发率严重影响了女性生育力,使得中重度IUA治疗更具挑战性。
IUA的病因是多方面的,Hooker等[2]提出刮宫等医源性子宫内膜损伤是IUA最重要的原因,其他原因包括生殖器结核、骨盆放射治疗和子宫手术(包括肌瘤摘除和子宫畸形矫治手术等),但这不能完全解释粘连形成的机制。临床上,并不是所有宫腔操作史的女性均会发生IUA,而少数无宫腔操作史的女性也可能会发生IUA,可见IUA的发生可能存在其他的协同作用因素。
以往的研究[3-5]讨论了导致纤维化的特定免疫途径和免疫细胞因子。然而,很少有学者直接研究在IUA的形成过程中,IUA与生殖道微生物及其诱导的免疫反应之间的关系。许多研究[6-8]表明:女性生殖道的微生物群在维持女性生殖系统的健康状态和疾病的发展过程中起着重要作用,而生殖道菌群失调会导致多种疾病,如产后子宫内膜炎、早产、盆腔炎、自然流产、分娩低出生体重儿等。IUA与其他纤维化受损的组织器官病因和进展机制相似,由此推测生殖道微生物群与IUA的发生具有相关性。组织损伤和微生态失衡不仅促进炎症的发生,而且通过激活先天性免疫和获得性免疫系统,释放大量促炎和促进纤维化的细胞因子。此外,IUA的病理改变还会影响子宫的生理和代谢产物,从而影响生殖道微生物群的多样性。本文对目前IUA和生殖道微生物群之间的关联和相互作用进行归纳和分析,旨在为其诊疗和预防提供新的思路。
1. 正常生殖道微生物群
女性生殖道微生物群是指定植在女性阴道、宫颈、宫腔等部位的微生物集合。同时,这些微生物的基因和基因组、产物与生殖道环境共同组成了女性生殖道微生物组。
1.1. 正常阴道微生物群构成
阴道微生物群是寄居于女性阴道所有微生物有机体的总称,包括细菌、病毒和真菌等。Diop等[9]对目前PubMed/Medline数据库中报道的在人阴道中分离或基于分子手段发现的581种细菌进行了分类,发现它们分布在10个门,主要是放线菌门(Actinobacteria)、拟杆菌门(Bacteroidetes)、厚壁菌门(Firmicutes)和变形菌门(Proteobacteria),共分为96个科,206个属。而真菌的种类较细菌少,分布在3个门,包括子囊菌门(Ascomycota)、担子菌门(Basidiomycota)、卵菌门(Oomycota)。常见的真菌包括念珠菌(Candida)、曲霉(Aspergillus)等[10-11]。
正常阴道菌群以乳杆菌为优势菌。阴道常见的乳杆菌的丰度与稳定性对维持阴道微环境健康和抑制不利因素方面具有非常重要的作用。1892年Albert等从健康妊娠妇女阴道内首次培养并分离到一种产生乳酸的革兰氏阳性菌。直到1928年才通过生化反应将其命名为嗜酸乳杆菌。刘朝晖等[12]在对5 236例主诉无外阴瘙痒且无外阴、阴道充血表现的妇女阴道微生态检测实验中发现:菌群正常的样本中菌群密集度大多为Ⅱ级和Ⅲ级,占97.7%;多样性多为Ⅱ级和Ⅲ级,占94.6%;优势菌以革兰氏阳性菌(即乳杆菌)为主,占99.9%。Ravel等[13]通过对392例无症状育龄期妇女阴道微生物群进行16S rRNA基因序列的进一步分析,发现73%阴道菌群落由一种或多种乳杆菌主导,这与运用传统分离技术鉴定阴道菌群得到的结论一致,并进一步将阴道菌群分为类型I[卷曲乳杆菌(Lactobacillus crispatus)(26.2%)]、II[加氏乳杆菌(Lactobacillus gasseri)(6.3%)]、III[惰性乳杆菌(Lactobacillus iners)(34.1%)]、IV[病原菌为主(28.1%)]和Ⅴ[詹氏乳杆菌(Lactobacillus jensenii)(5.3%)]5类。研究[14-17]表明:卷曲乳杆菌、加氏乳杆菌、詹氏乳杆菌等大多数乳杆菌都是益生菌,卷曲乳杆菌可以抑制多种阴道致病菌的黏附和增殖,加氏乳杆菌可以抑制病原菌的定植,詹氏乳杆菌也表现出了良好的抑菌、抗菌作用。惰性乳杆菌分泌过氧化氢和乳酸能力弱,其抵抗病原体的能力较其他乳杆菌明显低下,且与阴道菌群失调和细菌性阴道病存在一定的关系[18]。最新研究[19]发现惰性乳杆菌的生长依赖于半胱氨酸,通过联合使用半胱氨酸抑制剂与甲硝唑,可以抑制惰性乳杆菌,并增加卷曲乳杆菌的丰度。表明惰性乳杆菌的半胱氨酸依赖性是阴道菌群调控的潜在治疗目标。
1.2. 正常宫腔微生物群构成
在依赖分离培养技术研究菌群的时代,宫腔一直被认为是无菌的。但高通量测序技术的出现克服了宫腔样本生物量少、菌群难于培养的巨大障碍,为研究宫腔微生物群落开辟了新的可能。此外,随之发展的宏基因组技术更是将研究对象扩大到整个微生物组所有的DNA,在获得微生物群落的物种组成信息的同时,更能从中获得有关微生物群潜在的功能信息[20]。研究者[21]通过对女性生殖道微生物功能基因组学的研究,在生殖道菌群与育龄期女性生育相关疾病的关系上取得了多种进展。目前大多研究[22-23]表明宫腔菌群以乳杆菌为主导,同时也含有链球菌科(Streptococcaceae)及双歧杆菌科(Bifido-bacteriaceae)。但具体到宫腔菌群组成方面,不同研究的结果并不一致,如Moreno等[24]认为乳杆菌属(Lactobacillus spp.)在子宫内膜菌群中仍占比最高,此外也存在如双歧杆菌属(Bifidobacterium)、加德纳氏菌属(Gardnerella)、普雷沃氏菌属(Prevotella)、链球菌属(Streptococcus)等;但Chen等[25]检测到宫腔的含菌量仅为阴道的万分之一,乳杆菌属并非主要菌群,而假单胞菌属(Pseudomonas)、不动杆菌属(Acinetobacter)等占据了较大的构成比例。与阴道菌群不同的是,宫腔菌群种类呈高多样性和低生物量,且呈轻度弱碱性。
由于子宫腔菌群与阴道菌群的组成呈现出一定的一致性但又有差异,对于宫腔微生物的来源目前仍有较大争议。部分研究者[26]认为阴道和宫腔菌群差异是因为不同细菌侵入宫颈的能力不同,也有其他研究者[27]认为子宫腔菌群可能来源于下生殖道菌群上行,或胃肠道菌群迁移至其他部位的血行传播等。Wang等[28]的最新研究通过比较微生物组数据阐明了宫腔和阴道菌群存在交互和共变的特征,进一步通过动物模型和菌群移植实验发现了阴道菌群及特定细菌种类对子宫内膜组织的破坏性或保护性作用,提出通过操纵阴道微生态来保护宫腔健康的新思路。
2. 生殖道微生物群与IUA的相关性
女性生殖道微生态的平衡对健康起着关键作用。越来越多的证据[23, 29-30]表明:子宫内膜微生物群的组成和分布的变化与子宫内膜息肉、子宫内膜癌和不孕症等子宫内膜疾病有关。此外,器官纤维化与微生物群失衡有关[31]。
2.1. 阴道微生物群与IUA的相关性
女性阴道微生态是由阴道微生物菌群、内分泌调节系统、阴道解剖结构及局部黏膜免疫共同组成的一种生态系统,其中阴道微生物菌群的平衡在维持阴道微生态稳定中发挥重要作用。阴道菌群失调的发病机制不尽相同,但它们的共同点包括优势乳杆菌的减少、损失和厌氧菌属增多,从而损伤了阴道对于内源性或外源性微生物的增殖和入侵的保护屏障[32-34]。阴道微生态失调将引起阴道的清洁度、pH值发生变化,从而诱发阴道炎,同时也为内源性及外源性病原的上行性感染创造了有利条件,导致盆腔炎的发生,并进一步导致IUA[35]。
植枝福等[36]在对于100例IUA患者和100例健康女性阴道菌群结构的研究中发现:IUA患者的阴道微生态失调检出率为48%,高于对照组健康女性的31%,差异有统计学意义。Liu等[37]发现IUA对阴道细菌种类与数量影响不大,但在门水平上,IUA组的厚壁菌门(乳杆菌属厚壁菌门)明显低于正常组,而放线菌门和拟杆菌门的比例明显高于正常组;在属水平上IUA组乳杆菌属显著减少,加德纳菌属和普雷沃氏菌属等过度生长。赵田等[38]将IUA患者更细致地划分为轻度、中度和重度粘连,结果表明随着IUA的程度加重,菌群密集度、多样性和乳杆菌为优势菌的比例较宫腔正常对照组更低,非乳杆菌与真菌检出率逐渐增加,因此,菌群的数量、种类及各种菌落间活菌数的异常变化会增加IUA的发病风险。
2.2. 宫腔微生物群与IUA相关性
迄今为止,关于IUA患者子宫内膜菌群结构和分布的报道较少。Qiu等[39]的研究表明:IUA患者和无宫内病变不孕患者的宫腔内子宫内膜微生物群不同,子宫内膜微生物群的潜在差异可能导致IUA的发生。在门水平上,优势菌包括变形菌门(占64.48%以上)、厚壁菌门、拟杆菌门和放线菌门。在属水平上,IUA患者中克雷伯氏菌属(Klebsiella)、希瓦氏菌属(Shewanella)和乳杆菌属的比例高于非IUA女性(分别为20.67%和8.77%,13.37%和4.53%,12.74%和6.95%),而不动杆菌属的比例显著降低,这可能与惰性乳杆菌属增多和不同采样位点等因素相关。此外,该研究还表明微生物群落的构成结构随着IUA严重水平的不同而不同。如轻度IUA患者菌群明显区别于健康对照组,这表明微生物群可能在子宫内膜纤维化的早期发挥作用。
值得注意的是,IUA患者子宫内膜克雷伯氏菌的数量显著高于对照组,该菌主要富集于轻度 IUA 队列。克雷伯氏菌是一种肠杆菌科中的革兰氏阴性杆菌,是一种典型的条件病原体[40]。克雷伯氏菌菌株可以产生毒力因子(如脂多糖),它可作用于Toll样受体4(Toll-like receptor 4,TLR4),异常激活核因子κB(nuclear factor kappa-B,NF-κB)通路,使肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)、白细胞介素-1A(interleukin-1A,IL-1A)和许多促炎因子、抗炎因子的表达增加,开启炎症级联反应,从而诱导纤维化和炎症[41]。TLR4在子宫内膜炎症中具有重要作用[42]。Liu等[43]的研究表明LPS诱导的子宫内膜感染在IUA的发生中发挥了重要作用。因此,子宫内膜克雷伯菌可能参与了IUA的发生。但具体的作用机制需要进一步的实验加以验证,同时也应当注意宫腔微生物取材过程中的污染问题。
3. 生殖道微生物群对IUA机制的影响
3.1. IUA发病机制
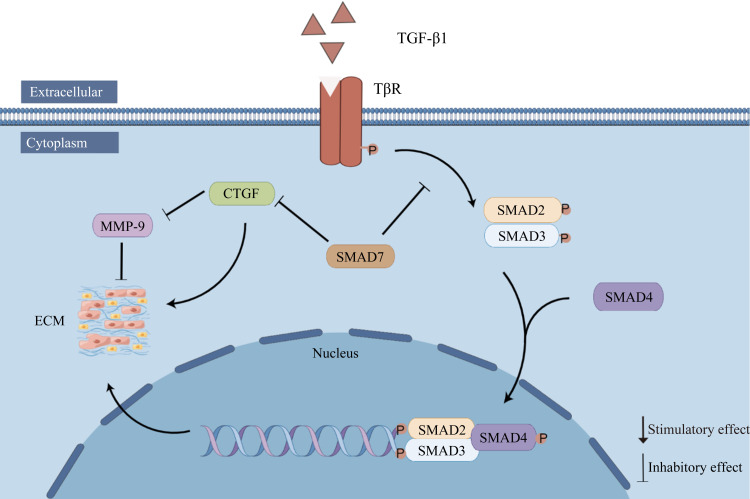
转化生长因子-β1(transforming growth factor-β1,TGF-β1)是生长因子超家族的一部分。TGF-β1通过激活SMAD(small mothers against decapentaplegic)蛋白依赖性与非依赖性途径参与细胞增殖、分化、凋亡及炎症浸润过程,也在上皮间质转化(epithelial-mesenchymal transition,EMT)和纤维化中起重要作用。SMAD蛋白家族是TGF-β1通路下游的底物分子,当TGF-β1与受体结合后,可以通过一系列反应诱导SMAD2蛋白和SMAD3蛋白磷酸化,二者磷酸化后和SMAD4蛋白结合形成三聚体复合物,并被转移到细胞核内与其他因子一起调控特定基因的表达。SMAD3可以直接与胶原蛋白启动子区域结合,促进胶原蛋白的表达;还可以抑制成纤维细胞中基质金属蛋白酶-1(matrix metalloproteinases-1,MMP-1)的活性,从而抑制细胞外基质(extracellular matrix,ECM)的降解。SMAD7蛋白作为抑制调控因子,具有通过竞争性结合TGF-β受体I而阻断该受体磷酸化SMAD2和SMAD3的作用,还能通过促进TGF-β受体降解,抑制TGF-β1通路的信号转导。目前研究[5]认为:TGF-β1/SMAD信号通路不但介导了肾、肺、肝、心等多种重要器官的纤维化,还与IUA的发病有着密不可分的关系(图1)。
图1.
IUA中TGF-β1/SMAD信号通路(本图由Figdraw绘制)
Figure 1 TGF-β1/SMAD signaling pathways in IUA (drawn by Figfraw) TGF-β1: Transforming growth factor-β1; TβR: Transforming growth factor-β receptor; SMAD: Small mothers against decapentaplegic; CTGF: Connective tissue growth factor; MMP: Matrix metalloproteinase; ECM: Extracellular matrix; P: Phosphorylation.
Salma等[5]研究发现IUA患者和实验动物模型中的TGF-β1和SMAD3蛋白质表达量高于对照组,而SMAD7基因表达水平则显著降低。因此,推测TGF-β1/SMAD3/SMAD7信号通路是IUA发病的主要调节因子。Chen等[44]发现IUA组织中激酶插入区受体(kinase insert domain containing receptor,KDR)的表达明显高于正常组织,并且KDR的表达与IUA的严重程度呈正相关。Niu等[45]通过使用中药调肾通络方下调SMAD2、SMAD3与SMAD4基因的表达水平,并且上调SMAD7基因使得TGF-β1/SMAD通路促纤维化功能受到抑制,从而降低了大鼠IUA损伤模型中子宫内膜组织的纤维化水平,这充分说明了TGF-β1/SMAD通路对于IUA发病的重要性。
目前,研究[46]表明TGF-β1/SMAD通路的激活与微RNA(microRNA,miRNA)的异常表达密切相关。Li等[47]发现:在大鼠IUA模型的子宫内膜组织中,Ⅰ型胶原Α1(collagen type I alpha 1,COL1A1)、α-平滑肌肌动蛋白(α smooth muscle actin,α-SMA)、结缔组织生长因子(connective tissue growth factor,CTGF)和转录因子SP1的表达增加,而E-钙黏蛋白和miR-29的表达减少。且该研究进一步发现miR-29可通过下调TGF-β1/SMAD-CTGF途径抑制组织纤维化,此结论在人类子宫内膜基质细胞实验中也得到了再一次验证。Ning等[48]使用微阵列评估IUA患者子宫内膜组织和正常子宫内膜组织的miR表达谱,并验证了miR-326可通过抑制TGF-β1/SMAD3途径抑制子宫内膜纤维化,故miR-29b和miR-326已成为IUA治疗和进一步研究的潜在候选基因。
在NF-κB通路中,NF-κB蛋白家族可以选择性地与B细胞κ-轻链增强子结合,调控相关基因的表达。TLR4是TLR家族的重要成员,在识别病原相关分子模式后能够引起NF-κB抑制蛋白(inhibitor of nuclear factor kappa B,IκB)磷酸化,从而激活NF-κB。活化的NF-κB从胞浆三聚体中释放出来,进入细胞核并发挥调节基因表达的作用。在IUA组织中NF‐κB 通路的异常激活参与了IUA的纤维化进展。
各类胶原保持适当数量和比例,是维持平滑肌正常功能的必要条件。IUA组织中存在明显的胶原代谢异常,主要表现为胶原清除减少和异常沉积。NF‐κB通路即通过影响参与胶原代谢调控相关的蛋白酶来促进纤维化的发生。解整合素金属蛋白酶(a disintegrin and metalloproteinase,ADAM)15和ADAM17是两种兼具解整合素活性的金属蛋白酶,一方面通过其解整合素的活性促进血小板聚集、抑制纤维蛋白原水解并增强组织粘连的强度,另一方面通过其蛋白酶活性促进细胞外基质中胶原的异常水解,并在此基础上发生异常沉积,形成组织粘连[3]。MMP9是具有强大水解活性的胶原水解酶,可水解细胞外基质的胶原。尿激酶型纤溶酶原激活剂(urokinase-type plasminogen activator,uPA)和纤溶酶原激活剂抑制 剂-1(plasminogen activator inhibitor-1,PAI-1)则是一对功能相反的分子,前者促进纤维蛋白水解并阻碍组织粘连的形成,后者抑制纤维蛋白水解并促进组织粘连的形成[4]。IUA组织中ADAM15、ADAM17、PAI-1的mRNA表达量明显增加且与TLR4/NF‐κB呈正相关,uPA的mRNA表达量明显减少且与TLR4/NF‐κB呈负相关。这一结果提示TLR4/NF‐κB通路的激活能够影响蛋白酶的活力,促进胶原的异常水解、沉积,抑制纤维蛋白的水解,从而促进组织纤维化并发生IUA。
NF-κB信号通路与纤维化中TGF-β表达之间存在一定相关性。有研究[49-50]显示:IUA子宫内膜中NF-κB信号通路表达升高程度与TGF-β的表达呈正相关。其机制为通过IL-1b等促炎细胞因子激活NF-κB通路,促进NF-κB的p65亚基移位到细胞核,并结合到TGF-β启动子上,从而诱导上皮细胞中TGF-β的表达。
3.2. 生殖道微生物失调在IUA发生机制中的作用
IUA发生的主要原因包括流产刮宫术、产后刮宫术、子宫肌瘤切除术和子宫内膜切除术等医源性创伤[51],这些创伤会引起阴道组织损伤和病理性细菌入侵。创伤和细菌的感染不但介导了代谢产物变化与炎症反应,还影响阴道乳杆菌丰度与菌群成分,从而改变pH值并促进致病菌群在阴道的定植[52],造成阴道菌群失调。研究显示阴道菌群的失调不但会促进炎症的发生,还可通过菌群代谢物等成分招募巨噬细胞和中性粒细胞等并激活免疫系统,从而产生大量促炎症和促纤维化细胞因子,经过TGF-β1/SMAD信号通路和NF-κB信号通路等介导,从而导致IUA的发生[53]。
感染是导致IUA的原因之一,子宫内膜炎性反应在IUA发生过程中的作用逐渐被人们重视[54]。一项动物实验[43]发现:机械损伤联合子宫内膜感染较单纯机械损伤更易于建立稳定的IUA动物模型,组织损伤和细菌失衡不仅能促进炎症,而且通过招募和激活先天性免疫系统和获得性免疫系统,释放大量促炎和促纤维化细胞因子。当细菌感染时,辅助性T细胞1(helper T cell 1,Th1)反应会导致大量促炎症细胞因子的释放,以清除病原体。同时,释放一系列细胞因子[包括IL-25、IL-33、胸腺基质淋巴细胞生成素(thymic stromal lymphopoietin,TSLP)、IL-25],其中IL-33和TSLP由受损的上皮细胞释放,而其他细胞因子可以直接或间接地促进Th2免疫反应的发展,从而促进纤维化。
子宫内膜损伤破坏了表面屏障的功能,增加了共生细菌或其产物进入子宫内膜,导致炎症反应和纤维化修复的加重。免疫Th细胞根据功能不同可分为Th1细胞和Th2细胞2个亚群,它们在Th反应中起着重要作用。对于炎症性疾病,Th1表达较弱,而Th2表达较强,导致Th1与Th2失衡。受损的子宫内膜上皮细胞释放一系列免疫细胞因子,可直接或间接地促进Th2免疫反应的发展,从而促进纤维化。在大多数微生物入侵的情况下,随着乳杆菌等级和乳酸浓度降低,一些促炎细胞因子[如IL-6、IL-1、IL-8和肿瘤坏死因子-α(tumor necrosis factor,TNF-α)]会释放出来,促进纤维化。细胞因子IL-6可提高Th1细胞存活率,促进干扰素-γ(interferon-gamma,IFN-γ)的产生,而负反馈则可降低MMP活性。
免疫细胞通过感知微环境的变化在损伤修复中发挥重要作用。在最新的一项研究[55]中,通过将携带可募集免疫细胞促进组织再生修复的趋化因子12 (chemokine 12,CXCL12)基因的质粒MG36e(plasmid MG36e,pMG36e)转化到细菌中,构建了工程化的卷曲乳杆菌菌株,并干预患有或不患有糖尿病的IUA小鼠,结果表明阴道应用L.crispatus-pMG36e-mCXCL12菌株可显著降低IUA小鼠血清和子宫组织中促炎因子IL-1b和TNF-α的水平,并可抑制子宫组织中的炎症因子信号通路(TLR4/NF-κB)和纤维化信号通路(TGF-β1/SMAD)。高通量测序结果进一步表明:用L.crispatus-pMG36e-mCXCL12菌株处理大大增加了乳杆菌属的丰度,并减少了致病性克雷伯氏菌的数量,L.crispatus-pMG36e-mCXCL12可显著改善了糖尿病小鼠子宫腔的纤维化和炎症,并可恢复糖尿病小鼠的阴道内微生物群的平衡。因而推测 L.crispatus-pMG36e-mCXCL12菌株阴道给药可通过恢复微生物平衡,减少手术引起的炎症和纤维化,有效缓解IUA,提示工程菌株在人类疾病治疗中具有潜在的临床应用价值。
此外,研究[56]表明真菌微生物群对IUA发展具有重要影响,通过16S rRNA、真菌内部转录间隔区(internal transcribed spacer,ITS)测序,并结合动物实验的机制研究表明,近平滑念珠菌可通过下调NF-κB和IL-6而防止IUA进展过程中的炎症活动和纤维化,并能调节细菌微生物群,因而不仅丰富了生殖道微生物群在IUA发生机制中的作用,而且还为通过靶向真菌群预防IUA提供了潜在的干预策略。
综上所述,生殖道微生物群失衡是形成IUA的重要危险因素。促炎细胞因子IL-6和IFN-γ在IUA患者中大量增加,可促进纤维化,从而引起纤维蛋白原积累、细胞外基质沉积,最终诱导IUA。
4. 结 语
微生物在介导炎症/免疫反应、触发相关途径等方面发挥着重要作用,这已成为当前研究的热点。IUA发病机制复杂,严重危害育龄妇女的生殖健康。因此,研究IUA的发病机制,寻找有效的治疗方法具有重要意义。目前,对生殖道微生物的研究多聚焦于阴道菌群,而缺乏对上生殖道菌群的研究。因而,上生殖道菌群构成、菌群功能、异常微生态与疾病的关系等仍待进一步探索。为了更好地保护女性生育力,应当对导致女性生育力下降的菌群病理性转变进行进一步研究,以明确健康女性和IUA患者上生殖道微生物群的构成差异,并在此基础上予以相应的干预。此外,微生物群失调与疾病的因果关系尚未确立,仍需大量研究来证实具体菌群改变与特定疾病的关系及发生机制。随着微生物组研究的深入,联合多组学数据探究人体微生物群和疾病之间的作用机制,可为疾病的精准干预提供理论基础。
生殖道菌群失调可导致子宫内膜炎症和炎症因子或相关细胞因子的大量释放。促炎症细胞因子IL-6和IFN-γ在纤维化中发挥作用,可导致纤维蛋白原积聚、细胞外基质沉积,最终促进IUA。全面了解微生物和免疫功能将能更好地阐明微生物和免疫功能在IUA中的作用。
生殖道微生态失衡的发病机制不尽相同,但它们的共同点包括优势乳杆菌的减少和损失,降低了阴道对于内源性或外源性微生物的增殖和入侵的保护屏障。宫腔操作前密切关注患者阴道微生态情况,可以降低IUA可能发生的风险。此外,IUA治疗后复发也是临床棘手的问题,IUA的复发与治疗前后阴道微生态变化的相关性应是今后研究的方向之一,即从生殖道微生物群失衡介导Th1/Th2失衡的新视角,揭示IUA的发病机制。此外,通过抑制病原体、炎症因子和细胞因子可以成功地预防纤维化。上述发现为针对微生物和细胞因子干预的IUA防治提供了新的研究方向。
基金资助
湖南省自然科学基金(2021JJ40956)。
This work was supported by the Natural Science Foundation of Hunan Province, China (2021JJ40956).
利益冲突声明
作者声称无任何利益冲突。
作者贡献
赵子童、郑艺、刘颖、赵思怡、尧烁意 文献查阅及整理,论文撰写;毛雪涛 论文审阅及论文修改; 徐大宝、赵行平 论文构想、写作指导及校正。所有作者阅读并同意最终的文本。
原文网址
http://xbyxb.csu.edu.cn/xbwk/fileup/PDF/2022111495.pdf
参考文献
- 1. Vomstein K, Voss P, Molnar K, et al. Two of a kind? Immunological and clinical risk factors differ between recurrent implantation failure and recurrent miscarriage[J]. J Reprod Immunol, 2020, 141: 103166. 10.1016/j.jri.2020.103166. [DOI] [PubMed] [Google Scholar]
- 2. Hooker AB, Lemmers M, Thurkow AL, et al. Systematic review and meta-analysis of intrauterine adhesions after miscarriage: prevalence, risk factors and long-term reproductive outcome[J]. Hum Reprod Update, 2014, 20(2): 262-278. 10.1093/humupd/dmt045. [DOI] [PubMed] [Google Scholar]
- 3. 付青, 卢秀琴, 王延明, 等. 宫腔粘连分子机制的研究进展[J]. 临床与实验病理学杂志, 2019, 35(9): 1079-1081. 10.13315/j.cnki.cjcep.2019.09.015. [DOI] [Google Scholar]; FU Qing, LU Xiuqin, WANG Yanming, et al. Research progress on molecular mechanism of intrauterine adhesion[J]. Chinese Journal of Clinical and Experimental Pathology, 2019, 35(9): 1079-1081. 10.13315/j.cnki.cjcep.2019.09.015. [DOI] [Google Scholar]
- 4. 靳灵鸽, 李珊珊, 郑萍, 等. 宫腔粘连组织中TLR4/NF-κB通路功能改变与细胞因子分泌、胶原代谢特征的相关性[J]. 海南医学院学报, 2019, 25(1): 33-36. 10.13210/j.cnki.jhmu.20181204.001. [DOI] [Google Scholar]; JIN Lingge, LI Shanshan, ZHENG Ping, et al. Correlation of changes of TLR4/NF-κB pathway function in intrauterine adhesion tissue with characteristics of cytokine secretion and collagen metabolism[J]. Journal of Hainan Medical University, 2019, 25(1): 33-36. 10.13210/j.cnki.jhmu.20181204.001. [DOI] [Google Scholar]
- 5. Salma U, Xue M, Ali Sheikh MS, et al. Role of transforming growth factor-beta1 and Smads signaling pathway in intrauterine adhesion[J]. Mediators Inflamm, 2016, 2016: 4158287. 10.1155/2016/4158287. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 6. Al-Nasiry S, Ambrosino E, Schlaepfer M, et al. The interplay between reproductive tract microbiota and immunological system in human reproduction[J]. Front Immunol, 2020, 11: 378. 10.3389/fimmu.2020.00378. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 7. Kalia N, Singh J, Kaur M. Microbiota in vaginal health and pathogenesis of recurrent vulvovaginal infections: A critical review[J]. Ann Clin Microbiol Antimicrob, 2020, 19(1): 5. 10.1186/s12941-020-0347-4. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 8. Smith SB, Ravel J. The vaginal microbiota, host defence and reproductive physiology[J]. J Physiol, 2017, 595(2): 451-463. 10.1113/JP271694. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 9. Diop K, Dufour JC, Levasseur A, et al. Exhaustive repertoire of human vaginal microbiota[J]. Hum Microb J, 2019, 11: 100051. 10.1016/j.humic.2018.11.002. [DOI] [Google Scholar]
- 10. Zheng NN, Guo XC, Lv W, et al. Characterization of the vaginal fungal flora in pregnant diabetic women by 18S rRNA sequencing[J]. Eur J Clin Microbiol Infect Dis, 2013, 32(8): 1031-1040. 10.1007/s10096-013-1847-3. [DOI] [PubMed] [Google Scholar]
- 11. Guo R, Zheng N, Lu H, et al. Increased diversity of fungal flora in the vagina of patients with recurrent vaginal candidiasis and allergic rhinitis[J]. Microb Ecol, 2012, 64(4): 918-927. 10.1007/s00248-012-0084-0. [DOI] [PubMed] [Google Scholar]
- 12. 刘朝晖, 张岱, 赵敏, 等. 5 236例健康妇女阴道微生态状况的分析[J]. 现代妇产科进展, 2009, 18(2): 129-131. 10.13283/j.cnki.xdfckjz.2009.02.013. [DOI] [Google Scholar]; LIU Zhaohui, ZHANG Dai, ZHAO Min, et al, The microecological evaluation of vaginal micro flora in the women without vaginal infections[J]. Progress in Obstetrics and Gynecology, 2009, 18(2): 129-131. 10.13283/j.cnki.xdfckjz.2009.02.013. [DOI] [Google Scholar]
- 13. Ravel J, Gajer P, Abdo Z, et al. Vaginal microbiome of reproductive-age women[J]. Proc Natl Acad Sci USA, 2011, 108(Suppl1): 4680-4687. 10.1073/pnas.1002611107. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 14. Ojala T, Kankainen M, Castro J, et al. Comparative genomics of Lactobacillus crispatus suggests novel mechanisms for the competitive exclusion of Gardnerella vaginalis[J]. BMC Genomics, 2014, 15: 1070. 10.1186/1471-2164-15-1070. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 15. Castro J, Henriques A, Machado A, et al. Reciprocal interference between Lactobacillus spp. and Gardnerella vaginalis on initial adherence to epithelial cells[J]. Int J Med Sci, 2013, 10(9): 1193-1198. 10.7150/ijms.6304. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 16. Zhang Z, Lv J, Pan L, et al. Roles and applications of probiotic Lactobacillus strains[J]. Appl Microbiol Biotechnol, 2018, 102(19): 8135-8143. 10.1007/s00253-018-9217-9. [DOI] [PubMed] [Google Scholar]
- 17. Antonio MA, Hawes SE, Hillier SL. The identification of vaginal Lactobacillus species and the demographic and microbiologic characteristics of women colonized by these species[J]. J Infect Dis, 1999, 180(6): 1950-1956. 10.1086/315109. [DOI] [PubMed] [Google Scholar]
- 18. Vaneechoutte M. Lactobacillus iners, the unusual suspect[J]. Res Microbiol, 2017, 168(9/10): 826-836. 10.1016/j.resmic.2017.09.003. [DOI] [PubMed] [Google Scholar]
- 19. Bloom SM, Mafunda NA, Woolston BM, et al. Cysteine dependence of Lactobacillus iners is a potential therapeutic target for vaginal microbiota modulation[J]. Nat Microbiol, 2022, 7(3): 434-450. 10.1038/s41564-022-01070-7. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 20. Marchesi JR, Ravel J. The vocabulary of microbiome research: a proposal[J]. Microbiome, 2015, 3: 31. 10.1186/s40168-015-0094-5. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 21. Benner M, Ferwerda G, Joosten I, et al. How uterine microbiota might be responsible for a receptive, fertile endometrium[J]. Hum Reprod Update, 2018, 24(4): 393-415. 10.1093/humupd/dmy012. [DOI] [PubMed] [Google Scholar]
- 22. Miles SM, Hardy BL, Merrell DS. Investigation of the microbiota of the reproductive tract in women undergoing a total hysterectomy and bilateral salpingo-oopherectomy[J]. Fertil Steril, 2017, 107(3): 813-820. https://www.fertstert.org/article/S0015-0282(16)63028-5/fulltext. [DOI] [PubMed] [Google Scholar]
- 23. Moreno I, Simon C. Relevance of assessing the uterine microbiota in infertility[J]. Fertil Steril, 2018, 110(3): 337-343. 10.1016/j.fertnstert.2018.04.041. [DOI] [PubMed] [Google Scholar]
- 24. Moreno I, Codoner FM, Vilella F, et al. Evidence that the endometrial microbiota has an effect on implantation success or failure[J]. Am J Obstet Gynecol, 2016, 215(6): 684-703. 10.1016/j.ajog.2016.09.075. [DOI] [PubMed] [Google Scholar]
- 25. Chen C, Song X, Wei W, et al. The microbiota continuum along the female reproductive tract and its relation to uterine-related diseases[J]. Nat Commun, 2017, 8(1): 875. 10.1038/s41467-017-00901-0. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 26. Hansen LK, Becher N, Bastholm S, et al. The cervical mucus plug inhibits, but does not block, the passage of ascending bacteria from the vagina during pregnancy[J]. Acta Obstet Gynecol Scand, 2014, 93(1): 102-108. 10.1111/aogs.12296. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 27. Baker JM, Chase DM, Herbst-Kralovetz MM. uterine microbiota: Residents, tourists, or invaders?[J]. Front Immunol, 2018, 9: 208. 10.3389/fimmu.2018.00208. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 28. Wang J, Li Z, Ma X, et al. Translocation of vaginal microbiota is involved in impairment and protection of uterine health[J]. Nat Commun, 2021, 12(1): 4191. 10.1038/s41467-021-24516-8 [DOI] [PMC free article] [PubMed] [Google Scholar]
- 29. Fang RL, Chen LX, Shu WS, et al. Barcoded sequencing reveals diverse intrauterine microbiomes in patients suffering with endometrial polyps[J]. Am J Transl Res, 2016, 8(3): 1581-1592. [PMC free article] [PubMed] [Google Scholar]
- 30. Walther-Antonio MR, Chen J, Multinu F, et al. Potential contribution of the uterine microbiome in the development of endometrial cancer[J]. Genome Med, 2016, 8(1): 122. 10.1186/s13073-016-0368-y. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 31. Beraza N. Fibrosis and the intestinal microbiome; a focus on chronic liver disease[J]. Curr Opin Pharmacol, 2019, 49: 76-81. 10.1016/j.coph.2019.09.012. [DOI] [PubMed] [Google Scholar]
- 32. Kovachev SM. Obstetric and gynecological diseases and complications resulting from vaginal dysbacteriosis[J]. Microb Ecol, 2014, 68(2): 173-184. 10.1007/s00248-014-0414-5. [DOI] [PubMed] [Google Scholar]
- 33. Van De Wijgert J. The vaginal microbiome and sexually transmitted infections are interlinked: Consequences for treatment and prevention[J/OL]. PLoS Med, 2017, 14(12): e1002478 [2022-01-20]. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5744905/. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 34. Witkin SS, Linhares IM. Why do lactobacilli dominate the human vaginal microbiota?[J]. BJOG, 2017, 124(4): 606-611. 10.1111/1471-0528.14390. [DOI] [PubMed] [Google Scholar]
- 35. 薛凤霞, 王宝晨, 王辰. 下生殖道感染诊治中面临的问题与挑战[J]. 中国妇产科临床杂志, 2016, 17(6): 481-482. 10.13390/j.issn.1672-1861.2016.06.001. [DOI] [Google Scholar]; XUE Fengxia, WANG Baochen, WANG Chen. Problems and challenges in the diagnosis and treatment of lower genital tract infections[J]. Chinese Journal of Clinical Obstetrics and Gynecology, 2016, 17(6): 481-482. 10.13390/j.issn.1672-1861.2016.06.001. [DOI] [Google Scholar]
- 36. 植枝福, 蒋晓莉, 周卓琳, 等. 阴道菌群结构分析在宫腔粘连患者中的临床意义[J]. 中国微生态学杂志, 2018, 30(9): 1076-1078. 10.13381/j.cnki.cjm.201809020. 30130237 [DOI] [Google Scholar]; ZHI Zhifu, JIANG Xiaoli, ZHOU Zhuolin, et al. Clinical significance of vaginal bacterial flora evaluation in patients with intrauterine adhesions[J]. Chinese Journal of Microecology, 2018, 30(9): 1076-1078. 10.13381/j.cnki.cjm.201809020. [DOI] [Google Scholar]
- 37. Liu Z, Kong Y, Gao Y, et al. Revealing the interaction between intrauterine adhesion and vaginal microbiota using highthroughput sequencing[J]. Mol Med Rep, 2019, 19(5): 4167-4174. 10.3892/mmr.2019.10092. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 38. 赵田, 周群英. 阴道微生态指标与宫腔粘连的相关性[J]. 中国计划生育学杂志, 2021, 29(7): 1475-1479. 10.3969/j.issn.1004-8189.2021.07.038. [DOI] [Google Scholar]; ZHAO Tian, ZHOU Qunying. The association bewteen vaginal microecological indexes and interuterine adhesions[J]. Chinese Journal of Family Planning, 2021, 29(7): 1475-1479. 10.3969/j.issn.1004-8189.2021.07.038. [DOI] [Google Scholar]
- 39. Qiu T, Liu L, Zhou H, et al. Analysis of endometrial microbiota in intrauterine adhesion by high-throughput sequencing[J]. Ann Transl Med, 2021, 9(3): 195. 10.21037/atm-20-2813. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 40. Bengoechea JA, Sa Pessoa J. Klebsiella pneumoniae infection biology: living to counteract host defences[J]. FEMS Microbiol Rev, 2019, 43(2): 123-144. 10.1093/femsre/fuy043. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 41. Clegg S, Murphy CN. Epidemiology and virulence of Klebsiella pneumoniae [J]. Microbiol Spectr, 2016, 4(1): UTI-0005-2012. 10.1128/microbiolspec.UTI-0005-2012. [DOI] [PubMed] [Google Scholar]
- 42. Yun BH, Chon SJ, Choi YS, et al. Pathophysiology of endometriosis: Role of high mobility group Box-1 and Toll-like receptor 4 developing inflammation in endometrium[J/OL]. PLoS One, 2016, 11(2): e0148165 [2022-01-20]. https://www.ncbi.nlm.nih.gov/pmc/articles/ PMC4752230/. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 43. Liu F, Zhu ZJ, Li P, et al. Creation of a female rabbit model for intrauterine adhesions using mechanical and infectious injury[J]. J Surg Res, 2013, 183(1): 296-303. 10.1016/j.jss.2012.11.009. [DOI] [PubMed] [Google Scholar]
- 44. Chen JX, Yi XJ, Gu PL, et al. The role of KDR in intrauterine adhesions may involve the TGF-beta1/Smads signaling pathway[J/OL]. Braz J Med Biol Res, 2019, 52(10): e8324 [2022-01-20]. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6787948/. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 45. Niu H, Miao X, Zhan X, et al. Tiaoshen Tongluo attenuates fibrosis by modulating the TGF-beta1/Smad pathway in endometrial stromal cells and a rat model of intrauterine adhesion[J]. Evid Based Complement Alternat Med, 2021, 2021: 6675329. 10.1155/2021/6675329. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 46. Zhang J, Jiang P, Tu Y, et al. Identification and validation of long non-coding RNA associated ceRNAs in intrauterine adhesion[J]. Bioengineered, 2022, 13(1): 1039-1048. 10.1080/21655979.2021.2017578. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 47. Li J, Cen B, Chen S, et al. MicroRNA-29b inhibits TGF-beta1-induced fibrosis via regulation of the TGF-beta1/Smad pathway in primary human endometrial stromal cells[J]. Mol Med Rep, 2016, 13(5): 4229-4237. 10.3892/mmr.2016.5062. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 48. Ning J, Zhang H, Yang H. MicroRNA326 inhibits endometrial fibrosis by regulating TGFbeta1/Smad3 pathway in intrauterine adhesions[J]. Mol Med Rep, 2018, 18(2): 2286-2292. 10.3892/mmr.2018.9187. [DOI] [PubMed] [Google Scholar]
- 49. Xue X, Chen Q, Zhao G, et al. The overexpression of TGF-beta and CCN2 in intrauterine adhesions involves the NF-kappaB signaling pathway[J/OL]. PLoS One, 2015, 10(12): e0146159 [2022-01-20]. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4697802/. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 50. Zhu HY, Ge TX, Pan YB, et al. Advanced role of hippo signaling in endometrial fibrosis: Implications for intrauterine adhesion[J]. Chin Med J (Engl), 2017, 130(22): 2732-2737. 10.4103/0366-6999.218013. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 51. Leung RK, Lin Y, Liu Y. Recent advances in understandings towards pathogenesis and treatment for intrauterine adhesion and disruptive insights from single-cell analysis[J]. Reprod Sci, 2021, 28(7): 1812-1826. 10.1007/s43032-020-00343-y. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 52. Donders GG, Bosmans E, Dekeersmaecker A, et al. Pathogenesis of abnormal vaginal bacterial flora[J]. Am J Obstet Gynecol, 2000, 182(4): 872-878. 10.1016/s0002-9378(00)70338-3. [DOI] [PubMed] [Google Scholar]
- 53. Zhao X, Zhao Q, Zhu X, et al. Study on the correlation among dysbacteriosis, imbalance of cytokine and the formation of intrauterine adhesion[J]. Ann Transl Med, 2020, 8(4): 52. 10.21037/atm.2019.11.124. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 54. 丘甜美, 何援利, 蔡慧华. 子宫内膜炎性反应与宫腔粘连的相关性[J]. 现代妇产科进展, 2019, 28(4): 317-318. 10.13283/j.cnki.xdfckjz.2019.04.021. [DOI] [Google Scholar]; QIU Tianmei, HE Yuanli, CAI Huihua. Correlation of endometrial inflammatory response with intrauterine adhesions[J]. Progress in Obstetrics and Gynecology, 2019, 28(4): 317-318. 10.13283/j.cnki.xdfckjz.2019.04.021. [DOI] [Google Scholar]
- 55. Kong Y, Liu Z, Xiao Q, et al. Protective effects of engineered Lactobacillus crispatus on intrauterine adhesions in mice via delivering CXCL12[J]. Front Immunol, 2022, 13: 905876. 10.3389/fimmu.2022.905876. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 56. Liu NN, Zhao X, Tan JC, et al. Mycobiome dysbiosis in women with intrauterine adhesions[J/OL]. Microbiol Spectr, 2022, 10(4): e0132422[2022-09-10]. https://www.ncbi.nlm. nih.gov/pmc/articles/PMC9431258/. [DOI] [PMC free article] [PubMed] [Google Scholar]