Abstract
目的
宫腔粘连(intrauterine adhesion,IUA)的治疗主要采用宫腔镜下宫腔粘连分离术(hysteroscopic adhesiolysis,HA),术后再辅以雌孕激素等药物治疗。IUA治疗后的宫内膜恢复是个难题,国内有多家医院使用生长激素(growth hormone,GH)进行经验性治疗,但其治疗IUA的作用机制尚未有明确的报道。本实验首次采用前期构建的孕鼠刮宫IUA模型,探讨GH对孕鼠刮宫IUA模型的辅助治疗作用,并通过免疫组织化学染色检测生长激素受体/Janus激酶(growth hormone receptor/Janus kinase,GHR/JAK)通路下游信号转导和转录激活因子(signal transducers and activators of transcription,STAT)3、磷酸化的信号转导和转录激活因子(phosphorylated signal transducer and activator of transcription,p-STAT)3、STAT5、p-STAT5的表达,以初步探究GH是否通过JAK通路调控参与促进IUA子宫内膜的生长,旨在为临床用药及治疗提供理论基础。
方法
取15只孕鼠麻醉后,将双侧胚胎取出。用刮匙沿大鼠宫腔的不同方向来回搔刮宫腔。成功建立孕鼠刮宫IUA模型后,将孕鼠随机分成3组(n=5):对照组、GH组和GH+JAK抑制剂AG490组(GH+AG490组)。对照组于刮宫后第7天经皮下注射生理盐水(0.4 mL/100 g);GH组于刮宫后第7天经皮下注射GH(0.15 U/100 g),GH+AG490组于刮宫后第7天经皮下注射GH(0.15 U/100 g)及经腹腔注射AG490 (1 mg/100 g)。以上均连续注射5 d。于第14天处死各组大鼠。切除大鼠子宫,通过HE染色来研究各组大鼠的子宫内膜形态、子宫内膜腺体数目,采用Masson染色观察大鼠子宫内膜纤维化程度,并通过免疫组织化学染色检测STAT3、p-STAT3、STAT5、p-STAT5的表达。
结果
1)GH组第14天腺体数目多于对照组(P<0.05);而GH+AG490组第14天子宫内膜腺体数目与GH组相比减少(P<0.05)。2)与对照组相比,GH组第14天大鼠子宫内膜间质纤维化面积减少(P<0.05);而GH+AG490组第14天大鼠子宫内膜间质纤维化面积比高于GH组(P<0.05)。3)与对照组相比,GH组STAT3、STAT5表达差异无统计学意义(均P>0.05);而GH组蛋白p-STAT3、p-STAT5的表达均较对照组增高(均P<0.05)。而与GH组相比,GH+AG490组STAT3、STAT5的表达均差异无统计学意义(均P>0.05);但p-STAT3、p-STAT5的表达下降(均P<0.05)。
结论
GH不仅可以促进孕鼠刮宫IUA模型子宫内膜腺体的生长,还能减经纤维化程度,可起到治疗IUA的作用,其机制可能与激活JAK/STAT3 、STAT5信号通路有关。
Keywords: 宫腔粘连, 生长激素, 子宫内膜腺上皮细胞, 动物模型
Abstract
Objective
The main treatment for intrauterine adhesion (IUA) is hysteroscopic adhesiolysis (HA), which most of treatment frequently employs estrogen and progesterone cycle therapy. The growth and coverage of endometrium after operation is a difficult problem, and several hospitals in China have performed growth hormone (GH) in empirically treating IUA, which has achieved excellent curative effects. Unfortunately, the mechanism of action has not yet been clearly elucidated. In previous study, an IUA animal model after surgical abortion and curettage in pregnant rats has been successfully established. In this experiment, the IUA animal model after surgical abortion and curettage in pregnant rats, which is more in line with the mechanism of human intrauterine adhesion, was used for the first time to investigate the therapeutic effect of GH on IUA in the pregnant rat curettage model. The expression of signal transducers and activators of transcription 3(STAT3), phosphorylated STAT3 (p-STAT3), STAT5 and p-STAT5 content were detected by immunohistochemistry to preliminarily explore the possible mechanism of GH involving in promoting endometrial growth of IUA, and to provide a theoretical basis for clinical medication and treatment.
Methods
Pregnant rats were anesthetized, and the bilateral embryos were removed completely. Then the rat endometrium was scraped with a curette in 4 different directions (front, back, left, and right). After the IUA animal model was established, the rats were randomly divided into 3 groups (n=5): a control group, a GH group, and a GH + AG490 group. Normal saline (0.4 mL/100 g) was injected subcutaneously at the 7th day after curettage in the control group;0.15 U/100 g of GH was injected subcutaneously at the 7th day after curettage in the GH group; 0.15 U/100 g of GH was injected subcutaneously and 1 mg/100 g AG490 was injected intraperitoneally at the 7th day after curettage in the GH+ AG490 group. All the rats were injected continuously for 5 days. The rats in each group were sacrificed at the 14th day. The uterus of rats in each group was stained with HE staining to explore the endometrial morphology and the number of endometrial glands in each group, and Masson staining was utilized to observe the degree of endometrial fibrosis. The levels of STAT3, p-STAT3, STAT5 and p-STAT5 were detected by immunohistochemistry.
Results
1) The number of glands in the GH group was more than that in the control group on the 14th day, with statistical difference (P<0.05). However, the number of endometrial glands in the AG490+GH group was decreased compared with the GH group on the 14th day (P<0.05). 2) The fibrosis ratio in the GH group was less than that in the control group at the 14th day after operation (P<0.05). However, the area of endometrial interstitial fibrosis in the AG490+GH group was much higher than that in the GH group 14 days after operation (P<0.05). 3) Compared with the control group, there was not significant difference in the levels of STAT3 and STAT5 in GH group (both P>0.05), while the levels of protein p-STAT3 and p-STAT5 were increased in the GH group (both P<0.05). Compared with the GH group, there was not significant difference in the levels of STAT3 and STAT5 in the AG490+GH group (both P>0.05), while the levels of p-STAT3 and p-STAT5 were decreased in the AG490+GH group (both P<0.05).
Conclusion
GH can not only promote the growth of endometrial glands in the IUA model, but also reduce the degree of fibrosis and play a role in the treatment of IUA, which may be related to the activation of the Janus kinase (JAK), JAK/STAT3 and STAT5 signaling pathways.
Keywords: intrauterine adhesion, growth hormone, endometrial epithelial cells, animal model
宫腔粘连(intrauterine adhesion,IUA)是指由于宫腔操作或宫腔感染引起子宫内膜损伤,使宫腔全部或部分闭合,导致患者出现月经量减少、闭经、不孕等临床表现的一种疾病[1]。目前IUA的治疗方法主要为宫腔镜下宫腔粘连分离术(hysteroscopic adhesiolysis,HA),术后再辅以药物促进内膜的生长与覆盖,常用的方法主要为雌孕激素周期疗法 [2]。但对于重度IUA,由于宫内膜雌孕激素受体减少,敏感度下降,部分患者临床效果欠佳,且大剂量地使用雌激素可以增加宫腔纤维化的发生概率,更容易形成宫腔瘢痕[3]。
生长激素(growth hormone,GH)是一种由脑垂体前叶嗜酸性细胞分泌的单一肽链的蛋白质激素。GH可以通过与细胞上的生长激素受体(growth hormone receptor,GHR)直接结合,从而导致GHR发生二聚化,与GHR相连的Janus蛋白酪氨酸激酶(Janus kinase,JAK)被激活后发生磷酸化,激活下游通路,使下游信号转导和转录激活因子(signal transducers and activators of transcription,STAT)磷酸化,形成有活性的磷酸化的信号转导和转录激活因子(phosphorylated signal transducer and activator of transcription,p-STAT),从而调控信号的转导。STAT蛋白是细胞质因子,GH可通过激活STAT1、STAT3和STAT5促进细胞的有丝分裂和细胞增殖,其中密切参与细胞增殖的关键信号分子是STAT3和STAT5[4]。有研究[5]报道:GH治疗可以使IUA患者子宫内膜增厚,改善月经量。目前,国内多家医院已使用GH对IUA及薄型子宫内膜进行经验性治疗,已获得较好的疗效。但GH对IUA的治疗作用,目前仍停留在临床研究及经验性应用,其作用机制尚未有明确的报道。本实验采用GH治疗孕鼠刮宫IUA模型观察子宫内膜的变化,并通过免疫组织化学检测GH/GHR/JAK通路下游STAT3、p-STAT3、STAT5、p-STAT5分子的表达,并利用JAK拮抗剂AG490验证GH是否可通过JAK/STAT3、STAT5来治疗IUA,以初步探究GH对IUA的治疗作用及其参与促进IUA子宫内膜生长的潜在机制,为GH治疗IUA提供实验依据。
1. 材料与方法
1.1. 材料
选择SD孕鼠15只,孕龄13~15 d,体重400~450 g。由中南大学湘雅三医院动物实验部负责饲养,动物在手术前均在控制温度[(23±2) ℃]和光照(12 h光照和12 h黑暗)的环境下单独饲养,自由饮食、饮水。实验程序均经中南大学湘雅三医院动物实验伦理委员会批准,全部动物实验均得到动物研究伦理委员会的批准(审批号:2019sydw0059),严格遵守美国国立卫生研究院有关实验动物护理和使用的指南和要求。
GH购自长春金赛药业有限责任公司;AuraStain SP鼠/兔免疫组织化学试剂盒购自长沙艾佳生物技术有限公司;AG490购自美国Sigma公司;STAT3、p-STAT3, STAT5、p-STAT5抗体均购自美国Abzoom公司。
1.2. 方法
1.2.1. IUA动物模型的构建及分组
取孕鼠按照40 mg/kg剂量于腹腔注射苯巴比妥钠进行麻醉。操作均由同一研究者进行。首先对大鼠术野进行剪毛备皮,面积约为3 cm×3 cm,用络合碘消毒后取下腹正中切口,长约4 cm,分层进入腹腔,暴露两侧子宫。先于双侧子宫近端作1 cm纵切口,将双侧胚胎取出。用刮匙沿大鼠宫腔的不同方向来回搔刮宫腔,当感觉到宫腔四壁粗糙时停止操作。术毕缝合子宫切口及腹壁切口。此种IUA动物模型造模方法的必要性及有效性已在前期实验[6]中得到验证。选取建模成功的大鼠15只,随机分为GH组[于刮宫后第7天皮下注射GH 0.15 U/100 g,连续注射5 d]、对照组[于刮宫后第7天经皮下注射生理盐水0.4 mL/100 g,连续注射5 d]、GH+AG490组[于刮宫后第7天经皮下注射GH(0.15 U/100 g)及腹腔注射JAK抑制剂AG490(1 mg/100 g),连续注射5 d],每组5只。于第14天处死各组大鼠。分别取两侧子宫制作切片,每组样本量为10,比较各组雌鼠子宫内膜HE切片组织形态的改变、子宫内膜腺体数目、子宫内膜纤维化程度,并采用免疫组织化学法检测STAT3、STAT5、p-STAT3、p-STAT5的表达。
1.2.2. HE染色
将样本制作成石蜡切片,连续切片(切片厚度为 4 μm)后行常规HE染色,并由同一位经验丰富的病理科医师对切片进行盲阅。每张HE切片在显微镜下随机选择4个低倍镜(×50)视野,计数子宫内膜腺体,并计算4个视野的平均值。
1.2.3. 子宫内膜纤维化程度检测
将大鼠子宫石蜡标本行4 μm连续切片,再进行Masson染色。每张Masson 切片随机选择4个高倍镜(×100)视野。使用Image-Pro Plus 6.0图像分析系统计算每个视野内子宫内膜间质纤维化面积以及子宫内膜间质与腺体面积之和。将子宫内膜间质纤维化面积除以子宫内膜间质及腺体总面积获得纤维化比率,每个视野取其平均值。
1.2.4. 免疫组织化学染色
实验操作步骤严格按试剂盒的说明进行,以枸橼酸盐缓冲液稀释后的微波抗原修复,用非免疫正常山羊血清封闭,一抗STAT3、STAT5、p-STAT3、p-STAT5按1꞉200的浓度稀释。再以二抗孵育,DAB显色。子宫内膜组织出现棕黄色或棕褐色颗粒为阳性表达。每张切片随机选择4个高倍镜(×200)视野,使用Image-Pro Plus 6.0图像分析系统计算内膜蛋白平均光密度(mean optical density,MOD),计算4个视野的平均值。MOD的高低决定蛋白阳性表达的强弱。
1.3. 统计学处理
本实验数据均采用SPSS 19.0统计学软件进行分析。计量资料用均值±标准差( ±s)表示。两组数据之间的比较采用Student’s t检验(t-test),以P<0.05为差异有统计学意义。
2. 结 果
2.1. GH对孕鼠刮宫IUA模型子宫内膜腺体的作用
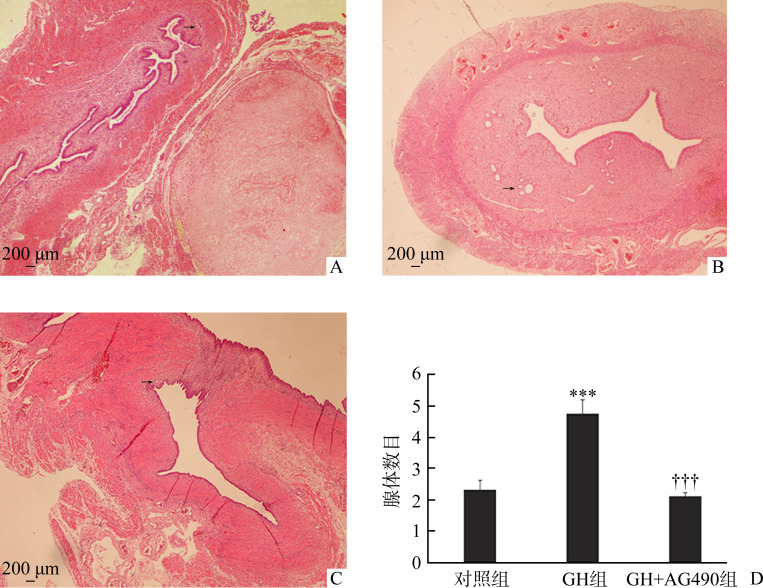
术后第14天,对照组宫腔可见一些肌纤维性粘连带,上皮层下腺体极稀疏,间质纤维细胞显著增生,有极少许炎细胞浸润(图1A)。而GH组术后第14天内膜增厚,腺体数目增多,偶有少许纤维增生(图1B)。对照组术后第14天的腺体数目为(2.32±0.60)个,GH组第14天腺体数目为(4.75±0.88)个,GH组腺体数目多于对照组(P<0.001)。GH+AG490组第14天子宫内膜腺体数目为(2.12±0.22)个,较GH组减少(P<0.001;图1C,1D)。
图1.
各组孕鼠刮宫IUA模型建模术后第14天子宫HE染色及子宫内膜腺体数目
Figure 1 HE staining of uterus and the number of endometrial glands on the 14th day after curettage in pregnant rats
A: Control group; B: GH group; C: GH+AG490 group; D: Comparison of gland number among the 3 groups. ***P<0.001 vs the control group; †††P<0.001 vs the GH group.
2.2. GH对子宫内膜纤维化的抑制作用
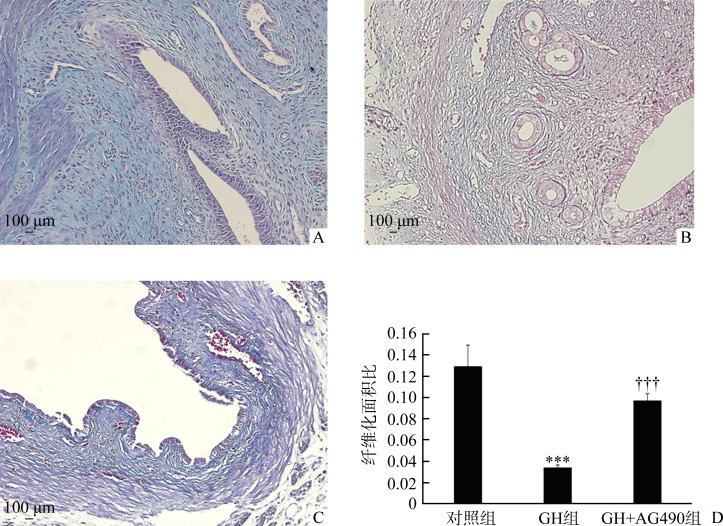
在术后第14天,对照组上皮层下腺体稀疏,间质纤维组织增多,胶原聚集,纤维化较明显,部分宫腔可见一些纤维肌性粘连带,而GH组第14天子宫内膜结构完整,内间质无水肿,间质胶原纤维排列整齐,为梭形,Masson染色呈蓝色。术后第14天,GH组大鼠子宫内膜间质纤维化面积比为(0.0345±0.0056),低于对照组(0.1301±0.0396),差异有统计学意义(P<0.001,图2)。而GH+AG490组大鼠术后第14天子宫内膜间质纤维化面积比为0.0978±0.0121,显著性高于GH组术后的第14天的面积比(P<0.001),但仍低于对照组。
图2.
各组孕鼠刮宫IUA模型建模术后第14天子宫Masson染色
Figure 2 Masson staining of uterus on the 14th day after operation
A: Control group; B: GH group; C: GH+AG490 group; D: Comparison of the fibrosis ratio among the 3 groups. ***P<0.001 vs the control group; †††P<0.001 vs the GH group.
2.3. GH治疗大鼠IUA的作用机制
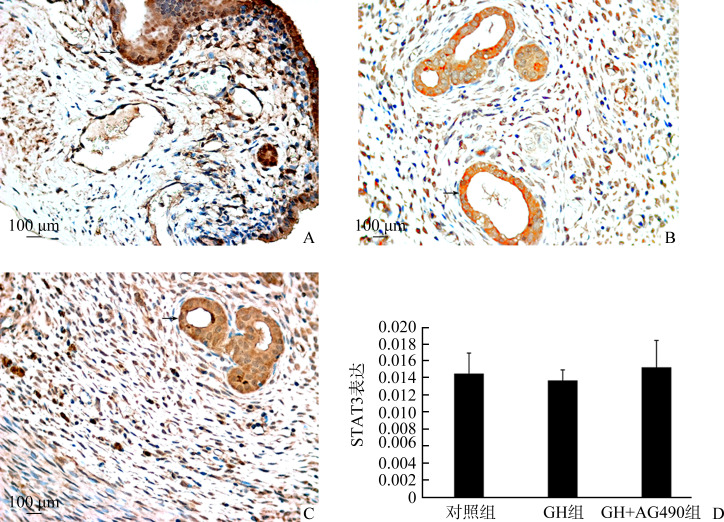
在造模术后第14天,对照组大鼠子宫内膜STAT3蛋白表达的MOD值为0.0145±0.005,而GH组大鼠子宫内膜STAT3蛋白表达的MOD值为0.0137±0.003,两组比较差异无明显统计学意义(P>0.05)。GH+AG490组大鼠子宫内膜STAT3蛋白表达的MOD值为0.01528±0.006,与GH相比,两组差异无明显统计学意义(P>0.05,图3)。
图3.
各组刮宫IUA模型术后第14天子宫内膜STAT3蛋白表达(SP)
Figure 3 Expression of STAT3 protein in endometrium on the 14th day after operation in the different groups (SP)
A: Control group; B: GH group; C: GH+AG490 group; D: No significant difference in STAT3 expression among the 3 groups (all P>0.05).
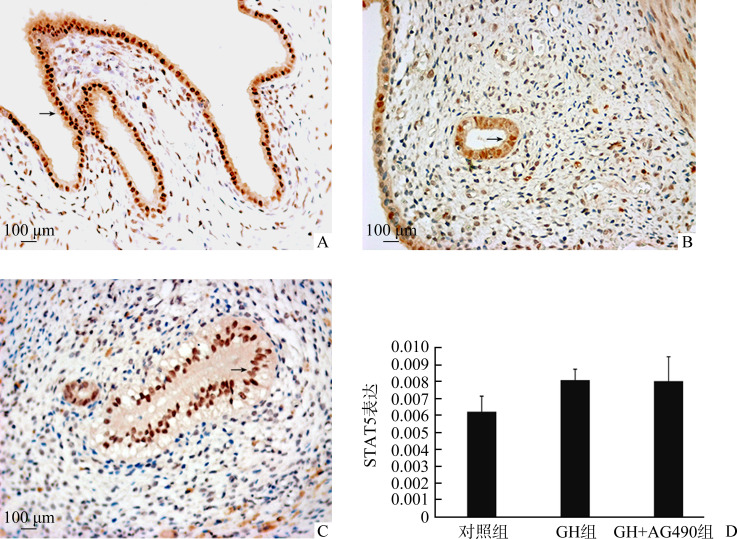
在造模术后第14天,对照组大鼠子宫内膜STAT5蛋白表达的MOD值为0.006 25±0.001 80,而GH组大鼠子宫内膜STAT5蛋白表达的MOD值为0.008 12±0.001 20,两组之间差异无明显统计学意义(P>0.05)。GH+AG490组大鼠子宫内膜STAT5蛋白表达的MOD值为0.008 06±0.002 80,与GH组相比,两组差异无明显统计学意义(P>0.05,图4)。
图4.
各组刮宫IUA模型术后第14天子宫内膜STAT5蛋白表达(SP)
Figure 4 Expression of STAT5 protein in endometrium on the 14th day after operation in the different groups (SP)
A: Control group; B: GH group; C: GH+AG490 group; D: No significant difference in STAT5 expression among the 3 groups (all P>0.05).
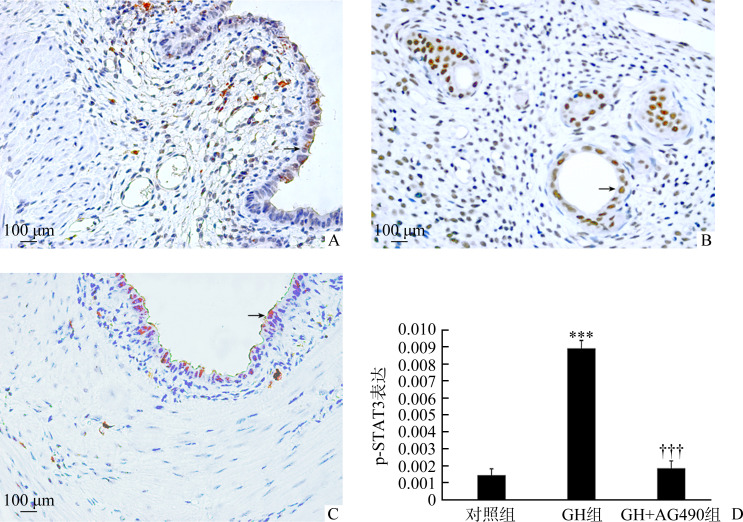
在造模术后第14天,对照组大鼠子宫内膜p-STAT3蛋白表达的MOD值为0.001 47±0.000 70,而GH组大鼠子宫内膜p-STAT3蛋白表达的MOD值为0.008 94±0.000 90,两组之间差异有统计学意义(P<0.001)。GH+AG490组大鼠子宫内膜p-STAT3蛋白表达的MOD值为0.001 89±0.000 80,与GH组相比,差异有统计学意义(P<0.001,图5)。
图5.
各组刮宫IUA模型术后第14天子宫内膜p-STAT3蛋白表达(SP)
Figure 5 Expression of p-STAT3 protein in endometrium on the 14th day after operation in the different groups (SP)
A: Control group; B: GH group; C: GH+AG490 group; D: Comparison of p-STAT3 expression among the 3 groups. ***P<0.001 vs the the control group; †††P<0.001 vs the GH group.
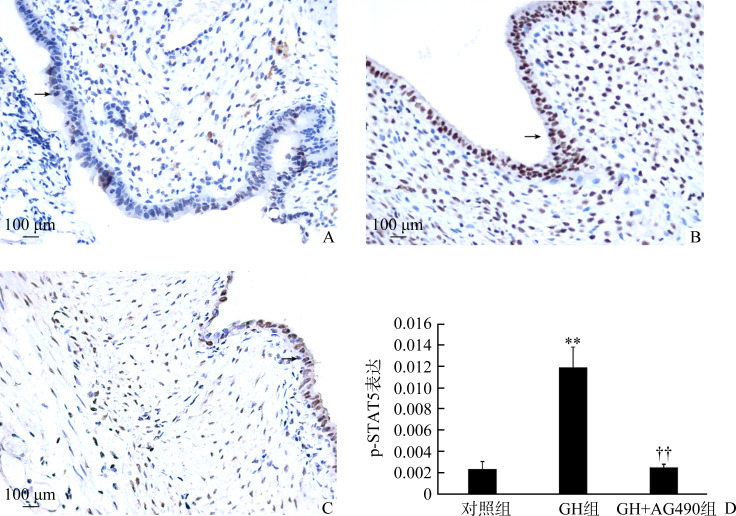
在造模术后第14天,对照组大鼠子宫内膜p-STAT5免疫表达的MOD值为0.002 39±0.001 40,而GH组大鼠子宫内膜p-STAT5免疫表达的MOD值为0.011 91±0.003 80,两组之间差异有统计学意义(P<0.01)。GH+AG490组大鼠子宫内膜p-STAT5免疫表达的MOD值为0.002 51±0.000 60,与GH组相比差异有统计学意义(P<0.01,图6)。
图6.
各组刮宫IUA模型术后第14天子宫内膜p-STAT5蛋白表达(SP)
Figure 6 Expression of p-STAT5 protein in endometrium on the 14th day after operation in the different group (SP)
A: Control group; B: GH group; C: GH+AG490 group; D: Comparison of p-STAT5 expression among the 3 groups. **P<0.01 vs the the control group; ††P<0.01 vs the GH group.
3. 讨 论
本研究采用孕鼠刮宫IUA模型研究GH治疗IUA的作用机制,发现GH可以促进孕鼠刮宫IUA模型子宫内膜腺体的生长,减少纤维化的形成,可有效治疗IUA。在本课题组的前期研究[6]中,根据IUA发生的危险因素,采用孕鼠刮宫建立IUA动物模型,并经鉴定可成功建立大鼠IUA动物模型,并且符合人类IUA的病因和病理表现。由于孕鼠子宫在妊娠后变薄变软,在清除胚胎后,子宫腔扩张,更易模仿人类进行刮宫。子宫壁在妊娠期变薄,通过刮宫操作更易充分刮除子宫内膜腺上皮,破坏部分间质,使大鼠的子宫内膜腺体及间质均损伤,更易引起IUA。在孕鼠刮宫模型中,结束妊娠后卵巢功能未恢复,雌激素下降,缺乏足够的可以迅速再生的上皮细胞,无法覆盖宫腔创面,从而裸露间质,使其纤维化程度增加。因此本实验首次采用这种更加符合人类IUA发生机制的孕鼠刮宫IUA模型,以便探讨GH对该动物模型IUA的辅助治疗作用。
目前,IUA手术治疗后的宫内膜恢复仍旧是困扰妇科医师的难题。有学者[7]使用雌孕激素及GH治疗80例HA术后的患者,雌孕激素治疗组患者月经恢复有效率为85%,再粘连率为25%,雌孕激素加GH组患者月经恢复有效率为97.5%,再粘连率为7.5%。林雪娥等[8]观察了120例使用雌孕激素及GH治疗的IUA患者,也得出类似结论。研究[9]表明:GH在HA后预防再粘连中的临床价值高,它可增加术后的子宫内膜厚度,促进月经恢复,减轻宫腔再粘连的严重程度,可以促进IUA患者子宫内膜的生长和发育。也有研究[10-12]报道:GH在体外受精-胚胎移植(in vitro fertilization-embryo transfer,IVF-ET)中对反应不良性子宫内膜有促进子宫内膜增殖、使其再发育的作用,可以增加子宫内膜厚度,改善薄型子宫内膜下血流状况,促进妊娠率。上述研究均提示GH可以起到加快子宫内膜的增殖,辅助治疗IUA的作用。
GH有非常广泛的作用,它可以刺激人体细胞生长及增殖,也有促进子宫内膜细胞增长的作用。GHR[4]是一种跨膜糖蛋白,在人体及动物的组织内分布广泛。GHR与GH结合后,会发生二聚化,然后激活相关信息通道及信息分子,在人体内发挥着重要的生物学作用。近年来的研究[13]发现许多信息分子可以在不同的通道中被JAK激酶激活,JAK激酶由JAK1、JAK2、JAK3和Tyk4等同工型激酶组成,是酪氨酸激酶家族重要的一员,与细胞信号传递密切相关。JAK2是GH与GHR结合后激活的重要的信息分子之一。当GH与GHR结合后,GHR发生二聚化后使下游信息分子JAK2激酶的酪氨酸侧链发生磷酸化,激活JAK2,逐渐使GHR质膜内侧C-端结构域的酪氨酸残基磷酸化,激活下游通路,活化STAT蛋白,使STAT蛋白在保守的C-端发生磷酸化,然后STAT蛋白二聚物被转运到细胞核中与DNA结合,启动相关基因表达[13]。GH可激活STAT1、STAT3和STAT5。在这众多的信息分子中,密切参与细胞增殖的关键信号分子是STAT5。这在动物模型上得到证明,如学者[14]在全长GHR敲除鼠、缺失活化JAK2能力的鼠和GHR391鼠(STAT5受损)3种鼠中观察到:对于GH依赖性细胞的生长,87%由鼠中JAK-STAT5信号通路调控,而13%由JAK2直接作用。除此之外,近年来,有学者[15]发现细胞内信号转导的新的重要通路JAK2/STAT3。STAT3是STAT蛋白家族的主要成员,是目前细胞因子领域研究的热点之一。STAT3信号因子可以介导产生多种信息因子,这些信息因子调控着靶细胞的增殖、活化和凋亡。当GHR与GH结合后,形成二聚化,激活JAK,JAK被磷酸化活化后,调控下游STAT3、STAT5蛋白磷酸化,从而形成p-STAT3、p-STAT5,p-STAT3、p-STAT5并进入靶细胞的细胞核内,与特异性的基因启动区域相结合,调控靶细胞基因的表达及相应蛋白的产生[4]。
AG490可以竞争结合受体的酪氨酸激酶,达到抑制JAK/STAT3、STAT5信号转导通路的目的[16]。本实验以AG490特异性地抑制JAK/STAT3、STAT5信号通路,结果显示GH组STAT3、STAT5的磷酸化蛋白表达强于对照组,这证明GH可以促进孕鼠刮宫IUA模型大鼠子宫内膜STAT3、STAT5的磷酸化水平;而GH+AG490组大鼠子宫内膜腺体的数量显著减少,纤维化程度加重,STAT3、STAT5的磷酸化的蛋白表达较GH组也降低,这证明GH可能通过激活GHR/JAK/STAT3、STAT5信号通路参与促进IUA子宫内膜的生长。
在本实验中,由于大鼠子宫较小,其子宫内膜难以与子宫肌壁分离,无法单独取得子宫内膜组织进行蛋白质印迹实验以定量相关蛋白,因此本课题组在前期研究中[17]进行了人子宫内膜腺体细胞培养,并进行了细胞层面的验证,实验结果表明GH可以通过GHR/JAK/STAT3/5信号通路促进子宫内膜腺体细胞的生长。本次动物实验结果与人子宫内膜腺体细胞实验结果一致。另外,本实验研究目的是探讨GH对孕鼠刮宫模型IUA的辅助治疗作用,所以在实验设计的初期因考虑实验动物福利问题,未设置空白对照组,这是本实验的不足之处。
综上所述,本实验结果表明GH可以促进孕鼠刮宫IUA模型子宫内膜腺体的生长,减少纤维化程度,起到治疗IUA的作用,其机制可能与激活GHR/JAK/STAT3/5信号通路有关。本研究为GH治疗IUA提供了实验依据。
| 英文缩写 | 中文名称 | 英文缩写 | 中文名称 | 英文缩写 | 中文名称 |
|---|---|---|---|---|---|
| 5-FU | 5-氟尿嘧啶 | FDA | 美国食品药品管理局 | PaCO2 | 动脉血二氧化碳分压 |
| 5-HT | 5-羟色胺 | GFP | 绿色荧光蛋白 | PaO2 | 动脉血氧分压 |
| ABC法 | 抗生物素蛋白-生物素-过氧化物酶复合物法 | GSH | 谷胱甘肽 | PBS | 磷酸盐缓冲液 |
| ACh | 乙酰胆碱 | HAV | 甲型肝炎病毒 | PCR | 聚合酶链反应 |
| AIDS | 获得性免疫缺陷综合征 | Hb | 血红蛋白 | PET/CT | 正电子发射计算机体层显像仪 |
| ALT | 谷丙转氨酶 | HBV | 乙型肝炎病毒 | PI | 碘化丙啶 |
| AngII | 血管紧张素II | HCG | 人绒毛膜促性腺激素 | PI3K | 磷脂酰肌醇3激酶 |
| Annexin V-FITC | 膜联蛋V标记的异硫氰酸荧光素 | HDL-C | 高密度脂蛋白胆固醇 | PLT | 血小板 |
| APTT | 活化部分凝血活酶时间 | HE | 苏木精-伊红染色 | PT | 凝血酶原时间 |
| AST | 谷草转氨酶 | HGF | 肝细胞生长因子 | PVDF | 聚偏氟乙烯 |
| ATP | 三磷酸腺苷 | HIV | 人类免疫缺陷病毒 | RBC | 红细胞 |
| BCA | 二辛可宁酸 | HPF | 高倍视野 | real-time PCR | 实时聚合酶链反应 |
| BMI | 体重指数 | HR | 心率 | real-time RT-PCR | 实时反转录聚合酶链反应 |
| BP | 血压 | HRP | 辣根过氧化物酶 | RIPA | 放射免疫沉淀法 |
| BSA | 牛血清白蛋白 | HSP | 热激蛋白 | RNA | 核糖核酸 |
| BUN | 尿素氮 | IC50 | 半数抑制浓度 | ROS | 活性氧 |
| CCK-8 | 细胞计数试剂盒-8 | ICU | 重症监护病房 | RT-PCR | 反转录聚合酶链反应 |
| COX-2 | 环氧合酶-2 | IFN | 干扰素 | SABC | 链霉抗生物素蛋白-生物素-过氧化物酶复合物法 |
| Cr | 肌酐 | IL | 白细胞介素 | SCr | 血肌酐 |
| CRP | C反应蛋白 | iNOS | 诱导型一氧化氮合酶 | SDS-PAGE | SDS聚丙烯酰胺凝胶电泳 |
| CT | 计算机体层摄影 | IPG | 固相pH梯度 | SO2 | 血氧饱和度 |
| CV | 变异系数 | JNK | 氨基末端激酶 | SOD | 超氧化物歧化酶 |
| DAB | 二氨基联苯胺 | LDL-C | 低密度脂蛋白胆固醇 | SPF | 无特定病原体 |
| ddH2O | 双蒸水 | LPS | 内毒素/脂多糖 | SP法 | 链霉菌抗生物素蛋白-过氧化物酶法 |
| DMEM | 杜尔贝科改良伊格尔培养基 | MAP | 平均动脉压 | STAT | 信号转导及转录激活因子 |
| DMSO | 二甲基亚砜 | MAPK | 丝裂原激活的蛋白激酶 | TBIL | 总胆红素 |
| DNA | 脱氧核糖核酸 | MDA | 丙二醛 | TBST | Tris-盐酸洗膜缓冲液 |
| ECG | 心电图 | miRNA | 微RNA | TC | 总胆固醇 |
| ECL | 增强化学发光法 | MMP | 基质金属蛋白酶 | TG | 三酰甘油 |
| ECM | 细胞外基质 | MRI | 磁共振成像 | TGF | 转化生长因子 |
| EDTA | 乙二胺四乙酸 | mTOR | 哺乳动物雷帕霉素靶蛋白 | Th | 辅助性T细胞 |
| EEG | 脑电图 | MTT | 四甲基偶氮唑盐微量酶反应 | TLR | Toll样受体 |
| EGF | 表皮生长因子 | NADPH | 还原型烟酰胺腺嘌呤二核苷酸磷酸 | TNF | 肿瘤坏死因子 |
| ELISA | 酶联免疫吸附测定 | NF-κB | 核因子-κB | TUNEL | 原位末端脱氧核苷酸转移酶标记法 |
| eNOS | 内皮型一氧化氮合酶 | NK细胞 | 自然杀伤细胞 | VEGF | 血管内皮生长因子 |
| ERK | 细胞外调节蛋白激酶 | NO | 一氧化氮 | VLDL-C | 极低密度脂蛋白胆固醇 |
| ESR | 红细胞沉降率 | NOS | 一氧化氮合酶 | WBC | 白细胞 |
| FBS | 胎牛血清 | NS | 生理氯化钠溶液 | WHO | 世界卫生组织 |
本刊对部分常用词汇允许直接使用缩写,即首次出现时可不标注中文。
基金资助
湖南省自然科学基金(2021JJ40918)。
This work was supported by the Natural Science Foundation of Hunan Province, China (2021JJ40918).
利益冲突声明
作者声称无任何利益冲突。
作者贡献
冯晴 实验实施和论文撰写;张爱倩 统计分析;徐大宝 论文构想和修订;曾飞 论文修改。所有作者阅读并同意最终的文本。
原文网址
http://xbyxb.csu.edu.cn/xbwk/fileup/PDF/2022111522.pdf
参考文献
- 1. Mentula M, Männistö J, Gissler M, et al. Intrauterine adhesions following an induced termination of pregnancy: a nationwide cohort study[J]. BJOG, 2018, 125(11): 1424-1431. 10.1111/1471-0528.15216. [DOI] [PubMed] [Google Scholar]
- 2. Wang J, Yang C, Xie Y, et al. Application of bioactive hydrogels for functional treatment of intrauterine adhesion[J]. Front Bioeng Biotechnol, 2021, 9: 760943. 10.3389/fbioe.2021.760943. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 3. Zhou Q, Wu X, Dai X, et al. The different dosages of estrogen affect endometrial fibrosis and receptivity, but not SDF-1/CXCR4 axis in the treatment of intrauterine adhesions[J]. Gynecol Endocrinol, 2018, 34(1): 49-55. 10.1080/09513590.2017.1328050. [DOI] [PubMed] [Google Scholar]
- 4. Chhabra Y, Lee C, Müller A, et al. GHR signalling: Receptor activation and degradation mechanisms[J]. Mol Cell Endocrinol, 2021, 520: 111075. 10.1016/j.mce.2020.111075. [DOI] [PubMed] [Google Scholar]
- 5. 邬晓琳, 黄玲玲, 梁蕾, 等. 重组人生长激素在人类辅助生殖技术助孕中的应用进展[J]. 中华生殖与避孕杂志, 2020, 40(3): 5. 10.3760/cma.j.cn101441-20190315-00099. [DOI] [Google Scholar]; WU Xiaolin, HUANG Lingling, LIANG Lei, et al. Application progress of recombinant human growth hormone in assisted reproductive technology[J]. Chinese Journal of Reproduction and Contraception, 2020, 40(3): 5. 5. 10.3760/cma.j.cn101441-20190315-00099. [DOI] [Google Scholar]
- 6. Qing F, Bingsi G, Xingping Z, et al. Establishment of an animal model of intrauterine adhesions after surgical abortion and curettage in pregnant rats[J]. Ann Transl Med, 2020, 8(4): 56. 10.21037/atm.2020.01.134. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 7. 江娟, 林美花, 郑少娜. 宫内节育器, 雌孕激素序贯结合生长激素对宫腔再粘连的预防效果观察[J]. 中国现代药物应用, 2021, 15(11): 3. 10.14164/j.cnki.cn11-5581/r.2021.11.071. [DOI] [Google Scholar]; JIANG Juan, LIN Meihua, ZHENG Shaona. Effect of IUD, estrogen and progesterone in combination with growth hormone on prevention of uterine cavity re adhesion[J]. Chinese Journal of Modern Applied Pharmacy, 2021, 15(11): 3. 10.14164/j.cnki.cn11-5581/r.2021.11.071. [DOI] [Google Scholar]
- 8. 林雪娥, 吴智仁, 陈国仁, 等. 宫内节育器 雌孕激素序贯结合生长激素预防宫腔镜宫腔粘连分离术后再粘连效果分析[J]. 基层医学论坛, 2021, 25(22): 3. 10.19435/j.1672-1721.2021.22.013. [DOI] [Google Scholar]; LIN Xue’e, WU Zhiren, CHEN Guoren, et al. Analysis of the effect of intrauterine device,estrogen and progesterone sequentially combined with growth hormone to prevent re-adhesion after hysteroscopic adhesion separation[J]. Grassroots Medical Forum, 2021, 25(22): 3. 10.19435/j.1672-1721.2021.22.013. [DOI] [Google Scholar]
- 9. 洪秀仪, 郑华丽. 生长激素在宫腔粘连分离术后预防再粘连中的作用[J]. 广东医学院学报, 2018, 36(2): 160-162. 10.3969/j.issn.1005-4057.2018.02.012. [DOI] [Google Scholar]; HONG Xiuyi, ZHENG Huali. Clinical effect of growth hormone on the prevention of re-adhesion after intrauterine adhesion separation[J]. Journal of Guangdong Medical University, 2018, 36(2): 160-162. 10.3969/j.issn.1005-4057.2018.02.012. [DOI] [Google Scholar]
- 10. 胡淑敏, 冷义福, 牟琳琳, 等. 生长激素在薄型子宫内膜患者冻融胚胎移植周期内膜准备中应用的临床研究[J]. 中华生殖与避孕杂志, 2019, 39(12): 5. 10.3760/cma.j.issn.2096-2916.2019.12.002 [DOI] [Google Scholar]; HU Shumin, LENG Yifu, MU Linlin, et al. Clinical research on the application of growth hormone in the preparation of thin endometrium[J]. Chinese Journal of Reproduction and Contraception, 2019, 39(12): 5. 10.3760/cma.j.issn.2096-2916.2019.12.002 [DOI] [Google Scholar]
- 11. 曹志文, 胡卫华. 生长激素宫腔灌注治疗薄型子宫内膜的研究[J]. 中国临床药理学与治疗学, 2019, 24(9): 6. 10.12092/j.issn.1009-2501.2019.09.004. [DOI] [Google Scholar]; CAO Zhiwen, HU Weihua. Study on the treatment of thin endometrium with intrauterine infusion of growth hormone[J]. Chinese Journal of Clinical Pharmacology and Therapeutics, 2019, 24(9): 6. 10.12092/j.issn.1009-2501.2019.09.004. [DOI] [Google Scholar]
- 12. 曲艳春. 重组人生长激素对体外受精-胚胎移植患者影响的分析[J]. 中国药物与临床, 2020, 20(4): 2. 10.1655/zgywylc2020.04.028. [DOI] [Google Scholar]; QU Yanchun. Analysis of the effect of recombinant human growth hormone on patients undergoing in vitro fertilization embryo transfer[J]. Chinese Remedies & Clinics, 2020, 20(4): 2. 10.1655/zgywylc2020.04.028. [DOI] [Google Scholar]
- 13. Chen B, Song L, Nie X, et al. CXCL1 regulated by miR-302e is involved in cell viability and motility of colorectal cancer via inhibiting JAK-STAT signaling pathway[J]. Front Oncol, 2021, 10: 577229. 10.3389/fonc.2020.577229. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 14. Barclay J, Kerr L, Arthur L, et al. In vivo targe-ting of the growth hormone receptor (GHR) Boxl se-quence demonstrates that the GHR does not signal exclusively through JAK2[J]. Mol Endocrinol, 2010, 24(1): 204-217. 10.1210/me.2009-0233. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 15. Liu Y, Liao S, Bennett S, et al. STAT3 and its targeting inhibitors in osteosarcoma[J]. Cell Prolif, 2021, 54(2): e12974 [2022-02-28]. https://pubmed.ncbi.nlm.nih.gov/ 33382511. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 16. Caceres-Cortes J. A potent anti-carcinoma and anti-acute myeloblastic leukemia agent, AG490[J]. Aticancer Agents Med Chem, 2008, 8(7): 717-722. 10.21037/atm.2019.12.08. [DOI] [PubMed] [Google Scholar]
- 17. Feng Q, Gao B, Huang H, et al. Growth hormone promotes human endometrial glandular cells proliferation and motion through the GHR-STAT3/5 pathway[J]. Ann Transl Med, 2020, 8(4): 53. 10.21037/atm.2019.12.08. [DOI] [PMC free article] [PubMed] [Google Scholar]
Associated Data
This section collects any data citations, data availability statements, or supplementary materials included in this article.
Supplementary Materials
| 英文缩写 | 中文名称 | 英文缩写 | 中文名称 | 英文缩写 | 中文名称 |
|---|---|---|---|---|---|
| 5-FU | 5-氟尿嘧啶 | FDA | 美国食品药品管理局 | PaCO2 | 动脉血二氧化碳分压 |
| 5-HT | 5-羟色胺 | GFP | 绿色荧光蛋白 | PaO2 | 动脉血氧分压 |
| ABC法 | 抗生物素蛋白-生物素-过氧化物酶复合物法 | GSH | 谷胱甘肽 | PBS | 磷酸盐缓冲液 |
| ACh | 乙酰胆碱 | HAV | 甲型肝炎病毒 | PCR | 聚合酶链反应 |
| AIDS | 获得性免疫缺陷综合征 | Hb | 血红蛋白 | PET/CT | 正电子发射计算机体层显像仪 |
| ALT | 谷丙转氨酶 | HBV | 乙型肝炎病毒 | PI | 碘化丙啶 |
| AngII | 血管紧张素II | HCG | 人绒毛膜促性腺激素 | PI3K | 磷脂酰肌醇3激酶 |
| Annexin V-FITC | 膜联蛋V标记的异硫氰酸荧光素 | HDL-C | 高密度脂蛋白胆固醇 | PLT | 血小板 |
| APTT | 活化部分凝血活酶时间 | HE | 苏木精-伊红染色 | PT | 凝血酶原时间 |
| AST | 谷草转氨酶 | HGF | 肝细胞生长因子 | PVDF | 聚偏氟乙烯 |
| ATP | 三磷酸腺苷 | HIV | 人类免疫缺陷病毒 | RBC | 红细胞 |
| BCA | 二辛可宁酸 | HPF | 高倍视野 | real-time PCR | 实时聚合酶链反应 |
| BMI | 体重指数 | HR | 心率 | real-time RT-PCR | 实时反转录聚合酶链反应 |
| BP | 血压 | HRP | 辣根过氧化物酶 | RIPA | 放射免疫沉淀法 |
| BSA | 牛血清白蛋白 | HSP | 热激蛋白 | RNA | 核糖核酸 |
| BUN | 尿素氮 | IC50 | 半数抑制浓度 | ROS | 活性氧 |
| CCK-8 | 细胞计数试剂盒-8 | ICU | 重症监护病房 | RT-PCR | 反转录聚合酶链反应 |
| COX-2 | 环氧合酶-2 | IFN | 干扰素 | SABC | 链霉抗生物素蛋白-生物素-过氧化物酶复合物法 |
| Cr | 肌酐 | IL | 白细胞介素 | SCr | 血肌酐 |
| CRP | C反应蛋白 | iNOS | 诱导型一氧化氮合酶 | SDS-PAGE | SDS聚丙烯酰胺凝胶电泳 |
| CT | 计算机体层摄影 | IPG | 固相pH梯度 | SO2 | 血氧饱和度 |
| CV | 变异系数 | JNK | 氨基末端激酶 | SOD | 超氧化物歧化酶 |
| DAB | 二氨基联苯胺 | LDL-C | 低密度脂蛋白胆固醇 | SPF | 无特定病原体 |
| ddH2O | 双蒸水 | LPS | 内毒素/脂多糖 | SP法 | 链霉菌抗生物素蛋白-过氧化物酶法 |
| DMEM | 杜尔贝科改良伊格尔培养基 | MAP | 平均动脉压 | STAT | 信号转导及转录激活因子 |
| DMSO | 二甲基亚砜 | MAPK | 丝裂原激活的蛋白激酶 | TBIL | 总胆红素 |
| DNA | 脱氧核糖核酸 | MDA | 丙二醛 | TBST | Tris-盐酸洗膜缓冲液 |
| ECG | 心电图 | miRNA | 微RNA | TC | 总胆固醇 |
| ECL | 增强化学发光法 | MMP | 基质金属蛋白酶 | TG | 三酰甘油 |
| ECM | 细胞外基质 | MRI | 磁共振成像 | TGF | 转化生长因子 |
| EDTA | 乙二胺四乙酸 | mTOR | 哺乳动物雷帕霉素靶蛋白 | Th | 辅助性T细胞 |
| EEG | 脑电图 | MTT | 四甲基偶氮唑盐微量酶反应 | TLR | Toll样受体 |
| EGF | 表皮生长因子 | NADPH | 还原型烟酰胺腺嘌呤二核苷酸磷酸 | TNF | 肿瘤坏死因子 |
| ELISA | 酶联免疫吸附测定 | NF-κB | 核因子-κB | TUNEL | 原位末端脱氧核苷酸转移酶标记法 |
| eNOS | 内皮型一氧化氮合酶 | NK细胞 | 自然杀伤细胞 | VEGF | 血管内皮生长因子 |
| ERK | 细胞外调节蛋白激酶 | NO | 一氧化氮 | VLDL-C | 极低密度脂蛋白胆固醇 |
| ESR | 红细胞沉降率 | NOS | 一氧化氮合酶 | WBC | 白细胞 |
| FBS | 胎牛血清 | NS | 生理氯化钠溶液 | WHO | 世界卫生组织 |
本刊对部分常用词汇允许直接使用缩写,即首次出现时可不标注中文。