Abstract
目的
中枢神经系统白血病(central nervous system leukemia,CNSL)是导致急性白血病患者复发和死亡的主要原因之一。本研究旨在通过流式细胞术(flow cytometry,FCM)动态监测不同类型急性白血病患者的脑脊液和骨髓的微小残留病(minimal residual disease,MRD),比较二者检测MRD的时效性和一致性,以进一步探讨监测脑脊液FCM在MRD的应用价值。
方法
回顾性分析2018年10月至2022年1月广东省人民医院血液科收治的199例急性白血病患者资料,采用多参数FCM,比较不同类型白血病患者脑脊液中的MRD情况以及同一患者脑脊液和骨髓标本中的MRD情况,并分析对其在评估患者预后价值中的作用。
结果
199例急性白血病患者中,脑脊液MRD阳性共31例(15.58%),其中18例(58%)比对应骨髓标本更早检测出MRD阳性。在19例急性T淋巴细胞白血病患者、134例急性B淋巴细胞白血病患者和46例急性髓系白血病患者中,脑脊液MRD阳性的患者分别有4例、18例和9例。不同分型的急性白血病中脑脊液MRD结果与骨髓MRD结果的一致性检验Kappa值仅为0.156,表明二者一致性较低。此外,动态监测脑脊液标本可能比监测骨髓标本能更早发现体内MRD变化情况。
结论
脑脊液FCM动态监测MRD可作为CNSL的监测指标,且监测脑脊液比监测骨髓标本可能更早发现MRD,脑脊液和骨髓二者相互补充可作为评价患者预后的指标,具有一定的临床指导意义。
Keywords: 流式细胞术, 脑脊液, 急性白血病, 微小残留病
Abstract
Objective
Central nervous system leukemia (CNSL) is one of the main causes of recurrence and death in patients with acute leukemia. This study aims to dynamically monitor minimal residual disease (MRD) in cerebrospinal fluid and bone marrow of patients with different types of acute leukemia by flow cytometry (FCM), and to compare the timeliness and consistency of MRD detection between the 2 methods to further explore the application value of monitoring MRD in cerebrospinal fluid.
Methods
A total of 199 patients with acute leukemia admitted to the Guangdong Provincial people’s Hospital between October 2018 and January 2022 were retrospectively analyzed, and multiparametric FCM method was adopted to summarize and analyze MRD in cerebrospinal fluid of patients with different types of leukemia and MRD in cerebrospinal fluid and bone marrow specimens of the same patients, and its role in assessing the prognostic value of patients was discussed.
Results
Among the 199 acute leukemia cases, a total of 31 cases (15.58%) were positive MRD in the cerebrospinal fluid, of which 18 cases (58%) were detected earlier than the corresponding bone marrow specimens. Among the 19 patients with acute T lymphoblastic leukemia, 134 patients with acute B lymphoblastic leukemia, and 46 patients with acute myeloid leukemia counted, there were 4, 18, and 9 patients with positive MRD in the cerebrospinal fluid. The Kappa value of the concordance test between the results of cerebrospinal fluid MRD and bone marrow MRD in different types of acute leukemia was only 0.156, demonstrating a low concordance between them.
Conclusion
Dynamic monitoring of cerebrospinal fluid MRD by FCM can be used as a monitoring index for central nervous system leukemia, and monitoring cerebrospinal fluid can detect MRD earlier compared with bone marrow, which complements each other as a sensitive index for evaluating prognosis with significant guidance in clinic.
Keywords: flow cytometry, cerebrospinal fluid, acute leukemia, minimal residual disease
急性白血病是一种造血干细胞突变引起的,易于复发、致死率高的恶性克隆性血液系统疾病,按照突变细胞不同可分为起源于淋巴细胞恶性增生的急性淋巴细胞白血病(acute lymphoblastic leukemia,ALL)和起始于髓系造血祖细胞或前体细胞的急性髓系白血病(acute myeloid leukemia,AML)。微小残留病(minimal residual disease,MRD)是指急性白血病病人经过医治后到达完全缓解效果,而体内仍残留有微量白血病细胞的状态[1]。随着全球医疗技术水平的不断提高,急性白血病患者经治疗后达到完全缓解的概率有很大提升,但急性白血病的致死率仍然居高不下,有很大一部分患者经过治疗后出现复发,最终导致死亡,最主要原因是体内MRD的持续存在[2-3]。近年来研究[4]表明:MRD的检测结果和急性白血病复发风险高度相关,包括髓内复发和髓外复发[以中枢神经系统白血病(central nervous system leukemia,CNSL)为主],同时也是目前影响临床急性白血病治疗效果的主要因素之一。
国内外研究[5-6]表明MRD检测不仅可用于评价急性白血病的疗效,还可用于指导治疗方法的选择和提前干预。因此,MRD检测已成为降低白血病复发率、病死率、提高疗效和生存质量的关键环节之一。然而,MRD的细胞数目稀少,易与正常细胞混杂,检测方法的选择尤为重要。目前研究有多种检测MRD的方法,包括传统细胞形态学、荧光原位杂交技术、细胞遗传学、实时荧光定量PCR和流式细胞术(flow cytometry,FCM)等[7-8]。其中FCM以其简便、高效、灵敏、精准等优点,且对ALL和AML的诊断和治疗覆盖度极高,被临床所广泛认可[9]。
本研究旨在通过应用FCM动态监测不同类型急性白血病患者的脑脊液标本MRD,并与骨髓标本MRD进行比较,以期为指导临床急性白血病合理的个性化治疗、改善患者预后以及预防CNSL提供依据。
1. 对象与方法
1.1. 对象
选择2018年10月至2022年1月广东省人民医院(以下简称“我院”)血液科收治的急性白血病患者。纳入标准:在我院进行过脑脊液MRD检测和骨髓MRD检测;均按国际标准MICM分型进行细胞形态检测、细胞免疫表型检测、染色体检测及BCR::ABL1、PML::RARA融合基因的检测等进行诊断;病历记录较为完整详细。本研究已通过我院伦理审查委员会批准(审批号:KY-Q-2022-011)。
1.2. 仪器与试剂
FACSCanto II/FACSCanto TM流式细胞仪(三激光十色)、其他配套耗材、校准小球、商品化荧光素标记的流式抗体、红细胞裂解液、破膜剂、PBS缓冲液均购自美国BD公司。
1.3. 方法
1.3.1. 标本采集方法
采集骨髓和脑脊液标本,根据白血病患者初诊的免疫学分型选择单克隆抗体组合,按照试剂说明书制备样本及染色,取相应支数的流式测定管,按样品号编号,并在管上注明加入的抗体。各管加入相应组合的荧光抗体,取样品50 μL分别加入各试管中,混匀后置于避光处室温孵育20 min。然后加入裂解液2 mL,混匀后于室温避光裂解红细胞10 min。待红细胞裂解后,以1 200/min离心5 min,弃上清液。加入PBS 2 mL重悬细胞,混匀后以1 200/min离心 5 min,弃上清液。最后加入固定液300 μL重悬细胞,混匀后于4 ℃冰箱避光保存,24 h以内上机分析。
1.3.2. FCM检测
根据每个患者在最初诊断时的免疫表型及与正常细胞发育不同的特点,确立白血病相关的免疫表型作为MRD标志物。根据不同抗原与相应荧光标记的单克隆抗体发生特异性结合的特性,采用FCM分析所测细胞是否为白血病细胞,以及其免疫分型和分化程度,从而高效客观、灵敏准确、定量多参数地检测患者体内有无残留的MRD细胞。
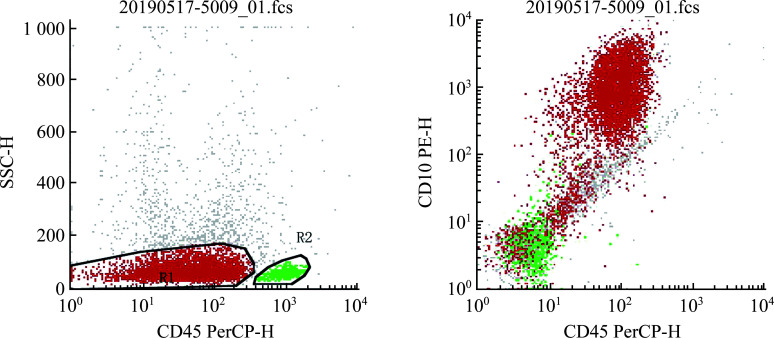
首先,采用CD45/SSC设门,特异性将白血病细胞与正常细胞群分离,R1细胞群和R2细胞群见图1。接着,再根据不同抗原表达情况进一步设门分析原始或幼稚的白细胞,以区别MRD细胞和正常细胞群。
图1.
FCM检测MRD的结果
Figure 1 Result of using flow cytometry (FCM) to detect minimal residual disease (MRD)
Using CD45/SSC gating to specifically separate leukemia cells from normal cell populations. Then, CD19 and CD10 antigen expression levels were used to further gate and analyze primitive or immature white blood cells, in order to distinguish between MRD cells and normal cell populations.
1.3.3. 脑脊液MRD阳性与骨髓MRD阳性时间的比较
在脑脊液中检测出阳性结果时对同一患者的骨髓标本进行MRD动态监测,以3个月为界限,若在3个月(不含)内骨髓标本也出现阳性结果则认为脑脊液标本没有比骨髓标本更早发现MRD;若在3个月后骨髓标本才出现阳性结果或是骨髓标本一直未检测出阳性结果,则认为脑脊液标本可以比骨髓标本更早发现MRD。对脑脊液标本比骨髓标本更早发现MRD的患者进行时间统计(期间骨髓标本结果均为阴性的统计到最后一次检测时间为止)。在随访过程中,出现过1次及以上MRD阳性则判定为(+),只有全程结果为阴性才判定为(-)。
1.4. 统计学处理
采用SPSS 20.0统计学软件对数据进行分析。计数资料采用例数和百分比表示,组间较采用χ 2检验,以P<0.05为差异有统计学意义。结果一致性采用Kappa检验,Kappa值为0~0.2表示一致性微弱;0.21~0.40表示一致性一般;0.41~0.60表示中度的一致性;0.61~0.80表示高度的一致性;0.81~1.00表示几乎一致。
2. 结 果
2.1. 不同类型急性白血病患者脑脊液MRD结果
2.1.1. 不同类型急性白血病患者占比
本研究共纳入199例急性白血病患者,其中AML46例(23.12%),ALL153例,包括19例急性T淋巴细胞白血病(acute T lymphoblastic leukemia,T-ALL)患者(9.55%)、134例急性B淋巴细胞白血病(acute B lymphoblastic leukemia,B-ALL)患者(67.34%)。
2.1.2. 不同类型急性白血病患者脑脊液MRD阳性分布情况
在199例急性白血病患者中,脑脊液MRD阳性患者共有31例;在19例T-ALL患者、134例B-ALL患者及46例AML患者中,脑脊液MRD阳性患者分别有4例、18例和9例(表1)。
表1.
不同类型白血病脑脊液MRD检测结果分布情况
Table 1 Distribution of cerebrospinal fluid MRD test results for different types of leukemia
| 分型 | 阳性例数 | 阴性例数 | 阳性率/% |
|---|---|---|---|
| 合计 | 31 | 168 | 15.58 |
| T-ALL | 4 | 15 | 21.05 |
| B-ALL | 18 | 116 | 13.43 |
| AML | 9 | 37 | 19.57 |
MRD:微小残留病;T-ALL:急性T淋巴细胞白血病;B-ALL:急性B淋巴细胞白血病;AML:急性髓系白血病。阳性率指所检查标本中阳性结果的比例。
T-ALL、B-ALL和AML脑脊液MRD的阳性率分别为21.05%、13.43%和19.57%(表1)。不同分型间急性白血病脑脊液标本MRD阳性率的差异均无统计学意义(均P>0.05)。
2.2. 不同类型急性白血病患者脑脊液与骨髓标本MRD检测结果的一致性比较
199名急性白血病患者的平均随访时间为11.1个月。脑脊液与骨髓MRD检测结果的Kappa值为0.156,表明脑脊液检测MRD与骨髓检测MRD结果一致性较弱(表2)。
表2.
脑脊液与骨髓标本MRD分布例数及一致性检验结果
Table 2 MRD distribution and consistency test results of cerebrospinal fluid and bone marrow samples
| 骨髓 | 脑脊液 | 合计 | Kappa值 | 一致性强度 | |
|---|---|---|---|---|---|
| + | - | ||||
| + | 20 | 64 | 84 | 0.156 | 微弱 |
| - | 11 | 104 | 115 | ||
MRD:微小残留病。
2.3. 脑脊液MRD阳性与骨髓MRD阳性时间的比较
在上述脑脊液MRD阳性的31例患者中,18例(58%)患者脑脊液标本比骨髓标本更早发现MRD,13例(42%)患者脑脊液标本未比骨髓标本更早发现MRD。对18例脑脊液标本比骨髓标本更早发现MRD的患者的进行时间统计,结果发现脑脊液标本比骨髓标本更早发现MRD阳性的时间最大值为16个月,最小值为3个月,平均比骨髓标本7.71个月。因此,动态监测脑脊液标本可能比监测骨髓标本更早发现体内MRD变化情况。
3. 讨 论
研究[10]表明:无论是ALL还是AML,颅脑白血病事件发生率较高。白血病细胞可通过多渠道上行至中枢神经系统,而很多治疗药物却难以透过血脑屏障,中枢神经系统中的白血病细胞无法被有效消除而残留,因此CNSL是导致急性白血病患者复发和死亡的根本原因。MRD的检测结果和急性白血病复发风险高度相关,研究[11-13]证实MRD还是判断预后的独立因素。本研究通过回顾性研究发现脑脊液标本比骨髓标本可能更早检测出白血病的MRD,对于CNSL患者的治疗和预后有一定的临床意义。
目前CNSL诊断金标准是在脑脊液中找到白血病细胞,但传统形态学敏感性差,会出现较多假阴性,导致临床漏诊率较高,为解决这一问题须采用高灵敏度和高特异性的检测。本研究采用FCM对脑脊液的MRD进行监测,FCM以其高灵敏度、高特异性和高覆盖率等优点而被临床认可,成为公认的检测MRD最主要的手段之一。已有研究[14-16]证明通过FCM对脑脊液MRD进行动态监测在CNSL的早期诊断和治疗中有非常重要的意义。在本研究中,各种类型急性白血病的脑脊液MRD检出率均较高,反映出有相当部分患者的中枢神经系统有残留的白血病细胞,通过对脑脊液MRD的动态监测可以极大程度提高CNSL的检出率。研究[17]表明:初诊时有无并发CNSL是评价儿童急性淋巴细胞白血病危险度的独立因素之一。因此,脑脊液MRD的检测可以作为急性白血病患者危险度分层的评价指标和为临床上中枢神经系统的定向治疗提供理论依据。
在本研究中,Kappa一致性检验的结果发现Kappa值为0.156,表明脑脊液MRD结果与骨髓MRD结果的一致性较弱。因此,笔者认为在大多时候检测同一患者体内的骨髓与脑脊液中是否残留白血病细胞的情况可能不一致,只检测骨髓MRD的结果不足以反映患者中枢神经系统的MRD。在MRD的检测中,同时监测骨髓和脑脊液十分重要。急性白血病的复发多见髓内复发,而中枢神经系统则是髓外复发最为常见的场所之一[18]。研究[19-20]发现临床直接治疗CNSL可以使复发率大大降低,通过对脑脊液MRD的检测结果结合骨髓MRD结果相互补充作为急性白血病治疗效果的评价指标,并以脑脊液MRD结果来判断是否需要对患者直接治疗CNSL,对降低患者的复发率有十分重要的意义。
本研究在31例MRD阳性患者中发现有18例患者脑脊液MRD可以比骨髓MRD更早检测出阳性,平均早发现7.71个月,其中以早3~6个月的患者占多数,因此笔者认为,动态监测脑脊液标本可能比监测骨髓标本更早发现患者体内MRD变化情况。目前国内外的研究大多集中于只检测骨髓中的MRD,较少同时对检测脑脊液MRD和骨髓MRD进行研究。但实际上,中枢神经系统才是白血病细胞残留最多的位置[21],一方面白血病细胞可通过毛细血管、神经等多种不同途径侵入中枢神经系统,脑脊液中营养丰富,有利于白血病细胞生长;另一方面由于血脑屏障的存在,脑脊液中的药物浓度难以达到治疗水平,在化学治疗过程中,中枢神经系统中的白血病细胞相对安全[22]。脑脊液的MRD检测有助于尽早评价急性白血病患者的疗效和预后。因此,采用FCM的方法检测急性白血病患者的脑脊液MRD,对制定合理的个体化治疗方案、改善患者预后及预防CNSL的发展十分重要。
本研究存在一定的局限性:首先,分析所用急性白血病患者的脑脊液MRD阳性样本较少,需要扩大样本数量以进一步研究脑脊液标本是否可以比骨髓标本更早诊出MRD;其次,由于脑脊液取材困难、有效细胞数少,目前仅有部分三甲医院开展FCM监测脑脊液MRD项目,未在临床上得到广泛应用。然而,对脑脊液MRD检测进行FCM分析可以提高CNSL的检出率,区分复发风险高和低的患者,可以为改善急性白血病患者预后的风险分层和中枢神经系统定向治疗提供实验室依据,降低患者的复发率。未来还需要更多的研究来证明脑脊液MRD监测作为判断急性白血病患者尤其是中枢神经系统浸润的患者预后的早期方法的临床应用价值。
基金资助
国家自然科学基金(82200118);广东省医学科学技术研究基金(B2021010);广东省基础与应用基础研究基金(2021A1515110860)。
This work was supported by the National Natural Science Foundation (82200118), the Guangdong Medical Science and Technology Research Foundation (B2021010), and the Guangdong Basic and Applied Basic Research Foundation (2021A1515110860), China.
利益冲突声明
作者声称无任何利益冲突。
作者贡献
罗燕飞 研究设计,数据分析,论文撰写与修改;林婷、冼璐桦、赵越、李文敏、刘均如、蓝名伟 数据收集与整理;单惠庄 研究设计,论文指导及修改。所有作者阅读并同意最终的文本。
Footnotes
http://dx.chinadoi.cn/10.11817/j.issn.1672-7347.2023.230243
原文网址
http://xbyxb.csu.edu.cn/xbwk/fileup/PDF/2023121838.pdf
参考文献
- 1. Blachly JS, Walter RB, Hourigan CS. The present and future of measurable residual disease testing in acute myeloid leukemia[J]. Haematologica, 2022, 107(12): 2810-2822. 10.3324/haematol.2022.282034. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 2. Bassan R, Brüggemann M, Radcliffe HS, et al. A systematic literature review and meta-analysis of minimal residual disease as a prognostic indicator in adult B-cell acute lymphoblastic leukemia[J]. Haematologica, 2019, 104(10): 2028-2039. 10.3324/haematol.2018.201053. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 3. 郭青, 金润铭. 微小残留病检测指导白血病治疗的研究进展[J]. 中国实用儿科杂志, 2016, 31(4): 264-268. 10.7504/ek2016040606. [DOI] [Google Scholar]; GUO Qing, JIN Runming. Progress of minimal residual disease detection in guiding the treatment of leukemia[J]. Chinese Journal of Practical Pediatrics, 2016, 31(4): 264-268. 10.7504/ek2016040606. [DOI] [Google Scholar]
- 4. Aitken MJL, Ravandi F, Patel KP, et al. Prognostic and therapeutic implications of measurable residual disease in acute myeloid leukemia[J]. J Hematol Oncol, 2021, 14(1): 137. 10.1186/s13045-021-01148-5. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 5. 张静, 王宗慧. 白血病与淋巴瘤的微小残留病检测手段前景及临床意义探讨[J]. 现代肿瘤医学, 2022, 30(21): 4009-4013. [Google Scholar]; ZHANG Jing, WANG Zonghui. Prospects and clinical significance of detection methods for minimal residual diseases in leukemia and lymphoma[J]. Journal of Modern Oncology, 2022, 30(21): 4009-4013. [Google Scholar]
- 6. Li W. Measurable residual disease testing in acute leukemia: Technology and clinical significance[M]. Brisbane (AU): Exon Publications; 2022. Oct 16. Chapter 5. 10.36255/exon-publications-leukemia-measurable-residual-disease. [DOI] [PubMed] [Google Scholar]
- 7. Chen XY, Wood BL. Monitoring minimal residual disease in acute leukemia: technical challenges and interpretive complexities[J]. Blood Rev, 2017, 31(2): 63-75. 10.1016/j.blre.2016.09.006. [DOI] [PubMed] [Google Scholar]
- 8. 王卫国. 急性白血病微小残留病检测方法临床应用的研究进展[J]. 山东医药, 2017, 57(38): 110-113. 10.3969/j.issn.1002-266X.2017.38.036. [DOI] [Google Scholar]; WANG Weiguo. Research progress on clinical application of detection methods for minimal residual disease in acute leukemia[J]. Shandong Medical Journal, 2017, 57(38): 110-113. 10.3969/j.issn.1002-266X.2017.38.036. [DOI] [Google Scholar]
- 9. 陈晓红, 吴广胜, 农卫霞, 等. 流式细胞术动态监测微小残留病在急性髓系白血病治疗中的临床意义[J]. 吉林医学, 2021, 42(3): 561-564. [Google Scholar]; CHEN Xiaohong, WU Guangsheng, NONG Weixia, et al. Clinical significance of dynamic monitoring of minimal residual disease by flow cytometry in the treatment of acute myeloid leukemia[J]. Jilin Medical Journal, 2021, 42(3): 561-564. [Google Scholar]
- 10. 王永斌, 张俊, 苏勇, 等. 脑脊液流式细胞学检测在急性淋巴细胞白血病并发中枢神经系统白血病中的诊断价值[J]. 现代肿瘤医学, 2020, 28(10): 1723-1725. 10.3969/j.issn.1672-4992.2020.10.026. [DOI] [Google Scholar]; WANG Yongbin, ZHANG Jun, SU Yong, et al. The diagnosis value of cerebrospinal fluid flow cytology in acute lymphoblastic leukemia complicated with central nervous system leukemia[J]. Journal of Modern Oncology, 2020, 28(10): 1723-1725. 10.3969/j.issn.1672-4992.2020.10.026. [DOI] [Google Scholar]
- 11. Jongen-Lavrencic M, Grob T, Hanekamp D, et al. Molecular minimal residual disease in acute myeloid leukemia[J]. N Engl J Med, 2018, 378(13): 1189-1199. 10.1056/NEJMoa1716863. [DOI] [PubMed] [Google Scholar]
- 12. Buldini B, Maurer-Granofszky M, Varotto E, et al. Flow-cytometric monitoring of minimal residual disease in pediatric patients with acute myeloid leukemia: recent advances and future strategies[J]. Front Pediatr, 2019, 7: 412. 10.3389/fped.2019.00412. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 13. 张静, 李芹, 陈辉, 等. 流式细胞术检测急性白血病微小残留病变68例临床分析[J]. 宁夏医科大学学报, 2019, 41(12): 1288-1290. 10.16050/j.cnki.issn1674-6309.2019.12.024. [DOI] [Google Scholar]; ZHANG Jing, LI Qin, CHEN Hui, et al. Clinical analysis of 68 cases of minimal residual disease in acute leukemia detected by flow cytometry[J]. Journal of Ningxia Medical University, 2019, 41(12): 1288-1290. 10.16050/j.cnki.issn1674-6309.2019.12.024. [DOI] [Google Scholar]
- 14. 卢雨昕, 徐刚. 流式细胞术在诊断儿童中枢神经系统白血病中的意义[J]. 中国小儿血液与肿瘤杂志, 2022, 27(1): 36-39. 10.3969/j.issn.1673-5323.2022.01.008. [DOI] [Google Scholar]; LU Yuxin, XU Gang. Flow cytometry in the diagnosis of central nervous system leukemia in children[J]. Journal of China Pediatric Blood and Cancer, 2022, 27(1): 36-39. 10.3969/j.issn.1673-5323.2022.01.008. [DOI] [Google Scholar]
- 15. 陈东玉, 党惠兵, 臧玉柱, 等. 脑脊液流式细胞学在鉴别诊断小儿急性淋巴细胞白血病并中枢神经系统白血病中价值[J]. 实验与检验医学, 2021, 39(3): 577-580. [Google Scholar]; CHEN Dongyu, DANG Huibing, ZANG Yuzhu, et al. Value of cerebrospinal fluid flow cytology in differential diagnosis of acute lymphoblastic leukemia with central nervous system leukemia in children[J]. Experimental and Laboratory Medicine, 2021, 39(3): 577-580. 10.3969/j.issn.1674-1129.2021.03.023. [DOI] [Google Scholar]
- 16. 谭畅, 李凤, 蒲泽晏, 等. 脑脊液MRD联合乳酸脱氢酶检测在中枢神经系统白血病诊断中的应用价值[J]. 国际检验医学杂志, 2017, 38(16): 2190-2192. 10.3969/j.issn.1673-4130.2017.16.006. 28070973 [DOI] [Google Scholar]; TAN Chang, LI Feng, PU Zeyan, et al. Application value of cerebrospinal fluid MRLCs combined with lactate dehydrogenase detection in diagnosis of central nervous system leukemia[J]. International Journal of Laboratory Medicine, 2017, 38(16): 2190-2192. 10.3969/j.issn.1673-4130.2017.16.006. [DOI] [Google Scholar]
- 17. Kruse A, Abdel-Azim N, Kim HN, et al. Minimal residual disease detection in acute lymphoblastic leukemia[J]. Int J Mol Sci, 2020, 21(3): 1054. 10.3390/ijms21031054. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 18. Kaynar LA, Özkurt ZN, Savaş EM, et al. Is flow cytometry useful in determining central nervous system involvement in patients with hematological malignancy? Analysis with a prospective cohort[J]. Leuk Res, 2023, 131: 107332. 10.1016/j.leukres.2023.107332. [DOI] [PubMed] [Google Scholar]
- 19. Xue YJ, Wang Y, Lu AD, et al. Clinical analysis of pediatric T-cell acute lymphoblastic leukemia using the MRD-oriented strategy system[J]. Clin Lymphoma Myeloma Leuk, 2023, 23(7): 477-483. 10.1016/j.clml.2023.03.013. [DOI] [PubMed] [Google Scholar]
- 20. 陈晶, 张会峰, 贺政新. 脑脊液流式细胞术诊断儿童中枢神经系统白血病的效能[J]. 医疗装备, 2019, 32(22): 55-56. 10.3969/j.issn.1002-2376.2019.22.035. [DOI] [Google Scholar]; CHEN Jing, ZHANG Huifeng, HE Zhengxin. Diagnostic efficacy of cerebrospinal fluid flow cytometry in children with central nervous system leukemia[J]. Medical Equipment, 2019, 32(22): 55-56. 10.3969/j.issn.1002-2376.2019.22.035. [DOI] [Google Scholar]
- 21. Paul S, Short NJ. Central nervous system involvement in adults with acute leukemia: diagnosis, prevention, and management[J]. Curr Oncol Rep, 2022, 24(4): 427-436. 10.1007/s11912-022-01220-4. [DOI] [PubMed] [Google Scholar]
- 22. Thastrup M, Duguid A, Mirian C, et al. Central nervous system involvement in childhood acute lymphoblastic leukemia: challenges and solutions[J]. Leukemia, 2022, 36(12): 2751-2768. 10.1038/s41375-022-01714-x. [DOI] [PMC free article] [PubMed] [Google Scholar]