Points clés
Les traitements ciblés forment un groupe de médicaments oraux destinés au traitement des tumeurs qui hébergent des mutations oncogènes spécifiques chez des malades atteints de cancer.
De 30 %–50 % des malades atteints d’un cancer du poumon non à petites cellules avancé peuvent héberger une mutation sur laquelle il est possible d’intervenir et qu’il est possible d’identifier par analyse moléculaire d’un spécimen de biopsie ou chirurgical.
Les personnes qui reçoivent un traitement ciblé obtiennent généralement une amélioration de leurs symptômes, de leurs taux de réponse (réduction de la taille de la tumeur) et de leur survie globale par rapport à celles qui reçoivent une chimiothérapie classique.
Le traitement ciblé est en général bien toléré et ne comporte par les mêmes risques de nausées, d’alopécie, d’immunodépression et de neutropénie fébrile que la chimiothérapie.
Le cancer du poumon est la principale cause de décès par cancer au Canada et sa forme non à petites cellules (CPNPC) représente 85 % des cas1. Le cancer du poumon a été associé à un pronostic sombre, particulièrement chez les personnes dont la maladie est métastatique. Depuis l’approbation initiale en 2003 du géfitinib par Santé Canada pour le traitement du CPNPC avancé, les traitements ciblés sont devenus une option thérapeutique importante et sont désormais largement utilisés dans la pratique clinique.
Qu’est-ce qu’un traitement ciblé?
Les traitements ciblés forment un groupe de médicaments anticancéreux personnalisés. Tandis que la chimiothérapie attaque toutes les cellules à division rapide, les traitements ciblés visent les cellules cancéreuses qui hébergent des altérations génomiques oncogènes spécifiques. Ces altérations oncogènes sont le principal déclencheur de la croissance des cellules cancéreuses et on dispose à présent de traitements qui les ciblent. De 30 %–50 % des cas de CPNPC hébergent des altérations oncogènes, dont près de 50 %–75 % peuvent être ciblées2. La prévalence des altérations oncogènes spécifiques varie selon l’âge, le degré d’exposition au tabagisme, l’ethnicité et l’histologie2.
Les inhibiteurs de la tyrosine kinase à petites molécules sont le type de traitement ciblé le plus fréquemment utilisé contre le CPNPC; ils agissent en inhibant les tyrosines kinases. Les tyrosines kinases sont des protéines membranaires composées d’un domaine extracellulaire (qui se fixe aux ligands) et intracellulaire. Dans des conditions physiologiques normales, la liaison du domaine extracellulaire aux ligands entraîne la phosphorylation et l’activation hautement régulée des protéines en aval. La présence d’une altération oncogène provoque une activation constitutive de la tyrosine kinase (c.-à-d., qu’elle n’a plus besoin de ligand pour être activée), d’où croissance et prolifération des cellules cancéreuses. Les traitements ciblés s’attaquent au cancer en inhibant l’hyperactivation des tyrosines kinases. Concrètement, les traitements ciblés sont des médicaments oraux qui peuvent être pris à domicile et qui évitent aux malades de fréquents déplacements à l’hôpital pour y recevoir des traitements intraveineux.
Qui est admissible au traitement ciblé?
Pour vérifier si la personne est une bonne candidate au traitement ciblé, il faut procéder au profilage moléculaire de la tumeur. Le profilage moléculaire peut se faire sur la plupart des spécimens de biopsie, souvent sur l’échantillon déjà utilisé pour poser le diagnostic histopathologique initial de cancer. Dans certains cas, surtout lorsqu’il est difficile d’obtenir une biopsie, l’analyse de l’ADN tumoral circulant (sanguin) permet aussi d’identifier les altérations géniques liées à la tumeur. Les techniques de séquençage de nouvelle génération permettent de débusquer en parallèle plusieurs altérations. Leurs capacités se sont rapidement développées au Canada depuis quelques années; même si les délais varient, idéalement, il s’écoule 1 ou 2 semaines entre la biopsie et l’obtention des résultats. La figure 1 décrit le processus de sélection des malades en vue d’un traitement ciblé.
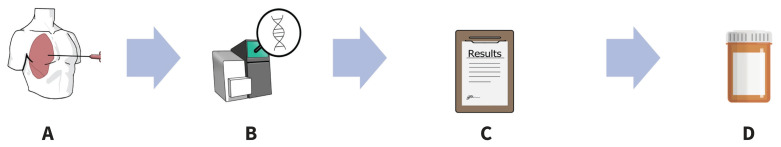
Figure 1:
Schéma illustrant le processus de sélection des malades en vue d’un traitement ciblé et sa prescription. (A) La personne subit une biopsie pour un diagnostic histopathologique de cancer du poumon non à petites cellules. (B) Le spécimen tumoral est envoyé pour analyse moléculaire. Si une mutation oncogène est détectée, la personne peut être candidate au traitement ciblé. (C) La personne revoit les résultats avec son oncologue et consent au traitement ciblé. (D) L’ordonnance peut être exécutée dans une pharmacie communautaire et le traitement ciblé peut être pris à domicile.
Dans la plupart des établissements, les épreuves moléculaires sont effectuées d’emblée (c.-à-d., à la demande de l’anatomopathologiste) dès qu’un nouveau cas de cancer du poumon non épidermoïde est diagnostiqué, alors que dans certains centres, elles doivent être prescrites par l’oncologue. De nombreux centres d’oncologie au Canada procèdent eux-mêmes aux épreuves moléculaires, mais d’autres doivent faire analyser leurs spécimens à l’extérieur. Tous les tests moléculaires standards peuvent être effectués au Canada.
Données probantes à l’appui des bienfaits
Le CPNPC métastatique est associé à un pronostic clinique sombre. L’efficacité des traitements contre le cancer se mesure généralement par les taux de réponse (proportion de malades obtenant une réduction substantielle de la taille de leur tumeur), la qualité de vie et la survie globale. Avant l’avènement des traitements ciblés pour la prise en charge du cancer du poumon métastatique, on administrait une chimiothérapie, et la survie médiane était inférieure à 9 mois, avec des taux de réponse de 25 %–35 %; et seulement 10 % de la patientèle survivaient audelà de 2 ans3.
Le traitement ciblé a énormément amélioré les résultats et la plupart des malades qui le reçoivent obtiennent une réduction majeure de la taille de leur tumeur, une amélioration de leurs symptômes et une survie plus longue4. Dans le contexte du cancer métastatique, les traitements ciblés sont administrés à des fins palliatives, avec pour objectif d’améliorer la qualité de vie et la survie globale plutôt que de guérir le cancer. Toutefois, 2 traitements ciblés, l’alectinib et l’osimertinib, ont donné lieu à une baisse significative du taux de récurrences lorsqu’ils étaient administrés en traitement adjuvant après une chirurgie pour un cancer non métastatique5,6.
Dix altérations différentes ont été identifiées et traitées au moyen de 20 agents ciblés efficaces (tableau 1)7. Des mutations du gène du récepteur du facteur de croissance épidermique (EGFR [epidermal growth factor receptor]) ont été découvertes en 2004 et comptent parmi les mutations les plus souvent identifiées en présence de CPNPC. Chez les personnes porteuses de la mutation EGFR classique, l’osimertinib, un inhibiteur de la tyrosine kinase de l’EGFR approuvé en 2021 par Santé Canada pour le traitement du CPNPC non métastatique, s’est révélé être l’agent optimal; il confère une survie globale médiane de 38,6 mois, contre 31,8 mois avec les inhibiteurs de la tyrosine kinase de l’EGFR d’ancienne génération8. Les personnes atteintes d’un CPNPC métastatique qui met en cause des translocations affectant le gène de la kinase du lymphome anaplasique (ALK [anaplastic lymphoma kinase]) obtiennent un taux de survie à 5 ans de plus de 60 % lorsqu’ils sont traités par alectinib, contre 45,5 % pour les personnes traitées par crizotinib, le premier inhibiteur de l’ALK approuvé9. Dans les cas de translocations impliquant le gène RET traités par selpercatinib, 84 % des malades ont obtenu une réduction majeure de la taille de leur tumeur et la réponse a persisté pendant près de 2 ans, même si aucun groupe de comparaison n’a été utilisé lors de cette étude de phase 2 qui ne comportait qu’un seul groupe10. La figure 2 montre la réponse radiographique chez une personne hébergeant la mutation du gène RET traitée par selpercatinib. Les agents ciblant les gènes KRAS, BRAF, MET, NTRK, ROS1 et HER2 ont aussi donné lieu à des bienfaits cliniques importants, même si, dans certains cas, les données sont trop récentes pour faire état des taux de survie à 5 ans2,4. Les personnes peuvent prendre leur traitement ciblé à domicile et obtiennent des taux de réponse remarquables, tout en maintenant leur qualité de vie et une bonne maîtrise de leurs symptômes, en plus d’avoir de meilleures chances de survie à long terme11–13.
Tableau 1:
Liste des traitements ciblés approuvés par Santé Canada selon les gènes porteurs d’altérations oncogènes7
| Gène affecté | Prévalence estimée dans les tumeurs de CPNPC*, % | Traitements ciblés approuvés |
|---|---|---|
| KRAS (G12C) | 12–15 | Sotorasib |
| EGFR | 12–15 | Afatinib, amivantamab, dacomitinib, erlotinib, géfitinib, osimertinib† |
| ALK | 2–7 | Alectinib, brigatinib, céritinib, crizotinib, lorlatinib |
| BRAF | 2–4 | Dabrafénib–tramétinib |
| MET | 3 | Capmatinib, tépotinib |
| ROS1 | 1–2 | Crizotinib, entrectinib |
| RET | 1–2 | Pralsétinib, selpercatinib |
| NTRK | < 1 | Entrectinib, larotrectinib |
Remarque: CPNPC = cancer du poumon non à petites cellules.
La prévalence varie significativement selon l’ethnicité.
L’osimertinib est approuvé comme traitement adjuvant après une résection chirurgicale.
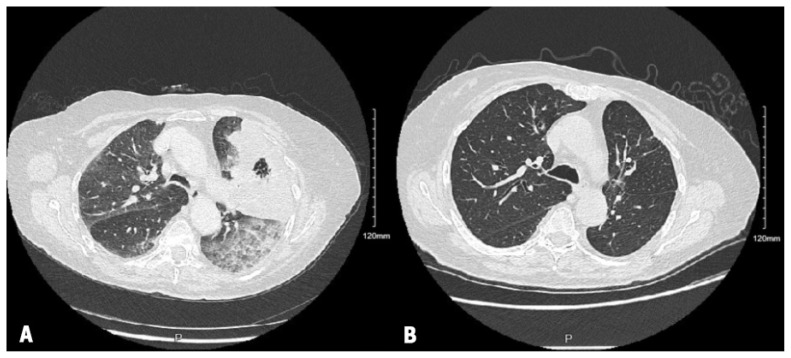
Figure 2:
Cliché de tomodensitométrie (TDM) axiale thoracique chez une femme de près de 80 ans atteinte d’un cancer du poumon métastatique hébergeant une altération du gène RET (exon 17 de l’ERC1 à exon 12 du RET) traité par selpercatinib (A) au moment du diagnostic et (B) 9 mois après le début du traitement, montrant une réponse radiographique sous la crosse de l’aorte.
L’efficacité des traitements ciblés est hétérogène; elle varie selon le médicament et la protéine ciblée. Cela entraîne des bienfaits variables sur les plans des taux de réponse, de la survie sans progression et de la survie globale. Étant donné la rareté de certaines mutations sur lesquelles il est possible d’intervenir, de nombreux agents ciblés ont été étudiés dans le cadre d’essais cliniques de phase 2 qui ne comportaient qu’un seul groupe.
Quels sont les risques?
Les traitements ciblés ont des profils d’innocuité plus favorables que la chimiothérapie. Les effets indésirables sont spécifiques à l’agent utilisé et à la protéine ciblée. Ces effets sont habituellement bénins et gérables avec de simples mesures de soutien. Le tableau 2 donne un aperçu des effets indésirables liés aux traitements ciblés. Si les symptômes persistent ou affectent la qualité de vie ou la capacité fonctionnelle d’une personne, il faut habituellement envisager des réductions de dose comme étape suivante dans la prise en charge. Les effets indésirables graves ou menaçant le pronostic vital sont rares. Le rapport risques:avantages des traitements ciblés sont presque toujours favorables au traitement, contrairement à la chimiothérapie cytotoxique classique. Et contrairement à la chimiothérapie, les traitements ciblés ne causent pas d’immunodépression notable et la plupart des épisodes de fièvre répondent aux soins cliniques habituels. Certains agents peuvent nécessiter des examens cardiaques (p. ex., électrocardiogramme, échocardiogramme). Cette surveillance est en général coordonnée par l’oncologue.
Tableau 2:
Effets indésirables liés aux classes d’agents, selon le gène visé*
| Gène visé | Effets indésirables courants | Effets indésirables graves |
|---|---|---|
| KRAS (G12C) | Fatigue, nausées, diarrhée, hausse des taux d’enzymes hépatiques, arthralgies | Pneumopathie |
| EGFR | Éruptions cutanées, anomalies unguéales, diarrhée | Pneumopathie, cardiomyopathie |
| ALK | Anomalies aux analyses de laboratoire (hausse du cholestérol ou des triglycérides, de la créatine kinase et du glucose), œdème périphérique, diarrhée, changements cognitifs‡ | Bradycardie, pneumopathie |
| BRAF | Pyrexie, nausées, diarrhée, hypertension | Cardiomyopathie |
| MET | Œdème périphérique, nausées, dyspnée, hausse de la créatinine, hausse de l’amylase sans pancréatite§ | Pneumopathie, épanchements pleuraux |
| ROS1 † | Diarrhée, nausées, troubles visuels, hausse des enzymes hépatiques, hypophosphatémie | – |
| RET | Diarrhée, sécheresse de la bouche, hypertension, nausées, œdème périphérique, hyponatrémie | – |
| NTRK | Fatigue, constipation, dysgueusie, étourdissements, dysesthésie, labilité de l’humeur, œdème périphérique | Troubles de l’humeur, risque accru de fractures (chutes) |
La liste des effets indésirables n’est pas exhaustive; les effets indésirables peuvent varier selon le médicament utilisé.
Dans certains cas, les inhibiteurs du récepteur tyrosine kinase neurotrophique (p. ex., entrectinib) sont aussi utilisés pour les mutations des protéines de fusion du gène ROS1; les effets indésirables communs sont énumérés à la rubrique du gène NTRK.
Les effets indésirables varient passablement d’un médicament à l’autre.
L’œdème périphérique est parfois notable.
Quelles sont les ressources nécessaires et comment accède-t-on aux traitements ciblés?
Les traitements ciblés sont habituellement plus coûteux que la chimiothérapie et parfois plus que l’immunothérapie. Des d’estimations calculées à partir des prix de gros en vigueur aux États-Unis, évaluent à 5000 $ US–10 000 $ US par mois le coût moyen d’un traitement ciblé. Les traitements durent en général jusqu’à l’apparition de signes de progression du cancer dans un contexte métastatique14,15. Toutefois, les coûts varient considérablement d’un agent à l’autre et au Canada, ils sont bien en deçà des tarifs, car les provinces bénéficient de rabais importants négociés par l’Alliance pharmaceutique pancanadienne, même si ces tarifs négociés ne sont pas divulgués publiquement. De façon générale, le coût des traitements ciblés devrait diminuer à mesure que d’autres agents verront leur brevet expirer et deviendront accessibles sous forme de médicaments génériques.
L’accès à ces médicaments diffère d’une province à l’autre, ce qui entraîne des disparités au Canada. Par exemple, les agents oraux sont remboursés de la même façon que les agents intraveineux dans certaines provinces (p. ex., la Colombie-Britannique), mais par des voies différentes dans d’autres provinces (p. ex., l’Ontario). L’accès aux traitements est difficile lorsqu’ils ne sont pas remboursés à l’échelle provinciale. Parmi les options offertes, mentionnons les régimes d’assurance publics ou privés, le paiement personnel et les programmes d’accès compassionnel ou de quote-part des sociétés pharmaceutiques.
L’avenir en la matière
Le traitement ciblé est la norme de soins pour le CPNPC métastatique dû à des altérations de certains oncogènes. À l’avenir, ces agents seront probablement utilisés à un stade moins avancé de la maladie et amélioreront les taux de guérison. Les traitements ciblés se perfectionneront à mesure qu’on intégrera les tests moléculaires à la pratique habituelle et que l’on identifiera plus de cas arborant des mutations qu’il est possible de cibler. On découvre toujours plus de ces altérations. Depuis la découverte de la première mutation (EGFR) en 2004, à la seconde (protéines de fusion ALK) en 2009, 10 altérations ont été identifiées et d’autres sont à l’étude. De plus, à mesure que les mécanismes de résistance aux traitements ciblés seront mieux compris, de nouveaux agents seront créés pour s’attaquer aux clones de cellules cancéreuses résistantes.
Remerciement
Les auteurs remercient Joshua Bélair pour son aide à la préparation de la figure 1.
Voir la version anglaise de l’article ici: www.cmaj.ca/lookup/doi/10.1503/cmaj.231562 ; pour le point de vue de la patiente au sujet du traitement ciblé contre le cancer, voir www.cmaj.ca/lookup/doi/10.1503/cmaj.240465-f
Footnotes
Intérêts concurrents: Natasha Leighl déclare avoir reçu des subventions de recherche ou une aide matérielle des sociétés Amgen, AstraZeneca, Eli Lilly, EMD Serono, Guardant Health, Inivata, Janssen, Merck Sharp & Dohme, Novartis, Pfizer, Roche et Takeda; des honoraires des sociétés BeiGene, Bristol Myers Squibb, Janssen, Merck, Novartis et Takeda; des bourses de voyage des sociétés AstraZeneca, Merck Sharp & Dohme, Roche, Janssen, Sanofi et Guardant Health; et elle a participé à des comités de surveillance de la sécurité des données pour les sociétés Mirati et Daichii Sankyo. Normand Blais fait état d’honoraires reçus des sociétés Amgen, AstraZeneca, Bayer, BeiGene, Bristol Myers Squibb, Eli Lilly, EMD Serono, Ipsen, Janssen, Merck, Novartis, Pfizer, Roche, Sanofi, Servier et Takeda. Paul Wheatley-Price déclare avoir reçu des honoraires de consultation des sociétés Merck, AstraZeneca, Roche, Bristol Myers Squibb, Amgen, Lilly, Novartis, Sanofi, Pfizer, GSK, Janssen, SteriMax, Bayer et Daiichi Sankyo. Il a participé à des comités de surveillance de la sécurité des données pour les essais REaCT-HER TIME et POISE en plus d’être président sortant et membre du conseil d’administration de l’organisme Cancer pulmonaire Canada. Aucun autre intérêt concurrent n’a été déclaré.
Cet article a été révisé par des pairs.
Les auteurs ont obtenu le consentement de la patiente.
Collaborateurs: Tous les auteurs ont contribué à l’élaboration et à la conception de l’étude ainsi qu’à l’ébauche du manuscrit, ont révisé de façon critique son contenu intellectuel important, ont donné leur approbation finale pour la version destinée à être publiée et assument l’entière responsabilité de tous les aspects du travail.
Traduction et révision: Équipe Francophonie de l’Association médicale canadienne
Références
- 1.Brenner DR, Poirier A, Woods RR, et al. Projected estimates of cancer in Canada in 2022. CMAJ 2022;194:E601–7. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 2.Chevallier M, Borgeaud M, Addeo A, et al. Oncogenic driver mutations in non-small cell lung cancer: past, present and future. World J Clin Oncol 2021;12:217–37. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 3.Schiller JH, Harrington D, Belani CP, et al. Comparison of four chemotherapy regimens for advanced non-small-cell lung cancer. N Engl J Med 2002;346:92–8. [DOI] [PubMed] [Google Scholar]
- 4.Xiao Y, Liu P, Wei J, et al. Recent progress in targeted therapy for non-small cell lung cancer. Front Pharmacol 2023;14:1125547. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 5.Wu Y-L, Tsuboi M, He J, et al. Osimertinib in resected EGFR-mutated non-small-cell lung cancer. N Engl J Med 2020;383:1711–23. [DOI] [PubMed] [Google Scholar]
- 6.Solomon BJ, Ahn JS, Dziadziuszko R, et al. LBA2 ALINA: efficacy and safety of adjuvant alectinib versus chemotherapy in patients with early-stage ALK+ non-small cell lung cancer (NSCLC). Ann Oncol 2023;34:S1295–6. [Google Scholar]
- 7.Tsao AS, Scagliotti GV, Bunn PA, et al. Scientific advances in lung cancer 2015. J Thorac Oncol 2016;11:613–38. [DOI] [PubMed] [Google Scholar]
- 8.Ramalingam SS, Vansteenkiste J, Planchard D, et al. Overall survival with osimertinib in untreated, EGFR-mutated advanced NSCLC. N Engl J Med 2020;382:41–50. [DOI] [PubMed] [Google Scholar]
- 9.Mok T, Camidge DR, Gadgeel SM, et al. Updated overall survival and final progression-free survival data for patients with treatment-naive advanced ALK-positive non-small-cell lung cancer in the ALEX study. Ann Oncol 2020;31:1056–64. [DOI] [PubMed] [Google Scholar]
- 10.Drilon A, Subbiah V, Gautschi O, et al. Selpercatinib in patients with RET fusion-positive non-small-cell lung cancer: updated safety and efficacy from the registrational LIBRETTO-001 phase I/II trial. J Clin Oncol 2023;41:385–94. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 11.Majem M, Goldman JW, John T, et al. Health-related quality of life outcomes in patients with resected epidermal growth factor receptor–mutated non–small cell lung cancer who received adjuvant osimertinib in the phase III ADAURA trial. Clin Cancer Res 2022;28:2286–96. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 12.Solomon BJ, Mok T, Kim D-W, et al. First-line crizotinib versus chemotherapy in ALK-positive lung cancer. N Engl J Med 2014;371:2167–77. [DOI] [PubMed] [Google Scholar]
- 13.Petrillo LA, El-Jawahri A, Gallagher ER, et al. Patient-reported and end-of-life outcomes among adults with lung cancer receiving targeted therapy in a clinical trial of early integrated palliative care: a secondary analysis. J Pain Symptom Manage 2021;62:e65–74. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 14.Shih Y-CT, Smieliauskas F, Geynisman DM, et al. Trends in the cost and use of targeted cancer therapies for the privately insured nonelderly: 2001 to 2011. J Clin Oncol 2015;33:2190–6. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 15.Skinner KE, Fernandes AW, Walker MS, et al. Healthcare costs in patients with advanced non-small cell lung cancer and disease progression during targeted therapy: a real-world observational study. J Med Econ 2018;21:192–200. [DOI] [PubMed] [Google Scholar]