Resumen
Objetivo:
Mostrar la experiencia global actual de la hemodinamia en cardiopatías congénitas en Chiapas después de haber alcanzado los primeros 1000 casos realizados desde el inicio de nuestro programa.
Método:
A través de un estudio retrospectivo que abarcó de abril de 2016 a junio de 2023 revisamos los expedientes electrónicos del total de pacientes que fueron llevados a cateterismo cardiaco durante ese periodo.
Resultados:
Se realizaron un total de 1000 procedimientos, 581 en pacientes del sexo femenino, con una mediana de edad de 4 años (1 día a 77 años). Del total de los procedimientos, 115 (11.5%) fueron cateterismos diagnósticos y 885 (88.5%) intervencionistas.
Conclusiones:
El cateterismo cardiaco en cardiopatías congénitas en el Estado de Chiapas ha desplazado a la cirugía cardiaca en un amplio porcentaje, y los resultados obtenidos son sin duda alentadores, lo cual representa ya una descentralización en la atención de las cardiopatías congénitas en nuestro país.
Palabras clave: Cateterismo diagnóstico, Cateterismo intervencionista, Cardiopatía congénita, Chiapas
Abstract
Objective:
To show the global experience of the interventionism in congenital heart diseases in Chiapas from its inception to recent days.
Method:
Through a retrospective study from April 2016 to June 2023, we reviewed the electronic files of the total of patients who underwent cardiac catheterism during the same period of time.
Results:
A total of 1000 procedures were performed, 581 in female patients, with a median age of 4 years (1 day to 77 years). Of the total procedures, 115 (11.5%) were diagnostic catheterizations and 885 (88.5%) were interventional.
Conclusions:
Cardiac catheterization in pediatrics in Chiapas has displaced cardiac surgery in a large percentage, and the results that have been obtained are undoubtedly encouraging, which already represents a decentralization in the care of congenital heart diseases in our country.
Keywords: Diagnostic catheterization, Interventional catheterization, Congenital heart disease, Chiapas
Introducción
Fue en el año de 1844 cuando Claude Bernard, fisiólogo francés, desarrolló un técnica para pasar un catéter desde la vasculatura periférica hasta las cámaras cardiacas1. No obstante, fue Werner Forssmann, en 1929, quien bajo guía fluoroscópica fue el primero en documentar un cateterismo cardiaco derecho en seres humanos2.
Si bien se considera que la cardiología pediátrica intervencionista inició a principios de los años 1950 con la publicación de Rubio-Álvarez y Limón-Laso, quienes describieron un método para tratar la estenosis pulmonar y tricuspídea mediante un catéter ureteral modificado3,4, no fue sino hasta mediados de 1980 que un amplio espectro de intervenciones percutáneas en niños pudieron ser llevadas a cabo, dando como resultado que la cardiología intervencionista en cardiopatías congénitas abriera un horizonte hacia grandes avances tecnológicos, los cuales se han dado a pasos agigantados hasta el día de hoy.
Las cardiopatías congénitas son la anormalidad genética más común. En años recientes, la prevalencia reportada de enfermedades cardiacas congénitas se ha elevado a aproximadamente 9 por cada 1000 recién nacidos vivos5. Si hablamos de nuestra población mexicana, para poder hacer frente a este número creciente de pacientes con defectos cardiacos al nacer es importante contar con el mayor número de profesionales en la cardiología intervencionista pediátrica en diferentes partes de nuestro país. Como ya comentamos en una publicación previa, la mayor cantidad de recursos humanos y materiales disponibles para la atención de las cardiopatías congénitas se ha concentrado principalmente en la Ciudad de México. No obstante, en la última década se ha iniciado un proceso de regionalización, lo cual ha permitido ampliar la cobertura de atención de los niños con cardiopatías congénitas a diferentes áreas de nuestro país6. Uno de los lugares, sin duda, en dar un paso agigantado hacia la atención integral y completa de estos pacientes es el Estado de Chiapas. Como ya hemos publicado, hemos logrado disminuir de manera notoria la cantidad de pacientes enviados al centro del país, pudiendo solventar la gran mayoría de los padecimientos en nuestra institución. Si nos referimos a materia de salud, según el último censo del Instituto Nacional de Estadística, Geografía e Informática (INEGI), en Chiapas, el 52% de la población total cuenta con algún tipo de derechohabiencia a un sistema de salud. Esto traduce que un gran sector de la población del Estado no cuenta con ningún tipo de servicio médico.
Las cardiopatías congénitas ocupan uno de los primeros lugares en cuanto a causa de mortalidad en el Estado de Chiapas. Sin embargo, ya en nuestra publicación previa habíamos comentado que Chiapas ha sufrido una metamorfosis positiva desde el año 2016, mejorando la calidad en la atención médica ofrecida a los pacientes con cardiopatías congénitas de este Estado, lo cual ha logrado disminuir el envío de pacientes hacia otras entidades en nuestro país, favoreciendo la regionalización. Lo anterior es sin duda gracias a la madurez que con el tiempo ha adquirido nuestro programa de hemodinamia en cardiopatías congénitas, y más aún al compromiso con los pacientes, que cada vez es mayor en nuestro departamento de cardiología.
Método
Se llevó a cabo un estudio retrospectivo que abarcó el periodo de abril de 2016 a junio de 2023, en el que incluimos a todos los pacientes que fueron llevados a cateterismo cardiaco fuera este diagnóstico o tipo intervencionista. Revisamos el expediente electrónico del total de los pacientes llevados a cateterismo cardiaco en nuestro Estado en el periodo referido.
Cateterismo cardiaco
Para todo paciente que fue llevado a la sala de hemodinamia se entregó consentimiento escrito para firma por los familiares y posteriormente se realizó cateterismo cardiaco, obteniendo acceso vascular por vía venosa o arterial femoral, subclavio, yugular interno o carotídeo, dependiendo del tipo de procedimiento y del plan de la intervención. En los casos que tuvieron indicación precisa se utilizó heparina intravenosa a una dosis de 100 U/kg (dosis máxima: 5000 UI) al inicio del procedimiento y dosis de refuerzo cada 60 minutos después de la última dosis.
Análisis estadístico
Las variables categóricas son expresadas como números y porcentajes, y las variables continuas como mediana y rangos. Todo el análisis estadístico fue realizado con el programa SPSS y Microsoft Excel 2011.
Resultados
Hemos realizado una actualización en cuanto a nuestra casuística para dar a conocer la experiencia que nuestro grupo ha tenido en la atención de pacientes con cardiopatías congénitas desde el inicio de nuestro programa, ya que recientemente alcanzamos el primer millar de casos realizados. De los 1000 procedimientos realizados, 581 fueron en pacientes del sexo femenino, con una mediana de edad de 4 años (rango: 1 día a 77 años). Del total de los procedimientos, 115 (11.5%) fueron cateterismos diagnósticos y 885 (88.5%) intervencionistas (Fig. 1). Dentro de los primeros, cabe señalar que realizamos estudios sobre todo de test de vasorreactividad pulmonar con uso de oxígeno al 100% para medición de Qp: Qs, presión pulmonar, resistencias vasculares pulmonares y sistémicas, y por ende, para definir si un paciente era o no candidato a ser llevado a corrección quirúrgica. Así también, se realizaron estudios diagnósticos para corroborar el diagnóstico en pacientes con cardiopatías congénitas, sobre todo complejas.
Figura 1.
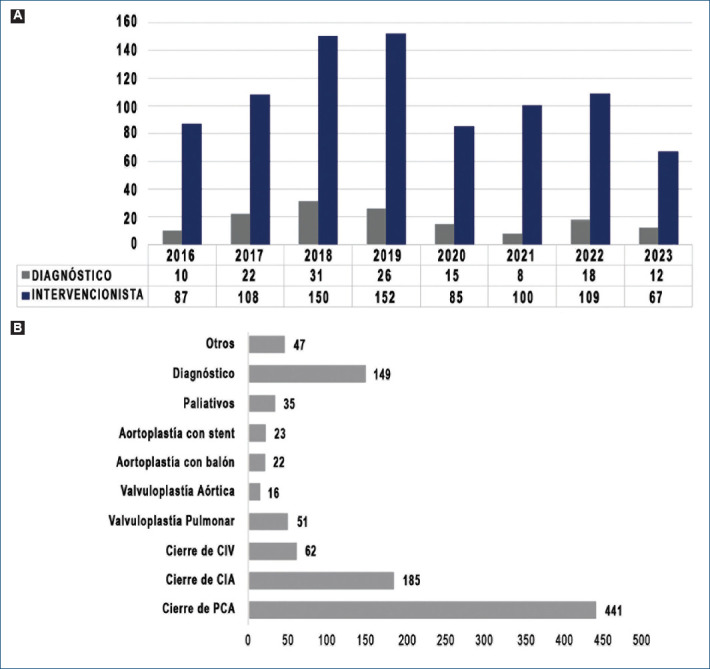
A: distribución específica por tipo de cateterismo cardiaco realizado. B: descripción del tipo de procedimiento de cateterismo cardiaco realizado. CIA: comunicación interauricular; CIV: comunicación interventricular; PCA: persistencia del conducto arterioso.
Con respecto al grupo de pacientes que llevamos a cateterismo intervencionista, podemos señalar que la mayoría de los estudios realizados fueron para cierre de conducto arterioso en un total de 441 pacientes (50.8%), cierre de comunicación interauricular en 185 pacientes (21.3%), cierre de comunicación interventricular en 62 pacientes (7.1%), valvuloplastia pulmonar con balón en 51 pacientes (5.8%), valvuloplastia aórtica con balón en 16 pacientes (1.8%), aortoplastia con balón en 22 pacientes (2.5%) y aortoplastia con stent en 23 pacientes (2.6%) (Fig. 2). Así mismo, hemos realizado otros procedimientos intervencionistas de alta complejidad que sin duda han permitido que en nuestro servicio podamos brindar atención no solo a pacientes chiapanecos, sino también de otros Estados como Veracruz, Villahermosa y Oaxaca, así como de otros países de Centroamérica, como Belice y Honduras (Fig. 3).
Figura 2.
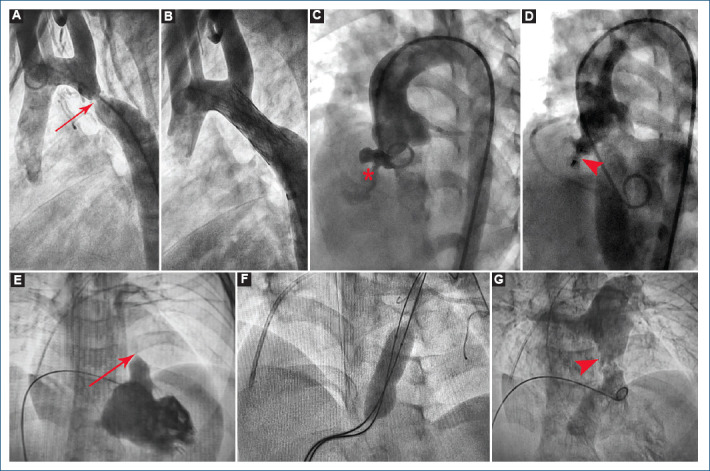
A: aortografía en arco aórtico en proyección lateral izquierda (LI) observando coartación aórtica (flecha). B: aortografía posterior a implantación de stent (aortoplastia con stent). C: ventriculografía izquierda en proyección de cuatro cámaras, observando el paso de medio de contraste a través de un defecto interventricular aneurismático (asterisco). D: ventriculografía izquierda posterior a cierre de comunicación interventricular con dispositivo Amplatzer® Duct Occluder (punta de flecha). E: ventriculografía derecha en proyección posteroanterior/craneal (PA/CRA) 30° observando estenosis valvular pulmonar grave (flecha). F: valvuloplastia pulmonar con técnica de doble balón. G: ventriculografía derecha posterior a valvuloplastia con mejoría importante en el paso de medio de contraste hacia la circulación pulmonar (punta de flecha).
Figura 3.
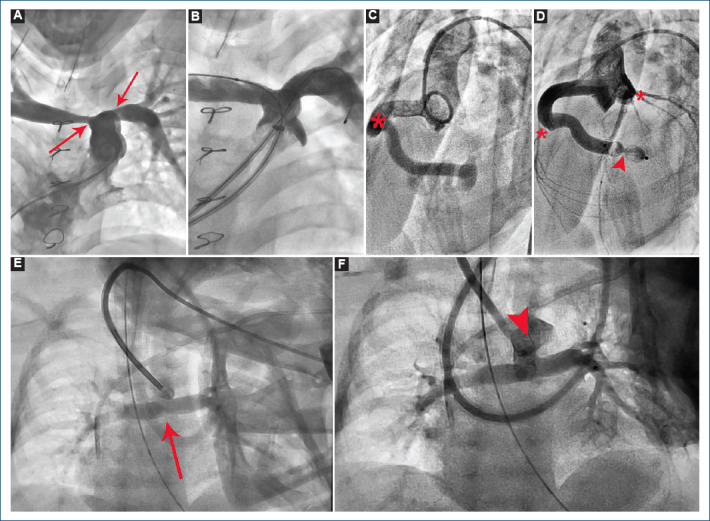
A: angiografía en tronco pulmonar en proyección posteroanterior/craneal (PA/CRA) 30° observando estenosis grave en el origen de ambas ramas pulmonares (flechas). B: angiografía en tronco pulmonar posterior a angioplastia con stent de ambas ramas pulmonares. C: aortografía en raíz aórtica en proyección axial larga observando fístula de la arteria coronaria derecha hacia el ventrículo derecho (asterisco); no se observa la distribución angiográfica coronaria habitual. D: angiografía dentro del origen de la fístula coronaria observando oclusión total con dispositivo Amplatzer® Vascular Plug II (punta de flecha), observando ya la distribución normal de las arterias coronarias (asteriscos). E: angiografía en proyección posteroanterior (PA) a nivel del origen del conducto arterioso por abordaje carotídeo; se observa escaso paso de medio de contraste hacia las ramas pulmonares (flecha). F: angiografía posterior a angioplastia con stent en conducto arterioso (punta de flecha).
Haciendo énfasis en los procedimientos que hemos realizado con mayor frecuencia, podemos decir que en los pacientes llevados a cierre de conducto arterioso utilizamos dispositivos Amplatzer®, siendo el más comúnmente utilizado el Amplatzer Duct Occluder® (ADO) en un total de 237 pacientes. En los demás pacientes utilizamos los dispositivos Amplatzer Duct Occluder II® (ADO II), Amplatzer Vascular Plug II® (AVP II), Amplatzer Vascular Plug IV® (AVP IV), Amplatzer Septal Occluder® (ASO) y otros de diferente marca, como Figulla®, Cocoon® y CERA®. El dispositivo ASO fue utilizado únicamente en pacientes con conductos amplios que no se lograron cerrar con el dispositivo de mayor diámetro exclusivo para cierre de conducto arterioso.
La mediana de edad fue de 6 años (rango: 20 días a 45 años) y la mediana de peso fue de 6.4 kg (rango: 1.7-69). La presión pulmonar media fue de 33 ± 6.6 mmHg y la media de Qp: Qs fue de 1.6 ± 0.4. En 19 pacientes se hicieron otro tipo de intervenciones además del cierre de conducto arterioso: en 11 cierre de comunicación interauricular, en 3 cierre de defecto septal interventricular, en 1 valvuloplastia aórtica con balón, en 2 valvuloplastia pulmonar con balón y en 2 aortoplastia con balón o stent (o ambos). Así también, comentar que del total de pacientes llevados a cierre de conducto arterioso, dos tuvieron un peso por debajo de los 2 kg al momento del procedimiento (un paciente de 1.9 kg y el otro de 1.7 kg), los cuales fueron resueltos sin ninguna complicación.
En cuanto a los pacientes que han sido llevados a cierre de comunicación interauricular, el dispositivo que con mayor frecuencia se utilizó fue el Amplatzer Septal Occluder®, en un total de 94 pacientes. Así también, se utilizaron dispositivos Cardia® (76 pacientes), CERA® (3 pacientes), Cocoon® (2 pacientes) y Figulla® (1 paciente). La media del tamaño de los dispositivos utilizados fue de 16 mm en los pacientes con una mediana de edad de 6 años (rango: 1-70), con una mediana de peso de 18 kg (rango: 6-110), una mediana de talla de 110 cm (rango: 60-175), presión pulmonar media de 30.5 ± 3.5 mmHg y media de Qp: Qs de 1.4 ± 0.3.
Con respecto a los pacientes que fueron llevados a cierre de comunicación interventricular, se utilizaron dispositivos AVP II en 33 pacientes, ADO en 14 pacientes, ADO II en 13 pacientes, dispositivo muscular en 1 paciente y ASO en 1 paciente. La mediana de edad fue de 6 años (rango: 1-30), con una mediana de peso de 19 kg (rango: 9.8-87), mediana de talla de 111 cm (rango: 72-175), presión pulmonar media de 34 ± 4.3 mmHg y media de Qp: Qs de 1.77 ± 0.3.
Cabe señalar que nuestro grupo ha adquirido gran experiencia en la realización de este tipo de procedimiento, ya que la casuística que tenemos hasta la fecha es cuantiosa, siendo nuestro centro uno de los que tienen mayor actividad en cuanto a tratamiento transcatéter de esta cardiopatía.
Como también se comentó en la publicación previa, hemos realizado procedimientos palitativos en pacientes que no podían ser llevados a una corrección quirúrgica total debido a la gran complejidad de su cardiopatía. Dentro de los procedimientos que realizamos se describen la angioplastía con stent en conducto arterioso o en fístula sistémica pulmonar ocluida en 27 pacientes (3.1%) y angioplastia con stent en el tracto de salida del ventrículo derecho en 8 pacientes (0.9%) con tetralogía de Fallot o con doble salida de ventrículo derecho y estenosis pulmonar grave. Asi mismo, realizamos diferentes procedimientos en pacientes con cardiopatías congénitas rescatables y que llegaron a nuestras salas de urgencias en estado crítico; dentro de estos podemos destacar procedimientos del tipo atrioseptostomía con balón en 13 pacientes, valvuloplastia aórtica crítica del recién nacido en 1 paciente, valvuloplastia pulmonar crítica con balón en 15 pacientes y aortoplastia con balón en coartación de aorta crítica en 20 pacientes.
Dentro de toda la experiencia que hemos acumulado en nuestros primeros años, hemos tenido casos con alto grado de complejidad y que se han acompañado de algunas complicaciones. Un paciente que fue llevado a cierre de conducto arterioso presentó como complicación una estenosis grave de la rama pulmonar izquierda, por lo que se requirió realizar angioplastia con stent en dicha rama y el paciente evolucionó de manera satisfactoria. En la publicación anterior reportamos también la embolización de dispositivos en cinco pacientes, lo cual representó el 1.3% en aquel momento; actualmente, el número de casos es de seis embolizaciones, que representa hoy día el 0.87% de un total de 688 procedimientos llevados a cabo para cierre de defectos septales y cortocircuitos aortopulmonares, lográndose el rescate percutáneo en cinco de ellos y con un solo paciente que requirió rescate quirúrgico. Así también, se reportaron otras complicaciones como embolización de stent PG2510B y desgarro de una rama accesoria de la vena femoral izquierda en una paciente que fue llevada a cierre de comunicación interauricular. Fueron reportadas también en la experiencia previa complicaciones importantes, como el caso de un pseudoaneurisma micótico en una paciente llevada a aortoplastia con stent y cierre de conducto arterioso con dispositivo, referida al Instituto Nacional de Cardiología y que se resolvió por vía quirúrgica con éxito. Otro caso fue el de una paciente en la que se sospechó erosión aórtica, por lo que fue llevada a tratamiento quirúrgico en el Centro Médico Nacional Siglo XXI, con buena evolución.
Y hablando sobre este tipo de casos con complicaciones de gran relevancia, tuvimos un paciente de 8 años con antecedente de corrección total de tronco arterioso tipo II a los 5 años de edad y que presentó como complicación esperada estenosis grave de ambas ramas pulmonares. El paciente fue llevado a angioplastia con stent de ambas ramas pulmonares, presentando durante la dilatación del balón de la rama pulmonar izquierda una apertura parcial del stent por ruptura secundaria iatrogénica del balón, lo cual se resolvió mediante una nueva técnica publicada por los autores (Fig. 4), la cual se mencionará mas adelante.
Figura 4.
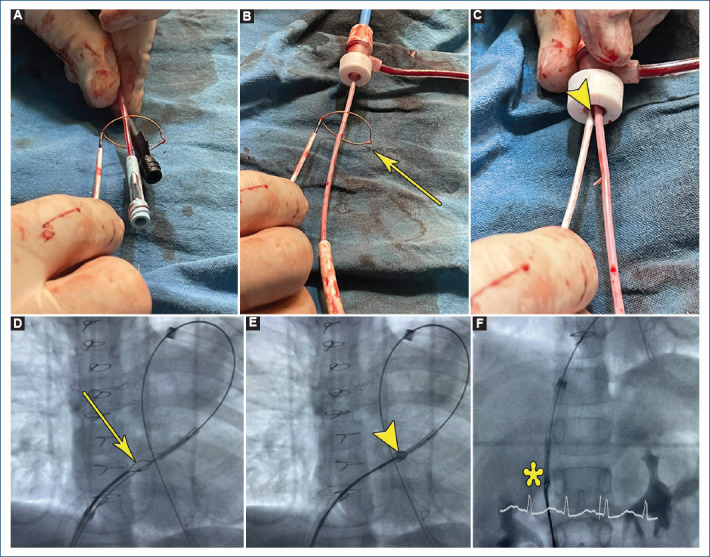
A: lazo avanzando a través de los lúmenes del catéter balón. B: lazo previo a cruzar la válvula hemostática (flecha) del introductor tipo Mullins. C: lazo dentro del introductor Mullins en el mismo lumen del catéter balón (punta de flecha). D: fluoroscopía. Lazo saliendo del introductor tipo Mullins y a través de la guía rígida y del catéter balón (flecha). E: fluoroscopía. Lazo atrapando y comprimiendo el extremo proximal del stent parcialmente dilatado (punta de flecha). F: fluoroscopía. Recuperación del stent hacia dentro del introductor tipo Mullins (asterisco) (imagen tomada de ref. 17, con autorización de los autores).
Reportamos una mortalidad del 1.8% en el total de los procedimientos realizados en nuestro Estado.
Discusión
Previo al inicio de nuestra experiencia en Chiapas se habían llevado a cabo algunos procedimientos intervencionistas en cardiopatías congénitas, como cierre de comunicación interauricular con dispositivo y aortoplastia con stent en dos pacientes adultos, además de un caso de cierre de conducto arterioso en un paciente pediátrico. Sin embargo, a partir del año 2016 se inició un programa formal de intervencionismo en nuestro Estado, el cual ha permitido otorgar grandes beneficios a través de procedimientos de cateterismo cardiaco a los pacientes con cardiopatías congénitas, llegando recientemente al caso número 1000.
En general, los procedimientos de cateterismo cardiaco que se realizan en el mundo son en su gran mayoría de índole intervencionista. En un estudio descriptivo realizado en Indonesia entre 2011 y 2017, el 91% del total de sus pacientes fueron llevados a cateterismo cardiaco intervencionista, y algo similar fue reportado en el Reino Unido, donde el porcentaje fue del 85%. En Pakistán, el número de procedimientos intervencionistas alcanzó el 50.4% de un total de 208 pacientes7-9. De todos los pacientes de nuestro estudio, el 88.5% fueron llevados a cateterismo cardiaco intervencionista.
Si bien la estadística de los procedimientos que hemos realizado desde un principio indica un alto índice de éxito, en la publicación anterior se hizo hincapié en las complicaciones que se presentaron en el periodo de estudio. En la literatura se han reportado varias complicaciones relacionadas con los dispositivos o con el procedimiento mismo. Dentro de las complicaciones que hemos tenido, una de ellas fue en un paciente llevado a cierre de comunicación interatrial con un nuevo dispositivo, el Cardia Ultrasept II®, el cual, después de la complicación ya informada previamente, decidimos dejar de utilizarlo y hacer uso de otros dispositivos, sobre todo de la marca Amplatzer®, mismos que hasta el momento se han utilizado sin ningún tipo de complicación. En general, en cuanto a la experiencia en el cierre de este tipo de defectos, tenemos un índice de cierre del 99.4%, ya que únicamente en un paciente no se logró el cierre debido a que el tabique interauricular estaba desalineado, por lo que se envío a corrección quirúrgica con buen resultado, y presentamos un índice de complicaciones del 1.6% del total de pacientes, representado por embolización del dispositivo en dos casos, los cuales fueron resueltos uno de forma percutánea y otro por vía quirúrgica, así como un caso de aparente erosión aórtica que, si bien aislamos este caso, representaría el 0.5% del total de procedimientos realizados. El estudio de cierre de defectos septales auriculares utilizando el dispositivo Amplatzer® (ASM PMS II), que fue un estudio prospectivo, no aleatorizado y multicéntrico, reportó un índice de cierre exitoso del 97.9%, reportando como una de sus complicaciones la erosión aórtica en el 0.3% del total de sus casos10. Butera et al.11 reportaron un índice menor del 1% de casos de embolización de dispositivos en 1013 pacientes.
En lo que respecta a la experiencia obtenida en el cierre de comunicación interventricular, hemos utilizado dispositivos más suaves y que se han implantado a través de sistemas liberadores con perfil más bajo, con la intención de disminuir las posibles complicaciones12. A la fecha hemos realizado 62 cierres de defectos perimembranosos y musculares, con una tasa de éxito del 100%, aunque con un índice de cierre del 95.2%, ya que en tres pacientes se presentó embolización del dispositivo, complicación que se resolvió durante el mismo evento de cateterismo cardiaco. No se reportó ningún caso de bloqueo atrioventricular completo. Otras publicaciones han reportado casos de bloqueo atrioventricular completo utilizando dispositivos más rígidos. En una revisión publicada en 2005 por Carminati et al.13, con 122 pacientes cateterizados, se reportó un 2.5% de riesgo para bloqueo cardiaco. En un periodo de estudio de 79 meses, Dilawar y Ahmad14 publicaron un total de 7 casos utilizando el dispositivo ADO 8/6 mm. Ebeid et al.15, en una revisión retrospectiva, reportaron un total de 20 pacientes utilizando el AVP II en 9 de ellos y el ADO II en 11 de ellos. El Said et al.16, en un análisis retrospectivo de 21 pacientes con comunicación interventricular perimembranosa, reportaron 19 pacientes con implantación exitosa de ADO. En la serie que publicamos en conjunto con dos instituciones más en el año 2020 reportamos el cierre en 118 pacientes utilizando ADO, ADO II y AVP II, con un índice de éxito del 98.3%12.
En general, sabemos que los procedimientos de cateterismo cardiaco en la población infantil no están exentos para nada de riesgos, ni por ende de complicaciones secundarias, tal como hemos mostrado en este artículo en el que compartimos nuestra experiencia tras haber iniciado el programa en el Estado de Chiapas. Sin duda, una de las complicaciones que ha tenido un alto impacto en nuestro quehacer como intervencionistas ha sido, como ya hemos comentado, el caso de un paciente de 8 años de edad que fue llevado a angioplastia con stent de ambas ramas pulmonares por estenosis grave de estas y presentó durante la angioplastia mala apertura de un stent por ruptura iatrogénica del balón en el que fue montado, lo cual imposibilitaba la recaptura del mismo. Esta eventualidad sin duda nos obligó a pensar en múltiples maneras en las cuales se podría resolver esta complicación, sin tener éxito, y finalmente con la ayuda de un lazo se logró capturar la porción proximal del stent (sitio parcialmente abierto), comprimiéndolo y capturándolo dentro del introductor largo. Esta técnica ha sido publicada recientemente17. Los avances tecnológicos han expandido las opciones terapeúticas para la rehabilitación de la estenosis de ramas pulmonares. Un estudio del Hospital de Niños de San Diego mostró que la ruptura de balones durante la implantación de un stent ocurría hasta en el 22.4% de los casos18. Otro estudio sobre complicaciones durante procedimientos de cateterismo cardiaco reportó en el año 2016 un índice de complicaciones del 14%, con un 9% de pacientes que fallecieron o presentaron eventos adversos mayores19.
Como ya comentamos en nuestra publicación previa, sigue siendo muy importante recalcar que, si bien somos un grupo relativamente joven, hemos logrado realizar una gran labor en pacientes con cardiopatías congénitas en nuestro Estado, y sin duda a lo largo de este tiempo hemos mejorado y madurado en nuestra toma de decisiones, y crecido a la vez en el ámbito de la investigación médica.
Conclusiones
La descentralización en la atención de las cardiopatías congénitas cada vez más se vuelve una realidad en nuestro país. La presencia de cardiólogos pediatras intervencionistas en varias partes de la República Mexicana ha hecho posible que el envío de pacientes hacia el centro del país sea cada vez menor. Sin duda, hoy en día la hemodinamia en el Estado de Chiapas se caracteriza por la atención global de todos los pacientes que así lo requieren, mostrando resultados muy positivos y alentadores que han permitido incluso que ya seamos centro de referencia para algunos otros Estados del sureste del país.
Agradecimientos
Nuestro agradecimiento a la Fundación Derechos de la Infancia, que desde un inicio nos brindó todo el soporte económico para la realización de todas las intervenciones a cientos de niños en nuestro Estado. Así también, agradecer infinitamente a la Fundación por la donación de la nueva sala de hemodinamia a nuestro hospital, con la cual contamos desde febrero del año 2022 y donde ya realizamos todos los procedimientos sin costo alguno para los pacientes.
Financiamiento
Ninguno.
Conflicto de intereses
Ninguno.
Responsabilidades éticas
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datos. Los autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informado. Los autores declaran que en este artículo no aparecen datos de pacientes.
Uso de inteligencia artificial para generar textos. Los autores declaran que no han utilizado ningún tipo de inteligencia artificial generativa en la redacción de este manuscrito ni para la creación de figuras, gráficos, tablas o sus correspondientes pies o leyendas.
Bibliografía
- 1.Bernard C. Leçons sur la chaleur animale. Paris: Bailliere et Fils; 1876. [Google Scholar]
- 2.Forssmann W. Die sondierrung des rechten Herzens. Klin Wochenschr. 1929;8:2085–7. [Google Scholar]
- 3.Rubio-Álvarez V, Limón-Lasón R, Soni L. Valvalotomías intracardiacas por medio de un catéter. Arch Inst Cardiol Mexico. 1953;23:183–92. [PubMed] [Google Scholar]
- 4.Rubio V, Limón-Lasón R. Treatment of pulmonary valve stenosis and of tricuspid valve stenosis using a modified catheter. Second World Congress of Cardiology Program Abstract. 1954;11:205. [Google Scholar]
- 5.Zhao QM, Liu F, Wu L, Ma XJ, Niu C, Huang GY. Prevalence of congenital heart disease at live birth in China. J Pediatr. 2019;204:53–8. doi: 10.1016/j.jpeds.2018.08.040. [DOI] [PubMed] [Google Scholar]
- 6.Calderón-Colmenero J, Cervantes-Salazar J, Curi-Curi P, Ramírez-Marroquín S. Problemática de las cardiopatías congénitas en México. Propuesta de Regionalización. Arch Cardiol Mex. 2010;80:133–40. [PubMed] [Google Scholar]
- 7.Dewi LGAP, Yantie NPVK, Gunawijaya E. Cardiac catheterization and percutaneous catheter in grown-up congenital heart diseases:single center experience at developing country. Med J Indones. 2018;27:38–43. [Google Scholar]
- 8.Somerville J. Grown-up congenital heart (GUCH) disease:current needs and provision of service for adolescents and adults with congenital heart disease in the UK. Heart. 2022;88(Suppl 1):i1–14. doi: 10.1136/heart.88.suppl_1.i1. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 9.Sultan M, Asif M, Maad U, Nadeem S, Khurram A, Hajira A. Cardiac catheterization in grown-up patients with congenital heart disease-indications and complications. Pak Heart J. 2012;45:174–9. [Google Scholar]
- 10.Shrivastava S, Shrivastava S, Allu SVV, Schmidt P. Transcatheter closure of atrial septal defect:a review of currently used devices. Cureus. 2023;15:e40132. doi: 10.7759/cureus.40132. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 11.Butera G, Romagnoli E, Carminati M, Chessa M, Piazza L, Negura D, et al. Treatment of isolated secundum atrial septal defects:impact of age and defect morphology in 1,013 consecutive patients. Am Heart J. 2008;156:706–12. doi: 10.1016/j.ahj.2008.06.008. [DOI] [PubMed] [Google Scholar]
- 12.Mijangos-Vázquez R, El-Sisi A, Sandoval-Jones JP, García-Montes JA, Hernández-Reyes R, Sobhy R, et al. Transcatheter closure of perimembranous ventricular septal defects using different generations of Amplatzer devices:multicenter experience. J Interv Cardiol. 2020;2020:8948249. doi: 10.1155/2020/8948249. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 13.Carminati M, Butera G, Chessa M, Drago M, Negura D, Piazza L. Transcatheter closure of congenital ventricular septal defect with amplatzer septal occluders. Am J Cardiol. 2005;96:52–8. doi: 10.1016/j.amjcard.2005.09.068. [DOI] [PubMed] [Google Scholar]
- 14.Dilawar M, Ahmad Z. Safety and efficacy of Amplatzer duct occluder for percutaneous closure of ventricular septal defects with tunnel shape aneurysm:medium term follow up. World J Cardiovasc Dis. 2013;3:228–33. [Google Scholar]
- 15.Ebeid MR, Batlivala SP, Salazar JD, Eddine AC, Aggarwal A, Dodge-Khatami A, et al. Percutaneous closure of perimembranous ventricular septal defects using the second generation Amplatzer vascular occluders. Am J Cardiol. 2016;117:127–30. doi: 10.1016/j.amjcard.2015.10.010. [DOI] [PubMed] [Google Scholar]
- 16.El Said HG, Bratincsak A, Gordon BM, Moore JW. Closure of perimembranous ventricular septal defects with aneurysmal tissue using the Amplazter Duct Occluder I:lessons learned and medium term follow up. Catheter Cardiovasc Interv. 2012;80:895–903. doi: 10.1002/ccd.23074. [DOI] [PubMed] [Google Scholar]
- 17.Mijangos-Vázquez R, Hernández-Reyes R. Partially open stent after balloon catheter iatrogenic perforation. How to solve this complication using a novel technique?The Mij-Her technique. Cardiol Young. 2022;33:144–6. doi: 10.1017/S1047951122001391. [DOI] [PubMed] [Google Scholar]
- 18.Ing Frank F. En:Informa Healthcare, editor. Complications during percutaneous interventions for congenital and structural heart disease. Boca Raton, FL: CRC Press; 2009. Stenting branch pulmonary arteries; pp. 95–116. [Google Scholar]
- 19.Lewis MJ, Kennedy KF, Ginns J, Crystal MA, Torres A, Vicent J, et al. Procedural success and adverse events in pulmonary artery stenting. JACC. 2016;67:1327–35. doi: 10.1016/j.jacc.2016.01.025. [DOI] [PubMed] [Google Scholar]


