RESUME
Objectif: Décrire les caractéristiques des patients atteints de (lupus érythémateux systémique (LES) ayant présenté une complication infectieuse et de déterminer la fréquence, le profil clinique, microbiologique et évolutif des infections rapportées.Méthodes: Etude descriptive, rétrospective menée au service de médecine interne La Rabta sur 11 ans ayant colligé les dossiers des patients atteints de LES ayant présenté un épisode infectieux.Résultats: Cinquante-six patients étaient colligés. Il s’agissait de 52 femmes et 4 hommes (genre ratio H/F= 0,07). L’âge moyen au moment du diagnostic du LES était de 35±13,8 ans. La durée moyenne d’évolution de la maladie était de 4,8±3,1ans. Soixante-dix-huit épisodes infectieux étaient notés. L’infection était inaugurale de la maladie chez 12 patients (21%) et était survenue après un délai moyen de 36 mois [1-156mois]. Quarante-trois patients (77%) recevait une corticothérapie et 37,5% un traitement immunosuppresseur. Les localisations les plus fréquentes étaient urinaires et pleuro-pulmonaires. L’agent causal était identifié dans 59 cas (76%). Les infections bactériennes étaient les plus fréquents (76%) dominées par les entérobactéries. Les infections virales (n=12) étaient dominées par le zona varicelle virus et le cytomégalovirus. Cinq patients avaient nécessité une prise en charge en réanimation. Une poussée lupique était notée au moment de l’épisode infectieux chez 20 patients. L’évolution était favorable chez 52 (93%) patients. Trois patients étaient décédés dans un tableau d’état de choc septique et un patient par une embolie pulmonaire probable.Conclusion: La survenue des complications infectieuses est responsable d’une morbi-mortalité importante au cours du LES. D’où l’importance d’un diagnostic précoce et d’une prise en charge adéquate.
ABSTRACT
Aim: To describe characteristics of systemic lupus erythematosus (SLE) patients with infectious complications and to determine frequency, clinical and microbiological features and outcomes of reported infections. Methods: This is a descriptive, retrospective study conducted over an 11-year period at the Internal Medicine Department La Rabta Hospital Tunis, collecting medical records of SLE patients who had experienced infectious complications. Results: Fifty-six patients were included, consisting of 52 females and 4 males (gender ratio M/F= 0.07). The mean age at SLE diagnosis was 35±13.8 years. The mean duration of the disease was 4.8±3.1 years. A total of seventy-eight infections were documented. Infection revealed the disease in 12 patients (21%) and occurred after an average delay of 36 months [1-156 months] of SLE diagnosis. Forty-three patients (74%) were receiving corticosteroid therapy, associated in 37.5% of cases with immunosuppressive treatment. Urinary and pleuro-pulmonary infections were most common infectious sites. An infectious agent was identified in 59 cases (76%). Bacterial infections were the most common (76%), dominated by the enterobacteria pathogen agent. Viral infections (n=12) were mainly caused by varicella-zoster virus and cytomegalovirus. Five patients required intensive care. Twenty patients experienced a lupus flare during the infectious episode. The outcome was favorable in 52 (93%) patients. Three patients died, two due to septic shock caused by pulmonary infection in two cases and cutaneous infection in one patient. One patient died from a probable pulmonary embolism. Conclusion: Infectious complications are responsible for significant morbidity and mortality during SLE. Hence the importance of early diagnosis and adequate management.
INTRODUCTION
Le lupus érythémateux systémique (LES) est une maladie auto-immune, multi-systémique chronique qui touche essentiellement la femme jeune en période d’activité génitale.
Elle se caractérise par la production des auto-anticorps pathogènes et une réaction inflammatoire incontrôlée (1).
Cette réaction inflammatoire peut cibler plusieurs organes à l’origine d’un grand polymorphisme clinique.
Le traitement de fond du LES repose sur les antipaludéens de synthèse.
Le recours aux corticoïdes, immunosuppresseurs et/ou biothérapies dépend de la nature et de la gravité des manifestations systémiques.
Le pronostic de cette maladie dépend du terrain, de la précocité de diagnostic et du traitement, de la présence des lésions viscérales graves et des complications infectieuses.
En effet les infections sont des complications fréquentes au cours du LES et constituent une source de morbidité et mortalité importante.
Elles sont responsables de plus de 20% d’hospitalisations des patients lupiques (2) et de 25% à 50% des décès (3, 4).
Plusieurs facteurs prédisposent aux infections, tel que la maladie lupique elle-même et les traitements utilisés, particulièrement les corticoïdes et les immunosuppresseurs.
L’objectif de cette étude était de décrire les caractéristiques épidémiologiques, cliniques, biologiques et thérapeutiques des patients atteints de LES ayant présenté une complication infectieuse et de déterminer la fréquence, le profil clinique, microbiologique et évolutif des infections rapportées chez ces patients.
méthodes
Il s’agit d’une étude rétrospective, descriptive et monocentrique menée à partir des dossiers médicaux des patients atteints de LES durant une une période de 10 ans allant de Janvier 2010 à Décembre 2021.
Le diagnostic de LES était retenu en se basant sur les critères de classification ACR 1997 (5) et/ou SLICC 2012 (6) et/ou ACR/EULAR 2019 (7 ).
L’épisode infectieux était retenu devant des manifestations cliniques évocatrices et des cultures positives.
En cas d’impossibilité d’isoler le germe, l’infection était retenue sur des arguments cliniques, biologiques et radiologiques évocateurs et sur la réponse thérapeutique.
Les patients lupiques ayant présenté une infection liée aux soins étaient exclus de notre étude.
L’étude statistique était réalisée à l’aide du logiciel SPSS version 25.
Les fréquences simples et les fréquences relatives (pourcentages) étaient calculées pour les variables qualitatives.
Les moyennes et l’écart-type étaient calculées pour les variables quantitatives.
résultats
Cinquante-six patients parmi 275 patients atteints de LES(20,3%) étaient colligés.
Il s’agissait de 52 femmes et 4 hommes avec un genre ratio H/F= 0,07.
L’âge moyen au moment du diagnostic du LES était de 35 ± 13,8 ans.
La durée moyenne d’évolution de la maladie était de 4,8 ± 3,1 ans avec des extrêmes de 0 et 11 ans.
Dix-huit patients (32%) avaient une ou plusieurs comorbidités : un diabète (n=9), une hypertension artérielle (n=7), une hypothyroïdie (n=5), une insuffisance coronaire (n=1), une dyslipidémie (n=1), un asthme (n=1) et une rhinite allergique chez un patient.
Les manifestations cliniques, les anomalies biologiques ainsi que le profil immunologique et thérapeutique des patients sont rapportés dans le tableau 1.
Tableau 1 : Profil clinique, biologique, immunologique et thérapeutique des patients colligés au moment de l’épisode infectieux .
| Manifestations cliniques | Effectif (%) |
|---|---|
| Atteinte cutanéo-muqueuse | 45 (80%) |
| Atteinte articulaire | 40 (71%) |
| Néphropathie glomérulaire | 25 (45%) |
| Péricardite | 17 (30%) |
| Pleurésie | 16 (29%) |
| Signes généraux | 14 (25%) |
| Atteinte neurologique | 11 (14%) |
| Atteinte digestive | 6 (11%) |
| Anomalies biologiques | |
| Anémie | 43 (77%) |
| Leucopénie | 22 (39%) |
| Lymphopénie | 46 (82%) |
| Neutropénie | 7 (12%) |
| Thrombopénie | 15 (27%) |
| Profil immunologique | |
| Anticorps anti-nucléaires | 56 (100%) |
| Anticorps anti-DNA | 45 (80%) |
| Anticorps anti-Sm | 22 (39%) |
| Anticorps anti nucléosome | 15 (27%) |
| Anticorps anti histone | 15 (27%) |
| Anticorps anti RNP | 8 (14%) |
| Anticorps anti Sm/RNP | 7 (12%) |
| Anticorps anti ribosome | 3 (5%) |
| Anticorps anti SSA | 20 (36%) |
| Anticorps anti SSB | 14 (25%) |
| Traitement | |
| Antipaludéens de synthèse | 41 (73%) |
| Corticoïdes | 43 (77%) |
| Cyclophosphamide | 17 (30%) |
| Azathioprine | 6 (11%) |
| Mycophenolate Mofétil | 2 (4%) |
| Méthotrexate | 1 (2%) |
Soixante-dix-huit épisodes infectieux étaient notés chez nos patients avec une fréquence moyenne de 1,3±0,7 épisode par patients (1-4).
Quinze patients avaient présenté plus qu’un épisode infectieux avec deux épisodes chez neuf patients, trois épisodes chez cinq patients et quatre épisodes infectieux chez un patient.
L’âge moyen de nos patients au moment du diagnostic de l’épisode infectieux était de 38,8 ± 14 ans.
L’infection était concomitante au diagnostic du LES chez 12 patients (21%) et était inaugurale de la maladie chez tous ces patients.
Chez les autres patients, déjà suivis pour un LES, une complication infectieuse était survenue après un délai moyen de 36 mois avec des extrêmes allant de 1 mois à 156 mois du diagnostic du LES.
Le tableau 2 résume les délais de survenue des complications infectieuses par rapport au diagnostic du LES.
Tableau 2 : Délai entre le diagnostic de la maladie lupique et la survenue des épisodes infectieux .
|
Délai (année) |
Effectif (%) |
|---|---|
|
<1 |
15 (27%) |
|
1-3 |
13 (23%) |
|
3-5 |
6 (11%) |
|
>5 |
10 (18%) |
Les infections urinaires et pleuro-pulmonaires étaient les localisations infectieuses les plus fréquentes dans notre étude.
Les localisations infectieuses sont résumées sur le tableau 3.
Tableau 3 : Répartition des différentes localisations infectieuses rapportées dans notre série .
|
Site infectieux |
Effectif (%) |
|
Urinaire |
38 (49%) |
|
Pleuro-pulmonaire |
13 (17%) |
|
Peau et tissus mous |
10 (13%) |
|
Digestif |
10 (13%) |
|
Hématologique |
4 (4%) |
|
Oculaire |
1 (1%) |
|
Osseux |
1 (1%) |
|
Ganglionnaire |
1 (1%) |
L’agent causal était identifié au cours de 59 infections(76%).
Les infections bactériennes étaient les plus fréquents, notées dans 49 cas (76% des infections).
Les entérobactéries étaient les germes les plus fréquents.
Les infections virales rapportées dans 12 cas étaient dominées par le zona varicelle virus (VZV) et le cytomégalovirus(CMV).
Le tableau 4 résume les différents germes responsables des épisodes infectieux dans notre série.
Tableau 4 : Répartition des germes responsables des épisodes infectieux .
|
Nature des germes |
Effectif (%) |
|---|---|
|
Bactérienne |
59 (76%) |
|
|
|
Virales |
12 (15%) |
|
|
|
Fongique |
5 (6%) |
|
|
|
Parasitaires |
2 (3%) |
|
Soixante-quatre hospitalisations étaient observées dont 37 hospitalisations pour prise en charge de l’épisode infectieux et 27 hospitalisations pour prise en charge de la maladie.
Cinq patients avaient nécessité une prise en charge en réanimation.
Chez neuf patients traités par Endoxan, un report des cures était indiqué devant la survenue de l’épisode infectieux.
Vingt patients (36%) avaient présenté une poussée lupique au moment de l’épisode infectieux.
Les poussées rénales et hématologiques étaient les plus fréquentes.
Chez ces patients, la CRP était élevée chez 10 patients avec un taux moyen de 63,5 mg/l avec des extrêmes de 49 et 377 mg/l.
Une hyperleucocytose était notée chez quatre patients.
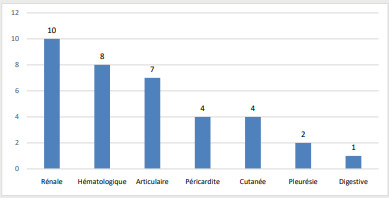
Les différentes poussées lupiques secondaires aux épisodes infectieux sont résumées sur la figure1.
Huit patients avaient plusieurs poussées concomitantes: articulaire et cutanée (n=2), articulaire et rénale (n=1),rénale et hématologique (n=1), articulaire et hématologique (n=1), rénale, articulaire et hématologique (n=1), rénale, hématologique avec épanchement pleural et péricardique(n=1) et cutanée, rénale avec un épanchement pleural(n=1).
Le traitement anti-infectieux était associé à celui de la poussée.
L’évolution était favorable chez 52 (92,8%) patients.
Trois patients étaient décédés dans un tableau d’état de choc septique.
Il s’agissait d’un état de choc à point de départ pulmonaire chez deux patients et cutané chez un patient.
Un patient était décédé par une embolie pulmonaire probable.
Figure 1. Répartition des différentes poussées observées dans notre série .
discussion
Les infections constituent l’une des principales causes de morbi-mortalité au cours du LES (8).
La fréquence des infections varie de 26% à 78% dans la littérature (9).
Elle était notée dans 20,3% des cas dans notre série
Cette fréquence est comparable à celle rapportée au Canada (25%) et en Inde (26,5%) (10, 11).
Elle est moins fréquente que celle observée en France (40%) et en USA (36,6) (12, 13)).
Dans notre série, La plupart des infections sont survenues au cours de la première année de la maladie (27%).
Nos résultats rejoignent ceux de la série chinoise de NG et al (14) et d’une série tunisienne de Jallouli et al (15).
Ceci renforce l’hypothèse de l’immunodépression induite par le LES lui-même.
Facteurs de risque et facteurs protecteurs
Le rôle protecteur des antipaludéens de synthèse a été suggéré par plusieurs études (16,17)
Dans notre série, 73,2% des patients étaient traités par un antipaludéen de synthèse au moment de l’épisode infectieux.
Dans l’étude prospective de Teh et al, publiée en 2018, portant sur 125 patients, 87,7% étaient sous hydroxychloroquine(16).
Cette même étude a conclu que l’hydroxychloroquine était un facteur protecteur (16).
De même dans l’étude de Herrinton et al, l’hydroxychloroquine avait un effet protecteur (17).
Ceci serait en raison de leurs propriétés anti infectieuses.
D’autres études suggèrent plutôt la responsabilité́ des corticoïdes et du traitement immunosuppresseur dans la majoration du risque infectieux chez les patients lupiques.
Dans notre étude, 77% et 37,5% des patients étaient traités par corticoïdes et immunosuppresseurs respectivement au moment de l’épisode infectieux
Nos résultats rejoignent ceux de Gladman, 80,7% et 37,6% des patients étaient sous corticothérapie et immunosuppresseurs respectivement lors de l’épisode infectieux ( 11 ).
En effet, une corticothérapie prolongée peut entraîner une lymphopénie et/ou une hypogammaglobulinémie, qui exposent à des infections opportunistes et/ou à des germes encapsulés ou encore à des infections virales ( 18 ).
Dans une étude rétrospective monocentrique française, la dose cumulée de corticoïdes était considérée comme le facteur de risque principal d’infection.
Ce risque était proportionnel à la dose et la durée des corticoïdes ( 13 ).
Ce risque est considéré comme élevé si la dose de prednisolone est >15mg ( 19 ).
Le cyclophosphamide (CYC) provoque une neutropénie à la fois par diminution de la production et une augmentation de la destruction des neutrophiles ( 20 ).
Le risque infectieux lié à l’utilisation du cyclophosphamide, est majoré par le fait qu’il est habituellement prescrit en association avec les corticoïdes.
Ce risque est plus important lorsque le cyclophosphamide est administré par voie orale que par voie veineuse discontinue, car la dose cumulée est plus importante.
Néanmoins, ce risque est moindre avec les autres immunosuppresseurs comme l’Azathioprine ou le Mycophénolate mofétil ( 18 ).
Germes incriminés et localisations infectieuses
Les infections au cours du LES peuvent toucher un ou plusieurs organes à la fois.
La prédominance de la localisation urinaire, respiratoire et cutanée était rapportée dans les différentes séries, dans plus des deux tiers des infections, ce qui rejoigne nos résultats (Tableau 5Tableau 5).
Tableau 5 : Localisations infectieuses dans notre série et dans la littérature .
| Auteurs | Nombre des épisodes infectieux | Localisations infectieuses les plus fréquentes |
|---|---|---|
|
Bosch et al, (28) |
63 |
|
|
Ruiz-Irastorza et al, (35) |
83 |
|
|
Navarro-Zarza et al, (9) |
297 |
|
|
Jallouli et al (15) |
146 |
|
|
Notre série |
78 |
|
Infections bactériennes
Les infections les plus fréquemment notées au cours du LES sont d’origine bactériennes rapportés dans 60% à 75% des cas ( 21 ).
Elle était notée dans 76% des cas dans notre série.
Le Streptococcus pneumonia (S.pneumonia), le staphylococcus aureus, l’Escherichia Coli, la salmonella non typhique et certaines mycobactéries sont les germes les plus incriminés ( 21 ).
Plusieurs études suggèrent que les patients lupiques sont plus susceptibles d’avoir une infection à S. pneumonia avec une fréquence de 6% à 18% de toutes les infections bactériennes avec des localisations pulmonaires survenant à un âge plus jeune et des formes plus sévères par rapport à la population générale (22,23)
Le Staphylococcus aureus est responsable de 15 à 35% des complications infectieuses chez les patients lupiques, principalement de la peau et des parties molles, mais également des articulations et des os( 21 ).
Les bactéries gram négatives sont les plus impliquées dans les infections des voies urinaires.
Escherichia Coli,est l’agent pathogène le plus fréquent.
Klebsiella spp. et Pseudomonas spp sont moins courants, mais également rapportés dans des différentes séries ( 1 ).
Les infections à Salmonella non typhiques, observé dans 7%% dans notre série, sont également fréquente au cours du LES( 24 ).
Elles sont souvent sources de formes septicémiques favorisées par le portage chronique ou de localisations rares (ostéoarticulaires, urinaires, endocardiques. . .)( 15 ).
Le Mycobacterium tuberculosis noté dans 3% des cas dans notre étude a une fréquence variant de 6 à 13% selon les études et notamment plus élevée dans les pays endémiques ( 25 )
La tuberculose au cours du LES est fréquemment extra-pulmonaire ( 19 , 25 ).
Dans notre étude, il s’agissait d’une tuberculose ganglionnaire et osseuse.
Infections virales
La fréquence des infections virales varie de 8,2% à 27,7% dans les différentes séries (11,15 ).
Elle était notée dans 15,3% dans notre série, dominée par les infections par le virus zona varicelle.
L’incidence annuelle des infections par le virus zona varicelle au cours du LES est de 6,4 à 32,5/1000 personnes-années (19 )
L’atteinte est souvent localisée au métamère mais des formes plus sévères et disséminées peuvent se voir (26).
Les infections par le CMV peuvent être asymptomatiques ou graves associant une réplication virale avec une atteinte spécifique d’organe susceptible de menacer le pronostic vital ou fonctionnel (27).
Infections fongiques et parasitaires
Comme dans notre étude, les candidoses représentent les complications fongiques les plus fréquentes.
Les localisations sont essentiellement buccales, buccoœsophagiennes et génitales (13,28 ).
Les infections parasitaires observées dans 3,5% des cas dans notre série, sont rapportées dans 4% à 10,2% dans la littérature ( 11 ,15).
Evolution
Les complications infectieuses constituent l’une des principales causes de morbi-mortalité au cours du LES.
Dans une cohorte européenne, sur une période de suivi de 10 ans, les infections constituaient la troisième cause de mortalité (25%), après les décès imputables à l’activité du LES elle-même (26,5%) et aux thromboses (26,5%) ( 29 ).
Tandis que les complications infectieuses étaient la première cause de décès dans les études de Abu-Shakra et al, Dhital et al, et Al-Adhoubi et al, (30-32) concordants avec nos résultats.
Particularités des complications infectieuses au cours du lupus
La différence entre une poussée lupique et une complication infectieuse est souvent difficile chez les patients lupiques vu la non-spécificité des signes généraux et du syndrome inflammatoire biologiques.
Certains marqueurs comme la CRP et la procalcitonine seraient rentables dans ce contexte.
Le taux faible de la CRP au cours des poussées, expliqué par une sa faible production au cours du processus inflammatoire ou par la sécrétion d’anticorps anti-CRP lors des poussées, rend ce marqueur intéressant notamment pour différencier une poussée lupique d’une infection bactérienne ( 33 , 34 ).
conclusion
Les infections sont des complications fréquentes au cours du LES.
Elles sont dominées par les infections urinaires, pulmonaires et cutanées.
Les atteintes viscérales graves de la maladie, l’utilisation des corticoïdes et des immunosuppresseurs s’avèrent être en rapport avec les épisodes infectieux.
La surveillance, le dépistage précoce des infections et la vaccination sont nécessaires au cours de cette pathologie afin de diminuer la fréquence et la gravité des complications infectieuses.
References
- Jung JY, Suh CH. Infection in systemic lupus erythematosus, similarities, and differences with lupus flare. Korean J Intern Med. 2017 mai;32(3):429–438. doi: 10.3904/kjim.2016.234. [DOI] [PMC free article] [PubMed] [Google Scholar]
- Goldblatt F, Chambers S, Rahman A, Isenberg D. Serious infections in British patients with systemic lupus erythematosus: hospitalisations and mortality. Lupus. 2009 juill;18(8):682–689. doi: 10.1177/0961203308101019. [DOI] [PubMed] [Google Scholar]
- Wang Z, Wang Y, Zhu R, Tian X, Xu D, Wang Q, et al. Long-term Survival and death causes of systemic lupus erythematosus in China: A systemic review of observational studies. Medicine. 2015 mai;94(17):e794. doi: 10.1097/MD.0000000000000794. [DOI] [PMC free article] [PubMed] [Google Scholar]
- Petri M. Infection in systemic lupus erythematosus. Rheumatic Disease Clinics of North America. 1998 mai;24(2):423–456. doi: 10.1016/s0889-857x(05)70016-8. [DOI] [PubMed] [Google Scholar]
- Hochberg MC. Updating the American College of Rheumatology revised criteria for the classification of systemic lupus erythematosus. Arthritis & Rheumatism. 1997 sept;40(9):1725–1725. doi: 10.1002/art.1780400928. [DOI] [PubMed] [Google Scholar]
- Petri M, Orbai AM, Alarcón GS, Gordon C, Merrill JT, Fortin PR, et al. Derivation and validation of the Systemic Lupus International Collaborating Clinics classification criteria for systemic lupus erythematosus. Arthritis & Rheumatism. 2012 août;64(8):2677–2686. doi: 10.1002/art.34473. [DOI] [PMC free article] [PubMed] [Google Scholar]
- Aringer M, Costenbader K, Daikh D, Brinks R, Mosca M, Ramsey-Goldman R, et al. 2019 European League Against Rheumatism/American College of Rheumatology classification criteria for systemic lupus erythematosus. Arthritis Rheumatol. 2019 sept;71(9):1400–1412. doi: 10.1002/art.40930. [DOI] [PMC free article] [PubMed] [Google Scholar]
- Kiriakidou M, Ching CL. Systemic lupus erythematosus. Annals of Internal Medicine. 2020 2 juin;172(11):ITC81–96. doi: 10.7326/AITC202006020. [DOI] [PubMed] [Google Scholar]
- Zonana-Nacach A, Camargo-Coronel A, Yañez P, Sánchez L, Jimenez-Balderas FJ, Fraga A. Infections in outpatients with systemic lupus erythematosus: a prospective study. Lupus. 2001 juill;10(7):505–510. doi: 10.1191/096120301678416088. [DOI] [PubMed] [Google Scholar]
- Shyam C, Malaviya AN. Infection-related morbidity in systemic lupus erythematosus: A clinico-epidemiological study from Northern India. Rheumatol Int. 1996 janv;16(1):1–3. doi: 10.1007/BF01419946. [DOI] [PubMed] [Google Scholar]
- Gladman DD, Hussain F, Iban D, Urowitz MB. The nature and outcome of infection in systemic lupus erythematosus. Lupus. 2002 avr;11(4):234–239. doi: 10.1191/0961203302lu170oa. [DOI] [PubMed] [Google Scholar]
- Costa-Reis P, Nativ S, Isgro J, Rodrigues T, Yildirim-Toruner C, Starr A, et al. Major infections in a cohort of 120 patients with juvenile-onset systemic lupus erythematosus. Clin Immunol. 2013 dec;149(3):442–449. doi: 10.1016/j.clim.2013.08.009. [DOI] [PubMed] [Google Scholar]
- Noel V. Risk factors and prognostic influence of infection in a single cohort of 87 adults with systemic lupus erythematosus. Ann Rheum Dis. 2001 dec;60(12):1141–1144. doi: 10.1136/ard.60.12.1141. [DOI] [PMC free article] [PubMed] [Google Scholar]
- Ng WL, Chu CM, Wu AKL, Cheng VCC, Yuen KY. Lymphopenia at presentation is associated with increased risk of infections in patients with systemic lupus erythematosus. QJM. 2006 janv;99(1):37–47. doi: 10.1093/qjmed/hci155. [DOI] [PubMed] [Google Scholar]
- Jallouli M, Frigui M, Marzouk S, Mâaloul I, Kaddour N, Bahloul Z. Complications infectieuses au cours du lupus érythémateux systémique : étude de 146 patients. Rev Med Interne. 2008 août;29(8):626–631. doi: 10.1016/j.revmed.2008.02.023. [DOI] [PubMed] [Google Scholar]
- Teh CL, Wan SA, Ling GR. Severe infections in systemic lupus erythematosus: disease pattern and predictors of infection-related mortality. Clin Rheumatol. 2018 août;37(8):2081–2086. doi: 10.1007/s10067-018-4102-6. [DOI] [PubMed] [Google Scholar]
- Herrinton LJ, Liu L, Goldfien R, Michaels MA, Tran TN. Risk of Serious Infection for Patients with Systemic Lupus Erythematosus Starting Glucocorticoids with or without Antimalarials. J Rheumatol. 2016 août;43(8):1503–1509. doi: 10.3899/jrheum.150671. [DOI] [PubMed] [Google Scholar]
- Michel M, Godeau B. Complications infectieuses des maladies systémiques. Réanimation. 2005 nov;14(7):621–628. [Google Scholar]
- Singh BK, Singh S. Systemic lupus erythematosus and infections. Reumatismo. 2020 nov 19;72(3):154–169. doi: 10.4081/reumatismo.2020.1303. [DOI] [PubMed] [Google Scholar]
- Mohamed DF, Habeeb RA, Hosny SM, Ebrahim SE. Incidence and risk of infection in Egyptian patients with systemic lupus erythematosus. Clin Med Insights Arthritis Musculoskelet Disord. 2014 janv;7:CMAMD.S15346. doi: 10.4137/CMAMD.S15346. [DOI] [PMC free article] [PubMed] [Google Scholar]
- Battaglia M, Garrett-Sinha LA. Bacterial infections in lupus: Roles in promoting immune activation and in pathogenesis of the disease. J Transl Autoimm. 2021;4:100078. doi: 10.1016/j.jtauto.2020.100078. [DOI] [PMC free article] [PubMed] [Google Scholar]
- Sciascia S, Cuadrado MJ, Karim MY. Management of infection in systemic lupus erythematosus. Best Pract Res Clin Rheumatol. 2013 juin;27(3):377–389. doi: 10.1016/j.berh.2013.07.002. [DOI] [PubMed] [Google Scholar]
- Schurder J, Goulenok T, Jouenne R, Dossier A, Van Gysel D, Papo T, et al. Pneumococcal infection in patients with systemic lupus erythematosus. Joint Bone Spine. 2018 mai;85(3):333–336. doi: 10.1016/j.jbspin.2017.05.012. [DOI] [PubMed] [Google Scholar]
- Abramson S, Kramer SB, Radin A, Holzman R. Salmonella bacteremia in systemic lupus erythematosus. Eight-year experience at a municipal hospital. Arthritis Rheum. 1985 janv;28(1):75–79. doi: 10.1002/art.1780280112. [DOI] [PubMed] [Google Scholar]
- Muhammed H, Jain A, Pattanaik SS, Chatterjee R, Naveen R, Kabeer H, et al. Clinical spectrum of active tuberculosis in patients with systemic lupus erythematosus. Rheumatol Int. 2021 déc;41(12):2185–2193. doi: 10.1007/s00296-021-04933-0. [DOI] [PubMed] [Google Scholar]
- Borba EF, Ribeiro ACM, Martin P, Costa LP, Guedes LKN, Bonfá E. Incidence, risk factors, and outcome of herpes zoster in systemic lupus erythematosus. JCR. 2010 avr;16(3):119–122. doi: 10.1097/RHU.0b013e3181d52ed7. [DOI] [PubMed] [Google Scholar]
- Chabert P, Hot A. Infection à cytomégalovirus au cours du lupus érythémateux systémique. Série de 12 cas cliniques et revue de la littérature. Rev Med Interne. 2021 avr;42(4):237–242. doi: 10.1016/j.revmed.2020.08.017. [DOI] [PubMed] [Google Scholar]
- Bosch X, Guilabert A, Pallarés L, Cervera R, Ramos-Casals M, Bové A, et al. Infections in systemic lupus erythematosus: a prospective and controlled study of 110 patients. Lupus. 2006 sept;15(9):584–589. doi: 10.1177/0961203306071919. [DOI] [PubMed] [Google Scholar]
- Cervera R, Khamashta MA, Font J, Sebastiani GD, Gil A, Lavilla P, et al. Morbidity and mortality in systemic lupus erythematosus during a 10-year period: a comparison of early and late manifestations in a cohort of 1,000 patients. Medicine (Baltimore) 2003 Sep;82(5):299–308. doi: 10.1097/01.md.0000091181.93122.55. [DOI] [PubMed] [Google Scholar]
- Abu-Shakra M, Urowitz MB, Gladman DD, Gough J. Mortality studies in systemic lupus erythematosus. Results from a single center. II. Predictor variables for mortality. J Rheumatol. 1995 juill;22(7):1265–1270. [PubMed] [Google Scholar]
- Dhital R, Pandey RK, Poudel DR, Oladunjoye O, Paudel P, Karmacharya P. All-cause hospitalizations and mortality in systemic lupus erythematosus in the US: results from a national inpatient database. Rheumatol Int. 2020 mars;40(3):393–397. doi: 10.1007/s00296-019-04484-5. [DOI] [PubMed] [Google Scholar]
- Al-Adhoubi NK, Al-Balushi F, Al Salmi I, Ali M, Al Lawati T, Al Lawati BSH, et al. A multicenter longitudinal study of the prevalence and mortality rate of systemic lupus erythematosus patients in Oman: Oman Lupus Study. Int J Rheum Dis. 2021 juin;24(6):847–854. doi: 10.1111/1756-185X.14130. [DOI] [PubMed] [Google Scholar]
- Meyer O. Anti-CRP antibodies in systemic lupus erythematosus. Joint Bone Spine. 2010;77(5):384–389. doi: 10.1016/j.jbspin.2010.04.010. [DOI] [PubMed] [Google Scholar]
- Kim HA, Jeon JY, An JM, Koh BR, Suh CH. C-reactive protein is a more sensitive and specific marker for diagnosing bacterial infections in systemic lupus erythematosus compared to S100A8/A9 and procalcitonin. J Rheumatol. 2012 Apr;39(4):728–734. doi: 10.3899/jrheum.111044. [DOI] [PubMed] [Google Scholar]
- Ruiz-Irastorza G, Olivares N, Ruiz-Arruza I, Martinez-Berriotxoa A, Egurbide MV, Aguirre C. Predictors of major infections in systemic lupus erythematosus. Arthritis Res Ther. 2009;11(4):R109. doi: 10.1186/ar2764. [DOI] [PMC free article] [PubMed] [Google Scholar]


