Abstract
目的
比较卵泡期和黄体期启动高孕激素状态超促排卵(PPOS)方案在35岁及以下卵巢储备功能减退(DOR)患者中的应用效果。
方法
回顾性分析2018年6月至2021年12月在温州医科大学附属第一医院生殖医学中心采用PPOS方案行体外受精/卵胞质内单精子注射-胚胎移植的483例35岁及以下DOR患者的资料,其中采用卵泡期PPOS方案226例(FPPOS+CC组),黄体期PPOS方案257例(LPPOS+CC组)。比较两组的基线特征、超促排卵结果和实验室相关指标,并比较获得第三天(以下简称D3)优质胚胎的患者超促排卵后第一次冻融胚胎移植的妊娠结局。
结果
两组间年龄、不孕年限、继发不孕占比、既往治疗周期数、体重指数、抗米勒管激素、窦状卵泡数、基础黄体生成素、基础孕酮水平、平均获卵数、MⅡ卵率、D3优质胚胎率、深度垂体抑制发生率、活产率和早产率等差异均无统计学意义(均P>0.05)。与FPPOS+CC组比较,LPPOS+CC组诱发排卵日黄体生成素(LH)水平[分别为4.0(2.7,5.3)和5.1(3.2,7.2)IU/L]、早发LH峰发生率(分别为3.13%和10.67%)、卵胞质内单精子注射双原核受精率(分别为72.16%和79.56%)均更低(P<0.05或P<0.01),而促性腺激素(Gn)天数[分别为11(9,12)和9(8,11)d]、Gn总量[分别为2213(1650,2700)和2000(1575,2325)IU]、诱发排卵日孕酮水平[分别为1.3(0.8,2.9)和0.9(0.6,1.2)ng/mL]、冻融胚胎移植的临床妊娠率(分别为61.88%和46.84%)和着床率(分别为42.20%和31.07%)均更高(均P<0.01)。
结论
35岁及以下DOR患者采用LPPOS+CC方案后冻融胚胎移植临床妊娠结局更佳。
Keywords: 卵巢储备功能减退, 黄体期,排卵, 卵泡期,孕激素, 胚胎移植, 妊娠结局
Abstract
Objective
To compare the pregnancy outcomes of luteal phase and follicular phase progestin-primed ovarian stimulation protocol with clomiphene citrate supplementation (LPPOS+CC and FPPOS+CC) in young women with diminished ovarian reserve (DOR).
Methods
A total of 483 women aged ≤35 years with DOR, who underwent in vitro fertilization (IVF)/intracytoplasmic sperm injection (ICSI)/embryo transfer (ET) with controlled ovarian stimulation using LPPOS+CC (n=257) or FPPOS+CC (n=226) protocols during June 2018 and December 2021 at the First Affiliated Hospital of Wenzhou Medical University, were included in this retrospective study. The baseline characteristics, superovulation results, laboratory related indicators between the two groups, and the pregnancy outcomes of women who achieved at least one high-quality cleavage-stage embryo or good-morphology blastocyst were compared between the two groups.
Results
No statistically significant differences were identified between the groups with respect to age, duration of infertility, proportion of secondary infertility, previous failed cycles, body mass index, anti-Müllerian hormone, antral follicle count, basal luteinizing hormone level, basal progesterone level, number of oocytes retrieved, oocyte maturation rate, high-quality cleavage-stage embryo cycle rate, the percentage of women with profound pituitary suppression, live birth rate and preterm birth rate (all P>0.05). The LH levels on the day of trigger [4.0 (2.7, 5.3) vs. 5.1 (3.2, 7.2) IU/L], the percentage of women with LH levels of >10 IU/L on the trigger day (3.13% vs. 10.67%), and the two pronucleus (2PN) rate of ICSI oocytes (72.16% vs. 79.56%) were significantly lower in the LPPOS+CC group than those in the FPPOS+CC group (P<0.05 or P<0.01). The duration of stimulation [11 (9, 12) vs. 9 (8, 11) d], the consumption of total gonadotropin [2213 (1650, 2700) vs. 2000 (1575, 2325) IU], the progesterone levels on the day of trigger [1.3 (0.8, 2.9) vs. 0.9 (0.6, 1.2) ng/mL], the clinical pregnancy rate [61.88% vs. 46.84%], and implantation rate [42.20% vs. 31.07%] in the LPPOS+CC group were significantly higher than those in the FPPOS+CC group (all P<0.01).
Conclusion
Compared to FPPOS+CC, the LPPOS+CC protocol appears to have better pregnancy outcomes for young women with DOR undergoing IVF/ICSI-ET.
Keywords: Diminished ovarian reserve; Luteal phase, ovulatian; Follicular phase,progestin; Embryo transfer; Pregnancy outcome
DOR是指卵母细胞数减少伴或不伴卵母细胞质量下降,引起女性生育能力下降,主要的评价指标包括AMH水平降低、窦状卵泡数减少、基础FSH水平升高[1-2]。人群中DOR的发生率为10%~35%[3]。与正常卵巢储备功能患者比较,DOR患者在辅助生殖技术治疗中获卵数更少,周期取消率更高[4]。由于辅助生殖技术治疗中获卵数与活产率之间存在显著相关性,因此对于寻求辅助生殖技术治疗的DOR患者,选择合适的超促排卵方案能提高获卵数、增加胚胎利用率,从而有助于改善其临床结局[5]。
尽管目前已经有多种超促排卵方案应用于DOR患者,但为DOR患者选择合适的方案仍然是一个挑战。近期多项研究表明,与采用长方案、短方案、拮抗剂方案或微刺激方案比较,DOR患者采用PPOS方案获卵数和可利用胚胎数更多[6-7]。然而,也有研究显示,PPOS方案由于持续使用孕激素会导致过度的垂体抑制[8]。本团队既往研究发现,与采用标准PPOS方案比较,35岁及以下DOR患者采用PPOS联合枸橼酸氯米芬方案(以下简称PPOS+CC方案)可以有效缓解垂体过度抑制,从而减少Gn用量[9]。本研究进一步采用卵泡期PPOS联合枸橼酸氯米芬(以下简称FPPOS+CC方案)和黄体期PPOS联合枸橼酸氯米芬(以下简称LPPOS+CC方案)超促排卵方案,观察年轻DOR患者在不同月经周期启动PPOS+CC方案超促排卵的临床结局,旨在为临床决策提供依据。
1. 对象与方法
1.1. 对 象
收集2018年6月至2021年12月在温州医科大学附属第一医院生殖医学中心采用PPOS+CC方案行IVF/ICSI-ET,且诊断为DOR的35岁及以下患者的临床资料。DOR的诊断须满足以下两个及以上条件:①基础FSH水平10 IU及以上;②FSH/LH比值为2及以上;③窦状卵泡数不超过8;④AMH不超过1.1 ng/mL。排除以下情况:①子宫畸形;②未经治疗的输卵管积水;③夫妻一方或双方染色体异常;④免疫性疾病或其他不利于妊娠的全身性疾病。对于有多个治疗周期的患者,选择第一个治疗周期。本研究通过温州医科大学附属第一医院伦理委员会审查(2020-02)。
1.2. 给药方法
1.2.1. FPPOS+CC方案
DOR患者于月经周期第2~3天开始每日口服10 mg醋酸甲羟孕酮(商品名为安宫黄体酮,2 mg/片,浙江仙琚制药股份有限公司)和100 mg枸橼酸氯米芬(商品名为法地兰,50 mg/片,塞浦路斯Codal Synto公司),并注射Gn,依据患者的年龄、基础FSH水平、窦状卵泡数和BMI选择起始剂量150~225 IU,定时监测卵泡发育大小及血清激素水平(FSH、LH、雌二醇和孕酮),根据卵泡发育情况和激素水平调整Gn用量,直至诱发排卵日。接受FPPOS+CC方案治疗的DOR患者纳入FPPOS+CC组。
1.2.2. LPPOS+CC方案
DOR患者于排卵后5~7 d开始使用10 mg醋酸甲羟孕酮+100 mg枸橼酸氯米芬+Gn。定时监测DOR患者卵泡发育大小及激素水平,根据卵泡发育情况和激素水平调整Gn用量,直至诱发排卵日。接受LPPOS+CC方案治疗的DOR患者纳入LPPOS+CC组。
1.3. 卵母细胞回收、IVF、冻融胚胎移植
当1~3个及以上优势卵泡直径在17 mm及以上时,予DOR患者皮下注射重组hCG注射液250 μg诱发排卵,36~38 h后在超声引导下经阴道穿刺取卵,取出的卵母细胞体外培养2~6 h后根据男方精液情况选择IVF或ICSI。卵母细胞取出后第3天进行卵裂期胚胎评估和培养,玻璃化冷冻卵裂期胚胎及囊胚。
所有患者均采用冻融胚胎移植,移植前内膜准备采用激素替代治疗方案,在月经来潮或药物撤退性出血的第2~5天开始口服戊酸雌二醇片,前四天每次2 mg,每天两次;后五天每次3 mg,每天两次;7~10 d后阴道超声检测子宫内膜厚度并监测外周血雌二醇、孕激素水平,酌情调整戊酸雌二醇的剂量。若子宫内膜厚度在8 mm及以上,则维持戊酸雌二醇剂量,同时给予孕激素转化内膜,转化内膜第4天移植卵裂期胚胎,第6天移植囊胚。所有胚胎移植均在腹部超声引导下进行。继续原剂量服用雌激素及黄体支持至移植后14 d。通过血清β-hCG水平判断是否妊娠,如未妊娠则停止黄体期支持;如妊娠则继续黄体支持直至妊娠10周停药。
1.4. 观察指标及判定结局
主要观察两种超促排卵方案过程中促排卵启动日、促排卵第4~5天及诱发排卵日的内分泌情况、超促排卵结果、妊娠结局和围产期结局。计算妊娠结局及围产期时,仅采用两种方案获得的胚胎首次移植且移植至少一个优质卵裂期胚胎(7~9个细胞,碎片率<20%)或囊胚(优于3BB级)[10]的移植周期。
使用Gn第8天超声检查未发现10 mm及以上的优势卵泡则取消周期。深度垂体抑制指诱发排卵日血清LH浓度低于1.0 IU/L[11];早发LH峰指诱发排卵日血清LH浓度超过10 IU/L[12]。MⅡ卵率(%)=MⅡ卵母细胞数/ICSI获卵数×100%;IVF 2PN受精率(%)=IVF 2PN受精数/IVF用于受精卵数×100%;ICSI 2PN受精率(%)=ICSI 2PN受精数/ICSI MⅡ卵母细胞数×100%;2PN受精卵裂率(%)=2PN受精卵裂数/2PN受精卵数×100%。移植后4~6周阴道超声检查可观察到宫内孕囊及原始心管搏动为临床妊娠;妊娠超过12周为持续妊娠;妊娠不足12周的流产为早期流产;12周至不足28周的流产为晚期流产;妊娠满28周但不足37周时分娩为早产;妊娠满28周及以上分娩的新生儿且7 d内有生命迹象为活产。新生儿的出生体重低于2500 g为低体重儿;新生儿的出生体重超过4000 g为巨大儿。
1.5. 统计学方法
使用SPSS 25.0进行统计分析。服从正态分布且方差齐性的计量资料以均数±标准差( ±s)表示,组间比较采用独立样本t检验,不满足方差齐性则采用连续矫正;非正态分布的计数资料以中位数(上下四分位数)[M(Q 1,Q 3)]表示,组间比较采用Mann-Whitney U检验;分类变量采用例数(百分比)[n(%)]或率(%)表示,组间比较采用χ 2检验或Fisher精确检验。采用二元logistic回归模型评估超促排卵方案类型、年龄、BMI、AMH水平、窦状卵泡数、Gn使用天数、Gn使用总量、获卵数、第三天(以下简称D3)优质胚胎数、是否深度垂体抑制、是否早发LH峰、移植日子宫内膜厚度等因素对临床妊娠的影响,计算OR值和95%CI。所有检验均为双侧检验,P<0.05为差异有统计学意义。
2. 结 果
2.1. 患者基线资料比较
共收集483例患者的临床资料,其中LPPOS+CC组257例,FPPOS+CC组226例,两组间年龄、不孕年限、继发不孕占比、既往治疗周期数、BMI、AMH、窦状卵泡数、FSH、LH及孕酮水平差异均无统计学意义(均P>0.05),见表1。提示两组基线资料具有可比性。
表1.
两组基线资料比较
| 组 别 | n | 年龄(岁) | 不孕年限(年) | 继发不孕 | 不孕因素* | 既往治疗周期数 | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 女方因素 | 男方因素 | 不明原因 | ||||||||||||
| LPPOS+CC组 | 257 | 34.0(30.9,35.0) | 2.2(1.0,5.0) | 181(70.43) | 138(53.70) | 81(31.52) | 50(19.46) | 0(0,1) | ||||||
| FPPOS+CC组 | 226 | 33.0(30.3,35.0) | 3.0(2.0,5.0) | 160(70.80) | 114(50.44) | 74(32.74) | 48(21.24) | 0(0,1) | ||||||
| Z/χ 2值 | — | -1.739 | -1.450 | 0.008 | — | — | — | -1.029 | ||||||
| P值 | — | >0.05 | >0.05 | >0.05 | — | — | — | >0.05 | ||||||
| 组 别 | n | BMI(kg/m2) | AMH(ng/mL) | 窦状卵泡数(个) | FSH(IU/L) | LH(IU/L) | 雌二醇(pg/mL) | 孕酮(ng/mL) | ||||||
| LPPOS+CC组 | 257 |
21.34 (20.00,23.73) |
0.79 (0.55,1.12) |
6(4,7) |
10.23 (7.83,13.84) |
3.82 (2.88,5.39) |
46.20 (34.20,61.00) |
0.47(0.33,0.64) | ||||||
| FPPOS+CC组 | 226 |
22.03 (20.11,24.85) |
0.83 (0.52,1.10) |
6(4,8) |
9.76 (7.50,13.32) |
3.88 (2.93,5.30) |
41.03 (26.90,59.85) |
0.47(0.34,0.70) | ||||||
| Z/χ 2值 | — | -1.641 | -0.101 | -0.621 | -0.766 | -0.408 | -2.140 | -0.795 | ||||||
| P值 | — | >0.05 | >0.05 | >0.05 | >0.05 | >0.05 | <0.05 | >0.05 | ||||||
—:无相关数据. *一对夫妻进行辅助生殖技术治疗可能既有女方因素又有男方因素,遂未进行统计分析. LPPOS:卵泡期高孕激素状态超促排卵;CC:枸橼酸氯米芬;FPPOS:黄体期高孕激素状态超促排卵;BMI:体重指数;AMH:抗米勒管激素;FSH:卵泡刺激素;LH:黄体生成素.
M(Q 1,Q 3)或n(%)
2.2. 两组超促排卵结果及促排过程中实验室相关指标比较
两组各有1例取消周期,因此两组取消周期率分别为0.39%(1/257)和0.44%(1/226),差异无统计学意义(χ 2=0.008,P>0.05)。两组超促排卵结果见表2。LPPOS+CC组Gn使用天数和使用总量较FPPOS+CC组增加(均P<0.01),ICSI 2PN受精率显著低于FPPOS+CC组(P<0.05)。两组间诱发排卵日>14 mm卵泡数、平均获卵数、ICSI MⅡ卵率、IVF 2PN受精率、2PN受精卵裂率、D3优质胚胎率差异均无统计学意义(均P>0.05)。上述结果提示,与LPPOS+CC方案比较,FPPOS+CC方案可能改善患者的卵巢反应性。
表2.
两组超促排卵结果比较
| 组 别 | n | Gn使用天数(d) | Gn使用总量(IU) |
诱发排卵日>14 mm 的卵泡数 |
平均获卵数 | ICSI MⅡ卵率 | |||
|---|---|---|---|---|---|---|---|---|---|
| LPPOS+CC组 | 256 | 11(9,12) | 2213(1650,2700) | 4(3,5) | 4(2,6) | 82.63(352/426) | |||
| FPPOS+CC组 | 225 | 9(8,11) | 2000(1575,2325) | 4(2,5) | 4(3,6) | 82.84(367/443) | |||
| Z/χ 2值 | — | -6.492 | -3.350 | -0.561 | -0.398 | 0.007 | |||
| P值 | — | <0.01 | <0.01 | >0.05 | >0.05 | >0.05 | |||
| 组 别 | n | IVF 2PN受精率 | ICSI 2PN受精率 | 2PN受精卵裂率 | D3优质胚胎率 | ||||
| LPPOS+CC组 | 256 | 71.32(475/666) | 72.16(254/352) | 99.18(723/729) | 53.53(387/723) | ||||
| FPPOS+CC组 | 225 | 73.80(383/519) | 79.56(292/367) | 98.52(665/675) | 53.98(359/665) | ||||
| Z/χ 2值 | — | 0.894 | 5.392 | 1.349 | 0.029 | ||||
| P值 | — | >0.05 | <0.05 | >0.05 | >0.05 | ||||
—:无相关数据. LPPOS:卵泡期高孕激素状态超促排卵;CC:枸橼酸氯米芬;FPPOS:黄体期高孕激素状态超促排卵;Gn:促性腺激素;ICSI:卵胞质内单精子注射;MⅡ:第二次减数分裂中期;IVF:体外受精;PN:原核.
M(Q 1,Q 3)或%(n)
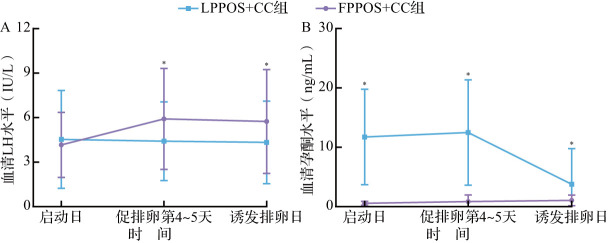
两种PPOS+CC方案诱发排卵日血清FSH和雌二醇水平差异无统计学意义(均P>0.05)。如表3和图1所示,LPPOS+CC组超促排卵第4~5天和诱发排卵日LH水平显著低于FPPOS+CC组(均P<0.01);LPPOS+CC组启动日、超促排卵第4~5天和诱发排卵日孕酮水平显著高于FPPOS+CC组(均P<0.01)。两组深度垂体抑制发生率差异无统计学意义(P>0.05),但LPPOS+CC组早发LH峰发生率显著低于FPPOS+CC组(P<0.01)。对于所有早发LH峰的患者在取卵术前均行阴道超声检查确定优势卵泡回声存在。上述结果提示,与FPPOS+CC组比较,LPPOS+CC组超促排卵期间年轻DOR患者呈持续的高孕激素状态并可以更好地抑制早发LH峰。
表3.
两组促排卵过程中血清内分泌激素水平动态变化情况比较
| 组 别 | n |
诱发排卵日血清 FSH(IU/L) |
诱发排卵日 雌二醇(pg/mL) |
LH(IU/L) | ||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 启动日 |
超促排卵 第4~5天 |
诱发排卵日 | ||||||||
| LPPOS+CC组 | 256 | 19.9(16.3,24.4) | 1569(934,2322) | 3.8(2.5,5.5) | 3.9(2.9,5.3) | 4.0(2.7,5.3) | ||||
| FPPOS+CC组 | 225 | 20.7(16.3,25.3) | 1459(974,2410) | 3.8(2.7,5.2) | 5.3(3.3,7.4) | 5.1(3.2,7.2) | ||||
| Z/χ 2值 | — | -0.403 | -0.003 | -0.005 | -5.567 | -4.806 | ||||
| P值 | — | >0.05 | >0.05 | >0.05 | <0.01 | <0.01 | ||||
| 组 别 | n | 孕酮(ng/mL) |
深度垂体 抑制发生率 |
早发LH峰 发生率 |
||||||
| 启动日 | 超促排卵第4~5天 | 诱发排卵日 | ||||||||
| LPPOS+CC组 | 256 | 10.4(6.0,15.1) | 11.8(5.6,18.1) | 1.3(0.8,2.9) | 2.73(7/256) | 3.13(8/256) | ||||
| FPPOS+CC组 | 225 | 0.5(0.3,0.7) | 0.7(0.5,1.0) | 0.9(0.6,1.2) | 1.78(4/225) | 10.67(24/225) | ||||
| Z/χ 2值 | — | -18.483 | -16.925 | -6.611 | 0.490 | 10.967 | ||||
| P值 | — | <0.01 | <0.01 | <0.01 | >0.05 | <0.01 | ||||
—:无相关数据. FSH:卵泡刺激素;LPPOS:卵泡期高孕激素状态超促排卵;FPPOS:黄体期高孕激素状态超促排卵;CC:枸橼酸氯米芬;LH:黄体生成素.
M(Q 1,Q 3)或%(n)
图1. 两组促排卵过程中血清LH和孕酮水平动态变化情况比较.
A:血清LH水平动态变化;B:血清孕酮水平动态变化. *P<0.01. LPPOS:卵泡期高孕激素状态超促排卵;CC:枸橼酸氯米芬;FPPOS:黄体期高孕激素状态超促排卵;LH:黄体生成素
2.3. 两组胚胎移植、妊娠结局及围产期结局比较
FPPOS+CC组中,2例未获卵,3例无MⅡ卵,12例无2PN受精,35例无D3优质胚胎,15例因内膜菲薄或个人原因未行冻融胚胎移植。LPPOS+CC组中,7例未获卵,3例无MⅡ卵,12例无2PN受精,57例无D3优质胚胎,17例因内膜菲薄或个人原因未行冻融胚胎移植。共有318例DOR患者行至少一个D3优质胚胎或囊胚的冻融胚胎移植治疗,其中LPPOS+CC组17例(10.63%)行囊胚移植,FPPOS+CC组15例(9.49%)行囊胚移植,差异无统计学意义(χ 2=0.112,P>0.05)。LPPOS+CC组的临床妊娠率、着床率显著高于FPPOS+CC组(均P<0.01),但两组持续妊娠率、流产率、异位妊娠率、双胎妊娠率、活产率、早产率、低出生体重率、巨大儿发生率差异均无统计学意义(均P>0.05),见表4。新生儿先天性畸形发生情况分别为LPPOS+CC组新生儿肢体异常1例,FPPOS+CC组新生儿唇腭裂1例。上述结果提示,两组间囊胚移植周期率相似,妊娠结局具有可比性;与FPPOS+CC组比较,LPPOS+CC组优质卵裂期胚胎或囊胚移植后临床妊娠率和着床率更优。
表4.
两组高孕激素状态超促排卵方案胚胎移植、妊娠结局及围产期结局比较
| 组 别 | n |
平均移植 胚胎数(个) |
平均移植日 内膜厚度(mm) |
临床妊娠率 | 着床率 | 早期流产率 | 双胎妊娠率 | 异位妊娠率 | ||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| LPPOS+CC组 | 160 | 2(2,2) | 9.5(8.5,11.0) | 61.88(99/160) | 42.20(119/282) | 18.18(18/99) | 13.13(13/99) | 0.00(0/99) | ||||||
| FPPOS+CC组 | 158 | 2(2,2) | 9.5(8.5,11.0) | 46.84(74/158) | 31.07(87/280) | 13.51(10/74) | 13.51(10/74) | 0.00(0/74) | ||||||
| Z/χ 2值 | — | -0.203 | -0.487 | 7.249 | 7.492 | 0.680 | 0.005 | — | ||||||
| P值 | — | >0.05 | >0.05 | <0.01 | <0.01 | >0.05 | >0.05 | — | ||||||
| 组 别 | n |
持续临床 妊娠率 |
活产率 | 早产率 | 低出生体重率 | 巨大儿发生率 | ||||||||
| 单 胎 | 双 胎 | 单 胎 | 双 胎 | 单 胎 | 双 胎 | |||||||||
| LPPOS+CC组 | 160 |
50.63 (81/160) |
50.00 (80/160) |
5.97 (4/67) |
61.54 (16/26) |
10.45 (7/67) |
73.08 (19/26) |
4.48 (3/67) |
0.00 (0/67) |
|||||
| FPPOS+CC组 | 158 |
40.51 (64/158) |
39.87 (63/158) |
10.91 (6/55) |
37.50 (6/16) |
18.18 (10/55) |
75.00 (12/16) |
3.64 (2/55) |
0.00 (0/16) |
|||||
| Z/χ 2值 | — | 3.281 | 3.294 | 0.979 | 2.295 | 1.507 | 0.019 | 0.054 | — | |||||
| P值 | — | >0.05 | >0.05 | >0.05 | >0.05 | >0.05 | >0.05 | >0.05 | — | |||||
—:无相关数据. LPPOS:卵泡期高孕激素状态超促排卵;FPPOS:黄体期高孕激素状态超促排卵;CC:枸橼酸氯米芬.
M(Q 1,Q 3)或%(n)
2.4. 年轻DOR患者PPOS后临床妊娠的影响因素
二元logistic回归分析结果,仅超促排卵方案与年轻DOR患者PPOS后临床妊娠相关(P<0.05),而年龄、BMI、AMH水平、窦状卵泡数、Gn使用天数、Gn使用总量、获卵数、优质胚胎数、是否发生深度垂体抑制、是否发生早发LH峰、胚胎移植日子宫内膜厚度均与临床妊娠无显著相关性(均P>0.05),见表5。提示患者的基线情况、超促排卵卵巢反应性、胚胎质量和内分泌水平并不影响临床妊娠结局。
表5.
年轻卵巢储备功能减退患者高孕激素状态超促排卵后影响临床妊娠的多因素分析结果
| 影响因素 | OR(95%CI) | P值 |
|---|---|---|
|
超促排卵方案(以FPPOS+CC 方案为参考) |
1.77(1.07~2.95) | <0.05 |
| 年龄 | 1.04(0.95~1.14) | >0.05 |
| BMI | 1.09(1.00~1.18) | >0.05 |
| AMH水平 | 1.46(0.93~2.29) | >0.05 |
| 窦状卵泡数 | 1.00(0.87~1.15) | >0.05 |
| Gn使用天数 | 1.00(0.83~1.19) | >0.05 |
| Gn使用总量 | 1.00(1.00~1.00) | >0.05 |
| 获卵数 | 1.08(0.95~1.22) | >0.05 |
| D3优质胚胎数 | 1.17(0.93~1.47) | >0.05 |
| 发生深度垂体抑制 | 1.50(0.53~4.30) | >0.05 |
| 发生早发LH峰 | 1.92(0.33~11.36) | >0.05 |
| 移植日内膜厚度 | 0.95(0.83~1.08) | >0.05 |
FPPOS:黄体期高孕激素状态超促排卵;CC:枸橼酸氯米芬;BMI:体重指数;AMH:抗米勒管激素;Gn:促性腺激素;LH:黄体生成素.
3. 讨 论
FPPOS+CC方案和LPPOS+CC方案均是在高孕激素状态下进行超促排卵,前者是在卵泡期予以孕酮药物制造的外源性高孕激素状态抑制早发LH峰[8],而后者是在黄体期以内源性高孕激素状态抑制早发LH峰。既往研究发现,35岁及以下DOR患者采用PPOS方案时,添加枸橼酸氯米芬可以有效缓解垂体过度抑制,减少Gn用量[9]。本研究通过回顾性分析483例35岁及以下DOR患者分别采用LPPOS+CC方案和FPPOS+CC方案超促排卵行IVF/ICSI-ET治疗的临床资料,比较两种方案的超促排结果、妊娠结局和围产期结局发现,年轻DOR患者采用LPPOS+CC方案后冻融胚胎移植临床妊娠率和着床率优于FPPOS+CC方案。
近期一项纳入12项研究的meta分析比较了卵泡期和黄体期超促排卵的辅助生殖技术治疗结果,发现虽然卵泡期和黄体期超促排卵后的临床妊娠率和活产率相似,但黄体期超促排卵的Gn使用天数和使用总量均显著增加[13]。最近的一项回顾性研究也报道黄体期超促排卵的Gn使用总量和Gn使用天数较拮抗剂方案增加,差异有统计学意义[14]。本研究结果与之前的这些研究结果基本一致。本研究进一步比较了两种方案超促排卵期间内分泌水平变化,发现LPPOS+CC组在超促排卵4~5 d和诱发排卵日的血清LH水平均显著低于FPPOS+CC组。适宜的LH浓度会刺激卵泡细胞发育和雄激素的释放,从而提高卵泡对卵泡刺激素的反应性[15]。因此,可能由于LPPOS+CC方案中年轻DOR患者血清LH水平低于FPPOS+CC方案,导致其Gn使用天数和使用总量多于FPPOS+CC方案。
本文资料显示,LPPOS+CC方案超促排卵第4~5天和诱发排卵日的血清孕酮水平均显著高于FPPOS+CC组,而LPPOS+CC方案超促排卵第4~5天和诱发排卵日的血清LH水平以及早发LH峰发生率均显著低于FPPOS+CC组。Karsch等[16]证实,高水平的孕激素对LH分泌产生负反馈抑制作用,并且这种抑制作用呈剂量依赖性。因此,LPPOS+CC方案中年轻DOR患者呈持续的高孕激素状态可以更好地抑制早发LH峰。
黄体期超促排的临床妊娠结局是否优于卵泡期超促排卵目前存在争议。有研究者回顾性比较了卵巢低反应者移植纯卵泡期超促排卵获得的胚胎、移植混合卵泡期和黄体期超促排卵获得的胚胎和移植纯黄体期超促排卵获得的胚胎患者的临床妊娠结局,发现移植纯黄体期超促排卵获得胚胎患者的临床妊娠率和着床率最佳[17-18]。但是,一项meta分析结果显示,黄体期超促排卵和卵泡期超促排卵的临床妊娠率和活产率相近[13]。既往大多数研究中,黄体期超促排卵过程会添加Gn释放激素拮抗剂来抑制早发LH[19-23]。Wang等[24]比较了黄体期促排卵方案与微刺激和短方案的临床结局。目前比较通过高孕激素水平抑制早发LH峰的黄体期与卵泡期超促排卵的妊娠结局的研究还不多。本文资料显示,LPPOS+CC方案促排后冻融胚胎移植周期的临床妊娠率和着床率优于FPPOS+CC方案,但优质胚胎率、持续妊娠率和活产率没有显著差异。此外,本研究通过二元logistic回归分析发现,年龄、深度垂体抑制和早发LH峰是否发生与临床妊娠率无关。既往研究显示,卵泡期和黄体期双重促排周期中卵泡期促排获得的胚胎与黄体期促排获得的胚胎的整倍体率相似[25-27]。研究显示,卵泡期和黄体期促排获得的颗粒细胞中性激素合成相关酶以及Gn受体的表达亦相似[28]。因此推测LPPOS+CC方案虽然对内源性早发LH峰抑制较好,但是两种方案对胚胎发育潜能的影响差异不大,这可能是LPPOS+CC方案高孕激素状态持续时间更长且孕激素水平更高,对后续冻融胚胎移植周期子宫内膜容受性产生有利影响,提高了临床妊娠率和着床率,但其机制还需进一步研究。
综上所述,相比FPPOS+CC方案,年轻DOR患者采用LPPOS+CC方案超促排卵获得的胚胎及其移植后临床妊娠率和着床率更佳。该结果为DOR患者的个体化治疗及临床结果的改善提供了新的依据。但是,本研究采用回顾性、单中心设计,存在一些固有的选择局限性和混杂偏倚。此外,本研究对象仅为35岁及以下的DOR患者,其他人群中两种PPOS+CC方案的临床应用效果尚需进一步研究验证。
Acknowledgments
研究得到温州市科技项目(Y2020078)、温州医科大学第一附属医院科研孵化项目(FHY2019043)和温州市生殖遗传重点实验室(2022HZSY0051)支持
Acknowledgments
This work was supported by the Science and Technology Project of Wenzhou City (Y2020078), Research Incubation Project of the First Affiliated Hospital of the Wenzhou Medical University (FHY2019043) and Key Laboratory of Reproduction and Genetics of Wenzhou City (2022HZSY0051)
[缩略语]
卵巢储备功能减退(diminished ovarian reserve,DOR);抗米勒管激素(anti-Müllerian hormone,AMH);卵泡刺激素(follicle-stimulating hormone,FSH);高孕激素状态超促排卵(progestin primed ovarian stimulation,PPOS);促性腺激素(gonadotropin,Gn);体外受精(in vitro fertilization,IVF);卵胞质内单精子注射(intracytoplasmic sperm injection,ICSI);IVF/ICSI-胚胎移植(IVF/ICSI-embryo transfer,IVF/ICSI-ET);黄体生成素(luteinizing hormone,LH);体重指数(body mass index,BMI);人绒毛膜促性腺激素(human chorionic-gonadotropin hormone,hCG);第二次减数分裂中期(metaphase of second meiosis,MⅡ);原核(pronucleus,PN);比值比(odd ratio,OR);置信区间(confidence interval,CI)
利益冲突声明
所有作者均声明不存在利益冲突
Conflict of Interests
The authors declare that there is no conflict of interests
参考文献(References)
- 1.PASTORE L M, CHRISTIANSON M S, STELLING J, et al. Reproductive ovarian testing and the alphabet soup of diagnoses: DOR, POI, POF, POR, and FOR[J]. J Assist Reprod Genet, 2018, 35(1): 17-23. 10.1007/s10815-017-1058-4 [DOI] [PMC free article] [PubMed] [Google Scholar]
- 2.Practice Committee of the American Society for Repro-ductive Medicine . Testing and interpreting measures of ovarian reserve: a committee opinion[J/OL]. Fertil Steril, 2015, 103(3): e9-e17. 10.1016/j.fertnstert.2014.12.093 [DOI] [PubMed] [Google Scholar]
- 3.JIAO Z, BUKULMEZ O. Potential roles of experimental reproductive technologies in infertile women with diminished ovarian reserve[J]. J Assist Reprod Genet, 2021, 38(10): 2507-2517. 10.1007/s10815-021-02246-6 [DOI] [PMC free article] [PubMed] [Google Scholar]
- 4.REED B G, BABAYEV S N, BUKULMEZ O. Shifting paradigms in diminished ovarian reserve and advanced reproductive age in assisted reproduction: customization instead of conformity[J]. Semin Reprod Med, 2015, 33(3): 169-178. 10.1055/s-0035-1552585 [DOI] [PubMed] [Google Scholar]
- 5.SUNKARA S K, RITTENBERG V, RAINE-FENNING N, et al. Association between the number of eggs and live birth in IVF treatment: an analysis of 400 135 treatment cycles[J]. Hum Reprod, 2011, 26(7): 1768-1774. 10.1093/humrep/der106 [DOI] [PubMed] [Google Scholar]
- 6.GUAN S, FENG Y, HUANG Y, et al. Progestin-primed ovarian stimulation protocol for patients in assisted reproductive technology: a meta-analysis of randomized controlled trials[J]. Front Endocrinol (Lausanne), 2021, 12: 702558. 10.3389/fendo.2021.702558 [DOI] [PMC free article] [PubMed] [Google Scholar]
- 7.TU X, YOU B, JING M, et al. Progestin-primed ovarian stimulation versus mild stimulation protocol in advanced age women with diminished ovarian reserve undergoing their first in vitro fertilization cycle: a retrospective cohort study[J]. Front Endocrinol (Lausanne), 2021, 12: 801026. 10.3389/fendo.2021.801026 [DOI] [PMC free article] [PubMed] [Google Scholar]
- 8.KUANG Y, CHEN Q, FU Y, et al. Medroxypro-gesterone acetate is an effective oral alternative for preventing premature luteinizing hormone surges in women undergoing controlled ovarian hyperstimulation for in vitro fertilization[J]. Fertil Steril, 2015, 104(1): 62-70.e3. 10.1016/j.fertnstert.2015.03.022 [DOI] [PubMed] [Google Scholar]
- 9.LIN Y, CHEN Q, ZHU J, et al. Progestin-primed ovarian stimulation with clomiphene citrate supple-mentation may be more feasible for young women with diminished ovarian reserve compared with standard progestin-primed ovarian stimulation: a retrospective study[J]. Drug Des Devel Ther, 2021, 15: 5087-5097. 10.2147/dddt.s338748 [DOI] [PMC free article] [PubMed] [Google Scholar]
- 10.DE LOS SANTOS M J, ARROYO G, BUSQUET A, et al. A multicenter prospective study to assess the effect of early cleavage on embryo quality, implantation, and live-birth rate[J]. Fertil Steril, 2014, 101(4): 981-987. 10.1016/j.fertnstert.2013.12.043 [DOI] [PubMed] [Google Scholar]
- 11.DONG J, WANG Y, CHAI W R, et al. The pregnancy outcome of progestin-primed ovarian stimulation using 4 versus 10 mg of medroxyprogesterone acetate per day in infertile women undergoing in vitro fertilisation: a randomised controlled trial[J]. BJOG, 2017, 124(7): 1048-1055. 10.1111/1471-0528.14622 [DOI] [PubMed] [Google Scholar]
- 12.ENGEL J B, LUDWIG M, FELBERBAUM R, et al. Use of cetrorelix in combination with clomiphene citrate and gonadotrophins: a suitable approach to ‘friendly IVF’?[J]. Hum Reprod, 2002, 17(8): 2022-2026. 10.1093/humrep/17.8.2022 [DOI] [PubMed] [Google Scholar]
- 13.LU B J, LIN CJ, LIN B Z, et al. ART outcomes following ovarian stimulation in the luteal phase: a systematic review and meta-analysis[J]. J Assist Reprod Genet, 2021, 38(8): 1927-1938. 10.1007/s10815-021-02237-7 [DOI] [PMC free article] [PubMed] [Google Scholar]
- 14.ZHAO W, SUN P, LI T, et al. Outcomes and cost-effectiveness comparisons of progestin-primed ovarian stimulation, GnRH antagonist protocol, and luteal phase stimulation for fertility preservation[J]. Int J Gynaecol Obstet, 2023, 163(2): 645-650. 10.1002/ijgo.14903 [DOI] [PubMed] [Google Scholar]
- 15.KUMAR P, SAIT S F. Luteinizing hormone and its dilemma in ovulation induction[J]. J Hum Reprod Sci, 2011, 4(1): 2-7. 10.4103/0974-1208.82351 [DOI] [PMC free article] [PubMed] [Google Scholar]
- 16.KARSCH F J. Central actions of ovarian steroids in the feedback regulation of pulsatile secretion of luteinizing hormone[J]. Annu Rev Physiol, 1987, 49: 365-382. 10.1146/annurev.ph.49.030187.002053 [DOI] [PubMed] [Google Scholar]
- 17.ZHANG Q, GUO X M, LI Y. Implantation rates subsequent to the transfer of embryos produced at different phases during double stimulation of poor ovarian responders[J]. Reprod Fertil Dev, 2017, 29(6): 1178-1183. 10.1071/rd16020 [DOI] [PubMed] [Google Scholar]
- 18.ALSBJERG B, HAAHR T, ELBAEK H O, et al. Dual stimulation using corifollitropin alfa in 54 Bologna criteria poor ovarian responders—a case series[J]. Reprod Biomed Online, 2019, 38(5): 677-682. 10.1016/j.rbmo.2019.01.007 [DOI] [PubMed] [Google Scholar]
- 19.BUENDGEN N K, SCHULTZE-MOSGAU A, CORDES T, et al. Initiation of ovarian stimulation independent of the menstrual cycle: a case-control study[J]. Arch Gynecol Obstet, 2013, 288(4): 901-904. 10.1007/s00404-013-2794-z [DOI] [PubMed] [Google Scholar]
- 20.KUANG Y, HONG Q, CHEN Q, et al. Luteal-phase ovarian stimulation is feasible for producing competent oocytes in women undergoing in vitro fertilization/intracytoplasmic sperm injection treatment, with optimal pregnancy outcomes in frozen-thawed embryo transfer cycles[J]. Fertil Steril, 2014, 101(1): 105-111. 10.1016/j.fertnstert.2013.09.007 [DOI] [PubMed] [Google Scholar]
- 21.MARTÍNEZ F, CLUA E, DEVESA M, et al. Comparison of starting ovarian stimulation on day 2 versus day 15 of the menstrual cycle in the same oocyte donor and pregnancy rates among the corresponding recipients of vitrified oocytes[J]. Fertil Steril, 2014, 102(5): 1307-1311. 10.1016/j.fertnstert.2014.07.741 [DOI] [PubMed] [Google Scholar]
- 22.PEREIRA N, VOSKUILEN-GONZALEZ A, HANCOCK K, et al. Random-start ovarian stimulation in women desiring elective cryopreservation of oocytes[J]. Reprod Biomed Online, 2017, 35(4): 400-406. 10.1016/j.rbmo.2017.06.002 [DOI] [PubMed] [Google Scholar]
- 23.LLÁCER J, MOLINER B, LUQUE L, et al. Luteal phase stimulation versus follicular phase stimulation in poor ovarian responders: results of a randomized controlled trial[J]. Reprod Biol Endocrinol, 2020, 18(1): 9. 10.1186/s12958-020-00570-7 [DOI] [PMC free article] [PubMed] [Google Scholar]
- 24.WANG N, WANG Y, CHEN Q, et al. Luteal-phase ovarian stimulation vs conventional ovarian stimulation in patients with normal ovarian reserve treated for IVF: a large retrospective cohort study[J]. Clin Endocrinol (Oxf), 2016, 84(5): 720-728. 10.1111/cen.12983 [DOI] [PubMed] [Google Scholar]
- 25.CIMADOMO D, VAIARELLI A, COLAMARIA S, et al. Luteal phase anovulatory follicles result in the production of competent oocytes: intra-patient paired case-control study comparing follicular versus luteal phase stimulations in the same ovarian cycle[J]. Hum Reprod, 2018, 33(8): 1442-1448. 10.1093/humrep/dey217 [DOI] [PMC free article] [PubMed] [Google Scholar]
- 26.UBALDI F M, CAPALBO A, VAIARELLI A, et al. Follicular versus luteal phase ovarian stimulation during the same menstrual cycle (DuoStim) in a reduced ovarian reserve population results in a similar euploid blastocyst formation rate: new insight in ovarian reserve exploitation[J]. Fertil Steril, 2016, 105(6): 1488-1495.e1. 10.1016/j.fertnstert.2016.03.002 [DOI] [PubMed] [Google Scholar]
- 27.VAIARELLI A, CIMADOMO D, TRABUCCO E, et al. Double stimulation in the same ovarian cycle (DuoStim) to maximize the number of oocytes retrieved from poor prognosis patients: a multicenter experience and SWOT analysis[J]. Front Endocrinol (Lausanne), 2018, 9: 317. 10.3389/fendo.2018.00317 [DOI] [PMC free article] [PubMed] [Google Scholar]
- 28.ESMAEILIAN Y, HELA F, BILDIK G, et al. IVF characteristics and the molecular luteal features of random start IVF cycles are not different from conven-tional cycles in cancer patients[J]. Hum Reprod, 2023, 38(1): 113-124. 10.1093/humrep/deac242 [DOI] [PubMed] [Google Scholar]