Abstract
目的
本研究旨在通过对鼻咽癌放疗后的放射性颅底坏死病例的回顾性分析,探讨建立一种用于指导临床治疗和预后风险评估的分型分期系统。
方法
总结广西壮族自治区人民医院耳鼻咽喉头颈外科2019年1月—2022年12月共计86例放射性颅底坏死患者的临床资料,其中17例放弃治疗,69例进行治疗。通过分析69例患者的电子鼻咽喉镜检查结合MRI、CT等影像学检查,提出放射性颅底坏死分型分期系统,进一步分析分型分期系统与患者的手术情况、手术效果和预后的关系。
结果
根据放射性颅底坏死对软组织、骨质、重要血管神经的破坏程度及范围,将其分为闭合型(5例)和开放型(64例),其中开放型又分5型:Ⅰ型(4例),Ⅱ型(6例),Ⅲ型(39例,其中Ⅲa型21例,Ⅲb型18例),Ⅳ型(12例),Ⅴ型(8例)。根据鼻内镜检查联合MRI或CT等影像学检查,结合是否二程放疗、感染累及的部位、骨质破坏范围、颈内动脉累犯程度、脑组织坏死程度进行计分和统计,按不同分数级别将病变分为4期:Ⅰ期4例(1~2分),Ⅱ期11例(3~4分),Ⅲ期24例(5~6分),Ⅳ期30例(≥7分)。69例患者中,22例选择保守治疗:Ⅰ期2例,Ⅱ期3例,Ⅲ期7例,Ⅳ期10例;47例选择鼻内镜手术治疗:Ⅰ期2例、Ⅱ期8例、Ⅲ期17例、Ⅳ期20例,其中16例行游离黏膜瓣和(或)带蒂鼻中隔黏膜瓣鼻咽颅底修复。按分期划分,Ⅰ、Ⅱ、Ⅲ期患者手术治疗后均获得较好效果,分期越高的患者预后越差,且围手术期并发症发生率越高。术后并发症有手术部位感染无法愈合、脑脊液鼻漏、进展性骨坏死、鼻咽部大出血及死亡等。
结论
放射性颅底坏死的分型分期系统可在定期随访中早期发现病变,在发现病变后能更好地应用于临床治疗指导和风险预后评估。
Keywords: 鼻咽肿瘤, 鼻咽坏死, 鼻内镜手术
Abstract
Objective
To establish a staging system for guiding clinical treatment and prognostic risk assessment by retrospectively analyzing the cases with radionecrosis of the nasopharynx and skull base (RNSB) after radiotherapy for nasopharyngeal carcinoma.
Methods
A total of 86 cases of RNSB from January 2019 to December 2022 visited Department of Otorhinolaryngology Head and Neck, the People's Hospital of Guangxi Zhuang Autonomous Region. Seventeen patients gave up the treatment, and 69 patients who underwent treatment were included for analysis. By analyzing the results of electronic nasopharyngolaryngoscopy combined with magnetic resonance (MR), CT, and other imaging examinations, a staging system for RNSB was proposed. The relationship between the staging system and the surgical effectiveness and clinical prognosis was further analyzed.
Results
According to the severity and extent of destruction of soft tissue, bone, and the adjacent neurovascular structures, the RNSB was categorized into closed type (n=5) and open type (n=64), of which the open type was subdivided into five types: type Ⅰ(n=4), type Ⅱ(n=6), type Ⅲ(n=39, of which 21 cases were type Ⅲa and 18 cases were type Ⅲb), type Ⅳ(n=12), and type Ⅴ(n=8). The clinical stage of RNSB were classified based on nasopharyngolaryngoscopy and imaging examinations, receiving the second course of radiotherapy or not, the involvement of the infection site, the extent of bone destruction, the degree of internal carotid artery involvement, and the degree of brain tissue necrosis: stageⅠ(1-2 scores), 11 cases at stageⅡ(3-4 scores), 24 cases at stage Ⅲ(5-6 scores), and 30 cases at stage Ⅳ(≥ 7 scores or more). Twenty-two patients chose conservative treatment (2 patients at stage Ⅰ, 3 patients at stage Ⅱ, 7 patients at stage Ⅲ, and 10 patients at stage Ⅳ). Forty-seven patients chose nasal endoscopic surgical treatment (2 patients at stage Ⅰ, 8 patients at stage Ⅱ, 17 patients at stage Ⅲ, and 20 patients at stage Ⅳ), of which 16 cases had received free mucosal flap and/or stented septum mucosal flap repair. Patients at stages Ⅰ, Ⅱ, and Ⅲ achieved satisfactory efficacy after surgical treatment. In addition, higher clinical stage was found to correlate with the worse prognosis and higher incidence of perioperative complications, which included failure of healing because of surgical site infection, cerebrospinal fluid nasal leakage, progressive osteonecrosis, nasopharyngeal hemorrhage, and death.
Conclusion
The staging system proposed in our study can be used for early detection of RNSB during regular follow-up, and is also valuable for clinical treatment guidance and prognosis assessment.
Keywords: nasopharyngeal carcinoma, radionecrosis of the nasopharynx and skull base, endoscopy
初治鼻咽癌主要以放疗为主。适形调强放疗已明显提高患者生存率,但仍不得不面对因放疗损伤导致的并发症,包括放射性咽炎、鼻窦炎、中耳炎、放射性脑病、放射性骨坏死等。放射性骨坏死可发生在任何骨骼中,但血供差的骨骼更易受累。鼻咽癌放射性颅底坏死常常在放疗后3~15年[1]出现,多表现为鼻内异味、恶臭,头痛,有时表现为爆炸性头痛,止痛治疗效果极差,以及反复出现的间歇性或持续性鼻出血,甚至鼻咽部大出血,给患者及其家庭造成严重伤害,是鼻咽癌放疗后严重并发症之一。近20年来,国内外众多学者开始关注鼻咽癌放疗后放射性颅底坏死,也做了大量的研究工作,提出了不同的(致病)假说,鼻内镜手术成为主要的治疗方式。但手术方案的选择,预后的评估等,都需要制定合理的分型分期用以评估病情,并指导临床治疗。有学者提出了相应的S-B分期[2]、依据CT的分级方式[3]等,但目前仍然没有统一的定量分析的分型分期应用于临床治疗指导。本研究结合86例患者的临床资料,根据放射性颅底坏死对软组织、骨质、重要血管神经的破坏情况,将其分为5型并进行分期,以便更好地指导临床治疗和预后风险评估。
1. 资料与方法
1.1. 临床资料
2019年1月-2022年12月在我院耳鼻咽喉头颈外科住院治疗的患者共86例,放弃治疗17例,进行治疗69例。治疗的患者中男49例,女20例。患者均有完整的临床资料,年龄33~75岁,平均54.6岁,中位年龄53岁。纳入标准:有明确的鼻咽癌放疗史,影像学有明显软组织坏死,和(或)不规则骨质破坏。排除标准:有手术禁忌证或严重基础疾病。
收集患者的一般资料:性别、年龄、入院日期、症状、基础疾病史、原发肿瘤资料等;临床检查:电子鼻咽喉镜检查及影像学检查(CT或MRI),了解软组织破坏程度、骨组织破坏程度、重要血管(颈内动脉)受累程度;手术治疗资料:手术部位以及具体手术方式;术后随访资料:手术效果评估及术后并发症记录。手术效果分为治愈(无明显主观症状,电子鼻咽喉镜及影像学检查坏死区域修复良好)、稳定(症状无改善,电子鼻咽喉镜及影像学检查软组织坏死及骨破坏无明显进展)、进展(症状加重,电子鼻咽喉镜及影像学检查软组织坏死及骨破坏区扩大)。
1.2. 放射性颅底坏死分型分期方法
结合所有患者的临床表现、电子鼻咽喉镜、CT和(或)MRI的检查结果进行评估,尝试建立一种基于放射性颅底坏死对软组织、骨质、重要血管神经破坏情况的分型分期方法,通过电子鼻咽喉镜检查结果,了解鼻腔及鼻咽部是否可见软组织坏死溃疡,将放射性颅底坏死分成闭合型坏死和开放型坏死,而开放型坏死再结合MRI及CT结果,将其分为两种情况:①坏死腔小于坏死开口;②坏死腔大于坏死开口。
根据MRI、CT等影像学检查结果显示的颅底坏死范围以及对软组织、骨质、重要血管神经的破坏情况,将开放型坏死分为5型:Ⅰ型为单纯软组织坏死,Ⅱ型为单纯骨质坏死,Ⅲ型为软组织+骨质坏死,Ⅳ型为合并脑组织坏死,Ⅴ型为合并肿瘤复发坏死,其中Ⅲ型根据是否累犯重要血管神经分为累及重要血管神经的坏死和未累及重要血管神经的坏死两个亚型(Ⅲa型和Ⅲb型)。
根据电子鼻咽喉检查联合MRI、CT等影像学检查,结合是否进行二程放疗、感染累及部位(鼻咽部黏膜、头长肌、咽旁间隙、咽鼓管区、翼腭窝、颞下窝、颈静脉孔区)、骨质破坏范围(枕骨斜坡、蝶骨、岩骨、筛骨、上颌骨、颈椎骨质)、颈内动脉累犯程度(紧贴颈内动脉,病变累及颈内动脉范围<1/2,累及颈内动脉范围>1/2,病变全包绕颈内动脉)、脑组织坏死程度(硬脑膜、脑组织)进行计分和统计,按不同分数级别将病变分为Ⅰ期(1~2分)、Ⅱ期(3~4分)、Ⅲ期(5~6分)、Ⅳ期(≥7分)。详细分数统计方案见表 1。
表 1.
放射性鼻咽颅底骨坏死分期分数计分方案
| 累犯病变范围 | 计分项目 | 分数 |
| 二程放疗(R) | 否 | 0 |
| 是 | 1 | |
| 感染累及部位(I) | 无感染症状和体征 | 0 |
| 鼻咽腔软组织、头长肌 | 1 | |
| 咽旁间隙、咽鼓管区、翼腭窝 | 2 | |
| 颞下窝、颈静脉孔区、椎旁软组织 | 3 | |
| 骨质破坏范围(E) | 无骨质破坏 | 0 |
| 上颌骨、筛骨骨质破坏 | 1 | |
| 枕骨斜坡、蝶窦骨质破坏 | 2 | |
| 岩骨、颈椎骨质破坏 | 3 | |
| 颈内动脉累犯程度(V) | 与颈内动脉内侧缘距离>5 mm | 0 |
| 与颈内动脉内侧缘距离<5 mm,或紧贴颈内动脉内侧缘 | 1 | |
| 病变累及颈内动脉,颈内动脉壁包绕范围<1/2 | 2 | |
| 病变累及颈内动脉,颈内动脉壁包绕范围>1/2,或将颈内动脉全包绕 | 3 | |
| 脑组织坏死情况(N) | 无硬脑膜及脑组织坏死 | 0 |
| 累及局部硬脑膜坏死 | 1 | |
| 合并脑组织坏死 | 2 | |
| 脑干受压变形 | 3 |
1.3. 随访与观察指标
1.3.1. 随访方法
随访开始时间定为患者确诊发病日期,结束时间为2023年8月,以死亡为终止事件。采用电话、信件、门诊、住院等方式进行随访。随访过程中记录患者的死亡时间及具体原因。
1.3.2. 观察内容
通过分型分期方法对患者进行相应的分型分期,同时每3个月复查电子鼻咽喉镜和鼻咽颅底MRI或CT等评估疗效;电子鼻咽喉镜观察术腔愈合情况;观察手术及非手术患者的治疗疗效,计算总的生存率并进行生存分析。
1.4. 统计学处理
采用R3.6.1统计学软件进行分析。计数资料用%表示,比较采用χ2检验。生存曲线采用Kaplan-Meier法进行单因素生存分析,log-rank检验进行分析。采用Cox比例风险模型进行多变量分析。P<0.05为差异有统计学意义。
2. 结果
2.1. 鼻咽癌放疗后放射性颅底坏死分型
根据放射性颅底坏死对软组织、骨质、重要血管神经的破坏情况,将其分为闭合型颅底坏死(5例)和开放型颅底坏死(64例)。
2.1.1. 闭合型颅底坏死
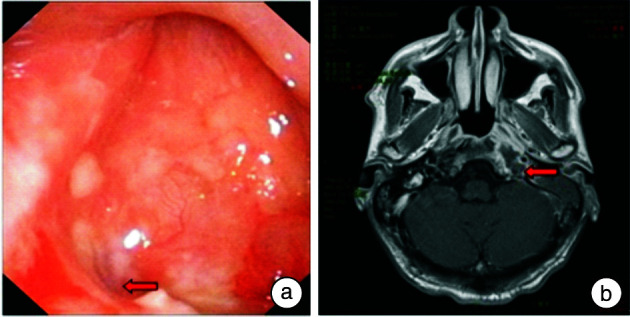
电子鼻咽喉镜检查见鼻咽部黏膜表面光滑,未见坏死组织(图 1a);但患者头痛明显,尤其是渐进性头痛,MRI示坏死腔(图 1b)。
图 1.
闭合型颅底坏死患者的临床资料
a:电子鼻咽喉镜检查见鼻咽部黏膜光滑,左侧咽隐窝结构清晰,未见新生物及坏死组织(红色箭头示左侧咽隐窝;b:MRI水平位示鼻咽部左侧咽旁间隙坏死腔,与鼻咽腔不相通(红色箭头示坏死腔)。
2.1.2. 开放型颅底坏死
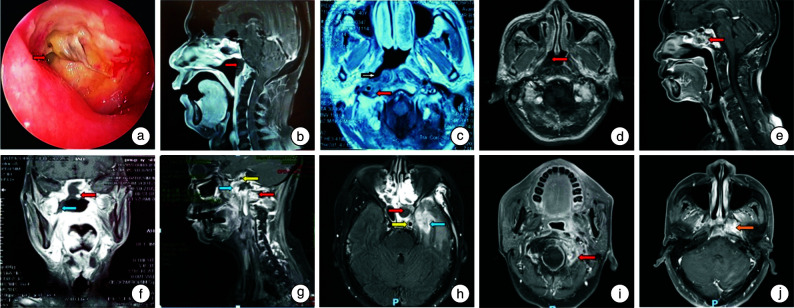
坏死腔与鼻咽腔相通,电子鼻咽喉镜检查见鼻咽部灰白色絮状坏死物(图 2a);MRI见开放性坏死腔:一种是坏死腔小于坏死开口(图 2b);另一种坏死腔大于开口,此种引流不佳(图 2c),临床表现以异味、臭味和头痛明显为主。开放型颅底坏死根据MRI和(或)CT显示颅底坏死范围以及对骨质的破坏情况再分为五型,Ⅰ型:单纯软组织坏死4例(图 2d);Ⅱ型:单纯骨组织坏死6例(图 2e);Ⅲ型:软组织合并骨组织坏死39例,其中Ⅲa型:软组织合并骨组织坏死,未累犯重要血管神经21例(图 2f),Ⅲb型:软组织合并骨组织坏死,累犯重要血管神经18例(图 2g);Ⅳ型:合并脑组织的坏死12例(图 2h);Ⅴ型:合并恶性肿瘤的坏死(非肿瘤区域坏死)8例,见图 2i、2j。
图 2.
开放型颅底坏死患者的临床资料
a:电子鼻咽喉镜检查见鼻咽部顶后壁坏死溃疡,其内可见大量灰白色絮状坏死物(红色箭头示坏死开口);b:MRI矢状位示鼻咽部顶后壁枕骨斜坡坏死,坏死腔小于坏死开口(红色箭头示坏死腔);c:MRI水平位示鼻咽部右侧咽旁间隙坏死,坏死腔大于坏死开口(白色箭头示坏死开口;红色箭头示坏死腔);d:MRI水平位示鼻咽部右侧咽隐窝软组织坏死(红色箭头示软组织坏死);e:MRI矢状位示蝶骨坏死,蝶窦区域结构紊乱(红色箭头示蝶骨);f:MRI冠状位示右侧壁软组织及蝶骨坏死(红色箭头示蝶窦底壁骨质坏死,蓝色箭头示鼻咽右侧壁软组织坏死);g:MRI矢状位示颅底坏死组织累及蝶骨、枕骨斜坡、颈内动脉,颈内动脉管径变形,动脉壁局部增厚(蓝色箭头示软组织坏死,红色箭头示骨质坏死,黄色箭头示颈内动脉);h:MRI水平位示蝶窦区坏死,且合并脑组织坏死(红色箭头示蝶窦区坏死,蓝色箭头示脑组织坏死,黄色箭头示颈内动脉);i:MRI水平位示左侧颈椎旁坏死腔,术后病理结果证实黏膜慢性炎(红色箭头示左侧颈椎旁坏死腔);j:MRI水平位示鼻咽部左侧咽旁间隙鼻咽癌肿瘤复发,术后病理证实为鼻咽部未分化非角化性癌(橙色箭头示肿瘤复发)。
2.2. 放射性颅底坏死各分期的治疗结果
根据电子鼻咽喉镜检查联合MRI、CT等影像学检查,结合是否二程放疗、感染累及部位、骨质破坏范围、颈内动脉累犯程度、脑组织坏死程度进行计分和统计,按不同分数级别将病变分为4期:Ⅰ期4例(1~2分),Ⅱ期13例(3~4分),Ⅲ期29例(5~6分),Ⅳ期23例(≥7分)。69例患者中,22例采取非手术治疗方式,包括抗生素治疗、鼻腔鼻咽部浸泡冲洗及鼻内镜下清理换药,从结果可看出早期患者治疗效果较好。47例患者选择了全身麻醉下鼻内镜手术治疗,其中16例同期行游离黏膜瓣修复和(或)鼻中隔带血管蒂黏膜组织瓣修复,从结果可见早期患者手术治疗效果也非常好,其中Ⅲ期患者的手术效果也非常显著,达到82.35%。
2.3. 随访与生存分析
截止到2023年8月,69例患者均住院复查获得信息资料。手术组和非手术组间的性别、年龄等基线治疗比较差异均无统计学意义(P>0.05),见表 4。将患者手术与否、新的分型、新的分期等情况进行生存分析。结果提示:69例患者的总生存率为66.67%。按新分型分期划分,不论选择手术还是非手术治疗,2组患者总生存期差异无统计学意义(P=0.86);不同分型的患者总生存率差异无统计学意义(P=0.42);不同分期的患者,分期越高预后越差,差异有统计学意义(P=0.000 37)。
表 4.
69例患者基线资料比较 例(%),X±S
| 因素 | 非手术组(n=22) | 手术组(n=47) | P |
| 年龄/岁 | 53.5±10.0 | 53.4±9.10 | 0.977 |
| 性别 | 0.101 | ||
| 男 | 19(86.4) | 30(63.8) | |
| 女 | 3(13.6) | 17(36.2) | |
| 二程放疗 | 16(72.7) | 39(83.0) | 0.349 |
表 2.
非手术治疗患者的临床疗效观察 例
| 分期 | 治愈 | 稳定 | 进展 | 死亡 | P |
| *代表非手术治疗的Ⅲ期死亡患者中有1例死于远处转移。 | |||||
| Ⅰ期 | 2 | 0 | 0 | 0 | 0.0142 |
| Ⅱ期 | 2 | 1 | 0 | 0 | |
| Ⅲ期 | 0 | 4 | 1 | 2* | |
| Ⅳ期 | 0 | 4 | 2 | 4 | |
表 3.
鼻内镜手术治疗患者的临床疗效观察 例
| 分期 | 治愈 | 稳定 | 进展 | 死亡 | P |
| *代表手术治疗的Ⅳ期死亡患者中有5例分别死于远处转移及新冠肺炎。 | |||||
| Ⅰ期 | 2 | 0 | 0 | 0 | <0.012 |
| Ⅱ期 | 7 | 1 | 0 | 0 | |
| Ⅲ期 | 9 | 5 | 1 | 2 | |
| Ⅳ期 | 0 | 5 | 1 | 14* | |
2.4. 围手术期并发症
47例手术患者中,术后并发症的总发生率为38.30%。最常见的术后并发症为手术部位无法上皮化19例(40.43%),脑脊液鼻漏7例(14.89%),进展性骨坏死9例(19.15%),鼻咽部大出血8例(17.02%);死亡16例(34.04%),其中5例分别死于肿瘤的远处转移及新冠肺炎。按分期划分,并发症发生率分布为:Ⅰ期无并发症发生,Ⅱ期12.50%,Ⅲ期47.05%,Ⅳ期100.00%。分期越高的患者围手术期并发症发生率越高(P<0.01)。
3. 讨论
放射性颅底坏死是鼻咽癌放疗后严重并发症之一,影响患者的生活质量[4-5]。由于颅底骨坏死的表现各异,因此目前放射性颅底坏死尚缺乏规范的临床分型分期。
关于放射性颅底骨坏死的分型分期的研究仍甚少,邱前辉等[3]曾根据鼻咽癌放疗后颅底组织坏死的CT影像进行分级,帮助评估预后风险及指导手术治疗。与之前的分级不同的是,本研究根据高清电子鼻咽喉检查结合MRI、CT等影像学检查,首次提出了一种新的放射性颅底坏死临床分型分期的方法。首先,根据鼻腔及鼻咽部是否可见坏死溃疡,将放射性颅底坏死分两型,即闭合型(图 1a)和开放型(图 2c)。由于坏死的分泌物引流不畅会导致坏死的恶性循环,这一分型将有助于评估坏死的引流情况。临床上发现,即便同样是开放型的鼻咽颅底坏死,其临床表现和预后仍有很大差别。
然而仅评估坏死的引流情况还远远不够,因为涉及到治疗决策,尤其是决定手术的范围以及是否需要术前行介入干预等手段时,往往缺乏统一的标准,因此需要更为细致的分型。根据MRI、CT等影像学检查显示鼻咽颅底坏死范围以及对骨质的破坏情况再进行分型,共分为Ⅰ型(单纯软组织坏死)、Ⅱ型(单纯骨组织坏死)、Ⅲ型(Ⅲa型:软组织合并骨组织坏死,未累犯重要血管神经;Ⅲb型:软组织合并骨组织坏死,累犯重要血管神经)、Ⅳ型(合并脑组织的坏死)、Ⅴ型(合并肿瘤复发坏死)。对于Ⅰ型患者,保守治疗可以取得不错的疗效,而Ⅱ型以上往往需要采取手术治疗。Ⅲb型以上的患者较Ⅱ~Ⅲa型的患者手术风险要高,考虑需要协同介入科、神经外科等科室合作,以尽量降低术中损伤颈内动脉出现大出血的风险。
鼻内镜下颅底坏死组织切除及修复创面是目前主要治疗放射性鼻咽颅底坏死的手段。但不同的病灶范围及严重程度手术的难度大小不一。因此我们按不同分数级别将病变分为4期,用以评估手术的难度及治疗效果。本课题组前期研究结合多年的临床经验总结[6],在分期系统中,不论是手术还是非手术治疗早期局限性病变(Ⅰ期和Ⅱ期)的治疗效果都非常好。但是对于广泛性的放射性颅底坏死来说,因为正常颅底解剖结构已经遭到破坏,鼻内镜手术难度明显增大,而且有时候无法彻底清除坏死软组织及骨组织。因此,对广泛性病变的患者来说,应先控制感染,再进行鼻内镜手术治疗,术中彻底清理坏死病变,包括坏死骨质,术腔引流通畅,有利于术后的上皮化,从而提高预后。本研究也显示Ⅲ期患者手术效果要好于非手术效果。而Ⅳ期患者也同样是我们的难题,坏死范围太大,预后很差,如何处理颈内动脉,是否能彻底切除坏死组织并进行有效的修复可能还是解决问题的关键所在。
鼻内镜颅底手术切除坏死病变,最关键是颈内动脉的定位和保护,防止由于颈内动脉破裂引起的致死性大出血。术中找到咽鼓管[7]、蝶翼突裂[8]、下颌神经、腭帆提肌、翼管神经等解剖标志,都可以比较准确定位颈内动脉。而介入治疗的参与,在术前可以对颈内动脉进行充分的评估和处理,在术中术后可以解决的颈内动脉出血的问题,包括颈内动脉栓塞、覆膜支架植入等技术,大大降低了手术的风险。当然随着鼻内镜手术技术的发展,越来越多的学者开始关注鼻咽癌放疗后鼻咽颅底坏死并发症,诊断广泛性的颅底骨坏死,鼻内镜手术也获得了很好的疗效,可应用鼻黏膜瓣[9]及带蒂筋膜组织瓣修复鼻咽颅底缺损[10-11]。对于病灶清除后裸露的颈内动脉或范围较大的颅底缺损,可采用带蒂组织瓣进行覆盖,常用的鼻腔带蒂组织瓣有鼻中隔瓣、鼻中隔鼻底瓣或鼻腔外侧壁瓣等。对于坏死面积较大或鼻中隔瓣已无法使用的患者,可考虑采用颞肌瓣[12]、颞顶筋膜瓣、前额帽状腱膜骨膜瓣[13]、股外侧肌游离皮瓣[14]等。带蒂组织瓣对颈内动脉的覆盖,可避免颈内动脉直接裸露,减少术后大出血的风险,还有助于修复创面,减轻术后出现开放性鼻音及鼻腔反流的并发症。我们的手术患者多数进行了鼻腔黏膜游离瓣及鼻中隔带蒂组织瓣的修复,在缺损范围较大的情况下可能还是无法达到有效的修复或修复效果不佳,尤其容易出现皮瓣远端坏死,这也可能是Ⅳ期患者预后不佳的因素之一,这有待我们进一步的观察和研究。
放射性颅底坏死行鼻内镜手术后出现并发症的风险评估也是围手术期重点关注的内容,更是指导(手术)治疗方案决策的重要依据。根据研究结果发现病变程度及范围越大,术后出现并发症的概率也明显增高,患者的分期越高,术后出现并发症的发生率越高(P<0.05)。术后并发症包括术腔感染迁延不愈、鼻咽部大出血、进食反流、吞咽困难甚至死亡等。当然影响预后的危险因素也很多,包括患者的性别、年龄、原发肿瘤部位、放疗剂量及范围、合并鼻窦炎、病变部位和范围、是否合并全身基础疾病,很多患者不同程度的头痛、进食和睡眠障碍,术前存在长期过度、不合理地使用抗菌药物、激素药物的现象,术前细菌培养和药敏试验证实多药耐药等;这些因素均会影响术腔的愈合,尤其是修复的组织瓣、黏膜瓣,引发颈内动脉大出血,甚至危及生命。
通过本研究,鼻咽癌放疗后放射性颅底坏死的分型分期可以合理地判断坏死病变范围和程度,定性与定量相结合对病变进行评估,可以对患者进行比较准确的术前评估,有利于治疗(手术)方案的选择。当然,应用分型分期进行术前评估时,必须考虑风险因素的作用,譬如颈内动脉、皮瓣修复等的影响。总的来说,鼻咽癌放疗后放射性颅底坏死患者病情复杂,特别是病变累及颈内动脉的患者,易出现颈内动脉破裂出血,还有行二程放疗后的患者,病程往往迁延不愈,治疗也十分棘手,有待临床进一步研究。
Funding Statement
广西科技基地和人才专项基金(No:桂科AD20297069);广西医疗卫生适宜技术开发与推广应用项目(No:桂卫S201649)
Footnotes
利益冲突 所有作者均声明不存在利益冲突
References
- 1.章 华, 高 可雷, 谢 志海, et al. 内镜手术治疗鼻咽癌放射治疗后颅底软组织坏死的临床研究. 中华耳鼻咽喉头颈外科杂志. 2021;56(1):26–32. doi: 10.3760/cma.j.cn115330-20200608-00483. [DOI] [PubMed] [Google Scholar]
- 2.汤 轶强, 敖 帆, 黄 敏, et al. 放射性鼻咽颅底骨坏死的S-B分期探讨. 实用癌症杂志. 2020;35(4):561–563. doi: 10.3969/j.issn.1001-5930.2020.04.011. [DOI] [Google Scholar]
- 3.邱 前辉, 陈 海铃, 崔 毅, et al. 鼻咽癌放疗后颅底组织坏死的CT影像分级及手术治疗探讨. 中国临床新医学. 2023;16(1):1–7. [Google Scholar]
- 4.Sathasivam HP, Davies GR, Boyd NM. Predictive factors for osteoradionecrosis of the jaws: A retrospective study. Head Neck. 2018;40(1):46–54. doi: 10.1002/hed.24907. [DOI] [PubMed] [Google Scholar]
- 5.Spillinger A, Park K, Shenouda K, et al. Endoscopic management of postradiation skull base osteoradionecrosis. Int Forum Allergy Rhinol. 2020;10(12):1329–1333. doi: 10.1002/alr.22715. [DOI] [PubMed] [Google Scholar]
- 6.兰 桂萍, 黄 波, 司 勇锋, et al. 内镜经鼻入路处理鼻咽癌放疗后颅底骨坏死临床体会. 中华耳鼻咽喉头颈外科杂志. 2016;51(5):367–371. doi: 10.3760/cma.j.issn.1673-0860.2016.05.010. [DOI] [PubMed] [Google Scholar]
- 7.Komune N, Matsuo S, Miki K, et al. Surgical Anatomy of the Eustachian Tube for Endoscopic Transnasal Skull Base Surgery: A Cadaveric and Radiologic Study. World Neurosurg. 2018;112:e172–e181. doi: 10.1016/j.wneu.2018.01.003. [DOI] [PubMed] [Google Scholar]
- 8.Wang WH, Lieber S, Mathias RN, et al. The foramen lacerum: surgical anatomy and relevance for endoscopic endonasal approaches. J Neurosurg. 2018:1–12. doi: 10.3171/2018.6.JNS181117. [DOI] [PubMed] [Google Scholar]
- 9.李 峰, 蔡 泽虹, 许 卫华, et al. 鼻黏膜瓣在鼻咽癌放疗后鼻咽颅底骨质裸露修复中的应用. 临床耳鼻咽喉头颈外科杂志. 2021;35(10):929–934. doi: 10.13201/j.issn.2096-7993.2021.10.014. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 10.高 俊潇, 邱 前辉. 黏膜瓣在鼻咽癌放疗后鼻内镜手术修复颅底组织缺损中的应用. 山东大学耳鼻喉眼学报. 2019;33(2):46–50. [Google Scholar]
- 11.邹 雄, 王 顺兰, 刘 友平, et al. 经鼻内镜鼻咽坏死清创联合带血管蒂鼻腔黏骨膜瓣修复术治疗鼻咽癌放疗后鼻咽坏死. 癌症. 2020;39(6):271–282. [Google Scholar]
- 12.高 可雷, 章 华, 谢 志海, et al. 颞肌瓣在鼻咽癌放疗后肿瘤或坏死灶切除术后修复重建中的应用. 中华耳鼻咽喉头颈外科杂志. 2022;57(11):1288–1293. doi: 10.3760/cma.j.cn115330-20211206-00774. [DOI] [PubMed] [Google Scholar]
- 13.Adel M, Chang KP. Using a nasoseptal flap for the reconstruction of osteoradionecrosis in nasopharyngeal carcinoma: a case report. J Otolaryngol Head Neck Surg. 2016;45:27. doi: 10.1186/s40463-016-0139-1. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 14.Vlantis AC, Wong E, Chiu TW, et al. Vastus Lateralis Muscle Free Flap for Skull Base Osteoradionecrosis in Nasopharyngeal Carcinoma. J Neurol Surg B Skull Base. 2018;79(4):349–352. doi: 10.1055/s-0037-1608714. [DOI] [PMC free article] [PubMed] [Google Scholar]