En mai 2010, à la suite de signalements d’effets indésirables neuropsychiatriques, Santé Canada a obligé les fabricants du plus récent médicament d’ordonnance pour l’abandon du tabagisme, la varénicline, d’apposer une étiquette d’avertissement sur l’emballage1. Des avertissements concernant les risques accrus d’agressivité et de pensées et comportements suicidaires sont obligatoires depuis 2004 sur l’emballage du bupropion, un autre médicament d’ordonnance pour arrêter de fumer2. Ces avis sont généralement réservés aux médicaments qui ont été associés aux problèmes de sécurité ou d’effets indésirables les plus graves. En 2008, une révision clinique3 publiée dans Le Médecin de famille canadien présentait une mise à jour sur la sécurité et l’efficacité des pharmacothérapies pour l’abandon du tabagisme, mais les récentes mises en garde de Santé Canada à propos des changements d’humeur, de l’hostilité, des comportements suicidaires, et des réactions cutanées sérieuses et parfois fatales ont été publiées ultérieurement et elles concernent les médecins de famille.
L’Association médicale canadienne a émis sa première mise en garde contre les dangers du tabac en 1954 et maintient qu’aider les patients à arrêter de fumer compte parmi les plus importants services que peuvent offrir les médecins4. Les guides de pratique clinique recommandent d’offrir à chaque patient disposé à essayer d’abandonner le tabac du counseling et une pharmacothérapie (parmi un choix de 6 options homologuées au Canada), à moins de contre-indications5–7. Les interventions pour l’abandon du tabagisme sont largement reconnues comme étant efficaces, rentables et significatives sur le plan clinique. Les statistiques sur le nombre de personnes qu’il est nécessaire de traiter (pour sauver 1 vie) se situant à aussi peu que 9, ces interventions se comparent très favorablement à celles utilisées pour d’autres maladies chroniques8.
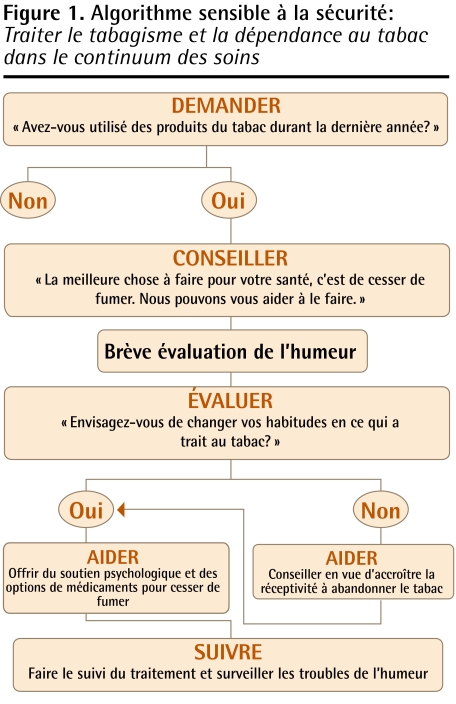
Les rapports d’effets neuropsychiatriques indésirables et les avertissements publiés par les instances de règlementation placent les médecins de famille dans une position précaire lorsqu’ils prennent en charge des patients ayant une dépendance au tabac. L’évaluation des risques neuropsychiatriques par rapport aux bienfaits connus des médicaments de sevrage du tabac (la thérapie de remplacement de la nicotine et le bupropion font presque doubler les taux de réussite, et la varénicline les fait presque tripler)6 pose des défis considérables. Le présent commentaire discute des relations entre l’humeur et le tabagisme, l’abstinence et les médicaments de sevrage. Il présente un algorithme pour guider la détection et la prise en charge des problèmes neuropsychiatriques. À notre connaissance, il s’agit de la première intégration formelle des considérations d’ordre neuropsychiatrique dans un algorithme de traitement pour cesser de fumer (Figure 1).
Figure 1.
Algorithme sensible à la sécurité: Traiter le tabagisme et la dépendance au tabac dans le continuum des soins
Considérations neuropsychiatriques et tabagisme
Les données factuelles existantes corroborent une morbidité concomitante considérable reliant la dépendance au tabac et la maladie mentale9. Il y a une relation directe selon la dose entre la consommation de tabac et la gravité des symptômes de dépression, ainsi que le risque de suicide. Par rapport à ceux qui n’ont jamais fumé, le taux de dépression chez les fumeurs est presque le double10 et le risque relatif de suicide réussi est de 2,5 fois plus élevé chez les fumeurs légers et de 4,3 plus grand chez les gros fumeurs11.
La nicotine est le principal facteur causant une dépendance, et elle affecte divers neurotransmetteurs qui influent sur l’humeur et la fonction cognitive12. Les symptômes reliés au sevrage de la nicotine comportent, entre autres, une humeur dépressive, de l’anxiété, de l’insomnie, de l’irritabilité, de la frustration, de la colère, de la difficulté à se concentrer, de l’agitation, un rythme cardiaque plus lent, un plus grand appétit ou un gain de poids13. Les symptômes du sevrage de la nicotine peuvent être plus prononcés chez ceux qui ont une maladie mentale préexistante.
La tabac contient aussi d’autres composés psychoactifs, notamment l’harmane et le norharmane, qui inhibent l’activité de l’enzyme monoamine-oxydase (MAO)14. Leur action est semblable à l’effet antidépresseur des inhibiteurs de la MAO disponibles sur le marché. À la cessation, le manque abrupt de nicotine et de ces agents similaires aux inhibiteurs de la MAO chez un fumeur neuroadapté offre une hypothèse biologiquement plausible expliquant le développement de certains symptômes neuropsychiatriques14. Chez les personnes ayant des antécédents dépressifs ou suicidaires, ces effets pourraient être considérablement plus prononcés et pourraient contribuer aux séquelles neuropsychiatriques observés dans certains cas.
Les hydrocarbures aromatiques polycycliques contenus dans le goudron produisent un enzyme cytochrome du foie (P450 1A2) qui entraine l’accélération du métabolisme de ses substrats, y compris plusieurs médicaments psychotropes et la caféine15. Lorsque les fumeurs réduisent considérablement leur consommation ou s’abstiennent complètement de fumer, le métabolisme de ces substrats peut ralentir substantiellement. Il est documenté que ce phénomène peut causer une augmentation des niveaux thérapeutiques dans le sang de médicaments comme l’olanzapine, la clozapine, l’halopéridol, la chlorpromazine et le diazépam. Réciproquement, le fait de recommencer à fumer après une abstinence prolongée peut entraîner une biodisponibilité réduite de ces médicaments et le risque accru inhérent de rechute dans les cas de problèmes comme la schizophrénie ou le trouble bipolaire. Par conséquent, la situation actuelle sur le plan du tabagisme, la quantité consommée et les changements dans la consommation ont tous des implications cliniques importantes dans la prise en charge des personnes qui prennent l’un ou l’autre de ces médicaments. Pareillement, les personnes pourraient avoir des symptômes d’intoxication à la caféine après avoir arrêté de fumer ou baissé leur consommation16.
Médicaments pour le sevrage et effets indésirables neuropsychiatriques
Quoiqu’ils soient rares, les effets indésirables signalés à propos de l’utilisation de la varénicline ou du bupropion chez les personnes avec ou sans maladie mentale préexistante peuvent inclure des changements d’humeur, de l’hostilité, une humeur dépressive, des pensées suicidaires et des suicides tentés ou commis. Certains des cas rapportés étaient apparemment compliqués par des symptômes de sevrage de la nicotine, tandis que d’autres se sont produits chez des personnes qui fumaient encore. En mai 2008, un rapport de l’Institute for Safe Medical Practices17 faisait état de presque 1 000 cas de problèmes graves reliés à la varénicline. On a immédiatement exprimé des inquiétudes au sujet de l’utilisation de la varénicline par des personnes conduisant un avion, un train ou d’autres véhicules et par des personnes dans d’autres milieux où une baisse de la vigilance ou du contrôle moteur pourrait entraîner des blessures graves. Par contre, on a aussi soulevé des préoccupations quant à la validité des constatations et des recommandations dans ce rapport18.
Au Canada, les avertissements de risque de suicide pour le bupropion et la varénicline sont semblables à ceux émis pour des anticonvulsifs, des antidépresseurs et le montélukast18. Comme dans les rapports de l’Institute for Safe Medical Practices, la surveillance subséquente à la mise en marché par Santé Canada ne prévoit pas de déclarations sur la fréquence ou la causalité putative des événements indésirables, ce qui rend difficile l’interprétation de la nature des événements indésirables neuropsychiatriques18. La majorité des rapports jusqu’à présent n’ont pas adéquatement traité de l’importance relative à attribuer aux variables reliées à l’abandon ou de leur contribution aux problèmes (p. ex. sevrage de la nicotine, effets sur le MAO, niveaux de caféine ou effets putatifs des médicaments). À ce jour, la somme des données probantes n’a pas permis de démontrer un lien de cause à effet entre l’utilisation d’une thérapie de remplacement de la nicotine, du buprorion ou de la varénicline et le développement de phénomènes dépressifs, suicidaires ou neuropsychiatriques, sauf des troubles du sommeil. Puisque la varénicline est un agoniste partiel des récepteurs de l’acétylcholine nicotinique α4β218, il n’y a pas d’hypothèse biologique connue selon laquelle un agoniste partiel serait directement ou de cause à effet associé à la dépression, à la psychose ou au suicide. Les risques neuropsychiatriques de la varénicline sont considérés comme rares; ce composé n’est pas associé à un risque accru de développer une maladie psychiatrique et est considéré comme un auxiliaire approprié pour l’abandon du tabagisme chez les patients qui ont une comorbidité médicale ou psychiatrique19.
Malgré la rareté de données scientifiques faisant valoir un lien de cause à effet entre la médication (thérapie de remplacement de la nicotine, bupropion ou varénicline) et les risques neuropsychiatriques, il y a un risque réel et excessivement pertinent de faire une dépression quand on arrête de fumer. Ce peut être le cas avec ou sans médicaments pour l’abandon du tabagisme chez des patients avec ou sans antécédents psychiatriques. Il est généralement accepté que les risques associés à la pharmacothérapie ne pèsent pas aussi lourds dans la balance en comparaison des risques que pose l’exposition aux 172 substances toxiques, 33 polluants atmosphériques dangereux, 47 produits chimiques considérés déchets dangereux et 67 carcinogènes connus chez l’humain ou l’animal qu’on trouve dans le tabac et la fumée de tabac.
Intégration de considérations neuropsychiatriques dans le traitement de la dépendance au tabac
Il est difficile pour les médecins d’exercer des degrés suffisants de vigilance à l’endroit des événements indésirables neuropsychiatrique, dans la prise en charge systématique de la dépendance au tabac, quel que soit le médicament adjuvant choisi pour aider les patients dans leur tentative d’abandon. Puisque 50 % des fumeurs ont des antécédents de dépression10 et que la cause principale d’incapacité est la dépression21, la surveillance de l’humeur revêt une importance particulière dans les milieux de soins primaires. La prudence dicte de dépister les problèmes d’humeur chez les patients qui fument ou ont une dépendance au tabac, qu’importe s’ils sont prêts à arrêter ou que des médicaments pour arrêter de fumer leur soient prescrits ou non.
Un algorithme qui porte sur le dépistage des problèmes d’humeur et de sécurité a été élaboré en collaboration avec des médecins de soins primaires pour surveiller les risques neuropsychiatriques causés par l’abstinence (Figure 1). Cet algorithme, adapté d’un outil du département américain de la Santé et des Services sociaux, identifie des points-clés pour dépister les troubles de l’humeur à l’aide de l’approche des 5-A5 (ask, advise, assess, assist, arrange) dans le traitement de la dépendance au tabac et tient compte des cycles en série de consommation du tabac, d’abstinence et de rechute. Les médecins décident de la pharmacothérapie en fonction des guides de pratiques exemplaires et de leur jugement clinique, sachant que des résultats de dépistage positifs à n’importe quelle étape du cycle indiquent qu’il faut faire une évaluation plus approfondie de l’humeur.
Dans ce contexte, la plus importante question permettant de prévoir des problèmes pourrait être: «Quels étaient vos émotions, vos pensées, votre humeur et votre comportement la dernière fois que vous avez arrêté de fumer ou réduit votre consommation?». Des constatations allant du risque de rechute aux symptômes de dépression indiquent qu’une surveillance en série est nécessaire et le recours à une échelle de mesure structurée pourrait être utile. Les épisodes de dépression majeure ou les problèmes neuropsychiatriques devraient être traités en fonction des conditions particulières. Le traitement de la dépression devrait être maintenu au moins pendant 6 mois après l’abandon et le traitement peut être individualisé pour se prolonger plus longtemps.
L’intuition clinique suggère qu’une thérapie prophylactique contre la dépression pourrait raisonnablement être indiquée pour les patients qui réduisent leur consommation ou cessent de fumer et qui ont des antécédents de dépression grave ou ont eu antérieurement un risque imminent de psychose ou d’autodestruction. La nortriptyline, un antidépresseur associé à des taux d’abandon plus élevés, n’est pas homologuée au Canada comme médicament pour cesser de fumer. Le bupropion est utilisé pour traiter la dépression et pour augmenter l’effet d’autres antidépresseurs, et l’admissibilité des patients devrait être évaluée individuellement en fonction des chances de réussite, des variables risques-bienfaits et de la préférence des patients. Le bupropion est associé à un risque plus faible de causer des manies par rapport à d’autres antidépresseurs, mais pourrait poser des risques neuropsychiatriques similaires à ceux de la varénicline.
De plus, il est important de faire la distinction entre de véritables pensées suicidaires et comportements connexes et d’autres formes de comportements autodestructeurs ayant des motivations différentes. Il faut prendre toutes les menaces au sérieux et agir en conséquence. Si les patients ont des symptômes atypiques ou s’ils commencent à avoir des idées ou comportements suicidaires, il est conseillé de cesser la médication contre le tabagisme et de demander immédiatement une attention médicale pour minimiser les préjudices et les événements indésirables. Les amis et la famille des personnes qui cessent de fumer devraient être encouragés à maintenir eux aussi une vigilance accrue.
Conclusion
La dépendance au tabac est une maladie chronique fréquente, mortelle et pourtant possible à traiter, qui est associée à de hauts degrés de troubles de l’humeur concomitants. On devrait offrir à chaque personne, ayant ou non une maladie mentale, qui est intéressée à arrêter de fumer une combinaison d’interventions psychosociales et de pharmacothérapie. Le traitement de remplacement de la nicotine, le bupropion ou la varénicline peuvent être considérés comme des options de première intention. Le dépistage et la prise en charge des troubles de l’humeur devraient être intégrés à la surveillance systématique de l’abandon du tabac. Cela inclut des évaluations en série pour écarter le risque de suicide imminent. Un algorithme sensible à la sécurité offre des conseils pour naviguer dans les décisions en fonction des risques et des bienfaits.
Acknowledgments
Ces travaux ont été financés par l’Alberta Cancer Legacy Fund des Services de santé de l’Alberta.
Footnotes
Cet article a fait l’objet d’une révision par des pairs
This article is also in English on page 647.
Intérêts concurrents
Jusqu’en 2009, Dr Els a reçu des subventions sans restrictions pour la formation et la recherche de Pfizer et de Johnson & Johnson. Mme Kunyk et Dr Sidhu n’ont aucun intérêt concurrent à déclarer.
Les opinions exprimées dans les commentaires sont celles des auteurs. Leur publication ne signifie pas qu’elles sont sanctionnées par le Collège des médecins de famille du Canada.
Références
- 1.Direction des produits de santé commercialisés, Direction générale des produits de santé et des aliments . Champix (varenicline tartrate)—changes to the Canadian product monograph. Ottawa, ON: Santé Canada; 2010. Accessible à: www.hc-sc.gc.ca/dhp-mps/medeff/advisories-avis/public/_2010/champix_2_pc-cp-eng.php. Accédé le 5 août 2010. [Google Scholar]
- 2.Direction des produits de santé commercialisés, Direction générale des produits de santé et des aliments . Important drug safety information for WELLBUTRIN SR and ZYBAN (bupropion HCI): warning for SSRIs and other newer anti-depressants regarding the potential for behavioural and emotional changes, including risk of self-harm—Biovail Pharmaceuticals Canada. Ottawa, ON: Santé Canada; 2010. Accessible à: www.hc-sc.gc.ca/dhp-mps/medeff/advisories-avis/prof/_2004/wellbutrin_zyban_hpc-cps-eng.php. Accédé le 12 novembre 2010. [Google Scholar]
- 3.Schmelzle J, Rosser WW, Birtwhistle R. Update on pharmacological and nonpharmacological therapies for smoking cessation. Can Fam Physician. 2008;54:994–9. [PMC free article] [PubMed] [Google Scholar]
- 4.Bureau de la santé publique de l’AMC . Tobacco. Ottawa, ON: Association médicale canadienne; 2007. Accessible à: www.cma.ca/index.php?ci_id=3401&la_id=1. Accédé le 21 avril 2011. [Google Scholar]
- 5.Fiore MC, Jaén C, Baker T, Bailey W, Benowitz N, Curry SJ, et al. Clinical practice guideline: treating tobacco use and dependence, 2008 update. Rockville, MD: US Department of Health and Human Services; 2008. Accessible à: www.surgeongeneral.gov/tobacco. Accédé le 5 août 2010. [Google Scholar]
- 6.Canadian Action Network for the Advancement, Dissemination and Adoption of Practice-informed Tobacco Treatment . CAN-ADAPTT: Canadian smoking cessation guideline. Toronto, ON: Canadian Action Network for the Advancement, Dissemination and Adoption of Practice-informed Tobacco Treatment; 2011. Accessible à: www.can-adaptt.net. Accédé le 21 avril 2011. [Google Scholar]
- 7.Raw M, Regan S, Rigotti NA, McNeil A. A survey of tobacco dependence treatment guidelines in 31 countries. Addiction. 2009;104(7):1243–50. doi: 10.1111/j.1360-0443.2009.02584.x. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 8.Woolf SH. The need for perspective in evidence-based medicine. JAMA. 1999;282(24):2358–65. doi: 10.1001/jama.282.24.2358. [DOI] [PubMed] [Google Scholar]
- 9.Lasser K, Boyd JW, Woolhandler S, Himmelstein DU, McCormick D, Bor DH. Smoking and mental illness: a population-based prevalence study. JAMA. 2000;284(20):2606–10. doi: 10.1001/jama.284.20.2606. [DOI] [PubMed] [Google Scholar]
- 10.Pratt L, Brody D. Depression and smoking in the US household population aged 20 and over, 2005–2008. Hyattsville, MD: USDHHS National Center for Health Statistics; 2010. NCHS data brief no. 34. Accessible à: www.cdc.gov/nchs/data/databriefs/db34.htm. Accédé le 5 août 2010. [PubMed] [Google Scholar]
- 11.Miller M, Hemenway D, Rimm E. Cigarettes and suicide: a prospective study of 50,000 men. Am J Public Health. 2000;90(5):768–73. doi: 10.2105/ajph.90.5.768. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 12.Benowitz N. Pharmacology of nicotine: addiction, smoking-induced disease, and therapeutics. Annu Rev Pharmacol Toxicol. 2009;49:57–71. doi: 10.1146/annurev.pharmtox.48.113006.094742. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 13.Hughes J. Nicotine withdrawal versus other drug withdrawal syndromes: similarities and dissimilarities. Addiction. 1994;89(11):1461–70. doi: 10.1111/j.1360-0443.1994.tb03744.x. [DOI] [PubMed] [Google Scholar]
- 14.Herraiz T, Chaparro C. Human monoamine oxidase is inhibited by tobacco smoke: beta-carboline alkaloids act as potent and reversible inhibitors. Biochem Biophys Res Comm. 2005;326(2):378–86. doi: 10.1016/j.bbrc.2004.11.033. [DOI] [PubMed] [Google Scholar]
- 15.Faber MS, Fuhr U. Time response of cytochrome P450 1A2 activity on cessation of heavy smoking. Clin Parmacol Ther. 2004;76(2):178–84. doi: 10.1016/j.clpt.2004.04.003. [DOI] [PubMed] [Google Scholar]
- 16.Swanson JA, Lee JW, Hopp JW, Berk LS. The impact of caffeine use on tobacco cessation and withdrawal. Addict Behav. 1997;22(1):55–68. doi: 10.1016/s0306-4603(96)00023-8. [DOI] [PubMed] [Google Scholar]
- 17.Moore TJ, Cohen MR, Furberg CD. Strong safety signal seen for new varenicline risks. Horsham, PA: Institute for Safe Medication Practices; 2008. Accessible à: www.ismp.org/docs/vareniclineStudy.asp. Accédé le 5 août 2010. [Google Scholar]
- 18.Rollema H, Coe JW, Chambers LK, Hurst RS, Stahl SM, Williams KE. Rationale, pharmacology and clinical efficacy of partial agonists of alpha-4beta2 nACh receptors for smoking cessation. Trends Pharmacol Sci. 2007;28(7):316–25. doi: 10.1016/j.tips.2007.05.003. Cyberpub. du 8 juin 2007. [DOI] [PubMed] [Google Scholar]
- 19.Tonstad S, Els C. Varenicline: smoking cessation in patients with psychiatric and medical comorbidity. Clin Med Insights Ther. 2010;2:681–95. Accessible à: http://la-press.com/article.php?article_id=2191. Accédé le 5 août 2010. [Google Scholar]
- 20.Repace JL. Exposure to second-hand smoke. In: Ott WR, Steinemann AC, Wallace LA, editors. Exposure analysis. Boca Raton, FL: Taylor & Francis Group; 2006. pp. 201–35. Accessible à: www.repace.com/pdf/EXPOSURE_TO_SECONDHAND_SMOKE.pdf. Accédé le 5 août 2010. [Google Scholar]
- 21.Organisation mondiale de la Santé . Depression. Genève, Suisse: Organisation mondiale de la santé; 2011. Accessible à: www.who.int/mental_health/management/depression/definition/en. Accédé le 5 août 2010. [Google Scholar]