Résumé
Objectif
Faire le résumé des anciens et des nouveaux moyens de traitement des verrues génitales ou condylomes et déterminer comment les utiliser de manière appropriée.
Sources des données
Une recherche documentaire a été effectuée dans les bases de données suivantes: MEDLINE, PubMed, EMBASE, base de données des synthèses systématiques et registre central des études contrôlées de la Collaboration Cochrane (en anglais), ACP Journal Club et Trip. Les bibliographies des articles extraits ont aussi été examinées. Les études cliniques, les articles de révision qualitative, les rapports consensuels et les guides de pratique clinique ont été retenus.
Message principal
Les verrues symptomatiques sont présentes chez au moins 1 % des personnes âgées entre 15 et 49 ans et on estime que jusqu’à 50 % des gens sont infectés par le virus du papillome humain à un moment donné de leur vie. L’imiquimod et la podophyllotoxine sont 2 nouveaux traitements pour les verrues génitales externes qui sont moins douloureux et peuvent être appliqués par les patients à la maison. De plus, il a été démontré que le vaccin quadrivalent contre le virus du papillome humain est efficace pour prévenir les condylomes et le cancer du col. Les plus anciennes méthodes thérapeutiques ont aussi leur place dans certaines situations, comme les verrues intravaginales, urétrales, anales ou récalcitrantes ou encore pour les patientes enceintes.
Conclusion
Les nouveaux traitements des verrues génitales externes peuvent réduire la douleur causée par la thérapie et le nombre de visites au cabinet. Les autres méthodes thérapeutiques demeurent utiles dans certaines situations.
Présentation du cas
Une femme de 24 ans se présente à votre cabinet et se plaint d’avoir depuis 3 mois des petites «bosses» sensibles qui piquent sur la vulve. Elle est une cycliste de compétition et, lorsqu’elle fait du vélo, ces bosses sont irritées et saignent même parfois. Elle n’est pas actuellement active sexuellement, mais elle a eu 4 partenaires sexuels masculins par le passé et sa plus récente relation a pris fin il y a 6 mois. À l’examen, vous observez de multiples lésions papillomateuses sur les lèvres externes qui ont l’apparence de verrues. Vous vous apprêtez à prendre de la podophylline, mais vous vous rappelez avoir entendu parler de nouveaux traitements topiques pour les verrues génitales qui sont plus pratiques et moins toxiques. Vous vous demandez aussi si vous devriez discuter du vaccin contre le virus du papillome humain (VPH) avec votre patiente.
Sources des données
Une recherche documentaire a été effectuée dans les bases de données MEDLINE, PubMed, EMBASE, la base de données des synthèses systématiques et le registre central des études contrôlées de la Collaboration Cochrane (en anglais), ACP Journal Club et Trip jusqu’à mars 2011. Des recensions ont été faites pour chaque traitement individuellement et se sont limitées aux articles en anglais. Les expressions de recherche étaient warts ou condyloma acuminata ou papilloma virus et venereal ou genital ou vaginal ainsi que le traitement spécifique. Les bibliographies des articles extraits ont aussi été examinées pour cerner des articles pertinents. Les articles portant sur les néoplasmes cervicaux et les études auprès de patients immunodéficients, séropositifs pour le VIH ou des hommes homosexuels ont été exclus.
La recherche a produit 77 articles pertinents dont le résumé a été évalué pour déterminer s’ils seraient inclus dans cette révision fondée sur des données probantes, la préférence étant accordée aux synthèses systématiques de la Collaboration Cochrane. De tous les articles extraits, 49 ont été lus et 30 ont été inclus dans la présente révision.
Les recommandations et le niveau des données probantes ont été classés à l’aide du système du Groupe de travail canadien sur les soins de santé préventifs (Tableau 1)1.
Tableau 1.
Grades des recommandations et niveaux des données probantes selon le Groupe d’étude canadien sur les soins de santé préventifs
| GRADE OU NIVEAU | RECOMMANDATION OU DONNÉES PROBANTES |
|---|---|
| A | Il y a de bonnes données probantes permettant de recommander l’acte clinique préventif |
| B | Il y a d’assez bonnes données probantes permettant de recommander l’acte clinique préventif |
| C | Les données probantes actuelles sont contradictoires et ne permettent pas de recommander ou non l’utilisation de l’acte clinique préventif; par ailleurs, d’autres facteurs pourraient influencer la prise de décision |
| D | Il y a d’assez bonnes données probantes permettant de ne pas recommander l’acte clinique préventif |
| E | Il y a de bonnes données probantes permettant de ne pas recommander l’acte clinique préventif |
| F | Les données probantes sont insuffisantes (en quantité ou en qualité) pour permettre de faire une recommandation; par ailleurs, d’autres facteurs pourraient influencer la prise de décision |
| I | Au moins 1 étude randomisée contrôlée, 1 synthèse systématique ou 1 méta-analyse effectuée de manière appropriée |
| II | Autres études comparatives, non randomisées, de cohortes, cas-témoins ou épidémiologiques et préférablement plus de 1 |
| III | Opinions d’experts ou déclarations consensuelles |
Adaptation du Groupe d’étude canadien sur les soins de santé préventifs1
Message principal
Les verrues génitales ou condylomes sont une cause fréquente de morbidité. La prévalence des verrues symptomatiques dans la population se situe à au moins 1 % chez les 15 à 49 ans2,3 et on estime que jusqu’à 50 % des gens seront infectés par le VPH à un moment donné de leur vie4. Au cours de la dernière décennie, de nouveaux traitements ont fait leur apparition et ont rendu certains des anciens traitements, comme la podophylline, moins populaires. Cette révision présente de nouvelles approches au traitement et à la prise en charge des verrues génitales, tout en incluant des rôles possibles pour certains des plus anciens traitements (Tableau 2 et Figures 1 et 2)5–21.
Tableau 2.
Options thérapeutiques privilégiées ou de rechange:Les variations dans les taux d’élimination et de récurrence reflètent celles observées d’une étude à l’autre
| TRAITEMENT, NIVEAU DES DONNÉES PROBANTES ET GRADE DE LA RECOMMANDATION | ÉLIMINATION % | RÉCURRENCE % | RÉGIME D’APPLICATION | EFFETS INDÉSIRABLES | UTILISATION INTRAVAGINALE OU INTRAANALE SÉCURITAIRE | UTILISATION SÉCURITAIRE DURANT LA GROSSESSE OU L’ALLAITEMENT |
|---|---|---|---|---|---|---|
| Traitements appliqués par la patiente | ||||||
| Crème d’imiquimod à 5 %5–7 (grade B, niveau I)* L’imiquimod à 3,75 % n’a pas été évalué pour le traitement des condylomes |
51 | 22–63 | Appliquer avec le doigt 3 soirs/semaine pendant 16 semaines. Laver le matin | Érythème localisé, sensation de brûlure, inflammation; rarement, une hypopigmentation Peut affaiblir les condoms et les diaphragmes en latex | Non | Non; innocuité inconnue |
| Solution ou gel de podophyllotoxine à 0,5 %7 (grade B, niveau I)* Plus efficace et moins toxique que la podophylline |
56 | 2–90 | Appliquer avec un tampon ou le doigt 2 fois/j pendant 3 j, arrêter 4 j et refaire pendant au plus 4 cycles. Limite de 10 cm2/j de surface de peau ou 0,5 ml/j | Sensation de brûlure localisée, douleur, démangeaison, érosion, inflammation | Non | Non; c’est un extrait de la podophylline qui est tératogène |
| Traitements administrés par le professionnel | ||||||
| Cryothérapie8–12 (grade B, niveau I)* | 27–88 | 25–55 | 1 fois par semaine avec un tampon de coton, un vaporisateur ou une cryosonde (pas dans le vagin) | Douleur localisée, inflammation, cicatrice Risque de perforation vaginale avec la cryosonde | Oui | Oui |
| TCA10,11,13 (grade B, niveau I)* | 63–70 | 35 | Une fois par semaine avec un tampon de coton ou un curedents | Douleur localisée et ulcération Peut être neutralisée avec une solution de bicarbonate de soude | Oui | Oui |
| Excision14 (grade B, niveau I)† | 35–72 | 19–79 | Anesthésie locale puis excision des lésions | Douleur, saignement, infection | Oui | Oui |
| Électrocautérisation14 (grade B, niveau II)† | 61–94 | 22 | Anesthésie locale puis destruction des lésions avec les outils de cautérisation | Douleur, saignement, infection Le professionnel devrait porter un masque qui filtre les virus | Oui | Oui |
| Traitements de rechange | ||||||
| Podophylline à 25 % dans une teinture de benjoin14–16 (grade C, niveau I)‡ | 23–72 | 23–65 | Une fois par semaine avec un tampon de coton ou un curedents Limite de 10 cm2 de surface de peau ou 0,5 ml par traitement | Sensation de brûlure localisée, douleur, démangeaison, érosion, inflammation | Limite <2 cm2 de surface de peau | Non; est tératogène |
| Onguent de sinécatéchine (extrait de thé vert) à15 %17,18 (grade B, niveau II; 2 études)‡ | 57 | 6,5 | Appliquer 3 fois/j pendant au plus 16 semaines | Érythème localisé, sensation de brûlure, douleur, rash, ulcération | Non; aucune étude | Non; aucune étude |
| Gel de fluorouracile à 1 % ou crème à 5 %19,20 (grade C, niveau II)‡ Utile pour les condylomes en grand nombre dans le vagin ou la région de l’urètre/méat où la cryothérapie ou le TCA ne sont pas tolérés |
80–90 | Aucune donnée | Insérer un plein applicateur dans le vagin 3 soirs par semaine | Érythème, érosion, œdème | Oui | Non; est tératogène |
| Interféron21 (grade C, niveau II)‡ | 44,4 | 21,1 | Insérer un plein applicateur dans le vagin 2 fois/j pendant 5 j durant 4 semaines | Maux de tête, sensibilité, fièvre transitoire | Oui | Non; aucune étude |
| Observation*14 | 40–60 | Aucune donnée | Aucune donnée | Aucune donnée | Aucune donnée | Aucune donnée |
TCA—acide trichloracétique
Thérapie de première intention
Thérapie de deuxième intention
Thérapie généralement non recommandée
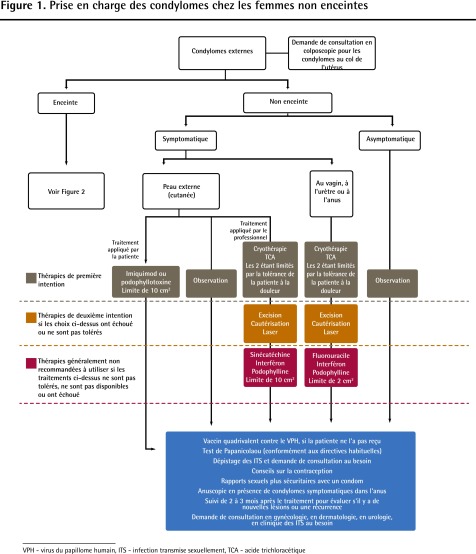
Figure 1.
Prise en charge des condylomes chez les femmes non enceintes
VPH - virus du papillome humain, ITS - infection transmise sexuellement, TCA - acide trichloracetique
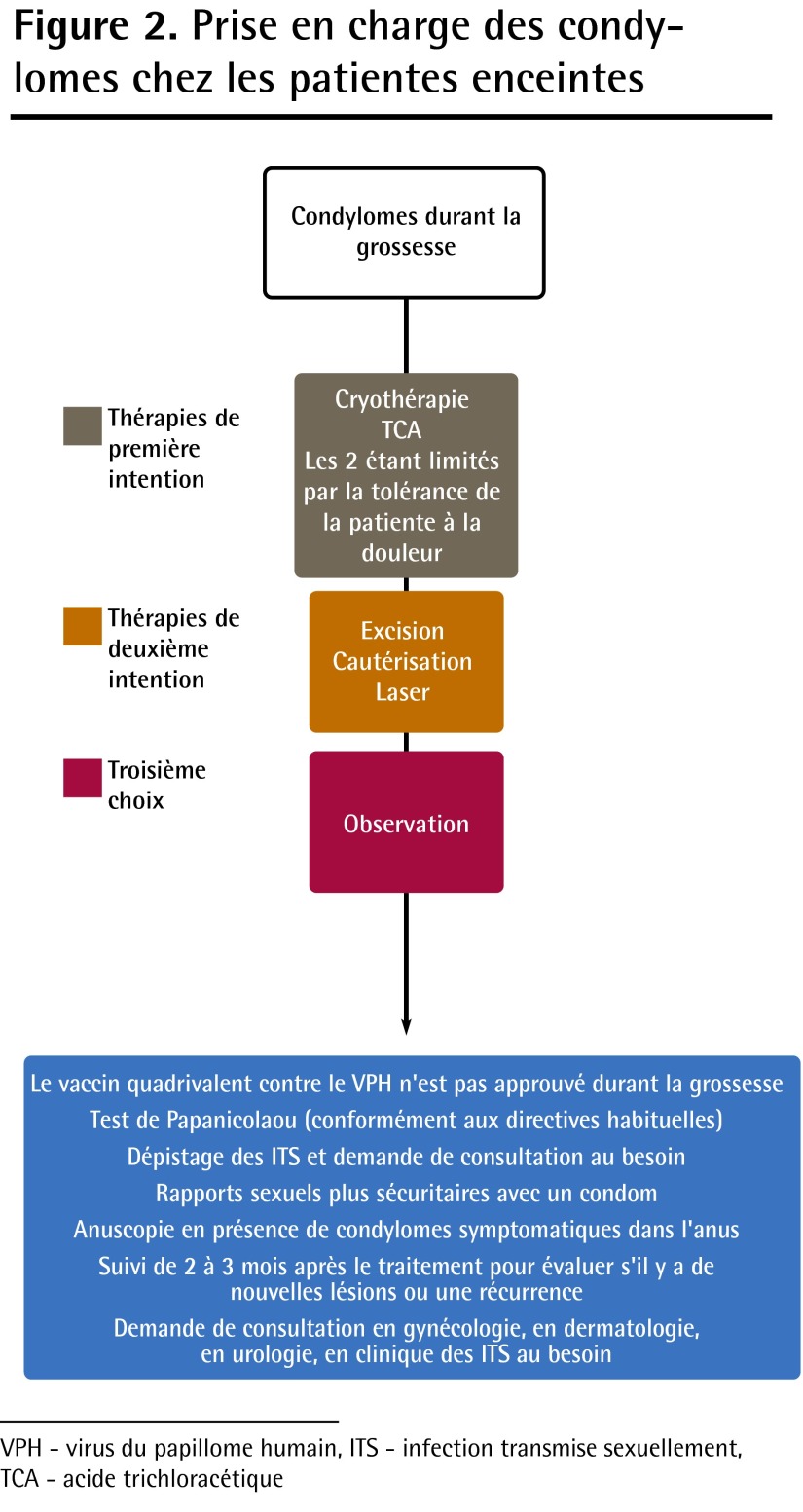
Figure 2.
Prise en charge des condylomes chez les patientes enceintes
VPH - virus du papillome humain, ITS - infection transmise sexuellement, TCA - acide trichloracetique
Les condylomes visibles peuvent être une source de détresse psychologique et physique pour les patients. Quoique les verrues soient souvent asymptomatiques, dans d’autres cas, elles peuvent causer de la douleur, des démangeaisons, une sensation de brûlure, de l’irritation au contact des vêtements et, occasionnellement, des saignements4. Ils peuvent aussi causer de la douleur et des saignements durant les rapports sexuels.
Le traitement des verrues génitales bénignes symptomatiques a pour but l’atténuation des symptômes physiques et l’amélioration cosmétique. De 40 % à 60 % des condylomes non traités disparaîtront spontanément dans un délai de 9 à 12 mois14, mais de nombreux patients ressentent une détresse psychologique due à leur présence et ont besoin d’une intervention pour les éradiquer (Encadré 1).
Encadré 1. Pour commencer.
Discuter des options thérapeutiques avec la patiente, y compris l’observation, et tenir compte de l’emplacement des condylomes, du degré de réceptivité à l’endroit d’un traitement douloureux (cryothérapie ou acide trichloracétique) et de la possibilité d’une grossesse
Prescrire un test de grossesse et discuter de contraception avec les femmes fertiles si elles sont traitées avec de l’imiquimod, de la podophyllotoxine ou de la podophylline
Commencer le traitement avec une thérapie de première intention et le poursuivre pendant la durée recommandée
Réévaluer à la fin du traitement et répéter si les lésions n’ont pas disparu ou si de nouvelles sont apparues
Si les lésions ne semblent pas répondre au traitement après 2 ou 3 cycles, essayer une autre thérapie de première intention. S’il y a une réponse au traitement, poursuivre avec cette thérapie et répéter les cycles de traitement au besoin
Continuer ainsi jusqu’à ce qu’un traitement qui fonctionne soit trouvé pour cette patiente. Choisir une thérapie de deuxième intention s’il est impossible de trouver une thérapie de première intention appropriée
Dans les situations où les thérapies de première intention ont échoué, sont contre-indiquées ou ne sont pas tolérées par la patiente et où les thérapies de deuxième intention ne sont pas disponibles ou faisables (p. ex. condylomes périurétraux), essayer une thérapie généralement non recommandée. Elles ne sont habituellement pas recommandées parce qu’il n’y a pas assez de données probantes, que leurs effets secondaires sont plus importants ou qu’elles sont tératogènes, mais elles restent utiles dans les cas difficiles
Si toutes les options thérapeutiques ont échoué, demander pour la patiente une consultation auprès d’une clinique locales des infections transmises sexuellement, d’un gynécologue, d’un dermatologues ou d’un urologue
Les condylomes sont causés par plusieurs souches du VPH et se transmettent par contact de peau à peau durant l’activité sexuelle. Ils sont donc considérés comme une infection transmise sexuellement (ITS)22. Un certain nombre de traitements différents sont disponibles. Certains d’entre eux peuvent être appliqués par les patients eux-mêmes, tandis que d’autres exigent qu’ils soient administrés par une infirmière ou un médecin. Dans cet article, j’ai inclus des traitements plus anciens (p. ex. podophylline), dont l’utilisation pourrait maintenant être reléguée aux cas difficiles, parce que de nombreux omnipraticiens en pratique depuis des décennies les connaissent. Il pourrait leur être utile de savoir ce qu’il advient présentement de ces traitements. J’ai aussi inclus certains nouveaux traitements moins utilisés (interféron, sinécatéchine) parce que les lecteurs pourraient en avoir entendu parler et se questionnent à propos de leur utilisation.
Le diagnostic des condylomes se fait par inspection visuelle en les identifiant par l’apparence des lésions qui est conforme à celle d’une verrue. Ils peuvent apparaître sous forme de plaques papillomateuses ou de lésions plates et il peut y en avoir un seul ou plusieurs ou bien ils peuvent former un condylome acuminé (crête de coq). Leur couleur peut être celle de la peau ou varier de blanc à rose ou à brun. Chez la femme, ils peuvent se trouver sur le col, la vulve, dans le vagin, le méat urétral ou la région périanale. Chez l’homme, ils peuvent se situer sur le scrotum, la verge, le gland et sous le prépuce du pénis ou dans la région périanale23.
Le diagnostic différentiel peut inclure les glandes sébacées, une verrue séborrhéique, un molluscum contagiosum, le psoriasis, le lichen plan, un nævus mélanocytaire, un fibroépithéliome, une néoplasie et un condylome plat (syphilis)23. Il se peut qu’une biopsie soit parfois indiquée pour confirmer le diagnostic et exclure la possibilité d’un cancer. Il n’est pas recommandé de procéder au test du blanchiment après application d’une solution d’acide acétique de 3 % à 5 % (vinaigre domestique) parce qu’il n’est pas considéré suffisamment spécifique pour être utile4. Les types 16 et 18 du virus du papillome humain causent plus de 70 % des cas de cancer invasif du col24. Plus de 90 % des cas bénins de l’infection (condylomes) ont pour origine les types 6 et 1115.
La transmission du VPH au nouveau-né peut entraîner chez ce dernier une papillomatose laryngée. Étant donné qu’il s’agit d’un problème rare et non cancéreux et qu’il n’est pas clair si le nouveau-né est infecté durant l’accouchement ou postpartum, la césarienne préventive n’est pas recommandée (grade C, niveau II)4.
Des experts ont publié une opinion consensuelle à l’effet qu’il faudrait essayer de réduire la charge de VPH chez la femme enceinte en traitant les verrues génitales avant l’accouchement, quoiqu’il n’y ait pas de données probantes indiquant que de tels traitement réduisent la charge virale (niveaux I à III)4. Il n’y a pas assez de données probantes pour dire que le traitement des condylomes visibles éradique l’infection au VPH ou qu’il prévient la transmission du virus4,25.
Autres moyens de prise en charge et de prévention
Le vaccin quadrivalent contre le VPH protège contre les VPH de types 6, 11, 16 et 18, les souches qui causent communément les verrues bénignes et le cancer du col. Des études initiales chez des femmes ont démontré que son efficacité pour prévenir les condylomes se situe entre 90 % et 100 %26. Après l’instauration d’un programme de vaccination en 2007, une étude de suivi 4 ans après auprès de jeunes femmes sexuellement actives en Australie a fait valoir un déclin marqué dans la prévalence des verrues génitales, soit de 11,7 % à 4,8% dès 2009 et une réduction constante mais plus lente depuis. On lui a aussi associé une baisse cependant moins dramatique dans l’incidence des condylomes chez les hommes hétérosexuels, potentiellement en raison d’une exposition réduite au virus étant donné qu’un plus grand nombre de leurs partenaires étaient vaccinées27,28.
À l’heure actuelle au Canada, le vaccin quadrivalent contre le VPH est approuvé pour les femmes de 9 à 26 ans. Il est recommandé d’offrir le vaccin aux femmes qui ont des condylomes et qui ne l’ont pas encore reçu (3 doses à 0, 2 et 6 mois). Quoiqu’il ne guérisse pas une infection active au VPH, il peut aider à prévenir une réinfection par d’autres souches (en particulier à celles de types 16 ou 18 qui sont à risque plus élevé). Il y a des données probantes de grade A, niveau I à l’effet qu’il prévient les verrues génitales23,27.
Le vaccin quadrivalent contre le VPH a un avantage accru en matière de rentabilité; il réduit le fardeau sur le plan des coûts, car il prévient à la fois les condylomes et le cancer du col, par rapport à la vaccination contre seulement le cancer du col3.
En plus de l’administration du vaccin quadrivalent contre le VPH, les recommandations suivantes aident à prévenir et à prendre en charge les verrues génitales:
Toutes les femmes devraient subir un test de Papanicolaou pour dépister une infection concomitante avec des souches cancérigènes.
Il faudrait faire un dépistage d’autres ITS chez les femmes, conformément aux lignes directrices sur les ITS. Il n’est pas indiqué de faire un dépistage des condylomes chez les partenaires4. Il n’est pas nécessaire de traiter les verrues génitales à moins qu’elles soient symptomatiques.
Il faudrait procéder à une anuscopie pour confirmer le diagnostic des condylomes symptomatiques dans l’anus (démangeaisons, douleur, saignements). Les verrues asymptomatiques peuvent être observées et un diagnostic n’est donc pas nécessaire. Elles peuvent se produire sans antécédents de pénétrations anales.
Il y aurait peut-être lieu de discuter de contraception et d’en prescrire, en particulier si on utilise un traitement des condylomes qui est contre-indiqué durant la grossesse. N’oubliez pas que l’imiquimod peut affaiblir les dispositifs de protection en latex comme le condom ou le diaphragme.
Les condoms offrent une protection, quoiqu’elle soit incomplète, contre la transmission du VPH (grade B, niveau II)29,30.
Il est recommandé de faire un suivi 2 ou 3 mois après avoir obtenu la disparition des verrues pour vérifier une récurrence ou de nouvelles lésions.
Les patients atteints de condylomes symptomatiques récalcitrants (difficiles à traiter) devraient faire l’objet d’une demande de consultation auprès d’une clinique locale des ITS, d’un gynécologue, d’un dermatologue ou d’un urologue.
Règlement du cas
Vous posez un diagnostic de condylomes. Vous faites un test de Pap et un dépistage de la gonorrhée et de la chlamydia. Vous dites à la patiente que les condoms pourraient aider à prévenir la transmission. Après avoir discuté la possibilité d’un traitement ou d’une observation, elle décide qu’elle aimerait traiter ses verrues génitales parce qu’elles la dérangent. Vous lui prescrivez un contraceptif oral avant de commencer le traitement et vous prenez des arrangements pour qu’elle reçoive un vaccin quadrivalent contre le VPH. Vous lui prescrivez de la crème d’imiquimod à 5 %, à appliquer à la maison 3 soirs par semaine pendant 16 semaines. Lorsque vous la voyez par la suite, 2 mois après la fin du traitement, il n’y a plus de condylomes visibles.
Limites
La présente révision était limitée par les données probantes disponibles en anglais au moment de la rédaction. Des synthèses systématiques sont disponibles concernant 5 des thérapies, et même dans ces cas, certaines des études utilisées dans les synthèses n’étaient pas de bonne qualité (p. ex. études sur le fluorouracile)20. D’autres thérapies ont fait l’objet de beaucoup plus de recherches antérieures (p. ex. imiquimod). Il n’y a pas beaucoup de renseignements sur l’innocuité durant la grossesse de l’imiquimod, de l’interféron et de la sinécatéchine. Dans certains cas, les résultats de la recherche restent à venir (p. ex. vaccin contre le VPH). Ce sujet mériterait d’être examiné à nouveau dans 4 ans.
Conclusion
Le moment et la façon de traiter les condylomes sont des décisions que devraient prendre ensemble le patient et le clinicien. Le choix du traitement devrait reposer sur la gravité des symptômes, tant psychologiques que physiques, et tenir compte des effets indésirables du traitement. La décision finale pourrait dépendre de l’étendue des verrues génitales et de la tolérance qu’a le patient aux traitements douloureux ou encore du temps que le patient est prêt à investir dans des traitements répétés. L’avènement de traitements que peuvent appliquer eux-mêmes les patients réduit le fardeau des visites fréquentes à la clinique.
POINTS DE REPÈRE DU RÉDACTEUR.
Presque toutes les verrues génitales sont bénignes et ne sont pas associées au cancer du col ou du pénis.
Le traitement des condylomes a pour but d’atténuer les symptômes et la détresse émotionnelle. La plupart des cas de verrues génitales disparaîtront spontanément, habituellement dans un délai de 12 mois, si elles ne sont pas traitées.
Aucune donnée probante ne corrobore que le traitement des condylomes visibles préviendra la transmission du virus.
Le vaccin quadrivalent contre le virus du papillome humain est efficace pour prévenir les condylomes, mais il ne fera pas disparaître ceux déjà présents.
Footnotes
Cet article donne droit à des crédits Mainpro-M1. Pour obtenir des crédits, allez à www.cfp.ca et cliquez sur le lien vers Mainpro.
The English version of this article is available at www.cfp.ca on the table of contents for the July 2013 issue on page 731.
Cet article a fait l’objet d’une révision par des pairs.
Intérêts concurrents
Aucun déclaré
Références
- 1.Groupe d’étude canadien sur les soins de santé préventifs New grades for recommendations from the Canadian Task Force on Preventive Health Care. CMAJ. 2003;169(3):207–8. [PMC free article] [PubMed] [Google Scholar]
- 2.Gall SA. Female genital warts: global trends and treatments. Infect Dis Obstet Gynecol. 2001;9(3):149–54. doi: 10.1155/S1064744901000278. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 3.Money DM, Roy M. Canadian consensus guidelines on human papillomavirus. J Obstet Gynaecol Can. 2007;29(8 Suppl 3):S1–56. doi: 10.1016/S1701-2163(16)32573-7. [DOI] [PubMed] [Google Scholar]
- 4.Workowski KA, Berman S, Centers for Disease Control and Prevention Sexually transmitted diseases treatment guidelines, 2010. MMWR Recomm Rep. 2010;59(RR-12):1–110. [PubMed] [Google Scholar]
- 5.Gotovtseva EP, Kapadia AS, Smolensky MH, Lairson DR. Optimal frequency of imiquimod (Aldara) 5% cream for the treatment of external genital warts in immunocompetent adults: a meta-analysis. Sex Transm Dis. 2008;35(4):346–51. doi: 10.1097/OLQ.0b013e31815ea8d1. [DOI] [PubMed] [Google Scholar]
- 6.Moore RA, Edwards JE, Hopwood J, Hicks D. Imiquimod for the treatment of genital warts: a quantitative systematic review. BMC Infect Dis. 2001;1:3. doi: 10.1186/1471-2334-1-3. Cyberpub. du 5 juin 2001. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 7.Yan J, Chen SL, Wang HN, Wu TX. Meta-analysis of 5% imiquimod and 0.5% podophyllotoxin in the treatment of condylomata acuminata. Dermatology. 2006;213(3):218–23. doi: 10.1159/000095039. [DOI] [PubMed] [Google Scholar]
- 8.Stefanaki C, Katzouranis I, Lagogianni E, Hadjivassiliou M, Nicolaidou E, Panagiotopoulos A, et al. Comparison of cryotherapy to imiquimod 5% in the treatment of anogenital warts. Int J STD AIDS. 2008;19(7):441–4. doi: 10.1258/ijsa.2007.007196. Erratum dans: Int J STD AIDS 2008;19(10):722. [DOI] [PubMed] [Google Scholar]
- 9.Stone KM, Becker TM, Hadgu A, Kraus SJ. Treatment of external genital warts: a randomised clinical trial comparing podophyllin, cryotherapy, and electrodesiccation. Genitourin Med. 1990;66(1):16–9. doi: 10.1136/sti.66.1.16. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 10.Abdullah AN, Walzman M, Wade A. Treatment of external genital warts comparing cryotherapy (liquid nitrogen) and trichloroacetic acid. Sex Transm Dis. 1993;20(6):344–5. [PubMed] [Google Scholar]
- 11.Godley MJ, Bradbeer CS, Gellan M, Thin RN. Cryotherapy compared with trichloroacetic acid in treating genital warts. Genitourin Med. 1987;63(6):390–2. doi: 10.1136/sti.63.6.390. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 12.Yliskoski M, Saarikoski S, Syrjänen K, Syrjänen S, Castrén O. Cryotherapy and CO2-laser vaporization in the treatment of cervical and vaginal human papillomavirus (HPV) infections. Acta Obstet Gynecol Scand. 1989;68(7):619–25. doi: 10.3109/00016348909013281. [DOI] [PubMed] [Google Scholar]
- 13.Sherrard J, Riddell L. Comparison of the effectiveness of commonly used clinic-based treatments for external genital warts. Int J STD AIDS. 2007;18(6):365–8. doi: 10.1258/095646207781024711. [DOI] [PubMed] [Google Scholar]
- 14.Wiley DJ, Douglas J, Beutner K, Cox T, Fife K, Moscicki AB, et al. External genital warts: diagnosis, treatment, and prevention. Clin Infect Dis. 2002;35(Suppl 2):S210–24. doi: 10.1086/342109. [DOI] [PubMed] [Google Scholar]
- 15.Mayeaux EJ, Jr, Dunton C. Modern management of external genital warts. J Low Genit Tract Dis. 2008;12(3):185–92. doi: 10.1097/LGT.0b013e31815dd4b4. [DOI] [PubMed] [Google Scholar]
- 16.BASHH HPV Special Interest Group . United Kingdom national guideline on the management of anogenital warts, 2007. Macclesfield, RU: British Association for Sexual Health and HIV; 2007. Accessible à: www.bashh.org/documents/86/86.pdf. Accédé le 28 mai 2013. [Google Scholar]
- 17.Tatti S, Stockfleth E, Beutner KR, Tawfik H, Elsasser U, Weyrauch P, et al. Polyphenon E: a new treatment for external anogenital warts. Br J Dermatol. 2010;162(1):176–84. doi: 10.1111/j.1365-2133.2009.09375.x. Cyberpub. du 27 juillet 2009. [DOI] [PubMed] [Google Scholar]
- 18.Tatti S, Swinehart JM, Thielert C, Tawfik H, Mescheder A, Beutner KR. Sinecatechins, a defined green tea extract, in the treatment of external anogenital warts: a randomized controlled trial. Obstet Gynecol. 2008;111(6):1371–9. doi: 10.1097/AOG.0b013e3181719b60. [DOI] [PubMed] [Google Scholar]
- 19.Batista CS, Atallah AN, Saconato H, da Silva EM. 5-FU for genital warts in non-immunocompromised individuals. Cochrane Database Syst Rev. 2010;(4):CD006562. doi: 10.1002/14651858.CD006562.pub2. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 20.Syed TA, Qureshi ZA, Ahmad SA, Ali SM. Management of intravaginal warts in women with 5-fluorouracil (1%) in vaginal hydrophilic gel: a placebo-controlled double-blind study. Int J STD AIDS. 2000;11(6):371–4. doi: 10.1258/0956462001916074. [DOI] [PubMed] [Google Scholar]
- 21.Yang J, Pu YG, Zeng ZM, Yu ZJ, Huang N, Deng QW. Interferon for the treatment of genital warts: a systematic review. BMC Infect Dis. 2009;9:156. doi: 10.1186/1471-2334-9-156. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 22.Ault KA. Epidemiology and natural history of human papillomavirus infections in the female genital tract. Infect Dis Obstet Gynecol. 2006;2006(Suppl):40470. doi: 10.1155/IDOG/2006/40470. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 23.Australia and New Zealand HPV Project . Guidelines for the management of genital HPV in Australia and New Zealand. 5 éd. Viral Sexually Transmitted Infection Education Foundation; 2007. [Google Scholar]
- 24.Ogunmodede F, Yale SH, Krawisz B, Tyler GC, Evans AC. Human papillomavirus infections in primary care. Clin Med Res. 2007;5(4):210–7. doi: 10.3121/cmr.2007.751. Cyberpub. du 17 décembre 2007. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 25.Lacey CJ. Therapy for genital human papillomavirus-related disease. J Clin Virol. 2005;32(Suppl 1):S82–90. doi: 10.1016/j.jcv.2004.10.020. [DOI] [PubMed] [Google Scholar]
- 26.FUTURE I/II Study Group. Dillner J, Kjaer SK, Wheeler CM, Sigurdsson K, Iversen OE, et al. Four year efficacy of prophylactic human papillomavirus quadrivalent vaccine against low grade cervical, vulvar, and vaginal intraepithelial neoplasia and anogenital warts: randomised controlled trial. BMJ. 2010;341:c3493. doi: 10.1136/bmj.c3493. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 27.Donovan B, Franklin N, Guy R, Grulich AE, Regan DG, Ali H, et al. Quadrivalent human papillomavirus vaccination and trends in genital warts in Australia: analysis of national sentinel surveillance data. Lancet Infect Dis. 2011;11(1):39–44. doi: 10.1016/S1473-3099(10)70225-5. Cyberpub. du 8 novembre 2010. [DOI] [PubMed] [Google Scholar]
- 28.Fairley CK, Hocking JS, Gurrin LC, Chen MY, Donovan B, Bradshaw CS. Rapid decline in presentations of genital warts after the implementation of a national quadrivalent human papillomavirus vaccination programme for young women. Sex Transm Infect. 2009;85(7):499–502. doi: 10.1136/sti.2009.037788. Cyberpub. du 16 octobre 2009. [DOI] [PubMed] [Google Scholar]
- 29.Manhart LE, Koutsky LA. Do condoms prevent genital HPV infection, external genital warts, or cervical neoplasia? A meta-analysis. Sex Transm Dis. 2002;29(11):725–35. doi: 10.1097/00007435-200211000-00018. [DOI] [PubMed] [Google Scholar]
- 30.Winer RL, Hughes JP, Feng Q, O’Reilly S, Kiviat NB, Holmes KK, et al. Condom use and the risk of genital human papillomavirus infection in young women. N Engl J Med. 2006;354(25):2645–54. doi: 10.1056/NEJMoa053284. [DOI] [PubMed] [Google Scholar]