Résumé
Objectif
Accroître l’utilisation d’approches éclairées par des données probantes pour diagnostiquer, investiguer et traiter en soins primaires les céphalées des patients.
Qualité des données
Une recherche documentaire exhaustive a été effectuée pour trouver des lignes directrices et des révisions systématiques publiées entre janvier 2000 et mai 2011. La grille d’évaluation de la qualité des recommandations pour la pratique clinique AGREE a servi à l’analyse critique des lignes directrices. Les 6 guides de pratique clinique de la plus grande qualité ont servi de base dans le processus d’adaptation.
Message principal
Un groupe d’élaboration multidisciplinaire de professionnels des soins primaires ont formulé 91 recommandations précises à l’aide d’un processus consensuel. Les recommandations portent sur le diagnostic, l’investigation et la prise en charge de la migraine, de la céphalée de tension, de la céphalée due à une surmédication et de la céphalée vasculaire de Horton.
Conclusion
Un guide de pratique clinique adapté au contexte des soins de santé au Canada a été produit en suivant un processus d’adaptation de lignes directrices dans le but d’aider les professionnels de toutes les disciplines des soins primaires à dispenser des soins éclairés par des données probantes aux patients souffrant de céphalées.
La céphalée compte parmi les raisons les plus fréquentes qui motivent les patients à consulter leur médecin de famille. Durant une vie, on estime que la prévalence de la céphalée est de 66 % : de 14 à 16 % pour la migraine, de 46 à 78 % pour la céphalée dite de tension et de 0,1 à 0,3 % pour la céphalée vasculaire de Horton1–3. Au Canada, au moins 2,6 millions de femmes adultes et près de 1 million d’hommes souffrent de migraine4. Environ 90 % de ceux qui souffrent de migraine signalent une douleur de modérée à grave, notamment 75 % qui rapportent un fonctionnement déficient et 33 % qui ont besoin de se reposer au lit durant une crise5. Les répercussions économiques de la céphalée sont aussi considérables. On estime que 20 % des absences au travail sont attribuables à la céphalée6.
D’énormes quantités de médicaments sans ordonnance sont prises pour des problèmes de maux de tête et le traitement est souvent sous-optimal1,7. Quoiqu’il y ait un grand nombre de personnes souffrant de migraine qui prennent un traitement de courte durée pour soulager leur céphalée, il y en a aussi beaucoup qui pourraient bénéficier d’une thérapie prophylactique mais qui n’en reçoivent pas. Chez plus de 1 personne sur 4 souffrant de migraine, une thérapie préventive serait indiquée5,8.
Il est essentiel de mieux informer et éduquer les patients et les professionnels de la santé pour améliorer la prise en charge de la céphalée en soins primaires, ce qui permettrait de poser promptement le diagnostic et de la traiter plus efficacement9. Pour ce faire, un consortium d’organisations et de cliniciens de l’Alberta ont élaboré un guide de pratique intitulé Guideline for Primary Care Management of Headache in Adults10.
Portée
Les lignes directrices de l’Alberta ont pour but d’aider les professionnels des soins primaires responsables de l’évaluation et de la prise en charge des céphalées chez les adultes. Ce guide de pratique clinique se concentre principalement sur les troubles de céphalées primaires (p. ex. migraine, céphalée de tension et céphalée vasculaire de Horton) et la céphalée due à une surmédication. Certains conseils sont aussi présentés concernant le diagnostic et l’investigation des troubles de céphalées secondaires et la prise en charge de la céphalée cervicogène et du trouble de l’articulation temporomandibulaire. Le guide sera utile à divers professionnels des soins primaires, notamment aux médecins de famille, aux physiothérapeutes, aux ergothérapeutes, aux infirmières, aux infirmières praticiennes, aux pharmaciens, aux psychologues et aux chiropraticiens.
Élaboration
Leadership. Le groupe Toward Optimized Practice (TOP), qui élabore et diffuse des guides de pratique clinique en soins primaires en Alberta, et l’Institute of Health Economics (IHE) étaient les principales organisations impliquées dans l’élaboration des lignes directrices. Ils ont formé 3 comités multidisciplinaires pour coordonner la production du guide.
Le Comité directeur assurait la supervision opérationnelle.
L’équipe d’élaboration du guide de pratique clinique (l’Équipe) a formulé les recommandations et se composait de 9 médecins de famille, 2 neurologues, un ostéopathe, un chiropraticien, 2 physiothérapeutes, un ergothérapeute, une infirmière, un pharmacien, 2 psychologues et un spécialiste de l’évaluation de la technologie de la santé.
Le Comité consultatif conseillait le Comité directeur concernant les questions stratégiques et était formé de représentants du Collège des médecins de famille de l’Alberta, du Collège des médecins et chirurgiens de l’Alberta, des Services de santé de l’Alberta, du ministère de la Santé de l’Alberta, de la Pain Society of Alberta et d’un groupe de défense des intérêts de patients souffrant de douleurs chroniques, ainsi que d’experts en élaboration et en diffusion de guides de pratique clinique.
Une équipe de chercheurs en technologie de la santé ayant une expertise méthodologique venant de l’IHE a aidé le Comité directeur et l’Équipe11.
Recherche documentaire
L’élaboration du guide de pratique clinique de l’Alberta reposait sur un processus d’adaptation de lignes directrices misant sur l’existence de guides de grande qualité et permettant aux élaborateurs de modifier les recommandations tirées des directives de base pour répondre aux besoins locaux du milieu de la santé12. L’adaptation est une solution de rechange populaire à une élaboration à partir de zéro, étant donné la nécessité de réduire la duplication et de contenir les coûts dans la création de lignes directrices éclairées par des données probantes13–15.
Le groupe de recherche a collaboré avec des bibliothécaires médicaux expérimentés pour effectuer une recension systématique des guides de pratique clinique (GPC) existants, publiés entre janvier 2000 et mai 2011. La recherche a permis de cerner 64 GPC, dont 18 ont été jugés pertinents après les avoir soumis à des critères de sélection spécifiques élaborés par le groupe de recherche et des experts en contenu de l’Équipe11. La qualité des lignes directrices a été évaluée séparément par 2 examinateurs (C.M. et N.A.S.) à l’aide de l’instrument AGREE (grille d’évaluation de la qualité des recommandations pour la pratique clinique)16,17, qui a été modifié pour réduire la subjectivité de la notation des éléments et permettre de faire la distinction entre des lignes directrices de bonne ou de mauvaise qualité18. Quoiqu’on ait publié en mai 2009 une version mise à jour de l’outil AGREE19,20, le groupe de recherche a décidé d’utiliser l’instrument original pour préserver l’uniformité avec les lignes directrices produites antérieurement par TOP et l’IHE. Parmi les 18 guides potentiellement admissibles, 6 ont été jugés de bonne qualité et choisis comme lignes directrices de départ.
Deux examinateurs (C.M. et N.A.S.) ont extrait les renseignements suivants sous forme de tableaux de données probantes : la source du guide, les recommandations, le nombre et le genre d’études utilisées pour créer les recommandations (p. ex. 5 études randomisées contrôlées) et la solidité des recommandations. Au total, 187 recommandations ont été présentées sous forme de tableau et celles qui étaient contradictoires ont été mises en surbrillance.
Recommandations pour la pratique
L’Équipe a passé en revue les 6 guides de départ, leurs documents connexes et les tableaux de données probantes au cours de 13 réunions d’une demi-journée : 1 rencontre en personne et 12 conférences par web au moyen de WebEx (Cisco Systems Inc.), qui permettait à tous les membres de l’Équipe de voir simultanément les documents et d’inscrire leurs préférences à l’aide d’un mode de scrutin en ligne. Les 2 coprésidents (W.J.B. et P.T.) ont dirigé toutes les séances et animé des tables rondes pour chaque recommandation afin d’assurer que chaque membre de l’Équipe avait une voix au chapitre.
Dans certains cas, l’Équipe a demandé des données factuelles additionnelles pour clarifier des incertitudes ou régler des désaccords concernant l’interprétation des données probantes tirées des guides de base ou lorsque de nouvelles interventions envisagées ne figuraient pas dans les lignes directrices de départ. Ces demandes de « mises de côté » ont déclenché l’examen d’études de recherche individuelles citées dans les guides de base, ainsi que des révisions systématiques additionnelles sur les troubles liés à la céphalée cernées à la suite d’une recension supplémentaire des ouvrages publiés entre janvier 2000 et octobre 201011. Les éléments mis de côté ont été référés à des sous-comités spéciaux de l’Équipe qui incluaient 1 coprésident ou les 2, un chercheur de l’IHE et au moins 1 bénévole de l’Équipe ayant de l’expertise dans le domaine en cause. Les décisions prises par consensus par les sous-comités ont ensuite été présentées à l’Équipe pour approbation finale. Il est arrivé à l’occasion que de nouvelles recommandations aient été produites à la suite des discussions sur les sujets mis de côté. Un sous-comité spécial, dont faisait partie un neuroradiologiste, a été formé pour produire les recommandations concernant l’imagerie diagnostique. Le processus d’élaboration du guide de pratique clinique a duré 23 mois et a généré 91 ébauches de recommandations.
Chaque recommandation dans le guide de pratique de l’Alberta vient de 1 ou plusieurs lignes directrices de base, est fondée sur des données probantes tirées de révisions systématiques ou semisystématiques, ou a été produite par les membres de l’Équipe qui se sont basés sur leur opinion professionnelle collective et une analyse des données scientifiques pertinentes. Le texte original des recommandations a été préservé autant que possible et des désignations ont été utilisées (p. ex. RS pour révision systématique, SC pour série de cas) pour établir un lien avec les données probantes citées dans les guides de base. Les principes énoncés dans l’outil GuideLine Implementability Appraisal, qui est conçu pour évaluer le caractère pratique des GPC, ont servi à orienter la formulation des recommandations21,22. Les définitions standardisées des types de recommandations présentées dans le GPC de l’Alberta ont été produites à partir des échelles d’évaluation des données probantes utilisées dans les guides de base. Les recommandations se classaient comme suit : à faire lorsque les données probantes étaient favorables à l’intervention, ne pas faire si elles laissaient entendre que l’intervention était inefficace ou nuisible et ne sait pas lorsqu’elles étaient équivoques, conflictuelles ou insuffisantes.
Une série de documents d’accompagnement ont été produits, adaptés ou adoptés à l’appui de la mise en œuvre des lignes directrices. Il s’agit notamment d’un algorithme de référence rapide, d’un document de synthèse, de fiches d’information destinées aux patients et d’outils pour la pratique (un tableau des médicaments, une fiche pour le bilan des céphalées, un journal de bord à l’intention du patient et une vidéo démontrant l’examen physique du cou)10.
Le Comité consultatif, un groupe témoin de médecins de soins primaires et les participants à 2 conférences de médecins de l’Alberta ont passé en revue l’ébauche du guide. Les fiches d’information destinées aux patients ont été examinées par un groupe témoin de patients et de gens du public. Les documents finaux tenaient compte des commentaires reçus et ont été approuvés en février 2012 par l’Équipe.
Message principal
La liste des lignes directrices de départ se trouve au Tableau 123–31. Les 91 recommandations du guide de l’Alberta sont divisées en 6 sections. Le guide de pratique clinique complet et les documents d’accompagnement sont accessibles sur le site web du groupe TOP10. Les renseignements contenus dans l’algorithme* de référence rapide sont présentés à la Figure 1 et aux Tableaux 2 à 410. À l’Encadré 1 se trouve un résumé de certaines pratiques générales.
Tableau 1.
Guides de départ utilisés pour produire Guideline for Primary Care Management of Headache in Adults
| GROUPES AUTEURS | DÉTAILS |
|---|---|
| US Headache Consortium23–26, 2000 | États-Unis : Neuroimagerie chez les patients ayant des céphalées non aiguës 23; prise en charge pharmacologique des crises de migraine aiguës24; prévention pharmacologique de la migraine25; traitement physique et comportemental de la migraine26 |
| Fédération européenne des sociétés de neurologie27, 2009 | Europe : Traitement pharmacologique de la migraine |
| Société Française d’Étude des Migraines et des Céphalées28, 2004 | France : Diagnostic et prise en charge de la migraine chez les adultes et les enfants |
| Scottish Intercollegiate Guidelines Network29, 2008 | Royaume-Uni : Diagnostic et prise en charge de la céphalée chez les adultes |
| Fédération européenne des sociétés de neurologie30, 2006 | Europe : Traitement de la céphalée vasculaire de Horton et d’autres céphalalgies autonome du trijumeau |
| Fédération européenne des sociétés de neurologie31, 2010 | Europe : Traitement de la céphalée de tension |
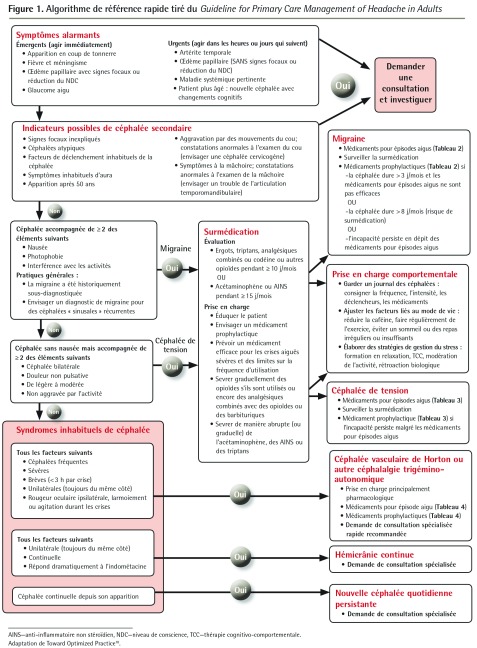
Figure 1.
Algorithme de référence rapide tiré du Guideline for Primary Care Management of Headache in Adults
AINS—anti-inflammatoire non stéroïdien, NDC—niveau de conscience, TCC—thérapie cognitivo-comportementale.
Adaptation de Toward Optimized Practice10.
Tableau 2.
Médicaments contre la migraine : A) Médicaments contre la migraine aiguë. B) Médicaments prophylactiques contre la migraine.
|
A) TYPE |
MÉDICAMENTS CONTRE LA MIGRAINE AIGUË |
|---|---|
| De première intention | 400 mg d’ibuprofène, 1000 mg d’AAS, 500 à 550 mg de naproxène sodique, 1000 mg d’acétaminophène |
| De deuxième intention | Triptans : 100 mg de sumatriptan par voie orale,
10 mg de rizatriptan, 12,5 mg d’almotriptan, 2,5 mg de zolmitriptan,
40 mg d’élétriptan, 2,5 mg de frovatriptan, 2,5 mg
de naratriptan
Antiémétiques : 10 mg de dompéridone ou 10 mg de métoclopramide pour la nausée |
| De troisième intention | 500 à 550 mg de naproxène sodique en combinaison avec un triptan |
| De quatrième intention | Combinaison d’analgésiques à dose fixe (avec codéine si nécessaire; non recommandée pour une utilisation régulière) |
| B) | ||||
|---|---|---|---|---|
|
| ||||
| MÉDICAMENTS PROHYLACTIQUES | POSOLOGIE INITIALE | TITRAGE*, AUGMENTATION DE LA DOSE QUOTIDIENNE | DOSE CIBLE OU MARGE THÉRAPEUTIQUE † | NOTES |
| De première intention | ||||
| • propranolol | 20 mg 2 fois par jour | 40 mg par semaine | 40 à 120 mg 2 fois par jour | À éviter en cas d’asthme |
| • métoprolol | 50 mg 2 fois par jour | 50 mg par semaine | 50 à 100 mg 2 fois par jour | À éviter en cas d’asthme |
| • nadolol | 40 mg par jour | 20 mg par semaine | 80 à 160 mg par jour | À éviter en cas d’asthme |
| • amitriptyline | 10 mg au coucher | 10 mg par semaine | 10 à 100 mg au coucher | À envisager si le patient souffre de dépression, d’anxiété, d’insomnie ou de céphalée de tension |
| • nortriptyline | 10 mg au coucher | 10 mg par semaine | 10 à 100 mg au coucher | À envisager si le patient souffre de dépression, d’anxiété, d’insomnie, ou de céphalée de tension |
| De deuxième intention | ||||
| • topiramate | 25 mg par jour | 25 mg par semaine | 50 mg 2 fois par jour | À envisager comme première option si le patient souffre d’embonpoint |
| • candésartan | 8 mg par jour | 8 mg par semaine | 16 mg par jour | Peu d’effets secondaires; expérience limitée en prophylaxie |
| • gabapentine | 300 mg par jour | 300 mg tous les 3 à 7 jours | 1200 à 1800 mg par jour divisés en 3 doses | Peu d’interactions médicamenteuses |
| Autres | ||||
| • divalproex | 250 mg par jour | 250 mg par semaine | 750 à 1500 mg par jour divisés en 2 doses | À éviter en cas de grossesse ou lorsqu’une grossesse est possible |
| • pizotifène | 0,5 mg par jour | 0,5 mg par semaine | 1 à 2 mg 2 fois par jour | Surveiller la somnolence et le gain de poids |
| • toxine botulique de type A | 155 à 195 unités | Pas de titrage nécessaire | 155 à 195 unités tous les 3 mois | Pour la migraine chronique seulement (céphalée de ≥ 15 jours/mois) |
| • flunarizine | 5–10 mg au coucher | Pas de titrage nécessaire | 10 mg au coucher | À éviter chez les patients qui souffrent de dépression |
| • venlafaxine | 37,5 mg par jour | 37,5 mg par semaine | 150 mg par jour | À envisager pour soulager la migraine chez les patients souffrant de dépression |
| En vente libre | ||||
| • citrate de magnésium | 300 mg 2 fois par jour | Pas de titrage nécessaire | 300 mg 2 fois par jour | L’efficacité peut être limitée; peu d’effets secondaires |
| • riboflavine | 400 mg par jour | Pas de titrage nécessaire | 400 mg par jour | L’efficacité peut être limitée; peu d’effets secondaires |
| • pétasite | 75 mg 2 fois par jour | Pas de titrage nécessaire | 75 mg 2 fois par jour | L’efficacité peut être limitée; peu d’effets secondaires |
| • coenzyme Q10 | 100 mg 3 fois par jour | Pas de titrage nécessaire | 100 mg 3 fois par jour | L’efficacité peut être limitée; peu d’effets secondaires |
AAS— acide acétylsalicylique.
La posologie peut être augmentée toutes les 2 semaines pour éviter les effets secondaires. Pour la plupart des médicaments, augmenter lentement la posologie jusqu’à la dose cible; un essai thérapeutique nécessite une durée de plusieurs mois. Le résultat prévu est une réduction et non une élimination des crises.
Si la dose cible n’est pas tolérée, essayer une dose plus faible. Si le traitement est efficace et toléré, le poursuivre pendant au moins 6 mois. Si plusieurs médicaments préventifs n’ont pas fonctionné, envisager une demande de consultation spécialisée.
Adapté de Toward Optimized Practice10.
Tableau 4.
Médicaments pour la céphalée vasculaire de Horton : Envisager une demande rapide de consultation spécialisée.
| MÉDICAMENTS | POSOLOGIE |
|---|---|
| Douleur aiguë | |
| Sumatriptan sous-cutané | 6 mg |
| Zolmitriptan intranasal | 5 mg |
| Oxygène à 100 % | 12 l/min durant 15 min avec masque sans réinspiration |
| Prophylactique * | |
| De première intention | |
| • vérapamil | 240 à 480 mg par jour (de plus fortes doses peuvent être nécessaires) |
| De deuxième intention | |
| • lithium | 900 à 1200 mg par jour |
| Autres | |
| • topiramate | 100 à 200 mg par jour |
| • mélatonine | Jusqu’à 10 mg par jour |
Si le patient a plus de 2 crises par jour, envisager la thérapie de transition jusqu’à ce que le vérapamil atteigne la concentration voulue (p. ex. 60 mg de prednisone durant 5 jours, ensuite réduire à 10 mg tous les 2 jours jusqu’à interruption).
Adapté de Toward Optimized Practice10.
Encadré 1. Pratiques générales pour la prise en charge des céphalées primaires chez les adultes.
Voici des pratiques générales
pour la prise en charge de la céphalée primaire chez les
adultes :
|
AINS—anti-inflammatoire non stéroïdien.
Section 1 : diagnostic et investigation de la céphalée
L’Encadré 2 présente les éléments importants de l’anamnèse des patients qui se présentent avec une première céphalée ou un changement dans les céphalées habituelles. L’Encadré 3 explique une approche à l’examen physique spécifiquement conçue pour les professionnels de soins primaire29. À l’Encadré 4, on présente les symptômes alarmants et d’autres indices possibles de céphalées secondaires29. Le Tableau 5 suggère une stratégie simplifiée pour diagnostiquer les troubles de céphalées primaires32,33.
Encadré 2. Éléments à considérer dans les antécédents de patients se présentant avec une céphalée pour la première fois ou qui ont observé des changements dans leur type de céphalée.
Explorer les éléments
importants suivants dans les antécédents de
céphalée :
|
Basé sur l’opinion des experts de l’équipe d’élaboration du guide de pratique clinique.
Encadré 3. Approche concernant l’examen physique de patients se présentant avec une céphalée pour la première fois ou qui ont observé des changements dans leur type de céphalée.
L’examen physique devrait
comprendre les éléments suivants :
|
Basé sur les lignes directrices du Scottish Intercollegiate Guidelines Network29 et l’opinion des experts de l’équipe d’élaboration du guide de pratique clinique.
Encadré 4. Symptômes alarmants et autres indices possibles de céphalées secondaires : Il faudrait envisager une demande de consultation ou une investigation appropriée.
|
Basé sur les lignes directrices du Scottish Intercollegiate Guidelines Network29 et l’opinion des experts de l’équipe d’élaboration du guide de pratique clinique.
Section 2 : migraine
À l’Encadré 5 se trouve un résumé d’une approche exhaustive à la prise en charge de la migraine. La Section 2 du guide comporte des recommandations concernant la prise en charge du mode de vie, le traitement pour épisodes aigus, la prophylaxie, la migraine menstruelle et le traitement de la migraine durant la grossesse. Le guide complet présente un tableau détaillé des médicaments pour la migraine qui inclut les formulations disponibles, les posologies habituelles, les contre-indications relatives et absolues et les événements indésirables. Aux Encadrés 6 et 7, on explique les indications de prescrire des médicaments prophylactiques pour la migraine et les éléments à prendre en compte28,29. Les médicaments recommandés sont présentés au Tableau 210.
Encadré 5. Prise en charge complète de la migraine.
Tenir compte de ce qui suit dans la prise
en charge de patients souffrant de migraine :
|
Basé sur l’opinion des experts de l’équipe d’élaboration du guide de pratique clinique.
Encadré 6. Prophylaxie pharmacologique pour la migraine.
Les médicaments prophylactiques
sont indiqués dans les circonstances suivantes :
|
AINS—anti-inflammatoire non stéroïdien.
Basé sur l’opinion des experts de l’équipe d’élaboration du guide de pratique clinique.
Encadré 7. Pharmacothérapie prophylactique pour la migraine.
Prendre en compte ce qui suit dans la
prescription de médicaments prophylactiques pour la migraine :
|
Section 3 : céphalée due à la tension
Cette section comporte des recommandations sur le mode de vie, la thérapie pour épisodes aigus et prophylactique, de même que la prise en charge des céphalées due à la tension durant la grossesse. La liste des médicaments recommandés se trouve au Tableau 310.
Tableau 3.
Médicaments pour céphalée de tension
| MÉDICAMENTS | POSOLOGIE |
|---|---|
| Douleur aiguë | |
| Ibuprofène | 400 mg |
| AAS | 1000 mg |
| Naproxène sodique | 500 à 550 mg |
| Acétaminophène | 1000 mg |
| Prophylactique | |
| De première intention | |
| • amitriptyline | 10 à 100 mg par jour |
| • nortriptyline | 10 à 100 mg par jour |
| De deuxième intention | |
| • mirtazapine | 30 mg par jour |
| • venlafaxine | 150 mg par jour |
AAS— acide acétylsalicylique.
Adapté de Toward Optimized Practice10.
Section 4 : céphalée due à la surmédication
Ceux qui souffrent de migraine sont particulièrement enclins à développer une céphalée due à la surmédication. Les recommandations relatives au diagnostic et à la prise en charge de la céphalée due à la surmédication sont présentées aux Encadrés 8 et 929.
Encadré 8. Diagnostic de la céphalée due à la surmédication.
Envisager les éléments
suivants dans le diagnostic de la céphalée due
à la surmédication :
|
AINS—anti-inflammatoire non stéroïdien.
Basé sur les lignes directrices du Scottish Intercollegiate Guidelines Network29 et l’opinion des experts de l’équipe d’élaboration du guide de pratique clinique.
Encadré 9. Prise en charge de la céphalée due à la surmédication.
Les plans thérapeutiques pour les
patients dont la céphalée est due à la
surmédication devraient comporter ce qui suit :
|
AINS—anti-inflammatoire non stéroïdien.
Basé sur les lignes directrices du Scottish Intercollegiate Guidelines Network29 et l’opinion des experts de l’équipe d’élaboration du guide de pratique clinique.
Section 5 : céphalée vasculaire de Horton
La céphalée vasculaire de Horton est prise en charge au moyen d’un certain nombre de pharmacothérapies qui peuvent être amorcées et surveillées en soins primaires, mais il est recommandé de demander sans délai une consultation chez un spécialiste parce que ce type de céphalée est peu commun, incapacitant et difficile à prendre en charge. Les médicaments recommandés se trouvent au Tableau 410.
Section 6 : autres troubles de céphalées
Cette section du guide insiste sur l’hémicrânie continue, la céphalée cervicogène et la céphalée secondaire à un trouble de l’articulation temporomandibulaire. Le traitement de ces problèmes exigera probablement une demande de consultation auprès d’un thérapeute ou spécialiste formé de manière appropriée.
Plans de mise en œuvre et de mise à jour
Le guide de pratique clinique a été diffusé au moyen de présentations et d’ateliers lors de conférences provinciales, régionales et nationales. Il figure aussi dans l’Infobase de l’AMC35 et il a compté parmi les 10 guides de pratique clinique les plus téléchargés pendant près de 6 mois. Il se trouve aussi dans le site web du Michael G. DeGroote National Pain Centre35 et est fiché dans la National Guideline Clearing House des États-Unis36. L’Université de Calgary en Alberta entreprend actuellement un projet pilote de présentation du guide par l’intermédiaire de webinaires interactifs.
La base des données probantes sur laquelle repose le GPC de l’Alberta fera annuellement l’objet d’une évaluation et des mises à jour seront apportées lorsque des changements aux recommandations s’imposeront en raison de nouvelles données probantes.
Limitations
L’exercice d’adaptation des guides empêchait de faire une analyse en profondeur de la validité ou une évaluation formelle de la force et de la qualité des données empiriques sous-jacentes, ce qui a compliqué la classification de la force et du type des recommandations. Pour régler ce problème, des définitions standardisées ont été produites pour les types de recommandations faites dans le GPC de l’Alberta (p. ex. ce que voulait dire une recommandation faire ou ne pas faire), à partir des échelles d’évaluation des données probantes utilisées dans les guides de départ qui se chevauchaient. Des désignations étaient utilisées (p. ex. RS pour révision systématique) afin d’établir des liens avec les types de données probantes citées en référence par les guides de base à l’appui de leurs recommandations10,11.
Le manque de données scientifiques probantes concernant les investigations des céphalées, leur diagnostic, les symptômes alarmants et les demandes de consultation a fait en sorte que de nombreuses recommandations dans ces domaines reposaient sur les opinions de l’Équipe ou des experts qui ont élaboré les guides de base. Toutefois, ces problèmes ont été compensés par l’utilisation de guides de base crédibles, d’une liste rigoureuse des types et des sources des données probantes pour toutes les recommandations et d’une documentation précise du processus de contextualisation subjective.
Les processus d’adaptation sont limités par la période de temps écoulée entre la publication des études primaires et leur incorporation dans les lignes directrices, ce qui signifie que les données probantes récemment publiées ne sont pas nécessairement intégrées dans le GPC de l’Alberta et que toutes les options thérapeutiques disponibles ne sont pas couvertes dans les guides de base. Pour y pallier, l’équipe de recherche a mis régulièrement à jour les recensions durant tout l’exercice d’adaptation des lignes directrices de l’Alberta.
Les membres de l’Équipe ont débattu à savoir s’il fallait incorporer de nouveaux traitements pour les céphalées qui n’étaient pas mentionnés dans les guides de base. Ils ont adopté une approche conservatrice selon laquelle une recommandation en faveur d’une intervention émergente n’était incluse que si elle avait fait l’objet d’une évaluation dans une révision systématique.
Aucun des guides de départ n’incluait d’évaluations économiques formelles ou d’analyses de rentabilité ni ne traitait des répercussions économiques des recommandations. En raison de contraintes de temps et de ressources, il n’y a pas eu d’analyse de rentabilité ou d’évaluation économique des répercussions du GPC de l’Alberta. Par ailleurs, si les guides de base mentionnaient des renseignements sur le plan économique, ces derniers ont été relevés dans les documents d’accompagnement11.
Conclusion
La forme et la concision du Guideline for Primary Care Management of Headache in Adults reflètent sa raison d’être : offrir aux professionnels des soins primaires canadiens de multiples disciplines un ensemble complet de ressources pour évaluer et prendre en charge les céphalées chez les adultes. Un résumé du guide de pratique clinique, un algorithme, de même que des outils pour la pratique et des fiches d’information destinées aux patients sont fournis pour renforcer la prise en charge complète des céphalées, soutenir l’engagement du patient et l’autogestion des soins, ainsi que favoriser des interventions éclairées par des données probantes.
Tableau 5.
Diagnostic des syndromes de céphalées primaires
| DESCRIPTION | SYNDROME DE CÉPHALÉE |
|---|---|
| Patients souffrant de crises de céphalées récurrentes et ayant des constatations normales à l’examen neurologique (chez certains patients, d’autres symptômes cliniques devraient aussi être pris en compte)* |
|
| Patients souffrant de céphalées ≥ 15 j/mois pendant > 3 mois dont les constatations à l’examen neurologique sont normales‡ |
|
| Patients souffrant de céphalée quotidienne continue pendant > 3 mois dont les constatations à l’examen neurologique sont normales§ |
|
AINS—anti-inflammatoire non stéroïdien.
Modification de l’International Classification of Headache Disorders32; données de Lipton et coll.33; et basé sur l’opinion des experts de l’équipe d’élaboration du guide de pratique clinique.
Si les patients ne répondent pas aux critères diagnostiques de la migraine.
Modification de l’International Classification of Headache Disorders32 et basé sur l’opinion des experts de l’équipe d’élaboration du guide de pratique clinique.
Modification de l’International Classification of Headache Disorders32 et basé sur l’opinion des experts de l’équipe d’élaboration du guide de pratique clinique.
Ce syndrome de céphalée moins courant devrait être envisagé chez des patients souffrant de céphalée continuelle.
Remerciements
Nous remercions les membres de l’Ambassador Program Guideline Development Group, du Comité consultatif et du Comité directeur de leur engagement et de leur travail diligent. Nous voulons aussi remercier toutes les organisations qui ont offert du soutien durant le processus d’élaboration du guide de pratique clinique, en particulier Toward Optimized Practice pour les conseils prodigués durant les étapes finales du processus et pour avoir affiché en ligne le guide complété. Nous exprimons une gratitude toute particulière au Dr James N. Scott (radiologie) et au Dr Robert Ashforth (radiologie) pour leurs précieuses contributions dans la composante portant sur l’imagerie diagnostique du guide. Nous remercions aussi Mme Wendy McIndoo de son aide sur le plan administratif, de même que Mme Liz Dennett et Mme Dagmara Chojecki de leur soutien sur le plan des services d’information. Le ministère de la Santé de l’Alberta a financé cette initiative. Les opinions exprimées dans le présent article ne représentent pas nécessairement la politique officielle du Ministère.
POINTS DE REPÈRE DU RÉDACTEUR
La céphalée est souvent ce qui motive les patients à consulter leur médecin de famille et son traitement est fréquemment sous-optimal. Le présent article explique l’élaboration par un groupe multidisciplinaire d’un guide de pratique clinique et ses principales recommandations pour aider les professionnels canadiens des soins primaires à dispenser des soins éclairés par des données probantes aux patients souffrant de céphalées.
La migraine, qui est historiquement sousdiagnostiquée, représente de loin le type le plus courant de céphalée incitant les patients à consulter. La neuroimagerie, l’imagerie par rayons X des sinus ou de la colonne cervicale et les électroencéphalogrammes ne sont pas recommandés pour l’évaluation systématique des patients souffrant de maux de tête. Une anamnèse et les constatations d’un examen physique et neurologique suffisent habituellement pour poser un diagnostic. Une thérapie complète pour la migraine comporte une prise en charge des facteurs déclencheurs et liés au mode de vie, des médicaments pour épisodes aigus et prophylactiques et des stratégies de prise en charge autonome de la migraine. Le guide traite aussi du traitement des céphalées de tension, vasculaires de Horton et dues à une surmédication.
Footnotes
Cet article donne droit à des crédits Mainpro-M1. Pour obtenir des crédits, allez à www.cfp.ca et cliquez sur le lien vers Mainpro.
Cet article a fait l’objet d’une révision par des pairs.
The English version of this article is available at www.cfp.ca on the table of contents for the August 2015 issue on page 670.
L’algorithme de référence rapide original en anglais est accessible en format facile à imprimer à www.cfp.ca. Allez au texte intégral de l’article en ligne et cliquez sur CFPlus dans le menu du coin supérieur droit de la page.
Intérêts concurrents
Le Dr Becker a agi comme membre au sein de conseils médicaux consultatifs pour AGA Medical, Allergan, Merck et Pfizer; a reçu des honoraires de conférencier d’Allergan, Merck, Pfizer, Serono et Teva; et a reçu du soutien à la recherche dans le cadre d’études cliniques multicentriques (a agi à titre de chercheur principal local) de la part d’AGA Medical, Allergan, Medtronic et Merck. Toutefois, ces intérêts n’ont eu aucune influence sur la conception, l’analyse des données, la formulation ou le contenu du guide. Aucun des autres auteurs n’avait de conflits d’intérêts à déclarer.
Références
- 1.Bigal ME, Lipton RB, Stewart WF. The epidemiology and impact of migraine. Neurol Neurosci Rep. 2004;4(2):98–104. doi: 10.1007/s11910-004-0022-8. [DOI] [PubMed] [Google Scholar]
- 2.Robbins MS, Lipton RB. The epidemiology of primary headache disorders. Semin Neurol. 2010;30(2):107–19. doi: 10.1055/s-0030-1249220. Publ. en ligne du 29 mars 2010. [DOI] [PubMed] [Google Scholar]
- 3.Stovner L, Hagen K, Jensen R, Katsarava Z, Lipton R, Scher A, et al. The global burden of headache: a documentation of headache prevalence and disability worldwide. Cephalalgia. 2007;27(3):193–210. doi: 10.1111/j.1468-2982.2007.01288.x. [DOI] [PubMed] [Google Scholar]
- 4.Cooke LJ, Becker WJ. Migraine prevalence, treatment and impact: the Canadian Women and Migraine Study. Can J Neurol Sci. 2010;37(5):580–7. doi: 10.1017/s0317167100010738. [DOI] [PubMed] [Google Scholar]
- 5.Lipton RB, Bigal ME, Diamond M, Freitag F, Reed ML, Stewart WF, et al. Migraine prevalence, disease burden, and the need for preventive therapy. Neurology. 2007;68(5):343–9. doi: 10.1212/01.wnl.0000252808.97649.21. [DOI] [PubMed] [Google Scholar]
- 6.Latinovic R, Gulliford M, Ridsdale L. Headache and migraine in primary care: consultation, prescription, and referral rates in a large population. J Neurol Neurosurg Psychiatry. 2006;77(3):385–7. doi: 10.1136/jnnp.2005.073221. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 7.Bigal M, Krymchantowski AV, Lipton RB. Barriers to satisfactory migraine outcomes. What have we learned, where do we stand? Headache. 2009;49(7):1028–41. doi: 10.1111/j.1526-4610.2009.01410.x. Publ. en ligne du 6 avr. 2009. [DOI] [PubMed] [Google Scholar]
- 8.Hazard E, Munakata J, Bigal ME, Rupnow MF, Lipton RB. The burden of migraine in the United States: current and emerging perspectives on disease management and economic analysis. Value Health. 2009;12(1):55–64. doi: 10.1111/j.1524-4733.2008.00404.x. Publ. en ligne du 30 juill. 2008. [DOI] [PubMed] [Google Scholar]
- 9.Becker WJ, Gladstone JP, Aube M. Migraine prevalence, diagnosis, and disability. Can J Neurol Sci. 2007;34(Suppl 4):S3–9. [PubMed] [Google Scholar]
- 10.Toward Optimized Practice . Guideline for primary care management of headache in adults. Edmonton, AB: Toward Optimized Practice; 2012. Accessible à: www.topalbertadoctors.org/cpgs/10065. Réf. du 26 août 2013. [Google Scholar]
- 11.Institute of Health Economics . Ambassador program guideline for management of primary headache in adults: background document. Edmonton, AB: Institute of Health Economics; 2013. Accessible à: www.ihe.ca/research-programs/hta/aagap/headache. Réf. du 26 août 2013. [Google Scholar]
- 12.Harstall C, Taenzer P, Angus DK, Moga C, Schuller T, Scott NA. Creating a multidisciplinary low back pain guideline: anatomy of a guideline adaptation process. J Eval Clin Pract. 2011;17(4):693–704. doi: 10.1111/j.1365-2753.2010.01420.x. Publ. en ligne du 16 sept. 2010. [DOI] [PubMed] [Google Scholar]
- 13.Fervers B, Burgers JS, Haugh MC, Latreille J, Mlika-Cabanne N, Paquet L, et al. Adaptation of clinical guidelines: literature review and proposition for a framework and procedure. Int J Qual Health Care. 2006;18(3):167–76. doi: 10.1093/intqhc/mzi108. [DOI] [PubMed] [Google Scholar]
- 14.Groot P, Hommersom A, Lucas P. Adaptation of clinical practice guidelines. Stud Health Technol Inform. 2008;139:121–39. [PubMed] [Google Scholar]
- 15.Muth C, Gensichen J, Beyer M, Hutchinson A, Gerlach FM. The systematic guideline review: method, rationale, and test on chronic heart failure. BMC Health Serv Res. 2009;9:74. doi: 10.1186/1472-6963-9-74. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 16.The AGREE Collaboration . AGREE instrument. Londres, RU: The AGREE Collaboration; 2001. Accessible à: www.agreetrust.org/resource-centre/the-original-agree-instrument/the-original-agree-instrument-translations. Réf. du 26 août 2013. [Google Scholar]
- 17.The AGREE Collaboration Development and validation of an international appraisal instrument for assessing the quality of clinical practice guidelines: the AGREE project. Qual Saf Health Care. 2003;12(1):18–23. doi: 10.1136/qhc.12.1.18. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 18.Scott NA, Moga C, Harstall C. Making the AGREE tool more user friendly: the feasibility of a user guide based on Boolean operators. J Eval Clin Pract. 2009;15(6):1061–73. doi: 10.1111/j.1365-2753.2009.01265.x. [DOI] [PubMed] [Google Scholar]
- 19.Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, et al. AGREE II: advancing guideline development, reporting and evaluation in healthcare. CMAJ. 2010;182(18):E839–42. doi: 10.1503/cmaj.090449. Publ. en ligne du 5 juill. 2010. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 20.The AGREE Next Steps Consortium . Appraisal of Guidelines for Research & Evaluation II. Londres, RU: The AGREE Next Steps Consortium; 2009. Accessible à: www.agreetrust.org. Réf. du 26 août 2013. [Google Scholar]
- 21.Shiffman RN, Dixon J, Brandt C, Essaihi A, Hsiao A, Michel G, et al. The Guide-Line Implementability Appraisal (GLIA): development of an instrument to identify obstacles to guideline implementation. BMC Med Inform Decis Mak. 2005;(5):23. doi: 10.1186/1472-6947-5-23. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 22.Yale University . GuideLine Implementability Appraisal (GLIA) New Haven, CT: Yale University; 2005. Accessible à: http://nutmeg.med.yale.edu/glia/login.htm;jsessionid%20=DFE8740FF9FF152296DD79BFBAA723B6. Réf. du 26 août 2013. [Google Scholar]
- 23.Frishberg BM, Rosenberg JH, Matchar DB, McCrory DC, Pietrzak MP, Rozen TD, et al. Evidence-based guidelines in the primary care setting: neuroimaging in patients with nonacute headache. St Paul, MN: US Headache Consortium; 2000. [Google Scholar]
- 24.Matchar DB, Young WB, Rosenberg JH, Pietrzak MP, Silberstein SD, Lipton RB, et al. Evidence-based guidelines for migraine headache in the primary care setting: pharmacological management of acute attacks. St Paul, MN: US Headache Consortium; 2000. [Google Scholar]
- 25.Ramadan NM, Silberstein SD, Freitag F, Gilbert TT, Frishberg BM. Evidence-based guidelines for migraine headache in the primary care setting: pharmacological management for prevention of migraine. St Paul, MN: US Headache Consortium; 2000. [Google Scholar]
- 26.Campbell JK, Penzien DB, Wall EM. Evidence-based guidelines for migraine headache: behavioral and physical treatments. St Paul, MN: US Headache Consortium; 2000. [Google Scholar]
- 27.Evers S, Afra J, Frese A, Goadsby PJ, Linde M, May A, et al. EFNS guideline on the drug treatment of migraine—revised report of an EFNS task force. Eur J Neurol. 2009;16(9):968–81. doi: 10.1111/j.1468-1331.2009.02748.x. [DOI] [PubMed] [Google Scholar]
- 28.Géraud G, Lantéri-Minet M, Lucas C, Valade D, French Society for the Study of Migraine Headache (SFEMC) French guidelines for the diagnosis and management of migraine in adults and children. Clin Ther. 2004;26(8):1305–18. doi: 10.1016/s0149-2918(04)80161-9. [DOI] [PubMed] [Google Scholar]
- 29.Scottish Intercollegiate Guidelines Network . Diagnosis and management of headache in adults. A national clinical guideline. Publication no. 107. Edinburgh, Écosse: Scottish Intercollegiate Guidelines Network; 2008. Accessible à: www.sign.ac.uk/guidelines/fulltext/107/index.html. Réf. du 26 août 2013. [Google Scholar]
- 30.May A, Leone M, Afra J, Linde M, Sandor PS, Evers S, et al. EFNS guidelines on the treatment of cluster headache and other trigeminal-autonomic cephalalgias. Eur J Neurol. 2006;13(10):1066–77. doi: 10.1111/j.1468-1331.2006.01566.x. Accessible à: www.guideline.gov/content.aspx?id=34898. Réf. du 10 juin 2015. [DOI] [PubMed] [Google Scholar]
- 31.Bendtsen L, Evers S, Linde M, Mitsikostas DD, Sandrini G, Schoenen J. EFNS guideline on the treatment of tension-type headache—report of an EFNS task force. Eur J Neurol. 2010;17(11):1318–25. doi: 10.1111/j.1468-1331.2010.03070.x. [DOI] [PubMed] [Google Scholar]
- 32.Headache Classification Subcommittee of the International Headache Society The International Classification of Headache Disorders: 2 édition. Cephalalgia. 2004;24(Suppl 1):9–160. doi: 10.1111/j.1468-2982.2003.00824.x. [DOI] [PubMed] [Google Scholar]
- 33.Lipton RB, Dodick D, Sadovsky R, Kolodner K, Endicott J, Hettiarachchi J, et al. A self-administered screener for migraine in primary care: the ID Migraine validation study. Neurology. 2003;61(3):375–82. doi: 10.1212/01.wnl.0000078940.53438.83. [DOI] [PubMed] [Google Scholar]
- 34.Association médicale canadienne . CMA Infobase: clinical practice guidelines database. Record ID 13271. Ottawa, ON: Association médicale canadienne; 2013. Accessible à: https://www.cma.ca/en/Pages/cpg-details.aspx?cpgId=13271&la_id=1. Réf. du 26 août 2013. [Google Scholar]
- 35.Michael G. Guidelines. Hamilton, ON: McMaster University; 2013. DeGroote National Pain Centre [site web] Accessible à: http://nationalpaincentre.mcmaster.ca/guidelines.html. Réf. du 11 juin 2015. [Google Scholar]
- 36.Guideline summary. Rockville, MD: Agency for Healthcare Research and Quality; 2013. National Guideline Clearinghouse [site web] Accessible à: www.guideline.gov/content.aspx?id=47060&search=guideline+for+primary+care+management+of+headache+in+adults. Réf. du 11 juin 2015. [Google Scholar]