PROCESSUS DE PRÉPARATION DES DOCUMENTS DE PRINCIPES
Un groupe de travail conjoint a été formé afin de préparer un document de principes sur le diagnostic et la prise en charge de l’asthme chez les enfants d’âge préscolaire. Ce groupe se composait de pédiatres universitaires et communautaires, de pneumologues pédiatres, d’un allergologue pédiatre et d’un médecin de famille ayant des compétences combinées en soins aigus et chroniques de l’asthme en pédiatrie ainsi qu’en transfert des connaissances.
Le document a été préparé conformément aux exigences de la Société canadienne de thoracologie (SCT) à l’égard des documents de principes. Le groupe a procédé à une analyse des publications scientifiques et convenu de messages clés par consensus unanime après de longues discussions sur l’analyse des données probantes et sur les lignes directrices existantes. Une fois rédigé, le document a été révisé par quatre experts externes, par le comité des Lignes directrices canadiennes en santé respiratoire de la SCT ainsi que par le comité de la pédiatrie communautaire et le comité directeur de la section de la santé respiratoire de la Société canadienne de pédiatrie (SCP). Le comité directeur de la SCT et le conseil d’administration de la SCP ont ensuite approuvé le document définitif.
PRÉAMBULE
Il règne une certaine incertitude quant au moment et à la manière de poser un diagnostic chez un enfant d’âge préscolaire ayant des symptômes évocateurs de l’asthme. Le vaste éventail de dénominations couramment utilisées chez les enfants d’âge préscolaire, qui dénotent la possibilité d’une physiopathologie (p. ex., bronchospasme ou hyperréactivité bronchique), des symptômes (p. ex., respiration sifflante ou toux chronique), des diagnostics vagues (bronchite sifflante ou happy wheezer) ou des diagnostics qui risquent d’être erronés (p. ex., bronchiolite répétée ou bronchite ou pneumonie récurrente),(1) confirment la nécessité d’adopter une terminologie claire.
Chez les enfants d’âge scolaire et les adultes, les recommandations des lignes directrices indiquent de procéder à des tests de la fonction pulmonaire, et particulièrement la spirométrie, pour confirmer le diagnostic.(2,3) Les enfants de moins de six ans peinent à effectuer la technique d’expiration forcée qu’exige la spirométrie, et les autres tests de la fonction pulmonaire adaptés aux enfants d’âge préscolaire sont soit trop peu spécifiques, soit limités à quelques centres universitaires à vocation pédiatrique. Ainsi, le moment de poser un diagnostic d’« asthme » chez les enfants d’âge préscolaire suscite la controverse. Certains experts préfèrent réserver ce diagnostic aux enfants ayant des symptômes persistants ou atopiques et parler de « respiration sifflante d’origine virale » lorsque les symptômes évocateurs d’asthme sont limités aux épisodes d’infections des voies respiratoires supérieures (IVRS).(4) D’autres spécialistes recommandent toutefois que ces deux groupes d’enfants soient considérés comme atteints d’asthme.
Compte tenu de ces considérations, une méthode pragmatique est proposée pour confirmer le diagnostic d’asthme chez les enfants de un à cinq ans, et le lecteur est invité à consulter la Mise à jour des lignes directrices 2012 de la SCT pour la prise en charge des enfants de six ans et plus.(2) Le présent document de principes est destiné aux médecins de famille, aux pédiatres, aux pneumologues, aux allergologues, aux urgentologues et aux autres professionnels de la santé.
Par le passé, trois grandes méthodes étaient proposées pour poser un diagnostic présomptif d’asthme chez les enfants d’âge préscolaire : une liste de symptômes évocateurs, l’exclusion d’autres diagnostics et un ensemble de caractéristiques prédictives d’asthme à l’âge de six ans, c’est-à-dire lorsque l’enfant est assez âgé pour se prêter à une spirométrie. La non-priorisation des listes de critères, dont le nombre nécessaire pour justifier un diagnostic n’est pas établi, complique la mise en œuvre. L’exclusion d’autres diagnostics, qui favorise des tests inutiles et l’anxiété chez les parents, confirme aux médecins l’absence d’autres affections, sans pour autant confirmer le diagnostic. Plusieurs caractéristiques sont liées à la persistance de l’asthme chez les enfants d’âge scolaire, telles que le nombre d’épisodes de respiration sifflante et les antécédents personnels ou familiaux d’atopie (définis dans l’indice prédictif d’asthme, dont la version anglaise, Asthma Predictive Index, est plus connue)(5) ou l’âge d’apparition et la trajectoire des symptômes au fil du temps.(6) Ces critères sont lentement devenus synonymes de diagnostic d’asthme chez les tout-petits, même si ce n’était pas l’intention première. Par ailleurs, les outils prédictifs sont loin d’être parfaits(7,8) et la future trajectoire des symptômes ne peut servir à poser un diagnostic, quel que soit l’âge.
La plupart des enfants atteints d’asthme souffrent de leurs premiers symptômes pendant la période préscolaire. Les enfants d’âge préscolaire présentent le plus fort taux de consultations à l’urgence et d’hospitalisations attribuables à des symptômes d’asthme, tous groupes d’âge confondus.(9,10) Les épisodes de respiration sifflante en début de vie s’associent à une limitation de la fonction pulmonaire à l’âge de six ans, qui subsiste généralement jusqu’à l’âge adulte.(11) Cette limitation est environ 10 % moins élevée que la valeur prédite du volume expiratoire maximal en une seconde (VEMS) des enfants en bonne santé.(11) On a déjà constaté un remodelage des voies respiratoires (des dommages irréversibles aux voies respiratoires) chez des tout-petits, qui peut expliquer le changement de trajectoire de la fonction pulmonaire.(12) Même si jusqu’à 60 % des enfants deviennent asymptomatiques à l’âge de six ans, les épisodes de respiration sifflante observés pendant la période préscolaire persistent ou récidivent souvent à l’âge adulte.(6) Fait important, les données indiquent que les épisodes récurrents de respiration sifflante pendant la période préscolaire répondent à un traitement aux corticostéroïdes inhalés (CSI), tout comme chez les enfants plus âgés et les adultes.(13) Il est donc important de poser un diagnostic rapidement, afin d’éviter les délais de traitement, de réduire la morbidité et peut-être même de maximiser la croissance et la fonction pulmonaires. Les critères opérationnels proposés visent à standardiser le diagnostic d’asthme en l’absence de tests de la fonction pulmonaire. Comme dans toutes les méthodes diagnostiques cliniques, un risque d’erreur de classification subsiste. Ces critères risquent d’entraîner un léger surdiagnostic d’asthme, mais de l’avis des auteurs, ce résultat l’emporte sur les effets négatifs d’un sous-diagnostic.
MESSAGES CLÉS
Les expressions bronchospasme, hyperréactivité bronchique, bronchite asthmatiforme et happy wheezer devraient être abandonnées.
Des épisodes récurrents de respiration sifflante chez l’enfant d’âge préscolaire peuvent s’associer à une morbidité notable et nuire à sa santé à long terme.
PRINCIPAUX CRITÈRES POUR DIAGNOSTIQUER L’ASTHME CHEZ LES ENFANTS D’ÂGE PRÉSCOLAIRE
L’asthme est un trouble inflammatoire des voies respiratoires qui se caractérise par des symptômes épisodiques ou persistants comme la dyspnée, l’oppression thoracique, la respiration sifflante, la production de mucus et la toux. Il s’associe à une obstruction variable des voies respiratoires, qui sont hyperréactives aux stimuli endogènes ou exogènes.(2) On présume que ces caractéristiques, bien vérifiées chez les enfants d’âge scolaire et les adultes, s’appliquent également aux enfants d’âge préscolaire. Ainsi, pour poser un diagnostic d’asthme auprès des enfants d’âge préscolaire, chez qui il n’est pas facile, sinon impossible, d’obtenir des mesures de spirométrie, il faut constater avec objectivité les signes d’obstruction des voies respiratoires (ou obtenir un compte rendu convaincant des symptômes) et la réversibilité de cette obstruction, c’est-à-dire la diminution des signes et symptômes grâce à des médicaments pour l’asthme, et ce, en l’absence de facteurs cliniques évocateurs d’un autre diagnostic (tableau 1). L’atopie personnelle (p. ex., eczéma, allergie alimentaire) et les antécédents familiaux d’asthme accroissent les présomptions diagnostiques, mais ne sont pas utiles dans ce contexte. Ces critères diagnostiques s’appliquent aux enfants ayant des épisodes récurrents de symptômes (au moins deux) ou d’exacerbations asthmatiformes, même s’ils se manifestent seulement lors d’infections respiratoires virales.
TABLEAU 1.
Critères diagnostiques opérationnels pour l’asthme chez les enfants de un à cinq ans
| 1. Constatation d’une obstruction des voies respiratoires | |
|
| |
| Méthode privilégiée | Constatation de sibilances et d’autres signes d’obstruction des voies respiratoires par un médecin ou un professionnel de la santé compétent |
| Autre méthode | Compte rendu convaincant des parents indiquant la présence de respiration sifflante ou d’autres symptômes d’obstruction des voies respiratoires |
|
| |
| 2. Constatation de la réversibilité de l’obstruction des voies respiratoires | |
|
| |
| Méthode privilégiée | Constatation de la diminution des signes d’obstruction des voies respiratoires après la prise de BACA ± corticostéroïdes par voie orale* par un médecin ou un professionnel de la santé compétent |
| Autre méthode† | Compte rendu convaincant des parents faisant foi d’une réponse symptomatique à un essai thérapeutique d’une durée de trois mois à une dose moyenne de CSI (accompagnés de BACA au besoin)* |
| Autre méthode‡ | Compte rendu convaincant des parents faisant foi d’une réponse symptomatique et répétée à un BACA |
|
| |
| 3. Aucune présomption clinique d’un autre diagnostic | |
Voir le tableau 3 pour obtenir plus d’information sur le traitement ou l’essai thérapeutique recommandé;
Chez les enfants qui ont des symptômes fréquents ou au moins une exacerbation exigeant des corticostéroïdes de secours par voie orale ou une hospitalisation;
Chez les enfants ayant des symptômes et des exacerbations légers et intermittents, le diagnostic est seulement présumé, car les comptes rendus des parents quant à la réponse à court terme aux β2-agonistes à courte durée d’action (BACA) inhalés ne sont peut-être pas fiables en raison d’une mauvaise perception ou de l’amélioration spontanée d’une autre affection. Comme il s’agit là d’une méthode diagnostique plus faible, il est préférable de la confirmer par une observation directe lorsque le patient est symptomatique. CSI corticostéroïdes inhalés
L’obstruction des voies respiratoires
Les sibilances sont le signe le plus spécifique d’obstruction des voies respiratoires. Elles s’observent surtout pendant l’expiration, mais deviennent perceptibles pendant l’inspiration lorsque l’obstruction s’aggrave, jusqu’à disparaître lorsque le débit d’air devient très restreint. C’est un professionnel de la santé compétent qui peut le constater avec le plus de fiabilité à l’aide d’un stéthoscope (méthode diagnostique privilégiée), mais elle est parfois audible sans stéthoscope. Par ailleurs, lorsque les parents parlent de « respiration sifflante », il est important de vérifier ce qu’ils veulent dire, parce que c’est un terme souvent utilisé pour décrire des bruits causés par une respiration nasale ou difficile, qui n’ont rien à voir avec l’asthme(14) (autre méthode diagnostique).
D’autres signes d’obstruction des voies respiratoires moins spécifiques sont souvent liés aux sibilances, mais peuvent se déclarer en son absence. À l’auscultation, le murmure vésiculaire peut être normal malgré une légère obstruction des voies respiratoires. À mesure que cette obstruction s’accroît, le murmure vésiculaire commence par diminuer aux bases pulmonaires, puis dans l’ensemble des poumons, pour devenir inaudible en cas d’asthme très sévère. Ce phénomène peut s’accompagner d’une tachypnée, d’un temps expiratoire prolongé, de signes d’utilisation des muscles accessoires (p. ex., un tirage inter-costal), d’une hypoxémie et, dans les cas graves, d’une altération de la conscience (p. ex., agitation ou apathie). La toux est le signe le plus observé et le symptôme le plus déclaré, mais n’est pas représentative de l’asthme. Sauf en cas d’infection respiratoire virale, une toux chronique observée pendant le sommeil ou déclenchée par une exposition à des allergènes, par l’effort, par le rire ou par les pleurs, accroît la probabilité d’asthme.(15)
La réversibilité de l’obstruction des voies respiratoires
L’asthme se caractérise par la réversibilité de l’obstruction des voies respiratoires, démontrée par une réponse évidente au traitement pour l’asthme dans le délai anticipé. Pour mieux définir la réversibilité, un professionnel de la santé doit constater la réponse aux ß2-agonistes à courte durée d’action (BACA), accompagnés ou non de corticostéroïdes par voie orale lors d’une exacerbation aiguë (méthode diagnostique privilégiée). Chez les enfants qui ne présentent pas de signe objectif d’obstruction des voies respiratoires et qui n’ont que des symptômes, on peut déterminer la réversibilité de l’asthme si les parents font un compte rendu convaincant d’une réponse symptomatique à un essai thérapeutique d’une durée de trois mois composé d’une dose moyenne de corticostéroïdes inhalés et de BACA au besoin (autre méthode diagnostique), ou un compte rendu convaincant de réponses répétées aux BACA administrés seuls au besoin (autre méthode diagnostique, plus faible) (tableau 1).
L’absence d’autre diagnostic
Il faut procéder à une anamnèse et à un examen physique complets et envisager soigneusement la possibilité d’autres affections ayant des manifestations similaires afin d’écarter la possibilité d’un autre dia-gnostic (tableau 2). Il est inutile d’effectuer d’autres examens à moins qu’un autre diagnostic que celui de l’asthme soit envisageable. Une radiographie pulmonaire peut être indiquée dans des situations précises, afin d’écarter d’autres causes de sibilances ou des affections concomitantes.
TABLEAU 2.
Signes et symptômes* (signes d’avertissement) évocateurs d’un autre diagnostic que l’asthme
| Signes ou symptômes | Autres diagnostics possibles |
|---|---|
| Rhinorrhée persistante | Rhinosinusite infectieuse ou allergique† |
| Stridor; respiration bruyante plus marquée en présence de pleurs ou d’une infection respiratoire, lors de la consommation d’aliments ou en décubitus dorsal | Rétrécissement des voies respiratoires supérieures
|
| Apparition aiguë d’une toux, de sibilances ou de stridor lors de la consommation d’aliments ou des jeux; antécédents d’étouffement, pneumonie récurrente au même endroit | Inhalation d’un corps étranger Inhalation d’aliment ou du contenu gastrique |
| Premier épisode de respiration sifflante chez un enfant de moins d’un an | Bronchiolite† |
| Contact avec des personnes malades, signes focaux à la radiographie thoracique | Pneumonie†, atélectasie†, tuberculose, coqueluche |
| Grave toux paroxystique, qui peut s’associer initialement au « chant du coq » | Coqueluche |
| Naissance prématurée, administration prolongée d’oxygène ± ventilation mécanique | Dysplasie bronchopulmonaire |
| Symptômes depuis la première enfance, pneumonie récurrente, signes focaux à la radiographie thoracique | Malformation pulmonaire congénitale |
| Toux grasse chronique, hippocratisme digital, retard staturopondéral, pneumonie récurrente, apparition avant l’âge d’un an ± stéatorrhée | Bronchiectasie, fibrose kystique |
| Détresse respiratoire néonatale, toux quotidienne à apparition précoce présente toute l’année, congestion nasale ± situs inversus | Dyskinésie ciliaire primaire |
| Toux en décubitus dorsal, lors de la consommation d’aliments, vomissements après l’alimentation, malaises abdominaux | Reflux gastro-oesophagien pathologique† |
| Dysphagie, toux déclenchée par la consommation d’aliments ou de boissons | Œsophagite éosinophilique |
| Intolérance alimentaire, toux grasse ou respiration bruyante après la consommation d’aliments | Trouble de déglutition ± aspiration |
| Infections récurrentes, persistantes, graves ou inhabituelles | Dysfonction immunitaire |
| Souffle cardiaque, insuffisance cardiaque, cyanose lors de la consommation d’aliments, retard staturopondéral, tachypnée, hépatomégalie | Œdème pulmonaire causé par :
|
Liste incomplète des signes et symptômes évocateurs d’autres diagnostics et qui requièrent d’autres examens ou une autre prise en charge chez les enfants d’âge préscolaire. Les signes et symptômes énumérés peuvent recouper plusieurs maladies;
Indique les diagnostics les plus fréquents ou les affections concomitantes qui s’associent le plus à l’asthme.
Les IVRS récurrentes, accompagnées d’une rhinorrhée, sont la principale cause de toux récurrente, mais ne s’associent pas à des sibilances ni à des difficultés respiratoires. La laryngite se manifeste par une obstruction des voies respiratoires supérieures, une toux aboyante et un stridor à l’inspiration. La laryngite est plus courante chez les enfants atteints d’asthme (et vice-versa).(16) Il peut être difficile de distinguer l’asthme de la bronchiolite chez les nourrissons, qui présentent aussi des signes d’obstruction des voies respiratoires et d’infection respiratoire virale. Même si elle ne cesse pas de se déclarer à un âge précis, la bronchiolite se présente généralement lors du premier épisode de toux, de respiration sifflante et de difficulté respiratoire chez un nourrisson de moins de 12 mois.(17) Les soins de soutien en sont le meilleur traitement.(18) En général, l’asthme fait son apparition chez les tout-petits (de un à trois ans). Toutefois, des épisodes récurrents (au moins deux) de respiration sifflante avant l’âge d’un an devraient éveiller des soupçons d’asthme et inciter le médecin à envisager de diriger l’enfant vers un spécialiste en vue de le faire évaluer. Chez les enfants d’un an et plus, la réponse aux médicaments pour l’asthme est probablement le meilleur moyen de distinguer la bronchiolite de l’asthme.
MESSAGES CLÉS
3. On peut poser un diagnostic d’asthme chez des enfants de un à cinq ans.
4. Pour diagnostiquer l’asthme, il faut constater les signes ou symptômes d’obstruction des voies respiratoires, la réversibilité de l’obstruction (diminution des signes ou symptômes après un traitement pour l’asthme) et l’absence de présomption clinique d’un autre diagnostic.
5. La bronchiolite se manifeste habituellement comme le premier épisode de respiration sifflante chez l’enfant de moins d’un an.
6. Le diagnostic d’asthme devrait être envisagé chez les enfants de un à cinq ans ayant des épisodes récurrents de symptômes ou d’exacerbations asthmatiformes, même s’ils se manifestent seulement lors d’infections virales.
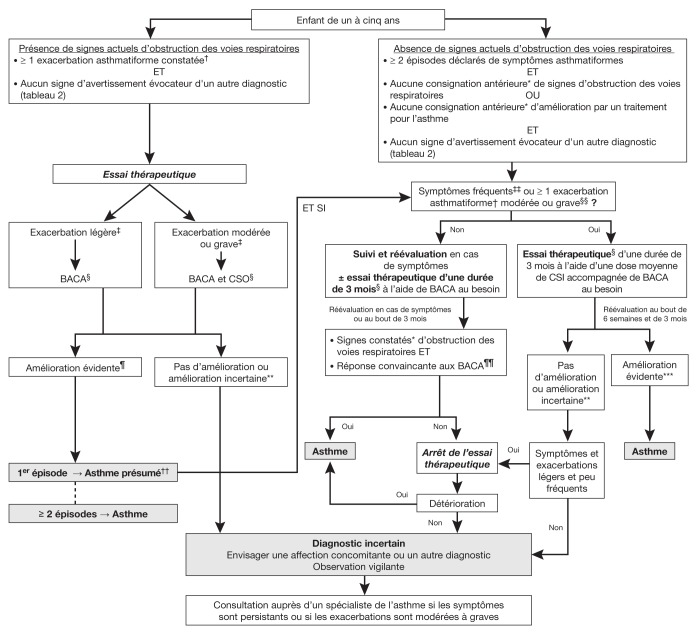
LE DIAGNOSTIC CHEZ UN ENFANT PRÉSENTANT DES SIGNES D’OBSTRUCTION DES VOIES RESPIRATOIRES (FIGURE 1)
Figure 1).
Algorithme diagnostique pour les enfants de un à cinq ans. *Corroboration par un médecin ou un professionnel de la santé compétent; †Épisodes de sibilances accompagnés ou non de difficultés respiratoires; ‡Gravité d’une exacerbation démontrée par une évaluation clinique des signes d’obstruction des voies respiratoires, conjuguée de préférence avec des mesures objectives comme la saturation en oxygène et la fréquence respiratoire, qui peut inclure un score validé tel que le score PRAM (Pediatric Respiratory Assessment Measure); §Les posologies figurent au tableau 3; ¶En fonction d’une diminution marquée des signes d’obstruction des voies respiratoires avant et après le traitement ou d’une réduction d’au moins trois points au score PRAM, compte tenu du délai de réponse prévue au traitement; **Un essai thérapeutique concluant est tributaire d’une bonne dose de médicament pour l’asthme, d’une bonne technique d’inhalation, de la consignation diligente des signes et symptômes et d’une réévaluation médicale au moment opportun. Si ces conditions ne sont pas respectées, il faut envisager de reprendre le traitement ou l’essai thérapeutique; ††Le diagnostic d’asthme repose sur des épisodes récurrents (au moins deux) d’exacerbations (signes démontrés) ou de symptômes asthmatiformes. S’il s’agit de la première occurrence d’exacerbation sans symptôme asthmatiforme préalable, le diagnostic d’asthme est présumé et sera confirmé par la récurrence des symptômes ou des exacerbations asthmatiformes et par la réponse au traitement pour l’asthme; ‡‡Symptômes asthmatiformes au moins huit jours par mois; §§Épisodes exigeant la prise de corticostéroïdes par voie orale (CSO) de secours ou une hospitalisation; ¶¶Dans ce groupe d’âge, il se peut que la valeur diagnostique des comptes rendus des parents quant à la réponse à court terme aux β2-agonistes à courte durée d’action (BACA) administrés au besoin ne soit pas fiable en raison d’une mauvaise perception ou de l’amélioration spontanée d’une autre affection. Il est préférable qu’un médecin ou un professionnel de la santé compétent constate l’obstruction des voies respiratoires et la réversibilité en présence de symptômes. ***Si le nombre d’exacerbations modérées à graves diminue de moitié, les exacerbations sont plus courtes et plus légères et les symptômes, moins fréquents et plus légers entre les épisodes. CSI corticostéroïdes inhalés
Lorsqu’un enfant a des sibilances ou d’autres signes d’obstruction des voies respiratoires, comme on s’y attend en soins aigus, la méthode diagnostique privilégiée consiste à ce qu’un médecin (ou un autre professionnel de la santé compétent) constate l’obstruction des voies respiratoires et l’atténuation de ces symptômes après un traitement pour l’asthme, en l’absence de présomption clinique d’un autre diagnostic. Le diagnostic d’asthme repose sur la présence récurrente de symptômes asthmatiformes antérieurs ou d’exacerbations (au moins deux) accompagnées de signes asthmatiformes constatés à la présentation. En cas de première exacerbation asthmatiforme, le diagnostic d’asthme est présumé et pourra être confirmé si ces signes ou symptômes se déclarent de nouveau et que l’enfant répond au traitement pour l’asthme.
L’atténuation des signes d’obstruction des voies respiratoires après la prise de BACA inhalés, de corticostéroïdes par voie orale ou de ces deux médicaments, constatée par un professionnel de la santé, est une preuve directe de la réversibilité de l’obstruction(19) (tableau 3). Puisque l’effet maximal des BACA survient au bout de 20 minutes, l’enfant dont les manifestations cliniques sont légères répondra rapidement à une seule dose suffisante de BACA. Celui qui présente une obstruction modérée à grave répondra à des doses répétées (deux à trois) de BACA administrées sur une période de 60 minutes.(20) Toutefois, il présentera une réponse sous-optimale aux BACA si la plus grande partie de l’obstruction n’est pas causée par un bronchospasme, mais par l’inflammation, particulièrement s’il est atteint d’un asthme de longue date et mal contrôlé. Les corticostéroïdes par voie orale devraient commencer à agir dans les quatre heures suivant leur administration,(21) même si leur effet maximal peut être constaté seulement quelques jours après le début du traitement.(22,23) Cet effet peut être difficile à distinguer d’une amélioration spontanée au fil du temps.
TABLEAU 3.
Essai thérapeutique pour confirmer la réversibilité de l’obstruction des voies respiratoires
| Présentation clinique de l’enfant | Agent | Dose | Nombre de doses/jour | Délai avant la réévaluation | |
|---|---|---|---|---|---|
| Signes d’obstruction des voies respiratoires (méthode privilégiée) | |||||
|
| |||||
| Signes cliniques légers* | Salbutamol inhalé | ≥ 4 bouffées† | 1re dose | 30 min | |
| Exacerbation modérée ou grave* | Salbutamol inhalé | ≥ 4 bouffées† | de 2 à 3 doses en 60 minutes | 60 min | |
| Corticostéroïdes par voie orale‡ | |||||
| Prednisone ou prednisolone (par voie orale) | de 1 mg/kg à 2 mg/kg (maximum de 50 mg)‡ | 1re dose | de 3 h à 4 h | ||
| Dexaméthasone | de 0,15 mg/kg à 0,60 mg/kg (maximum de 10 mg)‡ | 1re dose | de 3 h à 4 h | ||
|
| |||||
| Aucun signe d’obstruction des voies respiratoires (autre méthode) | |||||
|
| |||||
| Symptômes ou exacerbations légers et intermittents§ | Salbutamol inhalé | 2 bouffées toutes les 4 à 6 heures | Au besoin | 30 min | |
| Symptômes fréquents ou exacerbations modérées ou graves¶ | Salbutamol inhalé | 2 bouffées toutes les 4 à 6 heures | Au besoin | 30 min** | |
| Corticostéroïdes inhalés quotidiens | |||||
| Dipropionate de béclométhasone | 100 μg | Deux fois par jour | 3 mois†† | ||
| Ciclésonide | 200 μg | Tous les jours | 3 mois†† | ||
| Propionate de fluticasone | de 100 μg à 125 μg | Deux fois par jour | 3 mois†† | ||
Sauf indication contraire, tous les médicaments sont administrés par aérosol-doseur muni d’une chambre d’espacement à valve adaptée à l’âge, sous la supervision d’un professionnel de la santé (encadré du haut) ou des parents (encadré du bas); les doses sont indiquées à la sortie de la valve. Les médicaments indiqués dans les parties ombragées sont utilisés dans une indication non autorisée par Santé Canada pour ce groupe d’âge, à l’exception du diproprionate de béclométhasone qui est approuvé chez les enfants de cinq ans et plus. Puisque l’administration par aérosol-doseur est préférable, le budésonide n’est pas inclus dans ce tableau, car il n’est offert que pour nébulisation dans ce groupe d’âge au Canada.
La gravité des signes peut être établie d’après les lignes directrices nationales pour l’évaluation de la gravité(19) ou d’après le score PRAM (Pediatric Respiratory Assessment Measure; léger : PRAM 0 à 3; modéré : PRAM 4 à 7; grave : PRAM 8 à 12).(25,26)
La dose est fonction du protocole de traitement d’urgence selon l’âge ou le poids.(19)
La prednisone (ou la prednisolone) par voie orale peut être administrée à une dose de 1 mg/kg ou 2 mg/kg pendant une période de trois à cinq jours. La dexaméthasone par voie orale peut être administrée à une dose de 0,15 mg/kg à 0,3 mg/kg au moment de la première dose d’un traitement subséquent de prednisone pendant deux à quatre jours ou à une dose de 0,6 mg/kg dans le cadre d’un traitement de un à deux jours. (21–24)
Désigne des symptômes asthmatiformes légers qui se déclarent moins de huit jours par mois et des exacerbations bénignes qui n’exigent pas la prise de corticostéroïdes de secours par voie orale ou une hospitalisation et qui subsistent de quelques heures à quelques jours.
Désigne des symptômes asthmatiformes fréquents qui se déclarent au moins huit jours par mois; les exacerbations modérées ou graves désignent des épisodes comportant des signes asthmatiformes et exigeant la prise de corticostéroïdes de secours par voie orale ou une hospitalisation.
Tels qu’ils sont surveillés par les parents en vue d’en faire le compte rendu lors de la réévaluation médicale.
Accompagné d’une réévaluation médicale (ou d’une autre rencontre auprès d’un professionnel de la santé) au bout de six semaines, afin de vérifier l’observance de la médication pour l’asthme et la consignation dans un journal.
La constatation d’une réponse objective au traitement
Pour évaluer si l’état de l’enfant s’améliore après un traitement pour l’asthme, on peut observer des signes d’obstruction des voies respiratoires avant et après le traitement, tout en tenant compte du délai de réponse anticipé(20,21,23,24) (tableau 3). Afin de réduire le caractère subjectif de cette évaluation, on peut recourir à des mesures objectives (saturation en oxygène à l’air ambiant, fréquence respiratoire) ou à un score clinique standardisé, tel que le score PRAM (Pediatric Respiratory Assessment Measure). Selon cette méthode, une variation de trois points ou plus est considérée comme importante sur le plan clinique(25,26) (tableau 4). La récurrence des signes d’obstruction lorsque l’effet des BACA s’est estompé confirme le diagnostic.
TABLEAU 4.
Tableau de codification du score PRAM (Pediatric Respiratory Assessment Measure)
| Saturation en oxygène | ≥ 95 % | 0 | |
| 92 % à 94 % | 1 | ||
| < 92 % | 2 | ||
| Tirage sus-sternal | Absent | 0 | |
| Présent | 2 | ||
| Contraction des muscles scalènes | Absente | 0 | |
| Présente | 2 | ||
| Murmure vésiculaire* | Normal | 0 | |
| ↓ à la base | 1 | ||
| ↓ à l’apex et à la base | 2 | ||
| Minimal ou absent | 3 | ||
| Sibilances† | Absentes | 0 | |
| Expiratoires seulement | 1 | ||
| Inspiratoires (± expiratoires) | 2 | ||
| Audibles sans stéthoscope ou absentes (murmure vésiculaire minimal ou absent) | 3 | ||
| Score PRAM (maximum 12) | |||
| Score | 0 à 3 | 4 à 7 | 8 à 12 |
| Sévérité | Légère | Modérée | Sévère |
Adapté de Ducharme FM, Chalut D, Plotnick L et coll. The Pediatric Respiratory Assessment Measure: a valid clinical score for assessing acute asthma severity from toddlers to teenagers. J Pediatr 2008:152(4):476–80, 480.e1. Cet outil est disponible à l’adresse <www.chu-sainte-justine.org/childasthmatools>.
En cas d’asymétrie, la plage pulmonaire (apex-base) la plus touchée (droite ou gauche, antérieure ou postérieure) déterminera la cote pour ce critère.
En cas d’asymétrie, les deux foyers d’auscultation les plus touchés, où qu’ils soient (lobe supérieur droit, lobe moyen droit, lobe inférieur droit, lobe supérieur gauche, lobe inférieur droit), détermineront la cote pour ce critère. ↓ Réduit
LE DIAGNOSTIC CHEZ UN ENFANT QUI NE PRÉSENTE PAS DE SIGNE D’OBSTRUCTION DES VOIES RESPIRATOIRES (FIGURE 1)
De nombreux enfants qui consultent en milieu ambulatoire ne sont pas en crise. En général, leur examen physique est normal. Il arrive que des signes convaincants d’obstruction des voies respiratoires soient provoqués par une inspiration profonde ou par l’effort. Toutefois, l’examen physique demeure relativement peu sensible à l’obstruction des voies respiratoires, particulièrement si celle-ci est bien installée. Dans ce cas, il est acceptable de s’appuyer sur l’évaluation déjà consignée au dossier par un professionnel de la santé compétent, qui constate des sibilances ou d’autres signes d’obstruction des voies respiratoires et un soulagement des symptômes après la prise de BACA accompagnés ou non de corticostéroïdes par voie orale.
Chez les enfants qui ne présentent pas de signe d’obstruction des voies respiratoires, le diagnostic d’asthme est présumé en présence d’épisodes récurrents (au moins deux) de symptômes asthmatiformes, lorsqu’aucun signe antérieur d’obstruction des voies respiratoires et de réversibilité de cette obstruction n’a été constaté et en l’absence de présomption d’un autre diagnostic. On peut également présumer un diagnostic d’asthme en présence d’un seul épisode d’obstruction des voies respiratoires dont la réversibilité est constatée par un professionnel de la santé compétent et en l’absence d’épisodes antérieurs ou ultérieurs de signes ou symptômes asthmatiformes. Un essai thérapeutique peut alors confirmer le diagnostic.
Les enfants chez qui les symptômes sont légers et peu fréquents (moins de huit jours par mois) et chez qui les exacerbations sont légères (elles subsistent de quelques heures à quelques jours, sans qu’il soit nécessaire d’administrer des corticostéroïdes de secours par voie orale à l’enfant ou de l’hospitaliser), l’asthme est probable si les parents ont fait un compte rendu convaincant d’une réponse symptomatique rapide et répétée à des BACA administrés seuls, au besoin, mais il s’agit là d’une méthode diagnostique plus faible (tableau 3). Afin d’accroître la certitude diagnostique, il est préférable de suivre ces enfants et, lorsqu’ils redeviennent symptomatiques, de les faire réévaluer par un professionnel de la santé compétent qui cherchera les signes d’obstruction des voies respiratoires et de réversibilité.
Chez les enfants qui présentent des symptômes fréquents (au moins deux fois par semaine[3] ou au moins huit jours par mois) ou au moins une exacerbation asthmatiforme modérée ou grave (traitée aux corticostéroïdes par voie orale ou nécessitant une hospitalisation), il est proposé d’effectuer un essai thérapeutique à l’aide d’une dose quotidienne moyenne de CSI (200 μg à 250 μg) et de BACA au besoin, administrés par aérosol-doseur (tableau 3).
Il est proposé de faire l’essai d’une dose quotidienne moyenne de CSI (tableau 5) pour déterminer la réversibilité de l’obstruction des voies respiratoires, parce qu’il s’agit du traitement d’entretien privilégié à la fois pour la prise en charge des épisodes d’exacerbations récurrentes et des symptômes persistants de l’asthme. Son efficacité est bien démontrée dans des analyses systématiques d’essais aléatoires et contrôlés.(13,27) Puisque les CSI ont un délai d’action de une à quatre semaines(28) et que la plupart des essais en démontrent l’efficacité dans les trois à six mois(13,27), il est recommandé de procéder à un essai thérapeutique d’une durée minimale de trois mois. Dans ce groupe d’âge, le budésonide et la fluticasone sont les médicaments qui ont été les plus étudiés. Ils sont tous deux efficaces sur le plan clinique,(19,27) mais la fluticasone a moins d’effets sur la croissance que le dipropionate de béclométhasone et que le budésonide à des doses équivalentes.(29) Puisqu’il est préférable de l’administrer par aérosol-doseur, le budésonide n’est pas recommandé, car il est seulement offert pour nébulisation chez les enfants de moins de six ans au Canada. Un seul essai aléatoire publié porte sur le ciclésonide,(30) et aucun ne traite de la mométasone chez les enfants d’âge préscolaire. En raison des données probantes plus faibles que pour les CSI,(27) il n’est pas recommandé d’utiliser le montélukast dans le cadre d’un essai thérapeutique.
TABLEAU 5.
Catégories posologiques des corticostéroïdes inhalés (CSI)* chez les enfants de un à cinq ans
| Corticostéroïde (nom générique) | Dose quotidienne de CSI, en microgrammes (μg)† | |
|---|---|---|
|
| ||
| Faible | Moyenne | |
| Béclométhasone (QVAR®) | 100 | 200 |
| Ciclésonide‡ (Alvesco®) | 100 | 200 |
| Fluticasone (Flovent®) | 100 à 125§ | 200 à 250 |
Les catégories posologiques proposées se fondent sur une combinaison d’équivalence approximative des doses ainsi que sur les données d’innocuité et d’efficacité plutôt que sur les formulations des produits sur le marché. Les zones ombragées indiquent qu’il s’agit d’une utilisation dans une indication non autorisée par Santé Canada, à l’exception de la béclométhasone (QVAR), dont l’utilisation est approuvée chez les enfants de cinq ans et plus. Puisqu’il est préférable de l’administrer par aérosol-doseur, le budésonide ne figure pas dans le présent tableau, car il est offert seulement pour nébulisation chez les enfants de moins de six ans au Canada. Les fortes doses de CSI ne sont pas recommandées dans ce groupe d’âge, mais il est recommandé d’orienter l’enfant vers un spécialiste de l’asthme si sa maladie n’est pas contrôlée malgré une dose moyenne de CSI;
Les doses de CSI sont indiquées sous forme de dose quotidienne totale à la sortie de la valve; elles devraient être divisées en deux pour être administrées deux fois par jour, sauf indication contraire. Les CSI doivent être administrés à l’aide d’un aérosol-doseur et d’une chambre d’espacement à valve adaptée à l’âge;
Homologué pour une seule dose quotidienne au Canada;
La fluticasone n’est pas homologuée pour être utilisée en dose quotidienne unique au Canada, mais une dose quotidienne unique de 125 μg est parfois préférée à deux doses de 50 μg pour favoriser l’observance du traitement.
La constatation de la réponse symptomatique au traitement
Un essai thérapeutique concluant est tributaire de l’observance de la médication pour l’asthme, d’une bonne technique d’inhalation, d’une consignation diligente des signes et symptômes et d’une réévaluation médicale au moment opportun. Puisqu’il est plus facile à interpréter, il est préférable d’effectuer l’essai thérapeutique pendant la saison au cours de laquelle l’enfant est le plus symptomatique. Pour étayer un changement de fréquence et de gravité des symptômes pendant et entre les exacerbations asthmatiformes, il est conseillé que les parents assurent une surveillance prospective des principaux critères de contrôle de l’asthme, y compris les symptômes diurnes et nocturnes, l’utilisation de BACA de secours, la limitation à l’effort, l’absentéisme des activités habituelles et les exacerbations qui exigent des consultations médicales imprévues, la prise de corticostéroïdes par voie orale ou une hospitalisation. Il est proposé de tout consigner dans un journal pour éviter les souvenirs inexacts,(31) même si celui-ci peut être erroné ou incomplet.(32,33) La fiabilité des comptes rendus des parents sur la réponse aux CSI n’a pas été vérifiée par des études. Par ailleurs, il n’est pas démontré que, sur le terrain, cette méthode puisse vraiment distinguer les enfants atteints d’asthme de ceux qui ne le sont pas. Cependant, les comptes rendus des parents sont largement utilisés dans les essais cliniques pour corroborer l’efficacité des CSI chez les enfants d’âge préscolaire. Puisque, au fil du temps, les parents observent de moins en moins les consignes d’administration quotidienne d’un médicament d’entretien et de transcription des observations dans un journal, il est recommandé d’effectuer le suivi médical initial vers le milieu de l’essai thérapeutique (au bout de six semaines).
Il faut constater une diminution évidente et soutenue de la fréquence et de la gravité des symptômes ou des exacerbations dans le cadre de l’essai thérapeutique d’un médicament d’entretien pour l’asthme pour confirmer la réversibilité de l’obstruction des voies respiratoires, c’est-à-dire la réponse au traitement. Aucune étude n’a analysé l’importance des changements nécessaires pour respecter la définition d’une réponse clinique satisfaisante. Toutefois, d’après des essais de doses quotidiennes moyennes de CSI, il faut s’attendre à une diminution de près de la moitié du nombre d’exacerbations exigeant la prise de corticostéroïdes par voie orale (risque relatif [RR] 0,57, 95 % IC 0,40 à 0,80), à des exacerbations moins longues et moins aiguës(27) et à une diminution des symptômes entre les exacerbations. On peut également supposer une réversibilité lorsque les parents rendent compte de façon convaincante et répétée d’une réponse rapide à court terme aux BACA lors des périodes symptomatiques (tableau 3). Cette possibilité fait d’ailleurs partie des critères diagnostiques plus faibles de réversibilité (tableau 1). Les cliniciens devraient savoir que les enfants(34) et les adultes(35) ne perçoivent pas toujours la réponse aux bronchodilatateurs avec fiabilité et que l’amélioration de l’enfant à court terme peut être spontanée ou attribuable à l’évolution naturelle d’une autre affection. Si un essai thérapeutique bien mené n’est pas concluant, il faut envisager de nouveau la possibilité d’une affection concomitante ou d’un autre diagnostic.
L’arrêt du traitement
Chez les enfants qui ont des symptômes légers et peu fréquents et des épisodes légers accompagnés de signes asthmatiformes dont l’atténuation n’est pas évidente dans le cadre d’un essai thérapeutique, il est proposé de privilégier une période d’observation de trois à six mois après l’arrêt du traitement ou jusqu’à la récurrence des symptômes, selon la première des éventualités. Si les parents rendent compte de l’aggravation des symptômes à l’arrêt du traitement, le diagnostic d’asthme est plausible.
MESSAGES CLÉS
7. Chez les enfants de un à cinq ans qui ont déjà présenté des épisodes récurrents et déclarés (au moins deux) de symptômes asthmatiformes et qui ont des sibilances à l’examen, un médecin ou un professionnel de la santé compétent qui observe lui-même une amélioration après la prise d’un bronchodilatateur inhalé (avec ou sans corticostéroïdes par voie orale) confirme le diagnostic (méthode diagnostique privilégiée).
8. Chez les enfants de un à cinq ans qui ont déjà présenté des épisodes récurrents et déclarés (au moins deux) de symptômes asthmatiformes et qui n’ont pas de sibilances à l’examen, des symptômes fréquents ou toute exacerbation modérée à grave justifient un essai thérapeutique d’une durée de trois mois à l’aide d’une dose quotidienne moyenne de CSI (accompagnés de ß2-agonistes à courte durée d’action [BACA] au besoin). Une diminution évidente et reproductible de la fréquence et de la gravité des symptômes ou des exacerbations confirme le diagnostic (autre méthode diagnostique).
9. Les enfants de un à cinq ans qui ont déjà présenté des épisodes récurrents (au moins deux) de symptômes asthmatiformes, des symptômes peu fréquents et des exacerbations légères et qui n’ont pas de sibilances à l’examen, peuvent être suivis et réévalués par un professionnel de la santé lorsqu’ils sont symptomatiques. On peut aussi opter pour un essai thérapeutique à l’aide de BACA au besoin. Un compte rendu convaincant des parents faisant état d’une réponse rapide et répétée aux BACA laisse supposer un diagnostic (autre méthode diagnostique plus faible).
10. Pour bien interpréter un essai thérapeutique, les cliniciens doivent vérifier l’observance du traitement pour l’asthme, la technique d’inhalation et le compte rendu des symptômes qu’ont consignés les parents, lors d’une réévaluation médicale au moment opportun.
L’ORIENTATION VERS UN SPÉCIALISTE
Les recommandations relatives à l’orientation vers un spécialiste sont exposées au tableau 6.(3,36–40) Les tests de la fonction pulmonaire pour les enfants d’âge préscolaire, offerts dans certains centres universitaires à vocation pédiatrique, peuvent être utiles pour confirmer le diagnostic.(41–44) Il est proposé de faire subir des tests d’allergie aux enfants ayant des symptômes persistants, afin d’évaluer le rôle possible des allergènes de l’environnement et de donner des conseils sur les stratégies d’évitement à adopter.(39,45)
TABLEAU 6.
Raisons de diriger l’enfant vers un spécialiste de l’asthme en vue d’une consultation ou d’une prise en charge conjointe
| Incertitude diagnostique ou présomption d’autre diagnostic |
| Exacerbations récurrentes (≥2) exigeant la prise de corticostéroïdes de secours par voie orale, hospitalisation ou symptômes fréquents (≥8 jours par mois) malgré une dose quotidienne modérée (200 μg à 250 μg) de corticostéroïdes inhalés |
| Événement au potentiel fatal, tel que l’admission à l’unité de soins intensifs |
| Nécessité de tests d’allergie pour évaluer le rôle possible des allergènes environnementaux |
| Autres considérations (anxiété des parents, besoin de paroles rassurantes, éducation supplémentaire sur l’asthme) |
MESSAGE CLÉ
11. Il est recommandé d’orienter vers un spécialiste de l’asthme les enfants de un à cinq ans dont le diagnostic est incertain, chez qui on présume des affections concomitantes, dont les symptômes sont mal contrôlés et qui présentent des exacerbations malgré des doses quotidiennes de 200 μg à 250 μg de CSI, qui ont souffert d’un événement au potentiel mortel (pour lequel ils ont été hospitalisés aux soins intensifs ou intubés) ou qui requièrent des tests d’allergie pour évaluer le rôle possible des allergènes environnementaux.
LES MÉTHODES DE PRISE EN CHARGE
Les méthodes non pharmacologiques
Une fois le diagnostic d’asthme confirmé, les familles et les autres personnes qui s’occupent de l’enfant doivent recevoir une éducation sur l’asthme qui inclut un plan de traitement écrit soulignant l’importance d’observer la médication pour l’asthme et de respecter les directives pertinentes sur la technique d’utilisation de l’inhalateur muni d’une chambre d’espacement à valve.(2) Chez les enfants de un à trois ans, il est préférable d’utiliser une chambre d’espacement dont le masque est de la bonne dimension. Chez ceux de quatre et cinq ans, il est conseillé d’envisager l’utilisation d’une chambre d’espacement munie d’un embout buccal si un professionnel de la santé compétent peut vérifier que l’enfant l’entoure hermétiquement de ses lèvres et respire par la bouche. Il est important d’éviter les irritants, tels que la fumée de cigarette, et les aéroallergènes si l’enfant y est sensibilisé.
Les méthodes pharmacologiques
Une fois le diagnostic confirmé, le traitement de première ligne privilégié consiste à administrer quotiennement des CSI, à la plus petite dose efficace (tableau 5), aux enfants ayant des symptômes persistants (plus de huit jours par mois) ou des exacerbations modérées à graves (exigeant la prise de corticostéroïdes de secours par voie orale ou une hospitalisation).(13,27) Si le patient a subi un essai thérapeutique composé d’une dose moyenne de CSI, il faut titrer ce médicament à la plus petite dose efficace pour assurer le contrôle de l’asthme (figure 2). Tant qu’on ne possédera pas plus de données pour en étayer l’efficacité, il est préférable de ne pas conseiller et d’éviter les trois stratégies courantes suivantes : la prise quotidienne d’antagonistes des récepteurs des leucotriènes, moins efficaces que les CSI et qui constituent une solution de deuxième ligne;(46) l’augmentation de la dose quotidienne de CSI dans le cadre d’une IVRS, car elle n’a pas fait l’objet d’essais aléatoires chez les enfants d’âge préscolaire; et l’utilisation intermittente de médicaments d’entretien pour l’asthme à l’apparition des symptômes (p. ex., montélukast ou doses faibles à moyennes de CSI) dont la capacité à réduire le nombre ou la gravité des exacerbations de l’asthme n’a pas été démontrée.(27,47,48) En revanche, le recours à une forte dose préventive de CSI dès l’apparition des symptômes atténue la gravité et la durée des exacerbations chez les enfants d’âge préscolaire atteints d’un asthme d’origine virale modéré à grave, mais en raison du risque de surutilisation et d’effets secondaires, ce traitement doit demeurer la prérogative des spécialistes de l’asthme et n’être utilisé que si les CSI quotidiens échouent.(49) Chez les enfants ayant déjà présenté des symptômes légers et peu fréquents (moins de huit jours par mois), qui n’ont pas d’exacerbations ou dont les exacerbations sont légères à l’examen (sans corticostéroïdes de secours par voie orale ni hospitalisation et qui ne dépassent pas quelques heures à quelques jours), la prise de BACA au besoin peut suffire pour contrôler la maladie.
Figure 2).
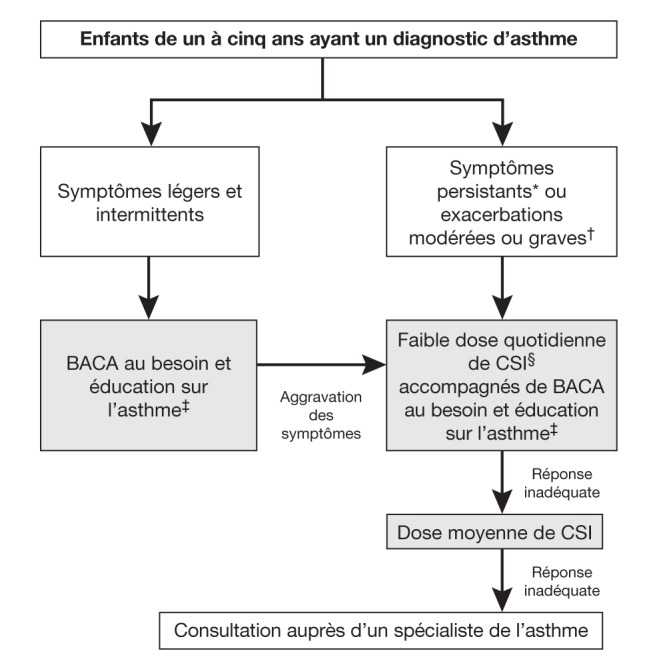
Algorithme de traitement pour les enfants d’âge préscolaire atteints d’asthme. *Au moins huit jours de symptômes par mois, au moins huit jours d’utilisation de β2-agonistes à courte durée d’action (BACA) inhalés par mois, au moins un réveil la nuit à cause des symptômes par mois, toute limitation à l’effort par mois ou toute absence à des activités habituelles en raison des symptômes d’asthme; †Épisodes exigeant la prise de corticostéroïdes de secours par voie orale ou une hospitalisation; ‡Éducation sur l’asthme, y compris l’assainissement de l’environnement et un plan d’autogestion écrit; §Les corticostéroïdes inhalés (CSI) sont plus efficaces que les antagonistes des récepteurs des leucotriènes (ARL).
Le suivi
Tous les trois ou quatre mois, il faut s’assurer du bon contrôle de l’asthme au moyen des mêmes critères que ceux utilisés chez les enfants d’âge scolaire et les adultes.(2) Une exacerbation qui exige la prise de corticostéroïdes systémiques de secours ou une hospitalisation est indicatrice d’une prise en charge sous-optimale et justifie une réévaluation rapide. Lorsque la maladie demeure bien contrôlée tout au long des trois mois précédant la réévaluation malgré l’exposition de l’enfant aux déclencheurs classiques et inévitables (p. ex., IVRS, air froid), il faut envisager de réduire graduellement la médication à la plus petite dose efficace. Compte tenu du fort taux de résolution des symptômes au sein de ce groupe d’âge, on peut tenter d’interrompre la médication lorsque les symptômes sont minimes avec la prise d’une faible dose de CSI pendant la saison au cours de laquelle l’enfant est généralement le plus symptomatique.
MESSAGE CLÉ
12. La prise quotidienne de CSI, à la plus petite dose efficace, est la méthode thérapeutique de première ligne à privilégier une fois le diagnostic d’asthme confirmé et les symptômes contrôlés.
LE TRANSFERT DES CONNAISSANCES ET LES OUTILS CLINIQUES
Le présent document peut être téléchargé à partir des sites www.lignesdirectricesrespiratoires.ca, www.cps.ca et www.pulsus.com.
Une présentation PowerPoint pour l’enseignement et l’autoapprentissage et un dépliant destinés aux professionnels de la santé figurent dans le site www.lignesdirectricesrespiratoires.ca, à l’onglet Outils et ressources de la page sur l’asthme.
En collaboration avec l’Université McGill, à Montréal, au Québec, la SCT a l’intention de préparer une application mobile pour faire connaître en pratique clinique les 12 messages clés et les autres recommandations des présentes lignes directrices.
Plusieurs types de journaux sur les symptômes de l’asthme sont proposés pour consigner la réponse à l’essai thérapeutique.
Dans le cadre des soins aigus, un module d’apprentissage virtuel du score PRAM figure dans le site www.chu-sainte-justine.org/pram.
L’Assemblée clinique sur l’asthme de la SCT est heureuse de s’associer à d’autres organisations et intervenants pour préparer des outils et ressources d’éducation qui appuient la mise en œuvre et l’adoption de ces messages clés auprès des divers groupes ciblés.
CONCLUSION
L’asthme est diagnostiqué chez les enfants de un à cinq ans qui ont déjà présenté des épisodes asthmatiformes récurrents, en fonction des signes (ou de comptes rendus convaincants de symptômes) d’obstruction des voies respiratoires et de réversibilité de cette obstruction après un traitement pour l’asthme et en l’absence de présomption clinique d’un autre diagnostic. Il est préférable qu’un médecin ou un autre professionnel de la santé compétent constate l’obstruction des voies respiratoires et la réversibilité de manière objective. Un algorithme diagnostique pragmatique est offert pour confirmer la présence d’asthme, d’asthme présumé ou de diagnostic incertain, en fonction de la présence ou de l’absence de signes d’obstruction des voies respiratoires à la consultation (figure 1). Une fois le diagnostic confirmé, la stratégie privilégiée consiste à administrer une faible dose quotidienne de CSI (de 100 μg à 125 μg par jour) et des BACA au besoin, aux enfants d’âge préscolaire ayant des symptômes persistants accompagnés ou non d’exacerbations modérées ou graves et à se limiter aux BACA au besoin, chez les enfants qui présentent des symptômes et des exacerbations légers et intermittents (figure 2).
LA SURVEILLANCE DU RESPECT DES MESSAGES CLÉS
Les paramètres suivants permettent de surveiller ou de vérifier l’observance de certaines des recommandations clés contenues dans le présent document de principes :
La moins grande utilisation de termes comme bronchospasmes, hyperréactivité bronchique, bronchite asthmatiforme et happy wheezer dans les dossiers médicaux.
Une consignation claire, dans le dossier médical des enfants d’âge préscolaire, de la présence ou de l’absence de signes et symptômes d’obstruction des voies respiratoires, de leur atténuation grâce au traitement et de la présomption clinique d’un autre diagnostic.
Chez les enfants de un à cinq ans ayant des symptômes fréquents accompagnés ou non d’exacerbations modérées à graves, la consignation de l’observation directe d’une réponse des signes d’obstruction des voies respiratoires aux BACA pour confirmer le diagnostic d’asthme.
Chez les enfants de un à cinq ans ayant des symptômes fréquents accompagnés ou non d’exacerbations modérées ou graves sans signes d’obstruction des voies respiratoires, la consignation d’un essai thérapeutique d’une durée de trois mois composé de CSI quotidiens pour confirmer le diagnostic d’asthme.
La proportion croissante d’enfants de un à cinq ans ayant déjà présenté des exacerbations asthmatiformes récurrentes (au moins deux), chez qui le diagnostic d’asthme est posé même si les épisodes sont déclenchés par des infections respiratoires virales.
LES FUTURES ORIENTATIONS
Constater les répercussions de ces nouveaux critères diagnostiques sur l’exactitude et la fréquence du diagnostic d’asthme, l’utilisation des médicaments et la santé des enfants d’âge préscolaire.
Explorer les perceptions des parents à l’égard de la méthode diagnostique proposée.
Vérifier la fréquence de la bonne consignation au dossier des trois critères d’asthme par des professionnels de la santé dans divers contextes.
Améliorer la capacité des parents à consigner les symptômes dans des journaux écrits, électroniques ou d’autres supports et en confirmer la fiabilité.
Améliorer la fiabilité et la faisabilité des tests de la fonction pulmonaire chez les enfants d’âge préscolaire pour diagnostiquer l’asthme avec objectivité, y compris de meilleures équations de référence pour détecter les enfants ayant une obstruction des voies respiratoires, proposer un classement de la gravité de l’obstruction des voies respiratoires fondé sur des données probantes et déterminer l’importance de l’amélioration de l’état du patient entre les rendez-vous, indicatrice d’une réponse marquée au traitement.
Explorer les répercussions de la mesure des tests de la fonction pulmonaire portables sur le contrôle de l’asthme, le risque de futures exacerbations et la trajectoire de la fonction pulmonaire des enfants d’âge préscolaire présentant des exacerbations asthmatiformes.
Acknowledgments
Les auteurs remercient la Société canadienne de thoracologie et la Société canadienne de pédiatrie d’avoir soutenu cette initiative. Ils tiennent à remercier les docteurs Paul Brand, Tom Kovesi, Rod Lim, Tim O’Callahan, Catherine Lemière, Diane Lougheed, Richard Leigh, Chris Licskai et Samir Gupta pour leurs commentaires constructifs lors de la révision. Ils sont également redevables à Mériem Bougrassa pour la coordination, à Annie Théoret pour son aide à la préparation du manuscrit et à Risa Shorr pour la recherche bibliographique.
Footnotes
INDÉPENDANCE ÉDITORIALE :
L’Assemblée clinique sur l’asthme de la SCT, qui relève du comité des Lignes directrices canadiennes en santé respiratoire et du conseil d’administration de la SCT, possède une indépendance sur le plan fonctionnel et éditorial vis-à-vis de toutes les sources de financement de la SCT. Aucun subventionnaire n’a participé à la collecte des données, à l’analyse de la révision ou à l’interprétation des publications scientifiques ni aux décisions relatives aux messages clés présentés dans le présent document.
CONFLITS D’INTÉRÊTS :
Les membres du groupe de travail ont déclaré leurs conflits d’intérêts potentiels au moment de leur nomination, lesquels ont été mis à jour tout au long du processus de rédaction conformément à la politique de divulgation des conflits d’intérêts de la SCT. Les déclarations de chaque membre au sujet des conflits d’intérêts figurent à l’adresse www.lignesdirectricesrespiratoires.ca/guideline/asthme.
TRANSFERT DES CONNAISSANCES ET OUTILS POUR LA PRATIQUE
RÉFÉRENCES
- 1.Hughes D. Recurrent pneumonia. Not! Paediatr Child Health. 2013;18:459–60. doi: 10.1093/pch/18.9.459. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 2.Lougheed MD, Lemiere C, Ducharme FM, et al. Canadian Thoracic Society 2012 guideline update: Diagnosis and management of asthma in preschoolers, children and adults. Can Respir J. 2012;19:127–64. doi: 10.1155/2012/635624. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 3.GINA Global Initiative for Asthma P Global strategy for asthma management and prevention. Global Initiative for Asthma 2014. < www.ginasthma.org/> (consulté en mai 2014).
- 4.Inoue Y, Shimojo N. Epidemiology of virus-induced wheezing/asthma in children. Front Microbiol. 2013;4:391. doi: 10.3389/fmicb.2013.00391. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 5.Castro-Rodriguez JA, Holberg CJ, Wright AL, Martinez FD. A clinical index to define risk of asthma in young children with recurrent wheezing. Am J Respir Crit Care Med. 2000;162:1403–6. doi: 10.1164/ajrccm.162.4.9912111. [DOI] [PubMed] [Google Scholar]
- 6.Martinez FD, Wright AL, Taussig LM, Holberg CJ, Halonen M, Morgan WJ. Asthma and wheezing in the first six years of life. The Group Health Medical Associates. N Engl J Med. 1995;332:133–8. doi: 10.1056/NEJM199501193320301. [DOI] [PubMed] [Google Scholar]
- 7.Leonardi NA, Spycher BD, Strippoli M-PF, Frey U, Silverman M, Kuehni CE. Validation of the Asthma Predictive Index and comparison with simpler clinical prediction rules. J Allergy Clin Immunol. 2011;127:1466–72.e6. doi: 10.1016/j.jaci.2011.03.001. [DOI] [PubMed] [Google Scholar]
- 8.Fouzas S, Brand PL. Predicting persistence of asthma in preschool wheezers: Crystal balls or muddy waters? Paediatr Respir Rev. 2013;14:46–52. doi: 10.1016/j.prrv.2012.08.004. [DOI] [PubMed] [Google Scholar]
- 9.Lougheed MD, Garvey N, Chapman KR, et al. Variations and gaps in management of acute asthma in Ontario emergency departments. Chest. 2009;135:724–36. doi: 10.1378/chest.08-0371. [DOI] [PubMed] [Google Scholar]
- 10.Lougheed MD, Garvey N, Chapman KR, et al. The Ontario Asthma Regional Variation Study: Emergency department visit rates and the relation to hospitalization rates. Chest. 2006;129:909–17. doi: 10.1378/chest.129.4.909. [DOI] [PubMed] [Google Scholar]
- 11.Grad R, Morgan WJ. Long-term outcomes of early-onset wheeze and asthma. J Allergy Clin Immunol. 2012;130:299–307. doi: 10.1016/j.jaci.2012.05.022. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 12.Saglani S, Payne DN, Zhu J, et al. Early detection of airway wall remodeling and eosinophilic inflammation in preschool wheezers. Am J Respir Crit Care Med. 2007;176:858–64. doi: 10.1164/rccm.200702-212OC. [DOI] [PubMed] [Google Scholar]
- 13.Castro-Rodriguez JA, Rodrigo GJ. Efficacy of inhaled corticosteroids in infants and preschoolers with recurrent wheezing and asthma: A systematic review with meta-analysis. Pediatrics. 2009;123:e519–e25. doi: 10.1542/peds.2008-2867. [DOI] [PubMed] [Google Scholar]
- 14.Cane RS, Ranganathan SC, McKenzie SA. What do parents of wheezy children understand by “wheeze”? Arch Dis Child. 2000;82:327–32. doi: 10.1136/adc.82.4.327. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 15.van Asperen PP. Cough and asthma. Paediatr Respir Rev. 2006;7:26–30. doi: 10.1016/j.prrv.2005.11.006. [DOI] [PubMed] [Google Scholar]
- 16.Gurwitz D, Corey M, Levison H. Pulmonary function and bronchial reactivity in children after croup. Am Rev Respir Dis. 1980;122:95–9. doi: 10.1164/arrd.1980.122.1.95. [DOI] [PubMed] [Google Scholar]
- 17.Koehoorn M, Karr CJ, Demers PA, Lencar C, Tamburic L, Brauer M. Descriptive epidemiological features of bronchiolitis in a population-based cohort. Pediatrics. 2008;122:1196–203. doi: 10.1542/peds.2007-2231. [DOI] [PubMed] [Google Scholar]
- 18.Oymar K, Skjerven HO, Mikalsen IB. Acute bronchiolitis in infants, a review. Scand J Trauma Resusc Emerg Med. 2014;22:23. doi: 10.1186/1757-7241-22-23. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 19.Ortiz-Alvarez O, Mikrogianakis A, comité des soins aigus de la Société canadienne de pédiatrie La prise en charge du patient pédiatrique présentant une exacerbation aiguë de l’asthme. Paediatr Child Health. 2012;17:257–62. [Google Scholar]
- 20.Cates CJ, Welsh EJ, Rowe BH. Holding chambers (spacers) versus nebulisers for beta-agonist treatment of acute asthma. Cochrane Database Syst Rev. 2013;(9):CD000052. doi: 10.1002/14651858.CD000052.pub3. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 21.Rowe BH, Spooner C, Ducharme FM, Bretzlaff JA, Bota GW. Early emergency department treatment of acute asthma with systemic corticosteroids. Cochrane Database Syst Rev. 2008:CD002178. doi: 10.1002/14651858.CD002178. [DOI] [PubMed] [Google Scholar]
- 22.Rowe BH, Spooner CH, Ducharme FM, Bretzlaff JA, Bota GW. Corticosteroids for preventing relapse following acute exacerbations of asthma. Cochrane Database Syst Rev. 2001:CD000195. doi: 10.1002/14651858.CD000195. [DOI] [PubMed] [Google Scholar]
- 23.Shefrin AE, Goldman RD. Use of dexamethasone and prednisone in acute asthma exacerbations in pediatric patients. Can Fam Physician. 2009;55:704–6. [PMC free article] [PubMed] [Google Scholar]
- 24.Keeney GE, Gray MP, Morrison AK, et al. Dexamethasone for acute asthma exacerbations in children: A meta-analysis. Pediatrics. 2014;133:493–9. doi: 10.1542/peds.2013-2273. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 25.Ducharme FM, Chalut D, Plotnick L, et al. The pediatric respiratory assessment measure: A valid clinical score for assessing acute asthma severity from toddlers to teenagers. J Pediatr. 2008;152:476–80. doi: 10.1016/j.jpeds.2007.08.034. [DOI] [PubMed] [Google Scholar]
- 26.Chalut DS, Ducharme FM, Davis GM. The preschool respiratory assessment measure (PRAM): A responsive index of acute asthma severity. J Pediatr. 2000;137:762–8. doi: 10.1067/mpd.2000.110121. [DOI] [PubMed] [Google Scholar]
- 27.Ducharme FM, Tse SM, Chauhan B. Diagnosis, management, and prognosis of preschool wheeze. Lancet. 2014;383:1593–604. doi: 10.1016/S0140-6736(14)60615-2. [DOI] [PubMed] [Google Scholar]
- 28.Bisgaard H, Gillies J, Groenewald M, Maden C. The effect of inhaled fluticasone propionate in the treatment of young asthmatic children: A dose comparison study. Am J Respir Crit Care Med. 1999;160:126–31. doi: 10.1164/ajrccm.160.1.9811024. [DOI] [PubMed] [Google Scholar]
- 29.Zhang L, Prietsch SO, Ducharme FM. Inhaled corticosteroids in children with persistent asthma: Effects on growth. Cochrane Database Syst Rev. 2014;7:CD009471. doi: 10.1002/14651858.CD009471.pub2. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 30.Brand PL, Luz Garcia-Garcia M, Morison A, Vermeulen JH, Weber HC. Ciclesonide in wheezy preschool children with a positive asthma predictive index or atopy. Respir Med. 2011;105:1588–95. doi: 10.1016/j.rmed.2011.07.017. [DOI] [PubMed] [Google Scholar]
- 31.Okupa AY, Sorkness CA, Mauger DT, Jackson DJ, Lemanske RF., Jr Daily diaries vs retrospective questionnaires to assess asthma control and therapeutic responses in asthma clinical trials: Is participant burden worth the effort? Chest. 2013;143:993–9. doi: 10.1378/chest.12-1055. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 32.Butz A. Use of health diaries in pediatric research. J Pediatr Health Care. 2004;18:262–3. doi: 10.1016/j.pedhc.2004.06.004. [DOI] [PubMed] [Google Scholar]
- 33.Stone AA, Shiffman S, Schwartz JE, Broderick JE, Hufford MR. Patient compliance with paper and electronic diaries. Control Clin Trials. 2003;24:182–99. doi: 10.1016/s0197-2456(02)00320-3. [DOI] [PubMed] [Google Scholar]
- 34.Couriel JM, Demis T, Olinsky A. The perception of asthma. Aust Paediatr J. 1986;22:45–7. doi: 10.1111/j.1440-1754.1986.tb00182.x. [DOI] [PubMed] [Google Scholar]
- 35.Wechsler ME, Kelley JM, Boyd IO, et al. Active albuterol or placebo, sham acupuncture, or no intervention in asthma. N Engl J Med. 2011;365:119–26. doi: 10.1056/NEJMoa1103319. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 36.Network BTSSIG British guideline on the management of asthma. Thorax. 2014;69:i1–i192. [Google Scholar]
- 37.Poowuttikul P, Kamat D, Thomas R, Pansare M. Asthma consultations with specialists: What do the pediatricians seek? Allergy Asthma Proc. 2011;32:307–12. doi: 10.2500/aap.2011.32.3445. [DOI] [PubMed] [Google Scholar]
- 38.Zealand TPSoN Best practice evidence based guideline: Wheeze and chest infection in infants less than one year. < www.paediatrics.org.nz2005:53> (consulté en avril 2005)
- 39.National Asthma E, Prevention P . Expert Panel Report 3: Guidelines for the Diagnosis and Management of Asthma. Bethesda: National Institutes of Health; 2007. [Google Scholar]
- 40.National Asthma Council Australia C . Asthma Handbook. National Asthma Council Australia; Melbourne: 2014. Version 1.1. < www.asthmahandbook.org.aug> (consulté en avril 2014) [Google Scholar]
- 41.Rosenfeld M, Allen J, Arets BH, et al. An official American Thoracic Society workshop report: Optimal lung function tests for monitoring cystic fibrosis, bronchopulmonary dysplasia, and recurrent wheezing in children less than 6 years of age. Ann Am Thorac Soc. 2013;10:S1–S11. doi: 10.1513/AnnalsATS.201301-017ST. [DOI] [PubMed] [Google Scholar]
- 42.Beydon N, Davis SD, Lombardi E, et al. An official American Thoracic Society/European Respiratory Society statement: Pulmonary function testing in preschool children. Am J Respir Crit Care Med. 2007;175:1304–45. doi: 10.1164/rccm.200605-642ST. [DOI] [PubMed] [Google Scholar]
- 43.Gaffin JM, Shotola NL, Martin TR, Phipatanakul W. Clinically useful spirometry in preschool-aged children: Evaluation of the 2007 American Thoracic Society Guidelines. J Asthma. 2010;47:762–7. doi: 10.3109/02770903.2010.485664. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 44.Sonnappa S, Bastardo CM, Wade A, et al. Symptom-pattern phenotype and pulmonary function in preschool wheezers. J Allergy Clin Immunol. 2010;126:519–26. doi: 10.1016/j.jaci.2010.04.018. [DOI] [PubMed] [Google Scholar]
- 45.Robinson M, Smart J. Allergy testing and referral in children. Aust Fam Physician. 2008;37:210–3. [PubMed] [Google Scholar]
- 46.Szefler SJ, Baker JW, Uryniak T, Goldman M, Silkoff PE. Comparative study of budesonide inhalation suspension and montelukast in young children with mild persistent asthma. J Allergy Clin Immunol. 2007;120:1043–50. doi: 10.1016/j.jaci.2007.08.063. [DOI] [PubMed] [Google Scholar]
- 47.Bisgaard H, Hermansen MN, Loland L, Halkjaer LB, Buchvald F. Intermittent inhaled corticosteroids in infants with episodic wheezing. N Engl J Med. 2006;354:1998–2005. doi: 10.1056/NEJMoa054692. [DOI] [PubMed] [Google Scholar]
- 48.Nwokoro C, Pandya H, Turner S, et al. Intermittent montelukast in children aged 10 months to 5 years with wheeze (WAIT trial): A multicentre, randomised, placebo-controlled trial. Lancet Respir Med. 2014;2:796–803. doi: 10.1016/S2213-2600(14)70186-9. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 49.Ducharme FM, Lemire C, Noya FJ, et al. Preemptive use of high-dose fluticasone for virus-induced wheezing in young children. N Engl J Med. 2009;360:339–53. doi: 10.1056/NEJMoa0808907. [DOI] [PubMed] [Google Scholar]