Abstract
Background
Despite the use of low-osmolar contrast media that have significantly reduced the occurrence of severe adverse reactions, contrast-induced (CI) acute kidney injury (AKI) remains the third cause of AKI in hospitals. We sought to estimate the frequency of CI-AKI among hospitalized patients undergoing image-guided cardiovascular procedures, to quantify the effect of risk factors on the development of this complication and to assess relative organizational and economic burden in healthcare.
Methods
A retrospective cross-sectional population-based study using the extensive French hospital discharge database (PMSI) was carried out. Hospitalizations with image-guided cardiovascular procedures using a contrast media were identified in adults over a 2-year period (2012–2013). Suspected CI-AKI was defined as the presence, during hospitalization, of a diagnostic code of AKI (International Classification of Diseases, 10th revision [ICD-10] codes: N141, 142, N144, N990, N17, N19 or R392) or a code of renal replacement therapy procedure (Classification Commune des Actes Médicaux [CCAM] codes: JVJB001, JVJF002-005 and JVJF008) as creatinine criteria were not available.
Results
During 1,047,329 hospitalizations studied, 32,308 suspected CI-AKI were observed, yielding a frequency of 3.1 %. By multivariate analysis, factors that significantly increased the risk of suspected CI-AKI included cardiogenic shock (odds ratio [OR] = 20.5, 95 % confidence interval [95 % CI] [18.7; 22.5]), acute heart failure (OR = 2.5, 95 % CI [2.4; 2.6]) and chronic kidney disease (OR = 2.3, 95 % CI [2.2; 2.3]. Renal replacement therapy was initiated during 6,335 (0.6 %) hospitalizations. The mean length of stay and cost of hospitalizations associated with suspected CI-AKI was higher than in hospitalizations without suspected CI-AKI (20.5 vs 4.7 days, p < 0.00001 and €15,765 vs €3,352, p < 0.0001, respectively).
Conclusions
This is the first large-scale population-based study to estimate frequency and health burden of suspected CI-AKI occurring after image-guided cardiovascular procedures, and the first available data in a French population. We showed that this iatrogenic complication remains of high concern despite prevention efforts and contrast media product improvement. From our results, suspected CI-AKI is associated with particularly high mortality, significantly extends hospitalizations, and leads to additional costs reaching a total of €200M per year.
Keywords: Contrast media, Cardiovascular procedure, Acute kidney injury, Epidemiology, Cost analysis
Background
The use of iodinated contrast media (ICM) improves the visualization of blood vessels during image-guided procedures [1]. However, it may lead to iatrogenic renal injury, causing contrast-induced (CI) acute kidney injury (AKI).
AKI, formerly known as acute renal failure, is common in hospitalized patients and is strongly associated with morbidity and mortality. It is a complex syndrome that may arise in response to various aetiologies, such as the use of nephrotoxic drugs.
CI-AKI is the third most common cause of AKI in hospitals, after functional and medicine-related causes [2]. Depending on the definition, the population and the procedure studied, CI-AKI frequencies reported in the literature range from 1.5 to 15 % [3–7]. In most patients involved, serum creatinine returns to normal values within 2 weeks [8]. However, a subset of this population will need renal replacement therapy with associated increased hospitalization times and costs, and increased mortality [9, 10].
Many individual risk factors for the development of CI-AKI have been reported [9–15], predominant are chronic kidney disease, diabetes mellitus, congestive heart failure and age over 70 years.
The frequency of CI-AKI was expected to decrease with the use of low-osmolar ICM. In order to provide insights on the current state of this complication to health professionals and authorities, we conducted a cross-sectional retrospective population-based study using hospital data. The objective was to estimate the frequency of CI-AKI among hospitalized patients who underwent image-guided cardiovascular procedures, to quantify the effect of risk factors on CI-AKI occurrence and to assess the relative organizational and economic burdens.
Methods
Data source
Subjects were identified from the extensive French hospital discharge database (Programme de Médicalisation des Systèmes d’Information [PMSI]), which covers all French public and private hospitals involved in medicine, surgery and obstetrics. In 2004, French hospitals adopted a prospective payment system. Since then, the PMSI database has become the basis of hospital funding by third-party payers. A standard discharge summary report is generated for each hospitalization, and includes information on patient characteristics (e.g. sex, age, residence code), the main diagnosis that led to hospital admission, examinations carried out during hospitalization, comorbidities and possible complications. Biological data are not recorded. Diagnoses are coded using the International Classification of Diseases, 10th revision (ICD-10); procedures using the French classification of procedures in medicine (Classification Commune des Actes Médicaux [CCAM]). The discharge summary is then linked to a diagnosis-related group, used for the classification of hospitalizations, which are associated with national fees. Permission to extract and use the PMSI data was obtained from the National Commission for Data Protection and Liberties.
Study population
The hospitalizations of adult patients (≥18 years) who had undergone image-guided cardiovascular interventions requiring intra-arterial or intra-venous ICM injections (Appendix 1) were extracted from 2012–2013 PMSI hospital databases. A committee of experts approved the selection of procedures.
Each hospitalization was considered as unique even though a patient could have had several different hospitalizations between January 1, 2012 and December 31, 2013.
Identification of suspected CI-AKI
The primary endpoint was the onset of a suspected CI-AKI during a hospitalization, defined as the presence of (Appendix 2):
a diagnosis of AKI (ICD-10 codes: N141, N142, N144, N990, N17, N19 or R392) or
a renal replacement therapy procedure (CCAM codes: JVJB001, JVJF002, JVJF003, JVJF004, JVJF005 or JVJF008).
When renal replacement therapy was used during the hospitalization of interest, the suspected CI-AKI was classified as requiring renal replacement therapy; otherwise, it was considered as without renal replacement therapy.
End-stage kidney disease patients were identified by searching for a relevant diagnosis (ICD-10 code: N185) or a procedure of renal replacement therapy for chronic kidney disease (ICD-10 code: Z992; CCAM code: JVJF004, JVJF008 or JVJB001) within the 2 years prior to the hospitalization of interest. These hospitalizations were excluded from the analysis of suspected CI-AKI requiring renal replacement therapy as the renal replacement therapy would most likely have been related to the underlying disease.
Collected data
All data were collected from the PMSI database. Known risk factors for developing CI-AKI (diabetes, chronic kidney disease, acute heart failure, onset of cardiogenic shock during the hospitalization) were recorded. The presence of diabetes (ICD-10 codes: E10-E14 or N083) or chronic kidney disease (ICD-10 code: N18) was searched for within the 2 years prior to the hospitalization, while acute heart failure (ICD-10 code: I50) and cardiogenic shock (ICD-10 code R570) were searched for only during the hospitalization.
In addition, sociodemographic characteristics (age and sex) and type of patient management (admission through the emergency department, hospitalization in an intensive care or resuscitation unit and hospital status) were collected.
Statistical analysis
Quantitative data are expressed as means with standard deviations (SDs) or 95 % confidence intervals (95 % CIs); categorical data as numbers and percentages. Quantitative variables were compared using the Student’s t-test; categorical variables using the Chi-squared test.
Multivariable analysis using a mixed model with fixed effects (PROC GLIMMIX), taking into account the variability between hospitals, was performed to study suspected CI-AKI risk factors that required renal replacement therapy or not: gender, age, chronic kidney disease, diabetes, acute heart failure, cardiogenic shock, admission by the emergency unit and hospital status. Co-variables that were considered significant (p < 0.05) in suspected CI-AKI onset during bivariate analysis were included in the multivariable analysis.
Statistical analysis was performed using SAS 9.3® software (SAS Institute Inc. Cary, NC, USA). The significance level was fixed at 0.05 for all analyses.
Economic analysis
The French Health Insurance perspective was used for the economic evaluation of hospitalizations. Each hospitalization is associated to a diagnosis-related group that is linked to a fixed tariff, which varies between public and private hospitals. Extra fees are added for hospitalizations with a visit to the intensive care unit, resuscitation unit, etc. All costs are expressed in 2015 euros. Costs incurred prior to this year were re-evaluated using the health service index (4011 E) (National Institute of Statistics and Economic Studies; Institut National de la Statistique et des Etudes Economiques [INSEE]).
Results
Hospitalization characteristics
During 2012–2013, a total of 1,047,329 hospitalizations involving an image-guided cardiovascular procedure requiring ICM administration was recorded in France. Hospitalizations most often included a coronary angiography procedure (45.4 %) and intraluminal dilation of one or several coronary vessels with endoprosthesis insertion (26.3 %). Procedures were not mutually exclusive. The most frequently reported reasons for hospitalization were cardiovascular events (Table 1).
Table 1.
Characteristics of patients and procedures during hospitalizations
| Hospitalizations (n = 1,047,329) | |
|---|---|
| Age (years), mean (SD) | 66.1 (13.8) |
| Men, n (%) | 712,586 (68.0 %) |
| Risk factors | |
| Diabetes | 270,463 (25.8 %) |
| Chronic kidney disease | 96,489 (9.2 %) |
| End-stage kidney disease | 57,118 (5.5 %) |
| Acute heart failure | 35,631 (3.4 %) |
| Cardiogenic shock | 2,202 (0.2 %) |
| Procedures (>2 %) | |
| Coronary arteriogram | 475,249 (45.4 %) |
| Intraluminal dilation of one or several coronary arteries with endoprosthesis insertion | 275 812 (26.3 %) |
| Intraluminal dilation of one or several lower limbs artery with endoprosthesis insertion | 54,420 (5.2 %) |
| Global arteriography of the abdominal aorta and lower limbs | 43,599 (4.2 %) |
| Intraluminal dilation of internal iliac artery and/or external iliac artery with endoprosthesis insertion | 32,631 (3.1 %) |
| Selective arteriography of 2 or more cervico-cephalic axes | 28,388 (2.7 %) |
| Intraluminal dilation of one or more lower limbs artery without endoprosthesis insertion | 25,875 (2.5 %) |
| Reasons for hospitalization (>5 %) | |
| Chronic ischaemic cardiomyopathy | 189,474 (18.1 %) |
| Angina pectoris | 165,852 (15.8 %) |
| Acute myocardial infarction | 105,772 (10.1 %) |
| Arterial embolism and thrombosis | 75,983 (7.3 %) |
| Atherosclerosis | 71,147 (6.8 %) |
| Emergency department admission | 151,826 (14.5 %) |
| Special unit admission | |
| Intensive care | 263,236 (25.1 %) |
| Resuscitation | 28,014 (3.6 %) |
| Deaths | 19,624 (1.9 %) |
| Hospital status | |
| Private | 442,957 (42.3 %) |
| Public | 604,372 (57.7 %) |
Data are presented as mean (SD) or n (%)
SD = standard deviation
Among all of the hospitalizations, the mean age was 66.1 years, and 68.0 % were male. Concerning risk factors, 25.8 % of hospitalizations involved patients with diabetes, 9.2 % with chronic kidney disease, 3.4 % with acute heart failure and cardiogenic shock occurred in 2,202 (0.2 %) of hospitalizations, among which 539 led to intra-aortic balloon pump use.
Suspected contrast-induced acute kidney injury
General description
Suspected CI-AKI was found in 3.1 % (n = 32,308) of hospitalizations involving an image-guided cardiovascular procedure using ICM. Patients who developed suspected CI-AKI were older than those who did not (mean [SD]: 70.6 [13.6] vs 65.9 [13.8] years, p = 0.0017), but there was no significant gender difference (67.8 vs 68.0 % male, p = 0.30).
The suspected CI-AKI proportion increased in hospitalizations involving patients with risk factors reaching 45.4 % (1,000/2,202) in hospitalizations during which patients presented with cardiogenic shock (Fig. 1).
Fig. 1.
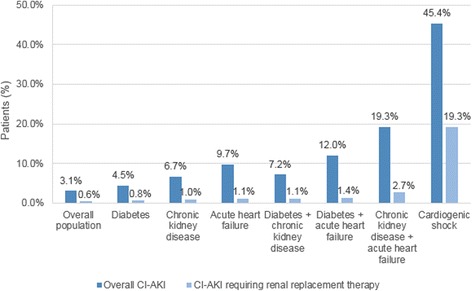
Proportions of hospitalizations with contrast-induced acute kidney injury, with and without renal replacement therapy. CI-AKI = contrast-induced acute kidney injury
Multivariable analysis of suspected CI-AKI risk factors indicated that the occurrence of cardiogenic shock during a hospitalization gave the highest odds ratio (OR) for suspected CI-AKI onset (OR = 20.5, 95 % CI [18.7; 22.5]). Other risk factors with high ORs were: age > 80 (OR = 2.7 95 % CI [2.6; 2.8]), acute heart failure (OR = 2.5, 95 % CI [2.4; 2.6]), emergency admission (OR = 2.5, 95 % CI [2.4; 2.6]) and chronic kidney disease (OR = 2.3, 95 % CI [2.2; 2.3]; Fig. 2). All co-variables were significant in the bivariate analysis.
Fig. 2.
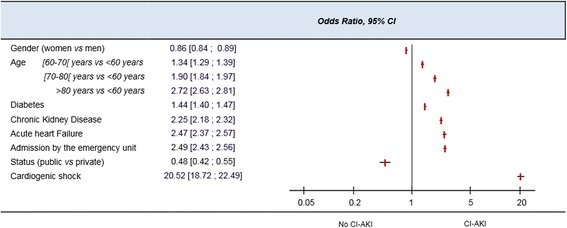
Risk factors for contrast-induced acute kidney injury onset. 95 % CI = 95 % confidence interval, CI-AKI = contrast-induced acute kidney injury
Proportion of stays leading to patient’s death was 1.9 %, with a higher for suspected CI-AKI hospitalizations (21.3 % vs 1.3 for hospitalizations without suspected CI-AKI, p < 0.0001). Proportion of stays leading to patient’s death associated with suspected CI-AKI ranged from 8.7 to 49.3 % in hospitalizations involving patients who presented with risk factors (Fig. 3).
Fig. 3.
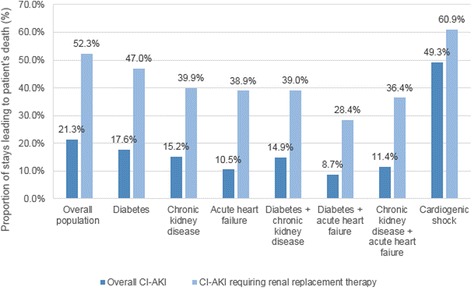
Proportion of stays leading to patient’s death associated with contrast-induced acute kidney injury, with and without renal replacement therapy. CI-AKI = contrast-induced acute kidney injury
Requirement for renal replacement therapy
Among the total population, 0.6 % (n = 6,335) required renal replacement therapy. This was higher among hospitalizations of patients with risk factors (Fig. 1).
Multivariable analysis of risks factors for suspected CI-AKI requiring renal replacement therapy indicated that the occurrence of cardiogenic shock during a hospitalization also gave the highest OR for suspected CI-AKI requiring renal replacement therapy (OR = 22.5, 95 % CI [20.0; 25.2]). Other risk factors with high ORs were emergency admission (OR = 2.2, 95 % CI [2.1; 2.3]) and chronic kidney disease (OR = 1.7, 95 % CI [1.6; 1.8]; Fig. 4). All co-variables were significant in the bivariate analysis.
Fig. 4.
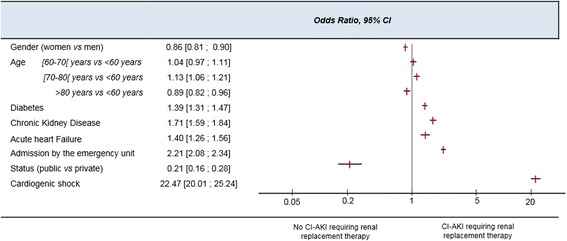
Risk factors for contrast-induced acute kidney injury requiring renal replacement therapy. 95 % CI = 95 % confidence interval
Hospitalizations during which suspected CI-AKI necessitated renal replacement therapy had a proportion of stays leading to patient’s death higher than hospitalizations with suspected CI-AKI and no renal replacement therapy (52.3 vs 13.7 %; p < 0.0001). Proportion of stays leading to patient’s during hospitalizations that involved patients with risk factors with suspected CI-AKI requiring renal replacement therapy ranged from 28.4 to 60.9 % (Fig. 3).
Additional costs associated with suspected CI-AKI
Total population
Suspected CI-AKI onset during a hospitalization led to a mean additional length of stay of 15.8 days (20.5 days, 95 % CI [20.2; 20.7] vs 4.7 days, 95 % CI [4.7; 4.7]; p < 0.00001; Fig. 5 and Table 2) and a mean extra cost of €12,413 (€15,765, 95 % CI [15,534; 15,995] vs €3,352, 95 % CI [3,343; 3,362]; p < 0.0001; Fig. 6 and Table 2).
Fig. 5.
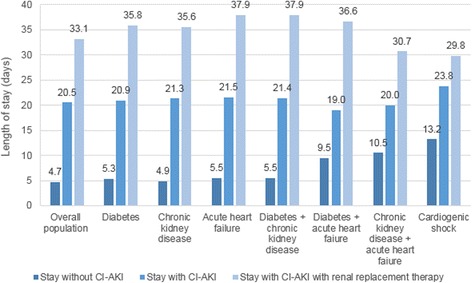
Lengths of stay associated with contrast-induced acute kidney injury, with and without renal replacement therapy. CI-AKI = contrast-induced acute kidney injury
Table 2.
Durations and costs of hospitalizations with and without contrast-induced acute kidney injury
| Duration of hospitalization (days), mean [95 % CI] | Cost of hospitalization (Euros), mean [95 % CI] | Additional cost (Euros) for French Health Insurance over 2 years | |
|---|---|---|---|
| Hospitalizations without suspected CI-AKI (n = 1,015,021) | 4.7 [4.7; 4.7] | 3,352 [3,343; 3,362] | - |
| Hospitalizations with suspected CI-AKI (n = 32,308) | 20.5 [20.2; 20.7] | 15,765 [15,534; 15,995] | 401,023,050 |
| Requiring renal replacement therapy (n = 6,335) | 33.1 [32.2; 34.0] | 31,979 [31,181; 32,777] | 181,348,244 |
Data are presented as mean [95 % CI]
Costs are presented in 2015 Euro
95 % CI 95 % confidence interval, CI-AKI contrast-induced acute kidney injury
Fig. 6.
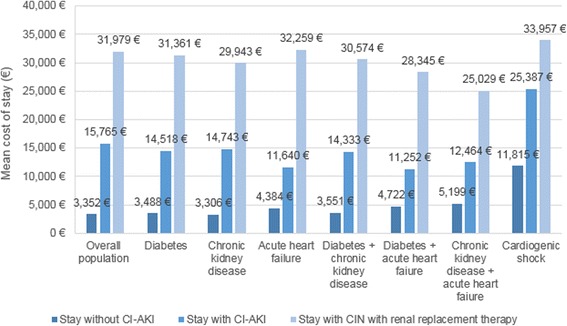
Costs of hospitalizations associated with contrast-induced acute kidney injury, with and without renal replacement therapy. CI-AKI = contrast-induced acute kidney injury
Additional lengths of stay and costs were higher for hospitalizations with suspected CI-AKI requiring renal replacement therapy than for hospitalizations without suspected CI-AKI, with a mean additional length of stay of 28.4 days (33.1 days, 95 % CI [32.2; 34.0] vs 4.7 days, 95 % CI [4.7; 4.7]; p < 0.00001; Fig. 5 and Table 2) and a mean additional cost of €28,627 (€31,979, 95 % CI [31,181; 32,777] vs €3,352, 95 % CI [3,343; 3,362]; p < 0.0001; Fig. 6 and Table 2). Overall, CI-AKI led to additional costs reaching a total of €401M over the 2-year period (Table 2).
Specific populations
Extra lengths of stay associated with suspected CI-AKI onset ranged from 9.5 to 16.4 days and from 20.2 to 32.4 days, depending on comorbidities, for hospitalizations of patients with suspected CI-AKI and suspected CI-AKI requiring renal replacement therapy, respectively (Fig. 5). Additional costs for these hospitalizations varied, respectively, from €6,530 to €11,437 and from €19,830 to €27,875, depending on comorbidities (Fig. 6).
Suspected CI-AKI onset led to an additional length of stay of 10.6 days and was associated with an extra cost of €13,572 for hospitalizations including patients with cardiogenic shock.
Discussion
To the best of our knowledge, this is the largest study to estimate the frequency and health burden of CI-AKI occurring after image-guided cardiovascular interventions. Furthermore, this is the first available data on the general French population. Indeed, the few studies that have reported this complication in France focused on units treating severe cases, such as intensive care units [16, 17].
Using a national claims database to obtain extensive real-life data, we identified more than 1 million hospitalizations involving an image-guided cardiovascular procedure requiring ICM administration over a 2-year period. This data sample allowed us to obtain robust results in the absence of important data such as creatinine results.
The frequency of suspected CI-AKI was 3.1 % in our study for the 1,047,329 hospitalizations including an image-guide procedure using ICM, which represents a substantial proportion. The reported frequencies of suspected CI-AKI vary widely in the literature, ranging from 1.5 to 15 % [3–7], depending on the patient population and baseline risk factors. Furthermore, as with any clinical event, the frequency also varies depending on the criteria by which it is defined. Differences in the definitions used make it difficult to compare results of clinical studies (Table 3). CI-AKI is classically defined in the recent literature as a rise in serum creatinine occurring within the first 24 h after contrast exposure and peaking up to 5 days afterward. In most instances, the rise in serum creatinine is expressed either in absolute terms (0.5–1.0 mg/dL; 44.2–88.4 μmol/L) or as a proportional rise in serum creatinine of 25 or 50 % above the baseline value.
Table 3.
Definitions of contrast-induced acute kidney injury
| Association/Reference | Definition |
|---|---|
| European Society of Urogenital Radiology [26] | Increase in serum creatinine >0.5 mg/dL (44 μmol/L) or >25 % within 72 h |
| Mehran et al. [22] | Increase in serum creatinine ≥0.5 mg/dL (44 μmol/L) or ≥25 % within 48 h |
| Acute Kidney Injury Network [27] | Increase in serum creatinine ≥0.3 mg/dL (26 μmol/L) or ≥50 % or oliguria (<0.5 mL/kg/h for >6 h) |
| Kidney Disease Improving Global Outcomes [28] | Increase in serum creatinine of ≥0.5 mg/dL (44 μmol/L) or ≥25 %, assessed 48 h after a radiological procedure |
GFR glomerular filtration rate
Renal replacement therapy was required in 0.6 % of hospitalizations, while the frequency of suspected CI-AKI requiring renal replacement therapy varies from 0.5 to 1 % in the literature [9, 18–20].
Our results come from a large and extensive database including all types of patients, with an extensive selection of image-guided cardiovascular procedures using ICM, thus allowing assessment of patients at all levels of severity.
The frequency of suspected CI-AKI was higher in hospitalizations involving patients with comorbidities (Fig. 1) and reached 45.4 % in hospitalizations with cardiogenic shock onset. This latter event was the greatest risk factor in our multivariable analysis with an OR of 20.5. Patients with chronic kidney disease or acute heart failure, and those who were admitted via emergency departments, had around twice the risk of developing CI-AKI.
CI-AKI was associated with extremely high in-hospital mortality of 21.3 %. The prognosis was even worse if the suspected CI-AKI required renal replacement therapy, with an in-hospital mortality reaching 52.3 %. Even though prior studies have reported mortality of 7 % for suspected CI-AKI without renal replacement therapy and 35 % for suspected CI-AKI requiring renal replacement therapy [9], but figures similar to ours have been reported in large retrospective cohort studies [10, 13, 21].
Surprisingly, mortality was lower during hospitalizations of patients with comorbidities than during those without (Fig. 3) despite a higher suspected CI-AKI frequency in these populations. One possible explanation for this lower mortality is the close monitoring of patients with important risk factors, leading to rapid detection and management of suspected CI-AKI. Furthermore, as it was not possible to study all of the confounding risks reported by Mehran et al., such as hypotension, contrast volume and haematocrit [22], the mortality results should be interpreted cautiously. Also, we could not analyse whether patients received non-steroidal anti-inflammatory drugs or were hyperglycaemic or volume depleted.
CI-AKI events were accompanied by an extreme increase in mean length of hospitalization (+15.8 days) and cost (+€12,413). The burden of this complication was higher when the suspected CI-AKI required renal replacement therapy, which increased the length of stay by 28.4 days and the cost by €28,627 compared with no CI-AKI. An economic analysis of the direct costs associated with CI-AKI has been conducted recently in the United States [23] – this study calculated the mean extra cost of CI-AKI onset to be $10,345 for the hospitalization in question and $11,812 for 1 year. The incidence data and results were calculated using a systematic search of the literature, and combined with unit costs, also obtained from the literature, using a decision-based analytical model. In our study, over the 2-year study period, it was estimated that onset of suspected CI-AKI during 1,047,329 hospitalizations led to additional overall expenditure for French Health Insurance of €401M.
Our study had several limitations, the majority of which are intrinsically linked to the PMSI database. This database is used in hospitals for budgetary reasons, and was not developed for epidemiological studies. Consequently, the data do not include results of clinical or biological testing. The absence of creatinine data represents the biggest limitation of our study. Therefore, to identify cases of suspected CI-AKI we selected, with the assistance of a Department of Medical Information doctor, the codes used in practice when this complication appears. Although the coding used to be poor in the early 2000’s, the quality has been widely improved in the past few years, showing high sensitivity and positive predictive value [24]. Furthermore, a selection of image-guided procedures usually requiring ICM administration was approved by a committee of experts. As the administration is not mandatory for all procedures selected and could not been verified, we conducted a secondary analysis on a restricted selection of image-guided cardiac procedures with mandatory use of ICM (DDQH and DGQH; Appendix 1). The results of this secondary analysis were similar to the main analysis and allowed us to validate the robustness of our results.
The PMSI database only allows observation of suspected CI-AKI with onset during hospitalization. However, CI-AKI onset can be up to 72 h after ICM administration and patients who are not considered at risk are often not hospitalized for such a long duration after the procedure. It is therefore possible that post-hospital events have not been taken into account. Nevertheless, as the mean length of hospitalization in this study was 4.7 days for patients without CI-AKI, we have assumed that the great majority of patients would still have been in hospital at the time of suspected CI-AKI onset, if it occurred.
Moreover, the PMSI database does not allow us to find the exact chronology of onset events during the hospitalization. Therefore, we have assumed that if, during a hospitalization that included a procedure requiring ICM administration, the patient presented with AKI, then the two events were related. However, we cannot state with certainty that all cases of AKI occurring in patients having ICM were attributed to CI-AKI. All cases of AKI, in the wider sense, have been taken into account and considered as suspected CI-AKI in this study. Nevertheless, some could be associated with cardiogenic shock or underlying conditions. This is, however, a limitation for most CI-AKI analyses as the accountability of ICM is often difficult to establish, even in clinical practice, as renal injury is multifactorial [25]. Furthermore, we observed cardiogenic shock in only 0.2 % of all hospitalizations, therefore, even if these events induced an AKI unrelated to ICM, it would not significantly impact our results. However, we note that we could not extract hypotension or use of potentially nephrotoxic agents (e.g. antibiotics or non-steroidal anti-inflammatory drugs) from the database, which are important potential causes of AKI.
Conclusion
This is the largest population-based study that has estimated the frequency and health burden of suspected CI-AKI occurring after image-guided cardiovascular procedures. We have shown that this iatrogenic complication remains of high concern despite prevention efforts and contrast media product improvement. In this study, suspected CI-AKI was associated with particularly high mortality, significantly extended hospital length of stay, and additional costs reaching a total of €200M per year. Even though results should be interpreted cautiously due to limitations regarding absence of creatinine data and the impossibility to identify all risk factors of CI-AKI, we believe they are strengthened by the extremely large sample used. Besides, they are informative on the economic burden of CI-AKI when data are scarce.
Key points
CI-AKI occurred in 3.1 % of image-guided cardiovascular procedures.
CI-AKI was associated with increased mortality.
CI-AKI was associated with significant hospital costs due to increased length of stay.
Acknowledgements
The authors thank Charlotte Cancalon for data management. Editorial support was provided by Jenny Lloyd (MedLink Healthcare Communications Ltd.).
Funding
This study received funding from GE Healthcare.
Availability of data and materials
All information supporting the conclusions of this manuscript is included within the article. Any additional information can be obtained upon request.
Authors’ contributions
GB and PA ensured the scientific accuracy of the study and participated in providing comments on the manuscript drafts. AS and LC were responsible for the study conception, design and data analysis. LC was a major contributor in writing the manuscript. SB contributed to the interpretation of data and provided comments on the final draft of the manuscript. All authors read and approved the final manuscript.
Competing interests
The authors declare that they have no competing interests.
Consent for publication
Not applicable.
Ethics approval and consent to participate
Institutional Review Board approval was not required because the study was based on the French hospital discharge database (PMSI). Written informed consent was not required because permission to extract and use the PMSI data was obtained from the National Commission for Data Protection and Liberties (CNIL).
Abbreviations
- 95 % CI
95 % confidence interval
- AKI
Acute kidney injury
- CCAM
French classification of procedures in medicine (Classification Commune des Actes Médicaux)
- CI
Contrast-induced
- ICD-10
International Classification of Diseases, 10th revision
- ICM
Iodinated contrast media
- INSEE
National Institute of Statistics and Economic Studies (Institut National de la Statistique et des Etudes Economiques)
- IQR
Interquartile range
- OR
Odds ratio
- PMSI
Programme for Medicalization of Information Systems (Programme de Médicalisation du Système d’Information)
- SD
Standard deviation
- WHO
World Health Organization
Appendix 1
Table 4.
Selected procedures (in the original French)
| CCAM code | Detail of procedure |
|---|---|
| DAAF001 | Dilatation intraluminale de la voie d'éjection du ventricule droit et du tronc de l'artère pulmonaire, par voie veineuse transcutanée |
| DAAF002 | Dilatation intraluminale de la voie d'éjection infraaortique, par voie artérielle transcutanée |
| DAAF003 | Agrandissement d'une communication interatriale, par voie veineuse transcutanée |
| DAGF001 | Ablation de corps étranger intracardiaque ou intravasculaire, par voie vasculaire transcutanée |
| DAHF001 | Biopsie de l'endocarde et du myocarde, par voie vasculaire transcutanée |
| DAMF001 | Création d'une communication interatriale, par voie veineuse transcutanée |
| DASF001 | Fermeture du conduit artériel, par voie vasculaire transcutanée |
| DASF002 | Fermeture d'une déhiscence d'une prothèse de cloisonnement intraatrial, par voie vasculaire transcutanée |
| DASF003 | Fermeture de communication interventriculaire, par voie veineuse transcutanée |
| DASF004 | Fermeture d'une communication interatriale, par voie veineuse transcutanée |
| DASF005 | Fermeture d'un foramen ovale perméable, par voie veineuse transcutanée |
| DBAF001 | Dilatation intraluminale de l'orifice aortique, par voie artérielle transcutanée |
| DBAF002 | Dilatation intraluminale de l'orifice pulmonaire sans perforation de la valve atrésique, par voie veineuse transcutanée |
| DBAF003 | Dilatation intraluminale de l'orifice atrioventriculaire droit, par voie veineuse transcutanée |
| DBAF004 | Dilatation intraluminale de l'orifice atrioventriculaire gauche, par voie veineuse transcutanée avec perforation du septum interatrial |
| DBAF005 | Dilatation intraluminale de l'orifice pulmonaire avec perforation de la valve atrésique, par voie veineuse transcutanée |
| DBLF001 | Pose d'une bioprothèse de la valve aortique, par voie artérielle transcutanée |
| DBLF009 | Pose d'une bioprothèse de la valve pulmonaire dans un conduit prothétique, par voie veineuse transcutanée |
| DBSF001 | Fermeture d'une déhiscence par désinsertion de prothèse orificielle cardiaque, par voie vasculaire transcutanée |
| DDAF001 | Dilatation intraluminale d'un vaisseau coronaire sans pose d'endoprothèse, par voie artérielle transcutanée |
| DDAF003 | Dilatation intraluminale de 3 vaisseaux coronaires ou plus avec pose d'endoprothèse, par voie artérielle transcutanée |
| DDAF004 | Dilatation intraluminale de 2 vaisseaux coronaires avec pose d'endoprothèse, par voie artérielle transcutanée |
| DDAF006 | Dilatation intraluminale d'un vaisseau coronaire avec pose d'endoprothèse, par voie artérielle transcutanée |
| DDAF007 | Dilatation intraluminale de 2 vaisseaux coronaires avec artériographie coronaire, avec pose d'endoprothèse, par voie artérielle transcutanée |
| DDAF008 | Dilatation intraluminale d'un vaisseau coronaire avec artériographie coronaire, avec pose d'endoprothèse, par voie artérielle transcutanée |
| DDAF009 | Dilatation intraluminale de 3 vaisseaux coronaires ou plus avec artériographie coronaire, avec pose d'endoprothèse, par voie artérielle transcutanée |
| DDAF010 | Dilatation intraluminale d'un vaisseau coronaire avec artériographie coronaire, sans pose d'endoprothèse, par voie artérielle transcutanée |
| DDFF001 | Athérectomie intraluminale d'artère coronaire par méthode rotatoire [rotationnelle], par voie artérielle transcutanée |
| DDFF002 | Athérectomie intraluminale d'artère coronaire, par voie artérielle transcutanée |
| DDPF002 | Recanalisation d'artère coronaire avec pose d'endoprothèse, par voie artérielle transcutanée |
| DDQH006 | Angiographie de pontage coronaire, par voie artérielle transcutanée |
| DDQH009 | Artériographie coronaire sans ventriculographie gauche, par voie artérielle transcutanée |
| DDQH010 | Artériographie coronaire avec ventriculographie gauche et artériographie thoracique [mammaire] interne unilatérale ou bilatérale, par voie artérielle transcutanée |
| DDQH011 | Artériographie coronaire avec angiographie d'un pontage coronaire et ventriculographie gauche, par voie artérielle transcutanée |
| DDQH012 | Artériographie coronaire avec ventriculographie gauche, par voie artérielle transcutanée |
| DDQH013 | Artériographie coronaire avec angiographie de plusieurs pontages coronaires sans ventriculographie gauche, par voie artérielle transcutanée |
| DDQH014 | Artériographie coronaire avec angiographie d'un pontage coronaire sans ventriculographie gauche, par voie artérielle transcutanée |
| DDQH015 | Artériographie coronaire avec angiographie de plusieurs pontages coronaires et ventriculographie gauche, par voie artérielle transcutanée |
| DDSF001 | Embolisation ou fermeture d'une fistule ou d'un anévrisme coronaire, par voie vasculaire transcutanée |
| DEEF001 | Repositionnement de sonde définitive intracavitaire de stimulation cardiaque, par voie veineuse transcutanée |
| DEEF002 | Repositionnement de sonde définitive intracavitaire de défibrillation cardiaque, par voie veineuse transcutanée |
| DFAF001 | Dilatation intraluminale de plusieurs branches de l'artère pulmonaire avec pose d'endoprothèse, par voie veineuse transcutanée |
| DFAF002 | Dilatation intraluminale d'une branche de l'artère pulmonaire sans pose d'endoprothèse, par voie veineuse transcutanée |
| DFAF003 | Dilatation intraluminale d'une branche de l'artère pulmonaire avec pose d'endoprothèse, par voie veineuse transcutanée |
| DFAF004 | Dilatation intraluminale de plusieurs branches de l'artère pulmonaire sans pose d'endoprothèse, par voie veineuse transcutanée |
| DFNF001 | Fibrinolyse in situ de l'artère pulmonaire, par voie veineuse transcutanée |
| DFNF002 | Thrombolyse mécanique ou thromboaspiration de l'artère pulmonaire, par voie veineuse transcutanée |
| DFQH001 | Artériographie sélective du tronc et/ou des branches de l'artère pulmonaire, par voie veineuse transcutanée |
| DFQH002 | Artériographie hypersélective des artères pulmonaires, par voie veineuse transcutanée |
| DFSF001 | Oblitération d'anévrisme sacculaire de l'artère pulmonaire, par voie veineuse transcutanée |
| DFSF002 | Embolisation de fistule artérioveineuse intrathoracique, par voie artérielle transcutanée |
| DGAF001 | Dilatation intraluminale de l'aorte thoracique sans pose d'endoprothèse, par voie artérielle transcutanée |
| DGAF003 | Dilatation intraluminale d'une coarctation de l'aorte abdominale, par voie artérielle transcutanée |
| DGAF004 | Dilatation intraluminale d'une coarctation de l'aorte thoracique avec pose d'endoprothèse, par voie artérielle transcutanée |
| DGAF005 | Dilatation intraluminale de l'aorte abdominale avec pose d'endoprothèse, par voie artérielle transcutanée |
| DGAF006 | Dilatation intraluminale d'une coarctation de l'aorte thoracique sans pose d'endoprothèse, par voie artérielle transcutanée |
| DGAF007 | Dilatation intraluminale de l'aorte thoracique avec pose d'endoprothèse, par voie artérielle transcutanée |
| DGAF008 | Dilatation intraluminale de l'aorte abdominale sans pose d'endoprothèse, par voie artérielle transcutanée |
| DGLF001 | Pose d'endoprothèse couverte bifurquée aortobisiliaque, par voie artérielle transcutanée |
| DGLF002 | Pose d'endoprothèse couverte aorto-uniiliaque, par voie artérielle transcutanée |
| DGLF003 | Pose d'endoprothèse couverte dans l'aorte thoracique, par voie artérielle transcutanée |
| DGLF005 | Pose d'endoprothèse couverte rectiligne dans l'aorte abdominale infrarénale, par voie artérielle transcutanée |
| DGLF006 | Pose d'un ballon de contrepulsion diastolique intraaortique, par voie artérielle transcutanée |
| DGLF012 | Pose d’endoprothèse fenêtrée ou multibranche dans l’aorte abdominale pour anévrisme complexe, par voie artérielle transcutanée |
| DGPF001 | Désobstruction de la bifurcation aortique, par voie artérielle transcutanée |
| DGPF002 | Recanalisation de la bifurcation aortique avec pose d'endoprothèse, par voie artérielle transcutanée bilatérale |
| DGQH001 | Artériographie globale de l'aorte abdominale et des membres inférieurs, par voie artérielle transcutanée |
| DGQH002 | Artériographie globale de l'aorte abdominale, par voie artérielle transcutanée |
| DGQH003 | Artériographie de l'aorte abdominale et des membres inférieurs, par injection intraaortique transcutanée lombale |
| DGQH004 | Artériographie de l'aorte et de ses branches, par injection intraveineuse transcutanée |
| DGQH005 | Artériographie globale de l'aorte thoracique et abdominale, par voie artérielle transcutanée |
| DGQH006 | Artériographie globale de l'aorte thoracique, par voie artérielle transcutanée |
| DGQH007 | Artériographie globale de la crosse de l'aorte et de ses branches cervicocéphaliques [Gerbe aortique], par voie artérielle transcutanée |
| DHAF001 | Dilatation intraluminale de la veine cave supérieure avec pose d'endoprothèse, par voie veineuse transcutanée |
| DHAF002 | Dilatation intraluminale de la veine cave inférieure sans pose d'endoprothèse, par voie veineuse transcutanée |
| DHAF003 | Dilatation intraluminale de la veine cave supérieure sans pose d'endoprothèse, par voie veineuse transcutanée |
| DHAF004 | Dilatation intraluminale de la veine cave inférieure avec pose d'endoprothèse, par voie veineuse transcutanée |
| DHGF001 | Ablation d'un filtre temporaire de la veine cave inférieure, par voie veineuse transcutanée |
| DHNF001 | Thrombolyse mécanique ou thromboaspiration de la veine cave supérieure, par voie veineuse transcutanée |
| DHNF002 | Fibrinolyse in situ fémoro-ilio-cave, par voie veineuse transcutanée |
| DHNF003 | Thrombolyse mécanique ou thromboaspiration de la veine cave inférieure, par voie veineuse transcutanée |
| DHNF004 | Fibrinolyse in situ de la veine cave inférieure, par voie veineuse transcutanée |
| DHNF005 | Fibrinolyse in situ de la veine cave supérieure, par voie veineuse transcutanée |
| DHNF006 | Fibrinolyse in situ fémoro-ilio-cave avec oblitération partielle de la veine cave inférieure [pose d'un filtre cave], par voie veineuse transcutanée |
| DHPF001 | Recanalisation de la veine cave supérieure sans pose d'endoprothèse, par voie veineuse transcutanée |
| DHPF002 | Recanalisation de la veine cave supérieure avec pose d'endoprothèse, par voie veineuse transcutanée |
| DHPF003 | Recanalisation de la veine cave inférieure sans pose d'endoprothèse, par voie veineuse transcutanée |
| DHQH001 | Phlébographie sélective de plusieurs branches des veines iliaques communes et/ou de la veine cave inférieure, par voie veineuse transcutanée |
| DHQH002 | Phlébographie de la veine cave inférieure [Cavographie inférieure], par voie veineuse transcutanée |
| DHQH003 | Phlébographie de la veine cave supérieure [Cavographie supérieure], par injection intraveineuse transcutanée |
| DHQH004 | Phlébographie sélective d'une branche de la veine iliaque commune ou de la veine cave inférieure, par voie veineuse transcutanée |
| DHQH005 | Phlébographie des veines iliaque et cave inférieure [Iliocavographie], par injection intraveineuse transcutanée fémorale unilatérale ou bilatérale |
| DHQH006 | Phlébographie globale de la veine cave supérieure [Cavographie supérieure], par voie veineuse transcutanée |
| DHQH007 | Phlébographie hypersélective d'une branche de la veine iliaque commune ou de la veine cave inférieure, par voie veineuse transcutanée |
| DHSF001 | Oblitération partielle temporaire de la veine cave inférieure, par voie veineuse transcutanée |
| DHSF002 | Oblitération partielle définitive de la veine cave inférieure, par voie veineuse transcutanée |
| EAAF002 | Dilatation intraluminale du tronc de l'artère carotide interne intracrânienne avec pose d'endoprothèse, par voie artérielle transcutanée |
| EAAF004 | Dilatation intraluminale du tronc de l'artère carotide interne intracrânienne sans pose d'endoprothèse, par voie artérielle transcutanée |
| EAAF900 | Dilatation intraluminale de branche de l'artère carotide interne avec pose d'endoprothèse, par voie artérielle transcutanée |
| EAAF901 | Dilatation intraluminale de branche de l'artère carotide interne sans pose d'endoprothèse, par voie artérielle transcutanée |
| EAAF902 | Dilatation intraluminale de l'artère vertébrale intracrânienne ou de l'artère basilaire avec pose d'endoprothèse, par voie artérielle transcutanée |
| EAAF903 | Dilatation intraluminale de l'artère vertébrale intracrânienne ou de l'artère basilaire sans pose d'endoprothèse, par voie artérielle transcutanée |
| EACF001 | Inversion du flux d'un anévrisme artériel intracrânien en période aigüe hémorragique, par voie artérielle transcutanée |
| EACF002 | Inversion du flux d'un anévrisme artériel intracrânien en dehors d'une période aigüe hémorragique, par voie artérielle transcutanée |
| EANF002 | Fibrinolyse in situ suprasélective d'artère intracrânienne, par voie artérielle transcutanée |
| EASF001 | Oblitération de plusieurs anévrismes sacculaires artériels intracrâniens en dehors d'une période aigüe hémorragique, par voie artérielle transcutanée |
| EASF002 | Occlusion intraluminale d'un vaisseau intracrânien afférent à une tumeur, par voie vasculaire transcutanée |
| EASF003 | Occlusion intraluminale de plusieurs vaisseaux intracrâniens afférents à une tumeur, par voie vasculaire transcutanée |
| EASF004 | Embolisation suprasélective unilatérale ou bilatérale de branche de l'artère carotide interne, par voie artérielle transcutanée |
| EASF005 | Embolisation d'une fistule artérioveineuse durale cranioencéphalique multipédiculaire, par voie artérielle et par voie veineuse transcutanées |
| EASF006 | Embolisation d'une fistule artérioveineuse durale cranioencéphalique unipédiculaire, par voie artérielle ou veineuse transcutanée |
| EASF007 | Oblitération intraluminale d'une artère intracrânienne porteuse d'un anévrisme en période aigüe hémorragique, par voie artérielle transcutanée |
| EASF008 | Oblitération intraluminale d'une artère intracrânienne porteuse d'un anévrisme en dehors d'une période aigüe hémorragique, par voie artérielle transcutanée |
| EASF009 | Embolisation d'une fistule artérioveineuse durale cranioencéphalique unipédiculaire, par voie artérielle et par voie veineuse transcutanées |
| EASF010 | Oblitération d'un anévrisme sacculaire artériel intracrânien en période aigüe hémorragique, par voie artérielle transcutanée |
| EASF011 | Oblitération d'un anévrisme sacculaire artériel intracrânien en dehors d'une période aigüe hémorragique, par voie artérielle transcutanée |
| EASF012 | Occlusion intraluminale d'un vaisseau intracrânien, par voie vasculaire transcutanée |
| EASF013 | Oblitération de plusieurs anévrismes sacculaires artériels intracrâniens en période aigüe hémorragique, par voie artérielle transcutanée |
| EASF014 | Embolisation sélective ou hypersélective unilatérale ou bilatérale de branche de l'artère carotide interne, par voie artérielle transcutanée |
| EASF015 | Embolisation d'une fistule artérioveineuse durale cranioencéphalique multipédiculaire, par voie artérielle ou veineuse transcutanée |
| EBAF001 | Dilatation intraluminale de l'artère carotide interne extracrânienne avec pose d'endoprothèse, par voie artérielle transcutanée |
| EBAF003 | Dilatation intraluminale de l'artère carotide interne extracrânienne sans pose d'endoprothèse, par voie artérielle transcutanée |
| EBAF004 | Dilatation intraluminale de l'artère carotide commune cervicale sans pose d'endoprothèse, par voie artérielle transcutanée |
| EBAF005 | Dilatation intraluminale de l'artère carotide externe sans pose d'endoprothèse, par voie artérielle transcutanée |
| EBAF006 | Dilatation intraluminale de l'artère carotide externe avec pose d'endoprothèse, par voie artérielle transcutanée |
| EBAF009 | Dilatation intraluminale de la bifurcation carotidienne sans pose d'endoprothèse, par voie artérielle transcutanée |
| EBAF010 | Dilatation intraluminale de l'artère carotide commune cervicale avec pose d'endoprothèse, par voie artérielle transcutanée |
| EBAF011 | Dilatation intraluminale de la bifurcation carotidienne avec pose d'endoprothèse, par voie artérielle transcutanée |
| EBAF013 | Dilatation intraluminale de l'artère vertébrale extracrânienne sans pose d'endoprothèse, par voie artérielle transcutanée |
| EBAF014 | Dilatation intraluminale de l'artère vertébrale extracrânienne avec pose d'endoprothèse, par voie artérielle transcutanée |
| EBNF001 | Fibrinolyse in situ sélective ou hypersélective d'une artère extracrânienne à destination cervicocéphalique, par voie artérielle transcutanée |
| EBNF002 | Fibrinolyse in situ suprasélective d'une artère extracrânienne à destination cervicocéphalique, par voie artérielle transcutanée |
| EBQH001 | Phlébographie globale d'un axe cervicocéphalique, par voie veineuse transcutanée |
| EBQH002 | Artériographie sélective de 3 axes cervicocéphaliques ou plus, par voie artérielle transcutanée |
| EBQH005 | Artériographie hypersélective cervicocéphalique, par voie artérielle transcutanée |
| EBQH007 | Artériographie suprasélective cervicocéphalique, par voie artérielle transcutanée |
| EBQH008 | Artériographie de plusieurs axes cervicocéphaliques, par injections intraartérielles transcutanées multiples |
| EBQH009 | Phlébographie d'un axe cervicocéphalique, par injection intrajugulaire transcutanée |
| EBQH010 | Artériographie d'un axe cervicocéphalique, par injection intraartérielle transcutanée unique |
| EBQH011 | Artériographie sélective d'un ou 2 axes cervicocéphaliques, par voie artérielle transcutanée |
| EBSF001 | Occlusion d'une fistule artérioveineuse directe cervicale ou crânienne, par voie vasculaire transcutanée |
| EBSF003 | Embolisation sélective ou hypersélective unilatérale ou bilatérale de branche de l'artère carotide externe, par voie artérielle transcutanée |
| EBSF004 | Embolisation suprasélective unilatérale ou bilatérale de branche de l'artère carotide externe, par voie artérielle transcutanée |
| ECAF001 | Dilatation intraluminale d'une artère du membre supérieur avec pose d'endoprothèse, par voie artérielle transcutanée |
| ECAF002 | Dilatation intraluminale d'une artère du membre supérieur sans pose d'endoprothèse, par voie artérielle transcutanée |
| ECAF003 | Dilatation intraluminale du tronc artériel brachiocéphalique ou de l'artère carotide commune intrathoracique sans pose d'endoprothèse, par voie artérielle transcutanée |
| ECAF004 | Dilatation intraluminale du tronc artériel brachiocéphalique ou de l'artère carotide commune intrathoracique avec pose d'endoprothèse, par voie artérielle transcutanée |
| ECJF001 | Thromboaspiration d'artère ou de pontage artériel du membre supérieur, par voie artérielle transcutanée |
| ECLF003 | Pose d'endoprothèse couverte dans une artère du membre supérieur, par voie artérielle transcutanée |
| ECLF004 | Pose d'endoprothèse couverte dans le tronc artériel brachiocéphalique ou l'artère carotide commune intrathoracique, par voie artérielle transcutanée |
| ECLF005 | Injection intraartérielle in situ sélective ou hypersélective d'agent pharmacologique anticancéreux au membre supérieur, par voie artérielle transcutanée |
| ECLF006 | Injection intraartérielle in situ suprasélective d'agent pharmacologique anticancéreux au membre supérieur, par voie artérielle transcutanée |
| ECNF001 | Fibrinolyse in situ suprasélective d'une artère ou d'un pontage artériel du membre supérieur, par voie artérielle transcutanée |
| ECNF002 | Fibrinolyse in situ sélective ou hypersélective d'une artère ou d'un pontage artériel du membre supérieur, par voie artérielle transcutanée |
| ECPF001 | Recanalisation d'une artère du membre supérieur avec pose d'endoprothèse couverte, par voie artérielle transcutanée |
| ECPF002 | Recanalisation d'une artère du membre supérieur avec pose d'endoprothèse, par voie artérielle transcutanée |
| ECPF003 | Recanalisation d'une artère du membre supérieur sans pose d'endoprothèse, par voie artérielle transcutanée |
| ECPF004 | Recanalisation de l'artère subclavière en amont de l'ostium de l'artère vertébrale sans pose d'endoprothèse, par voie artérielle transcutanée |
| ECPF005 | Recanalisation de l'artère subclavière en amont de l'ostium de l'artère vertébrale avec pose d'endoprothèse, par voie artérielle transcutanée |
| ECQH001 | Artériographie bilatérale du membre supérieur par voie artérielle ou injection intraartérielle transcutanée, avec manœuvre positionnelle |
| ECQH002 | Artériographie suprasélective du membre supérieur, par voie artérielle transcutanée |
| ECQH003 | Artériographie unilatérale de la main, par injection intraartérielle transcutanée |
| ECQH004 | Artériographie unilatérale du membre supérieur par voie artérielle ou injection intraartérielle transcutanée, avec manœuvre positionnelle |
| ECQH005 | Artériographie sélective ou hypersélective du membre supérieur, par voie artérielle transcutanée |
| ECQH006 | Artériographie du membre supérieur par injection intraartérielle transcutanée, sans manœuvre positionnelle |
| ECQH007 | Artériographie bilatérale de la main, par injection intraartérielle transcutanée |
| ECQH012 | Artériographie sélective ou hypersélective de la totalité de la moelle épinière, par voie artérielle transcutanée |
| ECQH013 | Artériographie sélective ou hypersélective d'un segment de la moelle épinière, par voie artérielle transcutanée |
| ECQH014 | Artériographie suprasélective de la moelle épinière, par voie artérielle transcutanée |
| ECQH015 | Artériographie sélective ou hypersélective d'artère intrathoracique à destination pariétale et/ou viscérale, par voie artérielle transcutanée |
| ECQH016 | Artériographie suprasélective d'artère intrathoracique à destination pariétale et/ou viscérale, par voie artérielle transcutanée |
| ECSF001 | Oblitération de plusieurs anévrismes sacculaires artériels du membre supérieur, par voie artérielle transcutanée |
| ECSF002 | Embolisation suprasélective d'une artère du membre supérieur, par voie artérielle transcutanée |
| ECSF003 | Oblitération d'un anévrisme sacculaire artériel du membre supérieur, par voie artérielle transcutanée |
| ECSF004 | Embolisation sélective ou hypersélective d'artère à destination bronchique ou pleuropulmonaire, par voie artérielle transcutanée |
| ECSF006 | Embolisation suprasélective d'artère à destination bronchique ou pleuropulmonaire, par voie artérielle transcutanée |
| ECSF008 | Embolisation sélective ou hypersélective d'une artère du membre supérieur, par voie artérielle transcutanée |
| EDAF001 | Dilatation intraluminale sélective ou hypersélective de l'artère rénale avec pose d'endoprothèse, par voie artérielle transcutanée |
| EDAF002 | Dilatation intraluminale de l'artère iliaque commune et/ou de l'artère iliaque externe sans pose d'endoprothèse, par voie artérielle transcutanée |
| EDAF003 | Dilatation intraluminale de l'artère iliaque commune et/ou de l'artère iliaque externe avec pose d'endoprothèse, par voie artérielle transcutanée |
| EDAF004 | Dilatation intraluminale de l'artère iliaque interne sans pose d'endoprothèse, par voie artérielle transcutanée |
| EDAF005 | Dilatation intraluminale d'une artère digestive avec pose d'endoprothèse, par voie artérielle transcutanée |
| EDAF006 | Dilatation intraluminale de l'artère iliaque interne avec pose d'endoprothèse, par voie artérielle transcutanée |
| EDAF007 | Dilatation intraluminale sélective ou hypersélective de l'artère rénale sans pose d'endoprothèse, par voie artérielle transcutanée |
| EDAF008 | Dilatation intraluminale d'une artère digestive sans pose d'endoprothèse, par voie artérielle transcutanée |
| EDAF009 | Dilatation intraluminale suprasélective de l'artère rénale sans pose d'endoprothèse, par voie artérielle transcutanée |
| EDAF010 | Dilatation intraluminale suprasélective de l'artère rénale avec pose d'endoprothèse, par voie artérielle transcutanée |
| EDJF001 | Thromboaspiration de l'artère rénale, par voie artérielle transcutanée |
| EDJF002 | Thromboaspiration d'artère digestive, par voie artérielle transcutanée |
| EDLF004 | Pose d'endoprothèse couverte dans l'artère iliaque commune et/ou l'artère iliaque externe avec embolisation de l'artère iliaque interne, par voie artérielle transcutanée |
| EDLF005 | Pose d'endoprothèse couverte dans l'artère iliaque commune et/ou l'artère iliaque externe, par voie artérielle transcutanée |
| EDLF006 | Pose d'endoprothèse couverte dans une artère digestive, par voie artérielle transcutanée |
| EDLF007 | Pose d'endoprothèse couverte dans l'artère iliaque interne ou une branche extradigestive de l'aorte abdominale, par voie artérielle transcutanée |
| EDLF008 | Pose d'endoprothèse couverte dans plusieurs artères digestives, par voie artérielle transcutanée |
| EDLF013 | Pose d'endoprothèse couverte dans l'artère rénale, par voie artérielle transcutanée |
| EDLF014 | Injection intraartérielle hépatique in situ sélective ou hypersélective d'agent pharmacologique anticancéreux non radio-isotopique sans embolisation de particules, par voie artérielle transcutanée |
| EDLF015 | Injection intraartérielle hépatique in situ suprasélective d'agent pharmacologique anticancéreux non radio-isotopique sans embolisation de particules, par voie artérielle transcutanée |
| EDLF016 | Injection intraartérielle hépatique in situ suprasélective d'agent pharmacologique anticancéreux non radio-isotopique avec embolisation de particules, par voie artérielle transcutanée |
| EDLF017 | Injection intraartérielle hépatique in situ sélective ou hypersélective d'agent pharmacologique anticancéreux non radio-isotopique avec embolisation de particules, par voie artérielle transcutanée |
| EDLF018 | Injection intraartérielle rénale in situ suprasélective d'agent pharmacologique anticancéreux avec embolisation de particules, par voie artérielle transcutanée |
| EDLF019 | Injection intraartérielle rénale in situ sélective ou hypersélective d'agent pharmacologique anticancéreux avec embolisation de particules, par voie artérielle transcutanée |
| EDLF020 | Injection intraartérielle rénale in situ sélective ou hypersélective d'agent pharmacologique anticancéreux sans embolisation de particules, par voie artérielle transcutanée |
| EDLF021 | Injection intraartérielle rénale in situ suprasélective d'agent pharmacologique anticancéreux sans embolisation de particules, par voie artérielle transcutanée |
| EDLL001 | Injection intraartérielle hépatique in situ d'agent pharmacologique radio-isotopique avec embolisation de particules, par voie artérielle transcutanée |
| EDLL002 | Injection intraartérielle hépatique in situ d'agent pharmacologique radio-isotopique sans embolisation de particules, par voie artérielle transcutanée |
| EDNF001 | Fibrinolyse in situ suprasélective de l'artère rénale, par voie artérielle transcutanée |
| EDNF002 | Fibrinolyse in situ sélective ou hypersélective de l'artère rénale, par voie artérielle transcutanée |
| EDNF003 | Fibrinolyse in situ d'une artère digestive, par voie artérielle transcutanée |
| EDPF001 | Recanalisation de l'artère iliaque interne avec pose d'endoprothèse, par voie artérielle transcutanée |
| EDPF002 | Recanalisation de l'artère rénale sans pose d'endoprothèse, par voie artérielle transcutanée |
| EDPF003 | Recanalisation d'une artère digestive sans pose d'endoprothèse, par voie artérielle transcutanée |
| EDPF004 | Recanalisation d'une artère digestive avec pose d'endoprothèse, par voie artérielle transcutanée |
| EDPF005 | Recanalisation de l'artère rénale avec pose d'endoprothèse, par voie artérielle transcutanée |
| EDPF006 | Recanalisation de l'artère iliaque commune et/ou de l'artère iliaque externe avec pose d'endoprothèse couverte, par voie artérielle transcutanée |
| EDPF007 | Recanalisation de l'artère iliaque interne sans pose d'endoprothèse, par voie artérielle transcutanée |
| EDPF008 | Recanalisation de l'artère iliaque commune et/ou de l'artère iliaque externe sans pose d'endoprothèse, par voie artérielle transcutanée |
| EDPF009 | Recanalisation de l'artère iliaque commune et/ou de l'artère iliaque externe avec pose d'endoprothèse, par voie artérielle transcutanée |
| EDQH001 | Artériographie suprasélective de branche extradigestive de l'aorte abdominale ou de branche de l'artère iliaque interne, par voie artérielle transcutanée |
| EDQH003 | Artériographie sélective ou hypersélective d'une branche extradigestive de l'aorte abdominale ou d'une branche de l'artère iliaque interne, par voie artérielle transcutanée |
| EDQH005 | Artériographie sélective et/ou hypersélective de plusieurs branches extradigestives de l'aorte abdominale ou de plusieurs branches de l'artère iliaque interne, par voie artérielle transcutanée |
| EDQH006 | Artériographie sélective et/ou hypersélective de plusieurs branches digestives de l'aorte abdominale, par voie artérielle transcutanée |
| EDQH007 | Artériographie suprasélective de branche digestive de l'aorte abdominale, par voie artérielle transcutanée |
| EDQH008 | Artériographie sélective ou hypersélective d'une branche digestive de l'aorte abdominale, par voie artérielle transcutanée |
| EDSF001 | Oblitération suprasélective de plusieurs anévrismes sacculaires d'artère digestive, par voie artérielle transcutanée |
| EDSF002 | Oblitération sélective ou hypersélective d'un anévrisme sacculaire de l'artère iliaque interne ou d'une branche extradigestive de l'aorte abdominale, par voie artérielle transcutanée |
| EDSF003 | Embolisation sélective ou hypersélective de l'artère rénale, par voie artérielle transcutanée |
| EDSF004 | Embolisation suprasélective de branche de l'artère iliaque interne ou de branche extradigestive de l'aorte abdominale, par voie artérielle transcutanée |
| EDSF005 | Embolisation sélective ou hypersélective d'une artère digestive, par voie artérielle transcutanée |
| EDSF006 | Embolisation suprasélective d'une artère digestive, par voie artérielle transcutanée |
| EDSF007 | Oblitération sélective ou hypersélective d'un anévrisme sacculaire de l'artère rénale, par voie artérielle transcutanée |
| EDSF008 | Embolisation suprasélective de l'artère rénale, par voie artérielle transcutanée |
| EDSF009 | Oblitération suprasélective d'un anévrisme sacculaire d'une artère digestive, par voie artérielle transcutanée |
| EDSF010 | Oblitération suprasélective d'un anévrisme sacculaire de l'artère iliaque interne ou d'une branche extradigestive de l'aorte abdominale, par voie artérielle transcutanée |
| EDSF011 | Embolisation des artères iliaques internes [hypogastriques] et/ou de ses branches pour hémorragie du post-partum, par voie artérielle transcutanée |
| EDSF012 | Embolisation sélective et/ou hypersélective de plusieurs artères digestives, par voie artérielle transcutanée |
| EDSF013 | Oblitération suprasélective d'un anévrisme sacculaire de l'artère rénale, par voie artérielle transcutanée |
| EDSF014 | Embolisation sélective et/ou hypersélective de plusieurs branches de l'artère iliaque interne ou de plusieurs branches extradigestives de l'aorte abdominale, par voie artérielle transcutanée |
| EDSF015 | Embolisation suprasélective de plusieurs artères digestives, par voie artérielle transcutanée |
| EDSF016 | Embolisation sélective ou hypersélective de l'artère iliaque interne ou d'une branche extradigestive de l'aorte abdominale, par voie artérielle transcutanée |
| EEAF001 | Dilatation intraluminale de plusieurs artères du membre inférieur sans pose d'endoprothèse, par voie artérielle transcutanée |
| EEAF002 | Dilatation intraluminale d'une artère du membre inférieur avec dilatation intraluminale de l'artère iliaque commune et/ou de l'artère iliaque externe homolatérale avec pose d'endoprothèse, par voie artérielle transcutanée |
| EEAF003 | Dilatation intraluminale d'une artère du membre inférieur sans pose d'endoprothèse, par voie artérielle transcutanée |
| EEAF004 | Dilatation intraluminale d'une artère du membre inférieur avec pose d'endoprothèse, par voie artérielle transcutanée |
| EEAF005 | Dilatation intraluminale d'une artère du membre inférieur avec dilatation intraluminale de l'artère iliaque commune et/ou de l'artère iliaque externe homolatérale sans pose d'endoprothèse, par voie artérielle transcutanée |
| EEAF006 | Dilatation intraluminale de plusieurs artères du membre inférieur avec pose d'endoprothèse, par voie artérielle transcutanée |
| EEJF001 | Thromboaspiration d'artère ou de pontage artériel du membre inférieur, par voie artérielle transcutanée |
| EELF002 | Pose d'endoprothèse couverte dans une artère du membre inférieur, par voie artérielle transcutanée |
| EELF004 | Injection intraartérielle in situ suprasélective d'agent pharmacologique anticancéreux au membre inférieur, par voie artérielle transcutanée |
| EELF005 | Injection intraartérielle in situ sélective ou hypersélective d'agent pharmacologique anticancéreux au membre inférieur, par voie artérielle transcutanée |
| EENF001 | Fibrinolyse in situ suprasélective d'une artère ou d'un pontage artériel du membre inférieur, par voie artérielle transcutanée |
| EENF002 | Fibrinolyse in situ sélective ou hypersélective d'une artère ou d'un pontage artériel du membre inférieur, par voie artérielle transcutanée |
| EEPF001 | Recanalisation d'une artère du membre inférieur avec pose d'endoprothèse, par voie artérielle transcutanée |
| EEPF002 | Recanalisation d'une artère du membre inférieur sans pose d'endoprothèse, par voie artérielle transcutanée |
| EEQH001 | Artériographie bilatérale de membre inférieur, par injection intraartérielle fémorale transcutanée bilatérale |
| EEQH002 | Artériographie sélective ou hypersélective du membre inférieur, par voie artérielle transcutanée |
| EEQH003 | Artériographie du pied, par injection intraartérielle ou voie artérielle transcutanée |
| EEQH004 | Artériographie suprasélective du membre inférieur, par voie artérielle transcutanée |
| EEQH005 | Artériographie globale du membre inférieur, par voie artérielle transcutanée |
| EEQH006 | Artériographie unilatérale du membre inférieur, par injection intraartérielle fémorale transcutanée |
| EESF001 | Oblitération d'un anévrisme sacculaire artériel du membre inférieur, par voie artérielle transcutanée |
| EESF004 | Embolisation hypersélective de plusieurs artères du membre inférieur, par voie artérielle transcutanée |
| EESF005 | Oblitération de plusieurs anévrismes sacculaires artériels du membre inférieur, par voie artérielle transcutanée |
| EESF006 | Embolisation suprasélective d'une artère du membre inférieur, par voie artérielle transcutanée |
| EESF007 | Embolisation sélective ou hypersélective d'une artère du membre inférieur, par voie artérielle transcutanée |
| EFAF001 | Dilatation intraluminale d'une veine du membre supérieur avec pose d'endoprothèse, par voie veineuse transcutanée |
| EFAF002 | Dilatation intraluminale d'une veine du membre supérieur sans pose d'endoprothèse, par voie veineuse transcutanée |
| EFJF001 | Thromboaspiration de la veine subclavière et/ou de la veine brachiocéphalique, par voie veineuse transcutanée |
| EFLF001 | Pose d'endoprothèse couverte dans une veine du membre supérieur, par voie veineuse transcutanée |
| EFNF001 | Fibrinolyse in situ de la veine subclavière et/ou de la veine brachiocéphalique, par voie veineuse transcutanée |
| EFPF001 | Recanalisation d'une veine du membre supérieur avec pose d'endoprothèse, par voie veineuse transcutanée |
| EFPF002 | Recanalisation d'une veine du membre supérieur sans pose d'endoprothèse, par voie veineuse transcutanée |
| EFQH001 | Phlébographie sélective du membre supérieur par voie veineuse transcutanée, sans étude des troncs veineux proximaux |
| EFQH002 | Phlébographie sélective de la veine brachiocéphalique ou de la veine cave supérieure, par voie veineuse transcutanée |
| EFQH003 | Phlébographie bilatérale du membre supérieur par injection intraveineuse transcutanée, avec étude des troncs veineux proximaux et de la veine cave supérieure |
| EFQH004 | Phlébographie bilatérale du membre supérieur par injection intraveineuse transcutanée, sans étude des troncs veineux proximaux |
| EFQH005 | Phlébographie unilatérale du membre supérieur par injection intraveineuse ou voie veineuse transcutanée, avec étude des troncs veineux proximaux et de la veine cave supérieure |
| EFQH006 | Phlébographie unilatérale du membre supérieur par injection intraveineuse transcutanée, sans étude des troncs veineux proximaux |
| EFQH007 | Phlébographie hypersélective de la veine brachiocéphalique ou de la veine cave supérieure, par voie veineuse transcutanée |
| EGAF001 | Dilatation intraluminale de la veine rénale sans pose d'endoprothèse, par voie veineuse transcutanée |
| EGAF002 | Dilatation intraluminale de la veine iliaque externe et/ou de la veine iliaque commune avec pose d'endoprothèse, par voie veineuse transcutanée |
| EGAF003 | Dilatation intraluminale de la veine iliaque externe et/ou de la veine iliaque commune sans pose d'endoprothèse, par voie veineuse transcutanée |
| EGAF004 | Dilatation intraluminale de la veine rénale avec pose d'endoprothèse, par voie veineuse transcutanée |
| EGJF001 | Thromboaspiration de la veine rénale, par voie veineuse transcutanée |
| EGJF002 | Thromboaspiration de la veine iliaque externe et/ou de la veine iliaque commune, par voie veineuse transcutanée |
| EGNF001 | Fibrinolyse in situ de la veine rénale, par voie veineuse transcutanée |
| EGNF002 | Fibrinolyse in situ de la veine iliaque externe et/ou de la veine iliaque commune, par voie veineuse transcutanée |
| EGPF001 | Recanalisation de la veine iliaque externe et/ou de la veine iliaque commune avec pose d'endoprothèse, par voie veineuse transcutanée |
| EGSF001 | Embolisation suprasélective de la veine testiculaire ou ovarique, par voie veineuse transcutanée |
| EGSF002 | Embolisation sélective ou hypersélective de la veine testiculaire ou ovarique, par voie veineuse transcutanée |
| EGSF003 | Embolisation des veines de drainage du pénis, par injection intraveineuse transcutanée |
| EHAF001 | Dilatation intraluminale de la veine porte ou d'une anastomose portocave avec pose d'endoprothèse, par voie veineuse transcutanée |
| EHAF002 | Dilatation intraluminale de la veine porte ou d'une anastomose portocave sans pose d'endoprothèse, par voie veineuse transcutanée |
| EHAF003 | Dilatation intraluminale de veine hépatique [veine sushépatique] sans pose d'endoprothèse, par voie veineuse transcutanée |
| EHAF004 | Dilatation intraluminale d'une endoprothèse vasculaire intrahépatique pour court-circuit [shunt] vasculaire portosystémique, par voie veineuse transcutanée |
| EHCF002 | Création d'un court-circuit [shunt] portosystémique intrahépatique par pose d'endoprothèse, par voie veineuse transcutanée |
| EHNF001 | Fibrinolyse in situ de la veine porte et/ou de ses affluents ou d'un court-circuit [shunt] vasculaire portosystémique, par voie veineuse transcutanée |
| EHPF001 | Recanalisation d'un court-circuit [shunt] vasculaire portosystémique, par voie veineuse transcutanée |
| EHQH001 | Phlébographie sélective de veine hépatique [sushépatique], par voie veineuse transcutanée |
| EHSF001 | Embolisation de varices œsogastriques ou des branches intrahépatiques de la veine porte, par voie veineuse transcutanée ou transpariétohépatique |
| EJQH001 | Varicographie du membre inférieur, par injection intraveineuse transcutanée |
| EJQH002 | Phlébographie bilatérale du membre inférieur par injection intraveineuse transcutanée au pied, avec iliocavographie par injection intraveineuse transcutanée fémorale bilatérale |
| EJQH003 | Phlébographie rétrograde du membre inférieur, par injection intraveineuse transcutanée fémorale homolatérale ou par voie veineuse fémorale controlatérale |
| EJQH004 | Phlébographie bilatérale du membre inférieur, par injection intraveineuse transcutanée au pied |
| EJQH005 | Phlébographie rétrograde du membre inférieur, par injection intraveineuse transcutanée poplitée |
| EJQH006 | Phlébographie unilatérale du membre inférieur, par injection intraveineuse transcutanée au pied |
| EJSF900 | Occlusion de veine saphène par laser, par voie veineuse transcutanée |
| EJSF901 | Occlusion de la grande veine saphène par radiofréquence, par voie veineuse transcutanée |
| EKQH002 | Angiographie d'un accès vasculaire artérioveineux du membre supérieur avec exploration des troncs veineux profonds proximaux et de la veine cave supérieure, par injection intravasculaire transcutanée |
| ELSF001 | Embolisation d'une fistule artérioveineuse rénale, par voie vasculaire transcutanée |
| ENAF001 | Dilatation intraluminale d'un pontage artériel non anatomique des membres avec pose d'endoprothèse, par voie artérielle transcutanée |
| ENAF002 | Dilatation intraluminale d'un pontage artériel non anatomique des membres sans pose d'endoprothèse, par voie artérielle transcutanée |
| ENFF001 | Thrombectomie ou embolectomie mécanique d'un pontage artériel non anatomique des membres, par voie artérielle transcutanée |
| ENNF001 | Fibrinolyse in situ d'un pontage artériel non anatomique des membres, par voie artérielle transcutanée |
| ENSF001 | Embolisation d'une malformation vasculaire ou d'une lésion vertébrale, par voie vasculaire transcutanée |
| ENSF002 | Embolisation de malformation artérioveineuse intraparenchymateuse de la moelle épinière, par voie vasculaire transcutanée |
| ENSF003 | Embolisation de malformation artérioveineuse durale spinale, par voie vasculaire transcutanée |
| EQQH001 | Mesure et enregistrement des pressions du cœur droit et de l'artère pulmonaire, avec injection de produit de contraste, par voie veineuse transcutanée |
| EQQH002 | Mesure et enregistrement des pressions du cœur gauche et de l'aorte, avec injection de produit de contraste, par voie artérielle transcutanée |
| EQQH004 | Mesure et enregistrement des pressions du cœur droit, de l'artère pulmonaire et du cœur gauche, avec injection de produit de contraste, par voie veineuse transcutanée avec perforation du septum interatrial |
| EQQH005 | Mesure et enregistrement des pressions du cœur droit, de l'artère pulmonaire et du cœur gauche, avec injection de produit de contraste, par voie veineuse transcutanée et par voie artérielle transcutanée ou cathétérisme du foramen ovale, avant l'âge |
| EQQH006 | Mesure et enregistrement des pressions du cœur droit, de l'artère pulmonaire et du cœur gauche, avec injection de produit de contraste, par voie veineuse transcutanée et par voie artérielle transcutanée ou cathétérisme du foramen ovale, à l'âge de |
| EZAF001 | Dilatation intraluminale d'un accès vasculaire artérioveineux d'un membre sans pose d'endoprothèse, par voie vasculaire transcutanée |
| EZAF002 | Dilatation intraluminale d'un accès vasculaire artérioveineux d'un membre avec pose d'endoprothèse, par voie vasculaire transcutanée |
| EZGF001 | Ablation d'une endoprothèse vasculaire ou d'un filtre cave ayant migré en position intracardiaque ou intravasculaire, par voie vasculaire transcutanée |
| EZJF001 | Thromboaspiration d'un accès vasculaire artérioveineux d'un membre avec dilatation intraluminale et pose d'endoprothèse, par voie vasculaire transcutanée |
| EZJF002 | Thromboaspiration d'un accès vasculaire artérioveineux d'un membre avec dilatation intraluminale sans pose d'endoprothèse, par voie vasculaire transcutanée |
| EZNF001 | Fibrinolyse in situ d'un accès vasculaire artérioveineux d'un membre avec dilatation intraluminale sans pose d'endoprothèse, par voie vasculaire transcutanée |
| EZNF002 | Fibrinolyse in situ d'un accès vasculaire artérioveineux d'un membre avec dilatation intraluminale et pose d'endoprothèse, par voie vasculaire transcutanée |
| EZNF004 | Fibrinolyse in situ d'un accès vasculaire artérioveineux des membres, par injection intravasculaire transcutanée |
| EZNF900 | Irradiation intravasculaire, au décours d'une dilatation de vaisseau par voie vasculaire transcutanée |
| EZPF003 | Désobstruction mécanique d'un accès vasculaire artérioveineux avec dilatation intraluminale et pose d'endoprothèse, par voie vasculaire transcutanée |
| EZPF004 | Désobstruction mécanique d'un accès vasculaire artérioveineux avec dilatation intraluminale sans pose d'endoprothèse, par voie vasculaire transcutanée |
| EZQH002 | Angiographie d'un accès vasculaire artérioveineux d'un membre, par voie vasculaire transcutanée |
| EZQH003 | Angiographie d'un accès vasculaire artérioveineux d'un membre, par injection intravasculaire transcutanée |
.
Appendix 2
Table 5.
Caption of codes used in methods (CCAM codes are in original French)
| Classification | Codes | Caption |
|---|---|---|
| CIM-10 | E10* | Insulin-dependent diabetes mellitus |
| E11* | Non-insulin-dependent diabetes mellitus | |
| E12* | Malnutrition-related diabetes mellitus | |
| E13* | Other specified diabetes mellitus | |
| E14* | Unspecified diabetes mellitus | |
| I50* | Heart failure | |
| N08.3 | Glomerular disorders in diabetes mellitus | |
| N14.1 | Nephropathy induced by other drugs, medicaments and biological substances) | |
| N14.2 | Nephropathy Induced By Unspecified Drug, Medicament Or Biological Substance | |
| N14.4 | Toxic nephropathy, not elsewhere classified | |
| N18* | Chronic kidney disease | |
| N18.5 | Chronic kidney disease, stage 5 | |
| N99.0 | Diagnosis - Postprocedural (Acute) (Chronic) Kidney Failure | |
| N17* | Acute Kidney Failure | |
| N19 | Unspecified Acute Kidney Failure | |
| R39.2 | Extrarenal uremia | |
| R57.0 | Cardiogenic Shock | |
| Z99.2* | Dependence on renal dialysis | |
| CCAM | JVJB001 | Séance d'épuration extrarénale par dialyse péritonéale pour insuffisance rénale chronique |
| JVJF002 | Épuration extrarénale par hémodialyse, hémodiafiltration ou hémofiltration discontinue pour insuffisance rénale aigüe, par 24 heures | |
| JVJF003 | Séance d'épuration extrarénale par hémoperfusion | |
| JVJF004 | Séance d'épuration extrarénale par hémodialyse pour insuffisance rénale chronique | |
| JVJF005 | Épuration extrarénale par hémodialyse, hémodiafiltration ou hémofiltration continue pour insuffisance rénale aigüe, par 24 heures | |
| JVJF008 | Séance d'épuration extrarénale par hémodiafiltration, hémofiltration ou biofiltration sans acétate pour insuffisance rénale chronique |
References
- 1.French Society of Radiology . Interventional radiology in France. 2011. [Google Scholar]
- 2.Nash K, Hafeez A, Hou S. Hospital-acquired renal insufficiency. Am J Kidney Dis Off J Natl Kidney Found. 2002;39:930–936. doi: 10.1053/ajkd.2002.32766. [DOI] [PubMed] [Google Scholar]
- 3.Song W, Zhang T, Pu J, Shen L, He B. Incidence and risk of developing contrast-induced acute kidney injury following intravascular contrast administration in elderly patients. Clin Interv Aging. 2014;9:85–93. doi: 10.2147/CIA.S55157. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 4.Moos SI, van Vemde DNH, Stoker J, Bipat S. Contrast induced nephropathy in patients undergoing intravenous (IV) contrast enhanced computed tomography (CECT) and the relationship with risk factors: a meta-analysis. Eur J Radiol. 2013;82:e387–399. doi: 10.1016/j.ejrad.2013.04.029. [DOI] [PubMed] [Google Scholar]
- 5.Garcia S, Ko B, Adabag S. Contrast-induced nephropathy and risk of acute kidney injury and mortality after cardiac operations. Ann Thorac Surg. 2012;94:772–776. doi: 10.1016/j.athoracsur.2012.04.089. [DOI] [PubMed] [Google Scholar]
- 6.Sharma J, Nanda A, Jung RS, Mehta S, Pooria J, Hsu DP. Risk of contrast-induced nephropathy in patients undergoing endovascular treatment of acute ischemic stroke. J Neurointerventional Surg. 2013;5:543–545. doi: 10.1136/neurintsurg-2012-010520. [DOI] [PubMed] [Google Scholar]
- 7.Lencioni R, Fattori R, Morana G, Stacul F. Contrast-induced nephropathy in patients undergoing computed tomography (CONNECT) - a clinical problem in daily practice? A multicenter observational study. Acta Radiol Stockh Swed. 2010;51:741–750. doi: 10.3109/02841851.2010.495350. [DOI] [PubMed] [Google Scholar]
- 8.Murphy SW, Barrett BJ, Parfrey PS. Contrast nephropathy. J Am Soc Nephrol JASN. 2000;11:177–182. doi: 10.1681/ASN.V111177. [DOI] [PubMed] [Google Scholar]
- 9.McCullough PA, Wolyn R, Rocher LL, Levin RN, O’Neill WW. Acute renal failure after coronary intervention: incidence, risk factors, and relationship to mortality. Am J Med. 1997;103:368–375. doi: 10.1016/S0002-9343(97)00150-2. [DOI] [PubMed] [Google Scholar]
- 10.Gruberg L, Mintz GS, Mehran R, Gangas G, Lansky AJ, Kent KM, Pichard AD, Satler LF, Leon MB. The prognostic implications of further renal function deterioration within 48 h of interventional coronary procedures in patients with pre-existent chronic renal insufficiency. J Am Coll Cardiol. 2000;36:1542–1548. doi: 10.1016/S0735-1097(00)00917-7. [DOI] [PubMed] [Google Scholar]
- 11.Mangano CM, Diamondstone LS, Ramsay JG, Aggarwal A, Herskowitz A, Mangano DT. Renal dysfunction after myocardial revascularization: risk factors, adverse outcomes, and hospital resource utilization. The Multicenter Study of Perioperative Ischemia Research Group. Ann Intern Med. 1998;128:194–203. doi: 10.7326/0003-4819-128-3-199802010-00005. [DOI] [PubMed] [Google Scholar]
- 12.McCullough PA. Beyond serum creatinine: defining the patient with renal insufficiency and why? Rev Cardiovasc Med. 2003;4(Suppl 1):S2–6. [PubMed] [Google Scholar]
- 13.Rihal CS, Textor SC, Grill DE, Berger PB, Ting HH, Best PJ, Singh M, Bell MR, Barsness GW, Mathew V, Garratt KN, Holmes DR. Incidence and prognostic importance of acute renal failure after percutaneous coronary intervention. Circulation. 2002;105:2259–2264. doi: 10.1161/01.CIR.0000016043.87291.33. [DOI] [PubMed] [Google Scholar]
- 14.Gruberg L, Mehran R, Dangas G, Mintz GS, Waksman R, Kent KM, Pichard AD, Satler LF, Wu H, Leon MB. Acute renal failure requiring dialysis after percutaneous coronary interventions. Catheter Cardiovasc Interv Off J Soc Card Angiogr Interv. 2001;52:409–416. doi: 10.1002/ccd.1093. [DOI] [PubMed] [Google Scholar]
- 15.Gruberg L, Dangas G, Mehran R, Mintz GS, Kent KM, Pichard AD, Satler LF, Lansky AJ, Stone GW, Leon MB. Clinical outcome following percutaneous coronary interventions in patients with chronic renal failure. Catheter Cardiovasc Interv Off J Soc Card Angiogr Interv. 2002;55:66–72. doi: 10.1002/ccd.10103. [DOI] [PubMed] [Google Scholar]
- 16.Valette X, Parienti J-J, Plaud B, Lehoux P, Samba D, Hanouz J-L. Incidence, morbidity, and mortality of contrast-induced acute kidney injury in a surgical intensive care unit: a prospective cohort study. J Crit Care. 2012;27:322.e1-5. doi: 10.1016/j.jcrc.2011.08.005. [DOI] [PubMed] [Google Scholar]
- 17.Lakhal K, Ehrmann S, Chaari A, Laissy J-P, Régnier B, Wolff M, Pajot O. Acute Kidney Injury Network definition of contrast-induced nephropathy in the critically ill: incidence and outcome. J Crit Care. 2011;26:593–599. doi: 10.1016/j.jcrc.2011.05.010. [DOI] [PubMed] [Google Scholar]
- 18.Morabito S, Pistolesi V, Benedetti G, Di Roma A, Colantonio R, Mancone M, Sardella G, Cibelli L, Ambrosino M, Polistena F, Pierucci A. Incidence of contrast-induced acute kidney injury associated with diagnostic or interventional coronary angiography. J Nephrol. 2012;25:1098–1107. doi: 10.5301/jn.5000101. [DOI] [PubMed] [Google Scholar]
- 19.Mitchell AM, Jones AE, Tumlin JA, Kline JA. Incidence of contrast-induced nephropathy after contrast-enhanced computed tomography in the outpatient setting. Clin J Am Soc Nephrol. 2010;5:4–9. doi: 10.2215/CJN.05200709. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 20.Freeman RV, O’Donnell M, Share D, Meengs WL, Kline-Rogers E, Clark VL, DeFranco AC, Eagle KA, McGinnity JG, Patel K, Maxwell-Eward A, Bondie D, Moscucci M, Blue Cross-Blue Shield of Michigan Cardiovascular Consortium (BMC2) Nephropathy requiring dialysis after percutaneous coronary intervention and the critical role of an adjusted contrast dose. Am J Cardiol. 2002;90:1068–1073. doi: 10.1016/S0002-9149(02)02771-6. [DOI] [PubMed] [Google Scholar]
- 21.Levy EM, Viscoli CM, Horwitz RI. The effect of acute renal failure on mortality. A cohort analysis. JAMA. 1996;275:1489–1494. doi: 10.1001/jama.1996.03530430033035. [DOI] [PubMed] [Google Scholar]
- 22.Mehran R, Aymong ED, Nikolsky E, Lasic Z, Iakovou I, Fahy M, Mintz GS, Lansky AJ, Moses JW, Stone GW, Leon MB, Dangas G. A simple risk score for prediction of contrast-induced nephropathy after percutaneous coronary intervention: development and initial validation. J Am Coll Cardiol. 2004;44:1393–1399. doi: 10.1016/j.jacc.2004.06.068. [DOI] [PubMed] [Google Scholar]
- 23.Subramanian S, Tumlin J, Bapat B, Zyczynski T. Economic burden of contrast-induced nephropathy: implications for prevention strategies. J Med Econ. 2007;10:119–134. doi: 10.3111/200710119134. [DOI] [PubMed] [Google Scholar]
- 24.Bossard N, Gomez F, Remontet L, Uhry Z, Olive F, Mitton N, Polazzi S, Schott A-M, Trombert B, Colonna M. Using data from the French hospital database (PMSI) to estimate district-specific cancer incidence: the ONCEPI group approach. Bull Epidémiologique Hebd. 2012;5–6:77–80. [Google Scholar]
- 25.Ehrmann S, Pajot O, Lakhal K. Néphropathie induite par les produits de contraste iodés en réanimation. Réanimation. 2011;21:463–473. doi: 10.1007/s13546-011-0434-9. [DOI] [Google Scholar]
- 26.Stacul F, van der Molen AJ, Reimer P, Webb JAW, Thomsen HS, Morcos SK, Almén T, Aspelin P, Bellin M-F, Clement O, Heinz-Peer G, Contrast Media Safety Committee of European Society of Urogenital Radiology (ESUR) Contrast induced nephropathy: updated ESUR Contrast Media Safety Committee guidelines. Eur Radiol. 2011;21:2527–2541. doi: 10.1007/s00330-011-2225-0. [DOI] [PubMed] [Google Scholar]
- 27.Mehta RL, Kellum JA, Shah SV, Molitoris BA, Ronco C, Warnock DG, Levin A, Acute Kidney Injury Network Acute Kidney Injury Network: report of an initiative to improve outcomes in acute kidney injury. Crit Care Lond Engl. 2007;11:R31. doi: 10.1186/cc5713. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 28.Section 4: Contrast-induced AKI. Kidney Int Suppl. 2012;2:69–88. [DOI] [PMC free article] [PubMed]
Associated Data
This section collects any data citations, data availability statements, or supplementary materials included in this article.
Data Availability Statement
All information supporting the conclusions of this manuscript is included within the article. Any additional information can be obtained upon request.


