Resumen
Objetivos
a) Valorar la aplicabilidad de una consulta de alta resolución (CAR) para el diagnóstico de pacientes ambulatorios con insuficiencia cardíaca (IC) de inicio; b) caracterizar a los pacientes con IC y fracción de eyección preservada (ICFE-P) comparados con los de fracción de eyección reducida (ICFE-R), y c) determinar el nivel de péptido natriurético tipo B (PNB) para identificar la IC en esta población.
Diseño
Estudio longitudinal observacional descriptivo.
Emplazamiento
Atención primaria especializada.
Participantes y mediciones
Ciento cuarenta y tres pacientes con síntomas iniciales de IC fueron incluidos en una CAR-IC con evaluación clínica, electrocardiograma, radiografía de tórax, PNB y ecocardiograma.
Resultados
Se diagnosticó IC en 65,7% de los pacientes: 67% ICFE-P y 33% ICFE-R. La mayoría de pacientes con ICFE-P eran mujeres (71,4 versus 38,7%; p = 0,002), con más edemas maleolares (61,9% versus 35,5%; p = 0,016) e índice de masa corporal (29,8 ± 5,1 versus 27,2 ± 5,0; p = 0,021). Ambos presentaron signos ecocardiográficos de disfunción diastólica e hipertensión pulmonar, con PNB (153,3 ± 123,1 versus 400,8 ± 579,8; p = 0,025) y troponina I (0,024 ± 0,019 versus 0,071 ± 0,12; p = 0,037) más elevados en ICFE-R. Resultaron predictores de ICFE-P el sexo femenino y los edemas maleolares, mientras que la onda Q, los valores elevados de PNB y la frecuencia cardíaca lo fueron de ICFE-R. El punto de corte de PNB = 60,12 pg/ml identificó IC con sensibilidad del 83% y especificidad del 84% (ABC = 0,898; IC 95% [0,848-0,948]; p < 0,001).
Conclusiones
La CAR-IC permitió el diagnóstico rápido y la caracterización de la IC de inicio, con mayor prevalencia de ICFE-P, en pacientes ambulatorios. El valor de PNB 60,12 pg/ml ofreció una sensibilidad y especificidad elevadas para identificar la IC en esta población.
Palabras clave: Insuficiencia cardíaca, Fracción de eyección, Ecocardiograma, Péptido natriurético tipo B, Consulta de alta resolución, Atención primaria
Abstract
Objectives
a) To assess the usefulness of a one-stop clinic for the diagnosis of outpatients with new onset heart failure; b) to characterize these patients comparing preserved (HF-PEF) versus reduced ejection fraction (HF-REF), and c) to determine brain natriuretic peptide (BNP) cut-off limit to identify HF in outpatients.
Design
Observational descriptive study.
Setting
Primary care.
Participants and measurements
A total of 143 outpatients with new onset HF were assessed in a one-stop clinic. A cardiologist evaluation, electrocardiogram, chest X-ray, BNP, and echocardiography (diastolic and systolic study) were performed.
Results
Almost two-thirds (65.7%) were diagnosed with HF: 67% with HF-PEF and 33% HF-REF. Women (71.4% versus 38.7%, P = .002), presence of swelling ankles (61.9% versus 35.5%, P = .016) and higher body mass index (29.8 ± 5.1 versus 27.2 ± 5.0 P = .021) were more frequent in the first group of patients. Echocardiographic signs of diastolic dysfunction and pulmonary hypertension were found in both groups, with higher values of BNP (153.3 ± 123.1 versus 400.8 ± 579.8 P = .025) and troponin I (0.024 ± 0.019 versus 0.071 ± 0.12, P = .037) in HF-REF patients. Female gender and swelling ankles were predictors of HF-PEF in the multivariate analysis, while Q waves and higher values of BNP and heart rate were predictors of HF-REF. A cut-off value of 60.12 pg/ml for BNP provided 83% sensitivity, 84% specificity (AUC = 0.898; 95% CI; 0.848-0.948; P <.001).
Conclusions
The one-stop HF clinic has diagnosed and characterized outpatients with new onset HF and high prevalence of HF-PEF. The cut-off value of 60.12 pg/ml for BNP provides high sensitivity and specificity to identify HF in this population.
Keywords: Heart failure, Ejection fraction, Echocardiogram, Brain natriuretic peptide, One-stop clinic, Primary care
Introducción
La insuficiencia cardíaca (IC) es un problema de salud muy prevalente en las consultas de atención primaria y causa una elevada morbimortalidad, ingresos hospitalarios, disminuye la calidad de vida e incrementa el gasto sanitario1, 2. El conocimiento sobre esta enfermedad se sustenta fundamentalmente en estudios efectuados en pacientes que ya han presentado ingresos hospitalarios. En los pacientes con síntomas iniciales que consultan ambulatoriamente, la IC está infradiagnosticada, al afectar frecuentemente a población de edad avanzada, con pluripatología que dificulta la interpretación de la sintomatología, y presentarse en una elevada proporción con fracción de eyección ventricular izquierda (FEVI) preservada3, 4.
La IC con FEVI preservada (ICFE-P) se define como la existencia de una semiología clínica compatible, hallazgos ecocardiográficos de FEVI superior al 50%, junto a alteraciones de la función diastólica y/o elevación de los niveles séricos de péptidos natriuréticos5. En atención primaria, el diagnóstico resulta difícil, por la falta de disponibilidad o el retraso de las exploraciones complementarias. Además, se desconocen los niveles de péptido natriurético tipo B (PNB) que pueden resultar útiles para el diagnóstico en los pacientes en los que se inicia de forma ambulatoria.
Modelos asistenciales como la integración de la atención especializada en el equipo de primaria o las consultas de alta resolución, que permiten la evaluación de los pacientes en una sola jornada6, 7, pueden ser útiles para el diagnóstico precoz, lo que permitiría una intervención multidisciplinaria temprana que podría modificar el curso clínico de la enfermedad y mejorar la calidad de vida de estos pacientes, incluidos los que presentan ICFE-P8, 9.
Los objetivos del estudio son: a) valorar la aplicabilidad de una consulta de alta resolución (CAR-IC), en un modelo de atención integrada en salud, para el diagnóstico de los pacientes con IC de debut en atención primaria; b) evaluar las características clínicas, bioquímicas y ecocardiográficas de los pacientes ambulatorios diagnosticados de ICFE-P comparados con los de IC con FEVI reducida (ICFE-R), y c) determinar el punto de corte de PNB para identificar la IC en esta población.
Material y métodos
En enero de 2008 se inició un modelo de asistencia integrada en el área de “Barcelona-Esquerra”, con la incorporación de un cardiólogo hospitalario en cada equipo de atención primaria6. Los pacientes ambulatorios con semiología indicativa de IC de inicio son derivados a la CAR-IC.
Se diseñó un estudio observacional longitudinal descriptivo de pacientes ambulatorios con semiología indicativa de IC de nueva aparición que fueron visitados en la CAR-IC entre abril de 2009 y diciembre de 2011. El estudio fue aprobado por el comité ético de investigación clínica del Hospital Clínic de Barcelona.
Población de estudio
Se incluyeron todos los pacientes consecutivos enviados a la CAR-IC en ese periodo que aceptaron y firmaron el consentimiento informado, y que no presentaron criterios de exclusión. Los criterios de exclusión fueron edad inferior a 18 años, comorbilidad con expectativa de vida inferior a un año, o imposibilidad para realizar el circuito diagnóstico.
La CAR-IC es una consulta en el hospital, de acto único para el diagnóstico ambulatorio rápido de la IC de inicio, cuyas características se presentan en la tabla 1.
Tabla 1.
Características de la consulta de alta resolución para el diagnóstico de la insuficiencia cardíaca
| Diagnóstico rápido y ambulatorio de la IC de reciente inicio en pacientes derivados desde atención primaria |
| Visita de acto único en el hospital |
|
Todas las exploraciones complementarias en un mismo día 1. Evaluación clínica por el cardiólogo 2. Electrocardiograma 3. Radiografía de tórax 4. Análisis completo con determinación de BNP 5. Ecocardiograma transtorácico: función sistólica y diastólica |
| Informe con resultados, orientación diagnóstica y terapéutica, dirigido al médico de familia |
| Seguimiento por el equipo de atención primaria y cardiólogo integrado en el centro de salud |
| Los pacientes diagnosticados de IC inician un programa de educación por enfermería |
BNP: péptido natriurético tipo B; IC: insuficiencia cardíaca.
Intervenciones
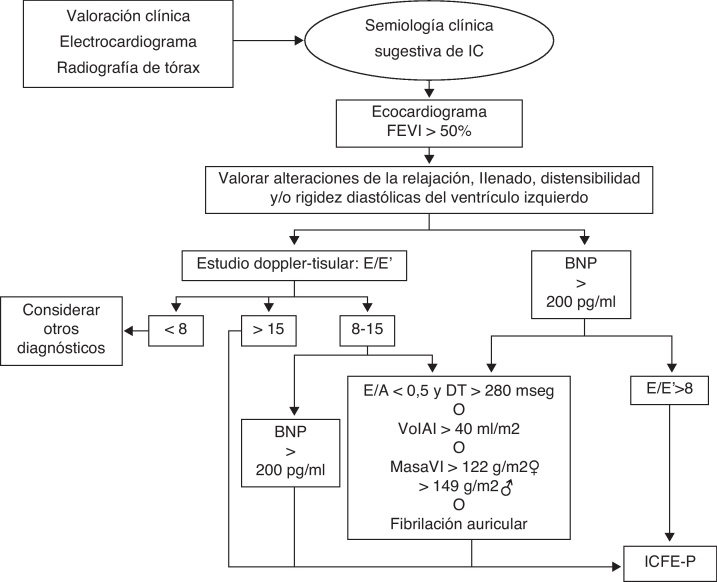
El diagnóstico de IC se realizó siguiendo las recomendaciones de la Sociedad Europea de Cardiología2. Los pacientes fueron diagnosticados de ICFE-R ante la coexistencia de una semiología compatible con IC más el hallazgo de disfunción sistólica en el ecocardiograma (FEVI inferior o igual al 50%). Cuando existía clínica compatible y la FEVI era superior al 50%, se aplicó el algoritmo adaptado de Paulus et al.5 para el diagnóstico de ICFE-P (fig. 1).
Figura 1.
Algoritmo diagnóstico de la ICFE-P. DT: tiempo de desaceleración de la válvula mitral; MasaVI: masa ventricular indexada por superficie corporal; VolAI: volumen de la aurícula izquierda indexado por superficie corporal. Adaptada de Paulus et al.5.
Dos cardiólogos desarrollaron la CAR-IC: evaluación clínica, interpretación del resultado de las exploraciones complementarias y asignación del diagnóstico definitivo, IC (ICFE-P o ICFE-R) o no IC. También elaboraron un informe y plan terapéutico para el equipo de atención primaria.
El estudio ecocardiográfico (Vivid 7, General Electric) constó de: FEVI y volúmenes del ventrículo izquierdo (VI) determinados por método Simpson biplanar, volumen de aurícula izquierda (VolAI), masa VI, velocidades precoz y tardía del llenado VI (E, A) y del anillo mitral lateral (E’, A’, Doppler tisular), tiempo de desaceleración del flujo de llenado precoz del VI, velocidades sistólica y diastólica del flujo de venas pulmonares, índice E/E’, estimación de la presión arterial pulmonar a partir de la velocidad pico de regurgitación tricuspídea. Dos ecocardiografistas, ciegos a la valoración del cardiólogo clínico, revisaron las imágenes y clasificaron el patrón diastólico en: normal (tipo 0), alteración de la relajación (tipo 1), seudonormal (tipo 2) y restrictivo (tipo 3).
La determinación de PNB se realizó en el Centro Diagnóstico Biomédico de nuestra institución utilizando el inmunoanálisis de quimioluminiscencia y autoanalizador ADVIA Centaur® PNB (Siemens Healthcare Diagnostics).
Análisis estadístico
Se realizó un análisis descriptivo y comparativo teniendo en cuenta los diferentes grupos diagnósticos: IC versus no IC, e ICFE-P versus ICFE-R. Se usó el paquete estadístico SPSS® versión 18.0. Las variables categóricas se expresaron en cifras absolutas y porcentajes, y el análisis comparativo se llevó a cabo con la prueba de χ2 o test de Fisher. Las variables cuantitativas se expresaron como media aritmética y desviación estándar, y se analizaron mediante la prueba t de Student para muestras independientes. Se realizó una regresión logística en la que se introdujeron todas las variables clínicas y bioquímicas con diferencias significativas en el análisis univariado al comparar ICFE-P versus ICFE-R y que clínicamente se consideraron relevantes, para calcular las odds ratio ajustadas con intervalo de confianza del 95% (IC 95%). Se calculó la curva COR para el diagnóstico de IC con los valores de PNB y el likelihood-ratio, definido como sensibilidad/(1-especificidad), para obtener el punto de corte, sensibilidad, especificidad, valores predictivos positivo y negativo. Los valores de p < 0,05 se consideraron estadísticamente significativos.
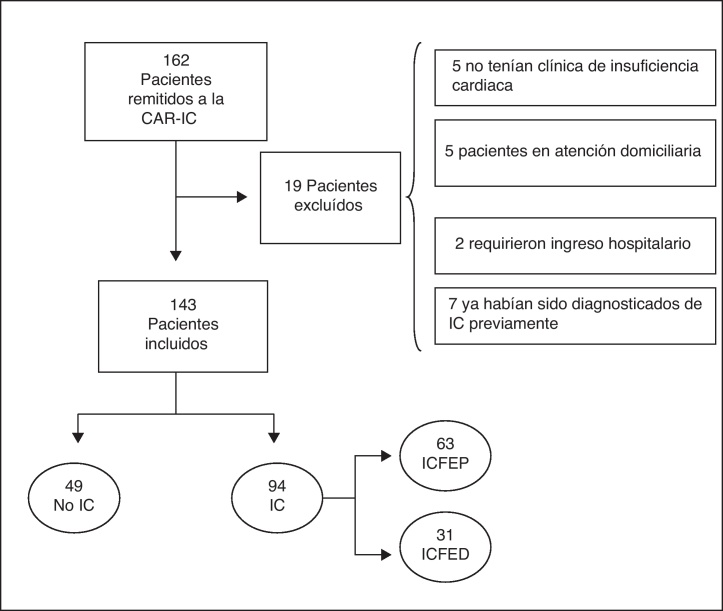
Esquema general del estudio: Diagrama de flujo de pacientes.
Resultados
Fueron enviados a la CAR-IC por su equipo de atención primaria 162 pacientes, de los que 143 cumplieron criterios de inclusión y no presentaron criterios de exclusión. El diagnóstico de IC se realizó en 94 pacientes (65,7%), de los cuales 63 (67,0%) fueron ICFE-P y 31 (33,0%) ICFE-R. El tiempo medio de espera para ser visitado fue 7 ± 3 días.
Los pacientes con IC tenían más antecedentes de hipertensión arterial y fibrilación auricular, sin diferencias entre ICFE-P o ICFE-R, así como un índice de comorbilidad Charlson superior e índice de masa corporal (IMC) inferior. Los pacientes con ICFE-P eran predominantemente mujeres, con más edemas maleolares y valores superiores de IMC y presión arterial sistólica respecto a los ICFE-R. Estos últimos eran mayoritariamente hombres, con antecedentes de tabaquismo y vasculopatía periférica, con tendencia a mayor comorbilidad (p = 0,05) y valores de frecuencia cardiaca más elevados (tabla 2).
Tabla 2.
Características clínicas de los pacientes según el diagnóstico final
| Variables | No IC (n = 49) | IC (n = 94) | p | ICFE-P (n = 63) | ICFE-R (n = 31) | p |
|---|---|---|---|---|---|---|
| Edad | 72,8 ± 8,7 | 75,7 ± 10,1 | 0,086 | 76,3 ± 8,7 | 74,5 ± 12,7 | 0,464 |
| Sexo femenino | 35 (71,4) | 57 (60,6) | 0,201 | 45 (71,4) | 12 (38,7) | 0,002* |
| Factores de riesgo cardiovascular y hábitos tóxicos | ||||||
| Hipertensión | 31 (63,3) | 76 (80,9) | 0,021* | 54 (85,7) | 22 (71) | 0,088 |
| Dislipidemia | 22 (44,9) | 43 (45,7) | 0,923 | 29 (46,0) | 14 (45,2) | 0,937 |
| Diabetes | 9 (18,4) | 24 (25,5) | 0,406 | 13 (20,6) | 11 (35,5) | 0,137 |
| Tabaquismo | 18 (36,7) | 36 (38,3) | 0,855 | 19 (30,2) | 17 (54,8) | 0,021* |
| Enolismo | 2 (4,1) | 12 (12,8) | 0,139 | 7 (11,1) | 5 (16,1) | 0,522 |
| Antecedentes patológicos | ||||||
| Neumopatía | 17 (34,7) | 26 (27,7) | 0,384 | 18 (28,6) | 8 (25,8) | 0,778 |
| Nefropatía | 2 (4,1) | 5 (5,3) | 1,000 | 2 (3,2) | 3 (9,7) | 0,327 |
| Fibrilación auricular | 4 (8,2) | 45 (47,9) | < 0,001* | 27 (42,9) | 18 (58,1) | 0,165 |
| ECV | 1 (2,0) | 10 (10,6) | 0,098 | 6 (9,5) | 4 (12,9) | 0,725 |
| Vasculopatía | 2 (4,1) | 8 (8,5) | 0,494 | 2 (3,2) | 6 (19,4) | 0,014* |
| Anemia Cr. | 7 (14,3) | 18 (19,1) | 0,467 | 11 (17,5) | 7 (22,6) | 0,553 |
| Depresión | 17 (34,7) | 32 (34,0) | 0,938 | 24 (38,1) | 8 (25,8) | 0,237 |
| Anamnesis y exploración física | ||||||
| Disnea CF | ||||||
| I-II | 46 (93,9) | 60 (63,8) | 40 (63,5) | 20 (64,5) | ||
| III-IV | 3 (6,1) | 34 (36,2) | < 0,001* | 23 (36,5) | 11 (35,5) | 0,923 |
| Crepitantes | 0 (0,0) | 28 (29,8) | < 0,001* | 19 (30,2) | 9 (29,0) | 0,911 |
| Edemas EEII | 6 (12,2) | 50 (53,2) | < 0,001* | 39 (61,9) | 11 (35,5) | 0,016* |
| Barthel | 98,5 ± 5 | 96,5 ± 9 | 0,087 | 96,8 ± 8,8 | 95,8 ± 9,6 | 0,610 |
| Charlson | 0,8 ± 0,9 | 1,9 ± 1,4 | <0,001* | 1,7 ± 1,3 | 2,3 ± 1,4 | 0,050 |
| IMC | 31,8 ± 4,3 | 28,9 ± 5,1 | 0,001* | 29,8 ± 5,1 | 27,2 ± 5,0 | 0,021* |
| PA sistólica | 137 ± 24 | 141 ± 24 | 0,299 | 145 ± 26 | 133 ± 17 | 0,005* |
| PA diastólica | 73 ± 11 | 74 ± 11 | 0,566 | 74 ± 11 | 75 ± 11 | 0,603 |
| FC (lpm) | 73 ± 11 | 73 ± 13 | 0,879 | 70 ± 12 | 79 ± 14 | 0,003* |
CF: clase funcional; Cr.: crónica; ECV: enfermedad cerebrovascular; EEII: extremidades inferiores; F;: fibrilación; FC: frecuencia cardíaca (expresada en latidos por minuto); IMC: índice de masa corporal; PA: presión arterial (expresada en mmHg).
Las variables cuantitativas se expresan como media ± desviación estándar y las variables cualitativas se expresan como recuento (porcentaje).
p estadísticamente significativa (< 0,05).
Los resultados de las exploraciones complementarias se indican en la tabla 3. Los hallazgos electrocardiográficos de fibrilación auricular, sobrecarga ventricular u onda Q de necrosis fueron más frecuentes en los pacientes diagnosticados de IC. Los pacientes con ICFE-R tenían mayor presencia de onda Q en el electrocardiograma y cardiomegalia en la radiografía de tórax respecto a aquellos con ICFE-P. La analítica mostró que los pacientes con IC tenían cifras más elevadas de PNB y troponina I ultrasensible, que fueron significativamente superiores en los pacientes ICFE-R, y mayor alteración de los parámetros de función renal.
Tabla 3.
Resultado de las exploraciones complementarias practicadas
| Variables | No IC (n = 49) | IC (n = 94) | p | ICFE-P (n = 63) | ICFE-R (n = 31) | p |
|---|---|---|---|---|---|---|
| Electrocardiograma | ||||||
| Fibrilación auricular | 2 (4,1) | 39 (41,5) | < 0,001* | 24 (38,1) | 15 (48,4) | 0,341 |
| BRIHH | 2 (4,1) | 12 (12,8) | 0,097 | 7 (11,1) | 5 (16,1) | 0,522 |
| Sobrecarga V. | 9 (18,4) | 52 (55,3) | < 0,001* | 31 (49,2) | 21 (67,7) | 0,089 |
| Onda Q | 3 (6,1) | 23 (24,5) | 0,007* | 10 (15,9) | 13 (41,9) | 0,006* |
| Radiografía de tórax | ||||||
| Cardiomegalia | 6 (12,2) | 53 (57,6) | < 0,001* | 29(47,5) | 24 (77,4) | 0,006* |
| Signos HTVC | 0 (0,0) | 51 (56) | <0,001* | 30 (50) | 21 (67,7) | 0,106 |
| Bioquímica | ||||||
| BNP (pg/ml) | 40,0 ± 26,1 | 234,9 ± 363,6 | <0,001* | 153,3 ± 123,1 | 400,8 ± 579,8 | 0,025* |
| FG (ml/min) | 57,9 ± 5,1 | 54,6 ± 9,3 | 0,008* | 54,29 ± 0,01 | 55,37 ± 7,64 | 0,603 |
| Hemoglobina (g/l) | 136,1 ± 14,0 | 132,4 ± 17,4 | 0,186 | 131,0 ± 16,5 | 135,0 ± 19,2 | 0,316 |
| Troponina I us. (ng/ml) | 0,017 ± 0,00 | 0,039 ± 0,073 | 0,004* | 0,024 ± 0,019 | 0,071 ± 0,12 | 0,037* |
| Albúmina (g/l) | 43,1 ± 2,3 | 41,3 ± 3,0 | < 0,001* | 41,3 ± 3,0 | 41,1 ± 2,8 | 0,694 |
| Microalbumina/Cr. orina (mg/g) | 30,5 ± 69,5 | 300,4 ± 847,5 | 0,004* | 315,7 ± 971,6 | 271,9 ± 558,3 | 0,818 |
| Proteinuria (mg/l) | 175,9 ± 181,6 | 571,3 ± 1367,7 | 0,009* | 595,0 ± 1563,6 | 527,0 ± 915,9 | 0,825 |
| Ecocardiograma | ||||||
| VolAI (ml/m2) | 32,3 ± 12,7 | 58,6 ± 22,5 | < 0,001* | 58,6 ± 24,3 | 58,5 ± 18,7 | 0,982 |
| FEVI () | 60,7 ± 4,2 | 51,6 ± 13,9 | < 0,001* | 60,2 ± 5,1 | 34,3 ± 9,2 | < 0,001* |
| MasaVI (g/m2) | 107 ± 20 | 135 ± 33 | < 0,001* | 128 ± 27 | 148 ± 41 | 0,015* |
| E/E’ | 7,2 ± 2,5 | 11,1 ± 5,9 | < 0,001* | 10,9 ± 5,3 | 11,5 ± 7,2 | 0,687 |
| PAPs (mmHg) | 32,3 ± 6,8 | 40,2 ± 11,2 | 0,008* | 40,4 ± 11,1 | 40,0 ± 11,6 | 0,880 |
| Valvulopatías | 7 (14,3) | 28 (29,8) | 0,041* | 17 (27) | 11 (35,5) | 0,397 |
| P. diastólico | ||||||
| Tipo 0 | 6 (12,2) | 0 (0,0) | < 0,001* | 0 (0,0) | 0 (0,0) | 0,038* |
| Tipo 1 | 43 (87,8) | 42 (44,7) | 32 (50,8) | 10 (32,3) | ||
| Tipo 2 | 0 (0,0) | 37 (39,4) | 25 (39,7) | 12 (38,7) | ||
| Tipo 3 | 0 (0,0) | 15 (16,0) | 6 (9,5) | 9 (29,0) | ||
BNP: péptido natriurético tipo-B; BRIHH: bloqueo de rama izquierda del haz de His; FEVI: fracción de eyección del ventrículo izquierdo; FG: filtrado glomerular estimado por la fórmula MDRD; HTVC: hipertensión veno-capilar; masaVI: masa ventricular izquierda indexada por superficie corporal; P: patrón; PAPs: presión arterial pulmonar sistólica estimada; V.: ventricular; valvulopatías: se consideraron significativas las valvulopatías de grado moderado o severo; VolAI: volumen auricular izquierdo indexado por superficie corporal.
Las variables cuantitativas se expresan como la media ± desviación estándar y las variables cualitativas se expresan como recuento (porcentaje).
p estadísticamente significativa (< 0,05).
En el ecocardiograma, la masa VI, VolAI, índice E/E’ y presión arterial pulmonar sistólica fueron superiores en la IC, sin diferencias entre los subgrupos. Los pacientes sin IC presentaban una función diastólica normal o patrón tipo 1, mientras que los patrones diastólicos seudonormal o restrictivo solo estaban presentes en los diagnosticados de IC. Los pacientes con ICFE-R tuvieron peor función diastólica.
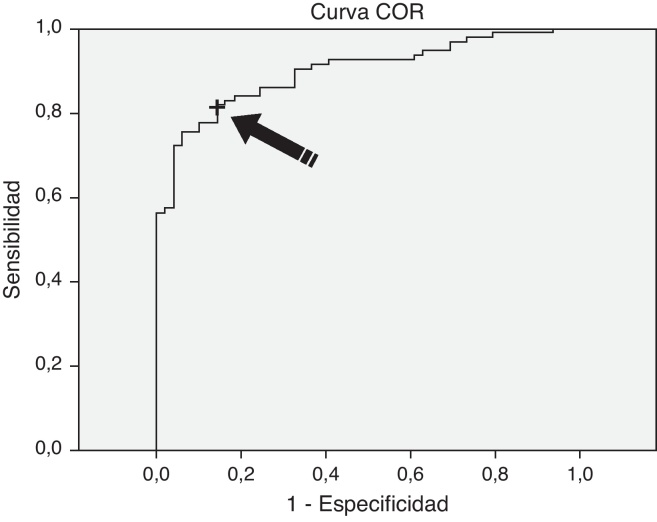
El PNB presentó valores medios significativamente diferentes entre los pacientes con diagnóstico no IC, ICFE-P y ICFE-R (tabla 3). La curva COR (fig. 2) confirmó que el PNB era un buen predictor del diagnóstico de IC (ABC = 0,898; IC 95% 0,848-0,948; p < 0,001) en esta población. El punto de corte de PNB 60,12 pg/ml obtuvo una sensibilidad del 83% y especificidad del 84% para identificar a los pacientes ambulatorios con IC de inicio, con valor predictivo positivo de 90,7% y valor predictivo negativo (VPN) de 71,9%.
Figura 2.
Curva COR de PNB: el valor 60,12 pg/ml (señalado con la flecha) obtuvo una sensibilidad del 83% y una especificidad del 84% para identificar la IC.
En el análisis de regresión logística (tabla 4) se incluyeron las variables edad, sexo, presencia de edemas, presión arterial sistólica, frecuencia cardíaca, Q de necrosis, cardiomegalia y PNB. El sexo femenino (OR = 6,662; IC95% 1,761-25,204; p = 0,005) y la presencia de edemas maleolares (OR = 7,259; IC95% 1,739-30,309; p = 0,007) fueron predictores de ICFE-P. En cambio, la presencia de onda Q patológica en el electrocardiograma (OR = 0,171; IC95% 0,042-0,695; p = 0,014), los valores elevados de PNB (OR = 0,994; IC95% 0,990-0,998; p = 0,003) y frecuencia cardíaca (OR = 0,948; IC95% 0,904-0,994); p = 0,027) aumentaron el riesgo de presentar ICFE-R.
Tabla 4.
Análisis de regresión logística de las principales variables
| Variable | Odds ratio (IC95%)a | p |
|---|---|---|
| Sexo femenino | 6,662 (1,761-25,204) | 0,005* |
| Edemas maleolares | 7,259 (1,739-30,309) | 0,007* |
| BNP (por cada incremento de 1 pg/ml) | 0,994 (0,990-0,998) | 0,003* |
| Onda Q patológica | 0,171 (0,042-0,695) | 0,014* |
| Frecuencia cardíaca (por cada incremento de 1 lpm) | 0,948 (0,904-0,994) | 0,027* |
| Cardiomegalia | 0,267 (0,070-1,024) | 0,054 |
Análisis multivariado con odds ratio ajustadas para el diagnóstico de ICFE-P versus ICFE-R y expresadas con el intervalo de confianza del 95%.
p estadísticamente significativa (< 0,050).
Discusión
Este estudio muestra cómo la CAR-IC permite el diagnóstico rápido y la caracterización de la IC que se manifiesta ambulatoriamente, a la vez que ofrece un punto de corte de PNB para su diagnóstico en atención primaria. La ICFE-P fue la manifestación de IC más prevalente, lo que se explica posiblemente por tratarse de pacientes ambulatorios con síntomas de inicio, diagnosticados precozmente. Mientras que la ICFE-P fue más frecuente en mujeres, el tabaquismo y la vasculopatía arterial periférica aumentaron el riesgo de presentar ICFE-R. Dichos antecedentes se correlacionarían con la etiopatogenia más común de ambos síndromes10: la ICFE-P se asocia a hipertensión y envejecimiento, mientras que la ICFE-R tiene como causa más frecuente la etiología isquémica. Los valores más elevados de troponina I en la ICFE-R sugieren lesión del miocito, ya sea por presiones de llenado y volúmenes ventriculares elevados por la IC, como por coexistencia de un posible sustrato isquémico subyacente. El papel de este biomarcador en el diagnóstico de la IC no está bien establecido, si bien se conoce su valor pronóstico11, 12.
Los pacientes que no presentaban IC tenían mayor IMC, correspondiente a obesidad (31 ± 4 kg/m2), lo que junto a la posible coexistencia de alteraciones respiratorias, puede justificar sus síntomas. Los pacientes con ICFE-P presentaron IMC más elevados, próximos a la obesidad (29,8 ± 5,1 kg) frente a los ICFE-R. Se ha descrito la relación entre obesidad y alteraciones cardíacas como hipertrofia VI, dilatación de cavidades, disfunción diastólica y semiología de IC13, 14.
La presencia de edemas fue un predictor de ICFE-P versus ICFE-R15, aunque los pacientes con IC tuvieron cifras elevadas de presión arterial pulmonar independientemente de la FEVI. En el momento del diagnóstico, los pacientes con IC tenían más alteración en la función renal y proteinuria. Esto pone de manifiesto la asociación de disfunción renal y cardiaca atribuibles a la hipertensión arterial, su factor etiopatogénico común, pero también a que ambas enfermedades pueden ser causa o consecuencia entre ellas16, siendo la insuficiencia renal un marcador de morbimortalidad en la IC17.
En la ecocardiografía, únicamente la FEVI diferenciaba a los subgrupos de IC, ya que las alteraciones de la función diastólica que conducen al diagnóstico de ICFE-P18, 19 se hallaron presentes también en la ICFE-R. El patrón diastólico tipo 1, alteración de la relajación, no implicó IC, ya que es fisiológico en pacientes hipertensos o de edad avanzada, y estuvo presente en el 87,8% de los pacientes sin IC. Sin embargo, los patrones diastólicos más patológicos, tipos 2 y 3, se relacionaron con la presencia de IC y peor función sistólica.
El punto de corte de PNB 60,12 pg/ml presentó una sensibilidad y especificidad superiores al 80% para predecir IC a nivel ambulatorio en fases iniciales del síndrome. En estos pacientes, un valor superior a este confirmaría el diagnóstico en el 90,7% de los casos, indicando la realización de un ecocardiograma que incluyera estudio de la función diastólica. Un valor inferior al propuesto haría improbable el diagnóstico, aunque con 28,1% de falsos negativos. En poblaciones con menor probabilidad de IC, el VPN aumentaría y el PNB aislado podría tener más rendimiento para descartar el diagnóstico, pero cuando existe alta sospecha clínica de IC, el PNB aislado no permite descartar IC con seguridad y debería realizarse una ecocardiografía.
El modelo asistencial presentado permite la evaluación completa de los pacientes derivados por el médico de familia en una consulta de acto único, con seguimiento en el centro de salud, de forma compartida por el médico de familia y el cardiólogo integrado. La CAR-IC favorece la identificación precoz de la IC, incluida la ICFE-P, en atención primaria. Por el diseño y objetivos del trabajo no se incluyeron pacientes que requirieron ingreso hospitalario o que precisaban atención domiciliaria, que podrían presentar unos parámetros clínicos y etiopatogénicos diferentes, lo que supone una limitación del estudio.
Existen pocos modelos de consulta de acto único en cardiología7, 20, 21 y son escasas las publicaciones de consultas monográficas para el diagnóstico de IC22. Las características clínicas de los pacientes con ICFE-P y ICFE-R del presente estudio coinciden con otros trabajos previos3, 15, 23, 24, 25. Las diferencias de este trabajo respecto a anteriores10, 14, 15, 23 son que el diagnóstico se basó en un algoritmo bien establecido2, 5, y no solo por criterios clínicos ni análisis retrospectivos, y que el estudio ecocardiográfico fue sistemático, se calculó la FEVI y se analizó específicamente la función diastólica, incluyendo medidas de Doppler tisular y venas pulmonares. Otra diferencia es que los pacientes eran ambulatorios y con IC de inicio y, finalmente, que se definió un punto de corte de PNB para identificar la IC en atención primaria. Un estudio reciente analizó el punto de corte para el diagnóstico en una población ambulatoria con sospecha de IC, pero utilizando NT-pro-PNB26.
La mejor caracterización de la IC en pacientes como los del estudio, principalmente los que presentan ICFE-P, permitirá un mayor conocimiento de este síndrome. Se dispone de escasa evidencia científica sobre la fisiopatología y el tratamiento de estos pacientes, por lo que se precisan más trabajos, algunos de ellos ya en marcha27, dirigidos al estudio de las bases moleculares, comorbilidades y nuevos biomarcadores que ayuden a mejorar el diagnóstico y pronóstico de la ICFE-P.
El diagnóstico rápido de los pacientes debe permitir la intervención precoz para su tratamiento y medidas de educación sanitaria. Aunque existe controversia8, 24, 25 y escasa evidencia del tratamiento farmacológico en la ICFE-P, la mortalidad absoluta es elevada28 y los programas de intervención estructurados, basados en gran parte en la educación de los pacientes, han sido eficaces en poblaciones con alta prevalencia de ICFE-P en nuestro medio8, 9.
Como conclusiones, la CAR-IC es eficaz para el diagnóstico rápido de los pacientes con sospecha de IC de inicio en atención primaria y ha permitido su caracterización mediante un estudio sistemático en una única jornada. La ICFE-P es la manifestación de IC más prevalente en la población estudiada. El sexo femenino y la presencia de edemas maleolares son predictores diagnósticos de ICFE-P. En cambio, la presencia de onda Q patológica en el electrocardiograma, los valores más elevados de PNB y de frecuencia cardíaca aumentan el riesgo de presentar ICFE-R.
El PNB ha ofrecido una sensibilidad y especificidad elevadas para identificar la IC en los pacientes ambulatorios de este estudio, pero ante la elevada sospecha diagnóstica de IC se debe completar el estudio con una ecocardiografía con estudio sistemático de la función sistólica y diastólica.
Lo conocido sobre el tema
-
1)
La insuficiencia cardiaca es un problema de salud prevalente en las consultas de atención primaria y causa una elevada morbimortalidad.
-
2)
La insuficiencia cardiaca que se manifiesta de forma ambulatoria está infradiagnosticada.
-
3)
En esta población, la proporción de insuficiencia cardiaca con fracción de eyección preservada parece ser elevada.
Qué aporta este estudio
-
1)
Se ofrece un modelo de atención en una consulta de alta resolución que resulta eficaz para el diagnóstico rápido de los pacientes con insuficiencia cardiaca.
-
2)
Se analizan las características clínicas de los pacientes con insuficiencia cardiaca en la que esta se manifiesta de manera ambulatoria, y las diferencias en la presentación entre los que tienen fracción de eyección preservada y reducida.
-
3)
Se determina un punto de corte de péptido natriurético tipo B diagnóstico para estos pacientes.
Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
Bibliografía
- 1.Anguita M., Crespo M., de Teresa E., Jimenez M., Alonso-Pulpón L., Muñiz J. Prevalencia de la insuficiencia cardíaca en la población general española mayor de 45 años. Estudio PRICE. Rev Esp Cardiol. 2008;61:1041–1049. [Google Scholar]
- 2.Dickstein K., Cohen-Solal A., Filippatos G., McMurray J.J., Ponikowski P., Poole-Wilson P.A. ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure 2008: The Task Force for the Diagnosis and Treatment of Acute and Chronic Heart Failure 2008 of the European Society of Cardiology. Developed in collaboration with the Heart Failure Association of the ESC (HFA) and endorsed by the European Society of Intensive Care Medicine (ESICM) Eur Heart J. 2008;29:2388–2442. doi: 10.1093/eurheartj/ehn309. [DOI] [PubMed] [Google Scholar]
- 3.Bursi F., Weston S.A., Redfield M.M., Jacobsen S.J., Pakhomow S., Nkomo V.T. Systolic and diastolic heart failure in the community. JAMA. 2006;296:2209–2216. doi: 10.1001/jama.296.18.2209. [DOI] [PubMed] [Google Scholar]
- 4.Grupo de Trabajo de Insuficiencia Cardíaca de la Sociedad Española de Medicina Interna (SEMI) La insuficiencia cardíaca en los servicios de medicina interna (estudio SEMI-IC) Med Clin (Barc) 2002;118:605–610. [PubMed] [Google Scholar]
- 5.Paulus W.J., Tschope C., Sanderson J.E., Rusconi C., Flaschskampf F.A., Rademakers F.E. How to diagnose diastolic heart failure: a consensus statement on the diagnosis of heart failure with normal left ventricular ejection fraction by the Heart Failure and Echocardiography Associations of the European Society of Cardiology. Eur Heart J. 2007;28:2539–2550. doi: 10.1093/eurheartj/ehm037. [DOI] [PubMed] [Google Scholar]
- 6.Falces C., Andrea R., Heras M., Vehí C., Sorribes M., Sanchis L. Integración entre cardiologıía y atención primaria: impacto sobre la práctica clínica. Rev Esp Cardiol. 2011;64:564–571. doi: 10.1016/j.recesp.2011.02.021. [DOI] [PubMed] [Google Scholar]
- 7.Falces C., Sadurní J., Monell J., Andrea R., Ylla M., Moleiro A. Consulta inmediata ambulatoria de alta resolución en Cardiología: 10 años de experiencia. Rev Esp Cardiol. 2008;61:530–533. [PubMed] [Google Scholar]
- 8.Falces C., López-Cabezas C., Andrea R., Arnau A., Ylla M., Sadurní J. Intervención educativa para mejorar la adherencia al tratamiento y prevenir reingresos en pacientes con insuficiencia cardíaca de edad avanzada. Med Clin (Barc) 2008;131:452–456. doi: 10.1157/13126954. [DOI] [PubMed] [Google Scholar]
- 9.Brotons C., Falces C., Alegre J., Ballarin E., Casanovas J., Cata T. Ensayo clínico aleatorizado para evaluar la efectividad de una intervención domiciliaria en pacientes con insuficiencia cardíaca: estudio IC-DOM. Rev Esp Cardiol. 2009;62:400–408. [Google Scholar]
- 10.Lee D.S., Gona P., Vasan R.S., Larson M.G., Benjamin E.J., Wang T.J. Relation of disease pathogenesis and risk factors to heart failure with preserved or reduced ejection fraction. Insights from the Framingham Heart Study of the National Heart, Lung and Blood Institute. Circulation. 2009;119:3070–3077. doi: 10.1161/CIRCULATIONAHA.108.815944. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 11.Miller W.L., Hartman K.A., Burritt M.F., Grill D.E., Jaffe A.S. Profiles of serial changes in cardiac troponin T concentrations and outcome in ambulatory patients with chronic heart failure. J Am Coll Cardiol. 2009;54:1715–1721. doi: 10.1016/j.jacc.2009.07.025. [DOI] [PubMed] [Google Scholar]
- 12.Tsutamoto T., Kawahara C., Nishiyama K., Yamaji M., Fujii M., Yamamoto T. Prognostic role of highly sensitive cardiac troponin I in patients with systolic heart failure. Am Heart J. 2010;159:63–67. doi: 10.1016/j.ahj.2009.10.022. [DOI] [PubMed] [Google Scholar]
- 13.Luaces M., Cachofeiro V., García-Muñoz-Najar A., Medina M., González N., Cancer E. Modificaciones anatomofuncionales del corazón en la obesidad mórbida. Cambios tras la cirugía bariátrica. Rev Esp Cardiol. 2012;65:14–21. doi: 10.1016/j.recesp.2011.06.018. [DOI] [PubMed] [Google Scholar]
- 14.Kuznetsova T., Herbots L., López B., Jin Y., Richar T., Thijs L. Prevalence of left ventricular diastolic dysfunction in a general population. Circ Heart Fail. 2009;2:105–112. doi: 10.1161/CIRCHEARTFAILURE.108.822627. [DOI] [PubMed] [Google Scholar]
- 15.Bathia R.S., Tu J.V., Lee D.S., Austin P.C., Fang J., Haouzi A. Outcome of heart failure with preserved ejection fraction in a population-based study. N Engl J Med. 2006;355:260–269. doi: 10.1056/NEJMoa051530. [DOI] [PubMed] [Google Scholar]
- 16.Kitzman D.W., Gardin J.M., Gottdiener J.S., Arnold A., Boineau R., Aurigemma G. Importance of heart failure with preserved systolic function in patients > or =65 years of age. CHS Research Group. Cardiovascular Health Study. Am J Cardiol. 2001;87:413–419. doi: 10.1016/s0002-9149(00)01393-x. [DOI] [PubMed] [Google Scholar]
- 17.Jones R.C., Francis G.S., Lauer M.S. Predictors of mortality in patients with heart failure and preserved systolic function in the DIG trial. J Am Coll Cardiol. 2004;44:1025–1029. doi: 10.1016/j.jacc.2004.05.077. [DOI] [PubMed] [Google Scholar]
- 18.Zile M.R., Gottdiener J.S., Hetzel S.J., McMurray J.J., Komajda M., McKelvie R. Prevalence and significance of alterations in cardiac estructure and function in patients with heart failure and a preserved ejection fraction. Circulation. 2011;124:2491–2501. doi: 10.1161/CIRCULATIONAHA.110.011031. [DOI] [PubMed] [Google Scholar]
- 19.Meta-analysis Research Group in Echocardiography (MeRGE) Heart Failure collaborators Independence of restrictive filling pattern and LV ejection fraction with mortality in heart failure: an individual patient meta-analysis. Eur Heart J. 2008:786–792. doi: 10.1016/j.ejheart.2008.06.005. [DOI] [PubMed] [Google Scholar]
- 20.Tenkorang J.N., Fox K.F., Collier T.J., Wood D.A. A rapid access cardiology service for chest pain, heart failure and arrhythmias accurately diagnoses cardiac disease and identifies patients at high risk: a prospective cohort study. Heart. 2006;92:1084–1090. doi: 10.1136/hrt.2005.079376. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 21.Montijano A.M., Caballero J. La consulta de acto único en cardiología. Rev Esp Cardiol. 2007;7:C30–C36. [Google Scholar]
- 22.Fox K.F., Cowie M.R., Wood D.A., Coats A.J., Poole-Wilson P.A., Sutton G.C. A rapid access heart failure clinic promptly identifies heart failure and initiates appropriate therapy. Eur J Heart Fail. 2000:423–429. doi: 10.1016/s1388-9842(00)00108-2. [DOI] [PubMed] [Google Scholar]
- 23.Lam C.S.P., Lyass A., Kraigher-Krainet E., Massaro J., Lee D.S., Ho J.E. Cardiac dysfunction and noncardiac dysfunction as precursors of heart failure with reduced and preserved ejection fraction in the community. Circulation. 2011;124:24–30. doi: 10.1161/CIRCULATIONAHA.110.979203. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 24.Zile M.R., Gaasch W.H., Anand I.S., Haass M., Little W.C., Miller A.B. Mode of death in patients with heart failure and a preserved ejection fraction. Results from the irbesartan in heart failure with preserved ejection fraction study (I-Preserve) Trial. Circulation. 2010;121:1393–1405. doi: 10.1161/CIRCULATIONAHA.109.909614. [DOI] [PubMed] [Google Scholar]
- 25.Anguita M., Castillo J.C., Ruiz M., Castillo F., Jiménez-Navarro M., Crespo M. Diferencias en el pronóstico de la insuficiencia cardíaca con función sistólica conservada o deprimida en pacientes mayores de 70 años que toman bloqueadores beta. Rev Esp Cardiol. 2012;65:22–28. [Google Scholar]
- 26.Verdú J.M., Comín-Colet J., Domingo M., Lupón J., Gómez M., Molina L. Rapid Point-of-Care NT-proBNP Optimal Cut-off Point for Heart Failure Diagnosis in Primary Care. Rev Esp Cardiol. 2012;65:613–619. doi: 10.1016/j.recesp.2012.01.019. [DOI] [PubMed] [Google Scholar]
- 27.Westenbrink D B., Damman K., Rienstra M., Maass A.H., van der Meer P. Heart failure highlights in 2011. Eur J Heart Fail. 2012;14:1090–1096. doi: 10.1093/eurjhf/hfs121. [DOI] [PubMed] [Google Scholar]
- 28.Meta-analysis Global Group in Chronic Heart Failure (MAGGIC) The survival of patients with heart failure with preserved or reduced left ventricular ejection fraction: an individual patient data meta-analysis. Eur Heart J. 2012;33:1750–1757. doi: 10.1093/eurheartj/ehr254. [DOI] [PubMed] [Google Scholar]