Abstract
目的
探讨牙周基础治疗对伴2型糖尿病的中、重度牙周炎患者牙周炎症控制、血清炎症指标以及糖代谢水平的影响。
方法
将前期临床试验人群中的56例中、重度牙周炎患者(平均临床附着水平>3 mm)纳入本研究进行亚组分析,采用重复测量的方差分析比较治疗组和对照组牙周指数(包括平均探诊深度、临床附着水平和探诊出血指数)、超敏C反应蛋白(hsCRP)、糖化血红蛋白(HbA1c)、空腹血糖在基线、1.5个月、3个月、6个月连续4次的变化。
结果
伴2型糖尿病的中、重度牙周炎患者在牙周治疗后平均探诊深度(F=62.898,P=0.000)、临床附着水平(F=51.263,P=0.000)和探诊出血指数(F=75.164,P=0.000)在治疗后逐渐改善,其中平均探诊深度(t=−2.050,P=0.045)和探诊出血指数(t=−4.538,P=0.000)显著优于对照组;治疗后hsCRP(F=6.391,P=0.010)、HbA1c(F=4.536,P=0.011)、空腹血糖(F=3.073,P=0.031)降低,其中hsCRP显著低于对照组(t=−2.261,P=0.028)。
结论
牙周基础治疗有助于改善伴2型糖尿病的中、重度牙周炎患者的牙周炎症和血清炎症指标以及糖代谢水平。
Keywords: 牙周炎, 糖尿病, 超敏C反应蛋白
Abstract
Objective
To evaluate the effects of periodontal treatment on the clinical response, systemic inflammatory parameters, and metabolic control of type 2 diabetes patients with moderate to severe periodontitis.
Methods
A total of 56 patients with mean clinical attachment level (CAL)>3 mm were included in the subgroup analysis. A repeated-measures ANOVA (group factor: treatment group and control group; time factor: initial visit, 1.5, 3, and 6 months) was used to analyze the probing depth (PD), CAL, bleeding on probing (BOP), high-sensitivity C-reactive protein (hsCRP), glycated hemoglobin (HbA1c), and fasting plasma glucose.
Results
Significantly lower PD (F=62.898,P=0.000), CAL (F=51.263,P=0.000), BOP (F=75.164,P=0.000), hsCRP (F=6.391, P=0.010), HbA1c (F=4.536, P=0.011), and fasting plasma glucose level (F=3.073,P=0.031) were observed after therapeutic periodontal improvement. The inter-group differences for PD (t=−2.050,P=0.045), BOP (t=−4.538,P=0.000), and hsCRP (t=−2.261, P=0.028) were statistically significant after therapy.
Conclusion
Non-surgical periodontal treatment can effectively improve periodontal status, circulating inflammatory status, and metabolic control of diabetic patients with moderate to severe periodontitis.
Keywords: periodontitis, diabetes, high-sensitivity C-reactive protein
牙周炎和糖尿病是影响人类健康的两大慢性疾病。我国成人牙周病的患病率高达80%~90%,是成人失牙的主要原因[1]。目前我国糖尿病总患病人数估计在9 240万[2]。牙周炎和糖尿病具备相互易感性,患2型糖尿病5年以上的患者牙周炎患病率超过85.72%[3],两者相互影响的双向关系一直是学者关注的热点[4]。
尽管存在一定的争议[5]–[6],多数研究[4],[7]支持牙周基础治疗在改善机体糖代谢方面的积极作用。有学者[7]对前期随机临床对照试验进行Meta分析,结果表明牙周治疗使得糖尿病患者糖化血红蛋白(glycated hemoglobin,HbA1c)平均下降0.4%。本文对前期随机、对照临床试验[8]中的中、重度牙周炎患者进行亚组分析,旨在观察牙周基础治疗对伴2型糖尿病的中、重度牙周炎患者牙周炎症控制、血清炎症指标以及糖代谢水平的影响,分析伴2型糖尿病的中、重度牙周炎患者是否从牙周治疗中获益更明显。
1. 材料和方法
1.1. 前期临床试验设计概况
研究设计为一随机、对照临床试验(中国临床试验中心注册号:ChiCTR-TRC-10001062)。从2008年11月—2009年10月将134名伴2型糖尿病的牙周炎患者随机分为3组,分别为治疗Ⅰ组(45例)、治疗Ⅱ组(45例)和对照组(44例)。
纳入标准:糖尿病确诊1年以上,糖尿病病情稳定,用药2月内无变化,无严重并发症;患有慢性牙周炎,全口存留≥16颗牙齿,且未经过系统牙周治疗,1年内未接受过洁治。
排除标准:患有影响牙周健康的其他系统性疾病,如冠心病等;除牙周炎外,身体其他部位存在活动性炎症;3个月内服用抗生素;妊娠期、哺乳期或治疗期间计划怀孕;拒绝参加本研究。
诊断标准:糖尿病诊断标准(1999年WHO诊断标准):糖尿病症状加任意时间血浆葡萄糖>11.1 mmol·L−1;或空腹血糖>7.0 mmol·L−1;或75 g无水葡萄糖口服糖耐量试验,2 h血糖浓度>11.1 mmol·L−1(200 mg·dL−1)。需要重复测量1次,诊断才能成立。
治疗设计如下:治疗Ⅰ组在基线时接受牙周基础治疗,3个月复诊时接受酌情龈下刮治;治疗Ⅱ组在基线时接受牙周基础治疗,3个月复诊时接受预防性龈上洁治,但不作深牙周袋进一步处理;对照组在整个观察期间均不作任何治疗。
牙周基础治疗包括口腔卫生宣传教育(oral hygiene instruction,OHI)、全口龈上洁治、龈下刮治、根面平整术、调  、拔除无法保留的患牙。所有基础治疗均在24 h内由1名有经验的牙周医师完成。牙周基础治疗后1.5、3和6个月对所有研究对象进行评价,并完成全口临床牙周检查、糖代谢水平(包括空腹血糖和HbA1c)和超敏C反应蛋白(high-sensitivity C-reactive protein,hsCRP)水平的检测。全口临床牙周检查包括平均探诊深度(probing depth,PD)、临床附着水平(clinical attachment level,CAL)和探诊出血指数(bleeding on probing,BOP)。临床试验的整个期间均不使用任何的抗生素,患者被要求保持原有的生活方式、饮食习惯、用药情况不变。
、拔除无法保留的患牙。所有基础治疗均在24 h内由1名有经验的牙周医师完成。牙周基础治疗后1.5、3和6个月对所有研究对象进行评价,并完成全口临床牙周检查、糖代谢水平(包括空腹血糖和HbA1c)和超敏C反应蛋白(high-sensitivity C-reactive protein,hsCRP)水平的检测。全口临床牙周检查包括平均探诊深度(probing depth,PD)、临床附着水平(clinical attachment level,CAL)和探诊出血指数(bleeding on probing,BOP)。临床试验的整个期间均不使用任何的抗生素,患者被要求保持原有的生活方式、饮食习惯、用药情况不变。
1.2. 研究方法
将前期临床试验人群中的56例中、重度牙周炎患者纳入本研究。纳入标准:伴2型糖尿病的牙周炎患者平均CAL>3 mm[9]。由于前期统计结果发现治疗Ⅰ组和治疗Ⅱ组(仅维护治疗方式不同)在改善牙周炎、机体炎症状态和代谢水平均无显著差异,故将治疗Ⅰ组、治疗Ⅱ组合并为治疗组(35例),与对照组(21例)进行比较分析。
1.3. 牙周指数检查
由1名经过培训的医师(intra-examiner Kappa值为80%~87%)使用Williams探针为所有研究对象做全口牙周检查(第三磨牙除外)。主要内容包括6个位点(近中颊侧、正中颊侧、远中颊侧、近中舌侧、正中舌侧、远中舌侧)的PD、CAL、BOP,记录牙周检查大表。
1.4. 糖代谢水平检测
所有研究对象均在早晨8~10点间,全口牙周探查前空腹抽取静脉血,检测空腹血糖值和HbA1c。HbA1c的测定采用NycoCard Reader Ⅱ多功能全定量特种蛋白金标检测仪测定。测量原理:硼化亲和、生化层析比色原理。操作严格按照仪器说明进行,变异系数(coefficient of variation,CV)为1.2%~2.8%。
1.5. hsCRP的检测
抽取静脉全血后注入非抗凝试管内,倾斜或直立于试管架上,放置1~2 h,4 000 r·min−1离心10 min,吸取上层淡黄色血清,分装到0.5 mLEP管中,编上编号,−70 °C保存待检测(避免反复冻融)。所有血清标本送到广州金域医学检验中心,采用免疫比浊法测量hsCRP,仪器采用罗氏全自动生化仪测量,CV为 1.5%~2.5%。
1.6. 统计分析
采用SPSS 13.0统计软件对实验数据进行分析,采用独立两样本t检验比较年龄、身体质量指数(body mass index,BMI)、糖尿病患病年限和缺牙数;采用Pearson卡方检验统计性别、吸烟、饮酒和规律锻炼情况;采用Fisher确切概率法比较糖尿病的治疗方案。两组人群的所有临床和实验室观测指标在基线、1.5个月、3个月、6个月连续4次的变化采用重复测量的方差分析进行比较,检验水平为双侧P<0.05。
2. 结果
2.1. 一般情况
从两组人群的基线资料可见,各组年龄、性别、BMI、糖尿病患病年限、缺牙数、吸烟情况、糖尿病治疗方案、饮酒和规律锻炼间差异均无统计学意义(P>0.05),即各组基线资料齐,具有较好的均衡性(表1)。
表 1. 两组人群治疗前的一般情况.
Tab 1 Participants characteristics of study groups at the first visit
| 一般情况 | 治疗组 | 对照组 | t/χ2值 | P值 |
| (n=35) | (n=21) | |||
| 年龄/岁 | 58.06±10.63 | 63.24±6.77 | −1.999 | 0.051 |
| 患糖尿病年限/年 | 7.49±5.47 | 9.81±8.30 | −1.263 | 0.212 |
| BMI | 24.45±3.45 | 24.17±2.23 | 0.336 | 0.738 |
| 缺牙数 | 4.80±4.12 | 5.71±4.00 | −0.813 | 0.420 |
| 性别(男/女) | 21/14 | 10/11 | 0.814 | 0.367 |
| 吸烟(是/否) | 8/27 | 6/15 | 0.229 | 0.633 |
| 糖尿病治疗方案 | 0.525 | 1.000 | ||
| 饮食控制 | 1 | 1 | - | - |
| 口服用药 | 30 | 18 | - | - |
| 胰岛素 | 4 | 2 | - | - |
| 饮酒(是/否) | 5/30 | 5/16 | 0.812 | 0.368 |
| 规律锻炼(是/否) | 27/8 | 18/3 | 0.611 | 0.434 |
2.2. 牙周状况
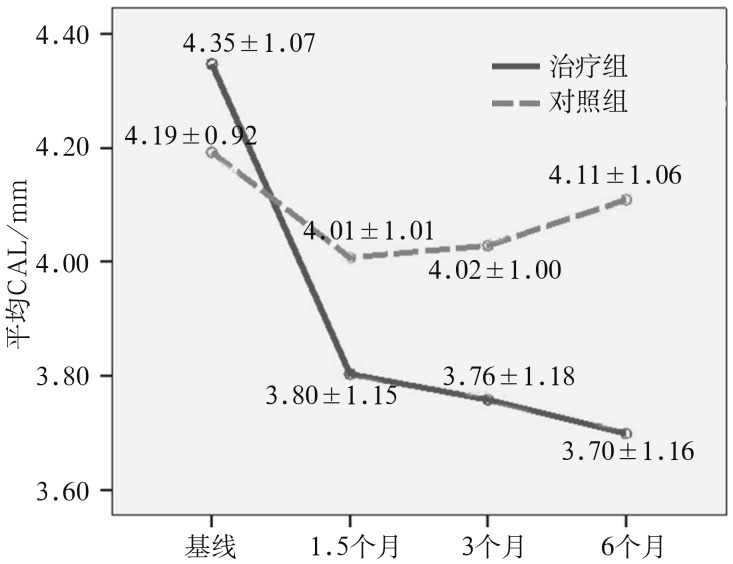
两组人群平均CAL在试验期间的变化见图1。治疗组平均CAL随时间呈显著下降趋势(F=51.263,P=0.000),6个月时降至最低,平均降低(0.65±0.07) mm;对照组平均CAL随时间呈先降后升趋势(F=3.458,P=0.043),对照组6个月和基线相比较平均CAL差异无统计学意义(P>0.05);治疗组和对照组之间差异无统计学意义(P>0.05)。
图 1. 两组平均CAL在治疗期间的变化.
Fig 1 The changes of mean CAL in two groups over the study period
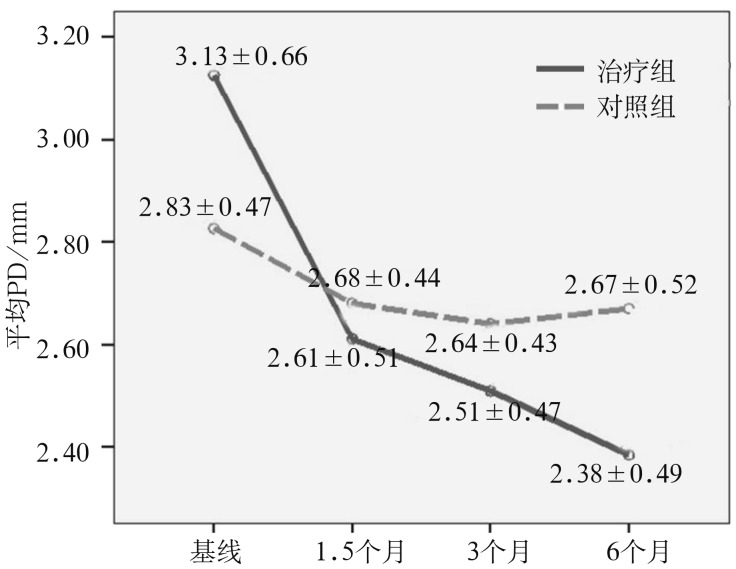
两组平均PD在试验期间随时间的变化见图2。治疗组平均PD随时间呈显著下降趋势(F=62.898,P=0.000),6个月时降到最低,平均降低(0.74±0.08) mm;对照组平均PD随时间基本呈轻度下降趋势(F=3.976,P=0.030),对照组6个月和基线相比较平均PD差异无统计学意义(P>0.05)。6个月时,治疗组平均PD显著低于对照组(t=−2.050,P=0.045)。
图 2. 两组平均PD在治疗期间的变化.
Fig 2 The changes of mean PD in two groups over the study period
两组人群BOP在试验期间的变化见图3。治疗组出血指数随时间呈显著下降趋势(F=75.164,P=0.000),6个月时降至最低,平均降低0.29±0.02;对照组出血指数较基线有轻度下降,平均降低0.09±0.04(P<0.05);治疗组出血指数下降的幅度显著高于对照组(t=−4.538,P=0.000)。
图 3. 两组出血指数在治疗期间的变化.
Fig 3 The changes of mean BOP in two groups over the study period
2.3. 全身状况
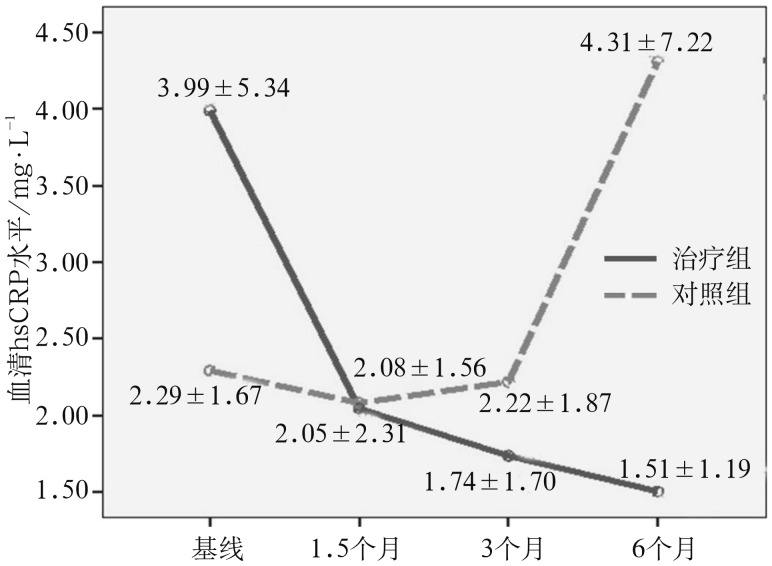
两组血清hsCRP在试验期间随时间的变化见图4。治疗组血清hsCRP随时间呈显著下降趋势(F=6.391,P=0.010),6个月时降到最低,平均降低(2.48±0.84) mg·L−1;对照组血清hsCRP随时间基本呈上升趋势,变化差异无统计学意义(F=1.837,P=0.185)。6个月时,治疗组血清hsCRP显著低于对照组(t=−2.261,P=0.028)。
图 4. 两组血清hsCRP在治疗期间的变化.
Fig 4 The changes of serum hsCRP in two groups over the study period
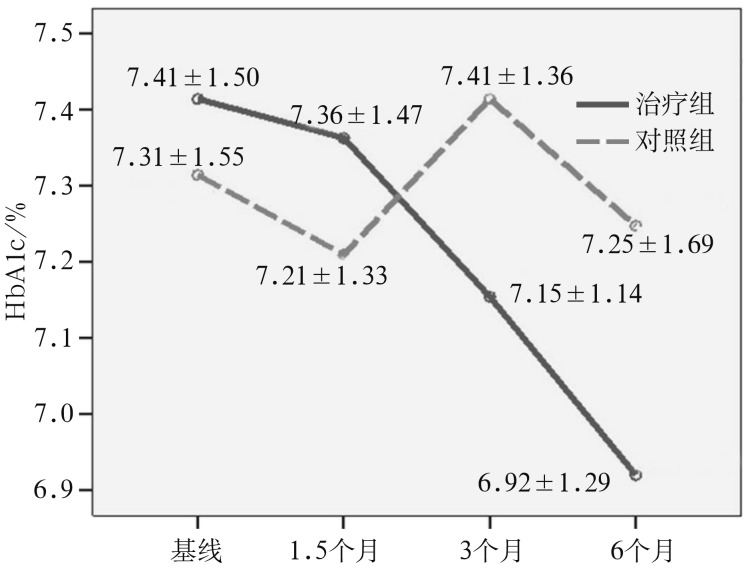
两组人群HbA1c在试验期间随时间的变化见图5。治疗组HbA1c随时间呈显著下降趋势(F=4.536,P=0.011),6个月时降到最低,平均下降0.49%±0.18%;对照组HbA1c在治疗期间的波动变化无显著差异(F=0.259;P=0.760);两组间差异无统计学意义(P>0.05)。
图 5. 两组HbA1c在治疗期间的变化.
Fig 5 The changes of HbA1c in two groups over the study period
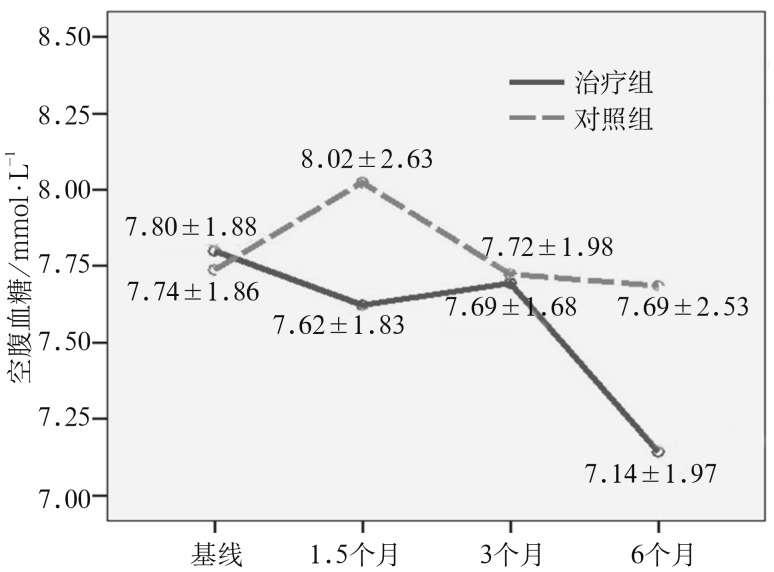
两组人群空腹血糖在试验期间随时间的变化见图6。治疗组空腹血糖随时间呈显著下降趋势(F=3.073,P=0.031),6个月时降到最低,平均下降(0.66±0.28) mmol·L−1 ;对照组空腹血糖在治疗期间的波动变化无显著差异(F=0.314;P=0.707);组间比较差异无统计学意义(P>0.05)。
图 6. 两组空腹血糖在治疗期间的变化.
Fig 6 The changes of fasting plasma glucose in two groups over the study period
3. 讨论
目前公认牙周基础治疗能有效地控制2型糖尿病患者牙周炎症。本研究结果显示,牙周指数(包括平均PD、CAL和BOP)在治疗后逐渐改善,6个月时降至最低,其中平均PD和BOP显著优于对照组。亚组分析结果显示:伴2型糖尿病的中、重度牙周炎患者从牙周基础治疗中获益更为明显,平均CAL降低(0.65±0.07) mm,优于之前报道的0.37~0.40 mm[8]。此外,对照组牙周指数也有轻度改善的原因在于:患者就诊时有意或无意地接受了口腔保健知识,更重视口腔卫生,口腔健康意识也在多次随访中不断被强化,但由此带来牙周指数的进步无法同治疗组相比。因此,牙周基础治疗能控制伴2型糖尿病的中、重度牙周炎患者牙周局部炎症,减少牙龈出血状况,治疗效果在6个月时达到最佳。
C反应蛋白(C-reactive protein,CRP)是一种非特异性的急性时相蛋白,通常被认为是炎症反应的下游因子,是机体慢性炎症反应的标志物。随着检测技术的进步,采用超敏感方法检测到的CRP,被称为hsCRP。本课题小组前期研究发现,慢性牙周炎与2型糖尿病患者血清hsCRP水平密切相关,即牙周感染越严重,血清hsCRP浓度越高[10]。牙周基础治疗能使2型糖尿病患者血清hsCRP水平降低1.56~1.63 mg·L−1 [8]。亚组分析结果显示:伴2型糖尿病的中、重度牙周炎患者在牙周治疗后hsCRP降低幅度更大,平均降低(2.48±0.84) mg·L−1 。因此,随着牙周炎症的控制和牙龈状况的好转,糖尿病患者血清hsCRP水平逐渐降低,即牙周基础治疗能起到改善机体炎症状态的作用。
有学者[11]指出牙周干预治疗正是通过降低患者血清CRP浓度来达到改善血糖控制的目的。近10年来,欧洲、美国、日本等各地的多项大样本纵向研究证实,高浓度CRP是健康人群发展为2型糖尿病的重要预测因子[12]。一些动物模型以及体外研究也证实CRP不仅仅是非特异性的炎症指标,它可激活或抑制多种信号途径而直接引起胰岛素抵抗[13]。研究[11]表明牙周炎导致宿主过激的免疫反应,引起2型糖尿病患者血清CRP水平升高,可能是联系两种疾病的重要纽带。
作为糖尿病控制情况的主要监测指标之一,HbA1c反应患者近8~12周总的血糖水平。本课题组前期研究结果发现:慢性牙周炎的严重程度与2型糖尿病患者糖代谢水平密切相关[10];牙周基础治疗虽然降低HbA1c水平0.22%~0.42%,空腹血糖(0.2~0.73) mmol·L−1,但部分结果尚未达统计学差异[8]。本亚组分析结果显示:伴2型糖尿病的中、重度牙周炎患者在牙周治疗后HbA1c显著下降0.49%±0.18%,空腹血糖显著降低(0.66±0.28) mmol·L−1。上述结果表明,随着牙周局部炎症状态的改善和血清hsCRP水平逐渐降低,糖尿病患者HbA1c水平也逐渐降低,即牙周基础治疗有助于改善伴2型糖尿病中、重度牙周炎患者的糖代谢水平。可能的机制为:牙周炎作为危害人类健康最常见的慢性感染之一,其牙周袋内的多种细菌微生物聚集在一起组成生物膜,在口腔局部长期存在,不但可以直接刺激牙龈组织生成CRP[14],更通过破损的毛细血管源源不断地向循环系统输送各种炎症介质[4];后者刺激机体内肝脏细胞和脂肪组织单核-巨噬细胞系统产生大量CRP[15]–[16],加重机体炎症负担和胰岛素抵抗。但伴2型糖尿病的牙周炎患者血清CRP可能发挥的细胞分子作用机制尚有待进一步的研究。
Funding Statement
[基金项目] 科技部“十一五”重点支撑计划基金资助项目(2007BAI18B02);广东省科技计划基金资助项目(2010B031600117)
References
- 1.孟 焕新. 牙周炎与糖尿病的关系[J] 北京大学学报: 医学版. 2007;39(1):18–20. [PubMed] [Google Scholar]
- 2.Yang W, Lu J, Weng J, et al. Prevalence of diabetes among men and women in China[J] N Engl J Med. 2010;362(12):1090–1101. doi: 10.1056/NEJMoa0908292. [DOI] [PubMed] [Google Scholar]
- 3.卢 怡, 施 生根, 牛 忠英, et al. 2型糖尿病患者牙周炎患病率与年龄、病程的相关性分析[J] 解放军医学杂志. 2010;35(7):875–876. [Google Scholar]
- 4.Preshaw PM, Alba AL, Herrera D, et al. Periodontitis and diabetes: a two-way relationship[J] Diabetologia. 2012;55(1):21–31. doi: 10.1007/s00125-011-2342-y. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 5.Auyeung L, Wang PW, Lin RT, et al. Evaluation of periodontal status and effectiveness of non-surgical treatment in patients with type 2 diabetes mellitus in Taiwan for a 1-year period[J] J Periodontol. 2012;83(5):621–628. doi: 10.1902/jop.2011.110133. [DOI] [PubMed] [Google Scholar]
- 6.Cirano FR, Pera C, Ueda P, et al. Clinical and metabolic evaluation of one-stage, full-mouth, ultrasonic debridement as a therapeutic approach for uncontrolled type 2 diabetic patients with periodontitis[J] Quintessence Int. 2012;43(8):671–681. [PubMed] [Google Scholar]
- 7.Teeuw WJ, Gerdes VE, Loos BG. Effect of periodontal treatment on glycemic control of diabetic patients: a systematic review and meta-analysis[J] Diabetes Care. 2010;33(2):421–427. doi: 10.2337/dc09-1378. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 8.Chen L, Luo G, Xuan D, et al. Effects of non-surgical periodontal treatment on clinical response, serum inflammatory parameters, and metabolic control in patients with type 2 diabetes: a randomized study[J] J Periodontol. 2012;83(4):435–443. doi: 10.1902/jop.2011.110327. [DOI] [PubMed] [Google Scholar]
- 9.Page RC, Eke PI. Case definitions for use in population-based surveillance of periodontitis[J] J Periodontol. 2007;78(7 Suppl):1387–1399. doi: 10.1902/jop.2007.060264. [DOI] [PubMed] [Google Scholar]
- 10.Chen L, Wei B, Li J, et al. Association of periodontal parameters with metabolic level and systemic inflammatory markers in patients with type 2 diabetes[J] J Periodontol. 2010;81(3):364–371. doi: 10.1902/jop.2009.090544. [DOI] [PubMed] [Google Scholar]
- 11.Nagasawa T, Noda M, Katagiri S, et al. Relationship between periodontitis and diabetes-importance of a clinical study to prove the vicious cycle[J] Intern Med. 2010;49(10):881–885. doi: 10.2169/internalmedicine.49.3351. [DOI] [PubMed] [Google Scholar]
- 12.Montonen J, Drogan D, Joost HG, et al. Estimation of the contribution of biomarkers of different metabolic pathways to risk of type 2 diabetes[J] Eur J Epidemiol. 2011;26(1):29–38. doi: 10.1007/s10654-010-9539-0. [DOI] [PubMed] [Google Scholar]
- 13.Tanigaki K, Vongpatanasin W, Barrera JA, et al. C-reactive protein causes insulin resistance in mice through Fcγ receptor IIB-mediated inhibition of skeletal muscle glucose delivery[J] Diabetes. 2013;62(3):721–731. doi: 10.2337/db12-0133. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 14.Lu Q, Jin L. Human gingiva is another site of C-reactive protein formation[J] J Clin Periodontol. 2010;37(9):789–796. doi: 10.1111/j.1600-051X.2010.01600.x. [DOI] [PubMed] [Google Scholar]
- 15.Endo Y, Tomofuji T, Ekuni D, et al. Experimental periodontitis induces gene expression of proinflammatory cytokines in liver and white adipose tissues in obesity[J] J Periodontol. 2010;81(4):520–526. doi: 10.1902/jop.2009.090574. [DOI] [PubMed] [Google Scholar]
- 16.Haider DG, Leuchten N, Schaller G, et al. C-reactive protein is expressed and secreted by peripheral blood mononuclear cells[J] Clin Exp Immunol. 2006;146(3):533–539. doi: 10.1111/j.1365-2249.2006.03224.x. [DOI] [PMC free article] [PubMed] [Google Scholar]