Zusammenfassung
Einleitung
Die Expansion des Spenderpools durch die Verwendung von Spenderorganen, die erweiterte Spenderkriterien erfüllen, verringert die Wartelistenmortalität mit einem erhöhten Risiko für das Patienten- und Transplantatüberleben nach Lebertransplantation. Die Eignung der Anzahl der erfüllten erweiterten Spenderkriterien nach der aktuellen Definition der Bundesärztekammer (BÄK-Score) für die Voraussage der frühen Ergebnisse nach Lebertransplantation ist unbekannt.
Patientenkollektiv
Untersucht wurden 257 erwachsene Empfänger, die zwischen dem 01.01.2007 und dem 31.12.2010 insgesamt 291 konsekutive Lebertransplantate erhielten.
Methoden
Primäre Studienendpunkte waren die 30-Tage-Mortalität, 3-Monats-Mortalität, das 3-Monats-Patientenüberleben, 3-Monats-Transplantatüberleben und die Notwendigkeit einer akuten Retransplantation innerhalb von 30 Tagen. Der BÄK-Score wurde als prognostisches Modell mit der ROC-Kurven-Analyse mit Bestimmung der Sensitivität, Spezifität und Gesamtmodellkorrektheit des Modells für die Voraussage der primären Studienendpunkte untersucht. Weiterhin wurden Kaplan-Meier-Überlebensanalysen, Log-Rank-Tests, Cox-Regressionsanalysen, logistische Regressionen und χ2-Tests durchgeführt.
Ergebnisse
Die Anzahl der erfüllten erweiterten Spenderkriterien hatte keinen signifikanten Einfluss auf die primären Studienendpunkte (p > 0,05) und das Patientenüberleben (p > 0,05). Die ROC-Kurven-Analyse zeigte für die Voraussage der primären Studienendpunkte Flächen ≤ 0,561 mit einer Gesamtkorrektheit des Modells < 58% bei einer Sensitivität < 52%.
Schlussfolgerung
Die Anzahl der erfüllten erweiterten Spenderkriterien nach der aktuellen Definition der Bundesärztekammer kann die frühe Prognose innerhalb der ersten 3 Monate nach Lebertransplantation als prognostisches Modell nicht voraussagen.
Schlüsselwörter: Lebertransplantation, Warteliste, Mortalität, Prognosemodelle, Spenderkriterien
Abstract
Introduction
Expansion of the donor pool by the use of grafts with extended donor criteria reduces waiting list mortality with an increased risk for graft and patient survival after liver transplantation. The ability of the number of fulfilled extended donor criteria as currently defined by the German Medical Association (BÄK-Score) to predict early outcome is unclear.
Patients
A total of 291 consecutive adult liver transplantations (01.01.2007–31.12.2010) in 257 adult recipients were analyzed.
Methods
Primary study endpoints were 30 day mortality, 3 month mortality, 3 month patient and graft survival and the necessity of acute retransplantation within 30 days. For primary study endpoints a ROC curve analysis was performed to calculate sensitivity, specificity and overall model correctness of the BÄK score as a predictive model. Further methods included Kaplan-Meier estimates, log-rank tests, Cox regression analysis, logistic regression analysis and χ2-tests.
Results
The number of extended donor criteria fulfilled had no statistically significant influence on the primary study endpoints (p > 0.05) or on patient survival (p > 0.05). ROC curve analysis revealed areas under the curve ≤ 0.561 for the prediction of primary study endpoints (overall model correctness < 58%, sensitivity < 52%).
Conclusions
The number of fulfilled extended donor criteria as currently defined by the German Medical Association is unable to predict early outcome after liver transplantation.
Keywords: Liver transplantation, Waiting list, Mortality, Prognostic models, Donor criteria
Der zunehmende Spenderorganmangel hat in Deutschland und im gesamten Eurotransplant-Bereich auf dem Gebiet der Lebertransplantation zu einer zunehmend aggressiven Nutzung von Spenderorganen, die sog. erweiterte Spenderkriterien erfüllen, geführt [2, 3, 8, 11, 12, 13, 14, 17, 18]. In dieser Arbeit wird die Eignung der Anzahl der erfüllten erweiterten Spenderkriterien nach der Definition der Bundesärztekammer als prognostisches Modell für die Voraussage des Patienten- und Transplantatüberlebens in den ersten 3 Monaten nach Lebertransplantation untersucht.
Hintergrund der Untersuchung
Im Mai 2004 wurden im Deutschen Ärzteblatt von der Bundesärztekammer Änderungen der Richtlinien zur Organtransplantation gemäß § 16 des Transplantationsgesetzes publiziert, die auf den Empfehlungen der Ständigen Kommission Organtransplantation beruhen und die u. a. die für die Lebertransplantation spezifizierten erweiterten Spenderkriterien zusammenfassend darstellen, die zur Integration in die Richtlinien für die Organvermittelung zur Lebertransplantation vorgesehen sind [4]. Im Einzelnen handelt es sich hierbei alternativ um 7 erweiterte Spenderkriterien, die in Tab. 1 zusammenfassend dargestellt sind. Die Definition dieser erweiterten Spenderkriterien erfolgte vor dem Hintergrund eines zunehmenden Bewusstseins der potenziell verheerenden Folgen suboptimaler Spenderorgane für das Transplantat- und Patientenüberleben nach Transplantation [2, 3, 8, 11, 12, 13, 14, 17, 18].
| Erweiterte Spenderkriterien | Anzahl |
|---|---|
| Alter des Spenders > 65 Jahre | 30 (10,3%) |
| Intensivtherapie einschließlich Beatmung des Spenders > 7 Tage | 66 (22,7%) |
| BMI des Spenders > 30 | 47 (16,2%) |
| Steatosis hepatis (histologisch gesichert) > 40% | 22 (7,6%) |
| SGOT oder SGPT > 3 × normal (letzter Wert vor der Spendermeldung) | 60 (20,6%) |
| Serumbilirubin > 3 mg/dl (letzter Wert vor der Spendermeldung) | 229 (78,7%) |
| Serumnatrium > 165 mmol/l (letzter Wert vor der Spendermeldung) | 10 (3,4%) |
BMI Body-Mass-Index, SGOT Serum-Glutamat-Oxalacetat-Transaminase, SGPT Serum-Pyruvat-Oxalacetat-Transaminase.
In Deutschland hat die Einführung der MELD („model for end-stage liver disease“) -basierten Organallokation für Spenderlebern im Dezember 2006 zu einer von ca. 20% auf ca. 10% verringerten Wartelistenmortalität bei gleichzeitig vermindertem Einjahresüberleben nach Lebertransplantation von fast 90% auf unter 80% geführt [15, 19]. Nach der Einführung der MELD-basierten Organallokation ist die Schwelle für realisierte Transplantationen von einem matchMELD von initial 25 Punkten auf mittlerweile 34 Punkte angestiegen [15]. Währenddessen wurde bei der Spenderorganqualität ein kontinuierlicher Rückgang in den meisten Ländern des Eurotransplant-Bereiches in den letzten 10 bis 15 Jahren beobachtet [15].
Die Expansion des limitierten Spenderpools durch die zunehmende Verwendung von Spenderlebern, die erweiterte Spenderkriterien erfüllen, geht mit einer Reduktion der Wartelistenmortalität und einer potenziellen Zunahme des Risikos für das Patientenüberleben und das Transplantatüberleben einher [2, 3, 8, 11, 12, 13, 14, 17, 18]. Dieses Dilemma zeigt, dass zuverlässige prognostische Modelle, die relevante Spendervariablen kombinieren, für die Voraussage des Patienten- und Transplantatüberlebens nach Lebertransplantation gebraucht werden, um die Optimierung der Spenderorganallokationsregeln und individuelle Spenderorganakzeptanzentscheidungen für Empfänger mit bestimmten klinischen Risikoprofilen vor der Transplantation unterstützen zu können. Dieses Szenario hat zu mehreren Versuchen geführt, das Spenderorganrisiko für den Empfänger zu beschreiben und mit Scores, z. B. mit dem in den USA für die amerikanischen Verhältnisse entwickelten Donor-Risk-Index, möglichst objektiv zu erfassen [5, 7].
Patienten und Methoden
Klinische und demographische Eigenschaften des untersuchten Kollektivs
Wir haben 291 konsekutive Lebertransplantationen inklusive 20 (6,9%) Split-Lebertransplantationen, 30 (10,3%) akute Retransplantationen definiert als Retransplantation innerhalb von 30 Tagen nach der vorausgegangenen Transplantation und 25 (8,6%) chronische Retransplantationen, die bei insgesamt 257 Patienten durchgeführt wurden, untersucht. Hierbei waren primäre Lebertransplantationen (n = 235), sekundäre Lebertransplantationen (1. Retransplantationen, n = 48), tertiäre Lebertransplantationen (2. Retransplantationen, n = 6) und quartäre Lebertransplantationen (3. Retransplantationen, n = 1) vertreten. Das Alter der Patienten lag im Durchschnitt bei 49,6 Jahren (18–69 Jahre). Alle Lebertransplantationen wurden bei insgesamt 177 Männern (64,4%) und 114 Frauen (35,6%) durchgeführt. Retransplantationen wurden nicht ausgeschlossen, um die generelle Anwendbarkeit der erweiterten Spenderkriterien nach Definition der Bundesärztekammer für die Voraussage des Überlebens nach Lebertransplantation testen zu können.
Alle Transplantationen in dieser Untersuchung wurden zwischen dem 01.01.2007 und dem 31.12.2010 an der Medizinischen Hochschule Hannover durchgeführt. Das Nachbeobachtungsintervall endete am 31.03.2011.
Die Verteilung der Indikationen, die zur Lebertransplantation im untersuchten Kollektiv geführt haben, sind in Tab. 2 zusammengefasst dargestellt. Die Todesursachen der nach Transplantation verstorbenen Patienten sind in Tab. 3 aufgeführt. In Tab. 4 sind die wichtigsten Spendereigenschaften aller 291 hirntoten Organspender zum Zeitpunkt der Organspende zusammengefasst.
| Indikationen | Anteil im Kollektiv |
|---|---|
| (%) | |
| Akutes Leberversagen | 10,3 |
| Alkoholbedingte Leberzirrhose | 8,6 |
| α-1-Antitrypsinmangel | 1,4 |
| Autoimmunhepatitis | 1,0 |
| Gallengangsatresie | 0,7 |
| Budd-Chiari-Syndrom | 2,1 |
| Kryptogene Leberzirrhose | 5,5 |
| Familliäre amyloidotische Polyneuropathie | 1,0 |
| Zirrhose bei chronischer HBV- + HCV-Infektion | 0,3 |
| Zirrhose bei chronischer HBV-Infektion | 4,5 |
| Hepatozelluläres Karzinom | 19,6 |
| Zirrhose bei chronischer HCV-Infektion | 5,5 |
| Intrahepatisches cholangiozelluläres Karzinom | 0,7 |
| Morbus Osler/Hämangiom | 0,3 |
| Neuroendokrine Lebermetastasen | 1,0 |
| Andere | 0,7 |
| Oxalose | 0,3 |
| Primär biliäre Zirrhose | 2,7 |
| Polyzystische Lebererkrankung | 3,4 |
| Primär sklerosierende Cholangitis | 8,2 |
| Re-TX wegen biliärer Komplikationen | 3,4 |
| Re-TX wegen chronischen Transplantatversagens | 5,5 |
| Re-TX wegen chronischer Abstoßung | 1,0 |
| Re-TX wegen primären Transplantatversagens (INF) | 6,2 |
| Re-TX wegen rekurrenter viraler Hepatitis | 0,3 |
| Re-TX wegen vaskulärer Komplikationen | 2,4 |
| Sekundäre biliäre Zirrhose | 1,7 |
| Morbus Wilson | 1,4 |
| Total | 100,0 |
HBV Hepatitis-B-Virus, HCV Hepatitis-C-Virus, INF initiale Nichtfunktion, Re-TX Retransplantation.
| Todesursache | Anteil im Kollektiv |
|---|---|
| (%) | |
| Kardiovaskuläres Ereignis | 12,2 |
| Hirnblutung | 2,1 |
| Zerebrale Ischämie | 4,7 |
| Unklare Ursache wegen mangelnder Daten | 10,5 |
| De-novo-Malignom | 3,2 |
| Gastrointestinale Ischämie | 3,2 |
| Gastrointestinale Perforation | 2,1 |
| Pilzinfektion | 5,8 |
| Sepsis | 21,1 |
| Intraabdominelle Blutung | 4,7 |
| Gallengangskomplikationen am Transplantat | 12,2 |
| Initiales Transplantatversagen | 2,1 |
| ARDS | 8,5 |
| Pneumonie | 3,2 |
| Polytrauma | 0,6 |
| Suizid | 0,6 |
| Tumorrezidiv | 3,2 |
| Gesamt | 100,0 |
ARDS „acute respiratory distress syndrome“.
| Median | MW | Min | Max | SD | IQR | |
|---|---|---|---|---|---|---|
| Donor-Risk-Indexa | 1,6 | 1,6 | 0,97 | 2,8 | 0,94 | 1 |
| ECD-Scorea | 2 | 1,8 | 0 | 4 | 0,33 | 0,45 |
| Spenderalter (Jahre) | 51 | 48 | 12 | 74 | 14,5 | 16,5 |
| Krankenhausaufenthalt des Spenders (Tage) | 4 | 5 | 1 | 51 | 5 | 4 |
| Spendergröße (cm) | 175 | 174 | 140 | 200 | 9 | 12 |
| Spendergewicht (kg) | 80 | 80 | 40 | 160 | 17 | 20 |
| Spender-BMI | 25 | 26 | 14 | 55 | 5 | 5 |
| Kalte Ischämiezeit (min) | 576 | 585 | 144 | 1098 | 157 | 178 |
| Warme Ischämiezeit (min) | 45 | 47 | 23 | 180 | 15 | 15 |
| Serumnatrium (mmol/l) | 148 | 148 | 130 | 189 | 7,9 | 10 |
| SGOT/AST (U/l) | 46 | 79 | 8 | 831 | 422 | 47 |
| SGPT/ALT (U/l) | 32 | 64 | 1 | 1136 | 268 | 41 |
| Serumbilirubin (µmol/l) | 9 | 11 | 1 | 85 | 15 | 8 |
Die präoperativen labMELD-Scores der Organempfänger lagen in dieser Untersuchung im Durchschnitt bei 22,2 Punkten (6–40 Punkte, Median: 20 Punkte; Interquartilsabstand (IQR): 21 Punkte). Ein labMELD-Score im Bereich von 0 bis 24 Punkten wurde in 167 Fällen und ein labMELD-Score im Bereich von 25 bis 40 Punkten wurde in 124 Fällen vor Transplantationen festgestellt.
Datenerhebung
Es handelt sich um eine retrospektive unizentrische Untersuchung mit kontinuierlicher Datenerhebung in einem deutschen Universitätsklinikum im Eurotransplant-Bereich.
Ein- und Ausschlusskriterien
Eingeschlossen wurden alle konsekutiven Lebertransplantationen bei erwachsenen Empfängern mit einem Mindestalter von 18 Jahren. Ausgeschlossen wurden alle kombinierten Transplantationen (z. B. kombinierte Leber- und Nierentransplantationen) und alle Empfänger, die ein Organ von einem lebenden Spender erhielten.
Studienendpunkte
Die primären Studienendpunkte waren die 30-Tage-Mortalität, die 3-Monats-Mortalität, das 3-Monats-Patientenüberleben, das 3-Monats-Transplantatüberleben und die Notwendigkeit einer akuten Retransplantation innerhalb von 30 Tagen. Sekundäre Studienendpunkte waren die Krankenhausaufenthaltsdauer und die Intensivaufenthaltsdauer in Tagen.
Statistische Methodik
Der statistische Einfluss der Anzahl der erfüllten erweiterten Spenderkriterien auf die 30-Tage-Mortalität, die 3-Monats-Mortalität, das 3-Monats-Patientenüberleben, das 3-Monats-Transplantatüberleben und die Notwendigkeit einer akuten Retransplantation innerhalb von 30 Tagen wurde mit dem χ2-Test und der logistischen Regression untersucht. Der statistische Einfluss der Anzahl der erfüllten erweiterten Spenderkriterien auf das Patientenüberleben in Tagen wurde mit der Cox-Regressionsanalyse untersucht.
Die Anzahl der erfüllten erweiterten Spenderkriterien nach Definition der Bundesärztekammer wurde als prognostisches Modell für die Voraussage der primären Studienendpunkte (30-Tage-Mortalität, 3-Monats-Mortalität, 3-Monats-Patientenüberleben, 3-Monats-Transplantatüberleben und die Notwendigkeit einer akuten Retransplantation innerhalb von 30 Tagen) mit der ROC („receiver operating characteristic“) -Kurven-Analyse untersucht. Hierbei wurde die Fläche unter der ROC-Kurve (AUROC), die Sensitivität, Spezifität und die generelle Korrektheit (generelle Korrektheit = [Sensitivität + Spezifität]: 2) der Voraussagen bestimmt [6, 9]. Die Cut-off-Werte wurden mit dem besten Youden-Index festgelegt (Youden-Index = Sensitivität + Spezifität – 1) [20].
Die Kaplan-Meier-Überlebensanalyse mit dem Log-Rank-Test wurde verwendet, um den statistischen Einfluss der Anzahl der erfüllten erweiterten Spenderkriterien auf das Transplantat- und Patientenüberleben in Tagen zusätzlich testen zu können. Dabei erfolgte für die verschiedenen primären Studienendpunkte die Gruppeneinteilung nach der Anzahl der erfüllten erweiterten Spenderkriterien ober- bzw. unterhalb der für den jeweiligen Studienendpunkt mit dem besten Youden-Index gefundenen Cut-off-Werte.
Für alle statistischen Tests wurde ein p-Wert kleiner als 0,05 als signifikant definiert. Alle statistischen Tests wurden mit der Statistiksoftware PASW Version 18.0 von IBM (Somers, NY, USA) durchgeführt.
Ergebnisse
Bei Empfängern mit einem niedrigen präoperativen labMELD-Score (< 25 Punkte, n = 167) war die Anzahl der erfüllten Spenderkriterien nach Definition der Bundesärztekammer statistisch signifikant höher als bei Patienten mit einem hohen präoperativen labMELD-Score (≥ 25 Punkte, n = 124) (durchschnittliche Anzahl der erfüllten erweiterten Spenderkriterien 1,49 vs. 1,26; p < 0,001; χ2). Die Kaplan-Meier-Überlebensanalyse zeigte, dass bei den Empfängern mit einem niedrigen labMELD-Score < 25 Punkte zum Zeitpunkt der Transplantation das postoperative Überleben signifikant besser (p = 0,008, Log-Rank-Test) war als bei Empfängern mit einem höheren labMELD-Score ≥ 25 Punkte.
Die Anzahl der erfüllten erweiterten Spenderkriterien hatte keinen statistisch signifikanten Einfluss auf die 30-Tage-Mortalität, die 3-Monats-Mortalität, das 3-Monats-Patientenüberleben, das 3-Monats-Transplantatüberleben und auf die Notwendigkeit einer akuten Retransplantation innerhalb von 30 Tagen (χ2: p > 0,05; logistische Regression: p > 0,05) und auf das Transplantat- und Patientenüberleben in Tagen (Cox-Regressionsanalyse: p > 0,05).
Die Anzahl der erfüllten erweiterten Spenderkriterien nach Definition der Bundesärztekammer zeigte als prognostisches Modell für die Voraussage der primären Studienendpunkte (30-Tage-Mortalität, 3-Monats-Mortalität, 3-Monats-Patientenüberleben, 3-Monats-Transplantatüberleben und die Notwendigkeit einer akuten Retransplantation innerhalb von 30 Tagen) in der ROC-Kurven-Analyse jeweils Flächen unter der ROC-Kurve (AUROC) ≤ 0,561 mit einer Gesamtkorrektheit des Modells < 58% und einer Sensitivität < 52% (Details s. Tab. 5 und Tab. 6). Bezüglich der Voraussage der Notwendigkeit einer akuten Retransplantation innerhalb von 30 Tagen zeigte die Anzahl der erfüllten Spenderkriterien in der ROC-Kurven-Analyse eine Sensitivität von 0% bei einer Spezifität von 99,2%, was einer Gesamtkorrektheit (Gesamtkorrektheit = [Sensitivität + Spezifität]: 2) der Voraussage von lediglich 49,6% entspricht (Tab. 6). Auch nach Ausschluss aller Retransplantationsfälle zeigte die Anzahl der erfüllten erweiterten Spenderkriterien nach Definition der Bundesärztekammer als prognostisches Modell für die Voraussage der primären Studienendpunkte in der ROC-Kurven-Analyse in keinem Fall eine Fläche unter der ROC-Kurve an, die größer als 0,7 war.
| Studienendpunkte | AUROC | Standardfehler | Asymptotische Signifikanz | Asymptomatisches 95%-KI | |
|---|---|---|---|---|---|
| Unteres Limit | Oberes Limit | ||||
| 30-TM | 0,538 | 0,053 | 0,460 | 0,434 | 0,614 |
| 3-MM | 0,561 | 0,043 | 0,144 | 0,477 | 0,646 |
| 3-MPÜ | 0,424 | 0,043 | 0,073 | 0,339 | 0,509 |
| 3-MTÜ | 0,446 | 0,038 | 0,157 | 0,371 | 0,521 |
| Akute ReTX | 0,371 | 0,047 | 0,020 | 0,279 | 0,462 |
AUROC Flächen unter den ROC-Kurven, KI Konfidenzintervall, ROC „receiver operating characteristics“.30-TM 30-Tage-Mortalität, 3-MM 3-Monats-Mortalität, 3-MPÜ 3-Monats-Patientenüberleben, 3-MTÜ 3-Monats-Transplantatüberleben, akute ReTX Notwendigkeit einer akuten Retransplantation innerhalb von 30 Tagen.
| Studienendpunkte | Cut-off-Werte | Bester Youden-Index | Sensitivität | Spezifität | Gesamtkorrektheit | |
|---|---|---|---|---|---|---|
| (%) | (%) | (%) | ||||
| Anzahl der erfüllten erweiterten Spenderkriterien | 30-TM | 1,5 | 0,108 | 48,6 | 62,2 | 55,4 |
| 3-MM | 1,5 | 0,158 | 51,7 | 64,1 | 57,9 | |
| 3-MPÜ | 1,5 | −0,178 | 35,6 | 46,6 | 41,1 | |
| 3-MTÜ | 1,5 | −0,123 | 35,8 | 51,9 | 43,9 | |
| Akute ReTX | 3,5 | −0,008 | 0,0 | 99,2 | 49,6 |
30-TM 30-Tage-Mortalität, 3-MM 3-Monats-Mortalität, 3-MPÜ 3-Monats-Patientenüberleben, 3-MTÜ 3-Monats-Transplantatüberleben, akute ReTX Notwendigkeit einer akuten Retransplantation innerhalb von 30 Tagen.
Die mit dem besten Youden-Index festgelegten Cut-off-Werte lagen für die primären Studienendpunkte 30-Tage-Mortalität, 3-Monats-Mortalität, 3-Monats-Patientenüberleben und 3-Monats-Transplantatüberleben bei 1,5 erfüllten erweiterten Spenderkriterien nach Definition der Bundesärztekammer und für den primären Studienendpunkt Notwendigkeit einer akuten Retransplantation innerhalb von 30 Tagen bei 3,5 erfüllten erweiterten Spenderkriterien (Tab. 6).
Die Kaplan-Meier-Überlebensanalyse konnte keinen statistisch signifikanten Einfluss eines oder mehrerer erfüllter erweiterter Spenderkriterien auf das Transplantat- und Patientenüberleben zeigen (p > 0,05; Log-Rank-Test). Auch für die Tatsache, ob mehr oder weniger als 1,5 erweiterte Spenderkriterien (ober- bzw. unterhalb des mit dem besten Youden-Index ermittelten Cut-off-Wertes 1,5) erfüllt waren, konnte in der Kaplan-Meier-Überlebensanalyse kein statistisch signifikanter Einfluss auf das Transplantatüberleben in Tagen (p > 0,05; Log-Rank-Test) und Patientenüberleben in Tagen gezeigt werden (p > 0,05; Log-Rank-Test).
Die Anzahl der erweiterten Spenderkriterien nach Definition der Bundesärztekammer hatte keinen statistisch signifikanten Einfluss auf die Dauer des Krankenhausaufenthaltes in Tagen (p > 0,05; Log-Rank-Test) und die Dauer des Intensivaufenthaltes in Tagen (p > 0,05; Log-Rank-Test).
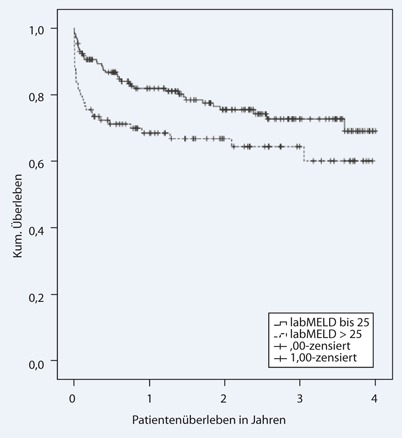
Von den untersuchten 291 konsekutiven Lebertransplantationen wurden nur 23 (7,9%) mit Transplantaten durchgeführt, für die keines der erweiterten Spenderkriterien nach Definition der Bundesärztekammer zutraf. Das bedeutet, dass in den letzen Jahren 92,1% (n = 268) der Spenderorgane aller hier untersuchten konsekutiven Lebertransplantationen mit Transplantaten durchgeführt wurden, für die mindestens ein erweitertes Spenderkriterium nach Definition der Bundesärztekammer zutraf. Der Vergleich des Patientenüberlebens nach Transplantation von Spenderorganen, für die keines der erweiterten Spenderkriterien nach Definition der Bundesärztekammer zutraf (n = 23) mit dem Patientenüberleben nach Transplantation von Spenderorganen, die mindestens ein erweitertes Spenderkriterium nach Definition der Bundesärztekammer erfüllten, zeigt in der Kaplan-Meier-Analyse keinen statistisch signifikanten Unterschied (p = 0,758, Log Rank). Interessanterweise war das Patientenüberleben nach Kaplan-Meier bei den Patienten, die ein Spenderorgan erhielten, das mindestens ein erweitertes Spenderkriterium nach Definition der Bundesärztekammer erfüllte (n = 268), dann signifikant schlechter, wenn diese Patienten vor der Transplantation einen labMELD-Wert über 25 Punkte hatten (n = 98; p = 0,020; Log Rank; Abb. 1). Diese Beobachtung trifft analog auch auf das Transplantatüberleben zu. Bei den Patienten, die ein Organ mit mindestens einem erweiterten Spenderkriterium erhielten, war das Transplantatüberleben dann signifikant schlechter, wenn der präoperative labMELD-Wert über 25 Punkte lag (n = 98; p = 0,028; Log Rank).
Diskussion
Die vorgestellte Analyse reflektiert eine unizentrische Erfahrung mit einem vergleichsweise kleinen Kollektiv an einem großen deutschen Transplantationszentrum im Eurotransplant-Bereich. Die Limitationen einer solchen Untersuchung können zu einem gewissen Grad auf der Bias der Zentrumserfahrung auf dem Gebiet der Lebertransplantation beruhen, da individuelle Spenderorganakzeptanzentscheidungen hierdurch schwer quantifizierbar und reproduzierbar beeinflusst werden können. Das kann dazu führen, dass prognostische Modelle, die wesentliche unbekannte, lokal relevante Entscheidungsfaktoren für Spenderorganakzeptanzentscheidungen nicht berücksichtigen, im klinischen Alltag vor Ort unbrauchbar werden. Volk et al. haben den Einfluss der auf spezifischer Zentrumserfahrung und lokalem Wettbewerb um verfügbare Spenderorgane beruhenden Bias auf Variationen der beobachteten Spenderorganqualität transplantierter Organ an verschiedenen Zentren in den USA beschrieben [18]. Hierbei konnte gezeigt werden, dass die Akzeptanz von Organen mit einem hohen Donor-Risk-Index insbesondere bei Patienten mit niedrigen labMELD-Scores vor der Transplantation zu einer Zunahme der postoperativen Mortalität führt [18]. Die Tatsache, dass in dieser Studie bei Empfängern mit einem niedrigen präoperativen labMELD-Score (< 25 Punkte, n = 167) die Anzahl der erfüllten erweiterten Spenderkriterien nach Definition der Bundesärztekammer statistisch signifikant höher war als bei Patienten mit einem hohen präoperativen labMELD-Score (> 25 Punkte, n = 124) bei trotzdem signifikant besserem Überleben der Empfänger mit einem niedrigeren labMELD-Score deutet auf eine möglicherweise spezifisch zentrumsbedingte Bias in unserem Zentrum in Hannover hin. Passend zu den Ergebnissen von Volk et al. [18] zeigt die vorliegende Studie, dass bei den Empfängern mit einem niedrigen labMELD-Score < 25 Punkte vor der Transplantation das postoperative Überleben signifikant besser (p = 0,008, Log-Rank-Test) war als bei Empfängern mit einem höheren labMELD-Score > 25 Punkte.
Eine relevante methodische Limitation für alle Untersuchungen zur Brauchbarkeit von Spenderrisikoscores als prognostische Modelle wird durch die Tatsache bedingt, dass es keinen anderen verfügbaren Spenderpool außer der Lebendspende mit erwarteten deutlich besseren Ergebnissen bezüglich der beobachteten Spenderorganqualität gibt. Trotzdem zeigt die tägliche klinische Erfahrung, dass die Qualität der Spenderorgane offensichtlich eine wichtige Rolle für die Prognose nach Lebertransplantation spielt und das obwohl es notorisch schwierig ist, die Spenderorganqualität objektiv zu erfassen und den Effekt der Spenderorganqualität objektiv zu bestimmen [2, 3, 8, 11, 12, 13, 14, 17, 18]. Die subjektive chirurgische Erfahrung legt nahe, dass die Spenderorganqualität während der Organentnahme oder kurz vor der Implantation bei der Inspektion leicht erkannt werden kann. Vor diesem Hintergrund wurden die erweiterten Spenderkriterien nach der Definition der Bundesärztekammer im Jahre 2004 im Deutschen Ärzteblatt publiziert, nachdem diese von der Ständigen Kommission Organtransplantation empfohlen wurden [4]. Eine Überprüfung der Eignung dieser erweiterten Spenderkriterien als prognostisches Modell für die Voraussage des Patienten- und Transplantatüberlebens in den ersten 3 Monaten oder der Notwendigkeit einer akuten Retransplantation in den ersten 30 Tagen erfolgte bisher noch nicht.
Diese Untersuchung zeigt, dass die Anzahl der erweiterten Spenderkriterien nach der Definition der Bundesärztekammer die frühe Prognose nach Lebertransplantation innerhalb der ersten 3 Monate als prognostisches Modell im untersuchten Kollektiv nicht voraussagen kann, weil die Gesamtkorrektheit des Modells für die Voraussage der 30-Tage-Mortalität, der 3-Monats-Mortalität, des 3-Monats-Patientenüberlebens, des 3-Monats-Transplantatüberlebens und der Notwendigkeit einer akuten Retransplantation innerhalb von 30 Tagen jeweils unter 58% liegt ( Tab. 5). Diese Interpretation wird dadurch untermauert, dass die Flächen unter der ROC-Kurve für die Anzahl der erweiterten Spenderkriterien für die Voraussage dieser primären Studienendpunkte in jedem Fall < 0,561 ist und somit deutlich unter der kritischen Mindestfläche von 0,7 liegt, die in der Literatur für ein klinisch sinnvoll brauchbares prognostisches Modell in der ROC-Kurven-Analyse gefordert wird [6, 9]. Darüber hinaus liegt die Sensitivität der Anzahl der erfüllten erweiterten Spenderkriterien für die Voraussage sämtlicher primärer Studienendpunkte unter 52% und ist damit für ein klinisch brauchbares prognostisches Modell inakzeptabel niedrig. Hierzu passend zeigt diese Untersuchung, dass die Anzahl der erfüllten erweiterten Spenderkriterien keinen statistisch signifikanten Einfluss auf die 30-Tage-Mortalität, die 3-Monats-Mortalität, das 3-Monats-Patientenüberleben, das 3-Monats-Transplantatüberleben und die Notwendigkeit einer akuten Retransplantation innerhalb von 30 Tagen (χ2: p > 0,05; logistische Regression: p > 0,05) und auf das Transplantat- und Patientenüberleben in Tagen (Cox-Regressionsanalyse: p > 0,05) hatte. Man würde zu Recht erwarten können, dass ein Spenderrisikoscore als zuverlässiges und glaubwürdiges prognostisches Modell einen statistisch signifikanten Einfluss auf die Entwicklung eines initialen Transplantatversagens nach Lebertransplantation hat.
Es passt in das oben gezeichnete Bild, dass diese Untersuchung zeigen konnte, dass in der Kaplan-Meier-Überlebensanalyse kein statistisch signifikanter Einfluss eines oder mehrerer erfüllter erweiterter Spenderkriterien auf das Transplantat- und Patientenüberleben gezeigt werden konnte (p > 0,05; Log-Rank-Test).
In diesem Licht erscheint es letztlich wenig überraschend, dass die Anzahl der erweiterten Spenderkriterien nach Definition der Bundesärztekammer auch keinen statistisch signifikanten Einfluss auf die Dauer des Krankenhausaufenthaltes in Tagen (p > 0,05; Log-Rank-Test) oder die Dauer des Intensivaufenthaltes in Tagen (p > 0,05; Log-Rank-Test) nach Durchführung der Lebertransplantation hatte.
Die Ergebnisse dieser Untersuchung zeigen, dass die Anzahl der erweiterten Spenderkriterien nach der aktuellen Definition der Bundesärztekammer für individuelle Spenderorganakzeptanzentscheidungen zur Lebertransplantation kaum hilfreich herangezogen werden kann. Offensichtlich gibt es diesbezüglich immer noch keine Alternative zur spezifischen chirurgischen Erfahrung auf dem Gebiet der Lebertransplantation.
Andere aktuelle Untersuchungen zum Einfluss der erweiterten Spenderkriterien auf die Prognose nach Lebertransplantation kommen zu ähnlichen Ergebnissen. Frühauf et al. konnten z. B. an einem größeren Datenpool zeigen, dass die Kombination der Spender- und Empfängereigenschaften entscheidend für die Prognose nach Lebertransplantation ist und nicht die alleinige Tatsache, ob erweiterte Spenderkriterien vorliegen [8]. Die einzige Ausnahme scheint im Gegensatz zu unseren Ergebnissen das Spenderalter zu sein. Eine spanische Arbeitsgruppe kam zu einem ähnlichen Ergebnis, das ebenfalls auf die große Bedeutung der Kombination der Spender- und Empfängervariablen hinweist. Hier war das schlechteste Szenario für das Transplantatüberleben mit der höchsten Wahrscheinlichkeit für die Entwicklung einer primären Transplantatdysfunktion nach Lebertransplantation dann gegeben, wenn 3 oder mehr erweiterte Spenderkriterien und ein labMELD-Score ≥ 29 zusammentrafen [3]. Die genaue Definition der erweiterten Spenderkriterien weicht in dieser Studie jedoch von der aktuellen Definition der Bundesärztekammer ab. Aus unserer Sicht kommt hier das Problem zum Tragen, dass es bisher keine universell akzeptierten erweiterten Spenderkriterien gibt [3, 8, 11, 12, 13, 14]. In unserer Studie hatte die Anzahl der erfüllten erweiterten Spenderkriterien nach der Definition der Bundesärztekammer keinen Einfluss auf die Prognose nach Lebertransplantation. Zu einem vergleichbaren Ergebnis kam die Heidelberger Arbeitsgruppe in einer Kohorte mit 165 Lebertransplantationen, die zwischen 2001 und 2004 durchgeführt wurden, bevor die erweiterten Spenderkriterien der Bundesärztekammer eingeführt wurden [14]. Die Heidelberger Arbeitsgruppe hat teilweise dieselben erweiterten Spenderkriterien untersucht wie unsere Studie. Allerdings wurde in der Heidelberger Untersuchung die Anzahl der erfüllten erweiterten Spenderkriterien nicht als prognostisches Modell betrachtet und nicht mit der ROC-Kurven-Analyse untersucht.
Aus unserer Sicht ist es wichtig, dass die erweiterten Spenderkriterien nach Definition der Bundesärztekammer nach deren Einführung bezüglich ihrer Bedeutung als prognostisches Modell evaluiert werden, da diese nach § 16 des Transplantationsgesetzes Einfluss auf die Richtlinien für die Organvermittelung zur Lebertransplantation haben. Aus unserer Sicht konnte u. a. aufgrund der Ergebnisse unserer Untersuchung für die Einführung dieser erweiterten Spenderkriterien bisher keine ausreichend gut fundierte wissenschaftliche Grundlage gezeigt werden. Die Berliner Arbeitsgruppe hat bereits 2008 darauf hingewiesen, dass speziell bei schwerkranken Patienten die Rolle der erweiterten Spenderkriterien für die Prognose nach Lebertransplantation entscheidend wichtig sein wird [11]. Dies können unsere Daten in gewisser Weise bestätigen. In unserer Untersuchung waren das Patienten- und das Transplantatüberleben bei den Patienten, die ein Spenderorgan mit erweiterten Spenderkriterien erhielten, dann signifikant schlechter, wenn der präoperative labMELD-Score > 25 war (Abb. 1).
Die Falsifizierbarkeit von Hypothesen, wie sie vom Erkenntnistheoretiker Karl Raimund Popper [10] in seinem epochalen Werk Logik der Forschung [8] definiert wurde, definiert die inhärente Testbarkeit jedweder wissenschaftlichen Hypothese. Auf der Grundlage der Ergebnisse dieser Studie erscheint die Hypothese, dass die Anzahl der erfüllten erweiterten Spenderkriterien nach der aktuellen Definition der Bundesärztekammer als prognostisches Modell für die Voraussage der Prognose nach Lebertransplantation innerhalb der ersten 3 Monate vor dem Hintergrund der aktuellen Allokationsregeln für Lebertransplantate herangezogen werden kann, als widerlegt.
Fazit
Die Anzahl der erweiterten Spenderkriterien nach der aktuellen Definition der Bundesärztekammer kann die frühe Prognose nach Lebertransplantation als prognostisches Modell unter den aktuellen Bedingungen nicht voraussagen.
Für den aktuellen Spenderpool in Deutschland und im Eurotransplant-Bereich ist eine Neudefinition der erweiterten Spenderkriterien für die Lebertransplantation notwendig.
Neu definierte erweiterte, prognoserelevante Spenderkriterien sollten möglichst auf einem hohen Evidenzgrad nach den Kriterien der evidenzbasierten Medizin beruhen.
Aussagekräftige Prognosescores werden gebraucht, um die aktuellen Allokationsregeln für Spenderlebern im Sinne einer Verbesserung der Ergebnisse nach Lebertransplantation, wie im Transplantationsgesetz gefordert, gezielt optimieren zu können.
Für die Entwicklung eines aussagekräftigen Prognosescores ist ein multizentrischer Ansatz notwendig, um den Einfluss eines möglichen Zentrumsbias möglichst gering zu halten.
Acknowledgments
Interessenkonflikt
Der korrespondierende Autor gibt für sich und seine Koautoren an, dass kein Interessenkonflikt besteht.
Footnotes
Die Autoren H. Schrem und B. Reichert haben zu gleichen Teilen zu diesem Artikel beigetragen.
Literatur
- 1.Barshes Am J Transplant. 2007;7:1265. doi: 10.1111/j.1600-6143.2007.01758.x. [DOI] [PubMed] [Google Scholar]
- 2.Bonney Transplantation. 2009;87:1858. doi: 10.1097/TP.0b013e3181a75b37. [DOI] [PubMed] [Google Scholar]
- 3.Briceño Transplantation. 2010;90:530. doi: 10.1097/TP.0b013e3181e86b11. [DOI] [PubMed] [Google Scholar]
- 4.Bundesärztekammer Dtsch Arztebl. 2004;5:246. [Google Scholar]
- 5.Cameron Ann Surg. 2006;243:748. doi: 10.1097/01.sla.0000219669.84192.b3. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 6.Cholongitas Aliment Pharmacol Ther. 2006;24:453. doi: 10.1111/j.1365-2036.2006.02998.x. [DOI] [PubMed] [Google Scholar]
- 7.Feng Am J Transplant. 2006;6:783. doi: 10.1111/j.1600-6143.2006.01242.x. [DOI] [PubMed] [Google Scholar]
- 8.Frühauf Transplantation. 2011;92:1378. doi: 10.1097/TP.0b013e318236cd2f. [DOI] [PubMed] [Google Scholar]
- 9.Hanley Radiology. 1982;143:29. [Google Scholar]
- 10.Karl Raimund Popper (2004) The logic of scientific discovery. Taylor and Francis, London, S 1–544
- 11.Mittler Transplantation. 2008;86:895. doi: 10.1097/TP.0b013e318186ad7a. [DOI] [PubMed] [Google Scholar]
- 12.Nickkholgh Nephrol Dial. 2007;Transplant:29. [Google Scholar]
- 13.Pratschke Chirurg. 2008;79:130. doi: 10.1007/s00104-007-1458-6. [DOI] [PubMed] [Google Scholar]
- 14.Schemmer Transplant Proc. 2007;39:529. doi: 10.1016/j.transproceed.2006.12.002. [DOI] [PubMed] [Google Scholar]
- 15.Schlitt Z Gastroenterol. 2011;49:30. doi: 10.1055/s-0029-1245946. [DOI] [PubMed] [Google Scholar]
- 16.Tector Ann Surg. 2006;244:439. doi: 10.1097/01.sla.0000234896.18207.fa. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 17.Volk Gastroenterology. 2008;135:1568. doi: 10.1053/j.gastro.2008.08.003. [DOI] [PubMed] [Google Scholar]
- 18.Volk Am J Transplant. 2011;11:958. doi: 10.1111/j.1600-6143.2011.03487.x. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 19.Weismüller Transpl Int. 2009;22:970. doi: 10.1111/j.1432-2277.2009.00915.x. [DOI] [PubMed] [Google Scholar]
- 20.Youden Cancer. 1950;3:32. doi: 10.1002/1097-0142(1950)3:1<32::AID-CNCR2820030106>3.0.CO;2-3. [DOI] [PubMed] [Google Scholar]


