Zusammenfassung
Das akute Leberversagen (ALV) ist ein seltenes, aber lebensbedrohliches Zustandsbild. Charakteristisch ist das rasche Auftreten eines schweren Leberschadens mit hepatozellulärer Nekrose und eingeschränkter Leberfunktion. Bei weiterhin hoher Mortalität ist ein frühzeitiges Erkennen und Einleiten einer ursachenspezifischen unterstützenden sowie v. a. intensivmedizinischen symptomatischen Therapie essenziell. Durch Fortschritte im Bereich der intensivmedizinischen Behandlung von Patienten mit akutem Leberversagen sowie der Lebertransplantation konnte das Überleben deutlich verbessert werden.
Schlüsselwörter: Akutes Leberversagen, ALV, Intensivmedizin
Abstract
Acute liver failure (ALF) is a rare condition with fatal outcome. Characteristic is rapid onset of liver damage without preexisting liver diseases, including hepatic encephalopathy and coagulopathy. Early and correct diagnosis is essential for further management of patients, since diagnosis impacts therapy choice. Survival of patients with ALF has improved dramatically due to advances in critical care medicine and the use of liver transplantation.
Keywords: Acute liver failure, ALF, Critical care medicine
Das akute Leberversagen (ALV) ist die schwerwiegendste, aber zugleich in Europa auch die mit Abstand seltenste Form der akuten Leberschädigung. Abzugrenzen ist das ALV von dem akut-auf-chronischen Leberversagen, das schwerwiegende Organdysfunktionen und -versagen bei Patienten mit Leberzirrhose umfasst. Die weltweit häufigsten Ursachen eines ALV sind virale Hepatitiden, die Paracetamolintoxikation und medikamentenassoziierte Reaktionen.
Unbehandelt ist die Prognose eingeschränkt, sodass eine zeitgerechte Diagnose und Therapie bei Patienten mit akutem Leberversagen entscheidend ist. Die medizinische Versorgung sollte in einem spezialisierten Zentrum mit intensivmedizinischer Betreuung und der Option auf eine Lebertransplantation erfolgen.
Definition und Diagnose
Das akute Leberversagen (ALV) wird definiert als eine schwerwiegende, potenziell reversible Störung der hepatozellulären Funktion bei Patienten ohne präexistente Lebererkrankung und einer Erkrankungsdauer zwischen 12 und 26 Wochen [1, 2]. Es beinhaltet das Auftreten einer Koagulopathie – definiert als International Normalized Ratio (INR) > 1,5 – und die Entwicklung einer hepatischen Enzephalopathie (HE).
Abhängig vom Manifestationszeitpunkt der Enzephalopathie kann das akute Leberversagen in 3 Subkategorien unterteilt werden [3]:
hyperakutes Leberversagen: <7 Tage,
akutes Leberversagen: 7–21 Tage,
subakutes Leberversagen: >21 Tage und bis <26 Wochen.
Die Subkategorien scheinen mit der Prognose der Erkrankung assoziiert zu sein ([4]; Abb. 1). Zum Beispiel haben Patienten mit hyperakutem Leberversagen eine bessere Langzeitprognose als Patienten mit subakutem Leberversagen. Die häufigste Ursache des hyperakuten Leberversagens ist die Paracetamolintoxikation, die per se mit einer besseren Prognose assoziiert ist [5].
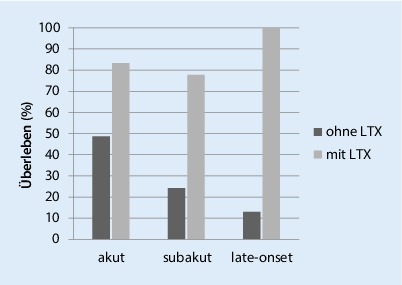
Bei Patienten mit neu aufgetretener kognitiver Einschränkung, Ikterus, Schmerzen im rechten Oberbauch oder weiteren unspezifischen Symptomen, wie Übelkeit und Unwohlsein, sollte grundsätzlich immer auch an die Möglichkeit eines ALV als Ursache der Beschwerden gedacht werden. Zur Abklärung der zugrunde liegenden Ursachen ist eine ausführliche Anamnese notwendig. Diese ist zeitnah durchzuführen, da eine milde HE rasch progredient verlaufen kann. Insbesondere sollten Medikamenteneinnahme, Alkoholkonsum, Pilzkonsum, stattgehabte Auslandsreisen sowie der Impfstatus erörtert werden. Besonderes Augenmerk soll auch auf Hinweise hinsichtlich des Vorliegens einer chronischen Lebererkrankung gelegt werden. Die Erstevaluation beinhaltet die Bestimmung der Transaminasen Glutamat-Oxalacetat-Transaminase (GOT), Glutamat-Pyruvat-Transaminase (GPT) sowie der Cholestaseparameter Gamma-Glutamyl-Transpeptidase (γ-GT), Alkalische Phophatase (AP), direktes und indirektes Bilirubin sowie Glutamat-Pyruvat-Transaminase (GLDH), Laktat-Dehydrogenase (LDH) sowie der Gerinnungsparameter (INR/Normotest, Fibrinogen, Thrombozyten, Faktor V), Serumammoniak (NH3) und Glukose. Zusätzlich sollten ein Differenzialblutbild, Kreatinin, Harnstoff, Elektrolyte, eine arterielle Blutgasanalyse sowie Laktat bestimmt werden.
Die Ursache des akuten Leberversagens kann in lediglich 60–80 % identifiziert werden. Dies ist von besonderer Bedeutung, da die entsprechende Ursache das weitere Management der Erkrankung mit beeinflusst und prognostische Informationen liefert [6]. Typischerweise wird die Diagnose anhand der Anamnese sowie des klinischen Befunds und der Laborparameter gestellt. Eine Bildgebung kann zur Beurteilung der Lebergröße und Leberperfusion hilfreich sein. Eine Leberbiopsie ist in der Regel nicht nötig, kann jedoch in unklaren Fällen zusätzliche Informationen zum Erkrankungsstatus (akut vs. chronisch) liefern. Bei kompromittierter Gerinnung hat die transjuguläre oder auch minilaparoskopische Gewebeentnahme gegenüber der perkutanen Leberbiopsie weniger Blutungskomplikationen [7, 8].
Klinische Symptome
Die klinischen Symptome bei Patienten mit akutem Leberversagen sind meist unspezifisch und können Abgeschlagenheit, Anorexie, Übelkeit, Erbrechen, Ikterus, Pruritus und Schmerzen im rechten Oberbauch beinhalten. Bei Fortschreiten der Erkrankung kann die klassische Trias bestehend aus Ikterus, Koagulopathie und HE beobachten werden.
Das Auftreten einer HE ist ein diagnostisches Charakteristikum des ALV. Die HE wird nach den West-Haven-Kriterien in 4 Stadien eingeteilt (Tab. 1). Der Anstieg von arteriellem Ammoniak sowie viele weitere neurotoxische Substanzen, wie γ‑Aminobuttersäure, Mercaptan und Phenole, tragen zur Entstehung der HE bei. Die Pathogenese der HE und des zerebralen Ödems bei akutem Leberversagen ist nicht vollständig geklärt. Es gibt Hinweise, dass eine systemische und lokale Entzündungsreaktion und zirkulierende Neurotoxine, insbesondere Ammoniak eine wichtige Rolle spielen. Der arterielle Ammoniakspiegel im Blut ist bisher der beste in der klinischen Routine verfügbare Surrogatmarker für eine HE beim ALV. Der wesentliche Stellenwert der Bestimmung des arteriellen Ammoniaks beim ALV liegt darin, dass im Fall einer neuaufgetretenen HE ein deutlicher Anstieg des arteriellen Ammoniaks den klinischen Symptome einer HE um 12–48 Stunden vorausgeht. Das heißt, dass durch zeitnahe Einleitung geeigneter therapeutischer, v. a. intensivmedizinischer Maßnahmen bei erhöhten Ammoniakwerten und noch unauffälligem klinischem Bild effektiv gegengesteuert werden kann. Erhöhte Ammoniakspiegel sind bei ALV mit einer schlechteren Prognose assoziiert [9, 10]. Ferner geht eine Progression der HE mit einer ungünstigen Prognose einher. Der Normalwert des Serumammoniaks beträgt <50 µmol/l. NH3-Werte > 100 µmol/l führen bei 70 % der Patienten zu einer schweren HE. In einer Studie konnte gezeigt werden, dass NH3-Werte > 200 µmol/l im Rahmen eines ALV in mehr als der Hälfte mit einer zerebralen Einklemmung assoziiert waren [10].
| HE-Grad | Neuropsychiatrischer Status | Asterixis |
|---|---|---|
| I |
Euphorie Milde Konfusion Verwaschene Sprache Schlafstörungen |
Möglich |
| II |
Zunehmendes Schlafbedürfnis Moderate Konfusion, inadäquates Verhalten |
Ja |
| III |
Eindeutige Konfusion Verwirrtheit Schläfrig, aber erweckbar |
Ja |
| IV | Koma | Nein |
Eine gefürchtete Komplikation des ALV ist das Hirnödem und der daraus resultierende erhöhte intrakranielle Druck [11]. Zu einem Hirnödem kommt es selten bei einer HE Grad I und II, in etwa 35 % bei HE Grad III und in etwa 75 % bei HE Grad IV. Kommt es zum Auftreten eines erhöhten intrakraniellen Drucks (klinisch oder wenn vorhanden, ICP-Messung ≥ 25 mmHg), ist die Überlebensrate ohne Lebertransplantation sehr eingeschränkt. In der klinischen Untersuchung können Veränderungen der Pupillen auf einen erhöhten Hirndruck hinweisen. Weitere Hinweise wären das Auftreten von Krampfanfällen, Hypertension, Bradykardie oder respiratorische Insuffizienz. Krampfanfälle werden bei Patienten mit akutem Leberversagen nicht selten beobachtet.
Prognostische Evaluation
Eine frühzeitige Risikostratifizierung bei Patienten mit ALV ist wichtig, da im Fall eines raschen Verlaufs mit einer etwaigen raschen Verschlechterung bereits in der Frühphase die Möglichkeit und Notwendigkeit einer Lebertransplantation abgeschätzt werden muss [12]. Verschiedene Scores, wie beispielsweise die King’s-College-Kriterien [13] oder die Clichy-Villejuif-Kriterien [14], stehen zur Verfügung und beinhalten unterschiedliche Variablen. Gemäß der Richtlinien zur Organtransplantation der Bundesärztekammer Deutschland ist die Indikation zur Lebertransplantation bei Patienten mit akutem Leberversagen nach den King’s-College- sowie nach den Spezialkriterien für die Paracetamolintoxikation zu richten. Die Clichy-Kriterien werden für Patienten mit einem akuten Leberversagen auf Basis einer viralen Hepatitis herangezogen, da sie nur im Rahmen eines ALV auf Basis einer HBV-Infektion validiert wurden. (Tab. 2 und 3) Zur Beurteilung der Dringlichkeit wird der Model-for-Endstage-Liver-Disease (MELD)-Score verwendet [15]. Nichtspezifische Scores, wie der MELD-Score oder intensivmedizinische Scores (APACHE II), konnten die Prognoseeinschätzung der Patienten mit ALV bis dato jedoch nicht sicher verbessern [16].
| Faktoren |
|---|
| HE Grad III und IV |
| Und |
| Faktor V < 20 % |
| Alter < 30 Jahre |
| Oder |
| Faktor V < 30 % |
| Alter > 30 Jahre |
| Paracetamol | Andere Ursachen |
|---|---|
| Arterieller pH < 7,3 (unabhängig vom Grad der HE) | Prothrombinzeit < 100 s (= Quick-Wert < 7 % bzw. INR > 6,7) |
| Oder | |
| Alle 3 der folgenden Kriterien | Mindestens 3 der folgenden Kriterien |
| Prothrombinzeit > 100 s (= Quick-Wert < 7 % bzw. INR > 6.7) | Alter < 10 oder > 40 Jahre |
| Kreatinin > 300 mmol/l | Ungünstige Ätiologie (kryptogene Hepatitis, Halothanhepatitis, Medikamententoxizität) |
| HE Grad 3–4 | Zeit von Ikterus bis HE: >7 Tage |
| Prothrombinzeit > 50 s (= Quick-Wert < 15 % bzw. INR > 4) | |
| Bilirubin > 300 mmol/l | |
Ätiologie
Die Ätiologie des ALV ist von prognostischer Bedeutung. Je nach zugrunde liegender Ursache soll neben umfangreichen symptomatischen Therapiemaßnahmen eine ursachenspezifische Therapie eingeleitet werden, wobei hier klar anzumerken ist, dass die wissenschaftliche Evidenz für viele kausale Behandlungsmöglichkeiten in vielen Fällen kaum in der Lage ist, den Level einer Expertenmeinung zu überschreiten [5, 17].
Die Inzidenz des ALV ist in Entwicklungsländern aufgrund von viralen Infektionen deutlich häufiger als in entwickelten Ländern, in denen hygienische Standards und Impfungen vorhanden sind. In westlichen Ländern sind Medikamente, wie Paracetamol die häufigste Ursache für ein akutes Leberversagen [18].
Virale Hepatitiden
Bei allen Patienten mit Verdacht auf ein ALV sollte eine Hepatitisserologie zum Ausschluss einer akuten viralen Infektion durchgeführt werden. Die häufigsten viralen Hepatitiden, die ein ALV auslösen können, sind durch die Hepatitisviren A, B (D) und E verursacht. Ferner ist auch ein ALV durch eine Infektion mit HSV, VZV, EBV, CMV und Adenoviren möglich [2].
In Entwicklungsländern sind virale Infektionen hauptverantwortlich für das Auftreten eines ALV und mit einer Mortalität von mehr als 50 % assoziiert [19]. Die Ansteckung mit Hepatitis-A-Virus erfolgt in aller Regel fäkal-oral. Im Falle einer akuten Hepatitis-A-Infektion entwickeln weniger als 1 % der Patienten ein ALV. Die Hepatitis-E-Infektion ist häufig in Endemiegebieten, wie Russland, Pakistan, Mexiko und Südostasien, und führt in etwa 1 % der Infektionen zum Tod. Auch in Deutschland konnten durchgemachte Hepatitis-E-Infektionen serologisch bei zumindest 17 % der Bevölkerung beobachtet werden [20]. Die überwiegende Anzahl der Infektionen verläuft asymptomatisch und selbstlimitierend, jedoch wurden auch fulminante Verläufe beobachtet. So konnte in einer in Deutschland durchgeführten retrospektiven Studie mit 80 Patienten gezeigt werden, dass bei 10–15 % der Patienten mit ALF HEV-RNA nachweisbar war [21]. Ein Impfstoff wurde in China bereits im Jahr 2012 zugelassen [22]. Der Impfstoff dürfte zuerst in Ländern mit einem erhöhten Risiko für eine Hepatitis-E-Übertragung eingesetzt werden und steht in Deutschland aktuell nicht zur Verfügung.
Das Hepatitis-B-Virus kommt endemisch in asiatischen Ländern sowie Afrika und Südeuropa vor. Die Transmission erfolgt durch Blut und Blutprodukte, vertikal oder im Rahmen sexueller Kontakte. Durch den Einsatz der Impfungen kam es zu einem deutlichen Rückgang der HBV-Infektionen. Die Prävalenz einer akuten oder chronischen Hepatitis-B-Infektion beträgt in Deutschland 0,8 % [23]. Ein akutes Leberversagen im Rahmen einer akuten Hepatitis-B-Infektion ist möglich, jedoch selten (0,1–0,5 %; [24]). Eine Reaktivierung einer stabilen subklinischen Infektion ist durch Chemotherapie oder Immunsuppression jedoch möglich und mit einer schlechten Prognose assoziiert. Eine Identifizierung der Risikopatienten und eine zeitgerechte antivirale Prophylaxe vor Beginn der immunsuppressiven Therapie (Chemotherapie, Kortisontherapie) ist von höchster Bedeutung [25, 26]. Die antivirale Therapie mit einem Nukleosid-/Nukleotidanalogon sollte erst mindestens 6 Monate, besser 12 Monate nach Beendigung der immunsuppressiven Therapie abgesetzt werden. Klinisch verläuft das akute Leberversagen auf Basis einer akuten Hepatitis-B-Infektion eher akut als hyperakut.
Eine Infektion mit dem Hepatitis-C-Virus führt fast nie zu einem akuten Leberversagen [5, 27]. Lediglich im Rahmen einer Koinfektionen mit dem Hepatitis-B-Virus wurden einige wenige fulminante Verläufe berichtet.
Als weitere Ursache für ein akutes Leberversagen wurden hepatotrope Viren, wie Herpes-simplex-1- und -2-Virus, Herpes-zoster-Virus, Ebstein-Barr-Virus oder Zytomegalievirus beschrieben.
Medikamentös-toxisch – Paracetamolintoxikation
Vorweg, Paracetamol ist unter Berücksichtigung einer entsprechenden Dosierung ein sicheres und effektives Analgetikum. Medikamentös-toxische Leberschäden sind für 50 % der akuten Leberversagen in den USA verantwortlich [5, 28]. Im Speziellen ist Paracetamol in den USA und anderen entwickelten Ländern die häufigste Ursache für ein akutes Leberversagen. Eine Intoxikation ist meist dosisabhängig und tritt nur sehr selten in therapeutischen Dosen auf. Die Metabolisierung von Paracetamol erfolgt in der Leber. Die höchste Mortalität konnte bei Patienten mit rezidivierenden Einnahmen über Stunden oder Tage beobachtet werden. Die therapeutische Dosis, die bedenkenlos eingenommen werden kann, beträgt für einen erwachsenen Patienten bis zu 4 g pro Tag. Ein akutes Leberversagen ist meist mit einer Paracetamoldosis von >10 g pro Tag assoziiert, kann jedoch bei speziellen Konstellationen auch bereits bei geringeren Dosen nicht ausgeschlossen werden [29]. Insbesondere eine vorbestehende Lebererkrankung, Malnutrition, Alkoholismus oder eine Komedikamenteneinnahme mit Cytochrom-P450-Induktion (z. B. Antikonvulsiva) können zu klinisch relevanten Leberschädigungen bis hin zum Leberversagen bei Dosen < 10 g führen. Assoziiert mit einer erhöhten Mortalität sind ein erhöhtes Alter, ein Transaminasen- und Bilirubinanstieg und das Vorhandensein einer Koagulopathie. Etwa die Hälfte der Patienten mit einem paracetamolinduzierten Leberversagen entwickeln zusätzlich ein akutes Nierenversagen auf Basis einer akuten Tubulusnekrose sowie einer vaskulär-endothelialen Schädigung [30].
Die Symptome der Paracetamolintoxikation sind anfangs mild und unspezifisch, sodass sich Patienten oft sehr spät an eine medizinische Einrichtung wenden. Da es sich um eine häufige und in der Frühphase kausal gut behandelbare Ursache des ALV handelt, sollte bei jedem Patienten mit Verdacht auf ein ALV ein Paracetamolspiegel bestimmt werden.
Der klinische Verlauf wird in 3 Stadien unterteilt: Zu Beginn zeigt sich eine asymptomatische bis symptomarme Phase mit allgemeinem Krankheitsgefühl und gastrointestinaler Symptomatik (0,5–24 h nach Einnahme). Bei entsprechender Anamnese und Verdachtsdiagnose einer Paracetamolintoxikation sollte der Patient unbedingt weiter stationär behandelt werden. Im weiteren Verlauf, nach subjektiver Besserung, kommt es zu einem Transaminasenanstieg, einer Bilirubinerhöhung sowie beginnender Koagulopathie (etwa 20 h nach Einnahme). Ferner können Oberbauchschmerzen und Ikterus beobachtet werden. Nach 3–4 Tagen kann sich das Vollbild eines ALV mit Ikterus, HE, ausgeprägter Koagulopathie sowie häufig einem akuten Nierenversagen präsentieren.
Der Großteil der Patienten mit einer Paracetamolintoxikation entwickelt jedoch bei frühzeitiger adäquater kausaler Therapie nicht das Vollbild eines ALV. Die Prognose ist bei rascher Diagnosestellung und Therapieeinleitung gut, bei Auftreten einer Enzephalopathie wurde eine Letalität von bis zu 30 % beobachtet.
Medikamentenassoziierte Leberschäden (DILI)
Einige Medikamente wurden mit Leberschäden und dem Auftreten eines ALF in Verbindung gebracht. Auch in diesem Fall ist eine ausführliche Medikamentenanamnese von Bedeutung. Anders als bei der Paracetamolintoxikation ist die Leberschädigung nicht dosisabhängig, sondern beruht auf einer idiosynkratischen Lebertoxizität dieser Medikamente. Lebertoxische Medikamente werden häufig in den Gruppen der Tuberkulostatika, Antiepileptika, Antibiotika usw. gefunden [31]. Häufig werden medikamentenassoziierte Leberschäden in den ersten 6 Monaten nach Medikamenteninitiierung und bei Patienten > 60 Jahre mit dem Bild eines subakuten Leberversagens gesehen, das auch nach Absetzen der Medikamente eine Progression aufweisen kann. Der zugrunde liegende Mechanismus ist bis dato nicht vollständig aufgeklärt. Vermutet wird eine multifaktorielle Genese aus genetischen, chemischen, pharmakologischen und Umweltfaktoren. Die Interaktion aus diesen Faktoren ist verantwortlich für den idiosynkratischen Effekt dieser Medikamente.
Knollenblätterpilzvergiftung
Der dem Champignon ähnelnde Knollenblätterpilz (Amanita phalloides, verna, virosa) ist von Juni bis Oktober zu finden und ist verantwortlich für schwere Pilzvergiftungen. Pilzvergiftungen im Allgemeinen führen zu gastrointestinalen Symptomen mit unterschiedlicher Latenzzeit. Im Generellen haben Pilze mit einer kurzen Latenzzeit (Minuten bis 4 Stunden) meist ein geringes Giftpotenzial, wogegen bei einer Latenzzeit von 12–16 h mit schweren Vergiftungen zu rechnen ist. Kurze Latenzzeiten schließen jedoch schwere Intoxikationen nicht aus. Die Einnahme von geringen Mengen von Amatoxin (7 mg) kann bereits tödlich verlaufen. In der Anamnese sollte eine rezente Pilzeinnahme erhoben werden.
Klinisch verläuft die Amanitaintoxikation in 3 Phasen:
Phase 1: Die Latenzzeit bis zum Auftreten der ersten Symptome ist lang. Das symptomfreie Intervall beträgt etwa 4–48 h. Es folgt das Auftreten von massiven gastrointestinalen Beschwerden, wie Übelkeit/Erbrechen, Koliken und Diarrhöen. In dieser Phase steht der Volumen- und Elektrolytausgleich der Exsikkose im Vordergrund.
Phase 2: Etwa 24–36 Stunden nach Konsum folgt ein symptomfreies, scheinbares Erholungsintervall. Hier besteht die Gefahr der Fehldiagnose einer überstandenen Gastroenteritis. Patienten sollten bei entsprechender Anamnese und Verdachtsdiagnose unbedingt weiter stationär beobachtet werden.
Phase 3: Nach 2–4 Tagen beginnt die Phase des akuten Leberversagens. Durch die Entstehung von Leberzellnekrosen kommt es zu einem massiven Anstieg der Transaminasen, in weiterer Folge zu Ikterus, Enzephalopathie und Koagulopathie. Durch den direkten nephrotoxischen Effekt auf den proximalen und distalen Tubulus kann sich ein akutes Nierenversagen entwickeln. Im Kindesalter verläuft eine Intoxikation in 50 % und im Erwachsenenalter in 8–22 % letal.
Schockleber – hypoxische Hepatitis
Die hypoxische Hepatitis (HH), auch ischämische Hepatitis oder Schockleber genannt, ist durch eine zentrilobuläre Leberzellnekrose und einen fulminanten Anstieg der Serumaminotransferasen als Folge von akutem kardialem, zirkulatorischem und/oder respiratorischem Versagen charakterisiert [32]. Die HH ist die mit Abstand häufigste Ursache der akuten Leberzellschädigung und -nekrose im Krankenhaus mit einer Prävalenz von bis zu 10 % bei kritisch kranken Patienten [33]. Die häufigsten HH auslösenden Ursachen sind akute beziehungsweise akut-auf-chronische kardiovaskuläre Erkrankungen mit einem reduzierten Herzauswurfvolumen sowie der septische Schock, wobei in der großen Mehrheit der Fälle ein reduziertes Herzzeitvolumen sowie eine multifaktorielle Ätiologie der HH zugrunde liegt. Kritisch kranke Patienten mit HH, insbesondere mit der Notwendigkeit einer Vasopressorentherapie, haben ein bis zu 5‑fach erhöhtes Mortalitätsrisiko [34]. Die HH kann verschiedene Komplikationen, wie spontane Hypoglykämien, Ikterus und Cholestase, respiratorische Insuffizienz als Folge des hepatopulmonalen Syndroms sowie eine Hyperammonämie und HE, verursachen [9, 35–38]. Ein frühestmögliches Erkennen ihrer zugrunde liegenden Ursachen sowie die unverzügliche Einleitung entsprechender Therapiemaßnahmen sind von zentraler prognostischer Bedeutung. Die Schockleber stellt in der Regel eine klare Kontraindikation für eine Lebertransplantation dar. In einer großen prospektiven Kohorte an Intensivpatienten konnte rezent gezeigt werden, dass eine vorbestehende Statintherapie das Risiko für das Neuauftreten einer Schockleber signifikant senken konnte [39].
Budd-Chiari-Syndrom
Das Budd-Chiari Syndrom beschreibt eine Gruppe von Erkrankungen und ist gekennzeichnet durch eine Blutabflussstörung aufgrund von Thrombosen im Bereich der Lebervenen, der Vena cava inferior oder des rechten Vorhofs [40]. Es ist ein sehr seltenes Krankheitsbild und betrifft vorwiegend Frauen zwischen dem 30. und 40. Lebensjahr. Risikofaktoren sind myeloproliferative Erkrankungen, orale Kontrazeptiva, Infektionen, Schwangerschaft sowie Erkrankungen des Gerinnungssystems. Klinisch imponiert Bauchschmerz, Aszites und eine Hepatomegalie. Die Therapie besteht im Wesentlichen in der Reduktion der portalen Hypertension und in der Vermeidung derer Komplikationen. Die Implantation eines transjugulären intrahepatischen portosystemischen Shunt (TIPS) ist eine sehr effektive Methode, um den intrahepatischen Druck zu senken. Alle Patienten mit einem Budd-Chiari-Syndrom sollten des Weiteren eine Antikoagulation mit Heparin und im weiteren Verlauf mit Marcoumar erhalten. Ein gutes Langzeitenüberleben konnte bei Patienten erzielt werden, die mit einem durchgeführten Stufenschema des European Network for Vascular Disorders of the Liver basierend auf einem schrittweisen Einsatz einer suffizienten Antikoagulation, Angioplastie bzw. Thrombolyse, TIPS oder Lebertransplantation therapiert wurden [41]. In 20 % der Patienten kommt es zu einem akuten Lebersagen mit insgesamt schlechter Prognose. Nach Ausschluss einer zugrunde liegenden Tumorerkrankung ist das akute Leberversagen auf Basis einer Lebervenenthrombose eine Indikation zur Lebertransplantation.
Morbus Wilson
Der Morbus Wilson ist eine autosomal-rezessive Erkrankung, betrifft Frauen häufiger als Männer und ist mit 2–3 % eine seltene Ursache für ein akutes Leberversagen. Das typische Alter bei der klinischen Erstpräsentation liegt zwischen dem 5. und 30. Lebensjahr. Im Labor findet sich eine Coombs-Test-negative hämolytische Anämie mit erhöhten Bilirubinspiegeln. Das Coeruloplasmin im Serum ist klassischerweise niedrig, kann aber auch normal sein. Hohe Kupferwerte im Serum und Urin sowie eine genetische Bestimmung sind diagnoseweisend, aber im Fall eines akuten Leberversagens häufig zu zeitintensiv. Ein Quotient aus Bilirubin und alkalischer Phosphatase > 2 gilt als hilfreicher Marker für das Vorliegen eines Morbus Wilson. Hinweisend kann auch eine erniedrigte alkalische Phosphatase sein. Da häufig fulminante Verläufe beobachtet werden, sind eine frühzeitige Diagnose sowie ein Transfer in ein Zentrum mit der Möglichkeit einer Lebertransplantation notwendig.
Autoimmunhepatitis (AIH)
Die Autoimmunhepatitis ist für rund 5 % der ALV verantwortlich und verläuft meist sehr schwer [42]. Häufig besteht bereits eine bisher nicht bekannte Leberkrankung. Die Diagnosefindung verläuft oft schwierig, da Autoantikörper in bis zu 30 % der Patienten mit akutem Leberversagen fehlen. Diagnostisch wegweisend sind der Nachweis von antinukleären Antikörpern (ANA), Smooth-muscle-Antikörpern (SMA), antimitochondrialen Antikörpern (AMA), antineutrophilen zytoplasmatischen Antikörpern (ANCA) sowie Serumimmunglobulin (Ig)-G. Bei negativen Autoantikörpern und Verdacht auf eine AIH wird eine Leberbiopsie zur Diagnosesicherung empfohlen. Bisher existieren lediglich kleine Fallserien zu Autoimmunhepatitis und ALV.
Tumorassoziiertes akutes Leberversagen
Eine Tumorinfiltration der Leber kann in seltenen Fällen zu einem ALV führen. Diagnostisch werden hier bildgebende Verfahren sowie eine Leberbiopsie empfohlen. Typische Tumorentitäten sind das Mammakarzinom, kleinzellige Bronchuskarzinom, Lymphom und Melanom. Eine Transplantation ist bei diesen Patienten keine Therapieoption.
Therapie des akuten Leberversagens
Die intensivmedizinischen Therapiemaßnahmen beim akuten Leberversagens sind in Abb. 2 zusammengefasst.
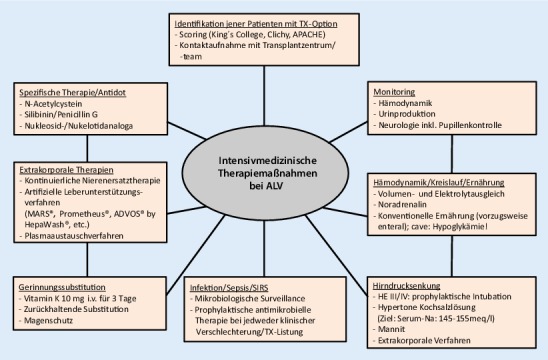
Allgemeine Empfehlungen
Patienten mit ALV können bei geringgradiger Gerinnungsfunktionsstörung, jedoch fehlender HE auf einer Normalstation behandelt werden. Ab einem INR > 1,5 und dem Auftreten einer HE sollte eine Kontaktaufnahme mit einem Transplantationszentrum sowie die Evaluation einer Aufnahme auf eine Intensivstation erfolgen [43]. Durch eine rasche Diagnostik und Einleitung einer ursachenspezifischen Therapie können so in weiterer Folge Leberschäden rückgängig gemacht werden oder auch weiterführende Schritte Richtung Lebertransplantation evaluiert werden.
Ursachenspezifische Therapie
Kann eine bestimmte Ursache als Auslöser des ALV identifiziert werden, muss die ursachenspezifische Therapie zur Prognoseverbesserung möglichst rasch eingeleitet werden. Bereits bei Verdacht auf eine Paracetamolintoxikation ist eine Therapie mit N‑Acetylcystein (NAC) indiziert. Durch die Einnahme großer Mengen an Paracetamol erschöpfen sich die zellulären Glutathionspeicher in der Leber und können nicht rasch genug wieder aufgefüllt werden. NAC ist in der Lage, die Glutathionspeicher wieder aufzufüllen und unterstützt zusätzlich mitochondriale Funktionen.
Die Datenlage zur Therapie mit NAC bei Paracetamolintoxikation ist gut und die Therapie zeigt auch Effektivität trotz eines späten Beginns nach Medikamenteneinnahme. In einer prospektiv randomisierten Studie konnte NAC auch bei nicht mit Paracetamol assoziierten Leberversagen das transplantatfreie Überleben verlängern. Dieser Vorteil konnte jedoch nur bei Patienten mit frühzeitigem Therapiebeginn und leichter bis moderater Enzephalopathie beobachtet werden. Die Therapie wird in Form eines Schemas verbreicht und im Allgemeinen gut toleriert (NAC: 150 mg/kg und Stunde für 1 h, dann 12,5 mg/kg und Stunde für 4 h, dann 6,25 mg/kg und Stunde als Erhaltungsdosis). Liegt die Paracetamoleinnahme unter 4 h kann zusätzlich eine Dekontamination mittels Aktivkohle durchgeführt werden.
Ein gutes Outcome kann in der Regel durch eine NAC-Verabreichung innerhalb von 10–12 h nach Paracetamolintoxikation erzielt werden. Die Rolle der Lebertransplantation bei Paracetamolintoxikation rückt durch die Fortschritte der intensivmedizinischen Behandlung immer mehr in den Hintergrund, sodass Indikation und Evaluation zur Lebertransplantation bei Paracetamolintoxikation im Generellen reevaluiert werden sollten.
Die Hepatitis-B-Infektion ist in Deutschland für etwa 20 % der ALV-Fälle verantwortlich und kann v. a. infolge einer Reaktivierung durch Immunsuppression fulminant verlaufen. Eine frühzeitige Therapieeinleitung mit Nukleosid-/Nukelotidanaloga vor Beginn der Immunsuppression kann ein ALV verhindern. Im Fall eines bereits entwickelten ALV ist die Therapie der Nukleosid-/Nukelotidanaloga bei sehr kurzer Therapiedauer und fehlendem Überlebensvorteil umstritten. In Konsensuspapieren ist jedoch der Einsatz der Nukleosid-/Nukelotidanaloga empfohlen, da sie im Fall einer Transplantation eine Reinfektion verhindern können.
Die Autoimmunhepatitis kann sich in Form eines ALV präsentieren und wird oft mit intravenösen Kortikosteroiden therapiert. Zur Wirksamkeit der Kortikosteroide sind nur wenige retrospektive Fallserien verfügbar. In einer retrospektiven Studie mit Patienten mit autoimmunem, medikamentösem oder unklarem Leberversagen zeigte die Gabe von Glukokortikoiden keinen Überlebensvorteil. Im Gegenteil, es wurde bei Patienten mit ALV und hohem MELD-Score eine Verschlechterung des Überlebens beobachtet. Dies ist möglicherweise durch das zusätzliche Risiko einer Sepsis und die dadurch verzögerte Lebertransplantation erklärbar. Ob Kortikosteroide bei speziellen Verlaufsformen des ALV, wie beispielsweise bei subakuten Formen, Vorteile bringen, ist bis dato nicht belegt und sie sollten daher außerhalb von klinischen Studien vorerst nicht angewandt werden. Anzumerken ist, dass im Rahmen einer schweren Autoimmunhepatitis ohne ALV gemäß der europäischen Leitlinien (EASL – „clinical practice guidelines“) die Gabe von Kortikosteroiden empfohlen wird [44].
Das akute Leberversagen auf Basis eines Morbus Wilson ist ohne Lebertransplantation mit einer hohen Mortalität assoziiert. Auch bei Patienten mit Budd-Chiari-Syndrom und ALV ist die Transplantation, nach Ausschluss von Kontraindikationen, die Therapie der Wahl.
Die frühzeitige Therapie der Knollenblätterpilzvergiftung besteht aus der Gabe von Aktivkohle und ausreichend Flüssigkeit. Penicillin G (frühzeitige Therapie der Knollenblätterpilzvergiftung vorwiegend in den USA, da dort Silibinin nicht verfügbar ist) und Silibinin (vorwiegend in Europa), gewonnen aus der Milchdistel, sind trotz unzureichender Datenlage als Antidote akzeptiert. Als Therapie werden 30–40 mg/kgKG Silibinin pro Tag intravenös verabreicht. Eine Listung zur Lebertransplantation sollte bei klinischer Verschlechterung bzw. fehlender Verbesserung früh erfolgen.
Intensivmedizinische Therapie
In der Behandlung von Patienten mit akutem Leberversagen konnte in den letzten Jahrzehnten eine deutliche Reduktion der Mortalität erzielt werden. Dies ist neben der Möglichkeit der Lebertransplantation v. a. durch eine Weiterentwicklung der intensivmedizinischen Behandlungsmöglichkeiten erreicht worden [45].
Organerhaltende Therapie
Hämodynamik/Kreislauf
Hämodynamisch präsentiert sich der Patienten mit akutem Leberversagen mit einem hohen Herzzeitvolumen, einem niedrigen arteriellen Mitteldruck und einem geringen peripheren Gefäßwiderstand. Um eine Vasopressortherapie zu umgehen, sollte eine frühzeitige und ausreichende Zufuhr kristalloider Flüssigkeit bei meist vorherrschendem Volumenmangel gewährleistet sein. Im Fall einer durch Volumen nicht kompensierbaren Hypotension ist der Beginn einer Vasopressortherapie mit Noradrenalin notwendig. Der zusätzliche Einsatz von Terlipressin kann derzeit nicht empfohlen werden.
Lunge
Bei zunehmender HE, spätestens ab einer HE Grad 3 oder respiratorischer Insuffizienz, sollte eine Intubation durchgeführt werden. Dies kann neben der Sicherung der Atemwege (Aspirationsschutz) möglicherweise durch zusätzliche Verabreichung von Analgosedativa eine Senkung des intrakraniellen Hypertonus bewirken.
Eine respiratorische Insuffizienz in Form eines ARDS kommt bei bis zu 20 % der Patienten mit ALV vor. Das Auftreten eines ARDS scheint jedoch nicht von vordergründiger klinischer Bedeutung zu sein, da es in zumindest einer großen Untersuchung nicht mit einer erhöhten Mortalität assoziiert war.
Nierenversagen
Rund 50–70 % aller Patienten mit ALV entwickeln ein akutes Nierenversagen. Dieses wird häufig bei schweren Verlaufsformen, ausgeprägter Enzephalopathie sowie bei Vasopressortherapie beobachtet und ist mit einer erhöhten Mortalität assoziiert [46]. Die Ursachen für ein akutes Nierenversagen sind multifaktoriell und können neben direkt toxischen Effekten auch Folge eines ausgeprägten SIRS sein. Neben der Beendigung der Gabe von nephrotoxischen Substanzen sollte auf eine ausreichende Volumenzufuhr geachtet werden. Im Fall des Einsatzes eines extrakorporalen Entgiftungsverfahrens (Nierenersatzverfahren oder Leberunterstützungsverfahren) werden kontinuierliche Verfahren bevorzugt. Diese bieten im Gegensatz zu intermittierenden Verfahren stabilere hämodynamische Bedingungen und reduzieren möglicherweise das Risiko eines Hirnödems. Ferner sind diese Verfahren in der Lage, die HE-verursachenden Neurotoxine effektiv zu eliminieren und somit dem Fortschreiten der HE entgegenzuwirken. Der frühzeitige Einsatz, spätestens ab einer HE III, ist möglicherweise vorteilhaft [47].
Hirndruckmonitoring/-therapie
Die HE spielt eine zentrale Rolle beim ALV und wiederspiegelt die Schwere des Leberschadens. Ziel ist es, das Auftreten beziehungsweise in der Regel eher das Fortschreiten einer Enzephalopathie sowie das Risiko eines erhöhten intrakraniellen Drucks und eines Hirnödems zu verhindern. Patienten ab HE Grad 3 oder 4 sollten frühzeitig beatmet und analgosediert werden sowie frühzeitig ein extrakorporales Verfahren (Nierenersatzverfahren, Leberunterstützungsverfahren) zur Senkung der Neurotoxine bei HE erhalten [47, 48] Das weitere Monitoring beinhaltet die Überwachung des arteriellen Serumammoniakspiegels und gegebenenfalls des Hirndrucks [49]. Die Anlage einer intrakraniellen Hirndruckmessung wird kontrovers diskutiert. Neben dem Vorteil einer raschen Erkennung von Hirndruckspitzen und der Kontrolle einer etwaigen Senkung des Hirndrucks besteht das Risiko einer Blutung durch die Katheteranlage. In einer rezent publizierten Studie konnte kein Überlebensvorteil für Patienten mit invasivem Hirndruckmonitoring gezeigt werden.
Zur medikamentösen Senkung des Ammoniakspiegels beim ALV gibt es wenig klare Daten. Die Verabreichung von L‑Ornithin-L-Aspertat (LOLA) wird explizit nicht empfohlen. So konnte in einer randomisiert kontrollierten Studie bei Patienten mit ALV keine Ammoniakreduktion und ein fast statistisch signifikanter Überlebensnachteil durch LOLA festgestellt werden [50]. In Anlehnung an das Management von traumatischen Hirnverletzungen zeigten generelle Maßnahmen zur Hirndrucksenkung, wie der Gebrauch von hypertonen Kochsalzlösungen (Ziel: Serumnatrium: 145–155 meq/l) oder Mannitol einen Überlebensvorteil. Vom systematischen Einsatz einer therapeutischen Hypothermie muss mit dem derzeitigen Wissensstand abgeraten werden.
Infektionen/Sepsis/SIRS
Patienten mit ALV haben ein deutlich erhöhtes Risiko für das Neuauftreten von Infektionen. Diese sind neben dem Hirnödem die Haupttodesursache. Durch den massiven Leberzelluntergang kommt es zur Ausschwemmung von proinflammatorischen Zytokinen und der Entwicklung eines SIRS, das für das Auftreten eines Multiorganversagens mitverantwortlich ist. Im Fall einer klinischen Verschlechterung, bei HE III/IV sowie im Fall einer Listung zur Lebertransplantation wird in der Regel eine prophylaktische antibiotische Therapie begonnen [51]. Eine antimykotische Therapie wird nur im Fall eines entsprechenden Erregernachweises empfohlen. Bisher konnte jedoch durch diese Maßnahme keine Reduktion der Mortalität beobachtet werden.
Gerinnung
Eine eingeschränkte Gerinnungssituation mit erhöhter INR ist ein wesentliches diagnostisches Element eines ALV. Das spontane Blutungsrisiko ist jedoch bei Patienten mit ALV gering. Laut aktuellen Leitlinien gibt es keine Richtlinien zur Behandlung bzw. Substitution von Gerinnungsprodukten. Bei fehlenden Zeichen einer aktiven Blutung ist eine Substitution mit FFP, Gerinnungsfaktoren oder Thrombozyten grundsätzlich nicht indiziert. Vitamin K (10 mg i. v. für 3 Tage) kann prinzipiell substituiert werden, um einen etwaigen zusätzlich bestehenden Vitamin-K-Mangel entsprechend zu behandeln. Bei einer Thrombozytenzahl < 50 G/l sollte im Fall einer aktiven Blutung oder vor invasiven Eingriffen eine Thrombozytensubstitution erfolgen, wobei betont werden muss, dass dies eine reine Expertenmeinung ohne klinische Evidenz ist. Ansonsten sollten lediglich bei einer bestehenden Thrombozytopenie < 10 G/l Thrombozyten verabreicht werden.
Um eine stressassoziierte gastrointestinale Blutung zu verhindern, wird bei Patienten mit ALV eine großzügige Indikationsstellung für einen Magenschutz mit Protonenpumpeninhibitoren oder H2-Blocker empfohlen, wobei auch hier Daten hinsichtlich eines etwaigen Vorteils für Patienten aus klinischen Studien bisher fehlen.
Leberunterstützungsverfahren
Bei extrakorporalen Leberunterstützungsverfahren werden zellfreie (artifizielle) von zellbasierten (bioartifiziellen) Leberunterstützungsverfahren unterschieden. Heutzutage sind lediglich zellfreie Leberunterstützungsverfahren für den Einsatz im Rahmen der klinischen Routine zugelassen. Die bekanntesten Systeme sind das MARS®-Verfahren („molecular adsorbent recirculating system“; Baxter/Gambro Hospal GmbH, Lund, Schweden) sowie die fraktionierte Plasmaseperation und Adsorption (FPSA, Prometheus®, Fresenius Medical Care, Bad Homburg, Deutschland). Vereinfacht zusammengefasst sind artifizielle Leberunterstützungsverfahren erweiterte Dialyseverfahren, die neben der Möglichkeit, wasserlösliche Substanzen zu eliminieren, auch in der Lage sind, eiweißgebundene Substanzten zu entfernen. Mit der Möglichkeit einer erweiterten Entgiftung können Patienten bis zur spontanen Regeneration der Leberfunktion oder bis zur Lebertransplantation überbrückt werden [52]. Durch das MARS®-System konnte eine Verbesserung der HE nachgewiesen werden [53]. In einer prospektiv randomisierten Studie (FUMAR-Studie) mit Patienten und akutem Leberversagen wurde eine konventionelle Behandlung mit einer konventionellen Behandlung und MARS®-Anwendung verglichen. In dieser Studie konnte kein Unterschied im 6‑Monats-Überleben oder transplantatfreien Überleben beobachtet werden [54]. Anzumerken ist hierbei, dass bereits 16 Stunden nach Randomisierung die Lebertransplantation durchgeführt wurde und somit keine seriöse Aussage hinsichtlich der Effektivität der MARS®-Therapie möglich war. Durch wiederholte und ausgedehnte Anwendungen konnte das Outcome der Patienten verbessert werden. Ein neues Leberunterstützungsverfahren auf Basis einer Albumindialyse (ADVOS® by HepaWash®, Hepa Wash GmbH, München, Deutschland) konnte eine Verbesserung der Hämodynamik bei Schweinen mit ALV erzielen [55]. In einer prospektiv randomisierten Studie mit 182 Patienten und ALV konnte durch den zusätzlichen Einsatz eines Plasmaaustauschverfahrens (8–12 l pro Tag an 3 Tagen) eine Verlängerung des transplantatfreien Überlebens beobachtet werden. Dieser Effekt wird von den Autoren durch die Abschwächung des Immunsystems durch den Plasmaaustausch erklärt [56].
Transplantation
Insgesamt werden 10 % aller Lebertransplantationen aufgrund eines ALV durchgeführt. Im Rahmen der Evaluation zu einer etwaigen Transplantation wird die zugrunde liegende Ursache des ALV berücksichtigt, da beispielsweise die Schockleber sowie ein tumorassoziiertes ALV klare Kontraindikationen für eine Lebertransplantation sind. Weitere Kontraindikationen sind ein florider Alkohol- und Drogengenabusus, das Vorliegen einer Sepsis mit positiver Blutkultur, Kreislaufinstabilität mit Katecholaminbedarf oder eine Hirnstammeinklemmung. Durch die Daten des European Liver Transplant Registry (ELTR) werden die Entwicklung und das Outcome von Patienten mit ALV und Lebertransplantation verfolgt. Insgesamt wurden 6374 Patienten mit ALV in den Jahren 1988–2009 in 23 europäischen Ländern transplantiert und dokumentiert. Das Überleben nach Transplantation betrug nach 1, 3, 5 und 10 Jahren 63 %, 59 %, 57 % und 50 %. In den letzten Jahren kam es zu einer stetigen Verbesserung der Überlebensraten nach Transplantation mit einem 1‑Jahres-Überleben von 79 % und einem 5‑Jahres-Überleben von 72 %. Es konnte auch über die Jahre eine deutliche Reduktion der Retransplantationsrate beobachtet werden. Die Ätiologie der Erkrankung hatte in diesem Kollektiv keinen Einfluss auf das Patienten- oder das Transplantatüberleben [57].
Es ist von besonderer Bedeutung, dass nach Ausschluss von Kontraindikationen eine Listung zur Lebertransplantation rasch erfolgt, sodass bei oft unvorhersehbarem Verlauf adäquat reagiert werden kann.
Fazit für die Praxis
Durch eine stetige Verbesserung der intensivmedizinischen Therapie konnte in der Behandlung von Patienten mit akutem Leberversagen eine deutliche Reduktion der Mortalität beobachtet werden.
Neben symptomatischer Therapie, bei der insbesondere durch den Einsatz von extrakorporalen Verfahren (z. B. Plasmaaustausch) das Überleben verbessert werden kann, gibt es abgesehen von N‑Acetylcystein aktuell kaum konservative Therapiestrategien mit ausreichendem Nachweis eines Behandlungsvorteils.
Eine interdisziplinäre Evaluation zur Organtransplantation sollte frühzeitig durchgeführt werden.
Einhaltung ethischer Richtlinien
Interessenkonflikt
K. Rutter, T. Horvatits, A. Drolz, K. Roedl, S. Siedler, S. Kluge und V. Fuhrmann geben an, dass kein Interessenkonflikt besteht.
Dieser Beitrag beinhaltet keine von den Autoren durchgeführten Studien an Menschen oder Tieren.
Literatur
- 1.Trey C, Davidson CS. The management of fulminant hepatic failure. Prog Liver Dis. 1970;3:282–298. [PubMed] [Google Scholar]
- 2.Lee WM, Squires RH, Jr., Nyberg SL, Doo E, Hoofnagle JH. Acute liver failure: Summary of a workshop. Hepatology. 2008;47(4):1401–1415. doi: 10.1002/hep.22177. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 3.O’Grady JG, Alexander GJ, Hayllar KM, Williams R. Early indicators of prognosis in fulminant hepatic failure. Gastroenterology. 1989;97:439–445. doi: 10.1016/0016-5085(89)90081-4. [DOI] [PubMed] [Google Scholar]
- 4.Oketani M, Ido A, Nakayama N, et al. Etiology and prognosis of fulminant hepatitis and late-onset hepatic failure in Japan: Summary of the annual nationwide survey between 2004 and 2009. Hepatol Res. 2013;43(2):97–105. doi: 10.1111/j.1872-034X.2012.01105.x. [DOI] [PubMed] [Google Scholar]
- 5.Ostapowicz G. Results of a prospective study of acute liver failure at 17 tertiary care centers in the United States. Ann Intern Med. 2002;137:947–954. doi: 10.7326/0003-4819-137-12-200212170-00007. [DOI] [PubMed] [Google Scholar]
- 6.Lidofsky SD. Liver transplantation for fulminant hepatic failure. Gastroenterol Clin North Am. 1993;22(2):257–269. [PubMed] [Google Scholar]
- 7.Denzer U, Helmreich-Becker I, Galle PR, Lohse AW. Liver assessment and biopsy in patients with marked coagulopathy: value of mini-laparoscopy and control of bleeding. Am J Gastroenterol. 2003;98(4):893–900. doi: 10.1111/j.1572-0241.2003.07342.x. [DOI] [PubMed] [Google Scholar]
- 8.Kalambokis G, Manousou P, Vibhakorn S, et al. Transjugular liver biopsy–indications, adequacy, quality of specimens, and complications–a systematic review. J Hepatol. 2007;47(2):284–294. doi: 10.1016/j.jhep.2007.05.001. [DOI] [PubMed] [Google Scholar]
- 9.Drolz A, Jäger B, Wewalka M, et al. Clinical impact of arterial ammonia levels in ICU patients with different liver diseases. Intensive Care Med. 2013;39(7):1227–1237. doi: 10.1007/s00134-013-2926-8. [DOI] [PubMed] [Google Scholar]
- 10.Bernal W, Hall C, Karvellas CJ, Auzinger G, Sizer E, Wendon J. Arterial ammonia and clinical risk factors for encephalopathy and intracranial hypertension in acute liver failure. Hepatology. 2007;46(6):1844–1852. doi: 10.1002/hep.21838. [DOI] [PubMed] [Google Scholar]
- 11.Gill RQ, Sterling RK. Acute liver failure. J Clin Gastroenterol. 2001;33(3):191–198. doi: 10.1097/00004836-200109000-00005. [DOI] [PubMed] [Google Scholar]
- 12.Simpson KJ, Bates CM, Henderson NC, et al. The utilization of liver transplantation in the management of acute liver failure: comparison between acetaminophen and non-acetaminophen etiologies. Liver Transplant. 2009;15(6):600–609. doi: 10.1002/lt.21681. [DOI] [PubMed] [Google Scholar]
- 13.O’Grady JG, Schalm SW, Williams R. Acute liver failure: redefining the syndromes. Lancet. 1993;342(8866):273–275. doi: 10.1016/0140-6736(93)91818-7. [DOI] [PubMed] [Google Scholar]
- 14.Bernuau J, Rueff B, Benhamou JP. Fulminant and subfulminant liver failure: definitions and causes. Semin Liver Dis. 1986;6(2):97–106. doi: 10.1055/s-2008-1040593. [DOI] [PubMed] [Google Scholar]
- 15.Bundesärztekammer Richtlinien zur Organtransplantation gem. §16 ABs. 1S. 1 Nrn. 2 u. 5 TPG. Dtsch Arztebl. 2013;110(6):A-241–A-242. [Google Scholar]
- 16.Schmidt LE, Larsen FS. MELD score as a predictor of liver failure and death in patients with acetaminophen-induced liver injury. Hepatology. 2007;45(3):789–796. doi: 10.1002/hep.21503. [DOI] [PubMed] [Google Scholar]
- 17.Bernal W, Auzinger G, Dhawan A, Wendon J. Acute liver failure. Lancet. 2010;376(9736):190–201. doi: 10.1016/S0140-6736(10)60274-7. [DOI] [PubMed] [Google Scholar]
- 18.Hadem J, Tacke F, Bruns T, et al. Etiologies and outcomes of acute liver failure in Germany. Clin Gastroenterol Hepatol. 2012;10(6):664–669 e2. doi: 10.1016/j.cgh.2012.02.016. [DOI] [PubMed] [Google Scholar]
- 19.Hoofnagle JH, Nelson KE, Purcell RH. Hepatitis E. N Engl J Med. 2012;367(13):1237–1244. doi: 10.1056/NEJMra1204512. [DOI] [PubMed] [Google Scholar]
- 20.Pischke S, Behrendt P, Bock CT, Jilg W, Manns MP, Wedemeyer H. Hepatitis E in Germany–an under-reported infectious disease. Dtsch Arztebl Int. 2014;111(35–36):577–583. doi: 10.3238/arztebl.2014.0577. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 21.Manka P, Bechmann LP, Coombes JD, et al. Hepatitis E virus infection as a possible cause of acute liver failure in europe. Clin Gastroenterol Hepatol. 2015;13(10):1836–1842. doi: 10.1016/j.cgh.2015.04.014. [DOI] [PubMed] [Google Scholar]
- 22.Zhang J, Zhang XF, Huang SJ, et al. Long-term efficacy of a hepatitis E vaccine. N Engl J Med. 2015;372(10):914–922. doi: 10.1056/NEJMoa1406011. [DOI] [PubMed] [Google Scholar]
- 23.Poethko-Muller C, Zimmermann R, Hamouda O, et al. Epidemiology of hepatitis A, B, and C among adults in Germany: results of the German Health Interview and Examination Survey for Adults (DEGS1) Bundesgesundheitsblatt Gesundheitsforschung Gesundheitsschutz. 2013;56(5–6):707–715. doi: 10.1007/s00103-013-1673-x. [DOI] [PubMed] [Google Scholar]
- 24.Khuroo MS, Kamili S. Aetiology and prognostic factors in acute liver failure in India. J Viral Hepat. 2003;10(3):224–231. doi: 10.1046/j.1365-2893.2003.00415.x. [DOI] [PubMed] [Google Scholar]
- 25.Torres HA, Davila M. Reactivation of hepatitis B virus and hepatitis C virus in patients with cancer. Nat Rev Clin Oncol. 2012;9(3):156–166. doi: 10.1038/nrclinonc.2012.1. [DOI] [PubMed] [Google Scholar]
- 26.Perrillo RP, Martin P, Lok AS. Preventing hepatitis B reactivation due to immunosuppressive drug treatments. JAMA. 2015;313(16):1617–1618. doi: 10.1001/jama.2015.2571. [DOI] [PubMed] [Google Scholar]
- 27.Schiodt FV, Davern TJ, Shakil AO, McGuire B, Samuel G, Lee WM. Viral hepatitis-related acute liver failure. Am J Gastroenterol. 2003;98(2):448–453. doi: 10.1111/j.1572-0241.2003.t01-1-07223.x. [DOI] [PubMed] [Google Scholar]
- 28.Reuben A, Koch DG, Lee WM. Drug-induced acute liver failure: Results of a U.S. multicenter, prospective study. Hepatology. 2010;52(6):2065–2076. doi: 10.1002/hep.23937. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 29.Schiodt FV, Rochling FA, Casey DL, Lee WM. Acetaminophen toxicity in an urban county hospital. N Engl J Med. 1997;337(16):1112–1117. doi: 10.1056/NEJM199710163371602. [DOI] [PubMed] [Google Scholar]
- 30.Auzinger G, Wendon J. Intensive care management of acute liver failure. Curr Opin Crit Care. 2008;14(2):179–188. doi: 10.1097/MCC.0b013e3282f6a450. [DOI] [PubMed] [Google Scholar]
- 31.U.S. National Library of Medicine. http://livertox.nih.gov/, Clinical and Research Information in Drug-Induced Liver Injury. Zugegriffen: 21. April 2016
- 32.Fuhrmann V, Jager B, Zubkova A, Drolz A. Hypoxic hepatitis – epidemiology, pathophysiology and clinical management. Wien Klin Wochenschr. 2010;122(5–6):129–139. doi: 10.1007/s00508-010-1357-6. [DOI] [PubMed] [Google Scholar]
- 33.Drolz A, Horvatits T, Roedl K, Fuhrmann V. Shock liver and cholestatic liver in critically ill patients. Med Klin Intensivmed Notfmed. 2014;109(4):228–234. doi: 10.1007/s00063-013-0320-5. [DOI] [PubMed] [Google Scholar]
- 34.Fuhrmann V, Kneidinger N, Herkner H, et al. Impact of hypoxic hepatitis on mortality in the intensive care unit. Intensive Care Med. 2011;37(8):1302–1310. doi: 10.1007/s00134-011-2248-7. [DOI] [PubMed] [Google Scholar]
- 35.Horvatits T, Trauner M, Fuhrmann V. Hypoxic liver injury and cholestasis in critically ill patients. Curr Opin Crit Care. 2013;19(2):128–132. doi: 10.1097/MCC.0b013e32835ec9e6. [DOI] [PubMed] [Google Scholar]
- 36.Jager B, Drolz A, Michl B, et al. Jaundice increases the rate of complications and one-year mortality in patients with hypoxic hepatitis. Hepatology. 2012;56(6):2297–2304. doi: 10.1002/hep.25896. [DOI] [PubMed] [Google Scholar]
- 37.Fuhrmann V, Kneidinger N, Herkner H, et al. Hypoxic hepatitis: underlying conditions and risk factors for mortality in critically ill patients. Intensive Care Med. 2009;35(8):1397–1405. doi: 10.1007/s00134-009-1508-2. [DOI] [PubMed] [Google Scholar]
- 38.Fuhrmann V, Madl C, Mueller C, et al. Hepatopulmonary syndrome in patients with hypoxic hepatitis. Gastroenterology. 2006;131(1):69–75. doi: 10.1053/j.gastro.2006.04.014. [DOI] [PubMed] [Google Scholar]
- 39.Drolz A, Horvatits T, Michl B, et al. Statin therapy is associated with reduced incidence of hypoxic hepatitis in critically ill patients. J Hepatol. 2014;60(6):1187–1193. doi: 10.1016/j.jhep.2014.01.019. [DOI] [PubMed] [Google Scholar]
- 40.Ludwig J, Hashimoto E, McGill DB, van Heerden JA. Classification of hepatic venous outflow obstruction: ambiguous terminology of the Budd-Chiari syndrome. Mayo Clin Proc. 1990;65(1):51–55. doi: 10.1016/S0025-6196(12)62109-0. [DOI] [PubMed] [Google Scholar]
- 41.Seijo S, Plessier A, Hoekstra J, et al. Good long-term outcome of Budd-Chiari syndrome with a step-wise management. Hepatology. 2013;57(5):1962–1968. doi: 10.1002/hep.26306. [DOI] [PubMed] [Google Scholar]
- 42.Lee WM. Etiologies of acute liver failure. Semin Liver Dis. 2008;28:142–152. doi: 10.1055/s-2008-1073114. [DOI] [PubMed] [Google Scholar]
- 43.Stravitz RT, Kramer AH, Davern T, et al. Intensive care of patients with acute liver failure: recommendations of the U.S. Acute Liver Failure Study Group. Crit Care Med. 2007;35(11):2498–2508. doi: 10.1097/01.CCM.0000287592.94554.5F. [DOI] [PubMed] [Google Scholar]
- 44.EASL Clinical Practice Guidelines Autoimmune hepatitis. J Hepatol. 2015;63(4):971–1004. doi: 10.1016/j.jhep.2015.06.030. [DOI] [PubMed] [Google Scholar]
- 45.Bernal W, Hyyrylainen A, Gera A, et al. Lessons from look-back in acute liver failure? A single centre experience of 3300 patients. J Hepatol. 2013;59(1):74–80. doi: 10.1016/j.jhep.2013.02.010. [DOI] [PubMed] [Google Scholar]
- 46.Tujios SR, Hynan LS, Vazquez MA, et al. Risk factors and outcomes of acute kidney injury in patients with acute liver failure. Clin Gastroenterol Hepatol. 2015;13(2):352–359. doi: 10.1016/j.cgh.2014.07.011. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 47.Slack AJ, Auzinger G, Willars C, et al. Ammonia clearance with haemofiltration in adults with liver disease. Liver Int. 2014;34(1):42–48. doi: 10.1111/liv.12221. [DOI] [PubMed] [Google Scholar]
- 48.Chevret L, Durand P, Lambert J, et al. High-volume hemofiltration in children with acute liver failure. Pediatr Crit Care Med. 2014;15(7):300–305. doi: 10.1097/PCC.0000000000000172. [DOI] [PubMed] [Google Scholar]
- 49.Kramer L, Tribl B, Gendo A, et al. Partial pressure of ammonia versus ammonia in hepatic encephalopathy. Hepatology. 2000;31(1):30–34. doi: 10.1002/hep.510310107. [DOI] [PubMed] [Google Scholar]
- 50.Acharya SK, Bhatia V, Sreenivas V, Khanal S, Panda SK. Efficacy of L‑ornithine L‑aspartate in acute liver failure: a double-blind, randomized, placebo-controlled study. Gastroenterology. 2009;136(7):2159–2168. doi: 10.1053/j.gastro.2009.02.050. [DOI] [PubMed] [Google Scholar]
- 51.Singanayagam A, Bernal W. Update on acute liver failure. Curr Opin Crit Care. 2015;21(2):134–141. doi: 10.1097/MCC.0000000000000187. [DOI] [PubMed] [Google Scholar]
- 52.Fuhrmann V, Horvatits T, Drolz A, Rutter K. Extracorporeal therapy of patients with liver disease in the intensive care unit. Med Klin Intensivmed Notfmed. 2014;109(4):246–251. doi: 10.1007/s00063-013-0321-4. [DOI] [PubMed] [Google Scholar]
- 53.Hassanein TI, Tofteng F, Brown RS, Jr., et al. Randomized controlled study of extracorporeal albumin dialysis for hepatic encephalopathy in advanced cirrhosis. Hepatology. 2007;46(6):1853–1862. doi: 10.1002/hep.21930. [DOI] [PubMed] [Google Scholar]
- 54.Saliba F, Camus C, Durand F, et al. Albumin dialysis with a noncell artificial liver support device in patients with acute liver failure: a randomized, controlled trial. Ann Intern Med. 2013;159(8):522–531. doi: 10.7326/0003-4819-159-8-201310150-00005. [DOI] [PubMed] [Google Scholar]
- 55.Al-Chalabi A, Matevossian E, Ak VT. Evaluation of the Hepa Wash(R) treatment in pigs with acute liver failure. BMC Gastroenterol. 2013;13:83. doi: 10.1186/1471-230X-13-83. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 56.Larsen FS, Schmidt LE, Bernsmeier C, et al. High-volume plasma exchange in patients with acute liver failure: An open randomised controlled trial. J Hepatol. 2015;64(1):69–78. doi: 10.1016/j.jhep.2015.08.018. [DOI] [PubMed] [Google Scholar]
- 57.Germani G, Theocharidou E, Adam R, et al. Liver transplantation for acute liver failure in Europe: outcomes over 20 years from the ELTR database. J Hepatol. 2012;57(2):288–296. doi: 10.1016/j.jhep.2012.03.017. [DOI] [PubMed] [Google Scholar]


