Samenvatting
Tropische kindergeneeskunde is een geijkte, maar niet nauwkeurig omschreven term. De ernstige gezondheidsproblemen van kinderen in de tropen en subtropen vinden namelijk hun oorzaak eerder in armoede, ongeletterdheid en oorlogen dan in specifieke tropische condities.
Tropische kindergeneeskunde is een geijkte, maar niet nauwkeurig omschreven term. De ernstige gezondheidsproblemen van kinderen in de tropen en subtropen vinden namelijk hun oorzaak eerder in armoede, ongeletterdheid en oorlogen dan in specifieke tropische condities. Daarnaast kwamen veel ziekten die nu als tropisch gezien worden, zoals malaria, dysenterie en cholera, in de vorige eeuw nog epidemisch in West-Europa voor. Ook in de meeste geïndustrialiseerde landen, waaronder Nederland en België, kent de samenleving nog steeds marginale bevolkingsgroepen waarvan de kinderen lijden aan ziekten die, door ongunstige socio-economische en culturele factoren bepaald, analoog zijn aan die welke men in de tropen en subtropen aantreft. Ten slotte, de verbeterde verbindingen tussen de tropen en West-Europa, de toegenomen immigratie uit tropische gebieden naar het westen en de transculturele adoptie vanuit de tropen maakt de kans groot dat de in Nederland en België praktiserende arts en verpleegkundige kinderen onder ogen krijgen die lijden aan een tropische ziekte. Dit laatste onderstreept nog eens het belang van tropische kindergeneeskunde als importgeneeskunde bij kinderen. Dit hoofdstuk beoogt ook een indruk te geven van de voornaamste ziekten bij kinderen die in de tropen (de Derde Wereld) leven, waarbij duidelijk wordt dat ondervoeding een belangrijke medeoorzaak van ziekte en sterfte is. Bij het deel van dit hoofdstuk dat infectieziekten in de Derde Wereld behandelt, komen (import)ziekten aan bod die aangetroffen kunnen worden bij kinderen die zelf uit de tropen afkomstig zijn of daar gedurende korte of langere tijd verbleven.
De volgende aspecten van de tropische kindergeneeskunde worden in dit hoofdstuk behandeld:
de gezondheidstoestand van kinderen in de Derde Wereld;
preventie van ziekte en sterfte (inclusief interventieprogramma’s);
lichaamsgroei en voeding;
ondervoedingsbeelden (epidemiologie, pathofysiologie, klinische ziektebeelden, diagnostiek, behandeling en preventie);
infectieziekten in de Derde Wereld.
Tropische kindergeneeskunde omvat:
ziekte en gezondheid van kinderen in de Derde Wereld;
importziekten vanuit de Derde Wereld (tropen).
De gezondheidstoestand van kinderen in de Derde Wereld
Van de totale wereldbevolking van bijna 6 miljard (2000) is ten minste 40-45% jonger dan achttien jaar. Circa 90% van deze jongeren leven in derdewereldlanden en landen van het vroegere Oostblok. Bijvoorbeeld, in Nigeria bedraagt het percentage kinderen onder de leeftijd van achttien jaar circa 50%, maar in Nederland en Belgie is dit amper 20%. Ook in ontwikkelde landen leven echter kinderen onder omstandigheden die met de Derde Wereld vergelijkbaar zijn. Te denken valt aan de verpauperde steden van de geïndustrialiseerde landen en aan oorlogssituaties.
De gezondheidstoestand van kinderen in minder ontwikkelde landen wordt gekenmerkt door een hoge sterfte van pasgeborenen, zuigelingen en kinderen jonger dan vijf jaar. Volgens het verslag van Unicef, The state of the world’s children 2001, bedroeg dit in 1999 respectievelijk 90 per 1000 kinderen in ontwikkelingslanden en 6 per 1000 (!) in ontwikkelde (geïndustrialiseerde) landen. De sterfte van pasgeborenen (0-28 dagen) is nauw verbonden met de voedings- en gezondheidstoestand van de moeder en de aanwezige medische voorzieningen. Het zuigelingensterftecijfer (aantal overleden kinderen gedurende het eerste levensjaar uitgedrukt per 1000 levendgeborenen: respectievelijk 63 en 6 in ontwikkelings- en geïndustrialiseerde landen) wordt sterk bepaald door leeftijd en scholing van de moeder en de incidentie van pasgeborenen met een laag geboortegewicht (lbw; < 2500 g). lbw kan veroorzaakt worden door een intra-uteriene groeivertraging en door een te korte zwangerschapsduur of door een combinatie van deze factoren. Voor de gehele wereld wordt een lbw-incidentie van 16% aangegeven: voor ontwikkelingslanden 17%, maar voor geïndustrialiseerde landen slechts 6% (Unicef, 2001). Dit verschil wordt voor een groot deel bepaald door een lager geboortegewicht voor de duur van de zwangerschap. lbw-zuigelingen hebben met name in het eerste levensjaar ook meer ziekten, als gevolg van diverse infecties. Vroege groeivertraging draagt bij tot een lager gewicht op eenjarige leeftijd en mogelijk zelfs op volwassen leeftijd. Verder blijkt ook dat in minder ontwikkelde landen gemiddeld 33% van de kinderen onder de leeftijd van vijf jaar een te kleine lengte voor de leeftijd heeft (< 2 sd onder de mediaan van de referentiepopulatie van het National Center for Health Statistics; nchs, 1976). Het percentage van te kleine kinderen is het hoogst in Zuid-Azië (48%) gevolgd door Afrika ten zuiden van de Sahara (37%) (tabel 30-3, zie verder).
| Laag gewicht (underweight) |
Vertraagde lengtegroei (stunting) |
|
|---|---|---|
| Afrika ten zuiden van de Sahara | 31 | 37 |
| Midden-Oosten en Noord-Afrika | 17 | 24 |
| Zuid-Azië | 49 | 48 |
| Oost-Azië en Grote Oceaan | 19 | 24 |
| Zuid-Amerika en het Caraïbisch gebied | 9 | 17 |
Zowel borstvoeding als een adequate geboorteregeling heeft een positieve invloed op de zuigelingensterfte. De sterftecijfers van zuigelingen en kinderen in de leeftijd van 0-5 jaar (under-5 mortality rate; u5mr) zijn belangrijke graadmeters voor de gezondheidstoestand van kinderen. Zij vormen tevens een belangrijke maat voor het niveau en de effectiviteit van de gezondheidszorg in een bepaald gebied. Jaarlijks sterven in minder ontwikkelde landen zo’n 12 miljoen kinderen voor hun vijfde verjaardag. Zeven van de tien gevallen van kindersterfte zijn te wijten aan diarree, pneumonie, mazelen, malaria en ondervoeding. Vaak bestaat er echter een combinatie van deze ziektebeelden die de dood veroorzaken, daarbij speelt ondervoeding een belangrijke rol (figuur 30-1).

Kernboodschappen over gezondheid en ziekte van kinderen in de Derde Wereld:
17% van alle pasgeborenen heeft een te laag geboortegewicht;
ruim 90 per 1000 (= 12 miljoen) kinderen sterven voor hun vijfde verjaardag (underfive mortality rate: u5mr 90%o);
acute luchtweginfecties, ondervoeding, diarree, malaria en mazelen zijn de top-5-oorzaken van sterfte;
in Afrika ten zuiden van de Sahara is aids een van de belangrijkste doodsoorzaken van kinderen;
kindersterfte is in de steden driemaal zo hoog als op het platteland;
kindersterfte is geassocieerd met grote bevolkingsdichtheid, armoede, onvoldoende scholing, gebrekkige hygiëne en slechte kwaliteit van het drinkwater.
Er zijn geografische verschillen in morbiditeit en mortaliteit. Ter illustratie: wereldwijd komen in Afrika ten zuiden van de Sahara verreweg de meeste (ruim 26 van de totaal circa 36 miljoen) gevallen van hiv of aids bij volwassenen en kinderen voor (unaids, 2001). Het is daar inmiddels een van de belangrijkste doodsoorzaken van kinderen; de sterfte aan malaria in de wereld treft hoofdzakelijk de jonge plattelandskinderen van tropisch Afrika. Anderzijds wordt in het algemeen de gezondheid van kinderen op het platteland minder bedreigd dan in de grote steden. Toenemende urbanisatie heeft geleid tot toegenomen morbiditeit en mortaliteit. Kindersterfte is in de steden driemaal zo hoog als op het platteland. Behalve malaria zijn geen van de belangrijkste doodsoorzaken van kinderen typisch voor de tropen, maar zijn ze eerder geassocieerd met factoren zoals grote bevolkingsdichtheid, armoede, onvoldoende scholing, gebrekkige hygiëne en slechte kwaliteit van het drinkwater.
Veel kinderen in de Derde Wereld hebben langdurig een onvoldoende inname (c.q. opname) van energie, hetgeen bijdraagt tot een achterblijvende lengtegroei. In situaties van plotseling optredende voedseltekorten of in het geval van een acuut verlopende koortsende ziekte treedt bovendien vermagering op, met als gevolg een te laag gewicht voor de lengte. Een klein deel hiervan, en dan voornamelijk de jonge kinderen, toont verschijnselen van ernstige ondervoeding (severe protein energy malnutrition; pem). Bij kinderen in de Derde Wereld bestaat er een synergie tussen een gebrek aan adequate voeding enerzijds en infectieziekten anderzijds. Beide factoren dragen bij tot een onvoldoende groei en een verhoogde morbiditeit en mortaliteit. Overigens, in sommige landen die tot (de invloedssfeer van) de voormalige Sovjet-Unie behoorden, werd gedurende het laatste decennium een toename van het aantal kinderen met difterie, polio, luchtweginfecties en cholera gevonden. Het percentage volledig gevaccineerde eenjarigen nam er sinds het midden van de jaren tachtig van de vorige eeuw af van 88% tot 77% in het begin van de jaren negentig, terwijl de kindersterfte weer toenam.
Preventie van ziekte en sterfte bij kinderen in de Derde Wereld
Door de who en Unicef werd in het begin van de jaren tachtig van de twintigste eeuw het zogenoemde gobi-programma gelanceerd. Dit programma beoogt de volgende aspecten van interventie te stimuleren: groei, diarreebehandeling met orale rehydratieoplossing (ors), langdurige borstvoeding en immunisatie.
Aan het gobi-programma werd ook een fff-programma gekoppeld (tabel 30-1), mikkend op het bevorderen van een goede geboorteregeling (family planning), het stimuleren van scholing voor vrouwen (female literacy) en het verrijken van de voeding voor zwangeren, zogenden en kinderen (food fortification). Verbetering van de algehele socio-economische conditie is fundamenteel voor een verbetering van de gezondheidstoestand van een bedreigde groep. Echter, structurele verbetering van de positie van de armen vraagt om wereldwijde politieke motivatie en besluitvorming.
| growth monitoring | volgen van gewicht en lengte |
| oral rehydration | orale rehydratie |
| breast feeding | borstvoeding |
| immunization | vaccinaties |
| female education | scholing van (jonge) vrouwen |
| food supplementation | bijvoeding van risicogroepen |
| family planning | geboorteregeling en –spreiding |
Aanzienlijke vooruitgang werd geboekt door een verbetering van de behandeling van acute gastro-enteritis door een correct gebruik van ORS. In 1995-2000 paste ruim 60% van alle huishoudens in de Derde Wereld ORS toe (UNICEF, 2001). Een juist en doelmatig gebruik van ors blijkt goed te realiseren onder (poli)klinische omstandigheden. Onder huiselijke omstandigheden is het effect van ORS echter minder overtuigend. Fouten gemaakt bij het samenstellen van de ORS en de slechte kwaliteit van het drinkwater spelen hierbij een belangrijke rol. Daarnaast resulteerde een intensivering van het immunisatieprogramma door het Expanded Programme on Immunization (EPI-WHO) in een toename van de vaccinatiegraad tot 83% (80% voor BCG) bij eenjarigen in 1997-1999. Het GOBI-programma heeft belangrijk bijgedragen tot een verdere daling van de sterfte bij kinderen jonger dan vijf jaar: de U5MR daalde in de periode 1960-1999 van 222 naar 90 (UNICEF, 2001). Een belangrijk deel van deze reductie komt door het terugdringen van de zo gevreesde mazelen door een verbeterde vaccinatiegraad. Desondanks bedroeg in 1995 de aan mazelen gerelateerde mortaliteit nog 7% van de u5mr (figuur 30-1). Wereldwijd trad er een daling van de kindersterfte op. In Afrika ten zuiden van de Sahara nam echter de absolute sterfte van kinderen toe (ruim 4 miljoen in 1999) door een toename van het aantal geboorten. Circa een kwart hiervan stierf aan de gevolgen van malaria. Gezien de gunstige effecten van vitamine-A-suppletie op de morbiditeit en de mortaliteit van gastroenteritiden, luchtweginfecties en mazelen, wordt sinds de jaren tachtig van de vorige eeuw in streken met een hoge U5MR om de drie tot zes maanden orale vitamine-A-suppletie gegeven (respectievelijk 100.000 en 200.000 E).
Interventieprogramma’s op het gebied van de jeugdgezondheidszorg kunnen slechts geringe verlichting bieden in een kansarme samenleving. Op de wereldtopontmoeting voor kinderen in 1990 (World Summit for Children) werden door de wereldleiders tien prioriteiten voor het volgende decennium geformuleerd. Hiervan had het merendeel betrekking op het welzijn van moeder en kind, zoals het terugdringen van de U5MR met eenderde of tot 70:1000 levend geboren kinderen; de reductie van de moederlijke sterfte met 50% en vermindering van de incidentie van LBW naar minder dan 10%. Verder streeft men naar een vaccinatiegraad van 90% bij alle eenjarigen. Ter vergelijking: in 1995 was in Nederland de vaccinatiegraad voor DKTP 1 tot en met 4 en BMR circa 96%. Echter, in de Verenigde Staten bedroeg dit voor een vergelijkbaar schema slechts 76% (hetgeen met name te wijten was aan de lagere vaccinatiegraad bij bepaalde sociaal zwakkere etnische groepen in de steden). Verder streeft men ernaar de kindersterfte veroorzaakt door diarree en luchtweginfecties met respectievelijk de helft en eenderde terug te dringen. In het jaar 2000 wilde men bereiken dat 80% van de kinderen (zowel jongens als meisjes) de basisschool kon afmaken en dat iedereen in de wereld veilig drinkwater en goede sanitaire voorzieningen had. Deze doelen lijken echter niet gehaald te worden. Bijvoorbeeld, in de meeste landen van Afrika ten zuiden van de Sahara bezocht in 1999 minder dan 60% van de kinderen de basisschool. Ten slotte werd tijdens deze wereldtop het streven geuit dat iedereen in de gelegenheid wordt gesteld zich te informeren over geboorteregeling en ook de mogelijkheid krijgt die toe te passen. Alle landen dienen dan de Conventie voor de Rechten van het Kind na te volgen.
Naast preventieve maatregelen is het ook belangrijk aandacht te schenken aan een verbeterde, geprotocolleerde, curatieve zorg (improved case management) voor het zieke kind in de eerste lijn, zoals benadrukt werd in het recente who/unicef-initiatief voor het zogenoemde Integrated Management of Childhood Illness (imci). Ook de Wereldbank onderschrijft deze gecombineerde aanpak, die kostenbesparend zou werken en bovendien een substantiële verbetering van het wereldgezondheidspeil zou kunnen geven, met name in de ontwikkelingslanden. Inmiddels wordt in een aantal landen onderzocht of het imci-programma inderdaad deze beoogde effecten heeft.
Kernboodschappen over gezondheid en ziekte van kinderen in de Derde Wereld:
voor verbetering van hun gezondheidstoestand zijn preventieve maatregelen het belangrijkst;
daarnaast is een goede behandeling van ziekten onontbeerlijk.
Genetische afwijkingen en enzymdefecten
De meeste genetische afwijkingen komen in de tropen in ongeveer dezelfde frequentie voor als in andere delen van de wereld. Op deze regel zijn enkele uitzonderingen. Zo lijken cystische fibrose (cf) en fenylketonurie zeer zelden in de tropen voor te komen. De vraag is of dit verklaard wordt doordat diagnoses gemist worden door beperktere mogelijkheden. Daarentegen worden hemoglobinopathieën en G6PD-deficiëntie frequent aangetroffen, waarschijnlijk omwille van een verminderde vatbaarheid voor malaria onder de heterozygote dragers van deze erfelijke aandoeningen. In tabel 30-2 wordt een overzicht gegeven van het voorkomen van enkele genetische afwijkingen bij kinderen afkomstig uit die delen van de wereld, die in Nederland en België ruim vertegenwoordigd zijn. Hier dient eveneens vermeld te worden dat alle pasgeboren en oudere zuigelingen, overal ter wereld, over een intestinale lactaseactiviteit beschikken, maar dat de overgrote meerderheid van de wereldbevolking die activiteit in de loop van de kinderjaren om genetische redenen verliest (‘adult type’-primaire lactasedeficiëntie). Dit fenomeen wordt dikwijls versneld door ondervoeding, door herhaalde episoden van gastro-enteritis en door parasitaire infestatie (zie giardiasis). Als lactosemalabsorptie gepaard gaat met klachten (onder andere opgeblazen gevoel, buikkrampen en diarree) spreekt men van lactose-intolerantie (zie ook hoofdstuk 19). Het persisteren van de intestinale lactaseactiviteit op volwassen leeftijd, zoals in Noord-Europa vrijwel de regel is (en ook bij enkele etnische groepen in onder andere Afrika), moet dus op wereldniveau als een uitzondering beschouwd worden.
| Kinderen uit: | Middellandse-Zeegebied | Suriname, Antillen | (Zuidoost-)Azië | Afrika |
|---|---|---|---|---|
| sikkelcelziekte | ++ | ++ | + | +++ |
| thalassemie | +++ | + | ++ | + |
| G6PD-deficiëntie | ++ | ++ | ++ | +++ |
+ komt soms voor, ++ komt voor, +++ komt vaak voor
Lichaamsgroei en voeding
De groei van een kind in de Derde Wereld verschilt van die van zijn leeftijdsgenoten in het Westen door het achterblijven van lengte en gewicht. Als oorzakelijke factoren worden voedingstekorten en infectieziekten genoemd. Daarnaast wordt de groei indirect beïnvloed door sociale factoren, zoals de socio-economische status (huisvesting, opleidingsniveau en werk van de ouders). Ook omgevingsfactoren, met name seizoensinvloeden, spelen hierbij een rol.
Het principe van de identificatie van at-risk-kinderen door het vastleggen van de groei werd in het begin van de jaren zestig van de twintigste eeuw door Morley als één van de eersten gepropageerd. Hij ontwikkelde een systeem waarbij het groeiverloop in de eerste levensjaren van elk kind wordt vastgelegd op een kaart, die aan de moeder in bewaring wordt gegeven. Deze road-to-health card was de voorloper van het child health passport. Dit laatste document, dat op het ogenblik in veel landen in gebruik is, bevat een grafiek waarop de groei vastgelegd kan worden. Verder biedt het de mogelijkheid informatie vast te leggen over de medische geschiedenis van het kind, zoals gegevens van primaire (onder andere vaccinaties), secundaire en tertiaire gezondheidscentra (ziekenhuisopnamen, medicijngebruik). Tevens kunnen eventuele risicofactoren uit de perinatale periode hierop worden aangegeven.
Het gewicht van het kind, gerelateerd aan de leeftijd, geeft informatie over de voedingstoestand. Dit gewicht wordt vergeleken met de groeicurve die is samengesteld op basis van de eerder vermelde Noord-Amerikaanse referentie (nchs, 1976). Indien het gewicht-naar-leeftijd 2 sd of meer onder het gemiddelde van deze referentiepopulatie ligt, wordt de diagnose significant malnutrition gesteld. Vervolgens dient de oorzaak van de groeiachterstand te worden achterhaald.
Groeivertraging in utero
De intra-uteriene groei blijkt in de Derde Wereld ten opzichte van het Westen in het algemeen in geringe mate achter te lopen. Als gevolg van methodologische problemen is nog niet vastgesteld in welke fase van de zwangerschap de groeisnelheid het meest achterblijft. Het is overigens gebleken dat tijdens de zwangerschap de behoefte aan extra energie beduidend minder is dan men aanvankelijk dacht. Recente gegevens ramen deze extra energiebehoeften op slechts 0,8 mJ/d (200 kcal/d) boven die van de niet-zwangere.
Er zijn aanwijzingen dat de uitrijping van de foetale organen, met name onder de negroïde bevolking, juist iets sneller verloopt dan in het Westen. Mogelijk verklaart dit, in vergelijking tot westerse prematuren van dezelfde zwangerschapsduur, de lage incidentie van hyalienemembranenziekte in de tropen. In de laatste jaren is gebleken dat door ingrijpende veranderingen in het metabolisme van de zwangere vrouw, er vele aanpassingen zijn die een adequate voeding van de foetus, ook tijdens een periode van marginale maternale voedselinname, mogelijk kunnen maken. Enkele van deze veranderingen van het maternale metabolisme, die waarschijnlijk gestuurd worden door foetale hormonen uit de placenta, zijn:
het aanleggen van een energievoorraad (de stapeling van enige kilo’s vet) gedurende de eerste 28 weken van de zwangerschap, wanneer de foetale behoeften nog relatief gering zijn. Deze energievoorraad kan weer gebruikt worden tijdens perioden van verhoogde behoefte: het laatste trimester van de zwangerschap en de lactatieperiode;
beperking van de lichaamsactiviteit;
een effectievere resorptie van allerlei nutriënten.
Postnatale catch-upgroei
Hoewel het gemiddelde geboortegewicht in de meeste tropische landen 300-600 g lager ligt dan dat in de meeste West-Europese landen, blijkt dit verschil op de leeftijd van een maand nagenoeg te zijn verdwenen, mits het kind volledige borstvoeding krijgt. Hoe deze inhaal- of catch-upgroei verklaard moet worden, is slechts ten dele duidelijk. Anders dan in het Westen blijkt het gemiddelde gewichtsverlies na de geboorte beperkt te blijven tot circa 3-4% van het geboortegewicht (voor de westerse landen is dit 4-8%), waardoor de postnatale groei sneller ingezet kan worden en het geboortegewicht reeds rond de vierde-vijfde dag alweer bereikt is (voor het westerse kind is dit na vijf tot acht dagen).
Een andere verklaring voor de grotere gewichtstoename gedurende de eerste levensmaanden (figuur 30-2) moet wellicht gezocht worden in het gegeven dat het jonge kind over het algemeen 24 uur per dag bij de moeder blijft. ‘s Nachts slaapt de moeder naast haar baby, waardoor het kind zowel warmte als borstvoeding kan krijgen. Overdag draagt de moeder het kind in het algemeen bij zich en kan het, zodra het een teken van honger geeft, borstvoeding krijgen (feeding on demand). Gemiddeld komt dit neer op maar liefst twaalf à dertien voedingen per dag. Door het regelmatig en herhaaldelijk leegmaken van de borsten met het zogen wordt de totale 24-uurs-moedermelkproductie gestimuleerd. De grote waarde van borstvoeding voor het kind is genoegzaam bekend. Het volume en de samenstelling van de moedermelk blijken meestal voldoende te zijn om gedurende ten minste de eerste vijf à zes levensmaanden een adequate groei en ontwikkeling veilig te stellen. Anderzijds biedt moedermelk vanwege de aanwezigheid van onder andere oligosachariden, immunoglobulinen, lactoferrine, lysozym en macrofagen een bescherming tegen infecties (zie ook hoofdstuk 6).
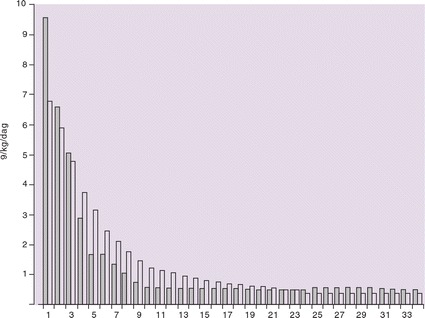
Groei tussen vier en achttien maanden
Vanaf de vierde tot achttiende levensmaand blijkt de gemiddelde gewichtstoename per kg per dag ten opzichte van de westerse referentiecurven terug te lopen. De lengtegroei vertoont hetzelfde beeld. Men dient zich echter te realiseren dat de referentiecurven gebaseerd zijn op gegevens van Noord-Amerikaanse kinderen van wie de meerderheid flesvoeding kreeg. Tot en met de leeftijd van zes maanden dekt borstvoeding over het algemeen de behoefte aan energie en eiwit en vertonen borstgevoede kinderen adequate groei. Echter, ook na de eerste zes levensmaanden blijft moedermelk de belangrijkste bron van eiwit. Preventie van groeiachterstand door middel van voedingsinterventie lijkt alleen zinvol voor kinderen jonger dan twee jaar, aangezien in deze periode de groeiachterstand ontstaat.
Primitieve hygiënische en sanitaire omstandigheden, samen met een niet-optimale voedingstoestand van de moeder en een verhoogd energieverbruik door arbeid (in Afrika wordt, afhankelijk van de streek, 60 à 90% van het werk in de landbouw door vrouwen uitgevoerd) zouden hierbij een rol spelen. Indien de moeder het kind bijvoeding geeft, is de samenstelling hiervan vaak inadequaat, waardoor de behoeften van het kind niet gedekt worden. Hoewel het toedienen van extra energie vanaf de zesde maand, in de vorm van bijvoeding, in het algemeen wordt aanbevolen, kleven hieraan ook belangrijke nadelen. Als nadelig effect kan genoemd worden de toenemende kans op gastro-intestinale infecties (weanling diarrhoea), met name in gebieden waar primitieve hygiënische en sanitaire omstandigheden prevaleren (onder andere besmet water). Verder bestaat het risico dat de bijvoeding de stimulans voor de lactatie doet afnemen. Elk kind zal men dus zolang mogelijk uitsluitend borstvoeding willen voorschrijven zolang de groei, afgezet op de groeicurve, niet naar beneden afbuigt. Vanaf een zekere leeftijd blijken de voordelen van het geven van bijvoeding echter zwaarder te wegen dan de nadelen. Nochtans zal men zo veel en zolang mogelijk de borstvoeding willen blijven stimuleren. Om dit te bereiken moet de bijvoeding altijd na de borstvoeding en met een lepeltje gegeven worden, en niet met de fles. Door contaminatie van de bijvoeding, maar eveneens door het geleidelijk verdwijnen van de prenataal verworven moederlijke antilichamen (immunoglobuline G) met daaraan gekoppeld de toegenomen autonomie van het kind (kruipen), verklaren dat het risico voor infecties op de leeftijd van ongeveer zes maanden zal toenemen. Vooral de gastro-enteritiden en luchtweginfecties nemen vanaf die leeftijd duidelijk in frequentie en ernst toe.
De periode waarin het kind van borstvoeding via bijvoeding overgaat op een voeding waarvan de samenstelling in hoofdzaak op die van de volwassene lijkt (4-18 maanden oud), wordt in het algemeen gekenmerkt door een vertraging van de groeisnelheid. Vooral bij kinderen bij wie de ene infectie de andere opvolgt zal dit het meest opvallend zijn. Naast de reeds genoemde luchtweg- en gastro-intestinale infecties spelen hierbij ook mazelen, kinkhoest, tuberculose en aids een belangrijke rol.
Groei tussen achttien maanden en vier jaar
In deze periode herstelt de gewichtstoename zich enigszins en kan er zelfs een geringe catch-up waargenomen worden. Toch blijft het gewicht op vierjarige leeftijd nog circa 2,5 kg onder dat van het westerse kind. De verschillen in groeisnelheid tussen het tropische en het westerse jonge kind (0-3 jaar) zijn weergegeven in figuur 30-2.
Groei na het vijfde jaar
Deze verloopt in de lengte ongeveer parallel, maar in een lager traject, aan die van het westerse kind, waardoor de uiteindelijke gemiddelde lengte op volwassen leeftijd ook aanzienlijk lager uitkomt. De puberteit treedt in het algemeen later in, waardoor de groei wel langer doorloopt.
Kernboodschappen over groei van het kind in de Derde Wereld:
het gemiddelde geboortegewicht ligt 300-600 g lager;
uitsluitend geven van borstvoeding in de eerste zes maanden voorkomt maag-darminfecties en garandeert goede groei;
na zes maanden buigt de groeicurve voor gewicht en lengte af;
inhaalgroei vindt daarna vrijwel niet plaats;
ziekte en gebrekkige voeding versterken elkaar in het ontstaan van slechte groei en ondervoeding;
uiteindelijk heeft gemiddeld 33% van de kinderen jonger dan vijf jaar een veel te kleine lengte (< -2 sd) voor de leeftijd.
Ondervoeding
Epidemiologie
Het is niet eenvoudig aan te geven hoeveel kinderen in de wereld aan ernstige ondervoeding lijden. Het is duidelijk dat deze aantallen zullen afhangen van de diagnostische criteria die gehanteerd worden. Om louter praktische redenen wordt door de internationale organisaties nog steeds de meeste waarde gehecht aan de antropometrische criteria (voedingstoestand uitgedrukt in lengte, gewicht voor de leeftijd en gewicht bij een gegeven lengte; middenomtrek van de linkerbovenarm). Op die basis zijn er volgens de Unicef wereldwijd bijna eenderde van alle kinderen jonger dan vijf jaar bij wie het gewicht voor de leeftijd 2 sd of meer onder de mediaan ligt van de referentiepopulatie (nchs 1976; zie eerder). Hoewel de absolute cijfers van ernstige ondervoeding toenemen, blijkt de prevalentie van ernstige ondervoeding in alle werelddelen, met uitzondering van Afrika ten zuiden van de Sahara, te verminderen. Anderzijds is het opmerkelijk dat een laag gewicht voor leeftijd, evenals een vertraging van de lengtegroei (onder de 2 sd van de referentiecurve), nog bijzonder vaak voorkomt in Zuid-Azië, ook al is de voedingstoestand er duidelijk verbeterd (tabel 30-3).
De voornaamste oorzaken van ondervoeding zijn armoede en onwetendheid, maar daarnaast spelen overbevolking, exploitatie, oorlogen en natuurrampen eveneens een belangrijke rol. Als ondervoeding puur het gevolg is van een kwantitatief en/of kwalitatief inadequate voedselconsumptie spreekt men van primaire ondervoeding. De voeding kan een of meerdere tekorten hebben van macronutriënten (koolhydraten en vetten als energiebron, eiwit voor de groei) of micronutriënten (bijvoorbeeld mineralen, vitaminen en sporenelementen). Het risico van ondervoeding neemt toe bij individuen met een verhoogde behoefte, zowel in kwantitatieve als in kwalitatieve zin. Kwetsbare groepen zijn snel opgroeiende jonge kinderen en adolescenten, evenals zwangere en lacterende vrouwen. Infectieziekten spelen een voorname rol bij het uitlokken van chronische en acute ondervoeding en bij een gecompenseerde relatieve ondervoeding. Iedere ziekteperiode gaat gepaard met een vermindering van de eetlust, waardoor de consumptie van voedsel nadelig wordt beïnvloed, terwijl de verliezen en de behoeften door de infectieuze episode toenemen. Ook kan de opname van de voedingsstoffen verstoord zijn. Dit laatste kan de verliezen doen toenemen. Door al deze factoren tezamen kan de behoefte niet meer door de inname gedekt worden. In dergelijke gevallen spreekt men van secundaire ondervoeding. Het zal duidelijk zijn dat er in de praktijk meestal sprake is van een combinatie van primaire en secundaire ondervoeding. Vanwege de verschillen in de etiologische momenten kan ondervoeding verschillende klinische vormen aannemen. Door toegenomen immigratie van ondervoede kinderen uit derdewereldlanden (onder andere door adoptie, overplaatsing voor medisch-heelkundige behandeling naar gespecialiseerde centra), worden primaire en secundaire ondervoeding meer en meer in westerse ziekenhuizen aangetroffen. Daarnaast heeft de toenemende intensivering van de behandelingsmethoden tijdens de kinderjaren, zoals maligne aandoeningen, chronische malabsorptie en andere ernstige chronische ziekten ook geleid tot toename van de klassieke ondervoedingsbeelden in onze ziekenhuizen. Mede hierom is het gerechtvaardigd op deze plaats aandacht te besteden aan deze ziektebeelden.
Primaire of secundaire ondervoeding:
primaire ondervoeding treedt op als gevolg van inadequate voedselconsumptie;
secundaire ondervoeding treedt op als gevolg van ziekte.
Pathofysiologie en terminologie
Er bestaat onenigheid over de terminologie en de pathofysiologie van de verschillende ondervoedingssyndromen. Ook het gegeven dat eenzelfde type ondervoeding naar gelang de leeftijd verschillende klinische vormen kan aannemen, heeft niet bijgedragen tot grotere duidelijkheid.
Terminologie
De twee belangrijkste klinische ondervoedingssyndromen - kwashiorkor en marasmus - worden veelal toegeschreven aan respectievelijk een deficiënte consumptie van eiwit en aan een combinatie van een tekort aan energie en eiwit. In een ontwikkelingsland kan men echter niet verwachten dat deze deficiënties totaal geïsoleerd voorkomen. Veeleer wordt het klinische patroon mede bepaald door een relatieve bijdrage van geassocieerde anomalieën in de toevoer en de homeostase van mineralen (zoals kalium, magnesium en calcium), van vitaminen (zoals vitamine A) en van sporenelementen (zoals ijzer, zink, koper, jodium, selenium). Deficiënties van sommige bestanddelen van de voeding geven aanleiding tot specifieke en klinisch gemakkelijk herkenbare deficiëntiesymptomen. Als voorbeeld moge dienen jodium, ijzer en selenium. Andere bestanddelen - zoals essentiële aminozuren, energie, zink, kalium, natrium - manifesteren zich hoofdzakelijk door een groeivertraging, en minder door specifieke symptomen. Daarnaast wordt het ziektebeeld mede bepaald door gelijktijdig verlopende ziekteprocessen zoals infecties en intoxicaties. Het klinische tableau kan verder nog vertroebeld worden door additionele fenomenen die niet per se deel uitmaken van de primaire pathologie, maar daar eerder het gevolg van zijn. Uit bovenstaande mogen we afleiden dat het niet zinvol is een ernstig ondervoedingsbeeld tot één enkelvoudige klinische entiteit te herleiden. Er bestaan waarschijnlijk evenveel vormen van ondervoeding als er omstandigheden zijn waaruit het kan ontstaan.
Schematisch kan men zich de volgende sequentie bij de ontwikkeling van de ondervoedingsbeelden voorstellen. Als gevolg van een globaal onvoldoende inname of opname van macronutriënten - waarbij de aard naar gelang de omstandigheden kan verschillen - zal het kind voor het instandhouden van de basale behoeften zijn reserves en eventueel zijn eigen lichaamsweefsel aanspreken. De lengtegroei stagneert en de normale gewichtstoename blijft achterwege. In de meest ernstige gevallen neemt het gewicht zelfs af. Dit beeld wordt marasmus genoemd. Marasmus wordt dikwijls beschouwd als een (adequate) adaptatie van het organisme wanneer door een chronisch voedseltekort of herhaalde infecties onvoldoende voeding geconsumeerd of opgenomen wordt voor de instandhouding van de weefsels en de groei. Met name is de energietoevoer limiterend. Een verhoogde cortisol- en een verlaagde insulinesynthese zouden hierbij een belangrijke rol spelen. Door het spierkatabolisme komen essentiële aminozuren vrij voor de eiwitsynthese in de lever, inclusief de transporteiwitten, albumine en lipoproteïnen. Er is geen oedeemvorming. Het metabolisme en het transport van de lipiden is niet aangedaan. Er wordt ook geen vetinfiltratie van de lever gezien.
Men spreekt van kwashiorkor wanneer er een ernstige metabole dysregulatie voorkomt bij een kind met een reeds bestaande lichte vorm van ondervoeding, bij wie de energetische behoefte gedekt was (geen marasmusontwikkeling en geen belangrijke vertraging van de lengtegroei). Men spreekt van een marasmus-kwashiorkor bij een kind met marasmus bij wie door een acuut probleem (bijvoorbeeld een tekort aan eiwitten of een infectieziekte) een ernstige metabolische dysregulatie in bijna alle organen ontstaat. Kenmerkend voor dit beeld is een geringe synthese van vele serumeiwitten. Intoxicaties, zoals met aflatoxinen, zouden hierbij eveneens een rol kunnen spelen.
Twee belangrijke hypothesen
De klassieke theorie schrijft kwashiorkor toe aan een eiwitdeficiëntie gekoppeld aan nutriënten die met de eiwitinname geassocieerd worden, zoals kalium, sommige sporenelementen (onder andere zink) en enkele vitaminen (onder andere van de B-groep). Infectieuze stress vormt een belangrijk uitlokkend moment. Deze theorie wordt door epidemiologische onderzoeken ondersteund: kwashiorkor komt vooral voor in gebieden waar het voedsel eiwitarm en de eiwit/energieratio laag is. Zolang de energietoevoer voldoende is en de eiwitinname tekortschiet, zal er een verhoogde insulinesecretie plaatsvinden en een verminderde productie van cortisol. Hierdoor zal de aminozuuropname in de spieren toenemen ten koste van de eiwitsynthese in de lever, met als gevolg een hypo-albuminemie en een hypo-lipoproteïnemie. Deze laatste zou bijdragen tot een leversteatose (vervetting). Tijdens een infectie zal het proces versterkt worden, doordat meer aminozuren gebruikt worden voor de synthese van acutefaseproteïnen (bijvoorbeeld ferritine en C-reactief proteine: crp).
De tweede theorie stelt dat kwashiorkor veroorzaakt wordt door oxidatieve stress door een verstoring van de balans tussen de productie van vrije radicalen en stoffen die neutraliserend kunnen werken, zoals β-caroteen, vitamine E, selenium en zink. Zo is de verhoogde productie en de onvoldoende neutralisatie van vrije radicalen een secundair fenomeen, dat kan worden toegeschreven aan sommige nutritionele tekorten, aan verstoorde metabole processen in de cel, en aan infecties. Zwaar ondervoede kinderen worden onderworpen aan een reeks noxae die aanleiding zullen geven tot een verhoogde productie van vrije radicalen. Oxidatieve stress kan ernstige levensbedreigende schade toebrengen aan allerlei weefsels (multi organ failure; mof). Dit zou de hoge mortaliteit kunnen verklaren. Een definitief bewijs voor deze theorie is echter nog niet geleverd.
Infectieuze stress speelt in beide theorieën een duidelijke rol.
Kernboodschappen (I) met betrekking tot ernstige eiwit- en energieondervoeding (protein energy malnutrition; pem):
ernstige ondervoeding ontstaat door meerdere oorzaken;
men onderscheidt marasmus, kwashiorkor en marasmic kwashiorkor;
marasmus kenmerkt zich door sterke vermagering;
marasmus ontstaat door chronisch gebrek aan nutriënten;
kwashiorkorbeelden kenmerken zich door hongeroedeem;
zij worden meestal uitgelokt door infecties;
er bestaan hierbij tekorten van zowel macro- als micronutriënten;
in feite is er een multi organ failure (mof).
Ziektebeelden
Gemakshalve worden de diverse ondervoedingsbeelden vaak onderverdeeld volgens de zogenoemde Wellcome-classificatie (tabel 30-4).
| Gewicht voor leeftijd* | Oedeemvorming | Geen oedeemvorming |
|---|---|---|
| 80-60% | kwashiorkor | ondervoeding |
| < 60% | marasmus-kwashiorkor | marasmus |
* percentage van het referentiegewicht voor een bepaalde leeftijd (NCHS-standaard)
Marasmus
Marasmus ontwikkelt zich in het algemeen op een jongere leeftijd (6 maanden-1 jaar) dan kwashiorkor en marasmus-kwashiorkor (tweede en derde levensjaar). Rekening houdend met de etiologische factoren zullen deze ondervoedingsbeelden over het algemeen niet meer voorkomen wanneer het kind de leeftijd van vijf jaar heeft bereikt, tenzij het lijdt aan een chronische ziekte zoals tuberculose. Nochtans zijn dergelijke gevallen bij grotere kinderen, adolescenten, zwangere en borstvoedinggevende vrouwen geen uitzonderingen in situaties waar chronisch en ernstig voedseltekort regel is en waarbij om andere reden de nutritionele tekorten nog verergerd worden door bijvoorbeeld een acute infectie, acute (seizoensgebonden) voedselschaarste, zwangerschap en lactatie, of oorlog. Ook kan men marasmus tegenkomen vóór de leeftijd van zes maanden bij onvoldoende moedermelkproductie, al dan niet bij een ingetrokken tepel. In de meeste gevallen ontstaan de ondervoedingsbeelden geleidelijk, maar kwashiorkor kan ook in enkele dagen optreden, bijvoorbeeld tijdens of na een ernstige infectieziekte zoals mazelen of Shigella-dysenterie (zie elders). Bij ernstige ondervoeding kunnen talrijke, meestal reversibele afwijkingen worden aangetroffen. Marasmus wordt gekarakteriseerd door het beeld van het magere, dystrofische oude mannetje of vrouwtje dat met grote verschrikte ogen gespannen rond zich heen kijkt (zie figuur 30-3). Het kind is vaak hongerig. Vanwege het sterk verminderde subcutane vet zit het kind erg ruim in zijn/haar huid. De lengtegroei is vertraagd.

Kwashiorkor en marasmus-kwashiorkor
Casus
Muhindo is twee jaar. De moeder komt ons raadplegen omdat haar zoon er al vijf dagen over het hele lichaam gezwollen uitziet. Hij is het vierde kind. Zijn moeder is zeven maanden zwanger. Sinds enkele maanden is hij volledig gespeend. Sinds twee weken vertoont hij een aanhoudende slijmerige diarree en is koortsig. Op het gezondheidscentrum werd ors voorgeschreven. Muhindo kreeg eveneens drie dagen cotrimoxazol, maar de behandeling werd niet afgemaakt vanwege de grote afstand tot het gezondheidscentrum en de prijs van de geneeskundige verzorging. Tot voor kort was de vader van Muhindo werkzaam op een plantage, hetgeen het gezin van een klein maar regelmatig inkomen verzekerde. Nu overleeft de familie van de producten afkomstig van de familiale velden (in totaal niet meer dan een halve hectare groot!). De familiale maaltijden bestaan hoofdzakelijk uit bonen, cassave, bananen, groenten, zoete aardappelen en maïs. Zeer zelden wordt een weinig vlees en palmolie gebruikt. De dieetanamnese van Muhindo leert ons dat bonen voor meer dan 80% van de eiwitinname instaan en dat minder dan 10% van de energie-inname van vetten afkomstig is. De totale eiwit- en energie-inname wordt op respectievelijk 70 en 95% van de behoeften geschat. Lichamelijk onderzoek: hierbij valt op dat Muhindo, ondanks de massieve oedemen, er uitgedroogd uitziet. Lengte en gewicht, met oedemen, zijn respectievelijk 77,4 cm (89% van NCHS-standaard voor de leeftijd) en 9,5 kg. Het haar is dof en ontkleurd. De huid is ontkleurd en gecraqueleerd. De lever wordt 3,5 cm onder de ribbenboog gepalpeerd. Biologisch onderzoek levert de volgende resultaten op: hematocriet 32%, totale eiwitten 40 g/l, serumalbumine 10 g/l. De urine vertoont geen afwijkingen. Op grond van het onderzoek wordt de diagnose kwashiorkor gesteld, zonder aanwijzingen voor een intercurrent infect.
Therapie: Muhindo wordt gedurende de eerste twaalf uur voorzichtig gerehydrateerd. Tegelijkertijd wordt de realimentatie gestart, gebruikmakend van energierijke melk. Vijf dagen later beginnen de oedemen af te nemen; het gewicht valt terug tot 8,3 kg (66% van de nchs-standaard voor de leeftijd, maar 80% van de NCHS-standaard voor de lengte); de serumalbumineconcentratie op dat ogenblik is 22 g/l. De realimentatie wordt voortgezet met energierijke melk en lokale voedingsmiddelen. Tien dagen later verlaat Muhindo het ziekenhuis met een gewicht van 8,7 kg (85% van de NCHS-standaard voor de lengte). Om een recidief te voorkomen wordt zijn familie naar een multidisciplinair follow-upprogramma verwezen, dat door het gezondheidsdistrict georganiseerd wordt.
Bij deze ziektebeelden staat, bij het stellen van de diagnose, de oedeemvorming centraal. Zolang het kind zit of staat is beginnend oedeem het eerst merkbaar op de voetrug en de pretibiale regio. In een later stadium breidt het zich uit over de bovenste ledematen (handen) en het hoofd (oogleden). In dit laatste geval herkent men het typische vollemaansgezicht. In liggende positie verplaatst het oedeem zich naar de bovenste ledematen en het aangezicht. De kinderen zijn apathisch en vertonen geen belangstelling voor de omgeving. Zij zien er miserabel uit en weigeren te eten. Bij onderzoek huilen zij constant op een klaaglijke wijze zonder dat er tranen te zien zijn (figuur 30-4).

Het haar is rossig, dof en dun, en valt gemakkelijk uit. Soms is het haar volledig ontkleurd (wit). Perioden van ondervoeding en adequate voeding zijn dan in de kleur van het haar terug te vinden, het zogenoemde flag-sign (figuur 30-5). De huid vertoont zeer uiteenlopende afwijkingen: deze is op vele plaatsen ontkleurd (hypopigmentatie), soms glanzend (pretibiaal), dun en kwetsbaar. Vaak vertoont de huid een gecraqueleerd aspect of schilfert af en zijn er fissuren. Vaak zijn er verschijnselen van een ontsteking waarneembaar. De hypopigmentatie is het duidelijkst aanwezig op de knieën, in de liezen, op de heupen en billen, alsook op de ellebogen en in het halsgebied. In de ernstigste gevallen komt de huid vooral in de plooien los te liggen, waardoor het onderhuidse weefsel bloot valt. Dit laatste is in prognostische zin erg ongunstig. Dit beeld wordt in de Engelse literatuur flaky-paint-dermatose genoemd (zie figuren 30-4 en 30-6).


Door dit ingewikkelde samenspel van afwijkingen zijn de functies van nagenoeg alle organen gestoord, er is in feite een multi-organ failure (mof). Het hart is klein als gevolg van een afname van de spiermassa. Het hartminuutvolume kan verminderd zijn, hetgeen een verlenging van de circulatietijd tot gevolg kan hebben. Hierdoor kan de perfusie van de verschillende weefsels, en zodoende de functie van de betreffende organen, beïnvloed worden. Zo kan een verminderde nierperfusie de vochtretentie en daardoor de oedeemvorming in de hand werken. Bij de behandeling van deze kinderen dient men daarom terdege rekening te houden met de verminderde hartfunctie. Wat betreft de renale functies is het concentrerende vermogen sterk verminderd, evenals het vermogen om verdunde urine uit te scheiden. Er bestaat een verminderd vermogen tot uitscheiding van H+-ionen tijdens zuurbelasting.
Ook de tractus digestivus vertoont ernstige afwijkingen, die tot een malabsorptie kunnen bijdragen (tabel 30-5). Dit geldt met name voor ernstige ondervoeding, maar ook voor relatieve ondervoeding. In de praktijk blijkt de resorptie van het voedsel voldoende gehandhaafd, waardoor het spijsverteringsstelsel de veiligste weg voor realimentatie blijft. Het dieet zal zoveel mogelijk aangepast dienen te worden. Lactosebeperking wordt soms aanbevolen, vanwege de afgenomen lactaseactiviteit van het darmepitheel. Een vetstapeling die aanleiding kan geven tot een leververgroting wordt hoofdzakelijk bij kwashiorkor waargenomen. De frequentie van voorkomen wisselt van streek tot streek, waardoor het aannemelijk wordt dat bepaalde, nog onbekende etiopathologische factoren tot deze afwijking kunnen leiden. In het algemeen zijn deze afwijkingen reversibel.
|
bacteriële overgroei verminderd resorberend vermogen (atrofisch darmepitheel) beschadiging van het darmepitheel (o.a. door infectie) afgenomen synthese van verteringsenzymen (o.a. lactase, door epitheelschade) afgenomen synthese van pancreassappen |
Waarschijnlijk ontstaat de leververvetting doordat de vetten niet voldoende gemobiliseerd kunnen worden. Het is niet uitgesloten dat toxische stoffen, bijvoorbeeld aflatoxine, een beschadigende invloed op het levercelmetabolisme kunnen uitoefenen, waardoor de lipoproteïnesynthese vermindert. Er is een verlaagde aanmaak van de meeste transporteiwitten in de lever, zoals het transferrine en het ceruloplasmine en van het retinolbindende proteïne. Vooral tijdens een infectie zal de synthese van de zogenoemde acutefase-eiwitten toenemen ten koste van de aanmaak van de transporteiwitten.
In de hersenen van de kinderen die aan ernstige ondervoeding overleden zijn, worden bij histologisch onderzoek zelden afwijkingen in de structuur van de neuronen waargenomen. Wel worden in sommige onderzoeken biochemische en fysiologische veranderingen vastgesteld, die in ernst toenemen naarmate de ondervoeding ernstiger is en vroeger optreedt. Hoewel deze veranderingen in het verleden geassocieerd werden met een verminderd intellectueel vermogen, blijkt de laatste tijd een direct causaal verband niet goed aantoonbaar. Extra psychomotore stimulatie van het kind tijdens de herstelfase brengt een duidelijke verbetering van de intellectuele vermogens, die niet uitsluitend kan worden toegeschreven aan de verbetering van de voedingstoestand.
Diagnostiek
De diagnose berust in de eerste plaats op een nauwkeurige anamnese, inclusief een dieetanamnese (tabel 30-6), en op een volledig klinisch onderzoek (tabel 30-7). Rekening houdend met de complexiteit van de pathogenese is het evident dat diepgaande onderzoeken nodig zijn ter aanvulling van onze kennis. Nochtans zijn laboratoriumfaciliteiten in veel gebieden waar ondervoedingsbeelden regelmatig voorkomen, meestal zeer beperkt. Bij voorkeur zou men graag oriënterende informatie willen krijgen (tabel 30-8). Ook is informatie over de lokale socio-economische en sanitaire condities, alsmede van de voedselconsumptie, van groot belang.
|
familieanamnese: - socio-economische status - alleenstaande vader of moeder - leeftijd van broers en zusters - aantal overleden broers en zusters geboortedatum, geboortegewicht en zwangerschapsduur borstvoeding psychomotorische ontwikkeling vaccinaties ontstaan en duur van de ziekte contact met tbc, mazelen, dysenterie enzovoort recente voedingsanamnese vocht- en voedselinname gedurende de laatste dagen braken en diarree: duur, frequentie en intensiteit symptomen van dehydratie: ingezonken ogen? tijdstip laatste mictie |
|
gewicht en lengte oedeem huid: trofische letsels en purpura haar: pigmentatie, aspect lichaamstemperatuur ademhalingsritme symptomen van circulatoire collaps: - temperatuur van de extremiteiten - hartritme - perifere en capillaire pols - bloeddruk Bewustzijn dorst tekenen van hydratie: - turgor - ingezonken ogen - slijmvliezen ogen: xerophthalmie hepatomegalie, icterus abdominale distensie, peristaltiek anemie infectie: kno, mond, huid longen: infectie, longoedeem |
|
Bloed Hb, Ht, differentiatie dikke druppel (in malariagebieden) totaal eiwit en albumine glucose elektrolyten (Na, K, Cl, gasanalyse, Mg, Ca) bilirubine en transaminasen Urine basaal onderzoek en sediment Röntgenonderzoek x-thorax (longoedeem, tbc) Microbiologisch onderzoek kweek van bloed, urine, feces aids-test Feces vertering, pH, parasieten tuberculinetest (Mantoux) |
Therapie
Ofschoon de resultaten van bovenvermelde onderzoeken belangrijke informatie voor de behandeling kunnen verschaffen, is het in veel gevallen ook zonder deze gegevens mogelijk het kind te genezen, mits men voldoende kennis bezit van de pathofysiologie van de lokale ziektebeelden en van de meest voorkomende complicaties. Bij de behandeling van zware ondervoeding zal men, zoals ook in figuur 30-7 is aangegeven, drie fasen kunnen onderscheiden:
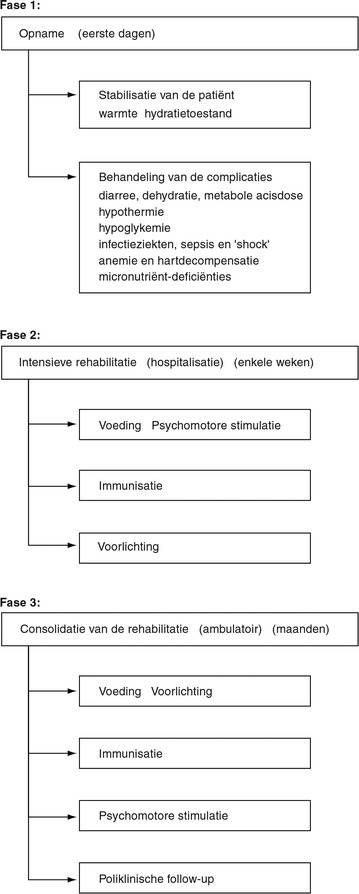
in eerste instantie moet de situatie van de patiënt gestabiliseerd worden en dienen de levensbedreigende complicaties voorkomen, opgespoord en behandeld te worden. Metabole ontregelingen en specifieke tekorten moeten worden gecorrigeerd;
zo snel mogelijk dient begonnen te worden met intensieve nutritionele rehabilitatie. Het kind zal gevoed en gestimuleerd moeten worden;
de moeder moet opgeleid worden voor verdere thuisbehandeling van haar kind; na ontslag zal het kind vervolgd dienen te worden om een recidief te voorkomen.
Metabole correctie, behandeling complicaties (onder andere dehydratie)
Bij ernstige ondervoeding wordt vooral gedurende de eerste dagen van de hospitalisatie een hoge sterfte gezien door de volgende oorzaken:
diarree, dehydratie en metabole acidose;
hypothermie;
hypoglykemie;
infectieziekten, sepsis en shock;
anemie en hartdecompensatie;
micronutriëntendeficiënties.
Dehydratie als gevolg van diarree is een veelvuldig voorkomende complicatie. Lichte tot matige uitdroging kan in het algemeen bestreden worden met de orale rehydratieoplossing (ors). In plaats van het door de who-unicef voor algemeen gebruik gepropageerde mengsel van glucosezout met bicarbonaat of citraat geeft men de voorkeur aan een ors (ReSoMal) met een iets lagere osmolariteit, die minder natrium, meer kalium en bovendien kleine hoeveelheden magnesium, zink en koper bevat (tabel 30-9). Deze oplossing dient wel frequent en in kleine hoeveelheden gegeven te worden. In het algemeen zal niet meer vocht dan circa 150 ml/kg in de eerste 24 uur mogen worden aangeboden, daar anders overmatige vochtretentie kan volgen (controle gewicht!). In geval van choleriforme (secretoire) diarree moet nochtans de standaard ors gebruikt worden. Borstvoeding zal altijd voortgezet dienen te worden. Systematisch deparasiteren wordt dikwijls aanbevolen. Bij ernstige uitdroging of wanneer het kind de ors niet verdraagt (bijvoorbeeld door hardnekkig braken), zal men liever eerder per druppelsonde dan per infuus het water en de elektrolyten willen toedienen. Intraveneuze rehydratie kan door onder andere overmatige vochttoediening verantwoordelijk zijn voor belangrijke iatrogene morbiditeit/mortaliteit, zoals hartdecompensatie en longoedeem, flebitis, ulceraties, necrose en sepsis. Het beleid van de rehydratie wordt bepaald en bijgesteld aan de hand van de klinische beoordeling (turgor, gewicht, perifere doorbloeding, vochtverlies via feces, braken, diurese, enzovoort). Vervolgens zal overgestapt moeten worden op het gebruikelijke energierijke dieet, in geleidelijk opklimmende concentratie (circa 150-175 ml/kg/d).
| Standaard ORS | ReSoMal | |
|---|---|---|
| Glucose | 110 | 125 mmol/l |
| Natrium | 90 | 45 mmol/l |
| Kalium | 20 | 40 mmol/l |
| Chloor | 80 | 70 mmol/l |
| Citraat | 10 | 7 mmol/l |
| Magnesium | - | 3 mmol/l |
| Zink | - | 0,3 mmol/l |
| Koper | - | 0,045 mmol/l |
| Osmolariteit | 311 | 300 mmol/l |
Hypothermie is een teken van ernstige malnutritie met volledige ontregeling van de homeostase, of van een sepsis. Hypothermie gaat gepaard met een hoge letaliteit. Het actief opsporen, voorkomen en behandelen van hypothermie is van vitaal belang.
Sufheid, convulsies en veranderingen in de bewustzijnstoestand zijn aspecifieke symptomen van hypoglykemie. Bij verdenking zal men onmiddellijk intraveneus glucose willen geven, liefst na capillaire bloedafname voor een glucosebepaling. Hypoglykemie kan voorkomen worden door gedurende de eerste dagen frequent (om de twee uren) of continu per maagsonde te voeden (ook ‘s nachts) en te waken voor nachtelijk afkoelen!
Infecties komen veel voor wegens de klassiek aanwezige immunodeficiëntie. Te noemen zijn: Gramnegatieve sepsis, meningitis, infecties van de luchtwegen, urinewegen en nieren, kno-infecties, stomatitis, diepe (spier)abcessen, dermatologische infecties, tbc of gastro-enteritiden door Salmonella of Shigella (zie hoofdstuk 15). Door de geringe afweer geven zij vaak weinig symptomen, onder andere kunnen koorts en een leukocytose ontbreken. Toch zijn de complicerende infecties een belangrijke oorzaak van sterfte en van uitblijvend herstel. Ondanks voldoende voedselopname kan gewichtstoename uitblijven. Ook kan het zich uiten in een toename van de oedemen (gewichtstoename) en vermindering van het serumalbumine. Sepsis en infectieziekten gaan vaak gepaard met hypothermie, hypoglykemie, purpura en shock. Respiratoire infecties komen veelvuldig voor, ook zonder koorts. Toepassing van routine-profylaxe met breedspectrumantibiotica wordt onder andere door de who aanbevolen. Wanneer ondanks antibiotische therapie en voldoende voedselinname geen verbetering optreedt, zal men een tuberculose moeten uitsluiten. De tuberculinetest is bij ernstige ondervoeding vaak onbetrouwbaar (foutnegatief). De diagnose zal dus ondersteund dienen te worden door een röntgenopname van de thorax of empirisch door verbetering van de klinische toestand na behandeling met tuberculostatica. De mortaliteit na mazelen bij ernstige ondervoeding is zeer hoog. Niet-geïmmuniseerde kinderen met ernstige ondervoeding zullen bij opname gevaccineerd moeten worden. Na herstel zal een herhalingsdosis van belang zijn omdat, gezien de immunodeficiëntie, de immuunreactie op de eerste vaccinatie onvoldoende geweest kan zijn.
Anemie bij zware ondervoeding wordt meestal multifactorieel bepaald. Foliumzuur-, riboflavine- of ijzerdeficiëntie en een hemolyse (malaria!) of een parasitaire infestatie kunnen hierbij een rol spelen. Men zal zeer voorzichtig om dienen te gaan met transfusies, gezien de reeds bestaande expansie van het circulatoire watercompartiment en de deficiënte hart- en nierfunctie. In sommige omstandigheden zijn transfusies toch nodig, zoals bij een zeer ernstige anemie (< 30 à 40 g Hb/l, Ht < 10 à 12%), een hypoalbuminemie (< 15 g/l) en in sommige gevallen hartdecompensatie. Bij voorkeur worden geconcentreerde rode bloedcellen of anders vers bloed gegeven, 10 a 15 ml/kg/d (langzaam toedienen). Dit kan eventueel herhaald worden. Tegelijkertijd met de transfusie wordt vaak een diureticum toegediend, bijvoorbeeld furosemide, 1 mg/kg, intraveneus. Digitalis kan gebruikt worden voor de behandeling van de hartdecompensatie, maar is gevaarlijk te hanteren door de veelal aanwezige hypokaliëmie! Micronutriëntdeficiënties komen veel voor bij ernstige ondervoeding. Om die reden worden dikwijls supplementen van vitaminen, mineralen en sporenelementen voorgeschreven. Een tekort aan kalium is een complicatie die tijdens de behandelingsfase tot een ernstige circulatoire collaps kan leiden. Ter voorkoming van deze levensbedreigende situatie zal men snel extra kalium willen geven (2 à 4 mEq/kg/d), zelfs als er (nog) een geringe urineproductie is. Zoals reeds aangegeven, dient men geen extra zout te geven! Magnesiumtekort komt regelmatig voor. Dit dient aangevuld te worden door circa 1,5 mEq/kg/d aan het dieet toe te voegen. Vitamine-A-deficiëntie kan snel tot blindheid leiden en is gedeeltelijk verantwoordelijk voor de hoge mortaliteit bij zware ondervoeding. Vitamine A wordt routinematig voorgeschreven aan elk ondervoed kind, met uitzondering van het borstgevoede kind jonger dan zes maanden. In sommige streken is een tekort aan sporenelementen aangetoond, met name zink en koper (bij suppletie: zink 1 mg/kg/d en koper 0,3 mg/kg/d). Men zal een ondervoed kind geen ijzer willen toedienen voordat het genezingsproces duidelijk begonnen is en het kind in gewicht aankomt. IJzersuppletie is pas aangewezen wanneer ook duidelijk een ijzerdeficiëntie aanwezig is.
Rehabilitatie
Dieet
De energiebehoeften zijn tijdens de herstelfase verhoogd. Bij de samenstelling van het dieet dient men hiermee rekening te houden. Het is dan ook noodzakelijk circa 150-200 kcal/kg/d (0,63-0,84 mJ/kg/d) te geven. Zeker bij aanwijzing van verstoorde leverfunctie (hyperbilirubinemie, gestegen transaminasen) zal men aanvankelijk niet te veel eiwitten willen toedienen (5% van de energietoevoer). De eiwitbehoefte kan op circa 3 g/kg/d worden gesteld indien men dierlijk eiwit geeft (dus ook melkeiwit).
Voor plantaardige eiwitten ligt de behoefte hoger: 5 à 6 g/kg/d (12% van de energietoevoer). Bij kwashiorkor (oedeem) dient de vochttoevoer de eerste dagen beperkt te blijven tot 100 à 150 ml/kg/d. Als het oedeem is uitgeplast (daling van het gewicht) kan de vochttoevoer verhoogd worden (150-200 ml/kg/d). Vanwege de geringe eetlust zal vaak gekozen worden voor een vloeibare voeding, die bij voorkeur in kleine porties over de dag én nacht verdeeld wordt. Soms is toediening per neussonde noodzakelijk. Meestal wordt het dieet samengesteld uit een mengsel van melk, suiker en plantaardige olie. Aan dit mengsel kan een zetmeelproduct worden toegevoegd. Extra zouttoediening wordt, gezien het verhoogde lichaamsnatrium, sterk ontraden. Recent zijn door de industrie energierijke voedingen ontwikkeld voor de rehabilitatie van zwaar ondervoede patiënten. Deze preparaten bevatten extra supplementen van de nodige micronutriënten.
Psychomotore retardatie
Een therapie die erop gericht is tijdens en vooral na de behandeling van de ondervoeding zo goed mogelijk de geestelijke ontwikkeling te stimuleren, zal de achterstand hierin geheel of nagenoeg geheel kunnen wegwerken. Het is van belang bij deze therapie ook de ouders te betrekken: moeders geloven maar al te vaak niet meer in de overlevingskansen van hun ernstig ondervoede kind. Het is noodzakelijk hen te helpen het zelfvertrouwen terug te vinden.
Preventie en voorlichting
De preventie van een recidief vormt één van de moeilijkste aspecten van een behandeling. Immers, de belangrijkste factor die hierbij een rol speelt is het sociaal-economisch milieu waarin het kind opgroeit. Dit is niet gemakkelijk te verbeteren. Wel zal men er zorg voor moeten dragen het kind zo goed mogelijk te immuniseren voordat het naar zijn eigen milieu terugkeert. Tijdens de opname zal veel aandacht besteed moeten worden aan een praktisch gerichte voorlichting aan de ouders. Hierbij moeten de volgende onderwerpen centraal staan:
aanbeveling van borstvoeding, die zolang mogelijk moet worden voortgezet;
bereiding van goedkope, niet te volumineuze, energierijke bijvoeding uit lokaal beschikbare producten;
preventie van infecties (hygiëne/immunisatie);
vroegtijdige behandeling van infectieziekten;
richtlijnen voor de behandeling van diarree/dehydratie, waarbij zo snel mogelijk energierijke voeding moet worden aangeboden;
onder ogen brengen van het belang van een regelmatige controle van zowel moeder als kind.
De aandacht die men bij die voorlichting aan deze verschillende onderwerpen besteedt - waarbij geboortebeperkende maatregelen zeker niet mogen worden vergeten - zal sterk afhangen van de sociale, maatschappelijke en religieuze structuur van het gezin van het kind. De voorlichting dient met deze factoren terdege rekening te houden.
Kernboodschappen (ii) met betrekking tot ernstige eiwit- en energieondervoeding (protein energy malnutrition; pem):
kwashiorkorbeelden hebben een hogere mortaliteit dan marasmus;
behandeling van ernstige ondervoeding is aanvankelijk klinisch;
rehabilitatie is bij voorkeur poliklinisch;
preventie vormt de enige oplossing.
Importziekten uit de Derde Wereld (infectieziekten, zie ook hoofdstuk 15)
In tabel 30-10 wordt een overzicht gegeven van het voorkomen van enkele virale, bacteriële en parasitaire infectieziekten uit die delen van de wereld van waaruit vele kinderen afkomstig zijn die nu in Nederland of België wonen. Bij kinderen die uit de tropen zijn teruggekeerd en vervolgens (acuut) ziek worden, zijn drie punten in de anamnese van belang:
de plaats van herkomst; een deel van de pathologie is namelijk geografisch bepaald;
de duur van het verblijf in de tropen;
het tijdstip van terugkeer in eigen land.
| Kinderen uit: | Middellandse-Zeegebied | Suriname, Antillen | (Zuidoost-)Azië | Afrika |
|---|---|---|---|---|
| virale infecties | ||||
| poliomyelitus | + | +? | ++ | ++ |
| mazelen | +? | +? | ++ | ++ |
| dengue | -? | + | ++ | + |
| gele koorts | - | -? | - | + |
| hepatitis Aen B | + | + | ++ | ++ |
| rabiës | +? | +? | + | + |
| aids | + | + | + | ++ |
| bacteriële infecties | ||||
| tuberculose | + | + | ++ | ++ |
| cholera | –? | – | + | + |
| salmonellose | + | + | + | ++ |
| shigellose | + | + | ++ | ++ |
| tetanus | + | +? | + | ++ |
| parasitaire infecties | ||||
| malaria | –? | +1 | + | ++ |
| leishmaniasis | + | +?2 | +? | ++ |
| amoebiasis | +? | +? | ++ | ++ |
| giardiasis | + | + | ++ | ++ |
| ascariasis | + | + | ++ | ++ |
| schistosomiasis | + | +3 | + | ++ |
– komt niet voor, – komt zelden voor, + komt soms voor, + komt voor, ++ komt vaak voor
1. Suriname, buiten de steden
2 Suriname
3 Suriname, alléén aan de kust: S. mansoni
Dit laatste moet gezien worden in relatie tot de incubatietijd van bepaalde infecties. De incubatietijd bedraagt bij virusinfecties (bijvoorbeeld dengue, andere arbovirussen, mazelen) en rickettsiosen (bijvoorbeeld fièvre boutonneuse en relapsing fever) in het algemeen minder dan twee weken, en bij buiktyfus maximaal vier weken. Malaria door Plasmodium falciparum treedt bij niet-immune personen vrijwel nooit later op dan zes maanden na het staken van de chemoprofylaxe. Echter, infectie door Plasmodium vivax en Plasmodium ovale kan nog na enkele jaren ziek-zijn met koorts veroorzaken (die door Plasmodium malariae zelfs nog na vele jaren!). Viscerale leishmaniasis, evenals een amoebenabces, geven meestal binnen enkele maanden klachten. Viscerale leishmaniasis kan zich echterook na vele jaren openbaren, evenals tuberculose, een amoebenabces en een gedissemineerde infectie door Strongyloides stercoralis.
Ook het opkomen van de klachten van de diverse ziektebeelden kan zeer wisselend zijn. Het acute fulminante beeld van een malaria-infectie steekt sterk af tegen het subacute/chronische of zelfs asymptomatische klachtenpatroon van de meeste overige parasitaire infecties. Bij de bespreking van de ziekteverschijnselen is met dit onderscheid rekening gehouden: de acute en de subacute/chronische klachten met de daarbij passende ziektebeelden worden apart besproken. Vervolgens worden diverse infectieziekten kort afzonderlijk belicht, al naar gelang de ziekte van parasitaire, virale of bacteriële oorsprong is.
Met betrekking tot de therapie, profylaxe en preventie worden de geldende principes besproken.
Informatie over importziekten, preventie en profylaxe is telefonisch en via het internet beschikbaar.
Ziekteverschijnselen
Acute klachten en symptomen
De klachten en symptomen van acuut verlopende tropische infectieziekten verschillen niet van die bij niet-tropische infectieziekten. Op de voorgrond staan koorts, diarree, algehele malaise, verminderde eetlust en exantheem (zie ook verder).
Koorts
Ook in de tropen wordt koorts meestal veroorzaakt door een relatief onschuldige virusinfectie, die zich vaak uit als een conjunctivitis met een loopneus, keelpijn, hoesten en weinig ziek-zijn. Soms zijn er ook klachten van de tractus digestivus. Toch is zowel in als na terugkeer uit de tropen koorts een verontrustende en potentieel spoedeisende klacht. Er is kans op allerlei exotische aandoeningen, waaronder malaria. Bij malaria is er een snel oplopende koorts (39-41 °C), vaak met koude rillingen en hevig zweten en hoofdpijn. Soms is er ook buikpijn en diarree. Een dergelijke aanval kan worden voorafgegaan door een prodromale fase met algehele malaise, hoofdpijn en vermoeidheid (griep). Bij de koorts kan hoesten en geelzucht optreden. Vaak is er een wisselende temperatuurverhoging. Wanneer koorts samen met lever- en miltvergroting voorkomt, moet gedacht worden aan leishmaniasis. Vooral bij kinderen met een marginale voedingstoestand is het klinische beeld van mazelen vaak fulminant en erg gecompliceerd. Veelvoorkomende virusinfecties, zoals die door het Ebstein-Barr-, dengue- en hepatitis- A-virus, kunnen in de tropen bij jonge kinderen mild verlopen. Evenwel, bij oudere kinderen en volwassenen kan bij dengue plotseling een ernstig beeld ontstaan met hoge koorts (tot 41 °C). Vaak is dit in combinatie met hevige hoofdpijn (achter de ogen), erge spier- en gewrichtspijn en roodheid van het gelaat, gezwollen oogleden, versterkte conjunctivale injectie (dengue facies) en een exantheem. Misselijkheid en braken kunnen optreden, de eetlust is slecht.
In een recent Engels onderzoek waren de belangrijkste oorzaken van koorts bij (volwassen) reizigers uit de tropen: malaria (30-40%), luchtweginfecties (3-11%), diarree/shigellose (5-7%), hepatitis (3-6%), urineweginfecties (3-4%), dengue (2-6%), buiktyfus (2%) en infectie door Ebstein-Barr-virus (1-2%).
Diarree (reizigersdiarree)
Diarree is het belangrijkste symptoom bij acute infecties van het maagdarmkanaal, gastro-enteritis en enterocolitis (zie ook hoofdstuk 19). Diarree kan vergezeld gaan van misselijkheid, braken en krampende buikpijn. Bij circa 10-15% van de gastro-intestinale infecties is er invasie van het darmslijmvlies (enterocolitis), met als gevolg bloederige ontlasting, meestal met slijmbijmenging. In de minder ontwikkelde landen is diarree een belangrijke doodsoorzaak bij jonge kinderen (figuur 30-1). De nietimmune reiziger die naar een ontwikkelingsland reist, is wat betreft zijn afweer te vergelijken met het autochtone jonge kind van dat land, immers: ‘travel broadens the mind and opens the bowels’. Bij 20-50% van niet-immune personen treedt tijdens een verblijf in de subtropen en tropen binnen de eerste twee weken na aankomst acute diarree op. Deze zogenoemde reizigersdiarree heeft sprekende namen als Delhi-belly, Maseru-tummy, Hongkong-dog of Tourista. Meestal duurt de diarree vrij kort, gemiddeld drie tot vijf dagen, en is het gekarakteriseerd door het optreden van frequente, waterdunne ontlasting, die tijdens een periode van vijf dagen gemiddeld twaalfmaal wordt geproduceerd. Vaak is er krampende buikpijn en misselijkheid en soms is er lichte koorts als bijkomende klacht. Rotavirus is wereldwijd de belangrijkste verwekker van diarree bij het jonge kind. Ook de andere virusinfecties, met name mazelen, kunnen gepaard gaan met diarree.
Van de bacteriële verwekkers van reizigersdiarree is enterotoxigene Escherichia coli (etec) wereldwijd de meest voorkomende oorzaak van waterige diarree. Een shigellose kan zich presenteren als een milde vorm, maar vaak ook als een fulminant beeld met hoge koorts en heftige diarree met bloed en slijm. Klassieke cholera (door Vibrio cholerae serotype O1, biotype El Tor of het serotype O139 (Bengal) gaat gepaard met levensbedreigend vochtverlies en het risico van hypovolemische shock, die binnen vier tot acht uur kan ontstaan. Percentueel gezien is cholera geen belangrijke verwekker van diarree (slechts bij 1% van alle reizigers naar Azië). Aeromonas hydrophila wordt vaak aangetroffen bij diarree in Zuidoost-Azië (Thailand). Parasitaire infectie zoals bij schistosomiasis kan in ernstige gevallen gepaard gaan met acute diarree, heftige krampen en ernstig ziek-zijn. Dit is met name het geval wanneer de parasieten in de intestinale venen huizen (zie verder). Onder alle leeftijdsgroepen kunnen bij invasie van het colonepitheel door de E. histolytica-trofozoïet (amoebencolitis) symptomen ontstaan die over één tot drie weken in ernst toenemen. Buikpijn en bloederige ontlasting staan op de voorgrond. Bij circa 33% van de gevallen is er koorts. Het fulminante beeld is zeldzaam. Infectie met de aan Cryptosporidium verwante kokkidieënsoort Cyclospora cayetanensis (cyanobacterium-like body; clb) werd aanvankelijk beschreven bij reizigersdiarree in Mexico, Haïti, Nepal en Indonesië, maar blijkt bijvoorbeeld ook in Turkije voor te komen. De klachten bij deze infectie duren meestal langer dan bij de meeste gevallen van diarree. Voor nadere details wordt verwezen naar de handboeken tropische geneeskunde en infectieziekten.
Diarree kan ook optreden na terugkomst in eigen land. Men vond bij kinderen die kort in de tropen verbleven verschillende incidenties van diarree in de leeftijdsgroepen van 0-2, 3-6, 7-14 en 15-20 jaar: respectievelijk 40, 8,5, 21 en 36%. Bij 0-2-jarigen was de diarree ernstiger en duurde langer (mediaan 17 dagen) vergeleken met de andere groepen: 3-5 dagen. Ook na een langer tropenverblijf is diarree een belangrijke klacht die bij 12% van de kinderen wordt gevonden.
Exantheem en andere huidverschijnselen
Huidverschijnselen treden op bij de meeste virale infecties, rickettsiosen en buiktyfus. Deze kunnen variëren van een wegdrukbaar fijn-grofvlekkig maculair-papuleus exantheem tot petechiën, purpura en huidbloedingen; deze laatste vaak als uiting van een hemorragische diathese of beschadiging van de wand van de kleine bloedvaten (zie Henoch-Schönlein) door bepaalde virusinfecties. Bij mazelen worden twee dagen voor het uitbreken van het exantheem op het wangslijmvlies kleine rode vlekjes met een witte rand gezien (vlekjes van Koplik), die circa vier dagen aanwezig blijven. Het exantheem kenmerkt zich door een erythemateus, maculopapulair beeld dat zich vanuit het gezicht over romp en extremiteiten verspreidt. Bij gepigmenteerde kinderen is het mazelenexantheem vaak beter te voelen dan te zien. Bij de milde vorm van dengue kan zich gedurende de eerste twee dagen een vluchtig, fijnvlekkig en wegdrukbaar exantheem openbaren. Na vijf tot zes dagen ontwikkelt zich een grover, wat verheven huiduitslag, die op de romp begint en zich verspreidt naar gezicht, armen en benen. De handpalmen en voetzolen blijven vrij. Bij de ernstige vorm worden verspreide bloedingen en hematomen gezien. In omstandigheden van gebrekkige hygiëne is scabiës een van de meest voorkomende oorzaken van, met name ‘s nachts, heftig jeukende huidafwijkingen vooral aan de polsen. De aandoening komt wereldwijd voor (zie hoofdstuk 29) en staat in de tropische kindergeneeskunde bovenaan bij de differentiële diagnose van jeukende huidafwijkingen, gevolgd door atopisch eczeem. Huidafwijkingen treden ook op bij een aantal in de tropen en subtropen voorkomende parasitaire infecties, zoals Leishmania. Hierbij wordt vaak een laesie op de wang aangetroffen, die uiteindelijk geneest als een gepigmenteerd atrofisch litteken. Bij sommige soorten leidt het tot een proliferatieve mucocutane afwijking van het gelaat en de mond. Afhankelijk van de geografie heeft het namen als Oriental-sore en Aleppobutton. Eén tot twee dagen na penetratie van de huid door de Schistosoma-parasiet kan een acute allergische dermatitis optreden, die na enkele dagen weer spontaan verdwijnt. Bij infectie met bepaalde Filaria-soorten (zie verder) komen forse vluchtige en van plaats wisselende urticariële zwellingen van de huid voor (Calabar-zwelling). Bij bepaalde worminfecties waar de mens de tussengastheer is (mijnwormen van dieren) en bij auto-infectie met Strongyloides stercoralis kunnen de larven guirlandeachtige urticariële huidafwijkingen veroorzaken (creeping eruption). Bij ascariasis kunnen allergische huid- en slijmvliesverschijnselen ontstaan zoals urticaria en angio-oedeem.
Belangrijkste verschijnselen en klachten van acute tropische ziekten zijn:
koorts;
algehele malaise;
huidafwijkingen;
diarree.
Subacute of chronische klachten en symptomen
Tijdens een tropenverblijf en na terugkeer kunnen subacute of chronische klachten en symptomen bestaan. Diarree met buikklachten staat vaak op de voorgrond, al dan niet samen met jeuk en huidverschijnselen. Ook worminfecties kunnen die klachten veroorzaken, maar vaak verlopen deze asymptomatisch. Een infectie met Entamoeba histolytica en Giardia (duodenalis, synoniem: intestinalis, lamblia) kan subacute of chronische (langer dan twee weken durende), intermitterende diarree en vage buikklachten veroorzaken. Bij giardiasis is er vaak een secundaire lactasedeficiëntie die een intolerantie voor zuivelproducten teweegbrengt (zie hoofdstuk 19). Andere oorzaken van langer aanhoudende vlokbeschadiging kunnen soortgelijke klachten geven. Te denken valt aan een acute gastro-enteritis, aan ondervoeding of aan een bacteriële overgroei van de dunne darm. Ook aids is tegenwoordig een belangrijke oorzaak van chronische diarree. Bij personen met afweerstoornissen is bij circa 20% van de gevallen Cryptosporidium parvum de belangrijkste verwekker van chronische diarree (zie ook hoofdstuk 19). Gedurende het invasiestadium kunnen larven van de rondworm (Ascaris lumbricoides) in de darm lokale ontstekingsverschijnselen geven met diarree en vage buikklachten. De lokalisatie van de echinococcuscyste en de mate van expansieve groei van deze cyste zullen bepalend zijn voor de klachten. Een cyste in de lever geeft bijvoorbeeld buikklachten, opgeblazen gevoel, misselijkheid en braken. Daarentegen zal een cyste in de hersenen het beeld geven passend bij een ruimte-innemend proces. Bij pijn rechtsboven in de buik, samen met koorts, moet met de mogelijkheid van een leverabces rekening worden gehouden (zie amoebiasis). De meest voorkomende mildere vorm van schistomiasis, door onder andere S. mansoni en S. japonicum, wordt gekenmerkt door krampende buikpijn en diarree (soms met bloed).
Ascarislarven kunnen bij het bereiken van de longen overgevoeligheidsreacties en bronchopulmonale klachten veroorzaken, gekenmerkt door hoesten, kortademigheid, pijn op de borst en piepen (Loeffler-syndroom). Bij buiktyfus wordt vaak in de tweede week op de onderzijde van borst en buik een betrekkelijk fijnvlekkige huiduitslag zichtbaar (roseola, roze spots). Zichtbare hematurie kan wijzen op schistosomiasis, vaak is de hematurie echter alleen microscopisch waar te nemen. Hematurie, dysurie of frequente mictie treedt in 50-70% van de gevallen van schistosomiasis op als gevolg van epitheliale ulceratie en blaaspoliepen.
Belangrijkste subacute en chronische klachten en verschijnselen van tropische ziekte zijn:
jeuk en huidverschijnselen;
buikklachten;
diarree;
koorts.
Diagnostische hulpmiddelen
Fecesonderzoek
Diarree met bloed en slijm, diarree die gepaard gaat met ernstig ziek-zijn of chronische diarree (duur > twee weken) zijn redenen voor microbiologische diagnostiek van de feces: bacteriële kweek en parasitologisch onderzoek. Bij afweerstoornissen is virologisch onderzoek zinvol. Voor het parasitologische onderzoek naar intestinale wormen en cysten zijn drie fecesmonsters vereist, die met een interval van ten minste 24 uur zijn afgenomen. Gezien de geringe uitscheiding biedt voor het aantonen van larven van Strongyloides stercoralis een feceskweek met incubatie bij kamertemperatuur meer zekerheid dan een direct preparaat. Bij S. mansoni zijn er meestal weinig eieren en kan een rectumbiopt of een rectumschraapsel meer duidelijkheid geven.
Bloed: dikkedruppelonderzoek, eosinofilie en serologie
Alleen met behulp van een dikkedruppelonderzoek of een bloeduitstrijk kan men de vier soorten malaria morfologisch van elkaar onderscheiden. Een gebruikelijke kleuring is die volgens Giemsa (zie diagnostiek malaria). Een dikkedruppelpreparaat kan, wanneer er microfilaria worden waargenomen, van groot belang zijn voor het bevestigen van de diagnose filariasis. Meestal is hiervoor een groter volume bloed nodig (5-10 ml, gehepariniseerd).
Eosinofilie wordt vaak gezien bij kinderen en volwassenen in en na terugkeer uit de tropen. Men spreekt van eosinofilie en hypereosinofilie bij een absoluut aantal eosinofielen van respectievelijk meer dan 0,3 × 109/l en meer dan 1,5 × 109/l. Eosinofiele granulocyten spelen een rol bij het opbouwen van immuniteit en het elimineren van worminfecties. Eosinofilie is een belangrijke aanwijzing voor de aanwezigheid van een parasitaire infectie, met name bij worminfecties met een weefselstadium in de levenscyclus. Echter, in meer dan 50% van de gevallen wordt geen oorzaak voor de eosinofilie gevonden. Bij sommige chronische worminfecties en bij immunosuppressie kan eosinofilie ontbreken. Eosinofilie en ijzergebreksanemie treden op bij een darminfectie door mijnwormen. Eosinofilie kan echter ook bij manifeste atopie optreden zonder dat er sprake is van een worminfectie. Hypereosinofilie wordt slechts bij een beperkt aantal worminfecties aangetroffen. Wel wordt het regelmatig gezien bij alle stadia van Toxacara, Trichinella spiralis en soms tijdens het invasiestadium van een infectie door Ascaris, Ancylostoma, Strongyloides en Schistosoma (Katayama-koorts; zie verder).
Bij de aanvraag voor serologie is het belangrijk informatie te verschaffen over het klinische beeld. Vooral bij invasieve parasitaire aandoeningen kunnen antilichamen worden aangetoond. In het algemeen pleit een seroconversie of een viervoudige stijging van de titer voor een recente infectie. Het eerste monster dient zo vroeg mogelijk in de ziekte te worden afgenomen en het tweede monster twee tot drie weken later. Voor serologisch onderzoek van virale infecties is het belangrijk de eerste ziektedag te vermelden (voor details wordt verwezen naar de afzonderlijke ziektebeelden).
Urine
Bij schistosomiasis van de urinewegen kunnen de eieren in een 24-uursportie worden aangetroffen.
Kernboodschappen over diagnostiek van importziekten in en na terugkeer uit de tropen:
bij elk geval van koorts tijdens een verblijf in, of na terugkeer uit, de tropen dient malaria te worden uitgesloten;
bij verdenking op malaria is een dikkedruppelpreparaat met spoed vereist;
eosinofilie wordt vaak gezien en kan veroorzaakt worden door een worminfectie;
sommige virale, bacteriële en parasitaire infecties kunnen door middel van serologisch onderzoek worden aangetoond;
voor parasitologisch fecesonderzoek zijn drie monsters, afgenomen met een tussentijd van 24 uur, noodzakelijk.
Parasitaire infectieziekten
Malaria
Casus
Een twaalfjarige jongen komt met zijn ouders uit Botswana (zuidelijk Afrika) op verlof naar Nederland. Hij gebruikt daar proguanil-hydrochloride (Paludrine®) als malariaprofylaxe (zie malariapreventie). Desondanks had hij drie weken geleden koorts. De dikkedruppeltest was destijds positief voor P. falciparum. Hij werd toen gedurende vier dagen behandeld met chloroquine (tabletten), maar dit verliep moeizaam door misselijkheid en braken. Toch was de koorts na twee dagen behandeling al verdwenen. Omdat hij echter twee dagen geleden (de dag voor vertrek!) weer koorts had gekregen, waren de ouders gisteren weer begonnen met een kuur chloroquine, maar hij werd weer misselijk. Hij wordt de dag na aankomst gezien.
Lichamelijk onderzoek: matig ziek, helder, niet nekstijf, temperatuur 39,8 °C, pols 110/min, rr 95/60 mmHg, goed doorbloede slijmvliezen, de milt is net te voelen. Verder geen abnormale bevindingen.
Beleid: er wordt met spoed een dikkedruppeltest voor malaria aangevraagd. Deze toont per gezichtsveld meerdere ringvormen van P. falciparum, waarmee de diagnose malaria tropica wordt bevestigd. Het overige laboratoriumonderzoek is als volgt: Hb 6,9 mmol/l, crp 22 mg/l, verder een normaal aantal leuko’s en geen afwijkingen van de differentiatie.
Hij wordt met spoed naar het ziekenhuis verwezen voor intraveneuze malariabehandeling met kinine.
Commentaar: terecht wordt op de eerste plaats aan malaria gedacht, ondanks de recente choroquinebehandeling en die van drie weken terug. Kennelijk had de laatstgenoemde kuur onvoldoende resultaat. Mogelijk kwam dit door onvoldoende opname van de ingenomen chloroquine (braken). Ook zou een (partiële) chloroquineresistentie een rol gespeeld kunnen hebben (lcr, 2002).
Epidemiologie
Bij de mens kunnen vier soorten malariaparasieten pathologie veroorzaken: Plasmodium falciparum, P. vivax, P. ovale en P. malariae. Alleen de door P. falciparum veroorzaakte malaria is levensgevaarlijk (malaria tropica) en is wereldwijd de belangrijkste parasitaire oorzaak van sterfte. Hiervan is de grootste sterfte op het platteland van tropisch Afrika, waar naar schatting meer dan 1 miljoen, voornamelijk kinderen, aan de gevolgen van malaria sterven. Infectie met P. falciparum kan leiden tot levensgevaarlijke hersenmalaria bij niet-immune personen. Hieronder vallen in endemische gebieden alle bezoekers, en jonge kinderen ouder dan zes maanden. Bij kinderen is ondanks ziekenhuisbehandeling de mortaliteit van hersenmalaria nog 15-30%. P. falciparum is ook overheersend in Oost-Azië,
Oceanië en het Amazonegebied. Tot na de Tweede Wereldoorlog kwamen infecties door P. vivax en P. malariae nog in grote delen van de wereld en zelfs in Nederland voor. Thans wordt ruim eenderde van de wereldbevolking (ruim twee miljard mensen) blootgesteld aan malaria, voornamelijk in Afrika, Azië en Latijns-Amerika. Wereldwijd zijn er ongeveer 300-500 miljoen gevallen van malaria per jaar. De incubatietijd is minimaal zeven dagen bij P. falciparum, en varieert bij P. malariae van 7-18 dagen maar kan ook 30-40 dagen duren. Bij P. ovale en P. vivax kan de incubatietijd langer worden onder invloed van (partiële) immuniteit, chemoprofylaxe of onvolledige behandeling. In de meeste gevallen van een P. falciparum-infectie treedt malaria binnen twee maanden na het staken van de chemoprofylaxe op of drie maanden na vertrek uit een endemisch gebied.
Pathofysiologie; klinische verschijnselen (zie ook figuur 30-8)
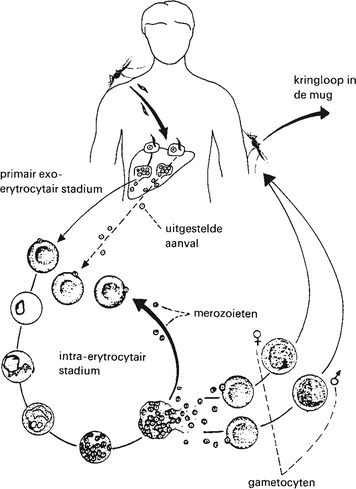
Malaria wordt veroorzaakt door Plasmodium-species die worden overgebracht door de beet van de geïnfecteerde vrouwelijke Anopheles-mug. Circa 70 soorten kunnen de ziekte overdragen.
Pathofysiologie. Door de beet van de mug bereiken de sporozoïten via de bloedbaan de lever, waar zij zich in de hepatocyt ontwikkelen tot leverschizont (exo-erytrocytaire cyclus). Na 1-2 weken komen uit de leverschizont de merozoïten vrij en begint de intra-erytrocytaire cyclus.
In de lever kunnen uit één parasiet 30.000 merozoïten ontstaan. Bij een infectie met P. ovale en P. vivax kunnen bovendien sporozoïten, in de vorm van hypnozoïten, nog jarenlang in de lever aanwezig blijven. Uit de leverschizont komen merozoïten vrij, die de erytrocyten binnendringen en zich vervolgens via karakteristieke ringvormen tot een amoeboïde vorm (trofozoïet) ontwikkelen. Door middel van celdeling ontstaat, afhankelijk van de soort, uiteindelijk een schizont met 6 tot 24 kernen. Uit de schizont komen weer merozoïten vrij die op hun beurt weer de erytrocyten binnendringen. Deze aseksuele intra-erytrocytaire voortplanting duurt 48 uur bij zowel P. falciparum, P. ovale als P. vivax en 72 uur bij P. malariae. De koorts die optreedt na het vrijkomen van de merozoïten zou kunnen samenhangen met het vrijkomen van pyrogenen uit de parasiet zelf of van endogene pyrogenen zoals interleukine-1 en de tumornecrosefactor (TNF). Seksuele voortplanting vindt plaats door het samenkomen van gameten die ontstaan zijn uit gametocyten, ook afkomstig van merozoïten. De gametocytenbevattende erytrocyten worden tijdens de bloedmaaltijd door de mug ingenomen. In de mug ontwikkelen zich vervolgens weer de sporozoïten en hiermee is de cyclus voltooid.
Anemie ontstaat door hemolyse, maar ook door beenmergdepressie. Er blijkt een duidelijke relatie te zijn tussen de mate van parasitemie en de ernst van de anemie, maar de mate van anemie kan niet geheel verklaard worden door het vernietigen van de erytrocyten. Bij chronische parasitemie speelt beenmergdepressie een belangrijkere rol dan bij een acute aanval. Splenomegalie wordt onder andere veroorzaakt door sekwestratie van erytrocyten. Trombocytopenie (grotendeels als uiting van hypersplenisme) treedt vaak op. Met name bij infectie door P. falciparum kunnen de volgende complicaties zich voordoen: cerebrale disfunctie (hersenmalaria, zie verder), hypoglykemie, lactaatacidose, nierinsufficiëntie (door acute tubulusnecrose, vooral bij volwassenen), longoedeem (ARDS; ten gevolge van een toegenomen capillaire permeabiliteit door complement-/cytokinegerelateerde mechanismen) en intestinale malabsorptie. De meest gangbare hypothese voor het ontstaan van hersenmalaria is de sekwestratie (het achterblijven) en ophoping van geïnfecteerde erytrocyten die vast gaan zitten aan de wand van de cerebrale venulen en capillairen (cyto-adherentie). Eenzelfde mechanisme kan zich ook in andere organen, zoals de darm, voltrekken en daar beschadiging van het slijmvlies geven, leidend tot intestinale malabsorptie en, in ernstige gevallen, tot ulceratie en bloedingen. Hypoglykemie wordt steeds vaker als complicatie herkend. Hiervoor worden de volgende mechanismen aangevoerd: een verhoogd glucoseverbruik door een versterkte anaërobe glycolyse in de weefsels (ook leidend tot lactaatacidose), afgenomen glycogeenreserves (met name bij zwangeren en kinderen), afgenomen gluconeogenese onder invloed van TNF
en andere cytokinen en ten slotte kan een versterkte insulineproductie door gebruik van de geneesmiddelen kinine en kinidine een rol spelen.
Klinische verschijnselen: er is een snel oplopende, met koude rillingen en hevig zweten gepaard gaande koorts tot 39-41 °C, hoofdpijn, soms buikpijn en diarree. Een dergelijke aanval kan worden voorafgegaan door een prodromale fase met algehele malaise, hoofdpijn en vermoeidheid (griep). Ziekteverschijnselen die zich als griep voordoen en langer dan twee dagen duren of in ernst toenemen kunnen door P. falciparum-infectie veroorzaakt worden. Het is belangrijk hiermee rekening te houden. Bij de koorts kan hoesten en geelzucht optreden, waardoor aan een andere oorzaak van een infectie (hepatitis) gedacht kan worden. De koorts is dagelijks, vaak is er een wisselende temperatuurverhoging. Er is geen huiduitslag. Hersenmalaria bij kinderen kenmerkt zich door stuipen en een verminderd bewustzijn. Onderscheid met goedaardige koortsstuipen kan moeilijk zijn. Bij twijfel over de oorzaak van de stuipen is in de tropen intraveneuze malariabehandeling aangewezen (zie verder). Klassieke symptomen van malaria kunnen ontbreken bij een malaria-aanval tijdens of kort na het staken van de chemoprofylaxe. Malaria door de drie andere soorten gaat ook met hoge koorts gepaard, maar de koorts treedt bij P. ovale of P. vivax niet dagelijks maar om de 48 uur op (malaria tertiana). Bij P. malariae is dit elke 72 uur (malaria quartana). Deze malaria is in het algemeen goedaardig.
Diagnostiek
Na terugkeer uit de tropen is bij verdenking op malaria snelle diagnostiek en verwijzing naar een ziekenhuis noodzakelijk. Ook in de tropen verdient het aanbeveling vóór het begin van de behandeling met spoed bloedonderzoek te verrichten. Alleen met behulp van dikkedruppelonderzoek of een bloeduitstrijk kan men de vier soorten malaria morfologisch van elkaar onderscheiden. Een gebruikelijke kleuring is die volgens Giemsa. Hierbij worden de kernen van alle stadia van de Plasmodiumsoorten roodgekleurd en het cytoplasma blauw. Bij aanwezigheid van parasieten wordt de parasietenindex bepaald. Dit is het percentage van erytrocyten dat geïnfecteerd is. Is de uitslag van het dikkedruppelonderzoek negatief en kan geen andere oorzaak voor de koorts gevonden worden, dan dient men deze elke 12-24 uur (twee tot drie keer) te herhalen, zo mogelijk met malariaserologie. Als de malariaserologie ook negatief uitvalt kan malaria uitgesloten worden.
Therapie
De toenemende resistentie van P. falciparum leidt tot minder differentiatie in het gebruik van geneesmiddelen. Voor de juiste keuze is daarom up-to-date informatie nodig (lcr en andere bronnen). Het op recept voorschrijven van een of meer geneesmiddelen voor de (nood)behandeling van malaria hoeft alleen te worden overwogen indien men langer dan één maand gaat verblijven in gebieden waar chloroquineresistentie heerst. Een veelbelovend en inmiddels ook in Nederland geregistreerd, anti-malariamiddel is artemisinine (artemether). Het is alleen in vaste combinatie met lumefantrine voor te schrijven. Artemisinine is afkomstig uit de plant Artemisia annua en werd als aftreksel in het oude China al tegen koortsende ziekten gebruikt. Het is zeer effectief tegen alle soorten (resistente) malaria. In de tropen is reeds bij verdenking op malaria behandeling vereist. Wanneer de patiënt uit een gebied komt waar malaria nog chloroquinegevoelig is, wordt in het algemeen een therapie aanbevolen van chloroquine (in België: eventueel gecombineerd met primaquine). Bij een chloroquineresistente malaria worden de volgende middelen aanbevolen: atovaquon en proguanil (Malarone®), echter niet bij kinderen met een gewicht minder dan 11 kg; kinine oraal of i.v., bij kinderen jonger dan acht jaar gecombineerd met clindamycine (oraal of i.v.), bij kinderen van acht jaar en ouder in combinatie met doxycycline, (oraal of i.v.). Als alternatief wordt in België mefloquine oraal aanbevolen. De keuze van de medicatie wordt mede bepaald door de leeftijd van het kind en de locatie waar het kind geïnfecteerd werd. Men doet er goed aan deskundigheid in te roepen alvorens met de behandeling te beginnen.
Profylaxe
Op de eerste plaats is dit gericht op het voorkómen van malaria tropica door P. falciparum. Doordat in steeds meer landen een resistentie wordt gevonden tegen de meest gebruikte profylaxemiddelen, is een absolute bescherming van deze middelen tegen malaria tropica niet te verwachten. Een infectie met P. malariae (malaria quartana) kan wel verhinderd worden. Anders ligt dit bij P. vivax en P. ovale (malaria tertiana). Bij deze twee soorten zullen parasieten als hypnozoïten in de lever kunnen overleven. Na het staken van de profylaxe kan nog na vier jaar een uitgestelde of hernieuwde aanval van malaria tertiana optreden.
De keuze van de profylaxe wordt bepaald door het resistentiepatroon (zie behandeling) van P. falciparum in het betrokken land (gebied). In Nederland is up-to-date informatie hierover beschikbaar bij het lcr. Voor België raadplege men het Instituut voor Tropische Geneeskunde in Antwerpen. De who geeft jaarlijks up-to-date informatie over malariaprofylaxe en behandeling, toegespitst op verschillende gebieden en landen (www.who.int/ith). De toenemende resistentie van P. falciparum heeft met betrekking tot de chemoprofylaxe geleid tot een indeling van de wereld in twee gebieden, één waarvoor proguanilhydrochloride, al of niet in combinatie met chloroquine, en één waarvoor mefloquine wordt geadviseerd.
Voor een verblijf van vier weken of minder wordt sinds kort de combinatie van atovaquon en proguanil (Malarone®) aanbevolen, echter niet bij kinderen < 11 kg (lcr, 2002).
Preventie
Chemoprofylaxe biedt geen 100% bescherming tegen malaria. Daarom zal duidelijk zijn dat bescherming tegen muggenbeten vanaf zonsondergang tot zonsopgang geboden is. Tijdens de nachtrust is het slapen in een muggenvrije kamer of onder een intact en goed sluitend, met permetrine geïmpregneerd, muskietennet belangrijk. Bedekkende kleding en het gebruik van insectenwerende middelen (diëthyltoluamide, deet) voorkomt muggenbeten.
Het ziet er niet naar uit dat binnen afzienbare tijd een effectief malariavaccin beschikbaar zal zijn. Tot dusverre zijn veldonderzoeken in onder andere Tanzania teleurstellend verlopen.
Kernboodschappen over malaria:
malaria komt wereldwijd in de tropen voor;
het is één van de belangrijkste oorzaken van ondervijfsterfte in Afrika ten zuiden van de Sahara;
bij ieder die tijdens of na een verblijf in de tropen koorts krijgt, moet met de mogelijkheid van malaria rekening worden gehouden;
bij verdenking op malaria wordt met spoed een dikkedruppelpreparaat verricht;
infectie door P. falciparum is levensgevaarlijk en wordt in principe klinisch behandeld;
chemoprofylaxe biedt geen volledige bescherming;
preventieve maatregelen zijn belangrijk;
er is nog geen vaccin beschikbaar.
Amoebiasis, intestinale vorm, leverabces
Epidemiologie
Infectie met Entamoeba histolytica vindt plaats via gecontamineerd water of voedsel en door fecaaloraal contact. Het is geassocieerd met intestinale en extra-intestinale ziekte. Circa 10% van de wereldbevolking is met deze darmprotozoa geïnfecteerd. Er zijn per jaar ongeveer 50 miljoen gevallen van invasieve amoebiasis en ongeveer 100.000 sterfgevallen. De infectie is endemisch in Afrika, Zuid-Amerika, Mexico en India, maar komt ook voor bij risicogroepen in de westerse wereld.
Pathofysiologie; klinische verschijnselen
Er zijn twee vormen, een actieve trofozoïet en een cyste.
Asymptomatische intestinale kolonisatie met cyste-uitscheiding komt het meeste voor. Deze nietinvasieve, zogenoemde luminale infectie kan gepaard gaan met buikpijn en een frequenter ontlastingpatroon. De klachten verdwijnen spontaan binnen acht tot twaalf maanden. Amoebencolitis ontstaat door invasie van het colonepitheel door de E. histolytica-trofozoïet. Alle leeftijdsgroepen kunnen getroffen worden. Symptomen ontstaan geleidelijk in de loop van één tot drie weken, er is buikpijn, bloederige ontlasting en pijn bij palpatie van het colon. Bij circa 33% van de gevallen is er koorts, en leververgroting kan optreden. Fulminante amoebencolitis is zeldzaam. Bij aanwezigheid van een afweerstoornis kan de aandoening levensgevaarlijk zijn, evenals bij corticosteroïdengebruik, jonge kinderen, zwangeren en ernstige ondervoeding.
Een leverabces is de meest voorkomende extra-intestinale manifestatie van een amoebeninfectie. Dit treedt meestal binnen twee tot zes maanden na een verblijf in een endemisch gebied op. De presentatie kan acuut verlopen met koorts, hevige pijn rechtsboven in de buik en snel optredend gewichtsverlies. Ook een minder heftig beloop is mogelijk, met vage buikklachten en geleidelijk gewichtsverlies. Diarree treedt bij 30-40% van de gevallen op.
Diagnostiek
Bij amoebendysenterie kunnen in het bloederige slijm van verse ontlasting binnen een uur na de productie erytrocyten-fagocyterende trofozoïeten worden aangetroffen. Vaak zijn er geen amoeben in de ontlasting aantoonbaar. Voor onderzoek naar cysten zijn drie monsters, verzameld met een tussentijd van 24 uur, vereist. Dit morfologisch onderzoek maakt echter geen onderscheid tussen cysten van de algemeen voorkomende E. dispar en de pathogene E. histolytica. Er kunnen specifieke antistoffen tegen E. histolytica in het serum worden aangetoond. Deze zijn met name bij invasieve amoebiasis verhoogd, maar minder vaak bij de luminale vorm. Indien het parasitologische onderzoek van de feces niets oplevert, kan sigmoïdo- of coloscopie meer duidelijkheid geven over de diagnose. Bij verdenking op een leverabces is zo mogelijk serologische diagnostiek en beeldvormend onderzoek (echo-, CT- of MRI-scan) van de bovenbuik aangewezen.
Therapie
Voor het bestrijden van een luminale infectie gebruikt men een contact-amoebicide. Een amoebencolitis wordt behandeld met een nitro-imidazol (metronidazol 50 mg/kg/24 uur in drie doses gedurende tien dagen), gevolgd door een kuur met een contact-amoebicide. Voor de behandeling van een amoebenabces is intraveneuze metronidazoltoediening aangewezen.
Preventie
Deze is gericht op verbetering van drinkwatervoorzieningen en persoonlijke hygiëne.
Kernboodschappen over amoebiasis:
amoebeninfectie kan buikpijnklachten en colitis (dysenterie) veroorzaken;
soms treedt systemische infectie en amoebenabces op;
een systemische infectie en amoebenabces wordt klinisch behandeld.
Viscerale leishmaniasis
Epidemiologie
Leishmaniasis is een zoönose. De parasieten komen wereldwijd voor en worden onderscheiden door hun geografische locatie. Van de circa 350 miljoen mensen die wonen in landen waar de vector aanwezig is, wordt het aantal gevallen van leishmaniasis op 12 miljoen geschat (3,5%). De presentatie is nogal variabel: de viscerale leishmaniasis is in landen rond de Middellandse Zee en in Brazilië overwegend een ziekte bij kinderen, terwijl in India juist volwassenen getroffen worden. Lymfekliervergroting treedt vaak op bij de Soedanese vorm van viscerale leishmaniasis. De incubatietijd van viscerale leishmaniasis is meestal weken tot maanden. De parasieten verblijven en vermenigvuldigen zich uitsluitend in de mononucleaire fagocyten.
Pathofysiologie; klinische verschijnselen
Bij de acute vorm is er koorts samen met lever- en miltvergroting. Onderscheid met malaria, buiktyfus, rickettsiosen, virale en bacteriële infecties, maar ook maligniteiten is noodzakelijk. De klassieke doch zeldzame vorm wordt gekenmerkt door forse hepatosplenomegalie en ondervoeding.
Diagnostiek
De diagnose wordt gesteld door aantonen van de parasieten in beenmerg- of miltpunctaat en/of het aantonen van antilichamen tegen deze protozoa. Opvallend zijn vaak de hoge bse, verhoogde crp, een normocytaire normochrome anemie, pancytopenie (met name neutropenie), hypergammaglobulinemie en matig verhoogde transaminasen.
Therapie
De behandeling berust nog steeds op de ruim 70 jaar geleden geïntroduceerde pentavalente antimoonverbindingen (20 mg/kg, gedurende 28 dagen). Klinische behandeling is noodzakelijk, gezien de vele bijwerkingen. Liposomaal amfotericine B is ook effectief gebleken.
Kernboodschappen over leishmaniasis:
leishmaniasis is een infectie van dieren (zoönose) en de mens;
er zijn verschillende klinische presentaties;
huidinfectie (cutane vorm);
systemische infectie: viscerale leishmaniasis;
protozoa vermenigvuldigen zich in monocytaire macrofagen;
koorts, lever- en miltvergroting maken verwarring met maligne aandoeningen mogelijk;
viscerale leishmaniasis wordt klinisch behandeld.
Giardiasis
Casus
Een bijna driejarige jongen, met zijn ouders uit Somalië gevlucht, bezoekt het spreekuur met de volgende klachten: sinds de dag van aankomst in Nederland (circa vier weken geleden) heeft hij vier- tot vijfmaal per dag dunnig-brijige ontlasting, zonder bloedbijmenging. Hij heeft weinig eetlust, klaagt over buikpijn en zou zijn afgevallen. Er bestaat geen koorts of andere klachten.
Lichamelijk onderzoek: gewicht < p3 en lengte < p10 (Nederlandse curve), tenger, niet echt ziek. BCG-litteken op linkerschouder, gering eczeem met krabeffecten aan de ellebogen (buigzijde) en in de knieholten, matig doorbloede slijmvliezen. Buik: wat bol, levendige peristaltiek, lever is 0,5 cm te voelen, milt niet. Verder geen bijzonderheden. Laboratoriumonderzoek: Hb 5,7 mmol/l, mcv 73 fl, leuko’s 7,4 × 109/l met in de differentiatie 8% eosinofielen, verder normaal. Urine: geen afwijkingen. Parasitologisch onderzoek van de feces wordt aangevraagd, hiervoor worden drie monsters met een interval van ten minste 24 uur verzameld en vervolgens ingestuurd. Dit onderzoek toont in alledrie de monsters Giardia-cysten en in één monster eieren van Ascaris lumbricoides. Therapie: de giardiasis wordt medicamenteus behandeld met tinidazol (voor dosering, zie onder), evenals de overige gezinsleden. Gezien het rode bloedbeeld is een ijzergebrek waarschijnlijk, men verwacht dat dit zal herstellen na de behandeling. De ascariasis wordt behandeld met mebendazol (zie onder), de andere gezinsleden worden meebehandeld. Commentaar: bij personen met een gezonde afweer en chronische diarree is alleen parasitologisch onderzoek van de feces aangewezen. Het is onbekend hoe de ijzergebreksanemie is ontstaan en wat de betekenis is van de eosinofilie. Een combinatie van een inadequate inname van ijzer samen met een geringe intestinale malabsorptie door de Giardia, zou een ijzergebrek hebben kunnen veroorzaakt. De eosinofilie kan samenhangen met de ascariasis, maar waarschijnlijker is een manifeste atopie (eczeem). De ascariasis zal in het algemeen geen chronische diarree veroorzaken. n.b. Als de diarree na behandeling nog aanhoudt, is herhaling van het parasitologisch onderzoek nodig. Levert dit niets op, dan moet aan het bestaan van lactose-intolerantie gedacht worden (zie hoofdstuk 19). Deze is dan waarschijnlijk secundair (als gevolg van giardiasis). Gezien de etnische herkomst zou zich ook reeds een primaire lactasedeficiëntie van het adulte type ontwikkeld kunnen hebben.
Epidemiologie
Giardiasis is wereldwijd de meest voorkomende parasitaire infectie en is evenals amoebiasis geassocieerd met een slechte kwaliteit van het drinkwater, gebrekkige hygiëne en grote bevolkingsdichtheid. Ook in de westerse wereld wordt deze parasiet, met name in besloten groepen zoals in kleuterdagverblijven of in de zwakzinnigenzorg, vaak aangetroffen. Giardiasis is een infectie van de dunne darm door de flagellaire protozoa Giardia duodenalis (synoniem: lamblia; intestinalis). De gastheer is de mens en andere zoogdieren, waaronder de hond en bever. In minder ontwikkelde landen kan de prevalentie oplopen tot 40%. Het voorkomen is soms leeftijdsgebonden. In Nigeria wordt de hoogste prevalentie (11%) van cyste-uitscheiders gevonden in de leeftijdsgroep van 2-3 jaar. In Lesotho is de prevalentie bij schoolkinderen wonend in de stad 19%.
Pathofysiologie; klinische verschijnselen
De Giardia-cysten zijn goed bestand tegen nadelige omgevingsfactoren (lange overlevingstijd). Besmetting vindt plaats, analoog aan amoebiasis, door gecontamineerd water, voedsel en direct fecaaloraal contact.
Excystatie tot trofozoïet vindt plaats onder invloed van het zure maagmilieu. De trofozoïeten bereiken het duodenum, waar zij zich verder ongeslachtelijk vermenigvuldigen. De incubatietijd is 12-19 dagen. Functionele en morfologische mucosabeschadiging treedt op door lokaal werkzame parasitaire factoren en door interactie met lokale en systemische factoren zoals de afweer van de gastheer. In het diermodel (door G. muris geïnfecteerde woestijnrat) blijkt de cyste-uitscheiding gastheeronafhankelijk te zijn en bepaald te worden door de genetische variabiliteit van de parasiet zelf.
Er is een grote verscheidenheid in presentatie. Van geïnfecteerde kinderen is 20-50% asymptomatische cyste-uitscheider. Subacuut en chronisch verlopende giardiasis komt meer voor dan de acute vorm die op een acute gastro-enteritis kan lijken. Bij de chronische vorm zijn er tussentijdse perioden met diarree, minder vaak is er een chronische diarree. De klachten duren zelden langer dan enkele jaren. Verschijnselen van lactose-intolerantie (zie ook hoofdstuk 19) kunnen enige weken tot maanden aanhouden ondanks effectieve antibiotische behandeling. In minder ontwikkelde landen kan giardiasis bij kinderen geassocieerd zijn met enige groeiachterstand.
Diagnostiek
Gezien het onregelmatige patroon van cyste-uitscheiding zijn voor het aantonen van cysten in de ontlasting drie fecesmonsters vereist, verzameld met een tussentijd van ten minste 24 uur. Trofozoïeten kunnen worden gevonden in vers opgevangen en vervolgens gefixeerde monsters.
Therapie
Tinidazol wordt gebruikt in een eenmalige dosering van 50 mg/kg of 2 g bij oudere kinderen. Als alternatief: metronidazol 15-20 mg/kg/24 uur in drie doses voor kinderen tot 10 jaar, 250 mg driemaal daags bij oudere kinderen, gedurende zeven dagen. Verschijnselen van lactose-intolerantie (zie ook hoofdstuk 19) kunnen enige weken tot maanden aanhouden, ondanks effectieve antibiotische behandeling. Voor therapeutische mogelijkheden zie de behandeling van diarree in 30.6.4).
Kernboodschappen over giardiasis:
giardiasis komt wereldwijd voor en is geassocieerd met een lage hygiënische standaard;
het is een belangrijke oorzaak van chronische (reizigers)diarree en van lactose-intolerantie;
giardiasis kan in tot 50% van de gevallen asymptomatisch verlopen;
behandeling is simpel en effectief;
preventie berust op goede hygiëne.
Ascariasis
Epidemiologie
De nematode (rondworm) Ascaris lumbricoides is een van de grootste en meest voorkomende intestinale parasieten bij de mens. Ascariasis komt wereldwijd voor en wordt vaker aangetroffen bij kinderen dan bij volwassenen. Circa een kwart van de wereldbevolking is met Ascaris geïnfecteerd. De infectie is geassocieerd met gebrekkige hygiëne, grote bevolkingsdichtheid en gebruik van humane ontlasting voor bemesting. Er is een lagere prevalentie in koude en droge gebieden, omdat de eieren het beste uitrijpen onder warme, vochtige omstandigheden. De infectie vindt meestal plaats door het nuttigen van rauw voedsel dat met eieren besmet is, of door contact met gecontamineerde aarde (jonge kinderen). De mens is de enige gastheer.
Pathofysiologie; klinische verschijnselen
Uit de ingeslikte eieren komen in de darm larven vrij die de darmwand kunnen penetreren en die vervolgens naar lever, hart en longen kunnen migreren (invasiestadium). In de capillairen van de long vindt rijping plaats die circa twee weken duurt. De uitgerijpte larven penetreren de alveolaire wand en migreren via de bronchiaalboom naar de bovenste luchtwegen. Bij het bereiken van de longen kunnen overgevoeligheidsreacties en bronchopulmonale klachten optreden, gekenmerkt door hoesten, kortademigheid, pijn op de borst en piepen (Loeffler-syndroom). Na ophoesten worden ze weer ingeslikt. In het jejunum en ileum groeien ze gedurende enkele maanden uit tot de volwassen rondworm. De gemiddelde worm is 10-30 cm lang en de volwassen vrouwtjes produceren gemiddeld 240.000 eieren per dag. Gedurende het invasiestadium kunnen larven in de darm lokale ontstekingsverschijnselen veroorzaken, met diarree en vage buikklachten. Allergische huidverschijnselen als urticaria en angiooedeem zijn mogelijk. De klachten van de chronische intestinale fase worden vooral bepaald door mechanische problemen, die samenhangen met het aantal aanwezige wormen (worm load).
Verreweg de meeste infecties verlopen asymptomatisch. Het is niet duidelijk welke rol een Ascaris-infectie speelt bij het ontstaan van ondervoeding. Complicaties treden zelden op (1 op 1000). Genoemd dienen te worden de acute klachten, die veroorzaakt kunnen worden door darmobstructie en door migratie van wormen in de galwegen.
Diagnostiek
Deze berust op het aantonen van de wormeieren in de feces (zie boven). In het invasiestadium kunnen larven in het sputum of bronchiale spoelsel worden gevonden. Er is dan meestal een eosinofilie, en op de X-thorax worden infiltratieve afwijkingen gevonden (pneumonitis). Bij allergische huid- en slijmvliesverschijnselen bestaat er ook een uitgesproken eosinofilie. Soms worden antilichamen gevormd.
Therapie
Mebendazol, 100 mg tweemaal daags gedurende drie dagen, geneest meer dan 90% van de infecties. Tijdens de behandeling kunnen soms wormen worden uitgebraakt; dit lijkt alarmerend, maar is niet gevaarlijk.
Kernboodschappen over ascariasis:
ascariasis is wereldwijd de meest voorkomende worminfectie;
meestal is er geen belangrijk ziek-zijn;
behandeling is simpel en effectief;
preventie berust op goede hygiëne.
Schistosomiasis
Epidemiologie
Schistosomiasis wordt veroorzaakt door een infectie met parasitaire trematoden (zuigwormen of botten; flukes), waarvan de volwassen vormen zich in de veneuze circulatie bevinden. Er zijn vijf soorten Schistosoma, die vrijwel alle infecties bij de mens veroorzaken. De soort infectie is afhankelijk van de geografische zone waar bepaalde zoetwaterslakken (vector) voorkomen. Voor het endemisch voorkomen van schistosomiasis zijn drie voorwaarden noodzakelijk:
een reservoir van geïnfecteerde individuen die de eieren met urine of feces uitscheiden;
de aanwezigheid van een geschikte slakkensoort als tussengastheer;
omstandigheden die blootstelling aan zoet oppervlaktewater mogelijk maken.
S. mansoni, S. japonicum en S. mekongi veroorzaken intestinale schistosomiasis, terwijl een infectie met S. haematobium en S. intercalatum leidt tot schistosomiasis van de urinewegen. Men schat het totale aantal geïnfecteerden in de wereld op circa 200 miljoen.
Pathofysiologie; klinische verschijnselen
De uit de slakken vrijgekomen en vrij rondzwemmende cercariae dringen door de menselijke huid en transformeren zich in de huid of de capillaire bloedvaten tot schistosomula. Een tot twee dagen na penetratie van de huid kan een acute allergische dermatitis optreden, die na enkele dagen weer spontaan verdwijnt. Na rijping migreren de schistosomula via de longen, lever en andere weefsels naar hun definitieve bestemming, de venen van het portale, peri-ureterale, peri-vesiculaire en peri-rectale gebied. Uit de schistosomula ontwikkelen zich mannelijke of vrouwelijke wormen, na paring in de veneuze plexus produceren de vrouwelijke wormen enkele honderden (S. haematobium, S. mansoni) tot enkele duizenden (S. japonicum) eieren die vanuit de veneuze plexus migreren. Circa de helft bereikt het lumen van blaas of darm, maar de overige raken gevangen in het naburige weefsel, waar zij lokale afweerreacties veroorzaken die leiden tot fibrose en collageenvorming. Tijdens de migratieperiode kan met name bij bezoekers aan een endemisch gebied een acuut ziek-zijn ontstaan, de zogenoemde Katayama-koorts. Deze gaat gepaard met een gegeneraliseerde lymfeklier-, lever- en miltvergroting en hypereosinofilie (zie elders). Antiparasitaire behandeling kan dit beeld verergeren, het leidt echter zelden tot mortaliteit.
Chronische schistosomiasis wordt bij 90% van de gevallen veroorzaakt door een reactie op de eieren die in de lichaamsweefsels zijn achtergebleven (granuloomvorming). De ernst van de ziekte wordt bepaald door de intensiteit van zowel de infectie (aantal wormeieren) als de afweer van de gastheer. De klinische symptomen, die met een chronische infectie samenhangen, kunnen pas na maanden tot jaren optreden en zijn mede afhankelijk van de soort Schistosoma. Infectie met S. haematobium kenmerkt zich in de vroegere stadia door een relatief hoge morbiditeit; 50-70% van de gevallen heeft hematurie, dysurie of frequente mictie ten gevolge van epitheliale ulceratie en blaaspoliepen. In de vergevorderde stadia is de morbiditeit gecorreleerd met de ernst van de afwijkingen. Ureter- en blaasfibrose kunnen calcificaties geven en leiden tot een hydro-ureter of een hydronefrose. In bepaalde gebieden is er een associatie met het ontstaan van blaascarcinoom. Infectie met S. mansoni, S. japonicum, S. mekongi en S. intercalatum, die in de intestinale venen huizen, kenmerkt zich door de volgende twee vormen: de meest voorkomende mildere vorm, met krampende buikpijn en diarree (soms met bloed) en de minder vaak voorkomende vorm met ernstig ziek-zijn, lever- en miltvergroting, portale hypertensie en slokdarmvarices. Omdat er een presinusoïdale leverfibrose is blijft de leverfunctie goed. Door migratie van eieren naar het centrale zenuwstelsel kunnen neurologische afwijkingen ontstaan met convulsies en een transverse myelitis.
Diagnostiek
De beste methode is het aantonen van eieren in urine of feces. Er zijn verschillende parasitologische technieken die de detectiegevoeligheid vergroten. Bij infecties met een lage wormlast en/of een lage ei-uitscheiding (S. mansoni) kan het nemen van een rectal snip de aanwezigheid van wormeieren in het weefsel alsnog bewijzen. Er is ook een soortspecifieke serologie voor schistosomiasis mogelijk. Schistosomiasis gaat gepaard met eosinifilie (zie elders) en een verhoogd IgE in het serum. Met behulp van echografie zijn vroege afwijkingen op te sporen. Eventuele calcificaties zijn op röntgenopnamen te zien.
Therapie
Effectieve behandeling is mogelijk met praziquantel (Biltricide®). Dit geneest 80-90% van alle infecties. De dosering is 40 mg/kg eenmalig voor een infectie met S. haematobium en S. intercalatum, of 60 mg/kg in twee à drie doses in 24 uur voor een infectie met S. mansoni, S. japonicum en S. mekongi.
Preventie
Dit is alleen mogelijk door in endemische gebieden elk contact met zoet oppervlaktewater te vermijden.
Kernboodschappen over schistosomiasis:
schistosomiasis wordt veroorzaakt door contact met besmet zoet oppervlaktewater;
infectie verloopt aanvankelijk meestal symptoomloos;
chronische problemen ontstaan door eieren in de weefsels;
infecties worden opgespoord door middel van laboratoriumonderzoek;
behandeling is altijd noodzakelijk;
preventie berust op het vermijden van geïnfecteerd zoet water.
Echinococcus-cyste (hydatidose)
Epidemiologie
Deze ziekte wordt veroorzaakt door het tussenstadium van de Echinococcus-cestoden (lintwormen), E. granulosis, E. multilocularis en E. vogeli. Net als bij alle andere lintwormen speelt zich de levenscyclus tussen een tussengastheer en een definitieve gastheer af. Hondachtigen zijn de definitieve gastheer en via hun excreta de belangrijkste vectoren. Contaminatie van de omgeving leidt tot consumptie van de wormeieren door omnivoren en herbivoren, zoals varkens, schapen, vee en de mens.
Echinococcus-cysteziekte door E. granulosus wordt gevonden in schapen-, geiten- en veehoudende agrarische gebieden zoals rond het Middellandse-Zeegebied, in het Midden-Oosten, de Hoorn van Afrika en in Uruguay. Infectie door E. multilocularis is endemisch in de arctische gebieden van Noord-Amerika en Eurazië. E. vogeli is endemisch in Zuid-Amerika.
Pathofysiologie; klinische verschijnselen
Na consumptie van met eieren besmet voedsel komen in de darm de larven vrij, die de darmwand penetreren en via het bloed en de lymfe zich verspreiden naar de lever, de longen of naar andere organen, waaronder het centrale zenuwstelsel en de nieren. Hier ontwikkelen zich de cysten die uitrijpen tot concentrische vormen (E. granulosis) of door uitgroei in naburige weefsels terechtkomen (E. multilocularis). Een hydatide cyste ontstaat doordat de groeiende cyste omringd wordt door fibreus weefsel (lokale afweerreactie). Binnen deze primaire uniloculaire cyste kunnen multipele dochtercysten ontstaan. Zeker op de kinderleeftijd verlopen de meeste infecties asymptomatisch, omdat het wel vijf tot twintig jaar kan duren voordat de cyste voldoende groot is om klachten te veroorzaken. Klachten en symptomen zijn afhankelijk van de plaats en de mate van expansieve groei van de cyste. Een hydatide cyste in de lever geeft bijvoorbeeld buikklachten, opgeblazen gevoel, misselijkheid, braken en drukpijn in de rechter bovenbuik. Een cyste in de hersenen gedraagt zich als een ruimte-innemend proces.
Diagnostiek
In 30% van de gevallen is er eosinofilie. Beeldvormend onderzoek levert, samen met serologisch onderzoek (elisa), meestal de diagnose.
Therapie
Stabiele, gecalcificeerde cysten behoeven geen behandeling. Symptomatische cysten worden het beste chirurgisch benaderd. In de gevallen waar dit niet mogelijk is biedt langdurige behandeling met een breedspectrumanthelminthicum verlichting van klachten. Gebruikt worden: mebendazol 40 mg/ kg/24 uur in drie doses, gedurende zes tot twaalf maanden, of albendazol 15 mg/kg/24 uur in twee doses, in twee kuren van ieder 28 dagen.
Kernboodschappen over echinococcose:
een echinococcus-cyste gedraagt zich als een ruimte-innemend proces;
beeldvorming leidt tot diagnose;
serologisch onderzoek ondersteunt dit;
behandeling bij voorkeur chirurgisch;
alternatief is langdurige anthelmintische behandeling.
Virale infectieziekten
Mazelen (zie ook exantheem en hoofdstuk 15)
Door een effectieve vaccinatie tegen mazelen komt deze ziekte in Nederland en België nog maar incidenteel voor. Meestal betreft het dan mazelen als importziekte bij vluchtelingen, asielzoekers of transcultureel geadopteerde kinderen. In minder ontwikkelde landen is mazelen nog steeds een belangrijke oorzaak van ziekte, ondervoeding en sterfte (figuur 30-1).
Epidemiologie
Mazelen wordt meestal overgebracht door direct contact met geïnfecteerde druppels, minder vaak door verspreiding via de lucht. In gematigde klimaten ligt de piek bij niet-gevaccineerden in de winter en de lente. In minder ontwikkelde landen treedt mazelen vooral op bij kinderen jonger dan twee jaar. In ontwikkelde landen was dit ook zo in de prevaccinatiefase. In grote gezinnen, waar de kinderen dicht op elkaar leven, brengen oudere kinderen (primaire) mazelen binnen het gezin waardoor zuigelingen en jongere kinderen (secundair) geïnfecteerd kunnen worden. Door het intensieve contact worden deze secundaire gevallen aan een grotere infectiedruk blootgesteld (zowel viraal als bacterieel) dan het primaire geval.
Pathofysiologie; klinische verschijnselen
Na een incubatietijd van tien tot twaalf dagen treedt de prodromale of catarrale fase op met koorts, conjunctivitis, een loopneus en hoesten. Twee dagen voordat de mazelen uitbreekt, ontstaat er een enantheem van het wangslijmvlies (vlekjes van Koplik), dat circa vier dagen aanwezig blijft. Op de vierde dag van de koorts treedt de uitslag op. Deze wordt gekenmerkt door een erythemateus maculopapulair exantheem, dat zich vanuit het gezicht verspreidt naar romp en armen en na twee dagen ook de benen bereikt. Bij donker gepigmenteerde kinderen is het vaak beter te voelen dan te zien: de huid voelt fluweelachtig-verheven aan. Op de tweede of derde dag begint het exantheem te vervagen, in volgorde van verschijning. De koorts daalt en de herstelfase begint. Aanhoudende koorts rechtvaardigt verdenking op een complicatie.
Complicaties
De belangrijkste complicatie die bijdraagt tot een hoge sterfte is de pneumonie. Het mazelenvirus zelf, maar ook andere virussen zoals het adeno- en het herpesvirus kunnen dit veroorzaken. Vaker is er echter een secundaire bacteriële infectie door S. pneumoniae of S. aureus. Laryngotracheobronchitis treedt vaak ten tijde van de huiduitslag op, maar kan soms na het verdwijnen van het exantheem ernstige vormen aannemen met een inspiratoire stridor en intrekkingen. Diarree treedt vaak op; dit wordt meestal door het mazelenvirus zelf veroorzaakt. Anorexie, malabsorptie en een ‘protein losing’-enteropathie kan leiden tot een negatieve energie- en stikstofbalans, waardoor het kind een van de ondervoedingsbeelden kan gaan vertonen (zie elders). Otitis media, corneabeschadiging, gingivostomatitis (herpes) komen vaak voor, terwijl in 0,1% van de gevallen een encefalitis kan optreden. Tijdens en na mazelen is de cellulaire afweer gedurende twee tot zes weken duidelijk afgenomen, hetgeen onder andere blijkt uit het negatief worden van een eerder positieve tuberculinetest. Er zijn aanwijzingen dat mazelen nog zes maanden na de infectie een toename van de morbiditeit en mortaliteit kan veroorzaken. Na mazelen kan tuberculose weer opflikkeren. In ziekenhuizen kan de mortaliteit oplopen tot 15-25%, bij ondervoede kinderen is de sterftekans groter, met name wanneer er ook een vitamine-A-deficiëntie aanwezig is. Bij een marginale vitamine-A-status kan een mazeleninfectie het klinische beeld van een vitamine-A-tekort (figuur 30-9) uitlokken, doordat de massale regeneratie van epitheel de vitamine-A-behoefte doet toenemen. Chronische diarree na mazelen draagt weer bij tot het ontstaan van ondervoeding.
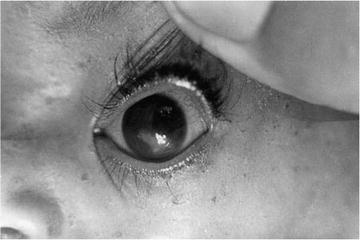
Diagnostiek
Zie hoofdstuk 15.
Therapie
Deze is in principe ondersteunend en symptomatisch met behulp van analgetica (paracetamol) en anti-hoestmiddelen. Door de who wordt voor de behandeling van complicerende bacteriële infecties cotrimoxazol als eerste keuze geadviseerd, en bij ernstig ziek-zijn een combinatie van amoxycilline en een aminoglycoside, indien deze voorhanden zijn. Op basis van de bevindingen van klinische trials adviseert men voor alle gevallen van mazelen (orale) vitamine-A-toediening, respectievelijk 100.000 à 200.000 E per dag gedurende twee dagen voor kinderen jonger en respectievelijk ouder dan een jaar.
Preventie
In minder ontwikkelde landen wordt vaccinatie met het Edmonston-Zagreb-vaccin toegepast op de leeftijd van negen maanden, in sommige Afrikaanse landen zelfs op de leeftijd van zes maanden. In Nederland en België is mazelen onderdeel van het gecombineerde bmr-vaccin.
Kernboodschappen over mazelen:
mazelen is nog steeds een belangrijke oorzaak van ziekte en sterfte in de Derde wereld;
het is een gegeneraliseerde infectie van huid- en slijmvliezen;
met name luchtwegen en maagdarmkanaal zijn aangedaan;
vaak zijn er secundaire bacteriële infecties;
mazelen gaat gepaard met verhoogde vitamine-A-behoefte;
dit lokt een vitamine-A-tekort uit;
vitamine-A-toediening vermindert kans op ernstige ziekte en sterfte;
vaccinatie beschermt tegen infectie.
Dengue
Epidemiologie
Dengue is een belangrijke oorzaak van koorts bij reizigers (zie koorts).
Denguekoorts is in principe een goedaardige aandoening, die veroorzaakt wordt door insecten overgebrachte (arthropod-borne; arbo) virussen, waarvan men vier serotypen kent. Dengue wordt verspreid door de overdag stekende Aedes aegypti-mug. Recent is ook Aedes albopictus, die ook in een gematigd klimaat voorkomt, als vector geïdentificeerd. Dengue komt thans vrijwel overal in de tropen voor, met name in verstedelijkte gebieden.
Men schat dat wereldwijd circa twee miljard mensen aan dengue zijn blootgesteld, waarvan er jaarlijks 10-40 miljoen voor het eerst geïnfecteerd worden. In Zuidoost-Azië traden in de afgelopen twintig jaar epidemieën van dengue haemorrhagic fever (dhf) op, welke meestal veroorzaakt werden door serotype 2. dhf en het dengue shock syndrome (dss) treden uitsluitend op bij herhaalde infectie en kunnen fataal verlopen bij circa 2% van de herinfecties. dhf en dss komen het vaakst voor bij kinderen van 4-9 jaar.
Pathofysiologie; klinische verschijnselen
Bij jonge kinderen verloopt dengue mild en is als zodanig niet te onderscheiden van andere virale luchtweginfecties. Er is koorts, rhinitis, pharyngitis, hoesten en soms zijn er ook gastro-intestinale klachten. Bij oudere kinderen en volwassenen is er een karakteristiek beeld. Na een incubatieperiode van twee tot zeven dagen ontstaat plotseling hoge koorts (tot 41 °C), met achter de ogen gelokaliseerde hoofdpijn en erge spier- en gewrichtspijn. Vaak is er roodheid van het gelaat, gezwollen oogleden en versterkte conjunctivale injectie (dengue facies). Tijdens de eerste twee dagen kan zich een vluchtige, fijnvlekkige en wegdrukbare, huiduitslag openbaren. Misselijkheid en braken kunnen optreden, de eetlust is slecht. Na vijf tot zes dagen daalt de temperatuur tijdelijk. Vervolgens ontwikkelt zich een wat verheven en grovere (tweede) huiduitslag, die op de romp begint en zich verspreidt naar gezicht, armen en benen. De handpalmen en voetzolen blijven vrij. Tegelijkertijd ontstaat weer matige koorts die binnen enkele dagen zakt. De huiduitslag verbleekt en verdwijnt binnen vijf dagen en wordt soms gevolgd door vervellingen. DHF en dss beginnen als gewone dengue, maar na twee tot vijf dagen gaat de algemene toestand snel achteruit, met een tekortschietende circulatie. Het kind is rusteloos, heeft koude extremiteiten, verspreide petechiën, subconjunctivale bloedingen, blauwe plekken en bloedt na uit de prikplaatsen. Ten gevolge van bloedindikking is er een verhoogde hematocriet, daarnaast is er trombocytopenie en een hypo-albuminemie. Tractus-digestivusbloedingen kunnen, samen met een verhoogde capillaire doorlaatbaarheid, irreversibele shock veroorzaken. Bij dhf en dss is de tourniquet-test positief. De who heeft de volgende criteria opgesteld voor de diagnose dhf: hoge, continue koorts gedurende twee tot zeven dagen; hemorragische diathese; hepatomegalie en shock, tezamen met twee afwijkende laboratoriumbepalingen (zie diagnostiek).
Diagnostiek
Een gelijktijdige afname van het aantal trombocyten (< 100 × 109/l) en een stijging van de hematocriet (> 20%), ten gevolge van stollingsstoornissen en lekkage van plasma, is pathognomisch voor dhf (who). Serologische diagnostiek is beschikbaar (elisa, IgM en IgG). Vroeg tijdens de koorts is ook virusisolatie mogelijk.
Therapie
Deze is slechts symptomatisch en ondersteunend: analgetica, ruim vocht toedienen en licht verteerbaar voedsel. Na de ziekte volgt volledig herstel. Bij dhf is ondersteunende behandeling en correctie van eventuele zuur-base- en elektrolytenstoornissen aangewezen. Bij dss is behandeling met plasma of vervangende middelen nodig, bij het optreden van ernstige bloedingen bloedtransfusies.
Preventie
Deze berust op het inperken van de vector, met name de Aedes aegypti, die zijn voorkeursbroedplaats in stilstaand water in en bij menselijke bewoning heeft (bijvoorbeeld in waterkruiken, bloemvazen, maar ook gebruikte autobanden). Het elimineren van broedplaatsen is een effectieve manier om transmissie van dengue te doorbreken. Thans wordt een gemodificeerd levend tetravalent denguevaccin bij kinderen beproefd.
Kernboodschappen over dengue:
dengue wordt door overdag stekende muggen overgebracht;
infectie veroorzaakt bij jonge kinderen milde klachten;
bij oudere kinderen en volwassenen staan hoge koorts, hoofd-, spier- en gewrichtspijnen op de voorgrond;
bij herhaalde infectie is er kans op het ontstaan van levensgevaarlijke dengue hemorrhagic fever (dhf) en het dengue shock syndrome (dss);
er is nog geen vaccinatie beschikbaar.
Bacteriële infecties
Shigellose
Epidemiologie
Shigellose wordt veroorzaakt door één van de verschillende Shigella-soorten, die behoren tot de familie van de Enterobacteriaceae. De presentatie kan variëren van milde waterige diarree tot fulminante dysenterie. Mensen en bepaalde mensapen zijn de enige gastheer voor Shigella. De verspreiding is vrijwel uitsluitend via fecaal-oraal contact en de ziekte is met name geassocieerd met gebrekkige hygiëne, slechte kwaliteit van het drinkwater, ondervoeding en grote bevolkingsdichtheid. De overdracht van Shigella verloopt gemakkelijk, doordat slechts een klein inoculum nodig is (102 tot 103 micro-organismen) om ziek te worden. S. dysenteriae is geassocieerd met epidemisch optredende dysenterie en heeft een sterfte van circa 5%. In sommige landen, zoals Bangladesh, is het micro-organisme endemisch geworden en werd daar de belangrijkste doodsoorzaak bij kinderen met diarree. S. flexneri komt endemisch meer voor in minder ontwikkelde landen, terwijl S. sonnei de meeste infecties in ontwikkelde landen veroorzaakt. S. boydii komt hoofdzakelijk in Zuid-Azië (bijvoorbeeld India) voor en geeft evenals S. sonnei meestal een waterige diarree.
Klinische presentatie
Er is een breed spectrum van klachten, variërend van milde tot ernstige waterige diarree, soms met strepen bloed, dan wel het klassieke dysenteriebeeld. Beginsymptomen zijn koorts, lusteloosheid en anorexie, die na 24-48 uur gevolgd wordt door het dysenteriesyndroom. Er is buikpijn en tenesmus (pijnlijke krampen optredend voorafgaand en tijdens de defecatie). De tenesmus is het gevolg van een proctitis. Vaak worden kleine hoeveelheden ontlasting geloosd, die hoofdzakelijk uit bloed en slijm bestaan. Tenesmus en veelvuldig persen kunnen leiden tot een rectumprolaps. De colitis kan heftig verlopen, aanleiding geven tot een protein-losing enteropathy en gecompliceerd worden door een toxisch megacolon en perforatie (als gevolg van een voortschrijden van de ontsteking in de gehele wand). Bij jonge kinderen kan door de hoge koorts, soms voordat er diarree optreedt, een convulsie optreden. Systemische complicaties treden vooral op bij S. dysenteriae, de meest levensbedreigende is het hemolytisch-uremisch syndroom (hus) (zie hoofdstuk 18).
Diagnostiek
Bewijzend is een positieve feceskweek. Indien kweken niet mogelijk is, zal men bij ernstig ziek-zijn af moeten gaan op het klinische beeld en de lokale epidemiologische situatie. Ter onderscheiding van amoebendysenterie: deze laatste veroorzaakt minder vaak koorts en treedt vaker bij volwassenen op. Bij bacteriële dysenterie bevat het bloederige slijm veel leukocyten, bij amoebendysenterie nauwelijks.
Therapie
Omdat bij een shigellose vooral bij jonge kinderen vaak een bacteriëmie ontstaat, is tijdige behandeling met de juiste antibiotica essentieel. Hiervoor kan men niet de kweekuitslag afwachten. De keuze hangt af van de epidemiologische achtergrond van de infectie. Is de infectie opgelopen in minder ontwikkelde landen dan is er grote kans op resistentie voor co-trimoxazol en ampicilline. Een fluorchinolonpreparaat is dan de eerste keus, ook bij kinderen (Dupont en Steffen, 2001).
Preventie
Omdat shigellose typisch een fecaal-orale infectie is, is de voornaamste preventie gericht op verbetering van de persoonlijke hygiëne. Er zijn orale vaccins in ontwikkeling, onder andere door gebruikmaking van recombinanttechnologie.
Kernboodschappen over shigellose:
shigellose is een infectie van het maagdarmkanaal;
wordt gekenmerkt door koorts en diarree met bloed en slijm (dysenterie);
leidt bij het jonge kind tot ernstig ziek-zijn;
wordt bij voorkeur klinisch behandeld met antibiotica;
er is nog geen vaccin beschikbaar;
preventie berust op goede hygiëne.
Buiktyfus
Casus
Een zesjarig meisje komt terug van een vijf weken durend verblijf bij haar vader in Vietnam (Can Tho, Mekong-delta). Circa een week na terugkomst in Nederland kreeg ze koorts en klaagde over hoofdpijn. De dienstdoende huisarts constateerde toen griep, nadat malaria met behulp van twee negatieve dikkedruppelpreparaten was uitgesloten. Zij bleef echter ziek, de koorts bleef onveranderd hoog (39,5-40 °C), ze kreeg vage buikpijn en had de laatste drie dagen geen ontlasting meer gehad. Zij wordt tien dagen na het begin van de klachten weer gezien.
Lichamelijk onderzoek: behoorlijk ziek, wel helder, niet nekstijf, temperatuur 39,9 °C, pols 70/min. bloeddruk 95/60 mmHg. Huid: gering fijnvlekkig exantheem op de romp, goed doorbloede slijmvliezen. De buik is wat gevoelig, geen tekenen van peritoneale prikkeling. De lever wordt even gevoeld, de milt circa 2 cm beneden de ribbenboog. Verder vallen geen bijzonderheden op.
Laboratoriumonderzoek: crp 110 mg/l, Hb 7,2 mmol/l, leuko’s 3,1 × 109/l, differentiatie nog niet bekend, urine: ketonen, verder geen afwijkingen. Dikkedruppeltest (spoed!): negatief. Beleid: gezien de anamnese (tropenverblijf, voortdurende koorts, vage buikklachten), relatieve bradycardie en palpabele milt, wordt de (waarschijnlijkheids)diagnose buiktyfus gesteld. Ze wordt voor aanvullende diagnostiek en behandeling (zie boven) verwezen naar het ziekenhuis.
Commentaar: bij elk geval van koorts uit de tropen dient met spoed malaria uitgesloten te worden. In de Mekong-delta komt malaria alleen bij de grens met Cambodja voor (lcr, 2001), malaria was toen de dienstdoende huisarts haar zag dus niet zo waarschijnlijk. Als dit malaria tropica was dan zou ze inmiddels, na tien dagen zonder adequate behandeling, levensgevaarlijk ziek zijn. Dengue zou aanvankelijk tot de mogelijkheden hebben gehoord (griep), maar de koorts duurde te lang. Ook aan een rickettsiose zal men moeten denken. Het beloop van de klachten en de bevindingen bij lichamelijk onderzoek (relatieve bradycardie, exantheem) passen het meest bij buiktyfus. De leukopenie met de sterk verhoogde crp (die past bij een bacteriële infectie) maakt buiktyfus nóg meer waarschijnlijk. Uit de bloedkweek werd een S. typhi gekweekt.
Epidemiologie
Buiktyfus (typhoïd fever, enteric fever) is in minder ontwikkelde landen een algemeen voorkomende ziekte die wordt veroorzaakt door een infectie met Salmonella typhi. Er is geen dierreservoir voor S. typhi en de ziektekiem wordt verspreid via gecontamineerd water en voedsel. De voornaamste infectiebronnen vormen de dragers en de symptomatische gevallen. S. typhi is goed bestand tegen diverse omgevingsfactoren. Ook andere soorten salmonella’s kunnen op buiktyfus lijken, maar verlopen minder ernstig (paratyfus).
Klinische presentatie
Na een incubatietijd van 8-28 dagen begint de ziekte als een griep met hoofd- en keelpijn. Binnen een week stijgt de koorts geleidelijk tot een continu hoge waarde. Hoesten komt vaak voor, een bloedneus incidenteel. Circa de helft van de kinderen heeft de eerste week diarree. Een betrekkelijk langzame pols bij hoge koorts rechtvaardigt verdenking op buiktyfus. Na de eerste week neemt het ziek-zijn toe en wordt het kind suffer en verward. Buikpijnklachten treden in de tweede week op en gaan vaak vergezeld van obstipatie. De buik is wat opgezet en vaak is er splenomegalie. Op de onderzijde van borst en buik wordt een betrekkelijk fijnvlekkige huiduitslag zichtbaar (roseola, roze spots). Bij een ernstige buiktyfus kan een levensbedreigende darmbloeding of zelfs een darmperforatie optreden.
Diagnostiek
Bij verdenking op buiktyfus is verwijzing naar een ziekenhuis noodzakelijk. Door middel van feces- en bloedkweken kan de S. typhi worden aangetoond en kan de gevoeligheid voor antibiotica bepaald worden.
Therapie
Voor asymptomatische dragers en bij een licht verlopend ziektebeeld wordt het gebruik van antibiotica ontraden (verlenging van de draagtijd). Bij ernstige symptomatologie is de therapie hetzelfde als die van een ernstig verlopende salmonellose (Dupont en Steffen, 2001). Ook bij kinderen heeft een van de fluorchinolonen de voorkeur, ondanks de (theoretische?) kans op kraakbeenbeschadiging.
Preventie
Er is een oraal en een parenteraal vaccin beschikbaar, dat evenwel geen volledige bescherming biedt.
Kernboodschappen over buiktyfus:
buiktyfus wordt veroorzaakt door Salmonella typhi;
sommige salmonellosen geven soortgelijk ziek-zijn (parafytus);
wordt bij voorkeur klinisch behandeld met antibiotica;
vaccinatie biedt beperkte bescherming;
preventie berust op goede hygiëne.
Diarree
Therapie
Bij volwassenen en de meeste kinderen verloopt in ongeveer 70% van de gevallen de diarree mild en behoeft, behalve ruime vochttoediening en een licht verteerbaar dieet, geen speciale behandeling. Bij frequente waterdunne ontlasting is het gebruik van ors nodig (zie elders). Bij sommige gevallen van cholera is intraveneuze vochttoediening aangewezen. Anti-diarreemiddelen zoals loperamide kunnen bij waterige diarree symptomatisch verlichting brengen, maar zijn gecontraïndiceerd bij kinderen jonger dan twee jaar (wegens kans op ileus) en bij verdenking op invasieve gastro-enteritis (diarree met bloed en slijm, al dan niet met koorts). Antibiotica worden, naast het gebruik van ors en een licht verteerbaar dieet, alleen aangeraden bij heftige of bloederige diarree en bij tekenen van algemeen ziek-zijn (onder andere hoge koorts). Als ‘blinde’ behandeling nodig mocht zijn, dan heeft bij verdenking op een bacteriële verwekker bij volwassenen een fluorchinolon de voorkeur, aangezien er slechts sporadisch resistentie tegen dit middel wordt gezien. Gebruikt wordt cipro- of norfloxacine in een dosering van respectievelijk 500 en 400 mg, tweemaal daags gedurende vijf dagen. Bij kinderen worden fluorchinolonen over het algemeen nog afgeraden gezien de (theoretische) kans op kraakbeenbeschadiging en alleen gebruikt bij ernstige infecties (zie ook shigellose en buiktyfus). Co-trimoxazol® wordt in andere gevallen aanbevolen. Co-trimoxazol® is ook effectief bij een infectie door Cyclospora. Tetracyclinen zijn effectief tegen infecties door Vibrio-soorten, maar zijn gecontraïndiceerd onder de leeftijd van acht jaar (wegens schadelijke werking op bot- en tandweefsel). Bij aanwijzingen voor een lactasedeficiëntie (leidend tot lactose-intolerantie, zie eerder en hoofdstuk 15) kan de lactose-inname beperkt worden met microbiologisch vervaardigd lactase (Kerulac®, Kerutabs®). Het eerstgenoemde medicament wordt als druppels toegevoegd aan niet-zure melkproducten en hiermee gedurende 24 uur geïncubeerd. Door deze behandeling daalt het lactosegehalte met 85-95%.
Preventie
Bij de preventie van reizigersdiarree is goede hygiëne van groot belang, maar praktisch vaak moeilijk uitvoerbaar. Slechts een klein percentage (10%) van de volwassen reizigers blijkt in staat alle noodzakelijke hygiënische voorzorgsmaatregelen te nemen. De volledig borstgevoede zuigeling heeft ook onder minder hygiënische omstandigheden weinig kans op diarree. Net zoals bij de jonge kinderen in de Derde Wereld neemt de kans op een maag-darminfectie sterk toe bij de introductie van een voedingssupplement. Wat betreft het effect van preventieve maatregelen zijn er geen gegevens beschikbaar over kinderen. Voor het nuttigen van voedsel geldt dat rauwe, ongekookte voedingsmiddelen moeten worden vermeden. In plaats van het lokale drinkwater gebruikt men mineraalwater (met intacte dop!) of gekookt dan wel gefiltreerd water. Een stelregel luidt: ‘cook it, boil it, peel it or forget it.’ Recente bevindingen in enkele geïndustrialiseerde landen (onder andere de Verenigde Staten), tonen een associatie tussen rotavirusvaccinatie en het optreden van invaginatie. Daarom wordt rotavirusvaccinatie niet meer toegepast. Dit is met name ook voor de Derde Wereld teleurstellend. Antibioticaprofylaxe ter voorkoming van reizigersdiarree is alleen aangewezen voor die kinderen bij wie zelfs milde diarree ernstige consequenties kan hebben.
Kernboodschappen over diarree:
acute diarree heeft in de meeste gevallen geen speciale behandeling nodig;
ruime vochtinname om dehydratie te voorkomen is belangrijk;
borstvoeding wordt altijd voortgezet;
flesvoeding wordt voortgezet;
lichte, gemakkelijk verteerbare voeding wordt aanbevolen;
bij uitdroging is het gebruik van ors nodig;
antibiotica zijn slechts aangewezen bij ernstig ziek-zijn en bij diarree met bloed en slijm (invasieve infectie);
bij de zuigeling tot de leeftijd van zes maanden is het uitsluitend geven van borstvoeding een effectieve vorm van preventie;
preventie berust op goede hygiëne;
preventie is lang niet altijd succesvol.


