Samenvatting
Om ziekteprocessen die zich afspelen in de longen, luchtwegen en longvliezen (pleurae) te kunnen begrijpen en de gevolgen ervan voor het functioneren van het lichaam te kunnen inschatten, is kennis nodig van de normale anatomie van de thoraxinhoud en de fysiologie van het functioneren van de long. Deze is te vinden in het boek Fysiologie en Anatomie uit de serie Basiswerken, waarnaar wordt verwezen. Alleen waar nodig zal er in het kort even op worden ingegaan.
7.1 Inleiding
Om ziekteprocessen die zich afspelen in de longen, luchtwegen en longvliezen (pleurae) te kunnen begrijpen en de gevolgen ervan voor het functioneren van het lichaam te kunnen inschatten, is kennis nodig van de normale anatomie van de thoraxinhoud en de fysiologie van het functioneren van de long. Deze is te vinden in het boek Fysiologie en Anatomie uit de serie Basiswerken, waarnaar wordt verwezen. Alleen waar nodig zal er in het kort even op worden ingegaan.
7.2 Respiratie en respiratoire insufficiëntie
Voordat de verschillende aandoeningen worden besproken eerst aandacht voor het klinische beeld van respiratoire insufficiëntie (longfalen), dat zich in ernstige situaties bij longziekten kan ontwikkelen. Centraal staat hierin het ontsporen van respiratie, diffusie en perfusie, al dan niet met elkaar gecombineerd.
Respiratie is het opnemen van zuurstof in het bloed en de afgifte van koolzuurgas naar de (relatieve) buitenwereld. Dit proces gebeurt met behulp van diffusie: het bewegen van deeltjes van een plaats waar ze meer voorkomen naar een plaats waar ze minder voorkomen, totdat een evenwicht is bereikt. Teneinde deze respiratie goed te laten verlopen, is een normale ventilatie van de long noodzakelijk: het tijdig verversen van de alveolaire lucht. Daarnaast is een normale bloeddoorstroming ofwel perfusie van de long essentieel. De respiratie kan namelijk niet zonder een goede ventilatie-perfusieverhouding. Onder normale omstandigheden passen beide zich aan aan de eisen die het lichaam aan de ademhaling stelt. De long heeft daarin bovendien een zeer grote reservecapaciteit.
Ziekteprocessen nu kunnen diffusie, ventilatie en perfusie dermate beïnvloeden dat de respiratie tekortschiet, waardoor een verhoging van de arteriële koolzuurspanning (= hypercapnie) kan optreden. Er is dan sprake van respiratoire insufficiëntie. De toegenomen koolzuurspanning in het bloed zal een verzuring (acidose) tot gevolg hebben.
Omdat deze acidose het gevolg is van een gestoorde respiratie, wordt het een respiratoire acidose genoemd. Daarnaast leidt het zuurstoftekort in de weefsels (= hypoxie), dat vaak tegelijkertijd aanwezig is, tot een overschakeling van de cellen op een anaërobe stofwisseling waarbij melkzuur als eindproduct vrijkomt. Deze stof zal nog extra bijdragen tot de verzuring (metabole acidose). De nier zal op de verzuring reageren door extra (basisch) bicarbonaat in de tubuluscellen aan te maken en aan het bloed af te geven. Tegelijkertijd worden H-ionen naar de inhoud van de tubulus uitgescheiden. Dit vindt plaats via uitwisseling tussen Na-ionen/H-ionen in het proximale deel van de tubuli en de lis van Henle, en van K-ionen/H-ionen in het distale deel van de tubuli en de verzamelbuisjes. In het proximale deel zullen de H-ionen zich met het HCO3 dat zich in het filtraat bevindt binden, dat geheel is opgebruikt op het moment dat het distale tubulusdeel wordt bereikt. Vanaf dat punt buffert het in het filtraat aanwezige fosfaat de H-ionen of deze reageren met NH3 (ammoniak), dat in de proximale tubuluswand is geproduceerd en door het niermerg heen diffundeert naar de inhoud van de verzamelbuisjes. Het gevormde NH4 wordt in de urine uitgescheiden in de vorm van NH4OH. Dit hele proces draagt bij tot normaliseren van de pH in het lichaam.
In dit verband is het nodig ook nog even in te gaan op de wijze waarop H-ionen op cellulair niveau zich gedragen. Bij acidose kan dit zodanige bijeffecten geven dat daardoor opnieuw ziek-zijn volgt. In het lichaam zijn de concentraties van H-ionen in en buiten de cel met elkaar in evenwicht, wat gebeurt door opname en afgifte door de cel. Het is eigenlijk een uitwisseling van positieve en negatieve deeltjes; het moet immers ‘elektroneutraal’ gebeuren, dat wil zeggen dat gelijktijdig een deeltje met negatieve lading (anion) mee wordt opgenomen of een deeltje met positieve lading (kation) wordt afgegeven bij opname van het H-ion in de cel en omgekeerd bij afgifte uit de cel.
Het in het menselijk lichaam best beschikbare kation is kalium.
Bovengenoemde gebeurtenissen geven aanleiding tot een hoog kalium, wat gevaarlijk is voor het hart. Een hoog natrium, dat ook kan ontstaan, is niet echt gevaarlijk.
Bij herstel van de acidose door behandeling gebeurt het omgekeerde en kan een hypokaliëmie ontstaan, wat net zo gevaarlijk is voor het hart. Men moet dus tijdens de behandeling de serumkaliumwaarden goed in de gaten houden en eventueel corrigeren met intraveneuze toediening van KCl (zie behandeling).
7.2.1 Oorzaken
Respiratoire insufficiëntie kan acuut ontstaan, maar ook chronisch aanwezig zijn. Ook kan een chronische insufficiëntie weer acuut verergeren.
Acute respiratoire insufficiëntie: Adult Respiratory Distress Syndrome (ARDS)
Dit ziektebeeld ontstaat bij van tevoren meestal gezonde volwassenen (voor de bij zuigelingen voorkomende vorm wordt verwezen naar het boek Kindergeneeskunde uit de serie Basiswerken) en gaat vergezeld van acute dyspnoe, tachypnoe en cyanose. Op de röntgenfoto zijn over beide longen lokaal verdichtingen te zien. Ze zijn het gevolg van beschadigingen van de alveolaire wanden (bijv. na aspiratie, door bijna-verdrinking of door inhalatie van giftige stoffen) of van de capillairwanden (bijv. bij sepsis of als gevolg van algehele intravasale stolling (AIS), we zien het ook bij een polytraumatise). In het ziekteverloop kunnen zich fibrotische processen (verbindweefseling) ontwikkelen. De behandeling is gericht op bestrijding van onderliggende oorzaken, verder zuurstoftoediening en zo nodig overbruggende beademing.
Chronische respiratoire insufficiëntie
Dit kan het gevolg zijn van het langduriger aanwezig zijn van stoornissen in de diffusie, de perfusie of de ventilatie; vaak ook een combinatie van de drie. Oorzaken hiervoor zijn chronische ziekteprocessen die zich in de longen en de pleurae afspelen, zoals ernstige COPD, vaatafwijkingen (pulmonale hypertensie, recidiverende of persisterende longembolieën), maar ook longoedeem als gevolg van een decompensatio cordis links. De gasuitwisselingsstoornis uit zich in verlaagde PaO2 (hypoxemie), maar vooral in een toegenomen PaCO2. Dit beeld wordt longfalen (in engere zin) genoemd.
Het is ook mogelijk dat het functioneren van de ademhaling door een verstoring in de bij het proces betrokken anatomie of fysiologie niet goed gebeurt (pompfalen). Dit kan bij:
stoornissen in de functie van het ademcentrum, door neurologische aandoeningen of na overdosering van geneesmiddelen zoals morfine en sommige slaapmiddelen;
neurologische aandoeningen en spierziekten waardoor slecht functionerende ademhalingsspieren (bijv. bij poliomyelitis anterior acuta en spierdystrofie) ontstaan;
instabiliteit van de thoraxwand, na bijvoorbeeld een thoraxtrauma waarbij ribben op meerdere plaatsen zijn gebroken;
ziekten aan de wervelkolom waardoor de ribben slecht kunnen bewegen, zoals bijvoorbeeld bij de ziekte van Bechterew of bij een ernstige kyfose;
vermoeidheid/zwakte van de ademhalingsspieren, door overbelasting (zoals bij chronische longziekten met een bemoeilijkte ademhaling), een slechte voedingstoestand of een slecht hart.
Een acute insufficiëntie kan, afhankelijk van de verergering in het onderliggend lijden, als complicatie optreden en het beeld erg doen verslechteren.
7.2.2 Verschijnselen
De verschijnselen bij respiratoire insufficiëntie worden in de eerste plaats bepaald door de veroorzakende aandoeningen; daardoor kan het beeld heel verschillend zijn.
Een aantal verschijnselen is echter te wijten aan de hypoxie en hypercapnie. Beide beïnvloeden de hogere hersenfuncties, zodat vaak verminderde psychische spankracht, initiatiefverlies, een verminderd reactievermogen, slaperigheid, sufheid en eventueel bewusteloosheid aanwezig zijn. Sufheid zal weer de hypoventilatie bevorderen, waardoor de longventilatie nog slechter wordt en zich een vicieuze cirkel ontwikkelt.
De pols is versneld en de patiënt transpireert en kan rooddoorlopen ogen hebben als gevolg van een toegenomen sympaticusactiviteit.
Hypercapnie geeft ook nog cerebrale vaatverwijding waardoor de druk binnen de schedel toeneemt en hoofdpijn ontstaat.
Tussen acute en chronische insufficiëntie bestaat een accentverschil in de klachten: cyanose en bewustzijnsverlies, maar ook onrust, verwardheid, zweten, hypertensie en tachycardie treden bij een langzaam ontstane chronische vorm veel minder op.
Om een indruk te krijgen van de mate van respiratoire insufficiëntie is bloedgasanalyse behulpzaam. Behalve de PaO2- en PaCO2-waarden kan daarin ook een verstoring van het zuur-basenevenwicht worden gemeten (zie het boek Pathologie uit de serie Basiswerken).
7.2.3 Behandeling
Therapie van respiratoire insufficiëntie bestaat uit de volgende maatregelen:
het zo goed mogelijk behandelen van de aandoening die ertoe heeft geleid;
het geven van zuurstof;
zo nodig corrigeren van de acidose met i.v. NaHCO3;
kunstmatige beademing indien noodzakelijk;
controle en bijsturing van plasma-kaliumwaarden tijdens de hersteltijd.
Zuurstof wordt gegeven op geleide van het klinisch beeld en de arteriële bloedgaswaarden (Astrup), waarbij een duidelijke hypoxie (PaO2 onder 8 kPa) bestaat. Onoordeelkundige toediening kan in bepaalde gevallen tot ademstilstand leiden. Bij hen waarbij hypercapnie langere tijd heeft bestaan, is door de hoge koolzuurspanning de gevoeligheid van het ademcentrum voor de prikkel hiervan sterk verminderd en intussen al overgeschakeld op zuurstof in het bloed als prikkel voor het ademcentrum (door de receptoren van het glomus caroticum, dat reageert op een verlaging van de arteriële zuurstofspanning). Indien door een (te) ruime zuurstoftoediening de hypoxemie wordt gecorrigeerd, bestaat het gevaar dat de prikkel van het glomus caroticum uitvalt terwijl de gevoeligheid van het ademcentrum in het verlengde merg niet hersteld is. Het gevolg is een ademdepressie waardoor de respiratoire insufficiëntie toeneemt in plaats van verbetert. In dat geval worden de adembewegingen langzamer, neemt de sufheid toe, gaat de patiënt klagen over hoofdpijn en wordt hij verward. De zuurstoftoediening moet worden verminderd en de ademhaling moet op een andere wijze worden verbeterd. Zo probeert men soms het zenuwstelsel te stimuleren met behulp van medicamenten (prethcamide of doxapram, beide zouden het ademcentrum stimuleren; ook aminofylline zou dit doen). Bij de acute vorm geeft het effect; de middelen worden bij de chronische vorm niet toegepast. De patiënt moet aangezet worden tot ademhalen en hoesten. De fysiotherapeut kan bij dit alles zeer behulpzaam zijn.
De K-depletie wordt gecorrigeerd met een ruime toediening van kaliumchloride (KCl).
Tot kunstmatige beademing wordt slechts overgegaan indien bovenbeschreven maatregelen geen effect hebben of wanneer men niet verwacht dat ze zullen helpen.
7.2.4 Cor pulmonale als complicatie
Respiratoire insufficiëntie wordt vaak gecompliceerd door de aanwezigheid van een cor pulmonale; dat houdt in een overbelasting van het rechter hart door longafwijkingen. Anatomisch vaatbedverlies of een vasoconstrictie van de longvaten, zoals dat reflectoir optreedt bij respiratoire insufficiëntie, kunnen pulmonale hypertensie geven waardoor het rechterhart wordt overbelast. Bij een geleidelijke ontwikkeling hiervan treedt hypertrofie op van de rechter hartspier; bij een plotselinge overbelasting is dit niet het geval.
De verschijnselen, diagnostiek en behandeling van hartfalen staan beschreven in het betreffende hoofdstuk van dit boek, en in het boek Pathologie uit de serie Basiswerken.
7.3 Symptomen en onderzoek bij longziekten
Het is gelukkig niet zo dat elke aandoening van de longen, luchtwegen of pleurae leidt tot het ernstige beeld van de respiratoire insufficiëntie, maar ook zonder dat kan de ziekte de patiënt behoorlijk belasten.
Zoals bij elk orgaansysteem herkennen we ziekten van de ademhalingsorganen vooral aan specifieke klachten; soms kan de diagnose pas na verder onderzoek worden gesteld.
7.3.1 Specifieke klachten
Specifieke verschijnselen die optreden bij ziekten van longen, luchtwegen en pleurae zijn hoesten, opgeven van sputum, dyspnoe (deze wordt graad I t/m IV geregistreerd), veranderingen in ademfrequentie en diepte van de ademhaling en piepende en brommende geluiden die de ademhaling kunnen begeleiden.
Voor de wijzen waarop deze symptomen totstandkomen en de waarde die eraan moet worden gehecht, wordt verwezen naar de beschrijving in het boek Pathologie uit de serie Basiswerken.
7.3.2 Lichamelijk onderzoek
Bij het lichamelijk onderzoek zijn de volgende observatiepunten van belang.
Ademhaling
De frequentie van de ademhaling kan abnormaal zijn in de vorm van een bradypnoe (te lage frequentie) of tachypnoe (te snel). De ademhalingsdiepte is soms zichtbaar afwijkend. We kennen de hyperpnoe (ademhaling met een te grote luchtverplaatsing ofwel een te diepe ademhaling) en de hypopnoe (oppervlakkig). Verder kennen we de hyperventilatie ofwel een ademhaling die aanleiding geeft tot een lage arteriële koolzuurspanning, en een hypoventilatie die leidt tot een hoge koolzuurspanning.
Tijdens het ademhalen kunnen soms geluiden worden gehoord. Bij bijvoorbeeld patiënten met astma is dit piepen en brommen, vooral tijdens de expiratie omdat de obstructie laag in de bronchiale boom is gelokaliseerd. Een vernauwing die hoger zit, zoals in de trachea of larynx, leidt juist tot de meeste problemen bij de inademing ofwel tot een inspiratoire stridor (zie het boek Pathologie uit de serie Basiswerken).
Tot slot: patiënten die lijden aan chronische longaandoeningen hebben soms de eigenaardigheid hun ademhaling met blazen en kreunen te ‘vergemakkelijken’.
Houding
Sommige kortademige patiënten ondervinden verlichting in zittende houding (orthopnoe genoemd). Anderen daarentegen vinden het juist prettig om plat op hun zij te liggen. Indien de kortademigheid vooral bij inspanning aanwezig is, noemen we dit een dyspneu d’effort. Kortademigheid in rust heet een dyspneu de repos (zie het boek Pathologie).
Cyanose
Als gevolg van een tekortschieten in de ademhaling kan cyanose aanwezig zijn. Dat is het gevolg van een te grote hoeveelheid gereduceerd hemoglobine in het capillaire bloed, namelijk meer dan 3,13 mmol/l (zie het boek Pathologie), wat in deze situatie ontstaat.
Trommelstokvingers
Als er sprake is van een langdurig bestaan van hypoxie, treedt een eigenaardig verschijnsel op. De eindkootjes van de vingers en tenen verbreden zich, waardoor ze gaan lijken op trommelstokken; de nagels krijgen het model van een horlogeglas. Alleen de weke delen blijken te zijn vervormd, waarbij vaatjes zijn verwijd. Het bot is normaal. Hoe deze vervormingen kunnen optreden is niet geheel opgehelderd; men denkt dat hypoxemie er een rol bij speelt. Trommelstokvingers kunnen echter ook zonder hypoxie voorkomen; dat is dan vaak familiair.
Pols en halsvenen
Een polsfrequentie van meer dan 120 slagen per minuut tijdens een astma-aanval wijst op een ernstige situatie, evenals het aanwezig zijn van een pulsus paradoxus. Bradycardie bij een ernstig benauwde patiënt kan wijzen op een dreigende verstikking. Een cor pulmonale gaat door de verhoogde centraal veneuze druk (CVD) vaak vergezeld van overvulde halsvenen.
Thorax
Bij onderzoek van de thorax moet gelet worden op de vorm en symmetrie, zowel in rust als tijdens de ademhaling. Een zieke thoraxhelft beweegt minder mee met de ademhaling. Bij een overwegend positieve druk in een thoraxhelft, zoals bij een pneumothorax, zijn de ribben aan de zieke kant moeilijker ‘te tellen’. Door de hand op de thorax te leggen is soms te voelen dat er slijm en dergelijke in de luchtwegen aanwezig is. De trillingen die ontstaan bij bewegingen van de bronchusinhoud door de langsstromende lucht, planten zich namelijk voort naar het oppervlak. Dit gebeurt ook wanneer de patiënt stemgeluid voortbrengt. De voortplanting van deze trillingen naar het oppervlak is bij ziekteprocessen anders dan onder normale omstandigheden.
Na deze relatief simpele onderzoeksmethoden kan men met behulp van percussie (vooral beoordeling van het geluid en bepaling van de long/levergrens) en auscultatie (afwijkende ademgeruisen bij de verschillende longaandoeningen) vaak al een idee krijgen welk ziekteproces aanwezig is.
7.3.3 Aanvullend specifiek (laboratorium)onderzoek
We kennen diverse meer speciële onderzoeken waarmee patiënten met longaandoeningen verder kunnen worden onderzocht. De belangrijkste zijn de volgende.
Beeldvormende technieken waarbij gebruikgemaakt wordt van röntgenstraling
Voor de diagnostiek van aandoeningen van luchtwegen, longen en pleurae is het röntgenologisch onderzoek een belangrijke ontdekking geweest. De long op zichzelf vormt weinig contrast voor röntgenstralen; het is immers een zeer luchthoudend orgaan. Abnormale structuren (ontstekingen, tumoren) zijn niet luchthoudend en springen daarom op een röntgenfoto direct in het oog. Enkele voorbeelden van thoraxonderzoeken zijn:
thoraxfoto. Er worden altijd ten minste twee opnamen gemaakt: een voor-achterwaartse en een dwarse. Bij de eerste gaan de röntgenstralen van voor naar achter door het lichaam waardoor een foto ontstaat waarop de ribben, het hart, de diafragmakoepels et cetera zichtbaar zijn. Bij de dwarse foto gaan de stralen van links naar rechts door het lichaam van de patiënt. De dwarse foto is nodig omdat op een voor-achterwaartse foto van de linkerlong ongeveer 1/5 deel schuilgaat achter het hart en de diafragmakoepel en van de rechterlong ongeveer 1/10 deel achter het diafragma verdwijnt;
tomografie. Dit wordt ook wel planigrafie of seriedoorsnee-onderzoek genoemd. De long wordt bij tomografie als het ware in plakken gesneden, waarvan afzonderlijke opnamen worden gemaakt. Tomografie dient voor nauwkeurige lokalisatie van de afwijking. De overprojectie van andere structuren in de thorax is veel minder, waardoor het lokaliseren van de afwijking vereenvoudigd wordt. Tomografie is tegenwoordig grotendeels vervangen door CT-scanning;
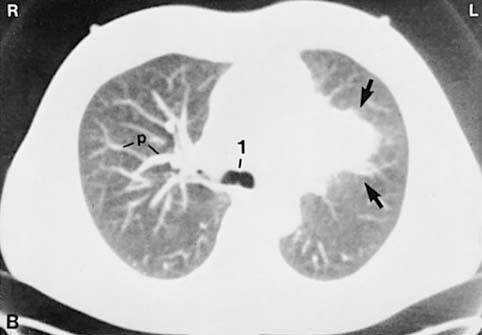
CT-scan (afb. 7.2). De techniek hiervan is beschreven in het leerboek Pathologie. De hoge-resolutie-CT-scan (HRCT) is nog gevoeliger en daarmee kunnen kleinere en grotere anatomische afwijkingen aan luchtwegen en alveoli en afwijkingen in het interstitium van longweefsel nauwkeuriger worden bekeken. Spiraal-CT, waarbij de stralenbron continu roteert en de patiënt als het ware door het beeld heen beweegt, is hier nog een waardevolle aanvulling op;
doorlichting. Hierbij is er sprake van een onderzoek naar bewegingsfenomenen, mits de patiënt goed meewerkt. De patiënt wordt gevraagd in en uit te ademen en gedurende die ademhalingsbewegingen wordt de beweeglijkheid van het diafragma gecontroleerd. Tegelijkertijd wordt nagegaan of het mediastinum zich verplaatst. Normaal is dit laatste niet het geval. Indien dit wel zo is, kan er sprake zijn van een vernauwing in een hoofdbronchus. Tijdens de inspiratie beweegt het mediastinum zich in de richting van deze bronchus; de lucht kan de vernauwing namelijk minder snel passeren, waardoor de long zich aan die kant minder snel vult. Tijdens de expiratie gebeurt juist het omgekeerde, omdat de lucht in de long aan de zieke zijde er minder snel weer uit kan. Vervolgens keert het mediastinum weer terug in de mediaanlijn. We noemen dit een positief holzknecht-fenomeen; het wordt nog wel eens bij longkanker gezien;
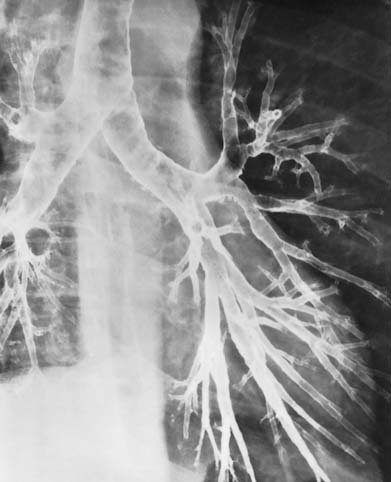
bronchografie. Indien men een patiënt een contrastvloeistof laat inademen, zal deze zich als een film over het slijmvlies van de luchtwegen verspreiden. Door vervolgens een röntgenfoto te maken wordt de bronchiale boom zichtbaar. Men kan zo afsluitingen en afwijkende bronchusvormen op het spoor komen (zie afb. 10.1007/978-90-313-7416-8_8#Fig1 en b). Deze onderzoeksmethode is inmiddels vrijwel overbodig geworden sinds de invoering van de CT-scan;
angiografie. Wanneer een contrastvloeistof in het bloed wordt ingebracht, is het mogelijk de bloedvaten die de long ‘doorstromen’ zichtbaar te maken. Een enkele maal is dit nodig om er bijvoorbeeld zeker van te zijn dat een geconstateerde ‘vlek’ op de long niet op een afwijkende vaatstructuur berust. De DSA-techniek (zie leerboek Pathologie uit de serie Basiswerken) wordt hierbij gehanteerd omdat daarbij de hoeveelheid contrastmiddel kan worden beperkt.

Andere beeldvormende technieken
Echografie (de techniek is beschreven in het leerboek Pathologie). Luchthoudend weefsel, wat de long is, reflecteert geen ultrasonore geluidgolven. Pathologische processen (tumoren, lymfeklieren, ontstekingen, pleuravocht) die vocht of cellen bevatten daarentegen wel;
MRI (magnetic resonance imaging) of kernspintomografie (zie voor beschrijving techniek leerboek Pathologie). Is behulpzaam in het onderscheiden van weefsels van elkaar en om afwijkingen aan de bloedvaten te onderkennen;
isotopenonderzoek (longscintigrafie). Dit wordt vooral gebruikt voor het vaststellen van longembolieën. Voor het vaststellen hiervan worden klompjes albuminemoleculen gemerkt met een isotoop (bijv. Tc99MAA) die worden geaccepteerd in het longbloedvaatnet. Op deze wijze kan een perfusiescan worden gemaakt. Voor onderzoek naar de longventilatie (ventilatiescan) wordt een gas gemerkt met een isotoop (bijv. Xe133-gas) geïnhaleerd.
Longfunctieonderzoek en bloedgasanalyse
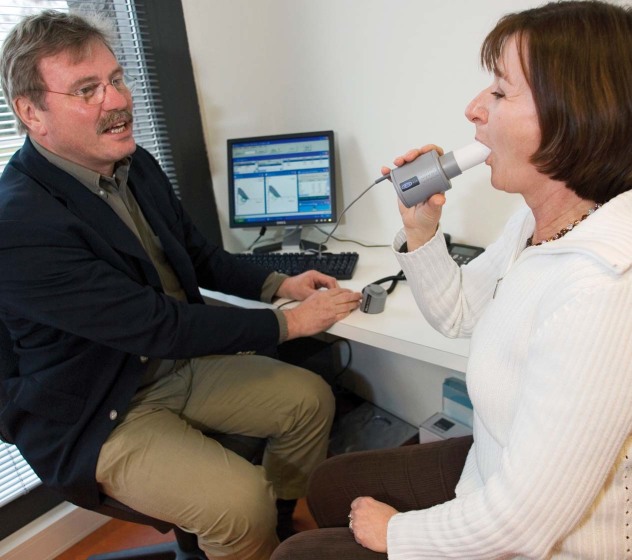
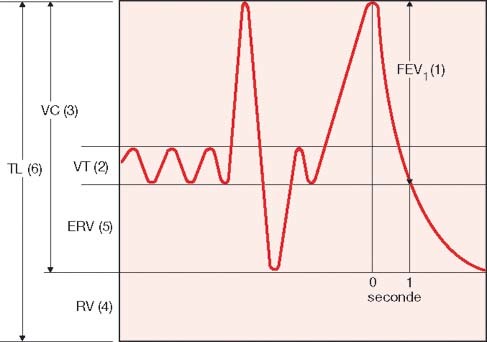
Het is zeer belangrijk om te weten in hoeverre de longfunctie bij de patiënt gestoord is. Daartoe kunnen statische en dynamische longvolumina gemeten worden. Ook kan door bloedgasanalyse het tekortschieten van de gasuitwisseling worden vastgesteld. Het instrument waarmee longvolumina kunnen worden gemeten heet de spirometer (afb. 7.3). Met behulp van dit apparaat wordt een spirogram berekend, waaruit statische en dynamische functies zijn af te leiden. De belangrijkste hiervan zijn in een overzicht beschreven (afb. 7.4).
Een andere wijze waarop de mate van luchtwegvernauwing kan worden gemeten is met behulp van de peakflowmeter. Dit instrument is wel minder nauwkeurig, maar heeft het voordeel dat het, ook thuis door de patiënt zelf, eenvoudig is te hanteren.
Voor bloedgasanalyse moet arterieel bloed worden gebruikt; als dat niet mogelijk is mag capillair bloed worden genomen. Hierin worden onder andere de zuurstof- (pO2) en de koolzuurspanning (pCO2) bepaald, evenals de pH. Na een arteriepunctie moet men bedacht zijn op nabloeding ten gevolge van de hogere druk in de arterie. De punctie-opening moet ten minste tien minuten zorgvuldig worden afgedrukt.
Allergieonderzoek
Bij astma- en ook wel COPD-patiënten is het vaak zinvol een allergieonderzoek te verrichten. De wijze waarop dit gebeurt staat beschreven in paragraaf 7.5.1.
Histaminedrempelbepaling
Ook dit onderzoek wordt bij astma- en COPD patiënten verricht en dient om hyperreactiviteit van de luchtwegen vast te stellen. De techniek staat eveneens beschreven in paragraaf 7.5.1.
Sputumonderzoek
De samenstelling van het sputum kan ons informeren over wat zich in de bronchiale boom afspeelt. Gekeken wordt naar de hoeveelheid en het aspect van het sputum. Is het sputum etterig, dan noemen we het purulent; is er wat bloedbijmenging, dan heet het sanguinolent. Astmapatiënten produceren soms taaiig sputum, dat er glazig uitziet. Indien nodig kan sputum gekweekt worden. Ook kan het worden onderzocht op de aanwezigheid van maligne cellen. De kleuring volgens Papanicolaou geeft wat dit betreft een heel betrouwbare uitslag.
Invasieve technieken
Scopieën
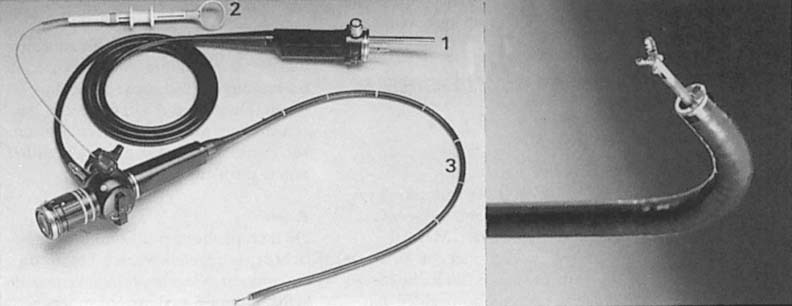
In de pulmonologie worden bronchoscopie (endoscopisch onderzoek van de luchtwegen), thoracoscopie (onderzoek van de pleuraholte) en mediastinoscopie (onderzoek van het mediastinum via een supraclaviculaire incisie) toegepast. Met de endoscoop kan behalve een directe inspectie van de afwijking, onder meer een biopsie worden verricht voor histologisch onderzoek (zie afb. 7.5).
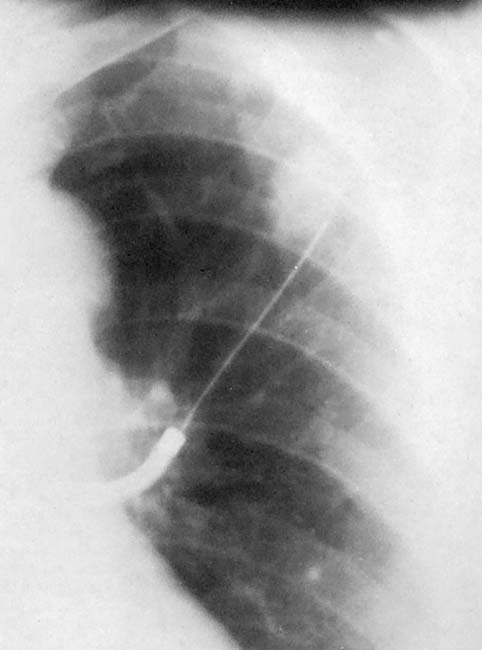
Pleurapunctie/pleurabiopsie
De punctie wordt vlak boven een rib uitgevoerd. Deze ingreep kan om diagnostische redenen, maar ook uit therapeutische overwegingen bedoeld zijn.
7.4 Ontstekingen van de luchtwegen en longen
7.4.1 Acute bronchitis
Acute bronchitis is een ontsteking van de luchtwegen die wordt veroorzaakt door micro-organismen. Meestal hebben we te maken met een virus dat na inhalatie in staat is het luchtwegepitheel aan te tasten. Voorbeelden van dergelijke virussen die bij volwassenen een acute bronchitis kunnen doen ontstaan, zijn adeno-, rhino-, influenzavirussen, respiratoir syncytieel (RS)-virus en andere, de laatste drie vooral in de wintermaanden. Secundair kan een bacteriële superinfectie optreden omdat een virusinfectie lokaal het epitheel beschadigt. Bacteriën zijn zelden primair de oorzaak van een acute bronchitis. De ziekte komt behoorlijk vaak voor bij astma en COPD. Bij deze patiënten verloopt het beeld ernstiger, omdat een keten aan reacties wordt uitgelokt die de bronchusobstructie bevorderen.
Symptomen
Een acute bronchitis treedt vaak aansluitend op aan een infectie van de bovenste luchtwegen. Neus- en keelklachten voorafgaande aan een acute bronchitis zijn dan ook geen zeldzaamheid. Hoesten en opgeven van grijzig of wat purulent sputum, met daarbij vaak pijn achter het borstbeen, zijn de belangrijkste verschijnselen. Inspanning, lachen, inademen van koude lucht en dergelijke lokken vaak het hoesten uit. Doordat het virus het luchtwegepitheel aantast, zijn zenuwuiteinden nu dichter aan het oppervlak gekomen; dit verklaart het extra prikkelbaar zijn van de luchtweg. Soms is een paar dagen koorts aanwezig.
Onderzoek
De diagnose wordt gesteld op het klinische beeld. De thoraxfoto zal geen afwijkingen te zien geven. Virusdiagnostiek (zie het boek Pathologie uit de serie Basiswerken) wordt alleen uitgevoerd als speciale omstandigheden daartoe aanleiding geven. Denk hierbij aan patiënten met een sterk verminderde afweer. Sputum kan eventueel worden gekweekt als het aspect purulent wordt. Betrokken bacteriën, die tevens een rol spelen bij een complicerende pneumonie, zijn de S. pneumoniae, de H. influenzae, de Moraxella catarrhalis en de P. aeruginosa. Bij influenza vooral de S. aureus.
Behandeling
De therapie bestaat uit symptoomgerichte maatregelen. Vaak is het nuttig het ophoesten van sputum te vergemakkelijken door bijvoorbeeld slijmverdunners als Bisolvon® of Fluimucil® voor te schrijven. Het hoesten zal dan ook verminderen. Is de hoest absoluut niet (meer) productief maar wel erg hinderlijk, dan mag een hoestdempend middel worden gebruikt zoals codeïne of Tuclase®.
Patiënten die behoren tot de risicogroepen hebben soms een aanvullende behandeling nodig met antibiotica en een prednisonkuur; bij hen wordt tevens vaccinatie tegen influenza toegepast.
7.4.2 Pneumonieën
Onder een pneumonie verstaan we een ontsteking van het longparenchym (longweefsel). Vaak echter zal niet alleen het parenchym ontstoken zijn, maar tevens in de buurt gelegen bronchi en bronchioli. Meestal is de wand van zo’n luchtpijptakje het eerst ontstoken, waarna het longweefsel in het proces betrokken wordt. Micro-organismen die verantwoordelijk zijn voor het ontstaan van pneumonieën worden als regel ingeademd (aërosol) of geaspireerd vanuit de oropharynx. Aanvoer via de bloedbaan is uiteraard ook mogelijk, maar dit gebeurt veel minder vaak.
Oorzaken
Pneumonieën kunnen zich primair ontwikkelen bij personen met van tevoren gezonde longen. Het secundair optreden op basis van reeds tevoren bestaande afwijkingen in longen en luchtwegen komt veel vaker voor. Bij deze laatste groep is er sprake van het bestaan van predisponerende factoren waartoe men rekent:
obstructie van de luchtwegen door bijvoorbeeld tumoren, een corpus alienum, aspiratie en cara;
aangetast luchtslijmvlies door virale infecties of door inwerking van chemische of fysische irritantia;
veranderd longweefsel zoals dat kan optreden bij een embolie;
retentie van slijm in de luchtwegen zoals dat voorkomt bij mensen die slecht doorademen, operatie- en bedlegerige patiënten evenals patiënten met neurologische stoornissen;
stuwing in de pulmonale circulatie.
Bij primaire infecties wordt datgene wat zich gaat afspelen in eerste instantie bepaald door de afweer van de gastheer. Bij secundaire infecties zijn het de predisponerende factoren die het ontstaan en verloop van de ontsteking bepalen. Het is van groot belang dat behalve het vaststellen van de pneumonie ook de predisponerende factoren gevonden en behandeld worden. Dit laatste vooral omdat anders de kans bestaat dat de pneumonie zich gaat herhalen. Daarnaast is het van belang, in verband met de keuze van een antimicrobieel middel, te weten welk(e) micro-organisme(n) betrokken is (zijn) bij de ontsteking. In de meeste gevallen is dit bij de longontsteking een bacterie.
Openbaart de longontsteking zich buiten het ziekenhuis, of in de eerste 72 uur van de ziekenhuisopname, dan spreekt men van een community acquired pneumonia (CAP). In dat geval zijn daar in de regel een beperkt aantal verwekkers bij betrokken (Streptococcus pneumoniae, Mycoplasma pneumoniae, Hemophilus influenzae, Staphylococcus aureus, Legionella pneumophila, Mycobacterium tuberculosis en virussen).
Ontstaat de longontsteking in het ziekenhuis na een opname van ten minste 72 uren, dan spreekt men van een nosocomiale pneumonie (ziekenhuisinfectie). Vijf procent van alle ziekenhuispatiënten loopt zo’n pneumonie op. De redenen daarvoor zijn uitvoerig besproken in het boek Pathologie uit de serie Basiswerken, waarnaar ook voor de specifieke problematiek van dergelijke ziekenhuisinfecties verwezen wordt. In 50% van de nosocomiale pneumonieën zijn gramnegatieve verwekkers (Klebsiella, Pseudomonas aeruginosa, Enterobacter, E. coli) betrokken, verder de Staphylococcus aureus en anaërobe bacteriën.
Patiënten met een sterk verminderde weerstand (immunodeficiëntie) hebben een veel grotere kans om, naast andere infecties, een longontsteking te krijgen. Er is hier vaak sprake van een opportune infectie waarbij verwekkers die normaliter nauwelijks pathogeen zijn, nu een ernstig ziek-zijn kunnen veroorzaken. Een voorbeeld hiervan is de Pneumocystis carinii bij de aidspatiënt.
Algemene symptomen en onderzoek
Een pneumonie kan gepaard gaan met de volgende symptomen:
koorts, soms hoge koorts voorafgegaan door een koude rilling;
hoesten dat diep wegkomt en soms met pijn in de borst gepaard gaat;
opgeven van purulent sputum;
soms pijn bij de ademhaling (pleurapijn);
dyspneu, tachypnoe eventueel met ‘neusvleugelen’;
cyanose;
soms ‘koortsuitslag’, vooral bij een acuut verloop zoals bij een lobaire pneumonie (zie verderop).
Bij onderzoek van de thorax valt op dat de zieke kant minder goed meebeweegt met de ademhaling. Bij percussie en auscultatie wordt verdichting van weefsel vastgesteld. Soms wordt pleurawrijven gehoord.
Met een röntgenfoto kunnen de bevindingen bij het lichamelijk onderzoek bevestigd worden. Soms is er sprake van dat een of meer longkwabben in hun geheel zijn ontstoken: dit heet lobaire of kroepeuze pneumonie. Meestal hebben we te maken met een haardsgewijs voorkomen van de ontsteking: dit wordt lobulaire pneumonie of bronchopneumonia genoemd. Dit kan met een röntgenfoto vastgesteld worden.
Het bloedonderzoek levert een verhoogde BSE, een verhoogde CRP (een eiwit dat in het bloed aanwezig is bij een acute ontsteking), een leukocytose en een linksverschuiving in het witte beeld op, tenminste als een bacterie de verwekker is. Van het sputum kan een microscopisch preparaat worden gemaakt, waarbij heel vaak al de verwekker zichtbaar wordt. Een nauwkeurige microbiële diagnose met een bijbehorend resistentiepatroon volgt na het inzetten van een kweek van het sputum.
Belangrijkste verwekkers en behandeling
In het voorgaande is al een aantal verwekkers genoemd die betrokken zijn bij longontsteking. Afhankelijk van de verwekker kan het ziektebeeld meer of minder ernstig verlopen of treden extra symptomen op. In het volgende wordt dit voor enkele bacteriële verwekkers beschreven.
Streptococcus pneumoniae
Streptococcus pneumoniae , kortweg de pneumokok, is in het bijzonder betrokken bij de lobaire pneumonie, maar is ook vaak bij de hypostatische pneumonie als verwekker aangetoond. Een hypostatische pneumonie is een longontsteking in de achterste longvelden ten gevolge van een slechte ventilatie van die longdelen. Dit kan voorkomen bij ouderen die weinig diep doorzuchten, bij hen die dit eveneens niet kunnen door neurologische of andere aandoeningen of bij bedlegerige patiënten. Bedlegerigheid geeft namelijk ook vaak aanleiding tot hypoventilatie van de onderste longvelden.
Als er sprake is van de lobaire vorm, gaat de pneumonie als regel vergezeld van hoge koorts na koude rillingen en kan het sputum roestbruin van kleur zijn (sputum rufum) (afb. 7.6a). Koortsuitslag (herpessimplexinfectie) begeleidt het beeld meestal.


De behandeling bestaat uit het toedienen van penicilline of, als daarvoor een overgevoeligheid c.q. resistentie bestaat, erytromycine. Het is zaak de diagnose snel te stellen en dan de antimicrobiële therapie direct te beginnen. Voorspoedig herstel volgt dan als regel. Een pneumokokkenpneumonie kan namelijk, vooral bij ouderen, ernstig verlopen en zelfs tot de dood leiden. Gezien dit feit gaat men tegenwoordig bij risicogroepen over tot vaccinatie met een pneumokokkenvaccin.
Staphylococcus aureus
Stafylokokkenpneumonieën verlopen ernstig en geven vaak aanleiding tot complicaties. Ze zijn gevreesd als complicatie bij influenza, komen voor bij intraveneuze druggebruikers en zijn bekend als ziekenhuisinfectie (afb. 7.6b).
De pneumonie kan zich acuut maar ook geleidelijk ontwikkelen. Zij is vaak dubbelzijdig en maakt de patiënten erg ziek. Hoge koorts en cyanose zijn aanwezig. Het etterige sputum kan bloed bevatten. Abcedering van het infiltraat, pleuritis exsudativa en empyeemvorming komen nogal eens voor als complicatie. Tevens kan zich een shock ontwikkelen.
De behandeling bestaat uit het toedienen van een gericht antibioticum omdat stafylokokken steeds vaker penicillinase maken en zo resistent zijn geworden tegen penicilline. Indien aanwezig moeten de shock en hypoxie adequaat bestreden worden.
Legionella pneumophila
Deze bacterie werd enige jaren geleden ‘nieuw’ als verwekker van pneumonieën ontdekt. Het blijkt echter een bacterie te zijn die zeer veelvuldig in ons milieu aanwezig is (modder, waterreservoirs, airconditioningssystemen) en voorheen ook al aanleiding gaf tot kleine epidemieën.
Een infectie met de L. pneumophila kan geheel symptoomloos verlopen. Ouderen, mensen met een verminderde weerstand en rokers kunnen er echt ziek van worden. In dat geval geeft het aanleiding tot een pneumonie, soms met gastro-intestinale verschijnselen. Ook sufheid en dergelijke kunnen aanwezig zijn. Kenmerkend voor het ziektebeeld is de aanwezigheid van hoge remitterende koorts en een in eerste instantie niet-productieve hoest. Soms dreigt een respiratoire insufficiëntie op te treden.
Voor de diagnostiek is speciaal sputumonderzoek (immunofluorescentietest) noodzakelijk. Met serodiagnostiek is het ook mogelijk zekerheid te krijgen omtrent de diagnose.
Een deel van de bacteriewand (antigeen) wordt in de urine uitgescheiden. Hierop is een test ontwikkeld (urinestick) die binnen enkele minuten uitslag geeft. De test is echter niet helemaal specifiek.
De behandeling bestaat uit het toedienen van levofloxacin.
Andere oorzakelijke bacteriën
Hemophilus influenzae. Deze bacil kan een vaste bewoner van de luchtwegen van COPD-patiënten zijn. De laatste tijd wordt hij echter steeds vaker als verwekker van longontstekingen gezien. De bacterie is gevoelig voor amoxicilline. Sinds twee jaar bestaat er een vaccin tegen de Hemophilus influenzae (Hemophilus influenzae B-vaccin).
Overige pneumonieën
Viruspneumonie
Pneumonieën ten gevolge van virusinfectie komen veel minder vaak voor dan bacteriële pneumonieën. De symptomen die erbij kunnen optreden variëren van licht tot zeer ernstig, soms zelfs tot de dood. Hoesten, koorts en het opgeven van sputum dat grijzig van aspect is, zijn de meest voorkomende klachten. Op de thoraxfoto is soms een driehoekige tot streperige schaduw waarneembaar. Een gerichte therapie is niet mogelijk.
Aspiratiepneumonie
Aspiratie van maaginhoud, zoals vooral bij comateuze patiënten, epileptici en alcoholisten voorkomt, leidt tot ernstige beschadiging van de longen. Behalve dat zich op meer plaatsen pneumonieën ontwikkelen, wordt ook het surfactans aangetast waardoor de gasuitwisseling sterk in gevaar komt en acute respiratoire insufficiëntie kan ontstaan.
Aspiratie van een corpus alienum geeft meestal aanleiding tot een pneumonie in de rechter middenkwab. Dit is anatomisch verklaarbaar. Het voorwerp glijdt het meest eenvoudig de rechter hoofdbronchus en daarna de rechter middenkwabsbronchus in omdat de bochten ten opzichte van de andere vertakkingen namelijk het minst scherp zijn. Het voorwerp moet onherroepelijk worden verwijderd omdat anders de pneumonieën steeds zullen terugkeren en op den duur aanleiding geven tot atelectasevorming en verbindweefseling van de middenkwab.
Complicaties
Pleuritis, pleura-empyeem en de vorming van een longabces zijn de belangrijkste complicaties die zich bij pneumonieën kunnen voordoen.
De pleuritis komt later nog ter sprake. Het pleura-empyeem is een ophoping van etter in de pleuraholte, gepaard gaande met steeds terugkerende koortspieken. Drainage door middel van een pleurapunctie en spoelen van de pleuraholte met een antibiotica-oplossing is over het algemeen een afdoende behandeling. Aan een longabces wordt gedacht als op de ingestelde therapie niet wordt gereageerd en de patiënt zieker wordt. Er is bovendien vaak een piekende koorts aanwezig. Op een röntgenfoto is het abces als een ronde schaduw waarneembaar, met een luchtsikkel en vaak een vloeistofspiegel.
Longabcessen kunnen zich in principe uit iedere bacteriële pneumonie ontwikkelen, mits de omstandigheden daartoe aanleiding geven. Het komt echter vaker voor bij longontstekingen die als complicatie bij sepsis optreden (hematogene besmetting van de long) en bij aspiratiepneumonieën. Ontwikkeling van een abces dreigt ook wanneer een oorzakelijke factor zoals een bronchusobstructie door een corpus alienum of tumor niet wordt opgeheven.
Behandeling van een abces
Doorbraak van een abces naar de luchtwegen zal leiden tot het ophoesten van een hoeveelheid, vaak stinkend (anaërobe flora) sputum. Het is zaak de abcesholte met behulp van fysiotherapie zo goed mogelijk leeg te houden. Daarnaast is intensieve antimicrobiële therapie nodig. Het genezingsproces is langdurig; genezing vindt uiteindelijk plaats met littekenvorming.
7.5 Astma en COPD
7.5.1 Inleiding
Astma en chronic obstructive pulmonary disease (COPD, hieronder vallen chronische bronchitis en longemfyseem) zijn veelvoorkomende aandoeningen in Nederland. Ze dragen bij tot 20-40% van het totale ziekteverzuim; 10-20% van de bevolking bezoekt regelmatig de huisarts (specialist) in verband met klachten.
De ziektebeelden zullen hierna elk afzonderlijk worden toegelicht. Vooraf een aantal eigenschappen die we zowel bij astma als bij COPD tegenkomen (tabel 7.1).
| astma | COPD |
|---|---|
| jonge leeftijd | oudere leeftijd |
| plotseling begin | geleidelijk aan ontstaan van klachten |
| allergie speelt duidelijke rol | roken speelt duidelijke rol |
| wisselende reversibele bronchusobstructie | aanhoudende nauwelijks reversibele bronchusobstructie |
Het begrip hyperreactiviteit
Bij alle bovengenoemde aandoeningen bestaat een overdreven gevoeligheid van de luchtwegen, ook wel hyperreactiviteit genoemd. Deze eigenschap kun je via dominante overerving krijgen, maar hij kan ook zijn verworven ten gevolge van milieufactoren (bijv. roken) of ziekteprocessen in longen en luchtwegen. Verderop wordt dit uitgelegd.
De hyperreactiviteit van de luchtwegen heeft tot gevolg dat op allerlei prikkels wordt gereageerd met:
samentrekking van gladde spiercellen;
zwelling van het slijmvlies door oedeemvorming en ontstekingsreacties;
aanmaken van extra slijm door de geprikkelde slijmklieren.
Alle drie geven aanleiding tot vernauwing van de luchtwegen, waardoor de patiënt zowel bij inspanning als in rust meer of minder ernstige benauwdheidsklachten krijgt. Daarnaast leiden ze tot andere respiratoire symptomen zoals hoesten, opgeven van sputum en piepen op de borst. De processen spelen zich vooral af in de kleinere luchtwegen. Het gevolg is luchtpijpvernauwing ofwel bronchusobstructie van de kleinere luchtwegen. Dan zal met name de uitademing belemmerd zijn (zie voor uitleg hiervan het boek Pathologie uit de serie Basiswerken). Bij longfunctiemeting weerspiegelt zich dit in een verlaagde FEV1 (forced expiratory volume one second, afb. 7.3). Bij zowel astma als COPD hebben we dus primair te maken met een uitademingsstoornis. Later, als situatie langer bestaat, kunnen ook andere stoornissen in de longfunctie optreden.
De prikkels waarop de bronchiale boom reageert worden ingedeeld in twee groepen:
-
aspecifieke prikkels, zijn van niet-allergische aard. Luchtverontreiniging, vochtigheid, mist, koude lucht en dergelijke vallen hieronder; chemische en fysische prikkels dus. Ook roken hoort hierbij, evenals geforceerd ademhalen (bijv. bij sporten).
De gevoeligheid van de luchtwegen voor aspecifieke prikkels kan in het laboratorium worden getest met behulp van een stof die hetzelfde effect geeft, bijvoorbeeld histamine of metacholine. We bepalen dan de histaminedrempel. Men laat de patiënt de stof (bijv. histamine) in nevelvorm in steeds hogere concentraties inhaleren. Met een spirograaf worden de reacties van de luchtwegen gemeten. Ontstaat bij een concentratie van kleiner dan 16 mg/ml aan histamine een duidelijke bronchusobstructie (FEV1 daalt meer dan 20%), dan achten we bij de persoon een duidelijk verhoogde gevoeligheid voor aspecifieke prikkels aanwezig. Men stelt dan dat er sprake is van een duidelijke hyperreactiviteit, het woord hyperreactiviteit in de engere zin van het woord gebruikend;
- specifieke (allergische) prikkels. Merkwaardigerwijs zijn veel (50%) van de astmapatiënten allergisch; sommige COPD-patiënten kunnen deze eigenschap ook hebben (heeft vaak eerder in hun leven gespeeld). Dit vermogen tot allergisch reageren (= atopie) is genetisch bepaald, zoals ook in sommige gevallen bij hyperreactiviteit. Dit gebeurt wel onafhankelijk van elkaar. Het is dus niet zo dat iedere astma (en zeker niet elke COPD-)patiënt ook allergisch is.De meest voorkomende stoffen waarvoor zich een allergie kan ontwikkelen en waarbij contact via inademen gemakkelijk realiseerbaar is, zijn:
- huisstof (eigenlijk de fecale uitscheidingsproducten van de huisstofmijt);
- pollen;
- haren/veren (eigenlijk huidschilfers) van katten, cavia’s, honden, vogels, soms ook van mensen;
- schimmelsporen (oude vochtige huizen).
Daarnaast kunnen ook niet ingeademde, maar opgegeten allergenen ernstige klachten uitlokken. Berucht is in dit verband het gebruik van Aspirine®. We kennen het ook na eten van schaaldieren, bepaalde fruitsoorten (bijv. kiwi), sommige graansoorten, noten en melkproducten (bijv. kaas).
De allergische reactievorm die centraal staat hierin is de zogenaamde ‘immediate type’-reactie (type-I-reactie). Hierbij speelt de mestcel een belangrijke rol. Deze is door herhaald contact met het allergeen gesensibiliseerd geraakt. De antilichamen van het IgE-type zitten daarbij aan het oppervlak van de mestcel. Bij een volgend contact met het allergeen zal de mestcel reageren met het vrijlaten van stoffen (mediatoren; histamine en tryptase) die verantwoordelijk zijn voor de daaropvolgende reacties die obstructie veroorzaken (afb. 7.7) (zie voor verdere uitleg het boek Pathologie uit de serie Basiswerken).

Bij een type-I-reactie verschijnen de klachten vrij direct na het contact met het allergeen (vroege reactie) of worden pas na enkele uren duidelijk zichtbaar (late reactie) doordat vrijgekomen mediatoren witte bloedcellen activeerden tot het produceren van onder andere leukotriënen. Dit neemt enkele uren in beslag. De leukotriënen geven sterke contractie van gladde spiercellen.
Het IgE kan soms in het bloed worden gemeten (phadiatroptest, RAST-test).
In het bloed en het sputum is het aantal eosinofiele granulocyten verhoogd. Eo’s spelen een rol bij de ontstekingsreacties die zich in de luchtwegen afspelen bij met name astma. Zijn de aantallen verhoogd, dan is een exacerbatie in de klachten te verwachten.
Met behulp van cutane en intracutane huidtests kan men een allergie aantonen. Wil men er zeker van zijn welk allergeen betrokken is bij de op dit moment aanwezige klachten, dan kan men het laten inhaleren en op geijkte momenten de FEV1 meten. Er zal dan zeker een bronchusobstructie optreden (een bronchusverwijdend middel dient dan wel bij de hand gehouden te worden).
Naast eerdergenoemde aspecifieke en specifieke (allergische) factoren bestaan er nog vele andere factoren die het uiteindelijke klinische beeld mede bepalen. Enkele daarvan zijn:
seizoensinvloeden. Chronische klachten zoals hoesten en opgeven van sputum verergeren in het najaar. Astma-aanvallen ten gevolge van allergie voor pollen verschijnen vooral in juni. Is een huisstofallergie de oorzaak voor astma, dan verschijnen de aanvallen het meest frequent in september. Dan sterven huisstofmijten namelijk massaal af, maar lozen nog net op het laatste moment hun feces. Omdat de vochtigheidsgraad van de lucht in september groter is, komen deze fecale producten gemakkelijk op inademingniveau;
menstruatie. Heel vaak verergeren astmaklachten net voor de menstruatie;
zwangerschap. Sommige patiënten hebben duidelijk minder klachten in de zwangerschap, andere juist meer;
luchtweginfecties. Ontstekingsreacties maken de luchtwegen, die toch al overgevoelig zijn, nog gevoeliger. Ze kunnen als ‘trigger’ voor het ontstaan van klachten functioneren;
diurnaal ritme (24-uurs-ritme). Men heeft vastgesteld dat de hyperreactiviteit over de gehele dag niet dezelfde is; in de vroege ochtenduren bestaat er een grotere gevoeligheid;
psychische factoren. Deze worden vaak in verband gebracht met de klachten. Ondanks uitgebreid onderzoek heeft men dit echter niet kunnen vaststellen, al lijkt het in individuele gevallen wel aan de orde te zijn;
mate van luchtvervuiling.
7.5.2 Astma bronchiale
Astma bronchiale is een chronische ziekte die bij 5-10% van de Nederlandse bevolking voorkomt; meer bij kinderen en jong-volwassenen, maar toch ook bij ouderen. Astma neemt de laatste tijd toe; er is geen verklaring voor.
Kenmerkend voor astma bronchiale zijn:
het aanvalsgewijs optreden van kortademigheid in rust; de ademfrequentie stijgt daarbij tot meer dan 25/minuut. De pols kan toenemen tot 110/minuut;
vaak kondigt de aanval zich aan met prikkelhoest; ook tijdens de aanval wordt vaak gehoest;
piepen op de borst; zichtbaar bemoeilijkte uitademing. Bij auscultatie is een piepend verlengd expirium te horen. Bij longfunctiemeting is de FEV1 sterk verlaagd;
gebruik van hulpademhalingsspieren (neusvleugelen) ter ondersteuning van de normale ademhalingsspieren;
het ontstaan van een steeds bollere thorax, doordat de lucht er gemakkelijker in gaat dan eruit (zie voor uitleg het boek Pathologie uit de serie Basiswerken); de uitademing wordt niet voltooid omdat tijdens de uitademing het ademcentrum het sein voor inademen alweer heeft gegeven. Het ademcentrum reageert namelijk op de CO2-concentratie in het bloed en deze is verhoogd tijdens een astma-aanval;
opgeven van taai-glazig, soms korrelig, sputum na de aanval;
hypercapnie en hypoxemie (waardoor hypoxie). Gevolg hiervan is een verstoring in het zuur-basenevenwicht (acidose);
dehydratie, ten gevolge van intensief ademhalen.
Tussen de aanvallen door is de patiënt relatief klachtenvrij en is de longfunctie normaal, behalve bij het ziektebeeld dat we (voorheen) astmatische bronchitis noemen, eigenlijk een combinatie van astma en chronische bronchitis (COPD).
Blijft de astma-aanval ondanks therapeutische maatregelen bestaan, dan spreekt men van een status asthmaticus. Deze kan zeer ernstig zijn en tot overlijden aanleiding geven (afb. 7.8).

7.5.3 COPD
Tot de COPD worden gerekend chronische bronchitis en longemfyseem.
Chronische bronchitis
De verschijnselen van een chronische bronchitis bestaan uit het langdurig optreden van hoesten, opgeven van sputum dat meestal grijs-grauwig van aspect is en kortademigheid. De klachten zijn vooral ’s morgens bij het opstaan aanwezig en verergeren vaak gedurende de wintermaanden. Er kunnen vervolgens ook perioden voorkomen waarbij de klachten sterk toenemen, het sputum geelgroenig gaat zien en in hoeveelheid toeneemt. We spreken in dat geval van een ‘sputuminfect’. Komen daar nog koorts, dyspneu d’effort en piepen bij, dan is er sprake van een acute bronchitis. Tijdens deze acute episoden is een duidelijke bronchusobstructie waarneembaar.
Longemfyseem
Bij longemfyseem is de luchthoudendheid van longdelen perifeer van de bronchioli toegenomen (afb. 7.9). Dit gaat gepaard met destructieve veranderingen in de wanden van de alveoli (zie afb. 7.10).
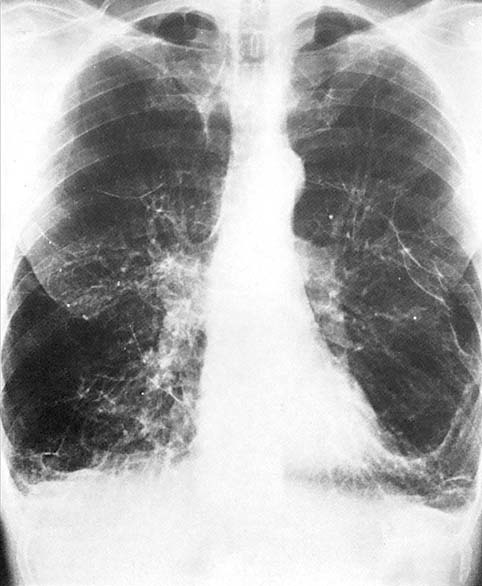

Etiologie en pathogenese
Longemfyseem komt eigenlijk alleen voor op oudere leeftijd. Op enkele uitzonderingen na is tijdens het leven steeds sprake geweest van het langdurig inwerken van irriterende prikkels, waardoor een disbalans is opgetreden tussen stoffen die normaal in de longfysiologie zijn opgenomen, zoals proteases (bevorderen de afbraak van eiwitstructuren) en anti-proteases (remmers van proteases). Dat geldt ook voor oxidanten (vrije radicalen, beschadigen lichaamscellen via oxidatie) en anti-oxidanten (neutraliseren het effect van oxidanten).
Te grote hoeveelheden van proteases en oxidanten (dit is de disbalans) leiden tot afbraak van longweefsel. Oxidanten inactiveren bovendien nog de van nature in de long aanwezige anti-proteases.
Oorzaken van balansverstoringen zijn:
-
roken (of gerookt hebben) van vooral sigaretten. Roken leidt tot ontstekingen in de kleinere luchtwegen, het slijmvlies wordt dikker, het aantal slijmbekercellen en daarmee de slijmproductie neemt toe. Het trilhaarepitheel raakt beschadigd, transformeert naar plaveiselepitheel, de natuurlijke klaring van slijm neemt af, sputum blijft hangen wat weer ontstekingen kan inleiden. Daarin betrokken neutrofielen en macrofagen geven onder andere elastase (een protease wat elastine afbreekt) af, ook komen zuurstofradicalen (oxidanten vrij. Tabaksrook op zich geeft ook een toename van oxidanten in longweefsel.
Nu is het zo dat slechts 15% van de rokers COPD krijgt; blijkbaar zijn nog andere factoren mee bepalend. Deze andere factoren zijn geslacht (mannen blijken gevoeliger), leeftijd, aanwezige bronchiale hyperreactiviteit, luchtverontreiniging, sociaal-economische status, dieet (weinig fruit, veel alcohol), chronische luchtwegaandoeningen als kind, laag geboortegewicht, en waarschijnlijk nog wel andere. Het is niet precies duidelijk/bewezen op welke wijze deze risicofactoren het proces beïnvloeden.
Van passief roken is niet aangetoond dat het aanleiding geeft tot COPD; wel raken luchtwegen geïrriteerd;
andere ziekten van longen en luchtwegen zoals bijvoorbeeld astma, cystic fibrosis (= taaislijmziekte) en bronchiëctasieën (= plaatselijke verwijdingen van de bronchiën);
alfa-1-antitrypsine(anti-protease)deficiëntie. Dit is een genetisch bepaalde aandoening met een sterk verhoogd risico op het ontstaan van longemfyseem. Bij minder dan 1 % van de emfyseempatiënten is dit de oorzaak; zij hebben al op jonge leeftijd klachten.
Het gevolg is dat de long zijn elasticiteit verliest en de alveolaire wanden verdwijnen. Ze worden groter en slapper. Er treedt compressie op van de kleinere luchtwegen, wat vooral merkbaar is tijdens de expiratie. De ventilatie van de longen is verre van ideaal. Het longvaatbed is door verlies van de alveolaire wanden verkleind; ook dit komt de effectiviteit van de respiratie niet ten goede: de ventilatie-perfusieverhouding is verstoord (zie par. 10.1007/978-90-313-7416-8_7#Sec1). Verlies van het longvaatbed zal verhoging van de pulmonale bloeddruk tot gevolg hebben. Dit kan leiden tot een cor pulmonale, zeker als er complicerende factoren aanwezig zijn (bijv. infecties, astmatische kortademigheid).
Symptomen en onderzoek
De belangrijkste klacht bij longemfyseem is het optreden van kortademigheid bij inspanning, vaak met cyanose. Dit is chronisch progressief over de jaren. Hiernaast zijn ook andere respiratoire symptomen aanwezig.
Aan de thorax valt de inspiratiestand op (vat- of tonvormig). De hulpademhalingsspieren zijn vaak sterk aangespannen. De ademhaling is abdominaal: de thorax beweegt in zijn geheel op en neer, bewegingen naar opzij ontbreken. Bij percussie worden laagstaande longgrenzen vastgesteld die bovendien slecht bewegen. De lever is palpabel. Er is een klein hartfiguur omdat er zich longweefsel tussen het hart en de voorste thoraxwand bevindt. Bij auscultatie is heel zacht ademgeruis te horen en een verlengde uitademing. De harttonen zijn zacht. Op de thoraxfoto valt de grote diameter van de thorax op. Het diafragma is sterk afgeplat en de longvelden zijn opvallend helder door de grotere luchthoudendheid van de longen. Bij longfunctiemeting valt een vergrote totale longcapaciteit (TLC) op en een toegenomen residu. De FEV1 is sterk gestoord. De bloedgasanalyse behoeft geen afwijkende uitslagen te geven. Bij de aanwezigheid van complicerende factoren kan heel snel een hypoxemie en hypercapnie ontstaan en acidose dreigen. Vaak hebben longemfyseempatiënten een hoge hemoglobineconcentratie (polycytemie), wat in feite moet worden beschouwd als een fysiologische aanpassing aan een pathologische situatie (zie het boek Pathologie uit de serie Basiswerken).
Vormen van longemfyseem
In de praktijk kennen we een tweetal longemfyseemtypen. De pink puffer imponeert door sterke kortademigheidsklachten, ziet er echter roze uit en heeft geen rechtsdecompensatie. Het andere type is de blue bloater. Deze is veel minder kortademig, maar trekt de aandacht door vrijwel voortdurend kuchen en rochelen. Er zijn bij dit type wel afwijkende bloedgaswaarden en cyanose aanwezig en vaak ook een cor pulmonale. We hebben wel eens gedacht dat de pink puffer harder vecht voor zijn zuurstof, terwijl de blue bloater het wat meer gelaten over zich laat komen. Meer waarschijnlijk is dat het verschil in aspect wordt veroorzaakt doordat een verschillend type emfyseem (pathologisch-anatomisch) aan de orde is. Het merendeel van de longemfyseempatiënten vertoont kenmerken van beide typen.
Complicaties
De meest frequent voorkomende complicaties zijn:
respiratoire insufficiëntie;
cor pulmonale;
pneumothorax (zie par. 7.11);
ribfracturen (de starre thoraxwand kan osteoporose van de ribben tot gevolg hebben, waardoor een gering trauma een rib al doet breken).
7.5.4 Behandeling van astma en COPD
De behandeling is gericht op:
luchtpijpverwijding;
anti-allergische maatregelen;
infectiebestrijding;
mucolyse;
ontstekingsremming;
vermijden van irritantia;
fysiotherapeutische maatregelen;
zuurstoftoediening.
Welke therapeutische maatregelen uiteindelijk van toepassing zijn hangt samen met de ernst en de oorzaak van de huidige klachten (bijv. allergie, infecties).
Luchtpijpverwijding
Middelen die in staat zijn direct luchtpijpverwijding te geven zijn:
bèta-2-sympathicomimetica. Voorbeelden hiervan zijn Ventolin®, Bricanyl® en Berotec®. Als regel geeft men deze middelen per inhalatie: dosisaërosol, poederinhalatie of inhalatie met behulp van een vernevelaar (voorzetkamer). Deze toedieningsvorm heeft het grote voordeel dat het medicament direct op de plek komt waar het moet werken: de luchtwegen. Algemene bijwerkingen blijven uit omdat het medicament niet of nauwelijks in de bloedbaan komt;
-
theofyllinepreparaten. Voorbeelden zijn Theolin Retard®, Theolair Retard® en Pediaphyllin®.
Theofylline werkt effectief; vanwege de smalle therapeutische breedte kan echter vrij snel vergiftiging optreden. De toediening is oraal; aminofylline wordt bij acute benauwdheid per infuus toegediend. Theofyllinepreparaten worden niet vaak meer voorgeschreven, vanwege de goede alternatieven die er zijn;
anticholinergica. Hiermee wordt het effect van de parasympathicus (n. vagus), die tot luchtpijpvernauwing aanleiding geeft, geblokkeerd. De belangrijkste vertegenwoordiger uit deze groep is Atrovent® Spiriva®, dat alleen per inhalatie kan worden toegediend.
Er zijn combinatiepreparaten die zowel bèta-2-sympathicomimetica als anticholinergica bevatten (Berodual®, Combivent®).
Anti-allergische maatregelen
Belangrijk hierbij is dat eventuele allergenen uit de directe omgeving worden verwijderd. Daartoe wordt geadviseerd in ieder geval de slaapkamer te saneren. Soms is het nodig huisdieren weg te doen.
Met een hyposensibilisatiekuur beoogt men via herhaalde intracutane injecties met een zeer lage concentratie van allergenen het lichaam te doen wennen aan dit allergeen, zodat allergische reacties voortaan uitblijven.
Toedienen van medicijnen die het bij allergische reacties vrijkomen van mediatoren voorkomen. Deze middelen moeten van tevoren worden gegeven. Voorbeelden zijn Lomudal® en Tilade®; beide dienen per inhalatie te worden toegediend. Zaditen®, een ander middel, is per os werkzaam. Vooral bij jonge volwassenen zijn deze middelen vaak nodig; bij hen kan de allergische component het ziektebeeld heel sterk bepalen. De middelen blijken tevens goed te werken bij inspanningsastma.
Infectiebestrijding
Het is belangrijk infecties aan longen en luchtwegen bij astma- en COPD-patiënten adequaat te bestrijden; ze doen de symptomen namelijk toenemen. De middelen die worden gebruikt zijn Bactrimel®, Amoxicilline® en Eusaprim® Vibramicin®. Het zijn breedspectrumpreparaten.
Mucolytica
Dit zijn middelen die de slijmproductie en de samenstelling ervan kunnen beïnvloeden. Ze kunnen heel behulpzaam zijn in de behandeling van de klachten. Voorbeelden zijn Bisolvon® en Fluimucil®.
Ontstekingsremming
Meer dan voorheen wordt bij de behandeling de nadruk gelegd op de ontstekingsremming. Dit gebeurt met behulp van corticosteroïden, die in de regel per inhalatie worden toegediend (bijv. Pulmicort®, Becotide®) en dan meestal worden gecombineerd met een luchtpijpverwijdend middel (bijv. Ventolin®). Het effect van corticosteroïden is het afremmen van:
de ontstekingsreacties waardoor de luchtpijpvernauwing afneemt en de hyperreactiviteit vermindert;
de migratie van leukocyten naar het zieke weefsel;
het vrijkomen van mediatoren.
Corticosteroïden helpen zeer effectief, maar geven wel aanleiding tot ernstige bijwerkingen. Bij toediening per inhalatie echter komt weinig van het hormoon in de bloedbaan terecht. Dient men het middel langere tijd per os toe (prednison of prednisolon Celestone®), dan moet zeker met de bijwerkingen worden gerekend. Parenteraal (dexamethason of hydrocortisonacetaat) worden corticosteroïden gegeven als de patiënt er ernstig aan toe is.
Er zijn combinatiepreparaten die zowel corticosteroïden als bèta-2-sympathicomimetica bevatten (Seretide®, Symbicort®).
Vermijden van irritantia
Niet roken hoort hier dus absoluut bij.
Fysiotherapie
Het aanleren van een goede adem- en hoesttechniek (longrevalidatie) is voor iedere patiënt met astma of COPD nuttig, ook ter voorkoming van klachten.
Zuurstoftoediening
Indien zuurstoftoediening nodig is bij bijvoorbeeld een astma-aanval of longemfyseempatiënten, dan moet dit altijd gebeuren op geleide van de bloedgasanalyse (zie par. 7.2.2).
Zelfcontrole
Met behulp van een peakflowmeter thuis kan de patiënt de mate van luchtwegobstructie vaststellen en daarnaar handelen door zelf medicatie aan te passen en/of naar de arts te gaan. Goede instructie hierover is wel noodzakelijk.
7.6 Longembolie en longinfarct
Een longembolie is een ziektebeeld dat ontstaat doordat een bloedstolsel ergens in het lichaam is losgeraakt, is meegevoerd met de bloedstroom naar de longvaten en vervolgens daar in een grotere of kleinere vertakking van de zich steeds verder vertakkende a. pulmonalis komt vast te zitten. Zo’n stolsel dat wordt meegevoerd heet een embolus. Meestal zijn ze afkomstig vanuit het perifere vaatstelsel (beenvenen: vooral de diep veneuze trombose (DVT) staat hier bekend om, en bekkenvenen: na operaties in dat gebied of na een bevalling) of het rechter hart. Soms wordt een dergelijke afsluiting gevolgd door een longinfarct. Dit gebeurt lang niet altijd omdat de long immers nog een andere bloedvoorziening (aa. bronchiales) bezit die de gestoorde zuurstofvoorziening kan compenseren. Is er wel sprake van een infarct, dan treden in het getroffen gebied bloeding en necrose op en zal ook wat bloed worden opgehoest.
7.6.1 Symptomen en onderzoek
Longembolieën komen meestal als ‘tweede ziekte’ voor en worden dan ook vaak in ziekenhuizen gezien. De diagnose is zeker niet altijd gemakkelijk te stellen. Er kunnen namelijk opvallend weinig symptomen aanwezig zijn. Patiënten krijgen ook wel eens de diagnose pneumonie opgeplakt omdat het beeld hier soms verrassend op kan lijken. Met grote regelmaat worden ook bij obducties longembolieën geconstateerd waarvan men van tevoren niet op de hoogte was.
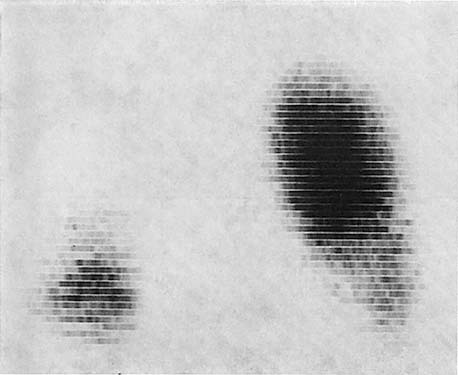
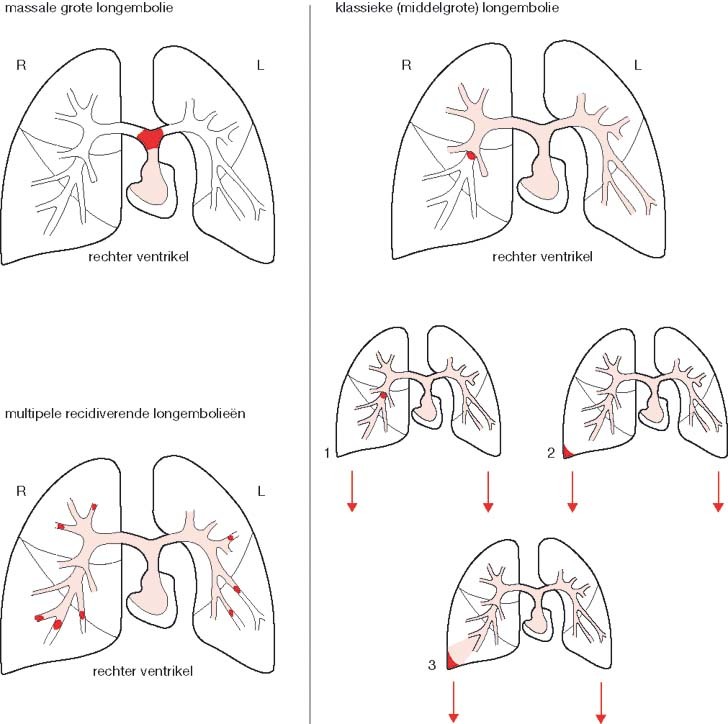
Toch blijkt het mogelijk de longembolieën op grond van grootte en klinische verschijnselen onder te verdelen in drie typen:
de massale grote longembolus;
de klassieke (middelgrote) longembolus;
de multipele recidiverende longembolieën.
Bij de massale grote longembolus is er sprake van een plotselinge afsluiting van een of beide hoofdtakken van de a. pulmonalis. Er ontstaan een sterke dyspneu en cyanose. Een acute rechtsdecompensatie volgt met daarbij een ernstige forward failure, waardoor shock en overlijden binnen enkele minuten volgt. De patiënt is zeer angstig.
Bij de klassieke longembolus is er een afsluiting van een of beide zijtakken van de a pulmonalis. Vaak is de patiënt van tevoren onrustig en angstig, zeker ook op het moment zelf. Hij voelt zich plotseling onwel; er is pijn in de aangedane zijde die toeneemt met de ademhaling. De zieke thoraxhelft beweegt minder. Temperatuurverhoging (subfebriel) en een tachycardie begeleiden het beeld. Het rechter hart kan tekenen van overbelasting vertonen. Soms is de diagnose niet zo duidelijk; dan kan een perfusiescan (zie 7.3.3.) hulp bieden. Bij een negatieve uitslag van dit onderzoek kan met zekerheid worden gezegd dat er geen sprake is van een longembolie. Wordt wel een ‘lege’ plek vastgesteld, dan kan dit op een embolie wijzen. Andere aandoeningen die dit ook kunnen veroorzaken moeten dan echter wel eerst worden uitgesloten. Een CT-scan of multislice-CT-scan kan eveneens behulpzaam zijn in de diagnostiek van de embolie. Een thoraxfoto levert weinig informatie: er is pas iets te zien als in het aangedane gebied de ontstekingsreactie op gang is gekomen (pas na 24 uur). Toch kan soms een afgesloten bloedvat worden waargenomen; bloed en stolsel zijn namelijk contrastrijk voor röntgenstralen.
Bepaling van D-dimeer in het bloed kan helpen uit te sluiten dat er sprake is van een trombo-embolisch proces. D-dimeer is een afbraakproduct van fibrine dat bij fibrinolyse vrijkomt. Bij een trombo-embolisch proces is altijd sprake van (fysiologische) fibrinolyse.
Bij twijfel aan de diagnose zal men alvast gaan behandelen alsof er een longembolie bestaat, om de behandeling later, wanneer het geen embolie blijkt te zijn, aan te passen aan de nieuwe diagnose.
Bij multipele recidiverende longembolieën is er sprake van met regelmaat ‘schieten’ van kleine embolietjes. Dit gebeurt symptoomloos. Op den duur echter ontwikkelt zich in toenemende mate kortademigheid; er ontstaat pulmonale hypertensie met een chronische overbelasting van het rechter hart omdat het pulmonale vaatbed sterk verkleind raakt. Aangezien dergelijke multipele longembolieën voornamelijk bij ouderen voorkomen, wordt een slecht hart vaak als oorzaak voor de aanwezige klachten gezien, wat het dus niet is. Perifere trombosevorming is meestal bij deze groep patiënten niet aantoonbaar. Een goede sluitende verklaring voor het ziektebeeld in zijn geheel is er tot nu toe niet (afb. 7.11 en 7.12).
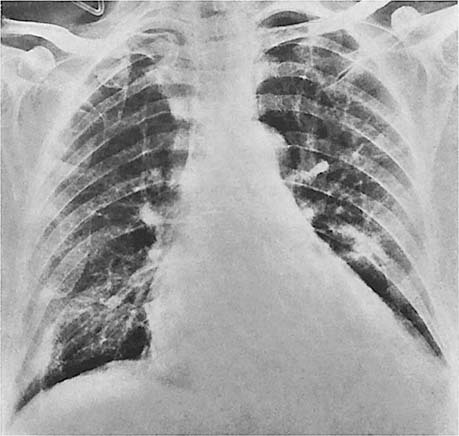
7.6.2 Behandeling
De therapie hangt af van de grootte van de longembolie en de ernst van het klinische beeld. Bij alle vormen wordt antistollingstherapie in de vorm van intraveneus toegediend heparine toegepast, waarbij na enkele dagen overgegaan wordt op orale middelen zoals coumarinederivaten (acenocoumarol, Marcoumar®, Warfarine). Deze antistolling is profylactisch bedoeld ter voorkoming van nieuwe trombusvorming.
Fibrinolytica zoals urokinase en streptokinase worden alleen bij levensbedreigende situaties toegepast. Met deze middelen lukt het soms pasgevormde stolsels op te lossen. Gezien de forse bijwerkingen worden ze zeker niet bij iedere patiënt met longembolie toegepast. Bij een deel van de patiënten treedt een spontane fibrinolyse op, waarna zich de lokale bloedvoorziening herstelt.
Bij de meeste patiënten blijft het stolsel zitten: vanuit de omgeving groeien bloedvaten en bindweefsel naar binnen en het bloedvat is blijvend afgesloten.
Bij een massale embolus is chirurgisch ingrijpen noodzakelijk.
7.7 Longcarcinoom
Longkanker is de meest voorkomende kanker in Nederland. Het betreft vrijwel altijd een bronchuscarcinoom en komt bij zowel mannen als vrouwen voor. Het vroeger aanwezige verschil in voorkomen tussen mannen en vrouwen, wat toegeschreven werd aan de slechtere rookgewoonten bij mannen, is inmiddels bezig te verdwijnen. Bij vrouwen staat longkanker nu op de derde plaats van de bij hen voorkomende typen kanker, na borstkanker en coloncarcinoom.
De leeftijd waarop longkanker zich meestal manifesteert ligt tussen de 60 en 75 jaar, maar dat wil niet zeggen dat longkanker niet op jongere leeftijd zou kunnen voorkomen. Longkanker heeft als regel een slechte prognose. De 5-jaarsoverleving is 0-10%, afhankelijk van het type longkanker.
7.7.1 Oorzaken
Er bestaat een duidelijk verband tussen het ontstaan van longkanker en roken. Polycyclische koolwaterstoffen (dus niet de nicotine) zoals die vooral in sigarettenrook voorkomen, vormen de carcinogene stoffen. Naast roken (polycyclische koolwaterstoffen: teer/sigaretten), wat overigens verreweg de belangrijkste oorzaak is, zijn er nog andere factoren die kunnen bijdragen tot het ontstaan van longkanker. Hiertoe horen:
luchtverontreiniging (bijv. stikstofoxide);
beroepsfactoren. In de industrie werken met zware metalen of asbest levert een verhoogd risico op longkanker;
andere longaandoeningen. Sommige daarvan geven een verhoogde kans op longkanker. We kennen dit bij longfibrose, littekens in de longen en COPD;
verminderd functioneren van de afweer. Beschadigingen opgelopen aan het immuunapparaat zullen ook de weerstand tegen kanker verminderen. De weerstand kan ook door een slechte voedingstoestand, waaronder vitaminegebrek, verminderen.
7.7.2 Typen
Histologisch wordt onderscheid gemaakt in verschillende typen longkanker.
Niet-kleincellige carcinomen (non–small cell lung cancer, NSCLC)
Planocellulair (plaveiselcel)carcinoom
Dit ontstaat in luchtwegepitheel dat eerst metaplastisch verandert, dat wil zeggen dat het trilhaarepitheel overgaat in plaveiselepitheel. Zoiets kan bij chronische irritatie gebeuren. Dit type longkanker heeft ook een sterke correlatie met roken. De tumor bevindt zich als regel centraal in de long, dat wil zeggen in de buurt van de hilus. Deze lokalisatie verslechtert de prognose. De tumor breidt zich gelijkmatig naar de omgeving uit en daarbij wordt nogal eens een bronchus afgesloten, wat weer leidt tot een obstructiepneumonie. Dit kan overigens ook het eerste ‘symptoom’ zijn. Het carcinoom komt vooral bij mannen voor (afb. 7.13).

Adenocarcinoom
Deze kankervorm is meestal in de longperiferie gelokaliseerd en wordt daardoor vrij laat ontdekt. Klachten van metastasen zijn vaak de eerste verschijnselen die optreden. Dit carcinoom komt in verhouding vaker bij vrouwen voor. Het bronchio-alveolaire carcinoom is een voorbeeld ervan. Deze tumor kan op verschillende plaatsen in de long tegelijkertijd voorkomen en ook interstitieel uitgroeien. Daardoor kan toenemende kortademigheid aanwezig zijn, zelfs hypoxie en hypercapnie. Soms ontstaat bronchorrhoea.
Grootcellige bronchuscarcinoom
Deze komen het vaakst voor: ongeveer 70% van alle longkankers hoort hiertoe (afb. 7.14).

Kleincellige carcinomen (small cell lung cancer, SCLC)
Het kleincellige carcinoom (oatcell-carcinoma) betreft ongeveer 20% van alle longkankers. De tumor kan zowel perifeer als centraal in de long gelokaliseerd zijn. Het groeit snel en metastaseert vroeg, redenen waarom de prognose slecht is. Men heeft de indruk dat dit type vaker bij jongere patiënten voorkomt. Er is een duidelijke correlatie met roken.
7.7.3 Symptomen
In een klein percentage wordt longkanker ontdekt op de thoraxfoto, die vaak om andere redenen is genomen. Meestal zijn dan nog geen klachten aanwezig en is er nog sprake van een vroeg stadium, waarbij soms curatieve behandeling mogelijk is. Je mag van geluk spreken als longkanker in zo’n vroeg stadium wordt vastgesteld. In verreweg de meeste gevallen zijn er symptomen en is men feitelijk te laat voor een curatieve behandeling. Longkanker kan lange tijd uitgroeien in het luchthoudende orgaan zonder veel weefsels te verstoren waardoor klachten ontstaan. Vooral als de tumor perifeer in de long is gelokaliseerd, ontstaan de klachten laat.
Zoals bij iedere patiënt met een maligne aandoening zal ook bij de patiënt met longkanker algemene malaise, anorexie en vermagering aanwezig zijn. Daarnaast zijn specifieke symptomen aanwezig, veroorzaakt door de tumorgroei zelf. Deze symptomen kunnen worden ingedeeld in twee groepen:
intrathoracale uitbreiding van het carcinoom;
extrathoracale uitbreiding van het carcinoom.
Bij intrathoracale uitbreiding gaat het om lokale uitgroei van de tumor en de vorming van metastasen in de thorax. Het kan gepaard gaan met:
prikkelhoest die niet of nauwelijks reageert op therapie. Is de patiënt een chronisch hoester dan valt op dat het hoesten van karakter verandert;
ophoesten van bloed bij het sputum;
obstructiepneumonie. De tumor sluit een bronchustak af waardoor zich atelectase en een pneumonie ontwikkelen;
-
heesheid door een verlamming van een van de stembanden. De innerverende zenuw (nervus laryngeus recurrens = stembandzenuw) verloopt in de hals en daalt, alvorens te eindigen in de stembanden, eerst af tot in de thorax. Met name de linker stembandzenuw verloopt door de top van de linkerlong en kan daar beschadigd worden door ingroei van tumorweefsel.
NB. Bij een stembandverlamming zal het hoesten ook minder effectief worden;
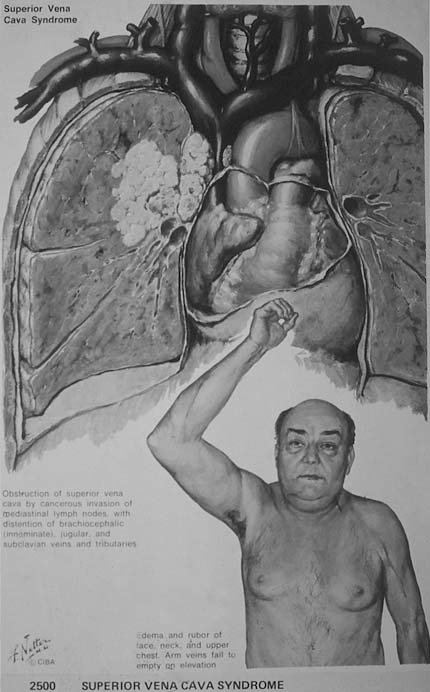
venacavasuperiorsyndroom. Tumorweefsel groeit door in de vena cava superior en vernauwt daardoor de diameter ervan. Het bloed raakt gestuwd en er treedt zwelling op aan hoofd, hals en armen. Voor de patiënt is dit heel onaangenaam (afb. 7.15);
slikklachten door doorgroei in de oesofagus;
eenzijdige diafragmaparalyse door ingroei in de verzorgende zenuw. Op de thoraxfoto en bij doorlichting is dit waar te nemen. Er is hoogstand van de aangedane diafragmahelft;
pleuritis carcinomatosa. Er zal dan sprake zijn van ‘vocht achter de longen’ omdat de pleura geprikkeld wordt tot extra vochtvorming;
intrathoracale pijn. Meestal een laat symptoom. Kan bij doorgroei in het mediastinum en bij lokalisatie in de grotere bronchi of pleurae aanwezig zijn;
dyspneu. Kan ontstaan als grotere bronchi worden afgesloten of als er sprake is van diffuse interstitiële doorgroei;
pancoast-syndroom. Tumorweefsel dat aanwezig is in de thoraxapertuur groeit door in de plexus brachialis. Pijn in de schouder en de arm verschijnt, met vaak een atrofie van de armmusculatuur.
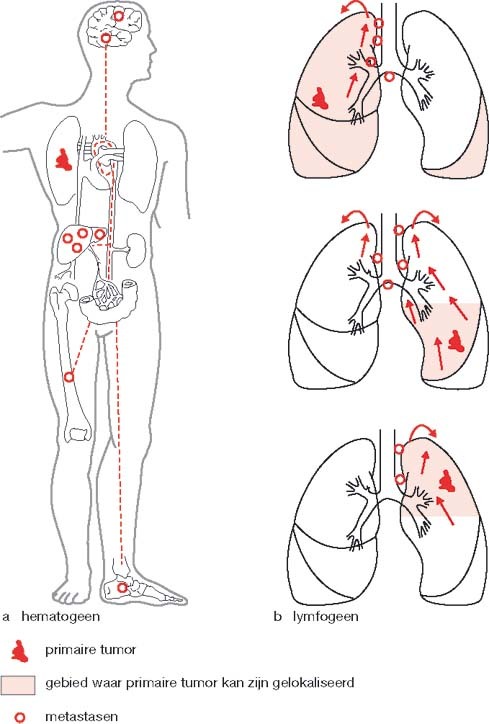
Bij extrathoracale uitbreiding gaat het om metastasering buiten de thorax (afb. 7.16). Dit kan via lymfogene en hematogene weg geschieden. Lymfogeen metastaseert longkanker het eerst naar de hilus, vandaar naar het mediastinum, de carina en de trachea (alle nog steeds intrathoracaal, eventuele symptomen ervan zijn hiervoor reeds vermeld). Van de trachea vindt uiteindelijk een verplaatsing plaats naar de supraclaviculaire lymfklieren en zo verderop. Hematogeen vindt metastasering plaats volgens het zogenaamde vena pulmonalistype en kunnen metastasen in principe overal in het lichaam uitgroeien. In de praktijk zijn ze echter vooral te vinden in hersenen, bot en lever. Hersenmetastasen kunnen aanleiding geven tot halfzijdige verlamming. Soms is zo’n verlamming het eerste verschijnsel van de aanwezige longkanker.
Metastasen in de botten geven aanleiding tot ernstige pijnen, die het klinische beeld eveneens kunnen beheersen.
7.7.4 Onderzoek
Lichamelijk onderzoek levert als regel merkwaardig weinig op. Voor de afronding van de diagnostiek van de primaire tumor alsmede aanwezige metastasen en het vaststellen van het stadium binnen de TNM-classificatie, zijn we dan ook aangewezen op aanvullende onderzoeksmethoden:
routine-laboratoriumonderzoek zoals bloedonderzoek naar leverfuncties;
- specifieke technieken. Tot deze laatste categorie horen:
- röntgendiagnostische technieken (thoraxfoto, planigrafie, bronchografie, angiografie en CT-scan);
- endoscopische ultrasonografie (echoscopie) via slokdarm of luchtpijp met de mogelijkheid om naaldpunctie van klieren in het mediastinum te doen;
- magnetic resonance imaging (MRI);
- scintigrafie (botscan);
- bronchoscopie gecombineerd met een biopt (transbronchiaal);
- cytologisch onderzoek van sputum (papanicolaou-methode).
7.7.5 Behandeling
Aan de hand van het TNM-classificatiesysteem en de daaraan verbonden beslisboom wordt besloten tot de meest geschikte behandeling. De mogelijkheden zijn:
operatie, met als doel de primaire tumor en de regionale metastasen te verwijderen. Deze behandeling is curatief bedoeld;
bestraling, wordt meestal niet als curatieve maatregel gezien. Men gebruikt het in palliatieve zin als de tumorgroei in het lichaam aanleiding heeft gegeven tot klachten zoals pijn bij botmetastasen en stuwing bij het venacavasuperiorsyndroom. Een enkele keer, wanneer er contra-indicaties voor een operatieve ingreep bestaan, bijvoorbeeld bij een slechte longfunctie, probeert men met bestraling toch curatief te zijn. Soms wordt bestraling gebruikt als voorbehandeling voor de operatie;
chemotherapie, de ervaringen hiermee zijn teleurstellend. Soms is er primair wel een goede reactie, maar die is zelden blijvend. Gecombineerd met een andere vorm van behandeling wordt het toch vaak toegepast;
- andere palliatieve maatregelen:
- laserbehandeling, waarmee lokaal tumorweefsel kan worden verwijderd. Soms vormt fotodynamische therapie hierin ondersteuning;
- plaatsen van stents: de cava stent bij het vena-cava-superiorsyndroom of een stent in de trachea als deze dreigt dicht te groeien. Intraluminale radiotherapie (=brachytherapie) is een andere mogelijkheid de luchtweg te openen.
Hiernaast zal symptoombestrijding een plaats hebben; daarbij moet vooral gedacht worden aan een adequate en afdoende pijnstilling.
7.8 Sarcoïdose
Sarcoïdose , ook wel de ziekte van Besnier-Boeck (Heerfordt-Schaumann) genoemd, is een aandoening die zich in vele organen en weefsels kan manifesteren. Bijna altijd zijn de longen aangedaan. We weten niet precies hoe de ziekte ontstaat. Inmiddels is echter wel komen vast te staan dat de T-helper-cellen (TH-cellen) bij deze personen extra actief zijn tegen stoffen die deze cellen triggeren. Dit kunnen stoffen zijn die van buiten komen (virussen, bacteriën, toxische stoffen, enz.), of het zijn lichaamseigen stoffen. Dat ze zo overdreven reageren zou verankerd liggen in hun DNA-structuur. Anderzijds kan ook worden gedacht aan de mogelijkheid dat binnen de T-celpopulatie onvoldoende suppressie (=afremming) van TH-cellen is georganiseerd. Gewoonlijk zijn in dit systeem activering en afstemming goed op elkaar afgesteld.
De verhoogde T-celactiviteit heeft een reeks reacties tot gevolg die, wat betreft de longen, inhouden: het zich ontwikkelen van granulomen, het ontstaan van alveolitis en op den duur bindweefselvorming (fibrosering). De aandoening komt vooral voor tussen het dertigste en het vijftigste levensjaar, blijkt geografisch bepaald te zijn en is mogelijk rasgebonden.
7.8.1 Symptomen
De symptomen zijn veelal niet specifiek. Ze bestaan uit malaise, moeheid, lusteloosheid, gewichtsverlies en koorts. Bij uitbreiding in de longen treedt kortademigheid op en kan prikkelhoest verschijnen. Huidafwijkingen, visusstoornissen en vergrote niet-pijnlijke lymfeklieren in liezen, oksels en dergelijke kunnen tegelijkertijd aanwezig zijn.
7.8.2 Onderzoek
Vaak worden de afwijkingen in de longen bij toeval ontdekt op een thoraxfoto. Vergrote lymfklieren in beide longhili zijn (zeer) verdacht voor sarcoïdose. Verder kunnen de longen op de foto een vlekkige/streperige tekening vertonen door de aanwezige granulomen, alveolitis en eventuele fibrosering. De CT-scan kan dit nog duidelijker in beeld brengen. Aangezien grote lymfklieren in de longhili ook kunnen voorkomen bij de ziekte van Hodgkin en het maligne granuloom, moet je zeker weten inderdaad te maken te hebben met een sarcoïdose. Daarom moet de diagnose worden bevestigd door histologisch onderzoek, dat in de praktijk meestal gebeurt bij weefsel dat verkregen is door middel van een transbronchiale biopsie. Bij dit microscopisch onderzoek zijn reuzencellengranulomen zichtbaar. Met behulp van longfunctieonderzoek is een verminderde soepelheid van de longen vast te stellen. Als uiting van het actief zijn van het proces zijn angiotensine converting enzyme (ACE) en interleukine-2-receptoreiwit (SIL-2R) in het bloed verhoogd aanwezig; dit kan worden bepaald.
7.8.3 Behandeling
Een behandeling is meestal niet nodig. De ziekte geneest in de regel spontaan. In een actief stadium waarbij verergering dreigt, worden corticosteroïden gegeven in een vrij forse dosering (bijv. 40 mg per dag). Daarmee wordt dan geprobeerd de weefselreacties af te remmen. De behandeling moet zeker enkele maanden worden volgehouden. De thoraxfoto en het longfunctieonderzoek, maar ook ACE- en SIL-2R metingen in het bloed, worden gebruikt om het effect van de behandeling te controleren.
7.9 Bronchiëctasieën
Onder bronchiëctasieën verstaan we plaatselijke verwijdingen van bronchiën. Deze kunnen over een bepaalde afstand gelijkmatig zijn verwijd (cilindrisch), grillig van model zijn en dan in het verloop meer lijken op spataderen (variceus) of eruitzien als ballonnetjes (sacculair). Meestal zitten ze in de middelgrote bronchiën; alleen de sacculaire zitten meer aan de uiteinden van de luchtpijptakken. Bronchiëctasieën kunnen lokaal, maar ook verspreid op verschillende plaatsen voorkomen.
7.9.1 Oorzaken
Bronchiëctasieën zijn meestal het gevolg van herhaald optredende infecties aan de luchtwegen en longen, zoals dat kan voorkomen bij COPD en zeker ook bij patiënten met cystic fibrosis (taaislijmziekte). Afhankelijk van de oorzaak zijn deze ectasieën in beide longen te vinden. Soms zijn bronchiëctasieën aangeboren, een ‘weeffout’ kan men zeggen. Lokale bronchiëctasieën kunnen het gevolg zijn van ter plekke doorgemaakte ziekteprocessen. Zo kennen we in de longtoppen ectasieën als gevolg van tuberculose en in de rechter middenkwab als gevolg van aspiratie van een corpus alienum.
7.9.2 Symptomen
Een patiënt met bronchiëctasieën zal veel hoesten en daarbij aanzienlijke hoeveelheden vies sputum ophoesten. De luchtwegen zijn in feite altijd chronisch geïnfecteerd. Het slijm en de ontstekingsproducten blijven gemakkelijk hangen in de lokale verwijdingen, omdat trilhaartransport daar ontbreekt, wat weer opnieuw ontstekingen bevordert. Frequent begeleiden bronchopneumonieën het ziektebeeld. Gemakkelijk verschijnt ook bloed bij het sputum; in het ernstigste geval kan dit een levensbedreigende hemoptoë zijn.
7.9.3 Onderzoek
De diagnose wordt gesteld met behulp van de CT-scan en/of bronchografie. Uit het sputum zijn vele micro-organismen te kweken (o.a. de pneumokok en de H. influenzae), die vaak vaste bewoners zijn van de ectasieën (kolonisatie).
7.9.4 Behandeling
De behandeling bestaat uit het stimuleren van het ophoesten van het sputum, waarbij de fysiotherapeut ondersteunend kan zijn. Complicerende bronchopneumonieën moeten effectief worden bestreden. Tegen de pneumokok en de H. influenzae kan worden gevaccineerd. Als lokale bronchiëctasieën tot problemen leiden en bij het optreden van ernstige bloedingen kan tot chirurgische behandeling worden besloten.
7.10 Pleura-aandoeningen
7.10.1 Hydrothorax
Onder hydrothorax wordt verstaan de aanwezigheid van een meer dan normale hoeveelheid vocht in de pleuraholte. Onder normale omstandigheden produceren de pleurabladen een geringe hoeveelheid vocht dat ervoor moet zorgen dat de weivliezen wrijvingsloos over elkaar bewegen. Resorptie van dit vocht staat normaal in evenwicht met de productie ervan.
Oorzaken
Een teveel aan vocht in de pleuraholte kan verschillende oorzaken hebben. Ook de samenstelling van dit vocht kan wisselend zijn, wat weer met de oorzaken te maken heeft. Zo kennen we het transsudaat en het exsudaat. Het transsudaat heeft een helder, lichtroze aspect. Het verschijnt in de pleuraholte door uittreding van vocht vanuit de begrenzende bloed-lymfcapillairen. De oorzaak is veelal stuwing in het afvoergebied van deze capillairen zoals dat kan optreden bij decompensatio cordis en ingroei van tumorweefsel in lymfklieren. Ook bij hypoproteïnemie treedt een transsudaat op.
Een exsudaat is lichtgeel van aspect en veelal iets troebel van aard. Dit laatste is het gevolg van een aanwezigheid van ontstekingsproducten zoals leukocyten. Het exsudaat treedt op bij ontstekingen aan de pleurae en bij tumorgroei (metastasen!) in de pleurabladen.
Symptomen
Alleen bij veel vocht ‘achter de longen’ treden kortademigheidsklachten op. Prikkelhoest kan eveneens aanwezig zijn.
Onderzoek
Soms is het mogelijk met behulp van percussie van de thorax de hydrothorax vast te stellen. De thoraxfoto is onmisbaar voor de bevestiging van de diagnose. Je kunt er vloeistofspiegels in de pleuraholten op waarnemen. Een pleurapunctie is nodig om achter de samenstelling van het vocht te komen, wat ook weer bijdraagt tot de diagnostiek van de oorzaak van hydrothorax.
Behandeling
De behandeling bestaat uit het bestrijden van de oorzaak van de hydrothorax. Dit is of wordt bij de desbetreffende ziektebeelden behandeld. Soms moet vocht worden weggepuncteerd.
7.10.2 Pleuritis
Een ontsteking van de pleurae wordt pleuritis genoemd. Er kan sprake zijn van een droge pleuritis (pleuritis sicca of ook wel pleuraprikkeling genoemd) zonder vochtophoping in de pleuraholte, en van een natte pleuritis (pleuritis exsudativa) met extra vocht in de pleuraholte.
Oorzaken
Oorzaken zijn:
bacterieel (als regel afkomstig uit ontstekingen in aan de pleura grenzende structuren zoals een pneumonie);
viraal (meestal betreft het een zelfstandige pleuritis zoals de ziekte van Bornholm);
longinfarct (zie par. 7.6);
tumorgroei, waarbij het vaak gaat om metastasen van tumoren elders in het lichaam. Ook doorgroei van tumoren vanuit aangrenzende structuren kan aanleiding geven tot een pleuritis carcinomatosa (zie par. 7.7.3);
Symptomen
Een droge pleuritis kenmerkt zich door pijn in de zij, vastzittend aan de ademhaling, wat wordt veroorzaakt door het bewegen van de ruwe (ontstoken) pleurabladen langs elkaar. Soms gaat het gepaard met pleurawrijven (voel- of hoorbaar). Een natte pleuritis kent de symptomen pijn en pleurawrijven juist niet, aangezien het vocht ervoor zorgt dat de pleurabladen elkaar niet raken. Bij deze patiënten staat kortademigheid op de voorgrond. Prikkelhoest kan tevens aanwezig zijn. Naast deze verschijnselen zijn uiteraard symptomen aanwezig die afkomstig zijn van de aandoening die aanleiding geeft tot het ontstaan van pleuritis.
Onderzoek
Voor de diagnose is een thoraxfoto belangrijk. Vooral onderzoek van het pleuravocht draagt bij tot de vaststelling van het betrokken micro-organisme.
Behandeling
De behandeling van een pleuritis bestaat in de eerste plaats uit het behandelen van de veroorzakende aandoening. Antibiotica zijn hierbij als regel onmisbaar, ook als het gaat om de behandeling van de pleuritis zelf. Pleurapuncties worden ook als therapeutische maatregel uitgevoerd, ter ontlasting als er veel exsudaat in de pleuraholte aanwezig is.
Pus moet te allen tijde verwijderd worden. Indien dit wordt verwijderd, stuit men echter op het probleem dat na een keer aanprikken in de pus de stolling in gang wordt gezet omdat tijdens de punctie weefselfactoren worden toegevoegd. Hierdoor weven zich fibrinedraden door de pusmassa en kan bij een eventuele latere keer de pus niet opnieuw gepuncteerd worden: het zit vast. Daarom wordt bij de eerste keer aanprikken elease of fibrinolysine toegevoegd; stolling wordt hierdoor voorkomen.
Een empyeem (zie hierna) moet worden gedraineerd, met daarnaast lokale en algemene ondersteuning van een gericht antimicrobieel middel.
Complicaties
Bij pleuritis kan het exsudaat overgaan in pus, waarna zich een pleura-empyeem ontwikkelt. De patiënt met zo’n empyeem is ernstig ziek en vertoont koude rillingen en nachtzweten. Er is pijn in de thorax, en dyspneu en prikkelhoest begeleiden het beeld. Bij een empyeem is in de meeste gevallen S. aureus betrokken.
7.10.3 Pleuratumoren
We kennen primaire en secundaire tumoren van de pleura.
Primaire tumoren
Een voorbeeld hiervan is het mesothelioom. Deze tumor kan solitair en multipel aanwezig zijn en is nogal kwaadaardig. Bij het ontstaan speelt waarschijnlijk asbestexpositie een rol.
De symptomen bestaan uit algehele malaise, gewichtsverlies, pijn in de thorax en kortademigheid.
Het onderzoek omvat onder andere een thoraxfoto waarop ronde schaduwen zichtbaar zijn, vaak op meer plaatsen. Met behulp van thoracoscopie wordt een biopsie genomen, waarna histologisch onderzoek de vermoedelijke diagnose kan bevestigen.
Het mesothelioom probeert men te behandelen met radiotherapie en lokale toediening van cytostatica. Een regelmatige pleurapunctie is noodzakelijk om vocht uit de pleuraholte te verwijderen.
Secundaire tumoren
Dit zijn de metastatische tumoren (pleuritis carcinomatosa). Vooral het mamma-, het bronchus- en het ovariumcarcinoom, evenals de maligne lymfomen, geven aanleiding tot pleurametastasen.
Het belangrijkste symptoom is dyspneu, vooral ten gevolge van de hydrothorax. Daarnaast komt soms prikkelhoest voor.
De behandeling bestaat uit het regelmatig uitvoeren van een pleurapunctie indien er veel vocht zit in de pleuraholte. De dyspneu kan na zo’n punctie duidelijk verminderen. Daarnaast kunnen cytostatica worden achtergelaten in de pleuraholte.
7.10.4 Hematothorax
Hematothorax betekent de aanwezigheid van bloed in de pleuraholte. Meestal is een thoraxtrauma de oorzaak. Daarnaast kan het als complicatie aanwezig zijn bij een spontane pneumothorax, een longinfarct of pleurametastasen. Een enkele maal treedt een bloeding op na een medische ingreep in de thoraxholte: dat dreigt vooral bij gebruikers van antistollingstherapie.
De klachten bestaan uit dyspneu en hoesten. Een grote bloeding kan gepaard gaan met shockverschijnselen.
De behandeling bestaat uit het zo goed mogelijk verwijderen van het bloed uit de pleuraholte. Gebeurt dit niet, dan zal verbindweefseling van de pleuraholte optreden. Bij grote bloedingen zal de chirurg een thoracotomie moeten verrichten teneinde de bloeding te stelpen.
7.11 Pneumothorax (klaplong)
Bij een pneumothorax (afb. 7.17) is er lucht aanwezig in de pleuraholte (pneu = lucht). Gewoonlijk zitten de pleurabladen dicht tegen elkaar aan en is er geen lucht in de pleuraholte, alleen een beetje vocht om tijdens het ademhalen het bewegen van de pleurae ten opzichte van elkaar te vergemakkelijken. De long blijft tijdens de adembewegingen tegen de borstwand aangezogen.

In de thoraxholte heerst normaal een negatieve druk. Als deze wegvalt, en dat gebeurt bij een pneumothorax, valt de long samen. De mate waarin dat gebeurt kan verschillen en hangt samen met de oorzaak.
7.11.1 Vormen
De pneumothorax kan verschillende oorzaken hebben. Vooral op grond daarvan onderscheiden we verschillende vormen:
Spontane (primaire) pneumothorax
Deze ontstaat geheel onverwachts. De oorzaak is niet duidelijk (= idiopathisch). Men denkt wel aan een toegenomen druk in de longblaasjes door vernauwing van de kleinere luchtwegen, als gevolg van ter plekke aanwezige ontstekingen. Tijdens de inspiratie worden de alveoli dan voldoende geventileerd, maar de uitademing is gedeeltelijk belemmerd (smoorklepfenomeen). Daardoor raken de alveoli steeds voller. Mocht zich dan een luchtdrukdaling (duikers, vliegers) voordoen, dan zetten de longblaasjes nog eens extra uit. Er ontstaat door de spanning een gat in de alveoluswand waardoor lucht in de viscerale pleura ontsnapt. De blaasjes die hierdoor ontstaan worden blebs genoemd. Knappen deze, dan ontstaat de pneumothorax.
Verder is opgevallen dat:
een primaire pneumothorax bij rokers tienmaal vaker voorkomt. Bij hen blijken inderdaad ontstekingen in de kleinste luchtwegen aanwezig. Het zou kunnen dat om dezelfde redenen luchtverontreiniging, allergieën et cetera tot een pneumothorax kunnen leiden, maar bewezen is dit niet;
de primaire pneumothorax vooral voorkomt tussen de 15-40 jaar (piek tussen 20-25 jaar);
het vooral mannen met een leptosome lichaamsbouw (lang en mager) betreft. Bij hen worden in 80% van de gevallen blebs, maar ook bullae (aaneengesloten alveoli door wegvallen van de tussenschotten) gevonden en wel in de longtop, waar de drukverhoudingen het ontstaan ervan begunstigen. Deze afwijkingen zijn op de thoraxfoto niet echt zichtbaar; zij kunnen wel met behulp van thoracoscopie worden vastgesteld;
er soms een erfelijke predispositie aanwezig lijkt;
het ontstaan geen verband houdt met lichamelijke inspanning. Dit dacht men oorspronkelijk wel; meestal is de persoon in rust.
Spontane (secundaire) pneumothorax
Deze is het gevolg van reeds aanwezige longaandoeningen, zoals COPD (met name longemfyseem), astma, longfibrose, maligniteiten, opportune longinfecties (zoals Pneumocytic carinii) en andere. Directe aanleidingen zijn de door de ziektes aanwezige bullae en blebs, ontstekingen en veranderingen in anatomische structuren die tot andere krachtverhoudingen leiden.
Traumatische pneumothorax
Directe zowel als indirecte traumata kunnen een pneumothorax tot gevolg hebben. Als daarbij tevens bloedvaten kapot gegaan zijn, is tegelijkertijd een hematothorax aanwezig.
Ook medisch handelen (bijv. thoracoscopie of zuigdrainage) kan aanleiding zijn geweest, evenals luchtdrukwisselingen.
Spanningspneumothorax
Als tijdens de inademing lucht door het gat kan passeren maar tijdens de uitademing niet kan ontsnappen, ontstaat een hoge intrapleurale (intrathoracale) druk. Als dat zo is, wordt niet alleen de ademhaling maar ook de circulatie belemmerd. Terugvloed van aderlijk bloed naar het hart raakt geblokkeerd en daarmee de cardiale output: er ontstaat acuut hartfalen. De situatie is levensbedreigend.
7.11.2 Symptomen
Een pneumothorax kan symptoomloos verlopen als er maar weinig lucht in de pleuraholte is binnengekomen. Het gat dicht zich spontaan en herstel volgt.
Is de pneumothorax van enige omvang, dan geeft dit vrijwel altijd aanleiding tot verschijnselen, zoals:
acute stekende pijn in de zij en soms ook in de schouder door prikkeling van de nervus phrenicus: de zenuw die het middenrif innerveert (referred pain). De pijn verandert na enige tijd van karakter, wordt continu en vervaagt;
dyspnoe; de ernst ervan hangt samen met de grootte van de pneumothorax. Deze dyspnoe verdwijnt geleidelijk aan over de eerste 24 uur.
Het afnemen van pijn en dyspnoe kan de suggestie geven dat het niet zo ernstig is, waardoor wordt afgezien van bezoek aan de arts.
Andere verschijnselen die mogelijk zijn:
cyanose en syndroom van Horner (afhangend ooglid), ten gevolge van tractie aan de grensstreng door beweging van het mediastinum;
droge hoest, orthopnoe en hemoptoë;
tachycardie en tachypnoe;
asymmetrie van de thorax; de adembewegingen zijn minder aan de aangedane kant. Bovendien tekenen de ribben zich niet af omdat door het wegvallen van de negatieve druk de tussenribspieren niet naar binnen worden getrokken. Dit, en de hogere druk in de pleuraholte, zorgen ervoor dat de borstkas iets bol staat. Bij auscultatie is er geen ademgeruis te horen;
- bij een spanningspneumothorax:
- ernstige tachycardie;
- hypotensie;
- cyanose;
- hypoxemie;
- sterke dyspnoe.
De verschijnselen zijn rechtstreek af te leiden uit cardiaal- en respiratoir falen.
7.11.3 Onderzoek
De thoraxfoto toont een ‘leeg’ veld: longvaattekening ontbreekt ter plekke. Een scherpe lijn van de pleura viscerale is zichtbaar. Het valt op dat het mediastinum is verplaatst naar de gezonde kant, omdat de elastische retractie aan de aangedane zijde vervalt.
7.11.4 Behandeling
Deze is afhankelijk van de ernst van de pneumothorax. Deze kan non-invasief en invasief zijn.
Non-invasief
Bij een kleine niet-traumatische pneumothorax met weinig of geen klachten is het verantwoord af te wachten. Meestal sluit het gat in de longen zich spontaan en wordt de lucht door de thoraxwand geabsorbeerd. Eventueel bedrust. Vaak wordt O2 gegeven, wat snellere absorptie tot gevolg heeft.
Invasief
Bij een grotere pneumothorax moet men vaak de lucht afzuigen (= aspiratie). Dit gebeurt door zuigdrainage via de 2e intercostale ruimte (midclaviculair) totdat er geen lucht meer uit komt. Als dit onvoldoende helpt, kan vacuümzuigdrainage worden toegepast. Een pleuradrain wordt via de 2e intercostale ruimte (midclaviculair) of de 5e intercostale ruimte (midaxillair = onder de oksel) aangebracht. Lucht wordt via de drain afgezogen (waterslot!) tot de long zich tegen de wand heeft aangelegd. Sommigen continueren dit tot ten minste 24 uur na ontplooiing van de long. Is na een week geen resultaat merkbaar, dan moet tot een andere behandeling worden besloten. Beide genoemde ingrepen gebeuren onder lokale anaesthesie.
Een andere methode is chemische pleurodese. Dit is het ‘vastzetten’ (plakken) van de pleurabladen door het uitlokken van een (steriele) ontstekingsreactie die door middel van verlittekening geneest; daarbij vergroeien de pleurabladen met elkaar. Dit gebeurt door het aanbrengen van tetracycline of van talksuspensie in de pleuraholte via de pleuradrain, of van talkpoeder via thoracoscopie. Bij thoracoscopie wordt een trocar ingebracht in de pleuraholte via de 5e intercostale ruimte onder de oksel. Via de trocar kunnen benodigde instrumenten worden ingevoerd. Pleurodese is een pijnlijk proces.
Een nieuwere methode is video-assisted thoracic surgery (VATS). Deze ingreep gebeurt onder algehele narcose. Er wordt een dubbellumen intubatie uitgevoerd, waardoor beide longen apart kunnen worden beademd. De beademing van de aangedane long wordt geblokkeerd. Door inbrengen van een trocar onder de oksel (5e intercostale ruimte) wordt de pleuraholte geopend en valt de long samen. De eventueel nog aanwezige lucht kan via de tube worden afgezogen. Optiek kan via een tweede trocar worden ingebracht; deze is verbonden met een videocamera. Via een derde trocar kunnen instrumenten worden ingebracht. Met deze techniek kan men luchtlekken sluiten, bullectomie of pleurectomie (resectie van de pleura patietalis met als gevolg vergroeiingen tussen longen en thoraxwand) uitvoeren, maar ook talkpoeder verstuiven teneinde pleurodese te bewerkstelligen. Dit kan ook worden bereikt door abrasie (= kwetsing) van de pleurae.
Conventionele chirurgische behandeling (thoracotomie) wordt onder de oksel of via het sternum uitgevoerd. Postoperatief zijn hier meer problemen te verwachten, vooral pijn. De behandeling komt in plaats van VATS, als deze niet voorhanden is.
Andere maatregelen zijn:
advies te stoppen met roken;
onderliggende oorzaken opsporen en behandelen;
eventueel zuurstoftoediening en pijnbestrijding.
7.11.5 Complicaties
Een spanningspneumothorax kan behalve long- en hartfalen nog mediastinaal emfyseem tot gevolg hebben. Via de scheden van bloedvaten ziet lucht kans om in de weefsels, zelfs tot de onderste huidlagen door te dringen. Je voelt het zitten: crepiteren van de huid met geluid alsof je door verse sneeuw loopt; erg gevaarlijk is het niet.
Bij een juiste behandeling van de pneumothorax volgt herstel. Het voorkomen van recidieven bepaalt vervolgens de prognose. Belangrijk in dit verband is de onderliggende oorzaken te behandelen. Is pleurodese toegepast, dan blijkt dit een recidief bij een spontane pneumothorax tot 8% te beperken.