Inleiding
In dit hoofdstuk worden door een gynaecoloog en verloskundige de fysiologie en pathologie van de verloskunde per tijdperk op een beknopte, heldere wijze behandeld. Dat zijn achtereenvolgens de zwangerschap, het ontsluitingstijdperk, het uitdrijvingstijdperk, het nageboortetijdperk en het kraambed. Elk onderdeel sluit af met een bespreking van de belangrijkste therapeutische interventies.
Zwangerschap algemeen
Inleiding
De Nederlandse verloskunde wordt gekenmerkt door een scheiding tussen vrouwen met een laag en vrouwen met een verhoogd risico op complicaties tijdens de zwangerschap, baring en kraamperiode. De eerste, grootste, groep wordt begeleid door de eerste lijn – verloskundige of verloskundig actieve huisarts – terwijl de tweede groep wordt gecontroleerd door de gynaecoloog. Centraal in de begeleiding door de eerste lijn staat de selectie op risicofactoren tijdens zwangerschap, baring en kraamperiode. In de groep waarbij een laag risico wordt vastgesteld, bestaat de mogelijkheid te kiezen voor thuisbevalling of poliklinische bevalling.
Op lokaal niveau worden steeds vaker samenwerkingverbanden (VSV) gevormd tussen eerste en tweede/derde lijn om de kwaliteit van de zorg te borgen en te verbeteren. Met behoud van ieders professionaliteit en zelfstandigheid wordt de communicatie bevorderd en de ketenzorg versterkt.
De inhoud van dit hoofdstuk is afgestemd op werkers in de eerste lijn; in het kort wordt aangegeven wat er in de eerste lijn gebeurt, waar de grens naar de tweede lijn ligt en wat aldaar vervolgens het beleid/de therapie zal zijn.
Waarschijnlijke zwangerschapstekenen
amenorroe;
subjectieve klachten: ochtendmisselijkheid, gespannen borsten, verandering van eetlust, slaperigheid en moeheid;
bevindingen bij onderzoek: vaginawand blauw verkleurd, cervix week, vaatpulsaties van arteria uterina, uterus (soms onregelmatig) vergroot, week van consistentie;
basale temperatuurcurve : de ochtendtemperatuur blijft langer dan 2 weken na de ovulatie 0,5 °C verhoogd (progesteroneffect).
Zwangerschapsreacties
Deze berusten allemaal op het aantonen van hCG (humaan choriongonadotrofine) in urine of serum. De moderne, gevoelige reacties, gebaseerd op monoklonale antistoffen, zijn al positief rond het tijdstip waarop de menstruatie uitblijft, dus circa 2 weken na de conceptie. De reactie is positief bij functionerend chorionweefsel, het embryo behoeft daarbij niet intact te zijn.
Zekere zwangerschap
Het horen van kinderlijke harttonen (vanaf 10-13 weken met dopplerapparatuur, vanaf 21-24 weken met de monoaurale stethoscoop) en het voelen van kindsbewegingen door de onderzoeker.
Het vaststellen van embryonale hartactie bij echoscopisch onderzoek: bij transvaginale echoscopie is deze al vanaf 5½ à 6 weken amenorroe waarneembaar, bij transabdominale echoscopie één tot enkele weken later.
Prenatale controle
Een belangrijk doel van prenatale zorg is op positieve wijze bijdragen aan de daling van zowel de maternale als de perinatale mortaliteit en morbiditeit. Hiertoe dienen afwijkingen tijdig herkend en behandeld te worden. Door regelmatig en correct uitgevoerde zwangerschapscontroles kunnen risicofactoren en afwijkende bevindingen tijdig worden onderkend en kan zo nodig verwijzing naar de tweede/derde lijn plaatsvinden.
Om optimaal aan een zwangerschap te kunnen beginnen kan een preconceptioneel consult van nut zijn.
Naast algemene adviezen over levenswijze – zoals dieetadviezen, het stoppen met roken en alcohol voor de zwangerschap – kan een familieanamnese eventueel erfelijke afwijkingen aan het licht brengen waarvoor prenatale diagnostiek of een consult van de klinisch geneticus nodig is.
De zwangerschapscontroles
Bij de zwangerschapscontroles dient aan de volgende punten aandacht te worden besteed:
een nauwkeurige anamnese betreffende de gezondheidstoestand van de vrouw, leefstijl, medicatie, allergieën, menstruatieanamnese, familieanamnese, het verloop van eventueel vorige zwangerschappen, baringen en kraamperioden;
bepaling van Hb, glucose op indicatie, bloedgroep/resusfactor D en kleine c evenals irregulaire antistoffen tegen erytrocyten;
bepaling van serologische reacties op syfilis, rubella, hepatitis B (HBsAg-screening) en hiv ;
gewicht en lengte waaruit de BMI valt te berekenen;
bepaling van systolische en diastolische bloeddruk;
op indicatie onderzoek van de urine op ketonen (hyperemesisklachten) of albumen (RR diastolisch ≥ 90 mmHg, en/of systolisch >140 en altijd bij ‘pre-eclamptische’ klachten (na 20 weken), ongeacht de bloeddruk);
vanaf 14 weken de hoogte van de fundus uteri bepalen. Deze wordt bepaald met symfyse, navel en processus xiphoideus als oriëntatiepunten; deze fundushoogte wordt uitgedrukt in weken amenorroe en moet worden vergeleken met de, volgens de amenorroe, te verwachten hoogte. Inmiddels is duidelijk geworden dat er een betere methode is om intra-uteriene groeiretardatie (IUGR) tijdig op te sporen. Vanaf 2014 wordt de hiervoor beschreven methode gefaseerd vervangen door het in centimeters meten van de afstand fundus uteri – bovenrand symfyse volgens een gestandaardiseerde methode. Deze afstand wordt afgezet in de individuele groeicurve voor de zwangere (GROW);
ligging van het kind (vanaf 28-30 weken);
controle van de harttonen van het kind (vanaf 11 weken mogelijk met doptone). Geadviseerd wordt om met luisteren met behulp van doptone te wachten tot 16 weken, mits er echoscopisch een intacte zwangerschap is vastgesteld rond 10-12 weken;
informeren naar leven voelen vanaf circa 20 weken;
Bij de eerste controle, die bij voorkeur plaatsvindt rond 8-9 weken, worden de eerste 6 punten onderzocht. Tevens wordt counseling ten aanzien van non-invasieve prenatale onderzoeken verricht. Bij iedere herhalingscontrole worden de laatste zes punten onderzocht. Bovendien worden de volgende zaken herhaald:
het Hb bij 30 weken en op indicatie bij 20 weken;
glucose/GTT op indicatie;
irregulaire antistoffen bij resus D- en resus c-negatieve zwangere en resusfactor van de baby bij elke resus D-negatieve zwangere (beide bij 27 weken);
het gewicht in ieder geval enkele malen in de zwangerschap, op indicatie bij elke controle;
uiteraard is bij elke controle het informeren naar het algemeen lichamelijk en psychisch welbevinden van de zwangere een standaardonderdeel. Eventueel kan, met behulp van een zelftest op internet, de mate van angst en somberheid/depressie worden gemeten (http://www.poppoli.nl/pop-poli/test-uzelf/).
Bij dit alles moet ook advies worden gegeven ten aanzien van de voeding en verdere leefgewoonten (roken, alcohol, werken). Tevens kunnen zwangerschapscursus, plaats van de bevalling en voorzieningen voor kraamhulp thuis ter sprake komen. Roken is uitgesproken ongunstig en werkt risicoverhogend op miskraam, vroeggeboorte, foetale groeivertraging, placenta praevia en abruptio placentae. Alcohol (bij dagelijks gebruik) veroorzaakt aangeboren afwijkingen en gedragsstoornissen bij het kind; deze kunnen al ontstaan tijdens de conceptie. Gebruik van ecstasy, cocaïne en andere harddrugs of van softdrugs in grotere hoeveelheden, ook alleen in het begin van de zwangerschap, verhoogt eveneens de kans op zwangerschapsproblemen en afwijkingen bij het kind.
Elke bij de (toekomstige) zwangere betrokken zorgverlener dient over te dragen dat roken en elk gebruik van alcohol/drugs rondom conceptie en tijdens de zwangerschap vermeden dient te worden.
Echoscopie
Er zijn voldoende argumenten om vroege echoscopie (eerste trimester) aan te bieden aan elke zwangere:
zekere termijnbepaling: géén termijndiscussie bij later in de zwangerschap optreden van positieve of negatieve discongruentie; géén termijndiscussie bij preterme partus of serotiniteit;
tweelingzwangerschappen worden vroegtijdig herkend en chorioniciteit kan betrouwbaar worden beoordeeld;
vaststellen van de intacte graviditeit;
indien gewenst en na counseling meting van de ‘nuchal translucency’ (NT) of nekplooimeting.
Later in de zwangerschap is echoscopie aangewezen bij:
twijfel omtrent groei van de foetus, zowel positieve als negatieve discongruentie;
(vermoeden op) liggingsafwijking van de foetus (vanaf 34/36 weken);
bloedverlies;
niet ingedaald voorliggend deel én geen SEO verricht (placentalokalisatie);
na counseling de screeningsecho bij 20 weken op structurele afwijkingen (SEO);
op indicatie geavanceerd echoscopisch onderzoek (GUO).
Het is thans verplicht om elke zwangere te counselen voor de SEO. De SEO is bedoeld om ernstige macroscopische afwijkingen op te sporen.
Gericht echoscopisch onderzoek ter detectie van congenitale afwijkingen (‘GUO, geavanceerd echoscopisch onderzoek’) wordt verricht in de centra voor prenatale diagnostiek. Indicaties zijn de volgende.
A priori verhoogd risico op congenitale afwijkingen (type I-indicaties):
aangeboren afwijking in de eerste graad (ouders, broer/zus van foetus)
aangeboren afwijking in de tweede graad bij 2 of meer in de derde graad
insulineafhankelijke diabetes mellitus;
bewezen teratogene middelen (medicijnen, drugs, röntgenstraling, chemotherapie);
monochoriale tweeling;
overige redenen (bijvoorbeeld consanguïniteit, ICSI-graviditeit).
Aandoeningen in de zwangerschap met verhoogd risico op congenitale afwijkingen (type II-indicaties):
echoscopische verdenking op structurele afwijkingen;
verdikte NT > 3,5 mm;
verhoogd AFP in het vruchtwater;
maternale infecties met foetaal effect (toxoplasmose, rubella, cytomegalie, coxsackie, Parvo B19);
ernstige negatieve discongruentie (foetale buikomtrek < P3);
ernstige positieve discongruentie (foetale buikomtrek > P97 indien geen eerdere SEO);
oligohydramnion (diepste vruchtwaterpocket < 2 cm);
polyhydramnion (diepste vruchtwaterpocket > 8 cm);
≥ 2 softmarkers bij SEO;
foetale hartritmestoornissen;
overige redenen (bijv cytogenetische bevindingen, irregulaire antistoffen);
Andere niet-invasieve prenatale onderzoeken
De kansberekenende test of combinatietest
Risicoberekening is mogelijk op het vóórkomen van het syndroom van Down, syndroom van Edwards en syndroom van Patau (respectievelijk trisomie 21, 18, 13). Hierbij wordt de dikte van de nuchal translucency (NT) gemeten door middel van echoscopie tussen 11 en 14 weken, gecombineerd met eiwit- en hormoonconcentraties uit het moederlijk serum en de leeftijd van de moeder. Op grond van de risicoberekening kan tot vervolgonderzoek worden overgegaan (risico > 1:200) of juist daarvan worden afgezien (risico < 1:200). Ook veel vrouwen ≥ 36 jaar kiezen thans voor deze non-invasieve test vanwege de veiligheid voor de zwangerschap.
Het is verplicht elke zwangere te informeren en indien gewenst te counselen voor deze risicoberekening, waarbij vrouwen zonder a priori verhoogd risico op deze chromosoomaandoeningen de test niet vergoed krijgen uit de basisverzekering.
NIPT (niet-invasieve prenatale test)
In het moederlijk plasme is foetaal DNA aanwezig. Met de NIPT (niet-invasieve prenatale test) kan DNA van het ongeboren kind worden onderzocht op trisomie 13, 18 en 21. Te veel DNA van deze chromosomen is een sterke aanwijzing voor trisomie 13, 18 of 21 bij de foetus. Als de NIPT niet-afwijkend is, kan invasieve prenatale diagnostiek achterwege worden gelaten (de kans dat er dan toch sprake is van een trisomie is kleiner dan 1 promille). Omdat er bij een afwijkende uitslag tóch sprake kan zijn van een kind zonder trisomie, wordt een positieve NIPT (indien ouders dit wensen óf indien ouders de zwangerschap wensen af te breken) altijd gevolgd door invasieve prenatale diagnostiek om zekerheid te krijgen. Screening van gezonde personen valt in Nederland onder de Wet op het bevolkingsonderzoek (WBO) en is vergunningplichtig. Met ingang van 1 april 2014 heeft de minister van Volksgezondheid, Welzijn en Sport een vergunning voor twee jaar afgegeven om elke zwangere met een verhoogd risico op trisomie 13, 18 of 21, gebleken uit de combinatietest , de keus te geven deze niet-invasieve test te laten uitvoeren binnen de kaders van de TRIDENT-studie. De vergunning is uitsluitend verleend aan de acht Universitaire Medische Centra. NIPT laten uitvoeren zonder voorafgaande risicoberekening is in principe niet mogelijk (medische redenen uitgezonderd). Ook vrouwen van 36 jaar en ouder, die vóór het invoeren van NIPT direct toegang hadden, en nog steeds hebben, tot invasieve diagnostiek, hebben alleen toegang tot NIPT indien de combinatietest daar aanleiding toe geeft (advies van de Gezondheidsraad 2013, overgenomen door de minister van Volksgezondheid, Welzijn en Sport).
NIPT kan, laboratoriumtechnisch, vanaf 10 weken zwangerschap worden uitgevoerd, maar in het kader van de TRIDENT-studie moet meestal eerst de uitslag van de combinatietest worden afgewacht. De uitslag van NIPT is binnen 10-15 werkdagen bekend.
Voor up-to-date informatie: www.meerovernipt.nl of www.niptconsortium.nl
Invasieve prenatale diagnostiek
Bij het kind kunnen chromosomale afwijkingen, zoals het syndroom van Down, of afwijkingen op DNA-niveau, bijvoorbeeld hemofilie A of cystische fibrose, worden vastgesteld door cellen van het kind of de placenta te onderzoeken. Deze cellen kunnen worden verkregen via een vlokkentest (chorionbiopsie waarbij cellen uit de placenta worden verkregen) of via een vruchtwaterpunctie. Ook later in de zwangerschap, als bij echoscopie verdenking is gerezen op een mogelijk genetische afwijking, kan dit onderzoek verricht worden.
Ziektebeelden in de zwangerschap
Anemie
De hoogte van het Hb ondergaat een fysiologische verandering naarmate de zwangerschap vordert. Dit heeft consequenties voor het beleid. Er is sprake van anemie als het veneuze Hb < P5 is (zie tabel 22.1). Het gebruik van ferropreparaten verergert de vaak reeds bestaande obstipatie. Deze preparaten worden slechts voorgeschreven indien het veneuze Hb onder de P5 is én de MCV een microcytaire anemie laat zien. Stijgt het Hb niet binnen enkele weken, dan is nader bloedonderzoek naar andere oorzaken van anemie nodig. Bij meerlingzwangerschap zijn ter preventie van anemie foliumzuur en ijzersuppletie aan te bevelen.
| preconceptioneel | 7,5 |
| zwangerschap in weken | |
| - tot en met 13 | 7,1 |
| - 14 tot en met 17 | 6,8 |
| - 18 tot en met 21 | 6,5 |
| - 22 tot en met 37 | 6,3 |
| - vanaf 38 | 6,5 |
| post partum in weken | |
| 1-5 | 6,5 |
| 6 | 7,2 |
Diagnose
Het hemoglobinegehalte wordt bij het eerste onderzoek en bij 30 weken verricht. Op indicatie (slechte voedingsgewoonte, tienerzwangerschap, niet-Noord-Europese afkomst, dragerschap hemoglobinopathie, meerlinggraviditeit, vorige graviditeit minder dan 1 jaar geleden) wordt ook bij 20 weken het Hb en zo nodig MCV bepaald. Ook extreme vermoeidheidsklachten kunnen reden zijn voor een Hb-bepaling.
Indien het veneuze Hb < P5 is, wordt het MCV bepaald en bij vrouwen van niet-Noord-Europese afkomst ook HbP-bepaling.
Indien de zwangere bekend is met (dragerschap) hemoglobinopathie en een laag Hb/MCV heeft, dan eerst serumferritine bepalen alvorens te behandelen met ijzermedicatie.
Therapie
Bij microcytaire anemie (te laag MCV) als gevolg van ijzergebrek starten met 1 dd 200 mg ferrofumaraat . Laat in de zwangerschap eventueel (en zelden noodzakelijk) i.v. of i.m. ferropreparaat.
Bij macrocytaire anemie: nadere analyse van de oorzaak. Bij foliumzuurtekort 5 mg foliumzuur per dag.
Bij zwangeren die van oorsprong afkomstig zijn uit (Noord-)Afrika of Suriname denken aan een hemoglobinopathie, zoals sikkelcelziekte en thalassemie. Bij zwangeren van negroïde afkomst – en een laag Hb – een sikkelceltest uitvoeren en indien deze positief is een Hb-elektroforese. Bij zwangeren uit het mediterrane gebied – en een laag Hb – een Hb-elektroforese laten verrichten om een thalassemie uit te sluiten. Indien een zwangere een heterozygote vorm heeft van sikkelcelziekte of een thalassemie, is het van belang ook de partner te screenen. Als deze ook heterozygoot is, kan de foetus de ernstige homozygote vorm hebben. Dit is door prenataal onderzoek aantoonbaar.
Bloedverlies en miskraam in de eerste helft van de zwangerschap; miskraam: dreigende, (in)complete, habituele, niet-vitale, geïnduceerde
Bloedverlies vroeg in de zwangerschap komt regelmatig voor en kan onder meer berusten op een innestelingsbloeding . Zolang het bloedverlies gering is en niet gepaard gaat met krampen is dit meestal een onschuldig maar voor de vrouw wel verontrustend verschijnsel. Echoscopie kan in deze gevallen de onrust (tijdelijk) wegnemen
De differentiaal diagnose bij bloedverlies tot 16 weken:
innestelingsbloeding
contactbloeding
dreigende miskraam
complete miskraam
incomplete miskraam
EUG (extra-uteriene graviditeit)
mola-graviditeit.
Dreigende miskraam
Pijnloos bloedverlies uit het ostium cervicis, meestal zonder of met geringe krampen. Het ostium is nog gesloten. Ongeveer 50% van deze zwangerschappen eindigt met een spontane miskraam.
Diagnose
De diagnose wordt gesteld op basis van anamnese en onderzoek. Een volledige anamnese, inclusief aard en hoeveelheid bloedverlies, aard en verloop subjectieve zwangerschapsklachten en vaginaal toucher geven meestal voldoende informatie om de voorlopige diagnose te stellen. Cave EUG Bij (een verdenking op) een EUG is een spoedverwijzing naar de gynaecoloog geïndiceerd.
Therapie
Voor een dreigende miskraam is geen therapie. Als er zich geen bijzonderheden voordoen, zijn uitleg, een afwachtend beleid en hernieuwde controle na 1 week voldoende (zie NHG-Standaard Miskraam).
Complete miskraam
Een soms nog intacte vruchtzak is uitgestoten, patiënte heeft geen pijn meer, vloeit minder en de cervix sluit zich weer.
Diagnose
Na een korte periode van toenemend krampende pijn in de onderbuik en bloedverlies is er sprake van het verlies van het zwangerschapsproduct; de pijn zakt snel af, evenals het bloedverlies. Het ostium sluit zich weer.
Therapie
In deze gevallen kan worden afgewacht onder controle van bloedverlies en temperatuur. Bij hernieuwd bloedverlies alsnog insturen voor nadere evaluatie.
Incomplete miskraam
Bloedverlies, vaak met krampen/verlies van weefsel waarbij de cervix openstaat.
Diagnose
Toename van buikpijn en bloedverlies; in 40-50% van de gevallen vindt bij afwachtend beleid binnen een week na het eerste bloedverlies een volledige uitstoting plaats.
Therapie
Bij miskraam in gang afwachten of miskraam compleet zal zijn.
Opname voor curettage is nodig bij een incomplete miskraam of bij te sterk bloedverlies. In plaats van curettage kan in het ziekenhuis ook misoprostol 4 tabl. van 200 microgram gegeven worden.
Bij resus D-negatieve zwangere met een complete miskraam waarbij de zwangerschapsduur ≥ 10 wk: 375 IE anti-D i.m. toedienen. Bij curettage wordt ongeacht de zwangerschapsduur altijd 375 IE anti-D i.m. toegediend.
Extra-uteriene graviditeit (EUG)
Vaginaal bloedverlies treedt bij circa 80% van de vrouwen met EUG op door regressieve veranderingen in de decidua (soms tijdens de te verwachten menstruatie). Hierbij staan doorgaans de pijn (soms uitstralend naar de rechterschouder) en eventuele shock op de voorgrond. Aan EUG dient altijd gedacht te worden bij acute buikpijn bij een vrouw in de fertiele leeftijd, zeker bij risicofactoren. (Zie diagnose.)
De voornaamste vormen van EUG zijn:
tubaire abortus : chronische buikpijn, palpabele weerstand naast de uterus en/of in het cavum Douglasi, zwangerschapsreacties soms nog positief;
tubaruptuur : acute buikpijn, shock, bij toucher hevig pijnlijk, ook het cavum Douglasi (cri de Douglas).
Diagnose
Klachten kunnen aanvankelijk geheel ontbreken. Later variëren deze van vaginaal bloedverlies, al dan niet in combinatie met buikpijn, tot shockverschijnselen ten gevolge van intra-abdominaal bloedverlies. Tegenwoordig bestaat, door de verbeterde (transvaginale) echoscopische techniek, de mogelijkheid van vroege diagnostiek van EUG, zelfs voordat klinische verschijnselen opgetreden zijn. Deze wordt uitgevoerd in het begin van de zwangerschap, bij vrouwen met predisponerende factoren voor een EUG. Die factoren zijn:
vroegere ontstekingsprocessen van de tuba, pelvic inflammatory disease (PID);
voorafgaande infertiliteit mogelijk door tuba-afwijkingen;
voorafgaande EUG;
aanwezigheid van een IUD in de uterus ten tijde van de conceptie;
zwangerschap na sterilisatie van de vrouw;
zwangerschap na IVF of vergelijkbare technieken.
Vrouwen met één van deze predisponerende factoren in de voorgeschiedenis moeten worden voorgelicht over de mogelijkheid van vroege echoscopische diagnostiek.
Bij echoscopie wordt niet altijd een EUG ontdekt; wel is het mogelijk aan te tonen dat het cavum uteri leeg is, dus geen zwangerschap herbergt. In combinatie met een positieve zwangerschapsreactie is dit een sterke aanwijzing voor een EUG. Ook bij irregulier bloedverlies in het prille begin van de zwangerschap is echoscopie geïndiceerd. Door seriële bepaling van bèta-hCG en transvaginale echoscopie, kan de diagnose EUG vrijwel altijd met zekerheid worden gesteld.
Specialistische therapie
Het beleid en de behandeling hangen af van het beloop van de bèta-hCG-spiegel en de klachten van de patiënte. Bij alle behandelingsopties is toediening van anti-D-immunoglobuline geïndiceerd bij vrouwen met een resusnegatieve bloedgroep, bij voorkeur binnen 72 uur na het stellen van de diagnose.
De behandeling kan bestaan uit methotrexaat (remt de celdeling) of (laparoscopische) chirurgie. Laparoscopische chirurgie is de behandeling van eerste keuze bij de behandeling van patiënten met een tubaire EUG. Tubasparende chirurgie heeft de voorkeur bij patiënten met kinderwens en contralaterale tubapathologie. Na tubasparende chirurgie is postoperatieve serum-hCG-monitoring noodzakelijk om persisterende trofoblast in een vroeg stadium vast te stellen. Een afwachtend beleid is een optie voor patiënten met symptoomarme EUG’s en initiële lage serum-hCG-concentraties die spontaan dalen.
Molagraviditeit
Verdenking op molagraviditeit bij sterke zwangerschapsverschijnselen, aanhoudend bloedverlies, te grote uterus, doptone negatief, ook na 12 weken. Omdat vrijwel elke zwangere echoscopie in het eerste trimester ondergaat, wordt deze diagnose tegenwoordig meestal als toevalsbevinding bij echoscopie ontdekt voordat er klachten zijn.
Diagnose
Door middel van echoscopie en uiteindelijk door pathologisch anatomisch onderzoek.
Specialistische therapie
Opname, evacuatie van de uterus (zuigcurettage).
Nacontrole: wekelijks bepaling van bèta-hCG in het serum, totdat de hCG-spiegel is gedaald tot niet meer aantoonbare waarden. Eventueel kan na zes maanden een nieuwe zwangerschap beginnen. Tot die tijd dient goede anticonceptie (bij voorkeur de pil) te worden toegepast.
Bij aanwijzingen van persisterende trofoblastactiviteit verwijzen naar een specialistisch centrum voor aanvullende diagnostiek en cytostatische behandeling.
Habituele miskraam
Van habituele miskraam wordt gesproken indien er sprake is van drie of meer achtereenvolgende spontane miskramen. Van alle klinisch gediagnosticeerde zwangerschappen eindigt ongeveer 15% in een miskraam. Na twee opeenvolgende miskramen stijgt het risico naar 17-35% en na drie naar 25-46%. De belangrijkste voorspellende factor voor een miskraam is een voorafgaande miskraam. De verwachte kans op habituele miskraam is 0,34%, de geobserveerde incidentie 0,5-1,0%. Daarom kan habituele miskraam maar ten dele door toeval worden verklaard en moet er in ongeveer de helft van de gevallen sprake zijn van een onderliggende oorzaak of van aanvullende risicofactoren.
Onderzoek (in tweede lijn)
Dit onderzoek is gericht op het opsporen van risicofactoren die de kans op spontane miskraam vergroten. Hierbij is de (familie)anamnese essentieel, aangezien habituele miskraam de eerste manifestatie kan zijn van een onderliggende aandoening.
Om een chromosoomafwijking bij een van de aanstaande ouders uit te sluiten, wordt gewoonlijk al na twee opeenvolgende klinische miskramen de mogelijkheid van genotypering ter sprake gebracht.
Bij ouders met een normaal karyogram vormt habituele miskraam op zichzelf geen indicatie voor antenatale diagnostiek in een volgende zwangerschap.
Bij een afwijkend chromosoomonderzoek bij (een van) de ouders kan chromosoomonderzoek in een volgende doorgaande zwangerschap geïndiceerd zijn.
Niet-vitale zwangerschap (voorheen missen abortion)
Van een niet-vitale zwangerschap spreekt men als bij (vroeg-)echoscopisch onderzoek geen embryo met hartactie wordt gezien, hetgeen (nog) niet tot een spontane miskraam heeft geleid. Er kan sprake zijn van een lege vruchtzak of van een embryo zonder hartactie waarbij dit wel mag worden verwacht op basis van de CRL (kopstuitlengte). Bij twijfel over de zwangerschapsduur echoscopie herhalen.
Therapie
Afwachten tot een spontane miskraam plaatsvindt; dit gebeurt in circa 50% van de gevallen. Indien na enige tijd – één/twee weken – geen spontane afstoting plaatsvindt en de vrouw wil niet langer afwachten, wordt ze verwezen naar de gynaecoloog. Ze heeft de keuze tussen curettage of misoprostol 4 tabl. à 200 microg. zo nodig na 2 dagen herhalen.
Abortus arte provocatus
Een ongewenste zwangerschap, vanwege aangeboren afwijkingen van de foetus of vanwege sociale omstandigheden, kan worden afgebroken met behulp van mifepriston 200 mg, een progesteronantagonist in combinatie met misoprostol (4 tabl. à 200 microg). In een deel van de gevallen zal een curettage hierbij alsnog nodig zijn. Ook kan primair voor een curettage worden gekozen. In ons land mag een zwangerschap worden afgebroken als de zwangerschapsduur niet verder gevorderd is dan 22-24 weken .
Geadviseerd wordt om de term ‘abortus’ alleen te gebruiken voor de abortus arte provocatus en voor het overige de term ‘miskraam’ te gebruiken.
Bloedverlies in de tweede helft van de zwangerschap
Bloedverlies in het tweede of derde trimester (na een amenorroe van ≥ 16 weken) is een reden tot specialistische verwijzing, tenzij het slechts gering bloedverlies post coitum betreft. Bij de verwijzing wordt géén vaginaal onderzoek verricht! Anamnese en uitwendig onderzoek kunnen een waarschijnlijkheidsdiagnose opleveren die richting geeft aan de mate van spoed.
De volgende oorzaken van bloedverlies in de tweede helft worden beschreven:
abruptio placentae;
placenta praevia;
randsinusbloeding en placenta circumvallata.
Opname in het ziekenhuis is geïndiceerd waarbij bloed voor transfusie snel beschikbaar moet zijn. Bij weeënactiviteit ten gevolge van het bloedverlies en goede foetale conditie: weeënremming en corticosteroïden voor 34 weken. Bij circa 36 weken en placenta praevia overwegen de zwangerschap electief per sectio caesarea te beëindigen.
Bij vitaal bloedverlies zwangerschap direct per sectio caesarea beëindigen.
(Bloeding door) placentaloslating (abruptio placentae)
Geheel of gedeeltelijk loslaten van de normaal geïmplanteerde placenta tijdens de zwangerschap.
Etiologie
De oorzaak is onbekend, factoren die een rol spelen zijn:
vasculaire afwijkingen (pre-existente hypertensie, zwangerschapshypertensie);
metabole en/of hemostatische afwijkingen en mogelijk aangeboren of verworven trombofilie (hyperhomocysteïnemie, proteïne-S-deficiëntie, proteïne-C-deficiëntie, factor V-mutatie, factor II-mutatie, APC-resistentie, anticardiolipineantistoffen of lupusanticoagulans);
roken en cocaïnegebruik;
een trauma (val op de buik, auto-ongeluk, huiselijk geweld) kan een abruptio tot gevolg hebben in de eerste 24 uur;
geboorte van de eerste van een tweeling.
De symptomen bestaan uit:
acute pijn in buik of rug, continu van karakter, maar niet altijd te onderscheiden van weeënactiviteit;
hypertone uterus (variërend van geringe contractiliteit tot ‘plankharde’ uterus);
gering bloedverlies, uitwendig (geen obligaat symptoom, aangezien de bloeding soms beperkt blijft tot achter de placenta);
foetale nood: afhankelijk van de omvang van de abruptio kan de foetale conditie variëren van ongestoord tot foetale sterfte kort na de abruptio.
Diagnose
In de typische gevallen: uterus plankhard (uterus ‘en bois’), kind in utero overleden (doptone en echoscopie negatief). Complicaties: intravasale stolling, stoornissen van nier- en leverfunctie.
In atypische gevallen is het kind soms nog in leven; de conditie wordt bepaald met cardiotocografie (CTG). Dit wordt ook wel ‘partiële abruptio’ genoemd. Meestal is de stollingsstoornis daarbij afwezig of minder ernstig dan in de typische gevallen met intra-uteriene vruchtdood.
Specialistische therapie
Geschat bloedverlies (bij complete abruptio in utero 2 liter!) altijd suppleren ter voorkoming nierschade.
Nauwkeurig vervolgen van stollingsstatus, diurese en tensieverloop.
Na optreden van intra-uteriene vruchtdood bij voorkeur spontane baring afwachten of inleiden van de baring (binnen 24-48 uur treedt deze meestal spontaan op).
Sectio caesarea slechts uitvoeren bij een gedeeltelijke abruptio placentae met levend kind. De beslissing of een sectio wel of niet moet worden verricht hangt af van factoren als conditie van het kind, conditie van de moeder en zwangerschapsduur.
(Bloeding door) placenta praevia
De placenta bedekt geheel of gedeeltelijk het ostium internum van de cervix. In de tweede helft van de zwangerschap kan een placenta, die aanvankelijk net tot het ostium internum reikte, wat verder van het ostium komen te liggen.
Er is meestal pijnloos bloedverlies, zonder of met geringe weeënactiviteit. Het bloedverlies kan acuut optreden, vaak ’s nachts. Bloedverlies treedt ook vaak periodiek op. Zolang het bloedverlies niet tot maternale hypovolemie en bloeddrukdaling leidt, blijft de foetale conditie meestal goed. Typisch bij het klinisch beeld is een niet-ingedaald voorliggend deel of een dwarsligging.
Diagnose
De diagnose wordt bevestigd door echoscopische placentalokalisatie. Bij abdominale beeldvorming (met volle blaas) kan in de helft van de gevallen de exacte lokalisatie van het ostium internum ten opzichte van de placenta moeilijk waargenomen worden. Vaginale echoscopie is met betrekking tot beeldvorming superieur.
Door deze vorm van diagnostiek zijn de begrippen ‘placenta praevia totalis’, ‘lateralis’ en ‘marginalis’ wat op de achtergrond geraakt. In feite worden diagnostiek en therapie bepaald door het klinische beeld, in combinatie met de vaststelling dat bij echoscopisch onderzoek de placenta tot over of tot aan het ostium internum cervicis reikt.
Specialistische therapie
De therapie is afhankelijk van de zwangerschapsduur en de hoeveelheid bloedverlies.
Zolang er sprake is van bloedverlies, is opname in het ziekenhuis geïndiceerd, waarbij bloed voor transfusie snel beschikbaar moet zijn. Bij weeënactiviteit door het bloedverlies en goede foetale conditie: weeënremming en corticosteroïden voor 34 weken. Ontslag indien minimaal 24 uur geen bloedverlies optreedt. Recidief treedt vaak op, waarbij telkens opname volgt.
Bij circa 38 weken overwegen de zwangerschap electief per sectio caesarea te beëindigen.
Bij vitaal bloedverlies zwangerschap direct per sectio caesarea beëindigen.
(Bloeding door) randsinus en placenta circumvallata
Een randsinusbloeding is eigenlijk niets anders dan een bloeding uit de rand van de placenta. Een placenta circumvallata is een afwijking waarbij de choriaalplaat inclusief de foetale vaten niet tot de rand van de placenta reikt en waarbij een bloeding kan optreden.
Diagnose
Diagnose is doorgaans pas mogelijk zodra de placenta geïnspecteerd kan worden. De differentiële diagnose is uiteraard: placenta praevia, abruptio placentae, dreigende vroeggeboorte, placenta circumvallata met bloeding, foetaal bloedverlies door vasa praevia (zeer zeldzaam) en cervicitis. De diagnose ‘randsinusbloeding’ wordt bij uitsluiting gesteld.
Specialistische therapie
Hiervoor is geen therapie, opname van de moeder en bewaken van conditie van moeder en kind en zo nodig ingrijpen zijn de handelingsopties, waarbij uiteraard de andere oorzaken van bloedverlies moeten worden uitgesloten.
Braken tijdens de zwangerschap; (hyper)emesis gravidarum
Emesis: door de verandering in de hoeveelheid hormonen en de andere stofwisseling wordt de zwangere in de eerste drie maanden van de zwangerschap vaak misselijk wakker; dat gaat vooral ’s ochtends gepaard met braken. De eetlust neemt overigens niet af.
Hyperemesis: al het eten en drinken wordt uitgebraakt, diurese minder dan 500 ml per etmaal; metabole acidose (aceton en diaceetzuur in de urine). Komt vaker voor bij meerlingzwangerschap en bij molagraviditeit; recidiveert vaak in de volgende zwangerschap.
Diagnose
De diagnose emesis wordt gesteld op basis van het klachtenpatroon.
De diagnose hyperemesis wordt gesteld door het aantonen van ketonen in de urine. Aanvullend wordt echoscopisch onderzoek verricht voor het aantonen/ uitsluiten van meerling of molagraviditeit.
Therapie
Emesis: uitleg van en begrip voor de klachten zijn een belangrijk begin. Daarnaast: ’s morgens een licht ontbijt in bed voor het opstaan, gevolgd door frequente, lichtverteerbare kleine maaltijden. Geuren (vlees braden, parfum, dieren) worden vaak slecht verdragen en verergeren de misselijkheid. Ook een koude maaltijd kan volwaardige voeding zijn. Laat de zwangere zelf uitvinden wat bij haar goed werkt, waarbij volwaardig en gezond tijdelijk op de tweede plaats komen (zo nodig multivitaminen adviseren). Eventueel kunnen gembercapsules (4 maal daags 250 mg) of accupunctuur verlichting geven. Anti-emetica (meclozine of cyclizine) voorschrijven indien de adviezen onvoldoende helpen.
Hyperemesis: opname en intraveneuze vochttoediening. In uitzonderlijke gevallen kan sondevoeding nodig zijn.
Fluor vaginalis
Voor achtergrond van diagnostiek en behandeling wordt verwezen naar ▶ H. 10.1007/978-90-368-0610-7_4 Gynaecologie.
In de zwangerschap is er gemiddeld een toename van de vaginale afscheiding die veroorzaakt wordt door de hoge oestrogeenspiegel bij zwangere.
In de zwangerschap is het onderzoek bij ‘pathologische’ fluor vaginalis hetzelfde als buiten de zwangerschap inclusief de behandeling. Sommige medicamenten zijn in de zwangerschap gecontra-indiceerd.
Een candida-infectie komt in de zwangerschap veelvuldig voor; de diagnose is waarschijnlijk bij kort bestaande klachten van jeuk of irritatie en witte, niet-riekende afscheiding. Bij lichamelijk onderzoek wordt een rode vulva of vaginawand en witte, brokkelige fluor gezien. Ook in de zwangerschap kan de infectie goed worden behandeld. In de à terme periode is laagdrempelig starten met medicatie (eenmalig 500 mg clotrimazol of 1200 mg miconazol vaginaal) te overwegen in verband met het voorkómen van spruw bij de baby.
Gastro-oesofageale reflux
Gastro-oesofageale refluxklachten, zoals zuurbranden en regurgitatie, opboeren, pijn op de borst, dysfagie, heesheid en hoesten, worden veroorzaakt door vertraagde lediging van de maag die bij zwangerschap optreedt. De klachten doen zich vooral voor tegen het einde van de zwangerschap en vaak ’s nachts.
Bij vrouwen die tijdens de zwangerschap last krijgen van maagzuur zonder voorafgaande refluxklachten zullen de klachten na het einde van de zwangerschap snel verdwijnen. Er zijn geen aanwijzingen dat refluxklachten tijdens de zwangerschap predisponeren tot het ontwikkelen van gastro-oesofageale refluxziekte later, maar er is wel een neiging tot herhaling in een volgende zwangerschap.
Diagnose
Het is van belang onderscheid te maken tussen patiënten met pre-existente gastro-oesofageale refluxziekte die zwanger worden, en vrouwen die tijdens de zwangerschap last krijgen van refluxklachten. Meestal is bij refluxklachten in de zwangerschap geen nadere diagnostiek nodig; indien geïndiceerd kan een gastroscopie zonder problemen worden verricht.
Therapie refluxklachten in de zwangerschap
Uitleg over het mechanisme van reflux, algemene adviezen en leefregels is als eerste geïndiceerd. Adviseer vooral frequente kleine maaltijden en matigheid met gebruik van koffie, sterke thee, vet en koolzuurhoudende dranken. In rusthouding niet helemaal plat liggen en niet eten vlak voor het naar bed gaan. Bij onvoldoende resultaat kunnen zowel antacida als sucralfaat veilig tijdens de hele zwangerschap en lactatie worden gebruikt. Indien H2-receptorantagonisten worden voorgeschreven, zijn cemetidine en ranitinide het best onderzocht, waarbij de laatste de voorkeur heeft in de zwangerschap. Indien de klachten zo ernstig zijn dat een maagzuursecretieremmer moet worden voorgeschreven, is omeprazol 1 dd 10, 20 of 40 mg het middel van keuze.
Therapie pre-existente refluxziekte en zwangerschap
Indien de patiënt maagzuursecretieremmers nodig heeft, is het raadzaam haar vóór de conceptie reeds over te zetten op omeprazol. Voor het overige gelden de adviezen als bij refluxklachten in de zwangerschap.
Cystitis en pyelitis gravidarum
Tijdens de zwangerschap neemt de blaascapaciteit af, stijgt het residu na de mictie en treedt gemakkelijker een vesico-ureterale reflux op. Bovendien kunnen door compressie door de zwangere uterus en door het progesteron, dat de gladde spiercel verslapt, ureters en pyela dilateren, hetgeen predisponeert tot een opstijgende infectie. Asymptomatische bacteriurie komt bij ongeveer 6% van alle zwangeren voor. Ongeveer 25% daarvan wordt vroeg of later in de zwangerschap symptomatisch en ontwikkelt een cystitis of pyelitis. Bij pyelonefritis is er hoge koorts en pijn in de nierstreek. Tijdens een pyelonefritis kunnen endotoxinen in het bloed vrijkomen en aanleiding geven tot complicaties zoals pulmonaire capillaire schade (ARDS) of diffuse capillaire endotheliale schade, die resulteert in afgenomen vaatweerstand en afname van de cardiale uitstroom (septische shock).
Diagnose
De diagnose cystitis wordt gesteld aan de hand van het klinische beeld, een nitriettest, sediment en urinekweek.
Bij verdenking op pyelitis worden ook bloedbeeld, nierfunctie, hoeveelheid urineproductie en bloedkweek bij temperatuurverhoging vanaf 39 °C verricht. Tevens worden de vitale functies bewaakt ter uitsluiting van septische shock of ARDS. Bovendien kan echoscopisch onderzoek van de nieren worden verricht bij een langzame reactie op antibiotica of bij een recidief infectie.
Therapie
Een asymptomatische bacteriurie is risicoverhogend voor het optreden van een pyelitis. In Nederland wordt niet routinematig gescreend op bacteriurie, waardoor de asymptomatische bacteriurie meestal niet wordt gevonden. Indien deze als toevalsbevinding toch wordt opgespoord, luidt het advies te behandelen met antibiotica.
Bij cystitis is de eerste keuze nitrofurantoïne met gereguleerde afgifte 2 dd 100 mg, ten minste 5 dagen. Na 36 weken en bij dreigende preterme geboorte evenals bij tekenen van weefselinvasie 3 dd amoxicilline/clavulaanzuur 500/125 mg voorschrijven.
Bij pyelitis ziekenhuisopname en intraveneuze antibiotische therapie met als eerste keuze cefalosporine intraveneus (cefuroxim 750 mg 3 dd of cefotaxim 1.000 mg 4 dd of ceftriaxon 2.000 mg 1 dd). Tweede keuze: amoxicilline/clavulaanzuur intraveneus (1.000/200 mg 3-4 dd). Antibiotica zo nodig later veranderen op geleide van het resistentiepatroon van de gekweekte bacterie.
Bij pyelitis zal opname van de zwangere nodig zijn, ook al omdat soms door de hoge koorts de baring op gang komt. Er is een vrij grote kans op recidief.
In het algemeen is de koorts binnen 48 uur na start van de medicatie gedaald. Wanneer de koorts niet binnen 72 uur is afgenomen, kan dit wijzen op bacteriële resistentie of urolithiasis, een perinefritisch abces of afwijkingen aan de urinewegen waarvoor nadere diagnostiek wordt geadviseerd. Na een koortsvrije periode van 24-48 uur kan worden overgegaan op orale antibiotica. Een totale duur van de kuur van ten minste 10 dagen wordt geadviseerd.
Indien de cystitis/pyelitis wordt veroorzaakt door groep B-streptokokken is antibioticaprofylaxe durante partu geïndiceerd ter bescherming van de neonaat.
Irregulaire antistoffen en preventie resus D-sensibilisatie
In de zwangerschap passeert maternaal IgG de placenta. Als gevolg van eerdere zwangerschappen en/of transfusies kan de moeder antistoffen hebben gevormd tegen foetale erytrocyten. Deze IgG-antistoffen kunnen bij het kind ernstige hemolyse veroorzaken. Het bekendste voorbeeld is de resus-D cde/cde-negatieve moeder die antistoffen maakt tegen het resus D-antigeen dat aanwezig is op de erytrocyten van haar kind. Als resuspositief wordt iedereen beschouwd die homozygoot of heterozygoot de eigenschap C, D of E heeft. Naast antistoffen tegen resus D worden regelmatig antistoffen tegen onder andere resus C, resus c, resus E en Kell gezien.
Circa 50% van de allo-antistoffen zijn resus D-antistoffen, de andere 50% zijn andere allo-antistoffen.
Algemeen beleid
Vroeg in de zwangerschap wordt iedere zwangere getest op de aanwezigheid van allo-antistoffen, hetgeen bij 27 weken wordt herhaald bij alle resus D- en resus kleine-c-negatieve zwangeren.
Bij aanwezigheid van allo-antistoffen volgt in de regel nadere typering om het klinisch belang voor de zwangerschap vast te stellen, vaak gevolgd door typering van de bloedgroep van de biologische vader. Dit om bijvoorbeeld uit te zoeken of er sprake is van hetero- of homozygotie. Afhankelijk van de gevonden antigenen bij vader kan het zinvol zijn de bloedgroep van de foetus met behulp van DNA geïsoleerd uit het plasma van de moeder of uit vruchtwater vast te stellen. Afhankelijk hiervan wordt het verdere beleid bepaald. Is er sprake van antistoffen die kunnen leiden tot hemolyse, zie dan verder specialistisch beleid.
Specialistisch beleid
Indien de zwangere antistoffen heeft, is kennis van de bloedgroep van de foetus van grote waarde. Is het kind bijvoorbeeld resus D-, resus c- of kell-negatief, dan is er geen kans op hemolyse door de antistoffen. Is het kind positief, dan is die kans wel aanwezig en moet diagnostiek naar tekenen van hemolyse worden verricht. Hiervoor gebruikt men de antibody-defendant cell medicated erytotoxicity-test (ADCC). Deze test bepaalt de kans dat er sprake is van hemolyse en wordt circa elke twee weken herhaald. Verder kan de bloedstroomsnelheid in de arteria cerebri media van de foetus worden gemeten, omdat dit een goede maat is voor anemie.
Bij tekenen van anemie kan een intra-uteriene transfusie worden gegeven. Dit gebeurt uitsluitend in het Leids Universitair Medisch Centrum op de afdeling Obstetrie.
Na de geboorte controle op hemolyse en zo nodig wisseltransfusie.
Preventie van resus D-sensibilisatie
Het anti-D-gammaglobuline dient liefst te worden toegediend binnen 24-48 uur, maar is mogelijk nog zinvol tot 7 dagen post partum:
na partus van een resus-positief kind (1.000 IE);
na een spontane miskraam ≥ 10weken en altijd bij abortus provocatus, curettage en na een EUG (375 IE);
na amnionpunctie en vlokkentest, bij bloedverlies tijdens de zwangerschap en na uitwendige versie(poging) (375 IE).
Met ingang van 1 juli 2011 is de preventie van resussensibilisatie in de zwangerschap veranderd. Bij 27 weken wordt uit het maternale serum de aanwezigheid van anti-D-antistoffen en de foetale bloedgroep/resusfactor bepaald. Elke resus-negatieve zwangere die een resus-postitief kind verwacht en geen anti-D-antistoffen heeft, krijgt bij 30 weken en direct post partum 1.000 IE anti-D-gammaglobuline i.m. toegediend. In sommige situaties is een dubbele gift anti-D nodig op geleide van de uitslag van de kleihauer-betketest.
Anno 2014 is er nog geen preventie voor resus-c-sensibilisatie. Opsporen, vervolgen en waar nodig foetale anemie behandelen zijn momenteel de behandelingsopties.
Diabetes mellitus en zwangerschapsdiabetes
Zie ook ▶ H. 10.1007/978-90-368-0610-7_3 Endocrinologie.
Er dient onderscheid gemaakt te worden tussen bestaande (en behandelde) diabetes mellitus (1 en 2) en zwangerschapsdiabetes. Voor het beleid bij diabetes mellitus zijn de volgende punten van belang:
bij type 1 en 2 streven naar goede instelling vóór de zwangerschap (HbA1c < 7); hiermee verkleint men de kans op congenitale afwijkingen;
verder streven naar nuchtere bloedsuikers < 7 mmol/l.; controles door internist en gynaecoloog!
echoscopie bij 20 weken: congenitale afwijkingen;
echoscopische groeicontrole vanaf circa 30 weken;
zwangerschap meestal niet langer dan 40 weken laten bestaan.
Invloed van diabetes mellitus op de zwangerschap
een kind met aangeboren afwijkingen (onder andere hart en nieren);
een vroeggeboorte;
een intra-uteriene vruchtdood in het 3e trimester;
een macrosoom kind met daardoor meer kans op een schouderdystocie.
Door de diabetogene werking van de zwangerschap verergert een bestaande diabetes mellitus en kan deze veel moeilijker te reguleren zijn dan buiten de zwangerschap, terwijl goed gereguleerd zijn voor de zwangerschapsuitkomst uitermate belangrijk is.
Tijdens de zwangerschap kan bij een gezonde vrouw ook een tijdelijke stoornis van de suikerstofwisseling ontstaan: zwangerschapsdiabetes . Deze aandoening ontstaat vrijwel altijd na 20-24 weken. Over het bestaan van en de therapie voor deze aandoening is nog steeds de nodige discussie.
Over screening voor zwangerschapsdiabetes (GDM) is veel discussie. Screening van alle zwangeren wordt niet zinvol geacht (tabel 22.2). Vrouwen met een verhoogd risico op GDM worden zowel in het 1e als in het 2e trimester gescreend. Indicaties voor screening zijn:
GDM in voorgeschiedenis (dan bij 16 én tussen 24 en 28 weken OGTT);
BMI > 30 kg/m2 bij de eerste prenatale controle;
eerstegraads familielid met diabetes;
eerder kind met geboortegewicht > P95 of > 4500 g;
een onverklaarde intra-uteriene vruchtdood in de voorgeschiedenis: polycysteusovariumsyndroom;
bepaalde etnische groepen waarin diabetes veel voorkomt (Zuid-Aziaten o.a. Hindoestanen, Afro-Caribiërs, vrouwen uit het Midden-Oosten, Marokko en Egypte).
|
screening 1e trimester |
random glucosebepaling zo nodig gevolgd door nuchtere glucose (< 6,1 mmol/l) NB bij > 11 mmol/l DM, direct verwijzen naar gynaecoloog) |
|
screening 2e trimester |
zie diagnostiek |
| diagnostiek: |
OGTT met 75 g glucose (nuchter < 7,0 mmol/l; 2 uurs < 7,8 mmol/l) Bij 1 of 2 afwijkende waarde(n) diagnose zwangerschapsdiabetes (GDM) |
| behandeling: |
- eerst dieet + controle dagcurve; - is dagcurve nog niet normaal dan insuline; - indien er sprake is van insulinegebruik en/of macrosomie (FAO > P95) vinden controles en partus plaats in de tweede lijn. In andere gevallen wordt de lokale afspraak gevolgd |
| NB. screening d.m.v. glucosecontrole in de urine is zinloos | |
Indien in de zwangerschap een symptoom zoals macrosomie (groei > P95 van met name de FAC) of polyhydramnion verdenking geeft op GDM, wordt diagnostiek door middel van OGTT verricht.
Infectieziekten in de zwangerschap: hepatitis B , varicella zoster , herpes , groep B-streptokok , parvovirus
Het doormaken van een infectieziekte in de zwangerschap heeft zowel voor de moeder als voor de foetus/neonaat soms ernstige consequenties. In de zwangerschap gaat een infectie van de moeder veel vaker dan buiten de zwangerschap gepaard met ernstige complicaties voor de moeder (bijvoorbeeld influenza). Tevens zijn er infectieziekten waarbij sprake is van een verhoogd risico op congenitale afwijkingen (bijvoorbeeld rubella), ontwikkelingsstoornissen (bijvoorbeeld cytomegalie) of sterfte (bijvoorbeeld listeriose).
Voor een goed en compleet overzicht van diagnose en therapie bij infectieziekte in de zwangerschap zie RIVM.nl/zwangerschapeninfectieziekten.
De volgende selectie uit infectieziekten en zwangerschap is gemaakt, omdat vragen hierover regelmatig terechtkomen bij de verloskundig niet-actieve huisarts.
Hepatitis B
Bepaling van HBsAg is een standaardbepaling bij elke zwangere bij de eerste controle. Incidentie: 2% van de Nederlandse bevolking heeft hepatitis B doorgemaakt waarbij 10% drager blijft (88% van de dragers is van niet-Nederlandse afkomst).
Bij een positieve screening wordt vervolgens HBeAg bepaald; aanwezigheid van dit e-antigeen wijst op een sterke virusvermeerdering met een hoge besmettelijkheid en een kans op verticale transmissie tijdens of na de baring van 85%. In het derde trimester kan behandeling met antiretrovirale middelen worden overwogen om deze kans te verkleinen.
Er is vrijwel nooit sprake van intra-uteriene besmetting van de foetus tijdens de zwangerschap; besmetting vindt plaats door contact met het moederlijk bloed tijdens de geboorte. Voor bescherming neonaat: zie ▶ H. 31. Elke zwangere die HBeAg-positief is en/of gestoorde leverfuncties heeft dient te worden doorverwezen naar de maag-darm-leverspecialist.
Varicella zoster en herpes zoster
Varicella zoster (waterpokken) wordt veroorzaakt door het (herpes) varicellazostervirus. De infectie heeft zowel voor de zwangere als voor de foetus soms ernstige gevolgen. Herpes zoster (gordelroos) is onschuldig; het is een recidief infectie, waarbij de moeder antistoffen meegeeft aan haar pasgeborene.
Zwangere: het doormaken van een varicellazosterinfectie in de zwangerschap heeft een risico van 5-10% op ernstige complicaties bii de zwangere zoals varicellapneumonie met een sterftekans van 14%.
Embryo/foetus: het doormaken van de infectieziekte veroorzaakt in het eerste trimester in 0,4% van de gevallen het congenitaal varicellasyndroom (hypoplasie van extremiteiten, afwijkingen van het centrale zenuwstelsel, van de ogen en van de huid), tussen 13 en 20 weken is dit percentage 2. Het varicellasyndroom wordt niet beschreven bij een besmetting na 20 weken zwangerschap.
Neonaat: varicella bij de moeder binnen vijf tot zeven dagen voor de partus tot twee tot vijf dagen na de geboorte kan oorzaak zijn van varicella bij de neonaat. De moeder beschikt dan nog niet over voldoende antistoffen om het kind passief te beschermen. Vooral bij prematuren is het gevaar op ernstige ziekte groot. Het kind moet passief worden geïmmuniseerd met varicellazoster-hyperimmuunserum (VZIG 50 IE/ml i.m.) en eventueel met aciclovir worden behandeld. Besmetting via derden (broertjes en zusjes) rond de bevalling verloopt minder ernstig. De pasgeborene doorloopt de infectie en bouwt zelf antistoffen op.
Beleid bij zwangere die contact heeft gehad met een varicellapatiënt:
Als de zwangere de ziekte heeft doorgemaakt in het verleden is verdere actie niet nodig, de anamnese is zeer betrouwbaar gebleken (bijna 100%).
Bij een risicocontact en reële blootstelling (zie verder) minder dan 4 dagen geleden moet met spoed de serostatus worden bepaald (verloskundig zorgverleners zijn op de hoogte van de spoedprocedure). Varicellazoster-immuunglobulinen worden in geval van seronegativiteit toegediend.
Toedienen van de immuunglobulinen 4 dagen na het risicocontact is zinloos.
Reële blootstelling wordt omschreven als:
gezinscontact: deel uitmaken van hetzelfde huishouden als de VZV-patiënt;
gezichtscontact (minder dan 2 meter) met een VZV-patiënt gedurende ten minste 5 minuten;
gedurende langer dan 1 uur in dezelfde ruimte verblijven als de VZV-patiënt;
Herpes simplex
Besmetting van de neonaat treedt op tijdens de baring (HSV type 2, herpes genitalis) of in/na de kraamperiode (HSV type 1, herpes labialis). Hoewel de neonaat na een besmetting relatief zelden ziek wordt (incidentie 2 à 3 per 100.000 levendgeborenen), is het verloop van de ziekte zeer ernstig met een hoge mortaliteit (70% bij gegeneraliseerde infectie!). Voor het verloop van de ziekte bij de pasgeborene is het van ondergeschikt belang of er sprake is van HSV type 1 of HSV type 2.
Het grootste risico op besmetting van de pasgeborene bestaat bij een primo-infectie (er zijn nog geen antistoffen) in de laatste 6 weken van de zwangerschap. In deze situatie wordt een primaire sectio verricht. Indien er sprake is van een recidief ten tijde van de baring, kan een vaginale baring geaccepteerd worden, waarbij de vliezen zo lang mogelijk blijven staan en geen schedelelektrode/MBO-onderzoek wordt verricht. Er worden kweken afgenomen bij de neonaat en hij/zij wordt 48 uur intensief geobserveerd. Een thuisbevalling is geen bezwaar, mits voorgaande maatregelen worden getroffen.
Indien er sprake is van een recidief tijdens de zwangerschap, zijn kweken en behandeling met aciclovir niet nodig (bij twijfel over primo-infectie wel onderzoek verrichten!).
Groep B-streptokokken
De groep B-streptokok (GBS) is jaarlijks oorzaak van 15-20 gevallen van perinatale/neonatale sterfte/ernstige morbiditeit. In Nederland is het percentage draagsters 15-20, waarbij in de helft van de gevallen de baby via verticale transmissie gekoloniseerd raakt. Hiervan krijgt (slechts) 1-2% ook daadwerkelijk de infectie, die in alle gevallen zorgt voor zeer ernstig zieke kinderen en een zich extreem snel ontwikkelend ziektebeeld met mogelijk sterfte en morbiditeit als gevolg .
In Nederland is geen screening van alle zwangeren op GBS-dragerschap. Wel dient bij een cystitis altijd een kweek te worden ingezet om GBS op te sporen/uit te sluiten. GBS in de urine wijst op een hoge kolonisatiegraad en is een reden voor behandeling alsmede voor antibioticaprofylaxe tijdens de ontsluitingsperiode (zie verder).
GBS-dragerschap risicofactoren:
vroeggeboorte (< 37 weken);
langdurig gebroken vliezen (> 18-24uur);
maternale koorts durante partu;
ernstige maternale kolonisatie in de huidige zwangerschap (GBS in urinekweek);
eerder kind met bewezen GBS-infectie.
Bij GBS-dragerschap zonder risicofactoren zijn geen bijzondere maatregelen nodig; goede observatie van de neonaat en instructie van kraamzorg en ouders zijn uiteraard wel noodzakelijk. Indien er sprake is van een of meer van de hiervoor genoemde risicofactoren is antibioticaprofylaxe geïndiceerd. Hiertoe wordt intraveneus 5 miljoen IE penicilline G of 2 gram amoxicilline/ampicilline toegediend, waarna elke 4 uur 2,5 miljoen IE of 1 gram toegediend wordt tot aan de geboorte. Bij allergie kan clindamycine (900 mg i.v. elke 8 uur) of erytromycine (500 mg i.v. elke 6 uur) worden gegeven
Er is sprake van adequate antibioticaprofylaxe als ten minste twee giften AB zijn gegeven voordat het kind wordt geboren. Bij adequate profylaxe wordt het kind na de geboorte 24-48 uur klinisch geobserveerd. Inadequate profylaxe is veelal een indicatie tot opname en AB-therapie bij de baby.
Bij de ‘early onset’ infectie staan de respiratoire problemen op de voorgrond; bij de ‘late onset’ infectie zijn symptomen van meningitis kenmerkend.
Informatie over GBS-dragerschap dient te worden overgedragen aan de verloskundig zorgverlener.
Parvovirus (‘vijfde ziekte’)
Humaan parvovirus B19 is de verwekker van de kinderziekte erythema infectiosum (‘vijfde ziekte’) , een rubella-achtige exanthemateuze aandoening, met vlindervormig exantheem op de wangen (appelwangen) en lichte temperatuurverhoging, die na enkele weken zonder problemen geneest. De ziekte komt vaak voor bij kinderen op de kindercrèche.
Het virus repliceert in de voorlopers van de erytrocyten: de reticulocyten. Bij infectie van een zwangere (licht koortsende ziekte met soms langdurig gewrichtspijn) kan in het begin van de zwangerschap vruchtdood ontstaan; in het tweede trimester, wanneer het bloedvolume van de foetus sterk toeneemt, kan hydrops foetalis optreden ten gevolge van anemie. Dit kan eventueel ook leiden tot vruchtdood. Bij een mild verloop kan spontaan herstel optreden. Een infectie na de twintigste week veroorzaakt geen intra-uteriene infectie meer. Het is wel mogelijk dat een infectie in het eerste trimester pas later symptomen geeft.
De diagnostiek wordt gesteld door het aantonen van parvovirus B19 IgM- en IgG-antistoffen. IgM-antistoffen blijven 2 tot 6 maanden aantoonbaar in het bloed. Bij foetale anemie en hydrops foetalis op basis van een infectie met het parvovirus kan een intra-uteriene bloedtransfusie via chordocentese levensreddend zijn. Gevaar dreigt wanneer deze ziekte zich voordoet bij kinderen op de kindercrèche, waardoor bij zwangeren die de infectie niet eerder doormaakten, de foetus geïnfecteerd kan worden. Bij vrouwen die werken met risicogroepen wordt IgM- en IgG-bepaling geadviseerd aan het begin van de zwangerschap.
Dreigende vroeggeboorte
We spreken van vroeggeboorte of preterme geboorte bij een partus vóór 37 weken. De symptomen van dreigende vroeggeboorte zijn weeënactiviteit gepaard met verstrijken en ontsluiten van de cervix. In 30% van de gevallen begint een vroeggeboorte met het aflopen van vruchtwater. De oorzaak is doorgaans onbekend, soms secundair aan algemene stoornissen (zoals een koortsende ziekte), afwijkingen van de zwangerschap (hydramnion, atypische abruptio placentae), afwijkingen aan het corpus of de cervix van de uterus of aangeboren afwijkingen van de foetus (zie specialistische therapie). Vroeggeboorte dient te worden onderscheiden in spontane vroeggeboorte (60% van de gevallen), waarbij door weeënactiviteit de baring op gang komt, en iatrogene vroeggeboorte (40% van de gevallen), waarbij de specialist de zwangerschap beëindigt, omdat dit beter is voor het kind of voor de moeder.
Soms is vroeggeboorte het gevolg van een cervixinsufficiëntie. In dat geval kan vroeg in een volgende zwangerschap bij 12-16 weken met een kunststof bandje de cervix worden versterkt (cerclage). Na 37 weken of als de bevalling eerder op gang komt, wordt dit bandje verwijderd.
Diagnose
De diagnose dreigende vroeggeboorte is niet altijd eenvoudig te stellen. Klinische tekenen van dreigende vroeggeboorte zijn:
de klacht: ‘weeën’; en
objectiveerbare regelmatige contracties van de uterus, elke 5-10 minuten; en
portioveranderingen; of
gebroken vliezen, al of niet in combinatie met uterusactiviteit en/of bloedverlies.
Bij een dreigende vroeggeboorte is onderzoek naar een (urineweg)infectie aangewezen, ook bij vrouwen zonder klachten, en is oriënterend echoscopisch onderzoek aangewezen.
Specialistische therapie
De behandeling bestaat uit opname in het ziekenhuis, bedrust en behandeling van een eventueel infectieuze ziekte. Daarnaast is evaluatie van de zwangerschap nodig: groeiretardatie? macrosoom kind? hydramnion?
Medicamenteuze behandeling bij dreigende vroeggeboorte bestaat uit toediening van weeënremmende medicatie (tocolyse) en corticosteroïden. Tocolyse heeft geen zin als het risico voor het kind in utero groter is dan daarbuiten. Zo is weeënremming (relatief) gecontra-indiceerd bij een intra-uteriene infectie, pre-eclampsie of foetale nood. De diverse middelen hebben ook hun specifieke relatieve contra-indicaties. Vergevorderde ontsluiting is op zich geen reden om weeënremming na te laten. Ook vaginaal bloedverlies is geen contra-indicatie voor weeënremming. Bij nog korte zwangerschapsduur (< 34 weken) en goede conditie van de foetus kan weeënremming met atosiban of nifedipine, altijd in combinatie met corticosteroïden ter bevordering van de foetale longrijping, zinvol zijn. Langdurige toepassing van weeënremming intraveneus of oraal heeft waarschijnlijk weinig zin.
Van weeënremming is bewezen dat een bevalling significant minder vaak plaatsvindt in de eerste dagen na toediening vergeleken met placebo. Dit heeft als groot voordeel dat in die periode door toediening van corticosteroïden de longrijping bevorderd kan worden. Bovendien kan die tijd gebruikt worden om de vrouw over te plaatsen naar een van de tien centra voor neonatale intensieve zorg (de zgn. ‘intra-uteriene’ overplaatsing).
Liggingsafwijkingen in de zwangerschap
De meeste voorkomende liggingsafwijking is de stuitligging (3,5% bij à terme graviditeit). Oorzaken zijn verminderde stabiliteit van de hoofdligging (slappe buikwand bij multipara, bekkenvernauwing, placenta praevia, vroeggeboorte, schedelafwijkingen van het kind) en verhoogde stabiliteit van stuitligging (oligohydramnion, strakke buikwand bij nullipara, onvolkomen stuitligging, soms congenitale afwijkingen van de uterus of het kind).
Bij een zwangerschapsduur van 20-25 weken ligt 30-40% van de foetussen in stuitligging, rond de 32 weken is dit 10-15%, terwijl dit percentage in de à terme periode is gedaald tot circa 3,5%. Bij kinderen die in stuitligging worden geboren is de kans op congenitale afwijkingen verhoogd.
Bij stuitligging bestaat tijdens de baring een verhoogde kans op complicaties door uitzakken van de navelstreng, hypoxie en acidemie. Daarnaast is er een grotere kans op mechanisch letsel door niet-vorderen van de baring vanaf de romp, waarbij (partiële) extractie nodig is, met als mogelijke gevolgen cerebraal letsel, plexuslaesies, fracturen van thoracale en lumbale wervelkolom en een leverruptuur. Een minder vaak voorkomende liggingsafwijking is de dwarsligging. Hierbij is er geen sprake van een voorliggend deel.
Diagnose
Berust op de anamnese en de bevindingen bij lichamelijk onderzoek (vorm en omtrek van de uterus; palpatie van hoofd, rug en stuit en plaats van foetale harttonen). Aanvullend onderzoek bestaat uit echoscopie van foetus en placenta.
Therapie
Bij stuitligging en dwarsligging is een poging tot versie naar hoofdligging (eventueel onder tocolyse) aangewezen, bij voorkeur bij een zwangerschapsduur van 35-37 weken. Relatieve contra-indicaties voor uitwendige kering zijn: bloedverlies in de graviditeit, hypertensie, litteken in de uterus, gebroken vliezen. Controle van de foetale hartslag voor en na iedere versie is aan te bevelen. Bij persisteren van de stuitligging en geen andere risicofactoren (groot kind, voetligging, etc.) kan een vaginale partus worden overwogen, maar kan ook een primaire sectio caesarea worden afgesproken. Dit in overleg met de as. ouders.
(Poly)hydramnion
Meest voorkomende oorzaken zijn: congenitale afwijkingen van het kind, tweeling transfusiesyndroom (TTS ) en diabetes mellitus. Meestal wordt geen oorzaak gevonden.
Diagnose
Positieve discongruentie; bij palpatie zijn delen van het kind moeilijk te voelen en harttonen moeilijk hoorbaar: door middel van echoscopisch onderzoek kan de diagnose gesteld worden (grootste vruchtwaterpocket > 8 cm).
Vervolgens kan gericht onderzoek naar de hiervoor genoemde oorzakelijke stoornissen (echoscopie/glucosebepaling) gedaan worden
Specialistische therapie
Bij voorkeur expectatief, uiteraard afhankelijk van de oorzaak; slechts ontlastende amnionpunctie bij ernstige mechanische klachten. Bij TTS is lasercoagulatie van de vaatverbindingen aangewezen. Deze behandeling wordt in Nederland alleen in het Leids Universitair Centrum verricht.
Meervoudige zwangerschap
Bij ongeveer 2% van de zwangerschappen is er op dit moment sprake van een tweeling. De frequentie is toegenomen door het stijgen van de leeftijd van de zwangere en door het toegenomen gebruik van voortplantingstechnieken zoals ovulatie-inductie en in-vitrofertilisatie. Door ovulatie-inductie ontstaan nog steeds zwangerschappen met drie of meer foetussen. Bij grote meerlingen wordt embryo-reductie nogal eens toegepast.
Risico’s van een meervoudige zwangerschap zijn: spontane vroeggeboorte, anemie van de zwangere, abnormale ligging van de kinderen, zwangerschapshypertensie, foetale groeiachterstand, weeënzwakte, kunstverlossingen en fluxus post partum. Het risico neemt toe met het aantal foetussen. Bij de geboorte verkeert het tweede kind soms in slechtere conditie door verminderde placentafunctie na de geboorte van het eerste kind.
Diagnose
Positieve discongruentie, het vinden van meer zones van harttonen, het palperen van meer dan twee grote delen.
Aanvullende diagnostiek: echoscopie. Door vrij algemeen toepassen van de zogenoemde ‘termijn-echo’, bij 10 tot 14 weken amenorroe, worden nu vrijwel alle meerlingzwangerschappen vroeg in de zwangerschap vastgesteld. Het is wenselijk om vroeg in de zwangerschap (bij voorkeur tussen 7 en 12 weken) vast te stellen en te documenteren of er sprake is van een mono- of diamniotische en vooral mono- of dichoriale zwangerschap (op basis van het echoscopisch aspect van het tussenschot). Dit omdat er bij een monochoriale zwangerschap kans is op een transfuseur-transfusésyndroom (TTS). Bij monochorioniciteit zijn er vaatverbindingen tussen beide placentae en bij het TTS-syndroom pompt de ene foetus meer bloed naar de andere foetus dan deze terugkrijgt. Het ene kind raakt overvuld, het andere wordt anemisch.
Specialistische therapie
Specialistische controle, met regelmatig echoscopisch onderzoek voor controle van de foetale groei en verschillen in groei, en tijdig opsporen van het, bij monochorialen – bij circa 10% – voorkomende, TTS-syndroom (transfuseur-transfusésyndroom).
(Zwangerschaps)hypertensie , (pre-)eclampsie en HELLP
Hypertensieve aandoeningen in de zwangerschap zijn een belangrijke oorzaak van perinatale morbiditeit en mortaliteit, kunnen ernstige maternale morbiditeit veroorzaken en vormen de belangrijkste oorzaak van maternale sterfte. Reeds vroeg in de zwangerschap dalen de systolische en diastolische bloeddruk, met 10-15 mmHg tot circa 30 weken, om weer te stijgen tot de uitgangswaarde.
In de zwangerschap wordt hypertensie gedefinieerd als een systolische bloeddruk ≥ 140 mmHg en/of een diastolische bloeddruk ≥ 90 mmHg (Korotkov V).
Er moet onderscheid gemaakt worden naar:
Chronische hypertensie. De bloeddruk is reeds voor de zwangerschap en/of voor 20 weken zwangerschap verhoogd.
Zwangerschapshypertensie. De hypertensie ontstaat na 20 weken bij een voorheen normotensieve vrouw
Pre-eclampsie. Er is naast hypertensie sprake van proteïnurie (≥ 300 mg/24 uur). Hierbij kunnen nierfunctiestoornissen, leverfunctiestoornissen (pijn boven in de buik), neurologische afwijkingen (ernstige hoofdpijn, visusstoornis, hyperreflexie, en convulsies bij eclampsie) en hematologische afwijkingen optreden. De combinatie van hemolyse, verhoogde leverenzymen en verlaagde trombocyten wordt HELLP genoemd.
Gesuperponeerde hypertensie/pre-eclampsie. Bij een patiënte met chronische hypertensie ontstaan na 20 weken symptomen die geassocieerd zijn met pre-eclampsie.
Eclampsie. Als na eerdergenoemde verschijnselen eclamptische aanvallen optreden: een korte tonische fase gevolgd door klonische krampen van extremiteiten en andere spiergroepen. Naast het risico van verwondingen hierdoor, bestaat er gevaar van aspiratiepneumonie en cerebrale bloedingen. Het kind kan door hypoxie worden bedreigd
Obstetrische complicaties zijn infarcering van de placenta, groeivertraging van het kind, eventueel intra-uteriene vruchtdood en abruptio placentae. Bij de moeder kan de verhoogde bloeddruk leiden tot eclampsie en eventueel hersenbloeding. Bij het ontstaan van het ziektebeeld spelen immunologische, genetische en omgevingsfactoren een rol. Hoewel de etiologie nog niet volledig is opgehelderd, lijken een deficiënte aanleg en vascularisatie van de placenta en het uitblijven van de maternale vaat-adaptatie eraan ten grondslag te liggen.
Er zijn diverse predisponerende factoren, waaronder nullipariteit, leeftijd > 40 jaar, chronische hypertensie, diabetes, adipositas, meerling- en molazwangerschap.
Diagnose
Om deze beelden te kunnen differentiëren, dient men te beschikken over een bloeddrukmeting vóór de zwangerschap of in het eerste trimester; bovendien is bloeddrukmeting na afloop van het kraambed (4-6 weken post partum) van belang om te weten of buiten de zwangerschap hypertensie aanwezig is.
Bij elke zwangerschapscontrole is bloeddrukmeting een vast onderdeel. Er wordt gebruikgemaakt van een handmatige bloeddrukmeter die wordt afgelezen op 2 mmHg nauwkeurig bij de vrouw in zittende positie na 2-3 minuten rust, waarbij Korotkov V wordt gebruikt. Automatische bloeddrukmeters zijn niet gevalideerd in de zwangerschap! Tevens dient de bloeddruk te worden gemeten indien de vrouw minder leven voelt of zich meldt met één of meerdere pre-eclamptische klachten (hoofdpijn, pijn/knellend gevoel in bovenbuik, visusstoornissen). Geïsoleerde bovenbuikpijn is een belangrijk symptoom in de tweede helft van de zwangerschap, waarbij altijd aan pre-eclampsie/HELLP gedacht moet worden. Bij HELLP kan er aanvankelijk sprake zijn van een milde hypertensie samen met het voor het overige ernstige ziektebeeld!
Indien er sprake is van hypertensie en/of pre-eclamptische klacht(en), dient ook urine te worden onderzocht op albumine.
Therapie
Matig ernstige hypertensie (systolisch ≥ 140 en < 170 mmHg of diastolisch ≥ 90 en < 110)
Bij chronische hypertensie verwijzen naar de gynaecoloog en instellen op veilige antihypertensiva: géén ACE-remmers (teratogene effecten, kans op nierbeschadiging foetus, intra-uteriene sterfte)!
Bij zwangerschapshypertensie verwijzen naar verloskundige zorgverlener die, afhankelijk van zwangerschapsduur, beleid zal bepalen. Indien verwijzing naar gynaecoloog nodig is, volgen er intensieve controles; moeder: controle proteïnurie, leverenzymen, nierfunctie, stolling (trombocyten); kind: foetale groei door middel van echoscopie, foetale conditie door middel van echo-doppleronderzoek en CTG.
Behandeling met extra rust, zo nodig klinisch. Zoutbeperking is niet zinvol en dient niet te worden geadviseerd.
Medicamenteuze therapie: methyldopa, labetalol, nifedipine altijd bij RR systolisch ≥ 170 mmHg en diastolisch ≥ 110 mmHg, maar kan ook zeker zinvol zijn bij RR diastolisch 95-110, afhankelijk van de zwangerschapsduur. Magnesiumsulfaat is het meest effectieve medicament voor preventie van eclampsie en ter voorkoming van volgende insulten na eclampsie.
Matig ernstige pre-eclampsie , (bloeddruk als boven, proteïnurie zonder klinische verschijnselen)
Opname in een ziekenhuis met intensieve controle van maternale en foetale conditie. Voor medicamenteuze antihypertensieve therapie: zie hiervoor. De keuze ten aanzien van wel/geen magnesiumsulfaat berust bij het ziekenhuis.
Ernstige pre-eclampsie, HELLP
Behandeling van beide ziektebeelden is identiek en bestaat in eerste instantie uit stabilisatie van de bloeddruk ter preventie van hersenbloeding en magnesiumsulfaat ter preventie van eclampsie De enige behandeling om deze ziekte definitief te genezen is het beëindigen van de zwangerschap. Dit laatste is natuurlijk sterk afhankelijk van de zwangerschapsduur, de ernst van de ziekte en de conditie van de moeder en de foetus.
De eerste medicamenteuze keuze bij of na een eclamptisch insult is magnesiumsulfaat i.v. of i.m. Bij een insult thuis eenmalig diazepam 10 mg rectaal. Eclamptische insulten post partum ontstaan meestal in de eerste 48 uur, maar zijn tot 2 weken na de bevalling beschreven.
Serotiniteit
Vanaf een (zekere) zwangerschapsduur van 42 weken (294 dagen) is er sprake van serotiniteit . Er bestaat dan een licht verhoogde kans op verslechtering van de foetale conditie. Vanaf 42 weken dient de foetale conditie om de dag te worden gevolgd door middel van CTG en kan de baring door inleiden worden nagestreefd.
In veel VSV’s is afgesproken bij 10 dagen overtijd en ongestoorde zwangerschap een consult met CTG en echo te verrichten in het ziekenhuis. Tevens kan vanaf 41 weken, conform de NVOG-richtlijn Serotiniteit, de mogelijkheid van inleiden besproken worden.
Diagnose
De diagnose wordt gesteld op grond van de vastgestelde à terme datum. Een vroege termijnbepaling door middel van echoscopie in het eerste trimester is daarbij het meest betrouwbaar.
Specialistische therapie
Specialistische behandeling en bewaking zijn noodzakelijk. Inleiden overwegen, maar als anamnese, obstetrisch en echoscopisch onderzoek en cardiotocogram optimaal zijn, is er geen dwingende indicatie tot het beëindigen van de zwangerschap bij serotiniteit.
Medicatie tijdens de zwangerschap
Bij het toedienen van ieder medicament in iedere fase van de zwangerschap dient men zich te realiseren dat alle kleinmoleculaire stoffen in principe de placenta zullen passeren. Van sommige medicamenten zal de concentratie in foetaal bloed en in vruchtwater gelijk zijn aan die van de serumconcentratie bij de moeder. Bij andere medicamenten blijkt echter een cumulatie in het kind op te treden. Hierbij kan de concentratie in foetaal bloed en vruchtwater vele malen hoger worden dan die in het moederlijke bloed (bijv. diazepam).
Enkele algemene richtlijnen:
In het eerste trimester van de zwangerschap dient bij de toediening van ieder medicament in principe rekening gehouden te worden met mogelijk teratogene effecten.
Na de embryonale fase moet bij iedere medicatie rekening worden gehouden met negatieve effecten op het foetale metabolisme en de foetale groei.
Tijdens de baring moet bovendien rekening worden gehouden met effecten ten aanzien van vitale functies als circulatie en ademhaling, die zich op het moment van de geboorte toch al ingrijpend dienen aan te passen.
Bij vrouwen die continu behandeld worden met medicamenten, dient reeds vóór de zwangerschap met de patiënte en eventueel behandelend specialisten overlegd te worden over risico’s van deze medicatie in de zwangerschap; soms zal de medicatie vóór de zwangerschap gewijzigd kunnen worden en soms geheel gestaakt. Een dergelijke nauwkeurige evaluatie geldt bijvoorbeeld voor antihypertensiva, psychofarmaca, anti-epileptica, thiouracilderivaten bij hyperthyreoïdie, orale antidiabetica, cytostatica en coumarinederivaten.
Bij vrouwen die behandeld worden voor hypothyreoïdie moet de medicatie zo vroeg mogelijk worden aangepast. De dosering moet meestal met 25-50% worden verhoogd, omdat de foetus in de eerste helft van de zwangerschap voor zijn schildklierhormonen volledig afhankelijk is van de moeder.
In de zwangerschap zijn het gebruik van tetracycline, streptomycine, sulfonamiden, jodiumpreparaten en secale alkaloïden gecontra-indiceerd.
Vaccinatie en zwangerschap: toedienen van ‘levende vaccinaties’ wordt afgeraden tijdens de zwangerschap. Toedienen van griepvaccinaties is standaard niet noodzakelijk bij de zwangere, maar risicogroepen dienen ook in de zwangerschap gevaccineerd te worden.
Nederlandse artsen zijn over het algemeen, terecht, zeer terughoudend met het voorschrijven van medicatie aan zwangere vrouwen. Toch moeten ook in de zwangerschap de nadelen van de medicatie en de nadelen van het onthouden van medicatie goed worden afgewogen.
Raadpleeg bij medicijngebruik niet het Farmacotherapeutisch Kompas, maar de informatie van het Lareb, bij voorkeur de online versie van Geneesmiddelen, zwangerschap en borstvoeding. met de laatste update (http://www.lareb.nl/Teratologie/Naslagwerk-GZB).
Voor individuele adviezen: Teratologie Informatie Service van het Lareb: tel. 073-6469702 (alleen voor zorgverleners).
Specialistische controle bij overige (verdenking op) pathologie
Bij een abnormaal verloop van de zwangerschap , respectievelijk bij verhoogd risico op een abnormaal verloop, staan de specialist veel mogelijkheden voor aanvullende diagnostiek ter beschikking. De voornaamste van deze technieken worden beschreven.
Amniocentese
Het via een punctie verkrijgen van vruchtwater met daarin foetale cellen. Indicaties: hogere leeftijd van de moeder (vanaf 36 jaar bij 18 weken zwangerschap), eerder kind met een chromosoomafwijking (familiair voorkomen van neuralebuisdefecten wordt tegenwoordig met GUO (geavanceerd ultrasonisch onderzoek) onderzocht), familiair voorkomen van geslachtsgebonden overerfbare ziekten, familiair voorkomen van bepaalde stofwisselingsziekten. Punctie kan vanaf 16 weken. Ook in ervaren handen heeft de punctie een risico van circa 0,3% op miskraam of preterme partus.
Met de invoering van NIPT zal het aantal vruchtwaterpuncties met indicatie trisomie 13,18 en 21 verminderen.
Chorionbiopsie (CVB)
Kan worden uitgevoerd na 11 weken, transcervicaal of transabdominaal, voor de detectie van chromosoomafwijkingen, geslachtsgebonden afwijkingen, DNA-afwijkingen en stofwisselingsziekten. De uitslag van het onderzoek is sneller en vroeger beschikbaar dan na een vruchtwaterpunctie. Het risico van de ingreep op miskraam is iets hoger dan dat van een vruchtwaterpunctie.
Echoscopie
Ter bepaling van de zwangerschapsduur vroeg in de zwangerschap, opsporen van meerlinggraviditeit, ter controle van de groei, placentalokalisatie en het detecteren van congenitale afwijkingen bij het kind.
Echo-doppleronderzoek
Hiermee kan het bloedstroomsnelheidsprofiel worden gemeten. In de arteria umbilicalis wijst een afwijkend profiel op een niet goed functionerende placenta, waardoor de foetus onvoldoende voedingsstoffen en uiteindelijk onvoldoende zuurstof krijgt. Extra bewaking door middel van echoscopie en CTG is dan geindiceerd.
Bij allo-antistoffen, zoals bij de resussensibilisatie, wijst een verhoogde bloedstroomsnelheid in de arteria cerebri media op anemie.
Cardiotocografie (CTG)
Dit onderzoek, waarbij de hartfrequentie van de foetus en (eventuele) baarmoedercontracties simultaan worden geregistreerd, geeft inzicht in de actuele toestand van de foetus. Minder leven voelen is een indicatie voor een CTG.
Onderzoek van het vruchtwater (na amniocentese) in het derde trimester van de zwangerschap
Door bepaling van de L/S-ratio (de verhouding tussen de fosfolipiden lecithine en sfyngomyeline) kan de rijpheid van de foetale longen worden voorspeld. Geeft deze bepaling aan dat de longen nog niet rijp zijn, dan kunnen corticosteroïden deze rijping versnellen, waardoor de kans op ademhalingsproblemen na de geboorte vermindert.
Het ontsluitingstijdperk (eerste tijdperk) en complicaties
Fysiologie
Tekenen die erop wijzen dat de baring is begonnen zijn: regelmatige pijnlijke weeën om de 5 minuten, verstrijken en/of ontsluiten van de portio, tekenen en/of breken van de vliezen.
Het ontsluitingstijdperk verloopt beter als er gelijkmatige druk is op de cervix door de vochtblaas bij staande vliezen of indien de goed ingedaalde schedel het voorliggende deel is. Rugligging van de vrouw is ongunstig voor de weeënactiviteit en voor de oxygenatie van het kind.
Controle: regelmatig controleren van de kinderlijke hartslag, alsmede van de frequentie, duur en sterkte van de weeën. Door middel van vaginaal toucher kan men de vordering van de baring vastleggen. Bij het toucher let men op:
Portio (consistentie, positie in bekken, mate van verstrijking);
Ontsluiting (0-10 cm);
Vliezen (staan of gebroken);
Indaling volgens vlakken van Hodge;
Aard van het voorliggend deel (schedel, stuit, ander deel);
Stand van het voorliggend deel.
Bij een fysiologische baring zullen de vliezen over het algemeen bij nagenoeg volkomen ontsluiting spontaan breken; anders kunnen zij bij volkomen ontsluiting en persdrang worden gebroken.
Het is van belang voor het verloop van de baring en het beoordelen van de progressie:
alert te zijn op het voorkómen van vroege en valse start. Een vroege/valse start is de situatie waarbij de vrouw subjectief goede weeën ervaart, terwijl er (nagenoeg) geen sprake is van portioveranderingen. De invloed die de baringsbegeleider hierop heeft moet niet worden onderschat! Het tijdig bezoeken van de vrouw waarbij, door middel van een goede anamnese en observatie én het verrichten van een vaginaal toucher, helder moet worden beoordeeld of de zwangere in partu is. Het normaal hervatten van de activiteiten of zorgen voor een goede nachtrust is bij niet in partu zijn essentieel.
te zorgen voor goede ondersteuning en observatie van hevige pijn/angst.
onderscheid te maken in de latente fase (tot 3-4 cm ontsluiting) en de actieve fase (vanaf 3-4 cm ontsluiting). Tijdens de latente fase is er sprake van matig frequente (2 per 10 min) en matig sterke weeënactiviteit bij een verstrijkende portio tot 3-4 cm ontsluiting. Deze fase is wisselend van duur maar fysiologisch niet langer dan 8 uur.Tijdens de actieve fase zijn er sterke frequente weeën en ten minste 3-4 cm ontsluiting bij een verstreken portio. Deze fase duurt bij primigravidae 6-8 uur en bij multigravidae 2-6 uur.
Inhoud verlostas
In de verlostas behoren de volgende zaken aanwezig te zijn:
bloeddrukmeter (met gewone en brede manchet) en stethoscoop;
plastic schort;
ten minste 4 paar steriele handschoenen en enkel verpakte steriele handschoenen voor het toucheren;
doptone, doptonegel en monoaurale stethoscoop;
laxeermiddel voor rectaal gebruik en glijmiddel voor VT;
koortsthermometer;
desinfectants, bijv. povidonjood, chloorhexidine;
steriele gaasjes, eventueel watten, pleisters;
buizen met dopjes om navelstrengbloed op te vangen;
steriele halfvaste katheter (14 mm);
steriele injectiespuiten (1 ml, 2 ml, 5 ml en 10 ml), steriele naalden voor i.m. injecties (bijv. 0,8 × 40 mm), voor perineuminfiltratie (bijv. 0,8 × 50 mm) en ‘babynaaldjes’ voor i.m. toediening medicatie aan pasgeborene (bijv. 0,5 × 25 mm), naaldcontainer;
(steriel verpakt vaginaal speculum);
halve Kocher (steriel verpakt) of (disposable) amnihook (waarmee de vliezen gebroken kunnen worden);
- partusset:
- 2 arterieklemmen volgens Kocher;
- navelstrengschaar;
- episiotomieschaar;
- slijmzuiger;
- navelstrengklemmen;
- hechtset:
- 1 anatomisch pincet;
- eventueel 1 chirurgisch pincet;
- naaldvoerder;
- atraumatisch hechtmateriaal met ronde, snijdende, niet-snijdende, ½ gebogen, 3/8 gebogen naalden, vicryl en vicryl rapide in diverse draaddikten;
chirurgische schaar met een spitse en een stompe bek, gaastampon (jojo) en steriele gaasjes;
centimeter, aluminiumdeken, unster;
beademingsballon (silicone) met inhoud van 500 ml, overdruksysteem en gesloten systeem, bijvoorbeeld Laerdal; zacht kindermasker nr. 0, 1 en 3, en zuurstofcilinder 0,8 liter met manometer en restdrukafsluiter; mayotube en maagsonde voor pasgeborene;
- medicamenten:
- oxytocine (max. 3 maanden te bewaren in verlostas);
- (methylergometrine in ampulvorm, max. 14 dagen te bewaren in verlostas);
- een lokaal anestheticum (lidocaïne 1% zonder epinefrine (= adrenaline)) in ampullen (en spray);
- vitamine K (fytomenadiondrank FNA, 10 mg/ml), geopend max. 3 maanden houdbaar;
- misoprostol 4 × 200 mg (in overleg met gynaecoloog);
stuwband, infuusset, infuusnaalden, infusievloeisof NaCl 0,9%.
Pijn bij de bevalling
Frequente en langer durende uteruscontracties of weeën kunnen als zeer pijnlijk worden ervaren. Angst en onzekerheid van de barende kunnen die indruk versterken. Een goede, ook mentale, voorbereiding en continue en persoonlijke zorg, van bij voorkeur een verloskundig zorgverlener, kunnen de pijnbeleving en de noodzaak tot medische behandeling van pijn aantoonbaar verminderen, hetgeen het geboorteproces ten goede komt.
Diagnose
Anamnese en observatie.
Therapie
Er is een scala aan niet-medicamenteuze mogelijkheden om de pijn te reduceren met wisselend ervaren resultaat. Te denken valt aan ontspanningstechnieken, ademhalingstechnieken, massage, warm bad of douche, TENS (transcutane elektrische neurostimulatie), acupunctuur.
Veel medicamenten kunnen depressie van ademhaling en circulatie van het kind veroorzaken. Als analgetica en/of sedativa komen eventueel in aanmerking: morfine 5 mg en/of promethazine (25 mg = 1 ml), beide parenteraal. Dit middel is eerste keuze bij een vroege of valse start (niet in de thuissituatie!).
Bij een thuisbevalling behoort geen medicamenteuze pijnstilling te worden gegeven.
Mocht de pijn toch te sterk worden, dan is opname meestal het beste. Alvorens de pijnstiller wordt gegeven, zal de toestand van het kind beoordeeld worden met behulp van een CTG. Onder klinische controle kan geleidingsanesthesie worden gegeven, waarbij het kind niet in aanraking komt met schadelijke medicamenten en toch een volledig anesthetisch effect bereikt kan worden (bij voorkeur epidurale analgesie). Bezwaren zijn het optreden van hypotensie, vooral bij rugligging, de soms ook optredende uitval van de motoriek van de benen, de mogelijk iets hogere frequentie van kunstverlossingen, het negatief effect op de weeënactiviteit met verhoogde kans op noodzaak tot bijstimulatie, koorts bij de moeder met eventueel foetale tachycardie tot gevolg.
Een andere mogelijkheid is een infuus met remifentanilpompje, waarmee de vrouw zelf de dosering bepaalt. Nadelen: de soms optredende maternale ademdepressie met bijbehorende verminderde oxygenatie, er is meestal geen sprake van volledige pijnstilling.
Inhalatieanalgesie is, vanwege de gevaren voor medewerkers op de verloskamer, lang verboden geweest. De nieuwe afzuiginstallaties zorgen ervoor dat deze mogelijkheid voor analgesie weer in opkomst is.
Onvoldoende vorderende ontsluiting en weeënzwakte
Een goed hulpmiddel bij de diagnose ‘onvoldoende vorderende ontsluiting’ is een partogram waarop verloop van weeënactiviteit en ontsluiting in de tijd worden weergegeven. Het is belangrijk onderscheid te maken tussen onvoldoende vorderen bij adequate weeën en onvoldoende vorderen bij inadequate weeën.
Als bij een barende in de actieve fase de ontsluiting trager vordert dan 0,5-1 cm per uur in een periode van 2-4 uur is er reden voor interventie. Deze bestaat in eerste instantie uit het breken van de vliezen (amniotomie) . Als dit niet leidt tot vorderen van de ontsluiting, is weeënstimulatie met oxytocine aangewezen (niet in de thuissituatie). Hiermee kan een langdurige baring met uitputting van de barende en daardoor een sterk toegenomen kans op een kunstverlossing worden voorkomen.
Bij stagnatie van de ontsluiting vanaf 7 cm zijn de mate van moulage, caput succedaneum en ligging van het caput van invloed op het al dan niet vaginaal bevallen.
Therapie
Amniotomie kan gewoon thuis, voor het overige dient verwijzing naar het ziekenhuis te volgen.
Weeënzwakte
Bij weeënzwakte moeten we onderscheid maken tussen:
Primaire weeënzwakte: vanaf het begin van de baring is er sprake van tekortschieten van de weeën in intensiteit, frequentie en duur, hetgeen niet verbetert in de actieve fase. De ontsluiting kan wel (sluipend) vorderen. Van belang is primaire weeënzwakte goed te onderscheiden van een valse/vroege start, daar de behandeling niet hetzelfde is!
Secundaire weeënzwakte: na een periode van goede weeënactiviteit zwakken deze sterk af en de ontsluiting vordert niet verder. Weeënstimulatie via amniotomie en zo nodig oxytocine zijn geïndiceerd. Ook hier geldt dat de onderliggende oorzaak nader geëvalueerd moet worden: secundaire weeënzwakte is regelmatig het gevolg van een volle blaas. Tevens is er vaak sprake van cefalo-pelviene disproportie, soms veroorzaakt door liggingsafwijkingen van de foetus.
Voortijdig breken van de vliezen
Bij voortijdig gebroken vliezen loopt vruchtwater af zonder regelmatige uteruscontracties. Bij gebroken vliezen is er een verhoogde kans op een intra-uteriene infectie. Perinatale complicaties worden voornamelijk bepaald door de zwangerschapsduur op het moment van het breken van de vliezen. De oorzaak van gebroken vliezen is doorgaans onbekend. Mogelijk spelen veranderde fysische eigenschappen van de vliezen een rol door verstoring in de synthese, verandering in structuur of versnelde afbraak. Infectie met ontstekingsreactie (bacteriële vaginose, groep B-hemolytische streptokokken) speelt soms een rol.
Diagnose
Inspectie van de vulva (vernixvlokjes?), geur beoordelen, eventueel meconium? De diagnose ‘gebroken vliezen’ kan meestal gesteld (of zeer aannemelijk gemaakt) worden op basis van een anamnese van plotseling vaginaal vochtverlies, de aanwezigheid van voortdurend vochtverlies en eventueel de echoscopische waarneming van weinig vruchtwater in utero. Bij twijfel kan men verder onderzoek doen van uit de vagina aflopend vocht of van vocht dat bij onderzoek met een steriel speculum uit de fornix posterior is verkregen. Indien de diagnose ‘gebroken vliezen’ zeer onwaarschijnlijk of zeer waarschijnlijk is, heeft het geen zin verder onderzoek te doen wegens de matige betrouwbaarheid van de testen.
Bij schedel vast in bekkeningang en goede cortonen: geen vaginaal toucher verrichten als er geen/weinig weeënactiviteit is. Een toucher zou de kans op een infectie doen toenemen en heeft bij niet in partu zijn geen meerwaarde.
Bij gebroken vliezen vóór een zwangerschapsduur van 37 weken wordt de zwangere opgenomen in het ziekenhuis.
Therapie
Indien de temperatuur normaal blijft en de zwangerschapsduur ≥ 37 weken is, kan thuis worden gewacht of de baring spontaan op gang komt. Hygiëneadviezen, controle van de foetale conditie door middel van doptone en 4 maal daags temperatuurcontrole zijn geïndiceerd. Wanneer de baby 24 uur na het breken van de vliezen nog niet (bijna) geboren is, zal overdracht naar de tweede lijn plaatsvinden. Inleiden van de baring met oxytocine kan overwogen worden. Ook kan nog 24 uur worden afgewacht, indien foetale en maternale conditie dit toelaten. Er wordt eenmalig een CTG gemaakt en 3 tot 4 maal daags temperatuur gemeten. Bij stijging van de temperatuur boven 37,8 °C wordt over het algemeen overgegaan tot medicamenteuze inleiding.
Wanneer tijdens de baring met gebroken vliezen geen temperatuurverhoging bij de moeder optreedt, de 24 uur (nagenoeg) niet zijn overschreden en het kind na de geboorte in goede conditie is, kan het kraambed thuis worden doorgebracht, uiteraard met goede observatie van het kind. Indien wel > 24 uur gebroken vliezen, wordt het kind de eerste 8-24 uur klinisch geobserveerd waarna ontslag naar huis volgt.
Bij tekenen van intra-uteriene infectie is het gebruik van een breedspectrumantibioticum noodzakelijk.
Uitdrijvingstijdperk (tweede tijdperk) en complicaties
Algemeen
Het uitdrijvingstijdperk begint bij onhoudbare persdrang en volkomen ontsluiting en eindigt bij de geboorte van het kind. Indien bij volkomen ontsluiting geen persdrang wordt aangegeven, kan beter met actief meepersen worden gewacht tot reflectoir persdrang ontstaat.
Controle tijdens de ongecompliceerde uitdrijving
Na iedere wee controle van de harttonen. Normaal is tijdens een perswee een deceleratie van de hartfrequentie waarneembaar, die na afloop van de wee vlot herstelt tot meer dan 120/min. Beoordeling van de progressie door middel van vaginaal toucher geschiedt als de schedel na een half uur nog niet zichtbaar is. Het beoordelen van de stand van het voorliggend deel kan nuttig zijn, omdat dit later in de uitdrijvingsperiode bemoeilijkt kan worden door het caput succedaneum.
Niet-vorderende uitdrijving
De situatie wordt bij nullipara opnieuw bezien als het kind niet binnen 60 minuten zichtbaar is, bij multipara binnen 30 min. Let dan onder andere op onvoldoende weeënactiviteit (caput succedaneum?) , afwijkende stand van de schedel (achterhoofd achter, kruinligging, aangezichtsligging, voorhoofdsligging), of een volle blaas als oorzaak van de stagnatie.
Bij stagneren van de progressie of bij aanhoudende verlaging van de frequentie van de harttonen, hetgeen wijst op foetale nood, is een kunstverlossing in de kliniek geïndiceerd. Bij aanhoudend goede conditie van het kind en blijvende progressie kan bij de nullipara een maximale uitdrijvingsduur van 2 uur worden aangehouden en bij de multipara van 1 uur. Bij een stagnerende uitdrijving, zeker als het caput voorbij de interspinaallijn is ingedaald, zal de baring meestal beeindigd worden door middel van een vaginale kunstverlossing met behulp van een vacuümextractie . Als de extractie niet vlot gaat, moet men overgaan tot het verrichten van een sectio caesarea.
Specialistische begeleiding van de baring
Zwangeren met een verhoogd risico op problemen tijdens de bevalling of zwangeren die tijdens de bevalling door de verloskundige worden verwezen, bevallen onder verantwoordelijkheid van de gynaecoloog in het ziekenhuis.
Het kind wordt vrijwel altijd bewaakt door middel van een cardiotocogram (CTG), waarbij hartfrequentie en weeënactiviteit continu worden geregistreerd. Zijn de vliezen gebroken, dan kan de hartfrequentie worden afgeleid via een elektrode, aangebracht in de schedelhuid. Routinematig meten van de weeëndruk via een in de baarmoeder ingebrachte druklijn wordt niet meer toegepast. De weeënfrequentie wordt uitwendig geregistreerd. Is de hartfrequentie of variatie in de hartslag afwijkend, dan kan dit wijzen op een minder goede foetale conditie. Om dit zeker te weten, kan bloed uit de schedel worden verkregen (microbloedonderzoek), waarbij onder andere de zuurgraad wordt bepaald die een goede maat is voor de foetale conditie.
Ruptuur en episiotomie
Een episiotomie dient voornamelijk om de uitdrijving te bekorten bij verschijnselen van foetale nood of langdurige uitdrijving. Ook een eerdere totaalruptuur, waarbij de m. sphincter ani geruptureerd was, geldt als een (relatieve) indicatie. Het perineum, de vagina en de m. sfincter ani moeten na de bevalling zorgvuldig worden geïnspecteerd. Vooral bij nulliparae kan een perineumruptuur ontstaan . Na hechten onder lokale anesthesie (lidocaïne 1%) geneest deze meestal zonder problemen. Bij aanwijzing dat de m. sfincter ani (gedeeltelijk) is beschadigd, dient deze zorgvuldig en onder goede anesthesie door de gynaecoloog gehecht te worden i.v.m. kans op blijvende incontinentie.
Nageboortetijdperk (derde) en vierde tijdperk en complicaties
Algemeen
Hoewel het kraambed reeds begint op het moment van de geboorte van de placenta, worden de eerste uren van het kraambed wel het vierde tijdperk genoemd, omdat zij functioneel verwantschap vertonen met het nageboortetijdperk : dezelfde risico’s van bloedingen zijn dan nog aanwezig.
Zorg voor het pasgeboren kind en behandeling asfyxie
Afnavelen gebeurt pas als het kind goed heeft gehuild en de longcirculatie gevuld is.
Op tijdstippen 1 min., 5 min. en 10 min. na de geboorte wordt de apgarscore bepaald (tabel 22.3). Met de apgarscore wordt de vitaliteit van het kind gemeten. De apgarscore na 5 en 10 minuten zijn een goede maat voor de conditie van de pasgeborene. De apgarscore, tenzij zeer laag na 5 en 10 minuten, zegt niets over de latere geestelijke ontwikkeling van het kind.
| apgarscore | 0 | 1 | 2 |
|---|---|---|---|
| hartfrequentie | afwezig | < 100/min | > 100/min |
| ademhaling | afwezig | onregelmatig, zwak gehuil, lucht happen | goed doorhuilen |
| spiertonus | slap | hypotoon | actief |
| reflexen op: | |||
| – slijmzuiger | geen | grimas | hoesten, niezen |
| – voetzool | geen | grimas | huilen, voet weg |
| kleur | blauw of wit | romp roze, extremiteiten blauw | geheel roze |
Ter voorkoming van hypothermie wordt de pasgeborene goed afgedroogd, in droge warme doeken gewikkeld en met mutsje op het hoofd op de buik van de moeder gelegd.
Door zorgvuldige inspectie kunnen kort na de geboorte veel aangeboren afwijkingen vroeg worden ontdekt.
Ook wordt het geboortegewicht gemeten.
Eerste hulp bij een asfyctisch kind
Visuele inspectie van mondholte, zo nodig met gaasje schoonvegen. Uitzuigen alleen als er sprake is van meconiumhoudend vruchtwater of andere luchtwegbelemmerde factoren. Standaard uitzuigen wordt niet meer geadviseerd, vanwege het beperkte nut en de bestaande risico’s op beschadigingen en bradycardie;
Baby goed afdrogen, in warme doeken wikkelen en mutsje opzetten. Beoordeel de conditie; bij apneu of hartslag < 100 start resuscitatie;
Overweeg hulp in te roepen van ambulance en zo mogelijk een collega, navel af en leg de baby op een vlakke, harde ondergrond met het hoofd in neutrale positie (iets achterover gekanteld);
Start altijd eerst de beademing met masker en ballon en omgevingslucht (21% zuurstof) en 5 rustige, langzame insufflaties. De longblaasjes kunnen zich openen. Vervolg de beademing met een frequentie van ± 40 per minuut. Beoordeel na 30 sec. de ademhaling en hartactie en ga bij onvoldoende respons over op beademing met 3 liter zuurstof. Bel nu zeker de ambulance!
Beoordeel opnieuw na wederom 30 sec. Indien de hartactie < 60/min. is (eenvoudig te controleren met doptone) bij adequate beademing (thoraxexcursies zichtbaar), ga dan over tot hartmassage. Zolang er geen adequate beademing is, is hartmassage zinloos!
Hartmassage: plaats 2 vingers ter hoogte van het sternum en oefen druk uit tot een diepte van ongeveer een derde tot de helft van de anterieure-posterieure diameter. Streef naar 90 compressies en 30 inflaties met minuut.
Beoordeel elke 30 seconden de conditie van de pasgeborene. Continueer hartmassage tot de hartslag > 60/min is of totdat de pasgeborene is overgedragen aan de kinderarts.
Geen enkele medicamenteuze therapie heeft bewezen van nut te zijn, uitgezonderd neutralisatie van recent aan de moeder toegediende opioïden met naloxon 0,10 mg/kg lich.gew. in de vena umbilicalis.
Na een geslaagde reanimatie heeft de pasgeborene vaak te maken met hypothermie, hypoglykemie en acidose. Iedere pasgeborene die beademend is met zuurstof en/of een 5 min. apgarscore heeft < 7 moet ter observatie worden opgenomen op de kinderafdeling, ook als het kind zich inmiddels volledig heeft hersteld. Het verdient aanbeveling tweemaal per jaar neonatale resuscitatie te trainen, indien men, anders dan in een noodsituatie, baringen begeleidt.
Geboorte van de placenta en retentio placentae
Het nageboortetijdperk wordt conservatief geleid zolang er geen bloedverlies optreedt: afwachten tot weer een wee optreedt, zodat de placenta op natuurlijke wijze loslaat, waarna deze geboren wordt met behulp van gesteunde buikpers. Bij manifest bloedverlies (dat ook latent kan zijn – blijkend uit stijging van de fundus uteri) is toediening van oxytocine i.m. en blaaskatheterisatie geïndiceerd, gevolgd door geboren laten worden van de placenta. Er is veel voor te zeggen routinematig oxytocine te geven als profylaxe, hoewel het nut in laag-risico zwangerschappen niet voldoende is aangetoond.
In de volgende situaties wordt in ieder geval actief geleid door middel van 10 IE oxytocine:
ruim bloedverlies, HPP of MPV in anamnese;
matige weeënactiviteit tijdens ontsluiting en/of uitdrijving;
een zeer langdurige of juist zeer snelle ontsluiting;
grande multi (> P4);
anemie;
grote uitzetting (polyhydramnion, meerlinggraviditeit, macrosomie);
na het toepassen van fundusexpressie;
bij uterus myomatosis (geen methylergometrine toedienen!);
bij kunstverlossingen.
Indien de placenta niet binnen 1 uur spontaan is geboren, spreken we van retentio placentae.
Therapie
In het ziekenhuis onder algehele narcose en antibioticascherm een manuele placentaverwijdering (MPV) verrichten.
In de thuissituatie worden bij een vastzittende placenta (nadat alle noodzakelijke handelingen zijn uitgevoerd) 30 minuten na de geboorte van het kind ambulance, infuus en verwijzing geregeld.
Controle na de geboorte
Controle van de moeder. Het eerste uur na de geboorte van de placenta dienen de stand van de fundus uteri, de consistentie van de uterus, pols en bloeddruk regelmatig gecontroleerd te worden.
Controle van het kind. In de eerste periode dient het kind regelmatig geobserveerd te worden op ademhaling, temperatuur, hartslag, kleur, opgeven van slijm, nabloeding uit de navelstreng.
Controle van de placenta op volledigheid van placentaweefsel en vliezen. Bij onvolledige placenta: natasten in de kliniek. Bij onvolledigheid van de vliezen: afwachten.
Nabloeding : haemorrhagia post partum (HPP)
Fluxus post partum of haemorrhagia post partum (bloedverlies van meer dan 1.000 ml/24 uur) is een relatief frequente (5% van de bevallingen) en veelal onverwachte complicatie en een van de belangrijke oorzaken van moedersterfte in Nederland. HPP wordt onderverdeeld in ‘vroege’ en ‘late’ hemorragie. De vroege vorm treedt op tijdens de eerste 24 uur na de bevalling. De late vorm treedt op na 24 uur, maar binnen 6 weken na de bevalling.
Men onderscheidt de volgende oorzaken:
Atone nabloeding. Hierbij is de uterus slap en wordt de bloeding minder bij contractie van de uterus. Uterusatonie komt vaker voor na overrekking van de uterus (bijv. polyhydramnion, meerlingen, macrosomie), een zeer snelle of zeer langdurige partus, grande multipariteit, chorioamnionitis, uterus myomatosus, na fundusexpressie en bij gebruik van uterusrelaxantia. Van de vroege nabloeding is de uterusatonie de meest voorkomende oorzaak.
Bij placenta accreta en placenta-afwijkingen zoals een bijplacenta, komen achtergebleven placentaresten frequenter voor. Achtergebleven placentaresten treden ook vaker op na extreme vroeggeboorte, eerdere retentio placentae en na manuele placentaverwijdering in de anamnese.
Traumatische bloeding. Hierbij is er hemorragie post partum bij goed gecontraheerde uterus en het bloed stolt goed. Oorzaken zijn een cervixruptuur, een vaginawandruptuur en – vooral bij een sectio in een voorafgaande zwangerschap – een uterusruptuur.
Bloeding bij verbruikscoagulopathie (intravasale stolling). De patiënt vloeit sterk en de uterus is gecontraheerd, maar het bloed stolt niet. Deze oorzaak wordt vooral gezien bij abruptio placentae.
De late nabloeding wordt vrijwel altijd veroorzaakt door een placentarest en treedt meestal 4-7 dagen na de bevalling op, maar soms ook nog in de weken daarna.
Diagnose
Bloedverlies wordt vrijwel altijd te laag ingeschat. De diagnose haemorrhagia post partum is primair gebaseerd op de schatting en het oordeel van de clinicus. Het wegen van verbanden en opgevangen bloed (in de thuissituatie met de unster) draagt bij aan een nauwkeuriger schatting. Bij patiënten met een klein circulerend volume, zoals bij ernstige (pre-)eclampsie, kan een bloedverlies van 500 à 1.000 ml reeds klinische betekenis hebben.
Therapie
Bij atone bloeding:
blaaskatheterisatie;
10 IE syntocinon en placenta geboren doen worden en inspecteren (compleet?);
massage van de fundus uteri en zo mogelijk aanleggen van baby;
zo nodig opnieuw toedienen van uterustonica, bijv. 10 IE oxytocine i.m;
bij > 500 ml en aanhoudend bloedverlies ambulance bellen en infuus inbrengen.
Bij rupturen zo snel mogelijk hechten. Bij verdenking op een cervixruptuur insturen.
Bij (verdenking op) een incomplete placenta altijd natasten onder algehele anesthesie met antibiotische profylaxe. Indien 7-10 dagen na de bevalling veel helderrood bloedverlies ontstaat, is de oorzaak vrijwel altijd een placentarest en is curettage aangewezen, eveneens onder antibiotische profylaxe.
Het kraambed en complicaties
Mobilisatie in het kraambed
Ter preventie van trombo-embolische processen dient de kraamvrouw zo snel mogelijk gemobiliseerd te worden, tenzij ernstige hypertensie of pre-eclampsie dit ongewenst maakt. Na een partus is er geen bezwaar tegen dat de vrouw gaat douchen of naar het toilet gaat, wanneer zij zich daartoe in staat voelt.
Fundus uteri, controle van
De hoogte van de fundus uteri dient regelmatig gecontroleerd te worden. Na een week behoort deze nog maar net palpabel zijn. De lochia verandert tegelijkertijd geleidelijk van sanguïnolent in sereus.
Op indicatie (laag Hb in de zwangerschap of belangrijk bloedverlies bij de partus) verricht men in het kraambed een controle van het Hb op de derde of vierde dag. Bij een Hb van minder dan 6,5 mmol/l is er een indicatie voor ijzertherapie.
Lactatie
Voor het op gang brengen van de lactatie is het van belang de baby binnen 1 uur post partum aan te leggen en zorg te dragen voor deskundige begeleiding. De eerste dagen is 8-12× voeden in 24 uur wenselijk en heeft diverse doelen. De prolactinespiegel in het maternale serum is hierdoor continu op hoog niveau, hetgeen de aanmaak van moedermelk bevordert. De baby krijgt zeer frequent kleine beetjes colostrum, hetgeen energierijk is en laxerend werkt. Daardoor wordt meconium vlot geloosd en is er minder kans op hyperbilirubinemie. De borstvoeding komt op de tweede of derde dag eerst goed op gang. Dan treedt ook borststuwing op; deze houdt ongeveer 24-48 uur aan en kan gepaard gaan met lichte temperatuurverhoging. Ter verlichting kan men koude (na de voeding of bij flesvoeding) of warme (half uur voor de voeding bij borstvoeding) kompressen geven. Bij borstvoeding dienen, vooral bij tepelkloven, de tepels ter preventie van mastitis goed schoon te worden gehouden. Accessoir mammaweefsel in de oksel kan ook gestuwd zijn.
Therapie
Ongeveer 70% van de Nederlandse kraamvrouwen kiest voor borstvoeding. Goede begeleiding en ondersteuning zijn van essentieel belang voor slagen en continueren van de borstvoeding.
Bij de anderen is het soms wenselijk de lactatie te remmen. De volgende maatregelen zijn daartoe mogelijk.
‘Opbinden van de borsten’ werd vroeger door strakke verbandwindsels bereikt. Het gebruik van een strakke beha heeft eenzelfde effect. Prikkeling van de tepels moet worden vermeden.
Medicamenteuze lactatieremming wordt vrijwel standaard toegepast indien de baby is overleden en incidenteel om andere redenen. Eerste keuze is cabergoline p.o. 1e dg 1 mg, zo nodig na 48 uur herhalen; onderdrukken van bestaande lactatie: 2 dd 0,25 mg gedurende 2 dgn. Bij medicamenteuze lactatieremming keert de ovulatie eerder terug. Het is dus van belang te zorgen voor goede anticonceptie.
Icterus neonatorum
Controle van de baby is belangrijk om fysiologische icterus te onderscheiden van niet-fysiologische icterus. De richtlijn uit 1994 (waarbij de grenswaarden voor fototherapie waren opgetrokken) is in 2008 fors herzien, vanwege een toename van het optreden van kernicterus.
Icterus binnen 24 uur na de geboorte is per definitie niet fysiologisch en verwijzing naar de kinderarts is noodzakelijk.
Direct na de geboorte wordt de voorafkans op hyperbilirubinemie bepaald (zie figuur 22.1). Aan de hand hiervan wordt de frequentie van de controles in de kraamperiode bepaald. Bij elke controle wordt op basis van observatie van kleur, voedselintake, de percentuele gewichtsafname, temperatuur, mictie, defecatie en gedrag beoordeeld of bilirubinebepaling nodig is. Observaties bij daglicht hebben de voorkeur. Bij donkere huiskleur is visuele beoordeling moeilijker; slijmliezen van ogen en mond, oogwit en eventueel hand- en voelpalmen bevatten minder pigment en kunnen helpen bij de beoordeling.
Indien bilirubinebepaling nodig is (bij twijfel altijd doen!) is bepalen van totaal serumbilirubine (TSB) (geconjugeerd plus ongeconjugeerd) de gouden standaard en is transcutane bilirubine(TcB-)meting een gevalideerde en betrouwbare manier om een schatting te doen (TcB + 50 = waarde voor bilicurve). De uitslag wordt geplot op de juiste bilicurve (risicoprofiel bepaalt curve) en afhankelijk van de uitslag wordt direct verwezen naar kinderarts of worden intensievere controles afgesproken.
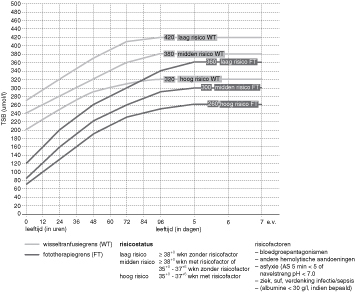
Zie voor uitgebreide informatie voor professionals en de stroomdiagrammen www.babyzietgeel.nl
Tromboflebitis, diepveneuze trombose en longembolie
Tromboflebitis komt met name in de kraamperiode regelmatig voor bij vrouwen met varices. Hoewel de kans op trombose hierbij licht verhoogd is, volstaat lokale behandeling.
De kans op een trombose/embolie is verhoogd tijdens de zwangerschap, maar met name in de kraamperiode. Meestal treedt deze op 1 tot 2 weken post partum. Predisponerende factoren zijn trombo-embolische accidenten in de familie, trombofilie en een sectio caesarea.
Diagnose
Symptomen van trombose zijn: zwelling, roodheid van een (onder)been en soms ook pijn in het been. Er is lichte tot matige temperatuurverhoging en vaak een verhoogde polsfrequentie. Bij verdenking op diepveneuze trombose kan het beste een (serieel) compressie-ultrasonografie worden verricht. Bij verdenking op longembolie kan ook in de zwangerschap een perfusiescan worden verricht. Als deze normaal is, dan wordt de diagnose verworpen. Als deze afwijkend is, volgt een ventilatiescan dan wel een spiraal-CT.
Bij een voorgeschiedenis en/of familieanamnese van trombose kan trombofilieonderzoek geïndiceerd zijn. Door zwangerschapsgerelateerde stollingsveranderingen wordt dat onderzoek bij voorkeur buiten de zwangerschap verricht (interval met zwangerschap ten minste 3 maanden). Indien het toch in de zwangerschap wordt verricht, moet bij het stollingsonderzoek rekening worden gehouden met zwangerschapsgerelateerde veranderingen.
Specialistische therapie
Bij tekenen van diepveneuze trombose moet de kraamvrouw met spoed worden opgenomen voor diagnostiek en behandeling. Meestal zal deze behandeling bestaan uit het subcutaan toedienen van laagmoleculairgewichtheparine. Dat zal 6-12 weken na de bevalling moeten worden gecontinueerd. Indien gekozen wordt voor coumarinederivaten als vervolgtherapie, dient het (LMW-)heparine ten minste 5 dagen na ontstaan van de VTE gecontinueerd te worden.
Gezien het lage risico op trombose is tromboseprofylaxe tijdens de zwangerschap niet geïndiceerd bij vrouwen met een asymptomatische erfelijke risicofactor als de factor V Leiden-mutatie. In het kraambed wordt deze vrouwen wel tromboseprofylaxe geadviseerd voor een periode van 4 tot 6 weken. Indien de profylaxe met LMW-heparine in lage dosering wordt gegeven, is het advies om deze bij een lichaamsgewicht van meer dan 80 kg te verdubbelen.
Cystitis
Bij een vaginale baring ontstaat gemakkelijk een cystitis, zeker als er is gekatheteriseerd. Behalve symptomen als pijn bij het plassen en pijn in de onderbuik, is koorts een veelvoorkomend symptoom bij kraamvrouwen. Diagnose en therapie zijn hetzelfde als in de zwangerschap, waarbij met het voorschrijven van de medicatie rekening gehouden moet worden met het al dan niet geven van borstvoeding.
Endometritis
Endometritis betreft een ascenderende infectie die geassocieerd is met langdurige baring, frequente touchers, kunstverlossing, bloedverlies en anemie, en die zich uit in koorts op de derde of vierde dag na de bevalling.
Diagnose
Naast de beschreven koorts is de uterus bij palpatie drukpijnlijk, niet goed geïnvolueerd en week. Vaginaal onderzoek kan pijnlijk zijn, lochia kan stinken.
Therapie
Antibiotica: amoxicilline 3 dd 375 mg ged. 5 dgn., evt. gecombineerd met metronidazol 3 dd 500 mg ged. 5 dgn. Uterotonica zijn niet zinvol.
Salpingitis en pelveoperitonitis
Salpingitis en pelveoperitonitis kunnen optreden in aansluiting op of tijdens een endometritis. De patiënte is ernstig ziek (misselijk, evt. braken), met buikpijn en koorts. Bij een heftige ontsteking zijn er ook tekenen van peritoneale prikkeling, en bij vaginaal toucher slingerpijn en opstootpijn.
Diagnose
Naast de pijnlijke uterus en onderbuikspijn staan ziek zijn en koorts op voorgrond en kunnen soms, bij vaginaal onderzoek, infiltraten worden gevoeld. Voor diagnostiek wordt materiaal van de lochia en/of de cervix uteri voor kweek en resistentiebepaling ingestuurd.
Specialistische therapie
Opname en behandeling met breedspectrumantibiotica. Bij abcesvorming kan drainage (vaginaal of abdominaal) noodzakelijk zijn.
Kraamvrouwenkoorts
Kraamvrouwenkoorts is een infectie met de groep A-streptokok die fulminant kan verlopen en die meestal kort na de bevalling ontstaat. Klinisch is er sprake van hoge koorts, algemene malaise en niet zelden een pijnlijke uterus bij palpatie. Directe klinische opname en intraveneuze antibiotische behandeling zijn geïndiceerd. Het grote gevaar is het optreden van septische shock, multiorgaanfalen en zelfs sterfte.
Mastitis puerperalis
Mastitis puerperalis ontstaat door invasie van bacteriën (meestal stafylokokken) langs tepelkloven tot in het interstitiële bindweefsel van de mammae. De aandoening ontstaat bijna altijd pas vanaf de tweede week na de bevalling.
Diagnose
De aandoening is in het algemeen eenzijdig, in tegenstelling tot stuwing van de borsten die ook eerder (2-4 dagen na de partus) optreedt. Een rode, warme, harde en pijnlijk plek in de borst, hoge koorts en een ziek of rillerig gevoel zijn kenmerkende symptomen. Bij ongeveer 10% van de vrouwen met mastitis ontstaat een abces.
Therapie
Bij dreigende mastitis: tepels verzorgen; borst zo vaak mogelijk ledigen, liefst door zogend kind waarbij de kin van baby zo mogelijk in de richting van de harde plek wijst of als aanleggen niet lukt door melk af te kolven . Daarnaast kan men voorzichtig tijdens het voeden/kolven de harde rode plek masseren in de richting van de tepel om volledige lediging van de borst te stimuleren. Na de voeding de borst koelen met ijskompressen en half uur voor de voeding deze vervangen door warme compressen. Zo nodig analgetica voorschrijven.
Antibiotica zijn aangewezen bij een mastitis indien voorgaande niet helpt, de hoge koorts > 24 uur aanhoudt en bij koude rillingen. De borstvoeding of het kolven ter lediging van de borst moet worden voortgezet.
Bij een abces moet borstvoeding worden gestaakt, moet het abces rijpen en is er een indicatie voor incisie en drainage.
Bekkeninstabiliteit, symfysiolyse, symfyseruptuur
Al tijdens de zwangerschap kan, door abnormale verweking van de symfyse, symfysiolyse optreden die aanleiding geeft tot instabiliteit van het bekken met pijn in de rug en ter hoogte van de sacro-iliacale gewrichten als gevolg.
Bij bekkeninstabiliteit (beter is het te spreken over bekkenklachten) is er in de zwangerschap en/of na de bevalling ook pijn midden voor in het bekken rond het schaambeen, soms uitstralend naar lies en benen; soms ook pijn onder in de rug of rond de stuit. Kenmerkend zijn pijn bij het opstarten van activiteit, toenemende pijn bij vermoeidheid en pijn bij bepaalde bewegingen zoals bukken, omdraaien in bed, lade dichtschoppen, in rugligging één been gestrekt optillen. Er is bij bekkenklachten geen duidelijk anatomisch substraat.
Tijdens de baring kan een scheur ontstaan in het kraakbeen van de symfyse, vooral na kunstverlossing en na geboorte van een groot kind. Kenmerkend is acute en hevige pijn ter plaatse van de symfyse: een (zeldzame) symfyseruptuur.
Diagnose
Bekkenklachten hebben geen anatomisch substraat, zodat een objectieve diagnose, ook niet door röntgenonderzoek, niet mogelijk is. De diagnose wordt gesteld op basis van anamnese en lichamelijk onderzoek.
De zeldzame symfyseruptuur ontstaat altijd bij de bevalling en kenmerkt zich door een acute en hevige pijn bij de symfyse. Bij lichamelijk onderzoek is er hevige pijn bij druk op de symfyse.
Therapie
De therapie bestaat vooral uit leefstijladviezen:
immobilisatie is niet nodig en verergert zelfs de klachten;
asymmetrische belasting van de symfyse en het bekken zo veel mogelijk vermijden;
fysiotherapie voor uitgebreide leefstijladviezen en oefeningen.
De aandoening geneest spontaan na enkele weken tot maanden. Voor belastende situaties kan evt. een individueel aangemeten bekkenband worden gebruikt.
Postpartumdepressie en puerperale psychose
Tien tot twintig procent van de vrouwen heeft depressieve klachten tijdens de zwangerschap of de eerste 3 maanden na de bevalling. Symptomen zijn slaapstoornissen, verminderde concentratie, gemakkelijk geïrriteerd zijn, geen plezier meer aan dingen beleven, verminderde eetlust, gevoelens van waardeloosheid en schuld, piekeren en malen, sombere stemming. Een EPDS-zelftest kan goed inzicht geven in de ernst van het probleem (http://www.lkpz.nl/epds.php).
Behandeling is voornamelijk ondersteunend, eventueel in combinatie met psycho-educatie en/of antidepressiva.
Soms is de onderliggende oorzaak een tijdelijke hypothyreoïdie die gediagnosticeerd en behandeld dient te worden.
Een puerperale psychose is een ernstige aandoening die bij 0,1-0,2% van de kraamvrouwen voorkomt. De psychose ontstaat meestal aan het eind van de eerste of aan het begin van de tweede week na de bevalling. Symptomen zijn slaapstoornissen, onrust, stemmingsstoornissen, prikkelbaarheid, verhoogde spraakzaamheid, achterdocht, verwardheid, wisselend bewustzijn, verlies van contact met de realiteit, hallucinaties en wanen, gedachten aan zelfdoding of de baby iets aandoen. Vrijwel altijd zijn opname en antipsychotica geïndiceerd, bij voorkeur op een psychiatrische afdeling gespecialiseerd in zorg voor moeder en kind.
Diagnostische en therapeutische technieken
Medicatie tijdens het kraambed en lactatieperiode
De mate waarin een medicament in de moedermelk komt is onder meer afhankelijk van de maternale serumconcentratie en de mate van vetoplosbaarheid van het medicijn. Over veel medicijnen is echter weinig informatie voorhanden. Medicijnen bij borstvoeding worden als volgt geclassificeerd:
Categorie I: gaat niet over in de moedermelk.
Categorie II: gaat wel over in de moedermelk, maar heeft bij gebruikelijke doseringen waarschijnlijk geen effect op het kind.
Categorie III: gaat over in de moedermelk en een effect op het kind is aanwezig of mogelijk.
Categorie IV: onbekend of het overgaat in de moedermelk of onvoldoende gegevens bekend over eventueel effect op het kind.
Bij kortdurende toediening van een middel met nadelige effecten op het kind kan het geven van moedermelk tijdelijk gestaakt worden (wel afkolven en melk weggooien!). Bij medicatie in de zwangerschap is het belangrijk dan al rekening te houden met de wens van de moeder borstvoeding te gaan geven. Voor nadere informatie zie literatuur: informatie van het Lareb, bij voorkeur de online versie van Geneesmiddelen, zwangerschap en borstvoeding met de laatste update http://www.lareb.nl/Teratologie/Naslagwerk-GZB. Voor individuele adviezen: Teratologie Informatie Service van het Lareb: tel. 073-6469702 (alleen voor zorgverleners).
Preventie hepatitis B-overdracht naar kind
Indien de moeder HBsAg-positief is, kan zij het kind tijdens de geboorte besmetten. Ter preventie wordt het kind binnen 2 uur na de geboorte passief geïmmuniseerd met 150 IE in 1 ml HBIg i.m. en binnen 48 uur actief geïmmuniseerd met HBvaxPRO kinderdosis 0,5 ml (5 µg) i.m. door de verloskundig zorgverlener. (Beide injecties bij voorkeur gelijktijdig toedienen maar niet in hetzelfde been.) De vervolgvaccinaties gaan via het Rijksvaccinatieprogramma (sinds augustus 2011 worden alle pasgeborene gevaccineerd tegen hepatitis B).
Vitamine K en vitamine D voor de pasgeborene
Alle kinderen krijgen direct na de geboorte 1 mg vitamine K p.o.
Omdat is gebleken dat een enkele maal in de eerste levensmaanden een tekort optreedt aan vitamine K, leidend tot bloedingen bij het kind, wordt geadviseerd kinderen die borstvoeding krijgen vanaf de 8e levensdag dagelijks 15 µg vitamine K toe te dienen. Na 3 maanden en/of indien de baby meer dan 500 ml flesvoeding in 24 uur krijgt, kan de toediening gestaakt worden.
Follow-up bij perinatale sterfte en traumatische partus
Doodgeboorte en neonatale sterfte zijn zeer ingrijpende gebeurtenissen die zich meestal in het ziekenhuis afspelen. De ouders moeten de gelegenheid krijgen van het kind afscheid te nemen, het te zien en aan te raken en zij moeten zo veel mogelijk herinneringen verzamelen (een of meer foto’s van het kind maken/krijgen, haarlokje, hand- en voetafdrukjes, geboortekaartje?) en zelf de begrafenis of crematie bijwonen en bij voorkeur ook regelen.
Meestal wil de moeder, als het enigszins mogelijk is, zo spoedig mogelijk het ziekenhuis verlaten. De huisarts en de eigen verloskundige behoren telefonisch op de hoogte te worden gesteld, zodat zij contact kunnen opnemen met het paar voor de verdere begeleiding. Degene die de bevalling heeft geleid moet, voordat de moeder het ziekenhuis verlaat, een controleafspraak maken om de hele gang van zaken nog eens uitvoerig te bespreken, ook de oorzaak van het overlijden en eventueel aanwezige vermijdbare factoren. Begeleiding van het paar gedurende de daaropvolgende maanden is meestal zeer nuttig en nodig; daarbij kan de huisarts een belangrijke rol spelen.
Aangifte moet wettelijk plaatsvinden bij de geboorte van elk levend geboren kind en van elk doodgeboren kind na een zwangerschapsduur van 24 weken of meer en/of een gewicht van 500 gram of meer. De Wet op de lijkbezorging is niet van toepassing bij doodgeboorte onder 24 weken of levendgeboren en < 24 uur overleden.
Ook na een traumatische zwangerschap of partus speelt begeleiding van de huisarts een belangrijke rol. Als moeder en kind (ogenschijnlijk) gezond weer thuis zijn verflauwt de aandacht voor de ingrijpende gebeurtenis, terwijl ouders juist dan vaak door een moeilijke periode gaan. Ook over het verloop van eventueel volgende zwangerschappen en baringen bestaan vaak zeer veel vragen die, in overleg met de huisarts, wellicht door de specialist gedeeltelijk kunnen worden beantwoord.



