Einleitung
Das Renin-Angiotensin-System (RAS) ist eines der wichtigsten blutdruckregulierenden Systeme mit mehreren Effektoren, den Angiotensin-Peptiden. Diese werden durch das Enzym Renin vom hochmolekularen Protein Angiotensinogen abgespalten und dann u. a. durch Angiotensin-Converting Enzyme (ACE) aktiviert. Das klassische ACE spaltet vom Dekapeptid Angiotensin I (Ang 1–10) das Angiotensin II (Ang 1–8) ab. Angiotensin II erhöht den Blutdruck durch Bindung an den Angiotensin-Typ-1-Rezeptor (AT 1 R) und nachfolgende Vasokonstriktion.
Angiotensin-Converting Enzyme 2 (ACE2)
Vor 20 Jahren wurde ein weiteres zum ACE homologes Enzym identifiziert 1 und daraufhin als ACE2 bezeichnet. Sowohl ACE2 als auch das klassische ACE liegen einerseits als sehr stark membrangebundene Enzyme in der Lunge und vielen anderen Organen vor 2 3 . Andererseits können aus den jeweiligen membrangebundenen Formen durch Spaltung kleinere lösliche Enzyme gebildet werden. Diese löslichen Formen von ACE und ACE2 zirkulieren in Körperflüssigkeiten und im Blutplasma.
Zunächst hatte sich im Wesentlichen die Grundlagenwissenschaft mit dem ACE2 beschäftigt – die klinische Bedeutung von ACE2 wurde als gering erachtet, weil es eine nur untergeordnete Rolle in der klassischen Kaskade des RAS zu spielen schien ( Abb. 1 ).
Abb. 1.
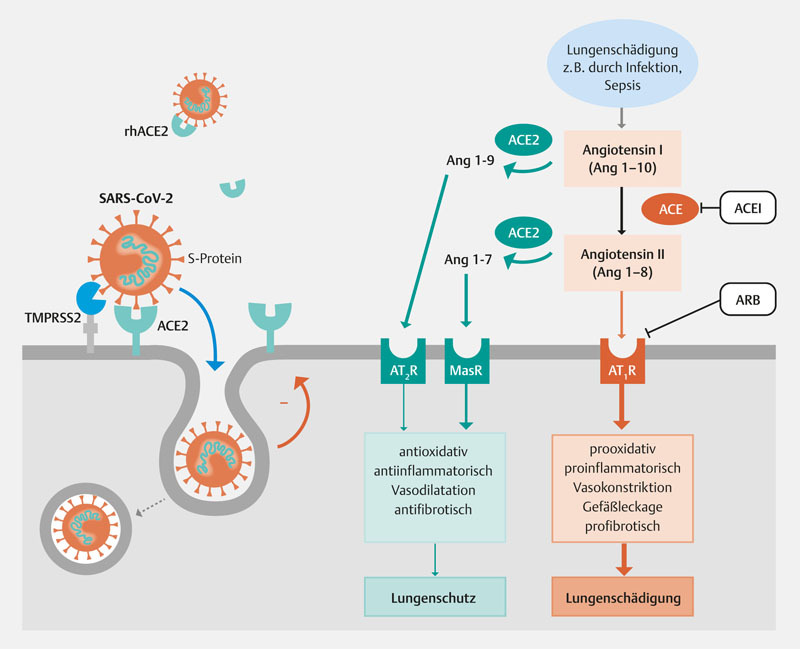
Das Renin-Angiotensin-System (RAS) in der Lunge im Kontext von COVID-19. Die besondere Rolle des ACE2 als Schlüsselelement in der gegenregulatorischen Achse (grün) des RAS ist dargestellt. ACE2 wirkt den negativen Effekten der Ang II/AT 1 R-Achse (rot) auf die Lungenschädigung entgegen. ACE2 wird in Epithelzellen der Atemwege gebildet, einschließlich der alveolären Epithelzellen vom Typ II in der Lunge. SARS-CoV-2 bindet über sein virales Spike-Protein an das membrangebundene ACE2 der Wirtszelle. Dies ermöglicht den Eintritt des Virus in die Zelle und die anschließende Replikation. SARS-CoV-2 benötigt zusätzlich die zelluläre Serinprotease TMPRSS2 für die zelluläre Aufnahme. Eine Herunterregulation von ACE2 durch SARS-CoV-2, wie sie für die SARS-CoV-Infektion nachgewiesen wurde, könnte die Balance zwischen den Achsen im RAS zugunsten der schädigenden Wirkung in der Lunge verschieben. ACE2, als vorwiegend membrangebundenes Enzym, kann in vivo in eine lösliche Form gespalten werden, die in den Körperflüssigkeiten zirkuliert. Ob eine Therapie mit der löslichen Form als rekombinantes humanes ACE2 (rhACE2) durch kompetitive Bindung an das Virus die Ausbreitung der Infektion verlangsamen kann, wird untersucht. Darüber hinaus könnte ein bereits für andere Erkrankungen zugelassener Inhibitor von TMPRSS2 für die Behandlung von SARS-CoV-2 durch Hemmung des viralen Zelleintritts in Betracht gezogen werden 7 .
Merke.
Der wichtigste Unterschied zwischen dem klassischen ACE und ACE2 wurde bereits bei der Entdeckung beschrieben: ACE2 kann nicht durch ACE-Inhibitoren (ACEI) gehemmt werden 1 4 .
Dieser Unterschied resultiert aus wichtigen strukturellen Verschiedenheiten von ACE und ACE2, die das jeweilige aktive Zentrum des Enzyms betreffen und zugleich auch die unterschiedliche Funktion erklären.
ACE ist eine Dipeptidyl-Carboxypeptidase und das wichtigste Enzym für die Konversion des Dekapeptids Angiotensin I (Ang I): durch Abspaltung von 2 Aminosäuren entsteht das vasokonstriktorisch wirkende Oktapeptid Ang II.
ACE2 hingegen ist eine Mono-Carboxypeptidase, die am Ende von Peptiden nur 1 Aminosäure abspaltet und aus Ang II ein anderes Peptid mit nur 7 Aminosäuren (Ang 1–7) bildet. Außerdem kann ACE2 auch 1 Aminosäure aus Ang I abspalten und damit Ang 1–9 bilden.
Blutdruckkontrolle und weitere Effekte
Ang II/AT 1 R-Achse
Die klassische Achse in der RAS-Kaskade, die entscheidend ist für Blutdruckkontrolle und Aldosteronsekretion, betrifft den Signalweg von Ang II zum AT 1 R 4 . Diese Ang II/AT 1 R-Achse hat nicht nur im Herz-Kreislauf-System, sondern zusätzlich in der Lunge und anderen Organen auf Gewebeebene 2 Relevanz: neben der Vasokonstriktion ist sie verantwortlich für schädigende Wirkungen durch Induktion von prooxidativen, proinflammatorischen und profibrotischen Veränderungen. Letztere spielen eine Rolle beim kardiovaskulären Remodeling in Herz, Gefäßen und Nieren 5 .
ACE2/Ang 1–7/MasR-Achse
Die ACE2/Ang 1–7/MasR-Achse vermittelt neben Vasodilatation antioxidative, antiinflammatorische und antifibrotische Schutzfunktionen. ACE2 wird u. a. in den Epithelzellen des oberen und unteren Respirationstrakts sowie in den Alveolarepithelien Typ II gebildet 5 . In mehreren tierexperimentellen Studien konnten eindrucksvoll schützende Effekte der ACE2/Ang 1–7/MasR-Achse zum Beispiel im Rahmen der Lungenschädigung bei Sepsis nachgewiesen werden 5 6 . Im Gegensatz dazu fördert die Aktivierung der Ang II/AT 1 R-Achse die Lungenschädigung – dementsprechend schützt die Behandlung mit ACEI oder AT 1 R-Antagonisten (Angiotensin-Rezeptorblocker, ARB) die Lunge 6 .
Diese aus tierexperimentellen Studien abgeleitete Hypothese über einen protektiven Effekt der RAS-Blocker bei Infektionen der Lunge scheint sich in der klinischen Anwendung zu bestätigen. Eine Analyse der publizierten Studien bei Patienten mit Pneumonie ergab: Der Einsatz von RAS-Blockern ist mit einer geringeren Inzidenz von Lungenentzündungen und einem verbesserten klinischen Outcome einschließlich bei Viruspneumonien verbunden 5 .
Neue Perspektive auf ACE2 durch SARS – Coronaviren
Die Sichtweise auf ACE2 erfuhr im Jahr 2003 eine eindrucksvolle Erweiterung: ACE2 wurde nämlich als Rezeptor für die Bindung von Coronaviren (SARS-CoV) entdeckt, die für das Severe Acute Respiratory Syndrome (SARS) verantwortlich sind 8 . Damit ergab sich über ACE2 und RAS eine unerwartete neue Verbindung zwischen Virologie und Herz-Kreislauf-Medizin. Diese Erkenntnis trat jedoch nach dem Ende der SARS-Epidemie 9 wieder in den Hintergrund und gewinnt nun im Kontext der COVID-19-Pandemie erneut sehr stark an Bedeutung aufgrund der Verbindung zwischen ACE2 und SARS-CoV-2.
Merke.
Dies beruht zunächst auf dem Nachweis, dass ACE2 auch den Bindungsrezeptor für das neue Virus der COVID-19-Infektion, SARS-CoV-2, darstellt 10 .
Dementsprechend können alle Zellen, die ACE2 und zugleich die zelluläre Serinprotease TMPRSS2 als weiteren notwendigen Kofaktor auf ihrer Zelloberfläche produzieren, potenziell SARS-CoV-2 aufnehmen und replizieren. Dieser Zusammenhang hat seit Beginn der COVID-19-Pandemie zahlreiche Kommentare und Spekulationen in Fachjournalen, Presse und Social Media provoziert. Es wurde befürchtet, dass Medikamente wie ACEI und ARB möglicherweise das Risiko für eine Infektion und den Krankheitsverlauf mit COVID-19 erhöhen 5 11 .
Obwohl, wie bereits erwähnt, ACEI keine hemmende Wirkung auf ACE2 ausüben können, gibt es im RAS zahlreiche Interaktionen und Rückkopplungsschleifen zwischen den Einzelkomponenten 4 . Am bekanntesten ist die negative Rückkopplung zwischen Ang II auf die Reninsekretion über AT 1 R, was die hohen Reninspiegel unter Therapie mit ACEI und ARB erklärt. Ein möglicher Zusammenhang zwischen ACE2 und RAS-Blockern ergibt sich vorwiegend aus tierexperimentellen Befunden.
Merke.
Tierexperimentelle Befunde zeigten eine Heraufregulation von ACE2 in kardiovaskulären Organen nach der Behandlung mit RAS-Blockern, v. a. nach Gabe von ARB 5 .
Was aber wäre, wenn das auch auf den Menschen zuträfe? Dann
könnte man von einer erhöhten Infektiosität durch eine verstärkte Aufnahme von SARS-CoV-2 unter der Therapie mit RAS-Blockern und einem damit verbundenen ungünstigen Einfluss auf COVID-19 ausgehen 5 .
hätte ein solcher Zusammenhang klinisch relevante Implikationen, weil RAS-Blocker als Basis einer leitliniengerechten Behandlung der arteriellen Hypertonie und auch anderer kardiovaskulären Erkrankungen wie Herzinsuffizienz mit reduzierter Ejektionsfraktion empfohlen werden.
wäre vor allem vor dem Hintergrund der hohen Prävalenz der arteriellen Hypertonie sowie ihrer Begleiterkrankungen die Gesamtpopulation und insbesondere die ältere Bevölkerung gefährdet 12 .
So war der Grund für den hohen Anteil der Hypertoniker an den initial berichteten komplizierten Verläufen der COVID-19-Patienten (einschließlich der Verstorbenen in China und Italien) mit hoher Wahrscheinlichkeit das hohe mittlere Alter mit der korrespondierenden hohen Hypertonieprävalenz in der älteren Bevölkerung 5 13 .
Empfehlung
Eine umfassende Beurteilung der komplexen Interaktionen im RAS und deren Modulation durch RAS-Blocker sowie deren Beziehung zur Pathogenese der COVID-19-Infektion zeigt: Befürchtungen eines erhöhten Risikos durch RAS-Blocker im Rahmen von COVID-19 sind nach heutigem Kenntnisstand nicht begründet 5 11 13 . Diese Einschätzung wurde in der Zwischenzeit in zahlreichen Stellungnahmen von internationalen und nationalen Fachgesellschaften (ESH, DHL) ebenfalls untermauert 14 15 .
Vor diesem Hintergrund soll eine leitliniengerechte Anwendung von ACEI und ARB bei stabilen Patienten mit Hypertonie oder anderen Erkrankungen (z. B. Herzinsuffizienz, chronische Nierenerkrankung, Diabetes) wegen der Bedenken während einer COVID-19-Pandemie nicht abgesetzt oder zurückgehalten werden 16 . Davon ausgenommen sind selbstverständlich schwerkranke COVID-19-Patienten mit kompliziertem Verlauf und arterieller Hypotonie, Kreislaufinstabilität, kardialer Schädigung und Herzinsuffizienz oder akuter Nierenschädigung mit schwerer Niereninsuffizienz. In diesen Situationen können eine individuelle Anpassung bzw. das kurzfristige Absetzen einer blutdrucksenkenden Therapie einschließlich der RAS-Blocker und eine leitliniengerechte intensivmedizinische Therapie geboten sein 5 .
Biographies
Prof. Dr. med. Reinhold Kreutz

Facharzt für Klinische Pharmakologie und Innere Medizin. Präsident der European Society of Hypertension (ESH). Direktor des Instituts für Klinische Pharmakologie und Toxikologie, Charité-Universitätsmedizin Berlin.
Dr. Engi Abd El-Hady Algharably

PhD in Klinischer Pharmazie, Ain-Shams-Universität, Kairo, Ägypten. Wissenschaftliche Mitarbeiterin am Institut für Klinische Pharmakologie und Toxikologie CMM, Charité-Universitätsmedizin Berlin.
Prof. Dr. med. Detlev Ganten

Präsident des World Health Summit. Er arbeitet wissenschaftlich auf den Gebieten der Herz-Kreislauf-Erkrankungen, Bluthochdruck, Genomforschung, Molekulare Genetik, Evolutionäre Medizin und Globale Gesundheit. Er war Gründungsdirektor des Max-Delbrück-Centrums für Molekulare Medizin (MDC) Berlin-Buch, Präsident der Helmholtz-Gemeinschaft Deutscher Forschungszentren (HGF), Mitglied im Nationalen Ethikrat und Vorstandsvorsitzender der Charité-Universitätsmedizin Berlin.
Prof. Dr. med. Franz H. Messerli

Senior Consultant, Universitätsspital Bern, Klinik für Kardiologie, emeritierter Professor für Medizin an der Icahn School of Medicine am Mount Sinai Health Medical Center und Gastprofessor an der Jagiellonen-Universität in Krakau, Polen. Er ist unter anderem Preisträger des Alberto Zanchetti Life Achievement Awards der European Society of Hypertension und Experte für hypertensive Herz-Kreislauf-Erkrankungen und präventive Kardiologie.
Footnotes
Interessenkonflikt Reinhold Kreutz hat Honorare für Vortragstätigkeit, Beratertätigkeit oder Unterstützung für Forschung erhalten von Bayer Pharma, Berlin-Chemie Menarini, Daiichi Sankyo, Ferrer, Sanofi, Servier außerhalb der aktuellen Arbeit.
Infobox 1.
Neben dieser schädigenden Achse hat das RAS zumindest 2 weitere gegenregulatorische (schützende) Arme:
Ein Arm betrifft den Signalweg über den Angiotensin-Typ-2-Rezeptor (AT 2 R), der ebenfalls hauptsächlich durch Ang II, aber zusätzlich auch über Ang 1–9 aktiviert wird.
Der andere, noch nicht so lange bekannte Arm betrifft den Mas-Rezeptor (MasR) -Signalweg, der hauptsächlich durch Ang 1–7 induziert wird 3 . An dieser Stelle hat das ACE2 eine Schlüsselposition als hauptverantwortliches Enzym für die Ang-1–7-Bildung.
Infobox 2.
Begründung der Empfehlung
Entscheidend ist, dass nach einer systematischen Auswertung der bislang publizierten Befunde eine Heraufregulation des ACE2-Proteins im Gewebe nicht konsistent zu belegen ist. Dies trifft erst recht auf den Menschen zu, wo bislang keine signifikante Beeinflussung von ACE2-Protein durch RAS-Blocker im Respirationstrakt als dem entscheidenden Zielorgan für COVID-19 nachweisbar ist 5 . Auf der anderen Seite wurde ein günstiger protektiver Einfluss von RAS-Blockern auf Lungenschädigungen in experimentellen Studien und auf klinisch relevante Endpunkte bei Patienten mit Pneumonie beschrieben 5 11 13 .
Kernaussagen.
Ausgangspunkt der hier diskutierten Problematik ist der Nachweis, dass ACE2 auch den Bindungsrezeptor für das neue Virus der COVID-19-Infektion, SARS-CoV-2, darstellt.
Eine Beeinflussung der Infektiosität von SARS-CoV-2, dem Erreger von COVID-19, durch RAS-Blocker aufgrund einer Aktivierung von ACE2 ist derzeit wissenschaftlich nicht belegt.
Der klinische Einsatz der RAS-Blocker ACEI und ARB soll im Kontext der COVID-19-Pandemie bei stabilen Patienten nach heutigem Kenntnisstand unverändert leitliniengerecht erfolgen.
Fachgesellschaften wie die ESH und die DHL befürworten diese Empfehlung.
Klinische Erfahrungen bei der Behandlung von COVID-19-Patienten sollten international zusammengeführt werden, v. a. in Bezug auf Komorbiditäten wie arterielle Hypertonie und entsprechende Begleittherapien.
Literatur
- 1.Tipnis S R, Hooper N M, Hyde R.A human homolog of angiotensin-converting enzyme. Cloning and functional expression as a captopril-insensitive carboxypeptidase J Biol Chem 200027533238–33243.. doi:10.1074/jbc.M002615200 [DOI] [PubMed] [Google Scholar]
- 2.Paul M, Poyan Mehr A, Kreutz R.Physiology of local renin-angiotensin systems Physiol Rev 200686747–803.. doi:10.1152/physrev.00036.2005 [DOI] [PubMed] [Google Scholar]
- 3.Santos R AS, Sampaio W O, Alzamora A C.The ACE2/Angiotensin-(1-7)/MAS Axis of the Renin-Angiotensin System: Focus on Angiotensin-(1-7) Physiol Rev 201898505–553.. doi:10.1152/physrev.00023.2016 [DOI] [PMC free article] [PubMed] [Google Scholar]
- 4.Arendse L B, Danser A HJ, Poglitsch M.Novel Therapeutic Approaches Targeting the Renin-Angiotensin System and Associated Peptides in Hypertension and Heart Failure Pharmacol Rev 201971539–570.. doi:10.1124/pr.118.017129 [DOI] [PMC free article] [PubMed] [Google Scholar]
- 5.Kreutz R, Algharably E A, Azizi M.Hypertension, the renin-angiotensin system and the risk of lower respiratory tract infections and lung injury: implications for COVID-19. European Society of Hypertension COVID-19 Task Force Review of EvidenceCardiovasc Res 2020; cvaa097. 10.1093/cvr/cvaa097 [DOI] [PMC free article] [PubMed]
- 6.Imai Y, Kuba K, Penninger J M.The discovery of angiotensin-converting enzyme 2 and its role in acute lung injury in mice Exp Physiol 200893543–548.. doi:10.1113/expphysiol.2007.040048 [DOI] [PMC free article] [PubMed] [Google Scholar]
- 7.Stahlmann R, Lode H.Therapie von COVID-19 – erste klinische Studien mit verschiedenen Wirkstoffen Dtsch Arztebl Int 2020117213–219.. doi:10.3238/arztebl.2020.0213 [DOI] [PMC free article] [PubMed] [Google Scholar]
- 8.Li W, Moore M J, Vasilieva N.Angiotensin-converting enzyme 2 is a functional receptor for the SARS coronavirus Nature 2003426450–454.. doi:10.1038/nature02145 [DOI] [PMC free article] [PubMed] [Google Scholar]
- 9.Fauci A S, Lane H C, Redfield R R.Covid-19 – Navigating the Uncharted N Engl J Med 20203821268–1269.. doi:10.1056/NEJMe2002387 [DOI] [PMC free article] [PubMed] [Google Scholar]
- 10.Hoffmann M, Kleine-Weber H, Schroeder S et al. SARS-CoV-2 Cell Entry Depends on ACE2 and TMPRSS2 and Is Blocked by a Clinically Proven Protease Inhibitor. Cell. 2020 doi: 10.1016/j.cell.2020.02.052. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 11.Danser A HJ, Epstein M, Batlle D. Renin-Angiotensin System Blockers and the COVID-19 Pandemic: At Present There Is No Evidence to Abandon Renin-Angiotensin System Blockers. Hypertension. 2020 doi: 10.1161/hypertensionaha.120.15082. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 12.Forouzanfar M H, Liu P, Roth G A.Global Burden of Hypertension and Systolic Blood Pressure of at Least 110 to 115 mm Hg, 1990–2015 Jama 2017317165–182.. doi:10.1001/jama.2016.19043 [DOI] [PubMed] [Google Scholar]
- 13.Vaduganathan M, Vardeny O, Michel T et al. Renin-Angiotensin-Aldosterone System Inhibitors in Patients with Covid-19. N Engl J Med. 2020 doi: 10.1056/NEJMsr2005760. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 14.European Society of Hypertension, ESH Im Internet (Stand 08.04.2020):www.eshonline.org/spotlights/esh-statement-on-covid-19/
- 15.Deutsche Hochdruckliga, DHL Im Internet (Stand: 08.04.2020):www.hochdruckliga.de/
- 16.Williams B, Mancia G, Spiering W.2018 ESC/ESH Guidelines for the management of arterial hypertension J Hypertens 2018361953–2041.. doi:10.1097/hjh.0000000000001940 [DOI] [PubMed] [Google Scholar]


