Abstract
目的
评价咖啡酸片治疗原发免疫性血小板减少症(ITP)的有效性和安全性。
方法
103例PLT>10×109/L且无严重出血症状的ITP患者纳入研究。根据治疗前血小板计数将患者分为:①A组(PLT<30×109/L):男27例,女24例,中位年龄48(18~84)岁;②B组(PLT≥30×109/L):男19例,女33例,中位年龄43 (18~83)岁。两组患者均给予咖啡酸片0.9 g/d(分3次口服),连用12周。治疗期间避免合用糖皮质激素、达那唑、TPO、利妥昔单抗等具有升血小板作用的药物。
结果
A组51例患者总有效率为51.0%,其中完全反应(CR)2例,有效(R)24例;26例治疗有效(CR+R)患者治疗前中位PLT为20.5(15.0~28.0)×109/L,治疗后中位PLT峰值为63.0(38.0~112.0)×109/L,中位起效时间为4(2~10)周;治疗前PLT≥20×109/L的患者有效率(CR+R)优于PLT<20×109/L的患者(68.0%对34.6%,P=0.017);年龄、性别、疾病分期与疗效无相关性(P>0.05)。B组52例患者中,21例(40.4%)获得CR。不良事件发生率为1.94% (2/103),包括Ⅰ度肝酶升高、Ⅰ度恶心各1例,均自行好转。
结论
咖啡酸片对ITP有较好的疗效,不良反应发生率较低且轻微。
Keywords: 血小板减少, 咖啡酸, 治疗结果, 药物毒性
Abstract
Objective
To determine the efficacy and safety of oral caffeic acid (CA) tablet in management of primary immune thrombocytopenia(ITP).
Methods
One hundred and three ITP patients with PLT>10×109/L and no serious bleeding symptoms from three centers were enrolled. According to their platelet count before CA treatment, these patients were divided into group A (PLT<30×109/L), including 24 females and 27 males with median age 48(18–84) years; and group B (PLT≥30 × 109/L), including 33 females and 19 males with median age 43(18–83) years. Patients in both groups took CA tablets orally of 300 mg three times per day for 12 consecutive weeks. Combined medicine treatment such as corticosteroids, danazol, TPO and Rituximab, which might increase the platelet count of these patients, were not allowed during CA therapy.
Results
In group A, the overall response rate was 51.0%(26/51), with 2 patients achieving complete response (CR) and 24 patients achieving response (R). Of 26 patients achieving response (CR+R), the median platelet count before CA therapy was 20.5 (15–28) ×109/L, and the median peak platelet count after CA therapy was 63 (38–112) ×109/L. The median time to achieving response was 4 (2–10) weeks. Patients with pretreatment PLT>20 × 109/L showed significantly better response than those PLT<20×109/L (68.0% vs 34.6%,P=0.017). In group B, the CR rate was 40.4%(21/52). Frequency of CA-related adverse events was 1.94% (2/103), including mild nausea in 1 case and elevation of liver enzymes in 1 case. Both were grade 1 and transient.
Conclusion
Caffeic acid was effective in patients with ITP with few and mild adverse effects.
Keywords: Thrombocytopenia, Caffeic acid, Treatment outcome, Drug toxicity
原发免疫性血小板减少症(primary immune thrombocytopenia, ITP)是临床最为常见的出血性疾病,成人年发病率为5~10/10万。ITP目前尚无根治方法,原则上一般只对PLT<30×109/L的患者进行治疗。对于PLT≥30×109/L的患者,如有出血表现或存在增加出血风险的因素(老年患者、口服抗凝剂、口服抗血小板药物、高血压控制不佳等),则需进行治疗以提升血小板水平。ITP的治疗首选糖皮质激素,二线治疗包括促血小板生成药物、利妥昔单抗、脾切除等。环磷酰胺、长春新碱、环孢素等免疫抑制剂的治疗效果尚缺乏随机对照多中心临床试验数据的支持[1]–[2]。
国内多项研究结果表明咖啡酸片能够有效治疗多种原因引起的血小板减少[3]–[5],但多为单中心的经验总结且联合应用泼尼松、硫唑嘌呤等其他药物。2012年9月至2013年12月,我们以3个中心的103例成人ITP患者为研究对象,采用前瞻性、单臂、多中心研究方法,观察咖啡酸片治疗ITP的有效性和安全性。
病例和方法
1.病例选择:依据文献[1]标准对患者进行诊断:①至少2次血常规检查显示血小板计数减少;②脾脏不肿大或仅轻度肿大;③骨髓巨核细胞增多或正常,有成熟障碍;④除外各种继发性血小板减少症。入组标准:①年龄≥18岁;②PLT<100×109/L但≥10×109/L;③WHO出血评分≤1分;④签署知情同意书。排除标准:①妊娠或哺乳期患者;②肝肾功能异常:血清转氨酶和胆红素≥正常值上限的1.5倍,肌酐≥150 mg/L;③咖啡酸过敏患者。试验期间出现以下情况允许退出及终止试验:①患者本人要求退出;②出现违背方案的伴随治疗;③治疗4周未见疗效;④研究者认为继续试验可能对患者不利。
2.试验设计与治疗方案:入组时间:2012年9月至2013年12月。采用前瞻性、单臂、多中心临床试验方法,由3家医院协同完成。根据治疗前血小板计数将患者分为A组(PLT<30×109/L)和B组(PLT≥ 30×109/L)。出血症状较重的患者住院治疗,待血小板计数提升至安全水平或出血症状消失后转为门诊治疗并随访。治疗方案:咖啡酸片(德州德药制药有限公司产品):0.9 g/d,分3次口服。本研究获得山东大学齐鲁医院医学伦理委员会批准。
3.伴随治疗:咖啡酸片治疗期间避免合用糖皮质激素、达那唑、TPO、利妥昔单抗等具有升血小板作用的药物;出现黏膜、内脏等部位活动性出血的患者予以血小板输注并使用抗纤溶药物;出现肝酶升高的患者给予保肝药物治疗;合并其他疾病而使用其他药物或治疗的患者,在观察表中记录药物名程、剂量、用法及用药时间。
4.随访及疗效判定:每2周随访1次,共随访12周。观察患者的生命体征、出血症状、血小板输注及不良事件,实验室指标包括血细胞计数和肝肾功能。治疗4周后评价疗效,无效患者继续用药至6周,仍无效者退组。因治疗无效退组的患者,退组前最后1次随访为终末随访。A组疗效判定标准参照文献[1]:①完全反应(CR):治疗后PLT≥100×109/L且没有出血;②有效(R):治疗后PLT≥30 × 109/L并且至少比基础血小板计数增加2倍,且没有出血;③无效(NR):治疗后PLT<30×109/L或者血小板计数增加不到基础值的2倍或者有出血。B组疗效判定标准:治疗后PLT≥100×109/L且没有出血判定为CR。
5.统计学处理:检验数据经统计学处理,定量指标的描述计算例数、中位数、最小值和最大值。分类指标的描述用各类的例数及百分比。计数资料的比较采用χ2检验。P<0.05为差异有统计学意义。
结果
1.一般资料:2012年9月至2013年12月3个中心共入组103例ITP患者。①A组:男27例、女24例,中位年龄48 (18~84)岁,中位病程7个月(12 d~62个月);新诊断ITP 11例,持续性ITP 24例,慢性ITP 16例;入组前中位疗程2(0~5)个,治疗前中位PLT为19 (12~28)× 109/L。②B组:男19例、女33例,中位年龄43 (18~83)岁,中位病程4.5个月(5 d~60个月);新诊断ITP 25例,持续性ITP 15例,慢性ITP 12例;入组前中位疗程1(0~5)个,中位PLT为49(30~86)×109/L;31例有出血症状(WHO出血评分为1分),7例因有明显的乏力症状需要治疗,5例患者因服用抗凝药物需要提升血小板水平,9例无症状但治疗意愿强烈的患者自愿加入本临床研究。
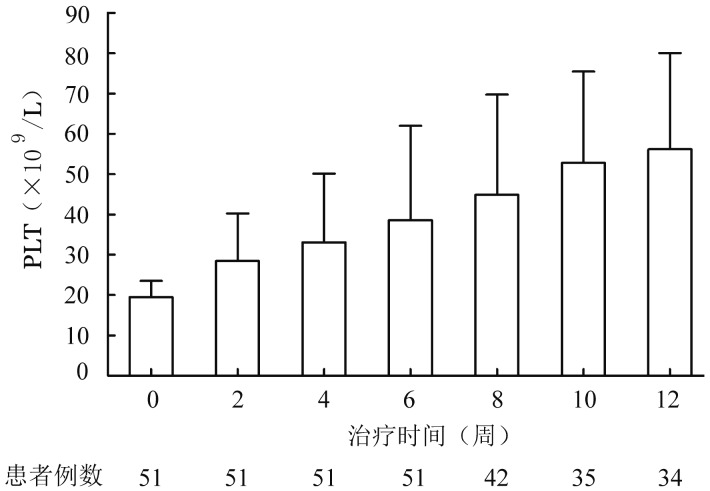
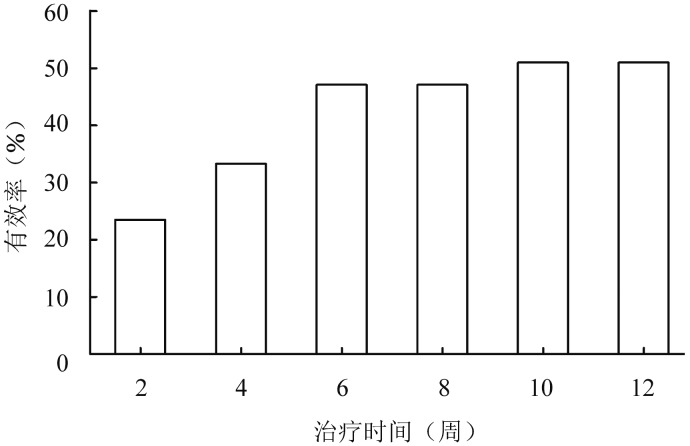
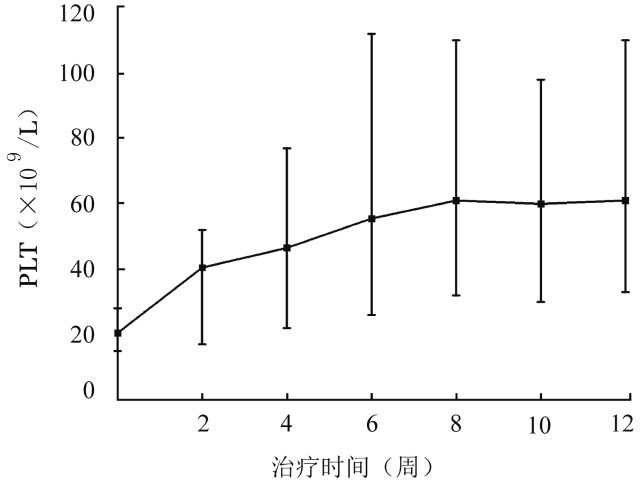
2.疗效:①A组51例患者治疗后血小板计数均值变化见图1。咖啡酸片的起效时间见图2。咖啡酸片治疗第2、4、6周时的总有效率(CR+R)分别为23.5%、33.3%、47.1%。第6周时仍无效的患者中有9例虽未达到R的标准,但PLT较治疗前有明显提升,出血症状显著改善,故继续服用,其中2例患者在第10周时达到R。26例治疗有效患者中位血小板计数的变化见图3。中位起效时间为4(2~10)周,有效患者治疗前中位PLT为20.5(15~28)×109/L,治疗后中位PLT峰值为63 (38~112)×109/L。②B组全部52例患者中有21例(40.4%)在治疗后达CR。
图1. A组(PLT<30×109/L)原发免疫性血小板减少症患者咖啡酸片治疗后血小板计数变化.
图2. A组(PLT<30×109/L)51例原发免疫性血小板减少症患者咖啡酸片治疗有效率(完全反应+有效)变化.
图3. A组(PLT<30×109/L)26例咖啡酸片治疗有效原发免疫性血小板减少症患者血小板计数的变化.
3.ITP患者临床特征与咖啡酸片疗效的相关性:①A组:年龄(<60岁与≥60岁)、性别对咖啡酸片疗效无影响(P>0.05),治疗前PLT≥20×109/L的患者疗效(CR+R)优于PLT<20×109/L的患者(68.0%对34.6%,P=0.017),ITP的分期(新诊断、持续性与慢性ITP)对咖啡酸片的疗效没有影响(P=0.374)(表1)。②B组:患者年龄、性别及疾病分期对咖啡酸片的疗效均无显著影响(P>0.05)。
表1. PLT<30×109/L原发免疫性血小板减少症(ITP)患者临床特征与咖啡酸片疗效的相关性[例(%)].
| 临床特征 | 例数 | CR+R | NR | P值 |
| 年龄 | 0.938 | |||
| ≥60岁 | 12 | 6(50.0) | 6(50.0) | |
| <60岁 | 39 | 20(51.3) | 19(48.7) | |
| 性别 | 0.121 | |||
| 男 | 27 | 11(40.7) | 16(59.3) | |
| 女 | 24 | 15(62.5) | 9(37.5) | |
| 疾病分期 | 0.374 | |||
| 新诊断ITP | 11 | 7(63.6) | 4(36.4) | |
| 持续性ITP | 24 | 13(54.2) | 11(45.8) | |
| 慢性ITP | 16 | 6(37.5) | 10(62.5) | |
| 治疗前PLT | 0.017 | |||
| <20×109/L | 26 | 9(34.6) | 17(65.4) | |
| ≥20×109/L | 25 | 17(68.0) | 8(32.0) |
注:CR:完全反应;R:有效;NR:无效
4.药物不良反应:全部103例患者治疗前后WBC、HGB、肾功能及胆红素均无明显变化。不良事件发生率为1.94%(2/103)。1例患者口服咖啡酸片第4周出现一过性肝酶升高(Ⅰ度),2周后自行好转。1例患者服药1周后出现轻度恶心(Ⅰ度)。2例患者均未因不良反应停药或减量。
讨论
ITP是免疫介导的血小板过度破坏及生成不足双重打击导致的自身免疫性疾病。成人ITP的一线治疗方案包括糖皮质激素和静脉免疫球蛋白(IVIG)。糖皮质激素包括常规剂量泼尼松和大剂量地塞米松。糖皮质激素的早期反应率高,但持续反应率较低。长期应用糖皮质激素可引起骨质疏松、股骨头坏死、高血压、糖尿病、感染、急性胃黏膜病变等不良反应。IVIG升血小板作用持续时间短,而且费用昂贵,主要用于ITP的紧急治疗。二线药物中TPO及TPO受体激动剂和利妥昔单抗疗效确切且相对安全[1]–[2],但价格昂贵。因此寻找一种经济且不良反应较少的药物具有重要的临床意义。
咖啡酸又称3, 4-二羟基肉桂酸或3, 4-二羟基苯丙烯酸,广泛存在于多种植物中,具有抗氧化、抗炎、止血、升白细胞及升血小板等作用[6]。动物实验发现咖啡酸可能通过刺激巨核细胞成熟、增加巨核细胞总数、对由阿糖胞苷诱发的小鼠血小板减少具有明显的治疗作用[7]。研究发现,咖啡酸能够降低化疗后肺组织急性损伤小鼠的肺组织毛细血管通透性[8],缩短白细胞及血小板减少症模型小鼠的TT、PT、APTT,提高纤维蛋白原含量,上调外周血血小板膜糖蛋白CD62p表达水平,活化血小板,增强止血和凝血功能[9]–[10]。
以往咖啡酸片治疗ITP的报道均为单中心回顾性分析[3]–[4]。本研究中,咖啡酸片治疗51例PLT<30×109/L的ITP患者的总有效率(CR+R)为51.0%,中位起效时间4周,不良反应轻微。进一步分析发现,咖啡酸的疗效与患者性别、年龄以及疾病分期无关,但与患者治疗前的血小板计数有关。治疗前PLT≥ 20×109/L的患者咖啡酸治疗的总有效率显著高于PLT<20×109/L的患者。
对于PLT≥30×109/L的ITP患者的治疗选择,国际工作组及我国专家共识均建议:无出血表现且不存在增加出血风险因素的患者可不予治疗,如果患者存在增加出血风险的因素,则需提升血小板计数至50×109/L或正常水平[1],[11]。国外研究发现,虽然ITP是一种良性疾病,但患者的生活质量差,一方面疾病本身所致的乏力影响患者体能,另外一方面的原因是患者对出血的恐惧以及治疗药物(如糖皮质激素)带来的不良反应。因此许多患者的治疗意愿非常强烈。本研究包括52例PLT≥30×109/L的患者,其中31例有出血症状(WHO出血评分为1分),7例有明显的乏力症状,5例因服用抗凝药物需要提升血小板水平,还有9例患者虽然没有出血及乏力等症状但治疗意愿强烈而自愿加入本临床研究。应用咖啡酸片治疗后,52例PLT≥30×109/L的ITP患者中有21例(40.4%)患者达到CR,表明咖啡酸片单药治疗对于这部分患者具有经济、有效且不良反应发生率低的优点。由于不能排除部分患者PLT自行恢复,所以我们将这部分病例与治疗前PLT<30× 109/L的患者分开进行疗效分析。
本组病例资料中,51例PLT<30×109/L的ITP患者的中位起效时间为4 (2~10)周,大部分患者在4周内起效,与国内其他研究[3]–[5]类似。咖啡酸片治疗有效的患者继续服用至12周疗效可以维持。另外,本研究中85例完成12周疗程的患者,仅1例患者在用药第4周出现Ⅰ度肝酶升高,另有1例患者服药1周后出现Ⅰ度恶心,2例患者均自行好转。
本研究结果初步表明咖啡酸片治疗ITP有效,不良反应发生率低且轻微,不失为ITP治疗的新选择。但本研究为单臂的临床研究,亦未纳入PLT< 10×109/L的患者。因此,咖啡酸片治疗ITP的疗效及安全性尚需进行大样本、多中心、随机对照临床研究加以验证。
Funding Statement
基金项目:国家自然科学基金(81270578、81370616);卫生公益性行业科研专项(201202017);卫生部临床学科重点项目(2010-2012);山东省优秀中青年科学家奖励基金(BS2011YY021)
References
- 1.中华医学会血液学分会血栓与止血学组. 成人原发免疫性血小板减少症诊断与治疗中国专家共识(2012年版)[J] 中华血液学杂志. 2012;33(11):975–977. [Google Scholar]
- 2.秦 平, 侯 明. 2012版成人原发免疫性血小板减少症诊治的中国专家共识解读[J] 临床血液学杂志. 2013;26(2):151–155. [Google Scholar]
- 3.林 文远, 陈 蓓莉, 莫 东华, et al. 咖啡酸片在特发性血小板减少性紫癜治疗中的疗效观察[J] 实用医学杂志. 2009;25(20):3491–3492. [Google Scholar]
- 4.李 英华, 罗 建民. CFA治疗糖皮质激素不敏感或不耐受慢性免疫性血小板减少症的临床观察[J] 临床血液学杂志. 2013;26(2):193–195. [Google Scholar]
- 5.刘 冯, 肖 丁华. 咖啡酸片治疗慢性难治性ITP的临床疗效观察[J] 淮海医药. 2011;29(5):377–379. [Google Scholar]
- 6.杨 九凌, 祝 晓玲, 李 成文, et al. 咖啡酸及其衍生物咖啡酸苯乙酯药理作用研究进展[J] 中国药学杂志. 2013;48(8):577–580. [Google Scholar]
- 7.张 强, 胡 志力, 王 福文, et al. 咖啡酸对阿糖胞苷致小鼠白细胞、血小板减少及血小板体积变化的预防和治疗作用[J] 中国临床药理学与治疗学. 2008;13(5):508–511. [Google Scholar]
- 8.祝 晓玲, 陆 阳, 李 成文, et al. 咖啡酸对化疗后骨髓抑制合并肺组织急性损伤小鼠毛细血管通透性及免疫功能的影响[J] 中药药理与临床. 2013;29(1):23–25. [Google Scholar]
- 9.祝 晓玲, 牟 金香, 任 海义, et al. 咖啡酸对白细胞及血小板减少症小鼠凝血功能的影响[J] 中药药理与临床. 2014;30(1):46–48. [Google Scholar]
- 10.祝 晓玲, 潘 秀芝, 任 海义, et al. 咖啡酸对白细胞及血小板减少症小鼠外周血血小板膜糖蛋白表达水平的影响[J] 中药药理与临床. 2013;29(2):24–26. [Google Scholar]
- 11.Provan D, Stasi R, Newland AC, et al. International consensus report on the investigation and management of primary immune thrombocytopenia[J] Blood. 2010;115(2):168–186. doi: 10.1182/blood-2009-06-225565. [DOI] [PubMed] [Google Scholar]