Abstract
目的
探讨口服美法仑联合大剂量地塞米松(MDex)方案一线治疗原发性轻链型淀粉样变(pAL)的疗效。
方法
收集2009年1月至2017年7月接受MDex方案治疗的76例初治pAL患者临床资料,对其疗效及生存进行回顾性分析。
结果
①76例患者中,男47例,女29例,中位年龄为56(20~74)岁。66例患者可进行梅奥2004分期(1、2、3期者分别为21、32、13例),65例(85.53%)患者存在≥2个器官受累。中位疗程数为5(1~21)个。②在可评价疗效的60例患者中,总体血液学缓解率为48.33%(29/60),完全缓解率和非常好的部分缓解率均为20.00%(12/60),获得最佳血液学缓解的中位时间为5(1~15)个月;总体器官缓解率为36.67%(22/60)。③生存患者的中位随访时间为23(1~113)个月,中位无进展生存(PFS)及总生存(OS)时间及分别为34、43个月。治疗3个月后仍存活患者的中位PFS和OS时间分别为46、65个月。④梅奥2004分期3期和1~2期患者的中位OS时间分别为5、65个月,差异有统计学意义(P=0.001)。
结论
MDex方案是pAL早期患者一种有效的治疗手段,但不适用于心脏受累的晚期患者。
Keywords: 美法仑, 地塞米松, 淀粉样变,轻链型, 治疗结果
Abstract
Objective
To evaluate the response of oral melphalan plus high-dose dexamethasone (MDex) for patients with primary light chain amyloidosis (pAL).
Methods
Clinical data, hematological and organ responses, and survival of 76 patients with pAL who had received MDex from January 2009 to July 2017 were retrospectively analyzed.
Results
Of 76 patients (47 males and 29 females with the median age of 56 [range, 20–74] years old), 19.70% patients were defined as Mayo 2004 stage 3, involvement of more than or two organs was presented in 65 (85.53%) patients. Among 60 response evaluable patients, overall hematological response was 48.33% with complete response of 20.00% and very good partial response of 20.00%, respectively. The median time to the hematological response was 5 (range, 1–15) months. 36.67% patients achieved organ response. After the median follow up of 23(range, 1–113) months for surviving patients, median progression-free survival (PFS) and overall survival (OS) were 34 and 43 months, respectively. In a three months landmark analysis, the median rates of PFS and OS were 46 and 65 months, respectively. The median OS rates of patients with Mayo 2004 stage 3 and non Mayo 2004 stage 3 were 5 and 65 months (P=0.001), respectively.
Conclusion
MDex was an effective treatment for patients with early stage pAL, but was not suitable for those with severe cardiac involvement.
Keywords: Melphalan; Dexamethasone; Amyloidosis, light chain; Treatment outcome
原发性轻链型淀粉样变(pAL)是一种异常单克隆免疫球蛋白轻链沉积在组织器官内造成多器官损害的系统性疾病,其预后取决于器官受累的范围及严重程度,尤其是心脏受累的严重程度[1]。自2004年起,国外多项报道显示,口服美法仑联合大剂量地塞米松(MDex)方案的血液学缓解率较高,耐受性良好,可作为非移植候选者的一线治疗方案之一[2]–[7]。国内尚无大宗报道。因此,在本研究中我们对接受MDex方案一线治疗的76例pAL患者临床资料进行回顾性分析,旨在探讨该方案一线治疗pAL的疗效。
病例与方法
1.病例:2009年1月至2017年7月在北京协和医院确诊为pAL并接受MDex方案作为一线治疗的患者共76例,所有患者均符合文献[8]诊断标准。收集患者的人口学、器官受累、实验室检查、骨髓细胞形态学、疗效评估和生存等数据。梅奥2004分期参照文献[1]标准进行,分为3期。梅奥2012分期参照文献[9]标准进行,分为4期。器官受累参照文献[10]标准进行判定。
2.治疗:采用MDex方案,具体为:口服美法仑10 mg/m2,每日1次,第1~4天;口服地塞米松40 mg,每日1次,第1~4天。每28 d为1个疗程。
3.疗效标准:参照文献[11]定义的标准进行血液学疗效和器官疗效评价。血液学疗效分为完全缓解(CR)、非常好的部分缓解(VGPR)、部分缓解(PR)、未缓解和疾病进展。获得以下任何一种器官缓解即定义为器官缓解:①肾脏缓解:24 h尿总蛋白(基线>0.5 g)下降超过基线值的50%,且血清肌酐或肾小球滤过率升高不超过基线值的1.25倍。②心脏缓解:血清N-末端脑钠肽前体(NT-proBNP)(基线>650 ng/L)下降超过30%或绝对值下降超过300 ng/L,或纽约心脏病协会(NYHA)心功能分级改善超过2级。③肝脏缓解:ALP水平下降超过基线值的50%或肝脏缩小2 cm以上。
4.随访:采用门诊或电话联系方式进行随访,末次随访时间为2017年8月1日。无进展生存(PFS)定义为开始治疗至疾病进展(血液学进展或死于原发病)或末次随访的间隔时间。总生存(OS)定义为治疗开始至任何原因死亡或末次随访的间隔时间。
5.统计学处理:采用SPSS 23.0软件进行统计学分析,采用Kaplan-Meier法绘制生存曲线。P<0.05为差异有统计学意义。
结果
1.一般临床资料:76例患者中,男47例,女29例,中位年龄为56(20~74)岁。κ型15例,λ型61例。器官受累:心脏54例(71.05%)、肾脏52例(68.42%)、肝脏21例(27.63%)、周围神经11例(14.47%)、胃肠道4例(5.26%),肺脏4例(5.26%)。65例(85.53%)患者存在2个或2个以上的器官受累。中位NT-proBNP为838(52~19 188)ng/L,中位24 h尿总蛋白量为2.26(0.05~34.00)g,中位血清肌酐为75(46~501)µmol/L,中位ALP为100(33~705)U/L,中位游离轻链差值(dFLC)为86.8(4.4~4 953.5)mg/L,中位骨髓浆细胞比例为0.040(0~0.240)。66例患者可进行梅奥2004分期,1、2、3期者分别为21例(31.82%)、32例(48.48%)和13例(19.70%)。52例患者可进行梅奥2012分期,1、2、3、4期者分别为23例(44.23%)、12例(23.08%)、15例(28.85%)和2例(3.85%)。
2.疗效评估:76例患者的中位疗程数为5(1~21)个。可评价疗效患者60例,另16例患者开始MDex方案化疗后未按时返回接受评估。总体血液学缓解率为48.33%(29例),包括CR 12例(20.00%)、VGPR 12例(20.00%)和PR 5例(8.33%)。获得最佳血液学缓解的中位时间为5(1~15)个月。总体器官缓解率为36.67%(22例),其中:心脏缓解率为25.00%(10/40),治疗至心脏缓解的中位时间为6(3~21)个月;肾脏缓解率为37.21%(16/43),治疗至肾脏缓解的中位时间为11(5~78)个月;肝脏缓解率为10.53%(2/19),2例患者治疗至缓解的时间分别为15和78个月。
3.生存分析:至末次随访时,76例患者中死亡31例,其中28例因恶性心律失常或心力衰竭死亡(12例于治疗3个月内死亡),1例因肝脏受累晚期、肝脏衰竭死亡,1例因消化道受累、肠梗阻死亡,1例死亡原因不详。失访10例。生存患者的中位随访时间为23(1~113)个月。所有患者的中位PFS、OS时间分别为34、43个月(图1)。3个月Landmark分析结果显示,治疗3个月后仍存活患者的中位PFS、OS时间分别为46、65个月(图2)。未获得(31例)和获得(29例)血液学缓解患者的中位OS时间分别为7个月和未达到,差异有统计学意义(P<0.001)(图3)。梅奥2004分期3期(13例)和1~2期(53例)患者的中位OS时间分别为5个月和65个月,差异有统计学意义(P=0.001)(图4)。
图1. 76例初治原发性轻链型淀粉样变患者经MDex方案治疗后的无进展生存(PFS)和总生存(OS)曲线.
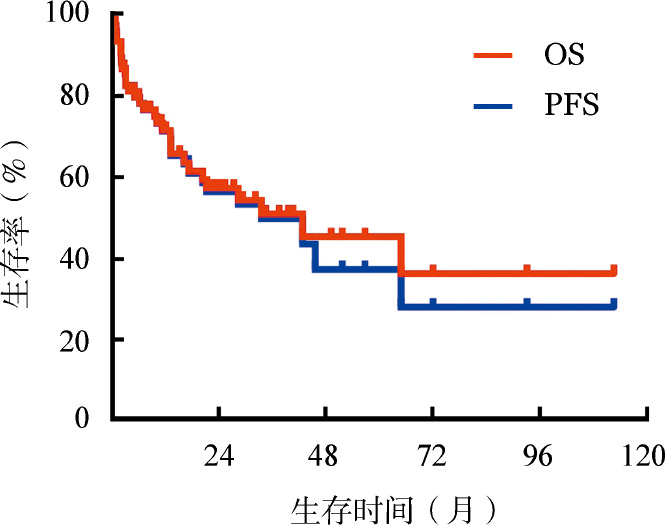
图2. 经MDex方案治疗3个月后仍存活的64例患者的无进展生存(PFS)和总生存(OS)曲线.
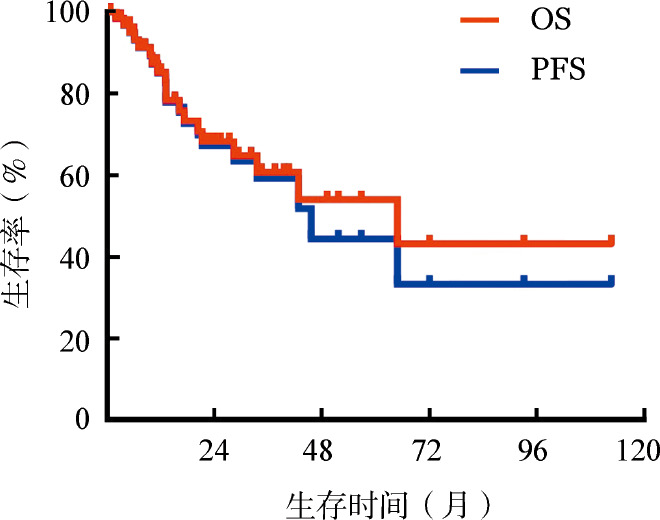
图3. 经MDex方案治疗后获得血液学缓解对患者总生存的影响.
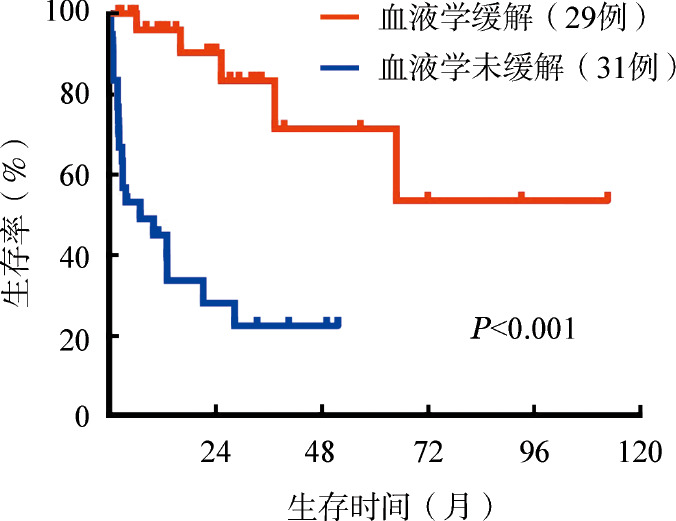
图4. 不同梅奥2004分期患者经MDex方案治疗后的总生存曲线.
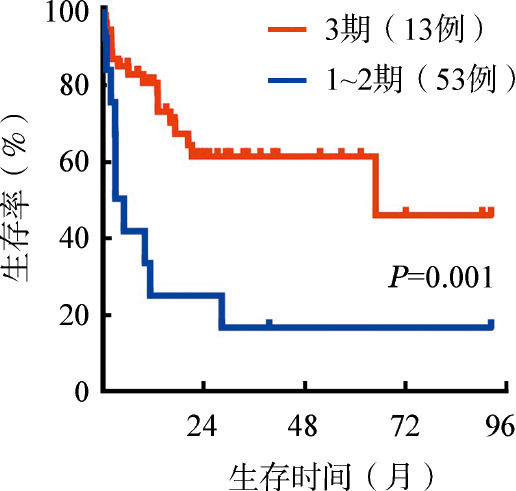
讨论
Palladini等[2]于2004年首次报道采用MDex方案治疗pAL。其后,报道治疗后患者的血液学缓解率高达67%,获得血液学缓解的中位时间为4.5个月,器官缓解率为48%,中位PFS和OS时间分别为46和61个月[4]。Jaccard等[3]的一项多中心研究结果显示MDex方案治疗pAL的血液学缓解率及器官缓解率分别为68%和39%,中位OS时间可达56.9个月。Gertz等[7]的研究结果则不如前述两项研究,MDex方案治疗后pAL患者的血液学缓解率及器官缓解率分别为55.9%和32.4%,3年的PFS及OS率分别为29.1%和58.8%。本组患者的血液学缓解率为48.33%,接近文献[7]报道的结果,但较文献[3]–[4]报道的结果明显偏低,中位OS时间也较短(分别为43、61、56.9个月)。分析可能的原因为:①本研究采用了更加严格的纳入血清游离轻链的血液学缓解评价标准[11],与文献[7]一致,而文献[3]–[4]报道的研究则以传统的血液学缓解评价标准为主;②本组患者的临床分期相对较晚,≥2个器官受累者占85.53%,梅奥2004分期3期者占19.70%,治疗开始后3个月内的早期病死率高达15.79%,与文献[3]报道的130 d内病死率14.6%相似,而文献[2]报道的3个月内早期病死率仅4.3%。但是,本组患者中治疗3个月后仍存活患者的预后则较好,中位PFS和OS时间分别为46、65个月,与文献[4]报道的结果相似。
Palladini等[4]对46例接受MDex方案治疗的pAL患者中位随访5年后,结果显示,未获得与获得血液学缓解患者的OS时间分别为25个月和未达到(P<0.01)。Lebovic等[5]的研究纳入了40例心脏受累的pAL患者,结果显示,未获得和获得血液学缓解患者的中位OS时间分别为9和22个月(P=0.005)。我们的研究结果显示,两组患者的中位OS时间分别为7个月和未达到(P<0.001)。上述研究结果表明,获得血液学缓解患者的预后明显好于未获得者,故获得血液学缓解是pAL患者治疗的首要目标。
Lebovic等[5]的研究显示心脏受累患者接受MDex方案治疗后,其中位OS时间仅为10.5个月。我们在研究中也发现,梅奥2004分期3期患者的OS时间明显短于1~2期者(5对65个月,P=0.001)。因此,MDex方案可能不适用于心脏受累的晚期pAL患者,这是因为心脏受累的晚期pAL患者治疗开始3个月内的早期病死率较高,而MDex方案起效较慢,获得血液学缓解的时间需4.5个月左右[2]。Jaccard等[12]的一项多中心研究结果显示对于梅奥2004分期3期的患者,采用硼替佐米、环磷酰胺联合地塞米松(VCD)方案可更快地获得血液学缓解,获得最佳血液学缓解的中位时间仅为2.1(0.7~11.0)个月,预计1年OS率为57%。我们中心的既往数据也显示VCD方案治疗初治pAL患者获得血液学缓解的中位时间为1(1~15)个月[13]。并且,目前美法仑在中国大陆尚未上市,患者获得药物相对不便。故对于心脏受累的晚期pAL患者,MDex方案并非首选方案,可考虑采用VCD方案。
综上,MDex方案治疗pAL患者有较高的血液学缓解率和PFS、OS率,可作为早期pAL患者的标准治疗方案之一。
References
- 1.Dispenzieri A, Gertz MA, Kyle RA, et al. Serum cardiac troponins and N-terminal pro-brain natriuretic peptide: a staging system for primary systemic amyloidosis[J] J Clin Oncol. 2004;22(18):3751–3757. doi: 10.1200/JCO.2004.03.029. [DOI] [PubMed] [Google Scholar]
- 2.Palladini G, Perfetti V, Obici L, et al. Association of melphalan and high-dose dexamethasone is effective and well tolerated in patients with AL (primary) amyloidosis who are ineligible for stem cell transplantation[J] Blood. 2004;103(8):2936–2938. doi: 10.1182/blood-2003-08-2788. [DOI] [PubMed] [Google Scholar]
- 3.Jaccard A, Moreau P, Leblond V, et al. High-dose melphalan versus melphalan plus dexamethasone for AL amyloidosis[J] N Engl J Med. 2007;357(11):1083–1093. doi: 10.1056/NEJMoa070484. [DOI] [PubMed] [Google Scholar]
- 4.Palladini G, Russo P, Nuvolone M, et al. Treatment with oral melphalan plus dexamethasone produces long-term remissions in AL amyloidosis[J] Blood. 2007;110(2):787–788. doi: 10.1182/blood-2007-02-076034. [DOI] [PubMed] [Google Scholar]
- 5.Lebovic D, Hoffman J, Levine BM, et al. Predictors of survival in patients with systemic light-chain amyloidosis and cardiac involvement initially ineligible for stem cell transplantation and treated with oral melphalan and dexamethasone[J] Br J Haematol. 2008;143(3):369–373. doi: 10.1111/j.1365-2141.2008.07327.x. [DOI] [PubMed] [Google Scholar]
- 6.Palladini G, Milani P, Foli A, et al. Oral melphalan and dexamethasone grants extended survival with minimal toxicity in AL amyloidosis: long-term results of a risk-adapted approach[J] Haematologica. 2014;99(4):743–750. doi: 10.3324/haematol.2013.095463. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 7.Gertz MA, Lacy MQ, Dispenzieri A, et al. Stem cell transplantation compared with melphalan plus dexamethasone in the treatment of immunoglobulin light-chain amyloidosis[J] Cancer. 2016;122(14):2197–2205. doi: 10.1002/cncr.30051. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 8.中国抗癌协会血液肿瘤专业委员会, 中华医学会血液学分会白血病淋巴瘤学组. 原发性轻链型淀粉样变的诊断和治疗中国专家共识(2016年版)[J] 中华血液学杂志. 2016;37(9):742–746. doi: 10.3760/cma.j.issn.0253-2727.2016.09.003. [DOI] [Google Scholar]
- 9.Kumar S, Dispenzieri A, Lacy MQ, et al. Revised prognostic staging system for light chain amyloidosis incorporating cardiac biomarkers and serum free light chain measurements[J] J Clin Oncol. 2012;30(9):989–995. doi: 10.1200/JCO.2011.38.5724. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 10.Gillmore JD, Wechalekar A, Bird J, et al. Guidelines on the diagnosis and investigation of AL amyloidosis[J] Br J Haematol. 2015;168(2):207–218. doi: 10.1111/bjh.13156. [DOI] [PubMed] [Google Scholar]
- 11.Comenzo RL, Reece D, Palladini G, et al. Consensus guidelines for the conduct and reporting of clinical trials in systemic light-chain amyloidosis[J] Leukemia. 2012;26(11):2317–2325. doi: 10.1038/leu.2012.100. [DOI] [PubMed] [Google Scholar]
- 12.Jaccard A, Comenzo RL, Hari P, et al. Efficacy of bortezomib, cyclophosphamide and dexamethasone in treatment-naïve patients with high-risk cardiac AL amyloidosis (Mayo Clinic stage III)[J] Haematologica. 2014;99(9):1479–1485. doi: 10.3324/haematol.2014.104109. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 13.Shen KN, Feng J, Huang XF, et al. At least partial hematological response after first cycle of treatment predicts organ response and long-term survival for patients with AL amyloidosis receiving bortezomib-based treatment[J] Ann Hematol. 2017;96(12):2089–2094. doi: 10.1007/s00277-017-3132-5. [DOI] [PubMed] [Google Scholar]


