Abstract
目的
评价重组人血小板生成素(rhTPO)减量维持治疗对于原发免疫性血小板减少症(ITP)的有效性和安全性。
方法
ITP患者接受连续2周的rhTPO治疗(300 U·kg−1·d−1),PLT ≥ 50×109/L者进入维持治疗。入组者初始给予隔日用药方案,根据血小板计数调整rhTPO给药间隔,维持PLT(30~100)×109/L,维持治疗共12周。
结果
在91例rhTPO治疗有效的患者中,14例退出研究(12例依从性欠佳,2例经研究者决定换用其他治疗方案)。77例患者完成研究,其中38例在12周维持治疗中始终维持治疗有效(PLT≥30×109/L)。在维持治疗第4、8、12周时,治疗有效率分别为92.6%(63/68)、82.7%(43/52)、85.0%(34/40)。所有接受治疗患者的中位血小板计数波动于(70~124)×109/L。rhTPO相关不良反应发生率为7.7%,均为轻度。
结论
延长给药间隔的减低剂量rhTPO维持治疗可使绝大多数ITP患者的血小板计数维持于安全水平,但给药间隔差异较大,需进行个体化调整。
Keywords: 血小板减少, 重组人血小板生成素, 治疗结果, 药物毒性
Abstract
Objective
To evaluate the efficacy and safety of maintenance therapy with reduced dose of rhTPO in the patients with primary immune thrombocytopenia (ITP) who attained stable platelet (PLT) counts after daily administration of rhTPO.
Methods
Treatment was started with a daily administration of rhTPO (300 U/kg) for 2 consecutive weeks. Patients who attained stable PLT≥50×109/L were enrolled to maintenance therapy starting with every other day administration of rhTPO, then adjusted dose interval to maintain platelet count (30–100) ×109/L.
Results
A total of 91 eligible patients were enrolled. Fourteen patients discontinued the study due to noncompliance (12/14) and investigator decision (2/14). Among 77 patients who completed the study, 38 patients with the administration of rhTPO at every other day or less could maintain PLT≥30×109/L for 12 weeks. The percentage of patients with a platelet response (PLT≥30×109/L) at 4th week, 8th week and 12th week of maintain therapy was 92.6% (63/68), 82.7% (43/52) and 85.0% (34/40), respectively. Median platelet counts remained in the range of (70–124) ×109/L. The overall incidence of rhTPO-related adverse events was 7.7%. All the adverse events were generally mild.
Conclusion
Extending the dose interval of rhTPO is feasible to maintain stable platelet count in the patients with ITP, but the optimal dose interval is uncertain and might vary with individuals.
Keywords: Thrombocytopenia, Recombinant human thrombopoietin, Treatment outcome, Drug toxicity
原发免疫性血小板减少症(ITP)是由于机体自身免疫功能异常,产生针对血小板/巨核细胞的抗体,导致血小板破坏过多或巨核细胞生成障碍,使患者血小板数量减少[1]–[2],临床上以不同程度出血为主要表现。近年来国内外ITP诊疗指南或专家共识均将治疗目标定为提升并维持血小板计数在“安全”范围内[3]–[4]。国内专家共识已将包括重组人血小板生成素(rhTPO)在内的促血小板生成药物推荐用于成人ITP的二线治疗和紧急治疗[4]。国内多项临床研究均显示,rhTPO短期使用(≤14 d)治疗ITP患者的有效率为60%~80%,但绝大多数患者在停药后2~4周血小板计数下降到基线水平[5]–[6]。罗米司亭和艾曲泊帕等TPO受体激动剂在ITP患者中长期治疗的安全性和有效性已被证实[7]–[8],rhTPO是否也可用于ITP患者的长期维持治疗,目前尚无相关临床研究。药代动力学研究显示,人体单次皮下注射rhTPO的消除半衰期为47~52 h[9],在维持治疗中能否将推荐的每日1次延长为隔日1次甚至间隔更长,有待进一步研究证实。
本研究旨在分析对rhTPO治疗有效的ITP患者接受rhTPO减量维持治疗的有效性和安全性。
病例与方法
1.受试者入选标准:①诊断符合文献[4]标准,入组前确诊为ITP至少1个月;②既往肾上腺糖皮质激素正规治疗无效或复发;③使用rhTPO前连续2次PLT<30×109/L,且rhTPO治疗有效(连续2次PLT≥50×109/L)。
2.排除标准:①妊娠或哺乳;②既往有血栓病史;③心肺功能明显异常;④肝肾功能异常(肌酐≥176.8 µmol/L,转氨酶、胆红素水平高于正常值上限2倍);⑤同时患有恶性肿瘤;⑥研究期间不能有效采取避孕措施;⑦同时应用其他治疗ITP的药物(入组前至少4周使用稳定剂量糖皮质激素者除外);⑧研究者认为患者不适宜参加本试验的其他情况。
3.试验设计与治疗方案:采用多中心、开放单臂试验方法,由13家医院协同完成,计划入组120例患者。试验分为两个阶段。①入组前筛选阶段:糖皮质激素正规治疗无效或复发的ITP患者,若连续2次PLT<30 ×109/L,给予rhTPO 300 U·kg−1·d−1,疗程≤14 d;PLT≥100×109/L时停用rhTPO,14 d内若连续2次PLT≥50×109/L,则进入维持治疗。②维持治疗:维持治疗疗程为12周。给药方法:rhTPO 300 U/kg,初始给药间隔为隔日1次,每周监测血小板计数,根据以下方案调整给药间隔:PLT连续2次>150×109/L者,停药观察,待PLT降至≤150×109/L恢复用药;PLT(100~150)×109/L者,延长给药间隔;PLT(30~100)×109/L者,剂量不作调整;连续2次PLT<30×109/L者退出研究。完成试验后至少随访1个月。
用药过程中如出现口、鼻或内脏等部位活跃出血,可输注血小板、静脉丙种球蛋白(IVIg)和(或)抗纤溶药物,禁用其他治疗ITP的药物。在维持阶段,由于合并疾病和(或)相关治疗药物导致血小板计数下降至<30×109/L,允许继续观察1周,期间rhTPO给药频率可酌情调整至每日1次;1周后,血小板计数仍低于30×109/L者退出研究。本研究获得所有参与单位伦理委员会的批准,受试者均知情同意并签署知情同意书。
4.研究终点:①主要研究终点:减量维持治疗有效率(接受治疗期间持续维持PLT≥30×109/L的患者比例),若两次复查PLT<30×109/L者视为维持治疗无效。②次要研究终点:长期维持治疗的安全性,药物不良事件按CTCAE3.0标准进行分级。
5.统计学处理:应用SPSS22.0软件进行统计学分析。符合正态分布的连续变量采用独立样本t检验;分类变量采用卡方检验。P<0.05为差异有统计学意义。
结果
1.一般资料:2011年6月至2014年6月13个中心共筛选入组91例患者。所有受试者中,女性51例,男性40例,中位年龄为37(3~74)岁;中位病程为10个月(1个月~30年);诊断时骨髓巨核细胞中位数为169(5~886)个,基线血小板计数中位数为10(0~44)×109/L,筛选期rhTPO使用时间中位数为9.5(3~22)d,rhTPO治疗后血小板计数峰值中位数为112.5(51~516)×109/L,其中51例患者在治疗后达到完全反应(CR)[4]。
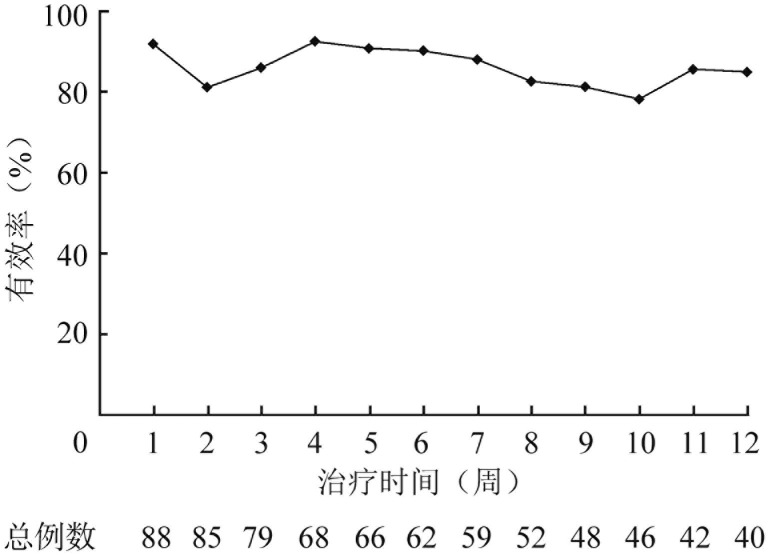
2.有效性:91例患者接受rhTPO维持治疗,其中12例因依从性差退出研究,2例研究者建议更换治疗方案。77例按照试验方案进行维持治疗,38例患者完成12周维持治疗,39例患者因维持治疗无效退出本研究(0~4、5~8、9~12周分别退出16、13、10例)。在维持治疗第4、8、12周,治疗有效率分别为92.6%(63/68)、82.7%(43/52)、85.0%(34/40)(图1);接受治疗的患者血小板计数中位数波动于(70~124)×109/L。
图1. 原发免疫性血小板减少症重组人血小板生成素减量维持治疗的有效率.
在入组患者中,6例(6.6%)患者合并使用稳定剂量糖皮质激素(泼尼松≤20 mg/d),其中2例在维持治疗的第4、5周停用,另4例逐渐减量,但至研究结束仍未停用;1例患者在研究期间因合并感染导致血小板计数下降,予IVIg输注,其余患者均未合并使用其他治疗措施。
根据血小板计数调整rhTPO给药间隔,不同患者之间的给药间隔无明确规律性,部分患者在整个维持治疗阶段的给药间隔也不一致。在完成治疗的患者中,持续隔日用药者为11例,每周1~3次者8例,每周1次甚至更少者8例(其中4例在维持用药1~3周停药,观察期间血小板计数正常)。
对入组时患者的性别、年龄、病程、诊断时骨髓中巨核细胞数量、对rhTPO治疗反应(是否达到CR)等因素进行单因素分析,结果表明仅rhTPO治疗反应与减低剂量维持治疗有效相关(表1)。
表1. rhTPO维持治疗原发免疫性血小板减少症患者疗效的单因素分析.
| 因素 | 无效组(39例) | 完成组(38例) | 统计量 | P值 |
| 年龄[岁,M(范围)] | 31(3~68) | 40.5(13~74) | −1.456(t值) | 0.150 |
| 男性[例(%)] | 14(35.9) | 19(50.0) | 1.563(χ2值) | 0.211 |
| 病程[例(%)] | 2.906(χ2值) | 0.234 | ||
| 1~3个月 | 9(23.1) | 15(39.5) | ||
| 4~12个月 | 9(23.1) | 6(15.8) | ||
| >12个月 | 17(43.6) | 12(31.6) | ||
| 不详 | 4(10.2) | 5(13.1) | ||
| 基线骨髓巨核细胞数[个,M(范围)] | 179.5(6~793) | 186(5~750) | −0.530(t值) | 0.958 |
| rhTPO治疗CR率[例(%)] | 16(41.0) | 25(65.8) | 4.741(χ2值) | 0.029 |
注:rhTPO:重组人血小板生成素;CR:完全反应
3.安全性:本研究中,无一例患者因rhTPO相关不良反应而退出研究。维持治疗期间共发生26例次不良反应,绝大多数为Ⅰ/Ⅱ度,可自行缓解或对症处理后缓解(详见表2)。研究者认为与rhTPO用药“可能有关”和“肯定有关”的不良事件被认定为rhTPO相关性不良事件,共有7例次(7.7%),分别为皮疹(2例)、肝酶升高(3例)及抗体产生(2例);无血栓并发症:仅2例患者在维持治疗结束后复查骨髓象,均未见网织纤维增多。所有患者在入组时无明显出血表现,其中4例患者在研究期间报告发生严重出血事件,其中月经过多2例、口腔血疱1例、创伤后局部血肿1例。口腔血疱者曾予IVIg治疗,余3例仅给予对症处理。
表2. 原发免疫性血小板减少症rhTPO维持治疗的不良事件发生情况.
| 不良事件 | 例数(%) |
| 肝酶升高(Ⅰ/Ⅱ度) | 6(6.6) |
| 感染 | 10(11.0) |
| 流感样症状(Ⅰ/Ⅱ度) | 8 |
| 肺感染(Ⅲ度) | 1 |
| 发热Ⅱ度 | 1 |
| 腹泻(Ⅰ度) | 1(1.1) |
| 皮疹(Ⅰ度) | 1(1.1) |
| 注射部位反应(Ⅰ度) | 1(1.1) |
| TPO抗体 | 2(2.2) |
| 创伤(Ⅰ度) | 1(1.1) |
| 出血事件 | 4(4.4) |
| 月经过多(Ⅰ度) | 2 |
| 口腔内出血(Ⅰ度) | 1 |
| 血肿(Ⅰ度) | 1 |
注:rhTPO:重组人血小板生成素
13例患者接受TPO抗体动态检测(筛选用药14 d后、退组/完成治疗以及治疗结束后1个月),其中2例为阳性,进一步检测中和抗体为阴性。在抗体阳性的患者中,1例在维持治疗4周后失去疗效,退出研究时检出抗体,未获得治疗结束1个月时的标本,该患者后续给予利妥昔单抗治疗,此后血小板计数恢复正常;另1例患者在筛选期结束后出现抗体,继续进入维持治疗,血小板计数维持在50×109/L以上,第10周时因感染导致血小板计数明显下降而退出研究,当时复查抗体为阴性。
讨论
近年来,国内多项研究显示rhTPO短期治疗ITP具有较高的有效率[5]–[6],[10]–[11],同时联合不同剂量糖皮质激素、利妥昔单抗以及环孢素A等可缩短药物起效时间,减少出血风险,进一步提高治疗有效率[12]–[15]。
部分慢性ITP患者仍需长期使用促血小板生成类药物方能维持血小板水平于安全范围内。目前艾曲泊帕和罗米司亭等在ITP患者中长期使用的有效性和安全性已被多项研究证实[7]–[8],[16],但绝大多数研究均采用“标准剂量”(维持原用药方案)治疗,小剂量用药或者延长给药间隔的“减低剂量”维持治疗仅见于个案报道或病例数较少的研究,是否有效尚无定论。Vlachaki等[17]报道,4例慢性ITP患者在经“标准剂量”艾曲泊帕治疗获得CR后,采用“减低剂量”维持治疗,均获得持续缓解。作者推测可能是种族、代谢酶以及转运体的遗传差异造成个体间药代动力学差异,使得部分患者可采用更小剂量、更长间隔进行维持治疗。Mitrovic等[18]报道1例难治性ITP患者经罗米司亭(每周4 µg/kg)治疗获得CR,此后采取按需治疗策略(PLT<150×109/L时给予罗米司亭250 µg或4 µg/kg)维持治疗,每周给药中位剂量降至1.9 µg/kg。但Park等[19]在一项关于罗米司亭的“减低剂量”治疗ITP患者的多中心、前瞻性研究中发现,经罗米司亭治疗有效者[即固定剂量使血小板计数达(50~200)×109/L至少4周],采用隔周给药维持方案,无论是原剂量或者增加至原剂量的1.5倍,均不能长期维持PLT>30×109/L。
本研究是迄今为止关于ITP患者“减低剂量”维持治疗中入组病例数最多的研究,采用延长rhTPO给药间隔的治疗方案,结果显示rhTPO维持治疗的有效率达80%以上,但退出研究的受试者比例较高(53/91)。首先,与罗米司亭类似,延长rhTPO给药间隔后,部分受试者的血小板计数不能维持于目标值以上。朱铁楠等[20]在血小板减少患者中多次皮下注射rhTPO药代动力学研究中发现血药浓度升高的水平与给药的累积剂量正相关,且药物在体内无蓄积倾向,故延长给药间隔导致稳态谷浓度呈下降趋势。“减低剂量”治疗可能使受试者体内的谷浓度不同程度下降,进而造成血小板计数下降。本研究中至少有20例患者采用隔日给药后不能维持PLT≥30×109/L而退出研究。延长给药间隔并酌情增加单次给药剂量能否提高治疗有效率值得研究。其次,本研究的方案设计与在其他促血小板生成药物的长期研究有所不同。本研究中连续两次血小板计数低于30×109/L者被视为治疗无效并退组。若患者因合并症和(或)相关用药导致血小板快速下降,仅给予1周的窗口期,若无法恢复至≥30×109/L,视为治疗失败;本研究中10例(25.6%)患者因合并感染和(或)出血事件(包括月经过多及外伤后局部大血肿)导致血小板计数明显下降。同时,本研究不允许使用其他治疗方法,仅有6例患者合并使用低剂量糖皮质激素,其中2例逐渐减量并停用。而其他促血小板生成药物的维持治疗研究多侧重于长期治疗的安全性,绝大多数研究并无针对于血小板反应的退组要求;同时允许合并用药和(或)解救治疗(包括切脾),联合其他治疗方案的患者占13%~33%[7]–[8]。最后,由于注射和监测频繁,患者依从性欠佳,导致部分患者给药调整不够及时,血小板水平出现骤降。
本研究中不同患者之间给药间隔并不一致,即使同一患者的给药间隔也并不固定。我们认为可能与rhTPO在不同患者个体间血药浓度差异较大[20],且血小板水平受合并疾病和(或)相关用药影响较大等因素相关。
本研究中,无一例患者由于药物不良反应而退出研究。与rhTPO相关的不良事件包括皮疹、肝酶升高、抗体产生,程度均较轻,与既往rhTPO短期应用的研究报道[5],[12],[21]类似。其中抗体产生值得引起临床重视。此前华宝来等[22]发现3.7%(3/81)的患者在用药后出现抗TPO抗体,但抗体不具有中和rhTPO的活性。在维持治疗期间,未出现新的与时间相关不良事件,且不良事件发生率无明显增加。在本研究中未发现血栓事件。
本研究显示,rhTPO的“减低剂量”维持治疗在ITP患者中具有较好的疗效,但给药间隔需进行个体化调整,药物的安全性与短期使用相当。本研究未获得足够数量的样本对受试者的骨髓中网织纤维增生情况、TPO抗体生成等进行评估,且随访时间相对较短,安全性评估尚不够全面;此外,延长给药间隔后酌情提高rhTPO单次给药剂量能否进一步提高有效率,希望在后续的研究中能够进一步明确。
References
- 1.McMillan R. Chronic idiopathic thrombocytopenic purpura[J] N Engl J Med. 1981;304(19):1135–1147. doi: 10.1056/NEJM198105073041904. [DOI] [PubMed] [Google Scholar]
- 2.Kelton JG, Gibbons S. Autoimmune platelet destruction: idiopathic thrombocytopenic purpura[J] Semin Thromb Hemost. 1982;8(2):83–104. doi: 10.1055/s-2007-1005045. [DOI] [PubMed] [Google Scholar]
- 3.Provan D, Stasi R, Newland AC, et al. International consensus report on the investigation and management of primary immune thrombocytopenia[J] Blood. 2010;115(2):168–186. doi: 10.1182/blood-2009-06-225565. [DOI] [PubMed] [Google Scholar]
- 4.中华医学会血液学分会止血与血栓学组. 成人原发免疫性血小板减少症诊断与治疗中国专家共识(2016年版)[J] 中华血液学杂志. 2016;37(2):89–93. doi: 10.3760/cma.j.issn.0253-2727.2016.02.001. [DOI] [Google Scholar]
- 5.赵 永强, 王 庆余, 翟 明, et al. 重组人血小板生成素治疗慢性难治性特发性血小板减少性紫癜的多中心临床试验[J] 中华内科杂志. 2004;43(8):608–610. doi: 10.3760/j.issn:0578-1426.2004.08.015. [DOI] [PubMed] [Google Scholar]
- 6.Wang S, Yang R, Zou P, et al. A multicenter randomized controlled trial of recombinant human thrombopoietin treatment in patients with primary immune thrombocytopenia[J] Int J Hematol. 2012;96(2):222–228. doi: 10.1007/s12185-012-1124-8. [DOI] [PubMed] [Google Scholar]
- 7.Kuter DJ, Bussel JB, Newland A, et al. Long-term treatment with romiplostim in patients with chronic immune thrombocytopenia: safety and efficacy[J] Br J Haematol. 2013;161(3):411–423. doi: 10.1111/bjh.12260. [DOI] [PubMed] [Google Scholar]
- 8.Saleh MN, Bussel JB, Cheng G, et al. Safety and efficacy of eltrombopag for treatment of chronic immune thrombocytopenia: results of the long-term, open-label EXTEND study[J] Blood. 2013;121(3):537–545. doi: 10.1182/blood-2012-04-425512. [DOI] [PubMed] [Google Scholar]
- 9.沈 彤, 文 爱东, 赵 磊, et al. 重组人血小板生成因子注射液的I期临床药代动力学[J] 医学争鸣. 2005;26(15):1427–1430. [Google Scholar]
- 10.郑 杰, 马 静瑶, 苏 雁, et al. 重组人血小板生成素治疗儿童重症免疫性血小板减少症25例临床观察[J] 中国实验血液学杂志. 2014;22(2):393–398. doi: 10.7534/j.issn.1009-2137.2014.02.023. [DOI] [PubMed] [Google Scholar]
- 11.刘 隽, 程 毅敏, 邹 丽芳, et al. 重组人血小板生成素治疗老年慢性免疫性血小板减少性紫癜的疗效观察[J] 中国临床医学. 2013;20(3):390–392. doi: 10.3969/j.issn.1008-6358.2013.03.047. [DOI] [Google Scholar]
- 12.Zhou H, Xu M, Qin P, et al. A multicenter randomized open-label study of rituximab plus rhTPO vs rituximab in corticosteroid-resistant or relapsed ITP[J] Blood. 2015;125(10):1541–1547. doi: 10.1182/blood-2014-06-581868. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 13.寿 黎红, 张 慧英. 重组人血小板生成素联合减量糖皮质激素治疗老年免疫性血小板减少症[J] 实用医学杂志. 2011;27(5):874–876. [Google Scholar]
- 14.计 成阜, 何 广胜, 周 海侠, et al. 重组人血小板生成素联合环孢素A治疗难治性血小板减少症16例[J] 实用医学杂志. 2013;29(22):3789–3790. doi: 10.3969/j.issn.1006-5725.2013.22.068. [DOI] [Google Scholar]
- 15.顾 史洋, 庄 静丽, 邹 善华, et al. 重组人血小板生成素联合糖皮质激素治疗重症新诊断原发免疫性血小板减少症患者临床观察[J] 中华血液学杂志. 2013;34(10):883–886. doi: 10.3760/cma.j.issn.0253-2727.2013.10.012. [DOI] [PubMed] [Google Scholar]
- 16.Cines DB, Gernsheimer T, Wasser J, et al. Integrated analysis of long term safety in patients with chronic immune thrombocytopaenia (ITP) treated with the thrombopoietin (TPO) receptor agonist romiplostim[J] Int J Hematol. 2015;102(3):259–270. doi: 10.1007/s12185-015-1837-6. [DOI] [PubMed] [Google Scholar]
- 17.Vlachaki E, Sousos N, Perifanis V, et al. Is there a role for low-dose eltrombopag as maintenance therapy in the treatment of immune thrombocytopenia?[J] Acta Haematol. 2015;133(1):78–82. doi: 10.1159/000361075. [DOI] [PubMed] [Google Scholar]
- 18.Mitrovic M, Elezovic I, Suvajdzic-Vukovic N. ‘On-demand’ romiplostim therapy in immune thrombocytopenia[J] J Clin Pharm Ther. 2016;41(3):351–353. doi: 10.1111/jcpt.12359. [DOI] [PubMed] [Google Scholar]
- 19.Park S, Yoon SS, Lee JH, et al. Multicenter, prospective study to evaluate the efficacy of biweekly romiplostim administration in patients with immune thrombocytopenia[J] Int J Hematol. 2016;103(1):44–52. doi: 10.1007/s12185-015-1889-7. [DOI] [PubMed] [Google Scholar]
- 20.朱 铁楠, 邹 晓阳, 段 云, et al. 血小板减少患者多次皮下注射重组人血小板生成素的药代动力学研究[J] 中国临床药理学杂志. 2004;20(4):274–277. doi: 10.3969/j.issn.1001-6821.2004.04.009. [DOI] [Google Scholar]
- 21.侯 明, 李 曼, 靳 征. 重组人血小板生成素注射液上市后不良反应监测研究[J] 中国新药与临床杂志. 2015;34(8):642–646. [Google Scholar]
- 22.华 宝来, 赵 永强, 朱 铁楠, et al. 血小板减少患者皮下注射重组人血小板生成素后抗体生成的动态监测[J] 血栓与止血. 2005;11(2):59–61. doi: 10.3969/j.issn.1009-6213.2005.02.004. [DOI] [Google Scholar]