Abstract
Musik spielt im Leben eines jeden Menschen nicht nur eine wichtige Rolle, sondern hat auch Effekte auf Herzfrequenz, Blutdruck und auf andere physiologische Parameter. Obgleich das Empfinden von Musik als subjektiv zu interpretieren ist, zeigen Studien, dass objektive Parameter wie Herzfrequenz, Blutdruck unter verschiedenen Umständen eindeutig durch Musik beeinflusst werden. Mittlerweile wird Musik in vielen Fachdisziplinen der Medizin, auch im Bereich der Intensivmedizin, angewendet. Besonders Schmerz, Stress und Angst können positiv beeinflusst werden, aber auch bei Patienten im Weaning, Delir oder bei operativen Eingriffen spielt Musik eine große Rolle. Nach vielen vorliegenden Berichten und guten prospektiv-randomisierten Studien ist ein positiver Effekt von Musik in vielen Fachdisziplinen der Medizin und auch in der Intensivmedizin beobachtet worden. Auch bei postoperativen Patienten, ob aus der Viszeralchirurgie, der Herzchirurgie, der Orthopädie und der Frauenheilkunde, um exemplarisch nur einige zu nennen, wurden positive Wirkungen von Musik hinsichtlich der Parameter Schmerz, Stress und Angst nachgewiesen. Auch wenn viele physiologische und pathophysiologische Zusammenhänge der Wirkung von Musik nicht im Detail geklärt sind, ist die zerebrale Verarbeitung unterschiedlicher Impulse für die Effekte von Musik entscheidend. Die besten Effekte wurden beim Hören klassischer Musik beobachtet, besonders Kompositionen von Bach, Mozart oder italienischen Komponisten sind hier zu nennen.
Schlüsselwörter: Herz-Kreislauf-System, Klassische Musik, Blutdruck, Herzfrequenz, Intensivmedizin
Abstract
Music not only plays an important role in everyone’s life, it also has effects on heart rate, blood pressure and other physiological parameters. Although music can be interpreted as a subjective feeling, studies have shown that objective parameters such as heart rate, blood pressure and other physiological parameters are clearly influenced by music in various circumstances. Meanwhile, music is used in many medical disciplines, including the area of intensive care medicine. Pain, stress and fear in particular can be influenced positively, but music also plays a major role in patients with delirium and during weaning or surgical interventions. According to many available reports and good prospective studies, a positive effect of music has been observed in many medical disciplines and also in intensive care. Also in postoperative patients, whether from visceral surgery, cardiac surgery, orthopaedics or gynecology, to name just a few, positive effects of music with regard to the parameters pain, stress and anxiety have been demonstrated. Even if many physiological and pathophysiological relationships between the effects of music are not explained in detail, the cerebral processing of different impulses is decisive for the effects of music. The most benefit on health is visible with classic music, particularly in compositions of Bach, Mozart or Italian composers.
Keywords: Cardiovascular system, Classical music, Blood pressure, Heart rate, Intensive care medicine
Einleitung
Es ist seit Jahrhunderten bekannt, dass Musik den Menschen beeinflussen kann und dass durch Musik bereits in der Antike bei Olympischen Spielen eine Leistungssteigerung bei Athleten beobachtet wurde [32, 36]. Aber auch zu Heilzwecken wurde Musik sowohl bei Naturvölkern als auch in den alten Hochkulturen bis zur griechisch-römischen Antike eingesetzt [3]. Darüber hinaus ist jedem bekannt, dass Musik Emotionen wecken und verstärken kann, die wiederum von verschiedenen Faktoren, wie Alter, Lebensumständen und Stimmungen, abhängig sind [27]. Seit einigen Jahren wurde darauf hingewiesen, dass Musik auch im Bereich der Medizin Effekte hat, die zu therapeutischen Zwecken angewendet werden können [2, 42]. Es handelte sich vielfach um kleinere Studien oder Fallbeobachtungen, sodass diese Untersuchungen relativ wenig wahrgenommen wurden und die Anwendung von Musik in der Medizin bisher nur in beschränkter Weise stattgefunden hat [52, 54]. In jüngster Zeit wurden nun mehrere prospektiv-randomisierte Studien vorgestellt, die den Stellenwert der Anwendung von Musik in der Medizin neu belebt haben [18, 28]. Dabei wurden besonders Beeinflussungen von Schmerz und Stress, von Blutdruck und Herzfrequenz, aber auch von intensivmedizinischen Themen, wie Beatmung und Delir, beschrieben [23, 51]. Trotz einiger neuer Studienergebnisse wird weiterhin diskutiert, ob Musik als Therapie in der Intensivmedizin als Sinn oder Unsinn anzusehen ist [45]. Auch wenn die beschriebene Evidenz dieser Studien bisher nicht so überzeugend ist, wie zur Einführung von Therapiemaßnahmen in der Intensivmedizin erwartet und gefordert wird, sind die bisher publizierten Ergebnisse zum Einsatz von Musik in der Intensivmedizin sicherlich interessant. In der vorliegenden Arbeit sollen deshalb Beobachtungen und Erfahrungen der Anwendung von Musik in der Intensivmedizin vorgestellt und kritisch diskutiert werden.
Zerebrale Verarbeitung von Musik
Musik beeinflusst zerebrale Prozesse und zahlreiche kognitive Funktionen, indem sie die Aktivitäten beider Gehirnhemisphären in die zerebralen Prozesse mit einbezieht [21]. Beide Gehirnhälften sind über das „Corpus callosum“ miteinander verbunden, das bei aktiven Musikern und Menschen, die Musik lieben und gern hören, stark ausgeprägt ist. Die Wege der zerebralen Verarbeitung von „Musikhören“, „Musikspielen“ und dem „Musikgedächtnis“ sind mittlerweile gut bekannt (Tab. 1). Musik entsteht im Gehirn, betrifft das ganze Gehirn und spricht etwa 95 % aller Menschen an; nur etwa 5 % der Menschen werden von der Musik nicht erfasst und gelten als unmusikalisch. Worte und Töne werden von 2 wichtigen Funktionen geprägt: vom Hören und Sehen [10]. Musikhören ist ein relativ komplexer Vorgang, der vom Ohr zur Hörrinde und vom Auge zur Sehrinde läuft. Drei Schritte des „Musikhörens“ sind bekannt: Im ersten Schritt werden Noten, Instrumente, Orchester usw. vom Sehareal erfasst, das optische Muster erkennt, deren Bedeutung aber nicht einschätzen kann. Im Hörareal werden akustische Impulse (Töne) gehört, die über Synapsen weitergeleitet werden und im Gehirn „Spuren“ hinterlassen [10, 21]. Im zweiten Schritt werden Gesehenes und Gehörtes zu einem Ganzen integriert, und beides (Gesehenes und Gehörtes) nimmt erstmals „Gestalt“ an und wird mit anderen Erfahrungen aus dem Gedächtnis abgeglichen, z. B. „Abspeicherung“ von Musikern, Flötisten, Geigern, Orchester usw. Musik wird also „gelernt“, akustisches „Material“ wird verarbeitet und im Gehirn „hinterlegt“ (Erinnerungen). Im dritten Schritt werden schließlich Gesehenes und Gehörtes nach Wichtigkeit bewertet. Das aktive Musizieren „Musikspielen“ betrifft im Gehirn die sensorischen Areale (Spüren und Tasten) und das Kleinhirn, das u. a. mitverantwortlich für den Rhythmus ist, für Takt, Gleichgewicht, Koordination. Auch das „Musikspielen“ läuft in mehreren Schritten ab: Der erste Schritt ist das bewusste Handeln, im zweiten Schritt werden die motorischen Areale des Gehirns aktiviert (Abb. 1). Die sensorischen Areale sind zum Spüren und Tasten unerlässlich [26]. Der Gedächtnisspeicher „Musikgedächtnis“ ist über die gesamte Großhirnrinde verteilt. Die Hirnareale, in denen Gehörtes, Gesehenes usw. zu einem Gesamten zusammengefügt werden, sind die „Assoziationsareale“. Hier werden wichtige Impulse für die Musikwirkungen gegeben [21, 26].
| Musikhören |
| Erkennen optischer Muster (Sehareal) |
| Hören von Tönen (Hörareal) |
| Integration von Gesehenem und Gehörtem |
| Abgleich mit Erfahrungen aus dem Gedächtnis |
| Bewertung von Gesehenem und Gehörtem nach Wichtigkeit |
| Musikspielen |
| Bewusstes Handeln |
| Startbefehl zum Musikspielen |
| Aktive Bewegung (motorische Areale) |
| Koordination durch Sensorik und Kleinhirn (Rhythmus, Takt) |
| Musikgedächtnis |
| Aktivierung von Assoziationsarealen (Frontalhirn) |
| Arbeitsgedächtnis (bisherige Musik, Vorlieben für bestimmte Musik) |
| Koordination von Hemmfunktionen |
| Empfindungen – Emotionen |
| Bewertung von Musik |
Anwendung von Musik in der Intensivmedizin
Es ist unbestritten, dass die Behandlung von kritisch Kranken auf Intensivstationen für alle Beteiligten immer eine besondere Herausforderung darstellt. Besonders durch die Komplexität der Krankheitsbilder und das Ineinandergreifen verschiedener pathophysiologischer Vorgänge ist die adäquate Behandlung oft schwierig und erfordert mitunter verschiedene therapeutische Maßnahmen, angefangen bei Medikamenten über Dialyseverfahren bis hin zur nichtinvasiven Atmungsunterstützung oder einer maschinellen Beatmung, wie das zur Zeit bei der Behandlung von COVID-19-Patienten sichtbar ist [38]. Manche Patienten haben im Rahmen einer intensivmedizinischen Behandlung erhebliche Beeinträchtigungen von Blutdruck und/oder Herzfrequenz, sind im Delir und/oder durch zusätzliche neurologische Affektionen gefährdet. Schließlich spielen Phänomene, wie akuter oder chronischer Schmerz, Stress und Angst, auf Intensivstationen immer eine wichtige Rolle [12]. Musikmedizinische Interventionen sind bei einigen dieser Krankheitsbilder bekannt und können sehr gut in der täglichen Patientenversorgung, auch auf einer Intensivstation, eingebracht werden [43, 45]. Dabei muss immer überlegt werden, welche Parameter beeinflusst werden sollen und wie die Anwendung von Musik im therapeutischen Gesamtkonzept sein kann [48].
Musik und kardiovaskuläre Parameter: Was ist bisher bekannt?
Bernardi und Mitarbeiter legten 2009 eine vielbeachtete systematische Untersuchung vor, bei der Effekte von klassischer Musik auf kardiovaskuläre Parameter in einer randomisierten Studie untersucht wurden [1]. Sie beobachteten 24 gesunde Probanden (Alter 25 ± 1 Jahre, 8 Männer, 16 Frauen), von denen 12 Probanden seit mindestens 3 Jahren Chorsänger waren und 12 Probanden als Kontrollgruppe herangezogen wurden. Die Probanden der Kontrollgruppe hatten keine Musikerfahrung. Alle 24 Studienprobanden hörten im Rahmen einer fest definierten Randomisierung über Kopfhörer 10 s lang Vokal- (Puccini „Turandot“) oder Instrumentalmusik (Beethoven „9. Symphonie“) bzw. Musik von Johann Sebastian (J. S.) Bach (Kantate 169: „Gott soll allein mein Herz haben“). Im Rahmen der Studie wurden auch Kompositionen von Giuseppe Verdi untersucht („Va, pensiero“ und „Libiamo ne’ lieti calici“). Aufgezeichnet wurden bei allen Probanden Elektrokardiogramm (EKG), Blutdruck (radiale Tonometrie), arterieller zerebraler Fluss (2 MHz transkranieller Doppler), respiratorische Veränderungen (Plethysmographie) und Endothelfunktion („skin photoplethysmography“). Die gemessenen Parameter wurden unter Ruhebedingungen aufgezeichnet, dann bei Musikexposition (randomisiert nach den Musikwerken 1–5) und während einer 2‑minütigen Ruhephase nach Hören der Kompositionen [1]. Es wurde in dieser Untersuchung nachgewiesen, dass der mittlere zerebrale Fluss beim Hören von „Va, pensiero“ (70,4 ± 3,3 cm/s) signifikant niedriger war als bei „Libiamo ne’ lieti calici“ (70,2 ± 3,1 cm/s; p < 0,02) bzw. Bach (70,9 ± 2,9 cm/s; p < 0,02). Die Beethoven-Symphonie hatte im Vergleich zu den Untersuchungen in Ruhe vor (67,6 ± 3,3 cm/s) und nach (69,4 ± 3,1 cm/s) Musikexposition keinen nennenswerten Einfluss auf den zerebralen Blutfluss (69,7 ± 3,0 cm/s). Es wurde beobachtet, dass jedes Crescendo zu einer endothelialen Vasokonstriktion führte mit einer Steigerung von Blutdruck und Herzfrequenz. Interessant waren Beobachtungen, dass Crescendos bei Vokal- oder Orchestermusik zu Vasokonstriktion, Blutdruck- und Herzfrequenzsteigerungen führten und vor allem das Hören der Bach-Kantate mit Vasodilatation und Blutdrucksenkung einherging. Diese Korrelationen waren gleichermaßen bei Choristen und Kontrollprobanden zu beobachten (p = ns). Es ist beachtenswert, dass die beobachteten Effekte bereits durch eine Beschallung von nur 10 s (!) erreicht wurden [1].
Einfluss verschiedener Musikstile auf kardiovaskuläre Parameter
In Untersuchungen von Trappe und Breker und Trappe und Voit konnte nachgewiesen werden, dass Musik (besonders klassische Musik) zu einer Senkung des systolischen und des diastolischen Blutdrucks führte [46, 47]. Diese Blutdrucksenkungen waren unter der Musik von J. S. Bach am stärksten ausgeprägt [46]. In der Studie von Bernardi wurde auf die Kompositionsform als wesentlicher Einflussfaktor hingewiesen und die Musik von J.S. Bach wurde als sehr günstig bewertet. Dennoch gibt es keine „spezifischen“ Merkmale, wie die Musik Bachs welche Wirkungen entfaltet. Hinweise, dass z. B. Rhythmen mit 6 Zyklen pro Minute günstig seien, wurden ebenso beschrieben wie positive Effekte bei „gleichförmiger“ Musik. „Ruhige“ Musik mit langsamen Tempo, langen Legatophasen und wenig ausgeprägter Dynamik gelten ebenfalls als günstig für die Wirkung auf das Herz-Kreislauf-System. Viele Studien haben sich in den letzten Jahren und Jahrzehnten mit Kompositionen von Wolfgang Amadeus Mozart beschäftigt. Sie zeigten, dass Mozarts Musik bei hypertensiven Ratten den Blutdruck senkt, wie wir das in einer eigenen Studie an Probanden auch gesehen haben [29, 47]. Kürzlich wurde von Gruhlke und Mitarbeitern nachgewiesen, dass es unter Musik von Mozart bei Patienten mit Myokardinfarkt zu einer deutlichen Blutdrucksenkung kam, die bei der Musik der Beatles nicht zu beobachten war [16]. Hughes und Mitarbeiter wiesen darauf hin, dass Musik von Mozart, ähnlich wie bei Bach, ein überdurchschnittliches Maß an Periodizität aufwies [19]. Auch die Musik von Johann Strauss jun. führte in einer eigenen Studie zu einer Senkung von Blutdruck und Herzfrequenz [47]. Auch Strauss’ Tänze basieren auf einfachen Strukturen, eingängigen Melodien und periodisch wiederkehrenden Formen. Die Tänze sind zu Unterhaltungszwecken geschrieben, in Dur-Tonarten, mit eingängigen Harmonieabfolgen und ohne markante Dissonanzen. Es war in unserer Studie überraschend, dass die Musik von ABBA keine bzw. nur sehr geringe Wirkungen auf Blutdruck und Herzfrequenz hatte [37, 47]. Der günstige Effekt von Musik wurde kürzlich von Burrai und Mitarbeitern in einer prospektiv-randomisierten Studie auch an 159 Patienten mit Herzinsuffizienz gesehen, die 30 min pro Tag über einen MP3-Player klassische Musik hörten und im Vergleich zur Kontrollgruppe signifikant bessere kardiovaskuläre Parameter („heart failure specific“ QOL, p < 0,001) im Verlauf zeigten [7].
Musik vor und nach kardiochirurgischen Eingriffen
Nilsson und Mitarbeiter berichteten bei 40 Patienten mit Bypassoperation oder Aortenklappenersatz über eine signifikant bessere Rate von Oxytocinausschüttung und Sauerstoffverbrauch unter Musik im Vergleich zur Kontrollgruppe (p < 0,05; [34]). In einer anderen ebenfalls von Nilsson publizierten Untersuchung an 58 Patienten, die sich einer Herzoperation unterzogen, war in der postoperativen Phase bei den mit Musik beschallten Patienten (30 min Musikexposition am 1. postoperativen Tag) der Kortisolspiegel signifikant niedriger (484,4 mmol/l) als in der Kontrollgruppe der Patienten, die keine Musik hörten (Kortisolspiegel 618,8 mmol/l; p < 0,02; [35]). Der Einfluss von Musik wurde auch bei der Abstoßung nach Herztransplantation untersucht, die unter einer Musik von Mozart wesentlich günstiger war; auch im Tiermodell wurden sehr positive Effekte hinsichtlich einer prolongierten Abstoßung beobachtet [30, 50].
Einfluss von Musik auf Angst und Stress
Angst und Stress werden bei kritisch kranken Patienten häufiger beobachtet [33, 39, 43]. Umbrello und Mitarbeitern fassten die Ergebnisse von 11 Studien zusammen (davon 10 RCT-Studien), die den Einfluss einer Musikintervention von 30 min (Spannbreite 15–60 min) bei 959 kritisch kranken Patienten hinsichtlich einer Beeinflussung von Angst und Stress auf einer Intensivstation im Vergleich zu einer Kontrollgruppe ohne Musik untersuchten [51]. Die Analyse der Daten zeigte, dass die Musikapplikation mit einer signifikanten Verringerung der Parameter Angst und Stress verbunden war. Auch in einer Analyse von Chlan und Mitarbeitern an 373 Patienten (12 Intensivstationen an 5 Kliniken), die bei Ateminsuffizienz akut beatmet werden mussten, wurde unter einer Musikbeschallung eine signifikante Verbesserung der Angstindizes beobachtet [8]. Effekte von Musik wurden auch im Bereich der postoperativen Intensivmedizin in einer Auswertung von 73 Studien mit 20–458 Patienten pro Studie von Hole et al. gezeigt [18]. Musik reduzierte postoperativ signifikant Angst und Schmerzen bei identischen Verweildauern zwischen Musik- und Nichtmusikgruppen. Die Ergebnisse zeigten, dass Auswahl und Zeitpunkt der Musikapplikation keine wesentliche Rolle spielte und dass die Effekte auch unter Vollnarkose nachzuweisen waren. Insofern stimmen die Ergebnisse der Analysen von Umbrello und Hole sehr überein [18, 51]. Es ist interessant, dass Brinkmann und Mitarbeiter bereits 2009 auf den günstigen Effekt von Musik auf Angstindizes im Vergleich zu einer Medikation mit Midazolam (0,05–0,1 mg/kg) vor chirurgischen Eingriffen bei 372 Patienten anhand des STAI-X-1-Angst-Scores hingewiesen hatten [5]. Musik (177 Patienten) führte vor und nach der Operation zu einer signifikanten Verbesserung der Angstscores durch Musik im Vergleich zu Patienten, die Midazolam erhielten (195 Patienten; vor Operation: Score 34 vs. 36, nach Operation: Score 30 vs. 34; p < 0,001). Musik beeinflusst ebenfalls Ängste signifikant besser im Vergleich zu einer Kontrollgruppe bei Entwöhnung von mechanischer Beatmung, wie eine Untersuchung von Hunter und Mitarbeitern bei 61 Patienten zeigen konnte [20].
Kortisol, Stress und Musik
Es ist unstrittig, dass Kortisol als akuter Biomarker für Stress angesehen werden kann [40]. In einigen Studien über die Wirkung von Musik und Stress wurde Kortisol als „Stressparameter“ herangezogen. Auch in den beiden von uns durchgeführten prospektiv-randomisierten Studien wurde vor und nach der Musikbeschallung der Kortisolspiegel aus dem Blut bestimmt [46, 47]. Wir konnten nachweisen, das bei Männern die Musik von Mozart und Strauss jun. zu signifikanten Senkungen des Kortisolspiegels führte (Tab. 2). Unter Mozart sank der Kortisolspiegel im Mittel um 6,42 µg/dl (p < 0,001), bei Strauss jun. um 5,25 µg/dl (p < 0,001). Bei ABBA fiel der Kortisolspiegel um 4,63 µg/dl (p < 0,001) und unter Ruhebedingungen (Kontrollgruppe) im Mittel um 3,13 µg/dl (p < 0,001; Tab. 2). Bei Frauen führte die Musik von Mozart und Strauss jun. ebenfalls zu signifikanten Senkungen des Kortisolspiegels (Tab. 3). Unter Mozart sank der Kortisolspiegel im Mittel um 2,28 µg/dl (p < 0,001), bei Strauss um 3,45 µg/dl (p < 0,001). Bei ABBA fiel der Kortisolspiegel im Mittel um 3,29 µg/dl ab (p = 0,001) und unter Ruhebedingungen (Kontrollgruppe) um 1,78 µg/dl (p = 0,003; Tab. 3). Bei jüngeren Probanden (Alter <50 Jahre) sank unter der Musik von Mozart der Kortisolspiegel im Mittel um 5,9 µg/dl (p < 0,001), bei Strauss jun. um 4,6 µg/dl (p < 0,001). Bei ABBA fiel der Kortisolspiegel um 3,61 µg/dl (p < 0,001) und unter Ruhebedingungen (Kontrollgruppe) um 2,7 µg/dl (p < 0,001; Tab. 4). Bei Probanden mit einem Alter ≥50 Jahre führte die Musik von Mozart und Strauss jun. ebenfalls zu signifikanten Senkungen des Kortisolspiegels. Unter Mozart sank der Kortisolspiegel im Mittel um 4,3 µg/dl (p < 0,001), bei Strauss jun. um 4,4 µg/dl (p < 0,001). Bei ABBA fiel der Kortisolspiegel um 3,27 µg/dl (p < 0,001) und unter Ruhebedingungen (Kontrollgruppe) im Mittel um 2,66 µg/dl (p < 0,001; Tab. 5). Ähnliche Beobachtungen, dass Musiktherapie zu einer signifikanten Senkung des Kortisolspiegels als „Stressmarker“ führte, wurden auch von anderen Autoren gemacht [13, 31, 44].
| Berechnungen zum Kortisolspiegel – Männer | ||||
|---|---|---|---|---|
| Mozart | Strauss | ABBA | Ruhe | |
| Ausgangswert (Median, Min/Max) |
17,65 µg/dl (6,33/33,3 µg/dl) |
14,85 µg/dl (6,62/26,1 µg/dl) |
||
|
Differenz nach – vor Beschallung (µg/dl) (Median, Min/Max) |
−6,42 (−13,2/6,42) |
−5,25 (−14,7/1,14) |
−4,63 (−13,6/4) |
−3,13 (−8,9/3,5) |
| 95 %-Konfidenzintervall für Median | [−7; −4,5] | [−7,83; −3,6] | [−6,5; −2,9] | [−4,4; −1,2] |
|
p-Wert für Vergleich Nach vs. vor Beschallung a |
<0,001 | <0,001 | <0,001 | <0,001 |
|
p-Wert für Vergleich Musik vs. Ruhe b |
0,012 | 0,010 | 0,124 | – |
a Wilcoxon-Vorzeichen-Rang-Test
b Mann-Whitney-U-Test
| Berechnungen zum Kortisolspiegel – Frauen | ||||
|---|---|---|---|---|
| Mozart | Strauss | ABBA | Ruhe | |
| Ausgangswert (Median, Min/Max) |
13,2 µg/dl (5,53/26,2 µg/dl) |
13,35 µg/dl (6,17/31 µg/dl) |
||
|
p-Wert des Vergleichs des Ausgangswerts Frauen vs. Männer b |
0,084 | 0,191 | ||
|
Differenz nach – vor Beschallung (µg/dl) (Median, Min/Max) |
−2,28 (−15,48/7) |
−3,45 (−14,4/4,7) |
−3,29 (−15,7/10,4) |
−1,78 (−12,9/4,91) |
| 95 %-Konfidenzintervall für Median | [−4,52; −1,59] | [−5; −1,55] | [−4,4; −0,73] | [−2,9; −0,72] |
|
p-Wert für Vergleich Nach vs. vor Beschallung a |
<0,001 | <0,001 | 0,001 | 0,003 |
|
p-Wert für Vergleich Musik vs. Ruhe b |
0,145 | 0,084 | 0,228 | – |
|
p-Wert des Vergleich der Differenz Frauen vs. Männer b |
0,065 | 0,058 | 0,387 | 0,191 |
a Wilcoxon-Vorzeichen-Rang-Test,
b Mann-Whitney-U-Test
| Berechnungen zum Kortisolspiegel – <50 Jahre | ||||
|---|---|---|---|---|
| Mozart | Strauss | ABBA | Ruhe | |
| Ausgangswert (Median, Min/Max) |
16,7 µg/dl (5,53/31,1 µg/dl) |
14,6 µg/dl (7,57/31 µg/dl) |
||
|
Differenz nach – vor Beschallung (µg/dl) (Median, Min/Max) |
−5,9 (−14,1/7) |
−4,6 (−14,7/4,7) |
−3,61 (−15,7/10,4) |
−2,7 (−12,9/4,9) |
| 95 %-Konfidenzintervall für Median | [−7; −1,52] | [−6; −1,3] | [−5,7; −2,24] | [−3,93; −0,44] |
|
p-Wert für Vergleich Nach vs. vor Beschallung a |
<0,001 | <0,001 | <0,001 | <0,001 |
|
p-Wert für Vergleich Musik vs. Ruhe b |
0,025 | 0,097 | 0,073 | – |
a Wilcoxon-Vorzeichen-Rang-Test
b Mann-Whitney-U-Test
| Berechnungen zum Kortisolspiegel – ≥50 Jahre | ||||
|---|---|---|---|---|
| Mozart | Strauss | ABBA | Ruhe | |
| Ausgangswert (Median, Min/Max) |
15,2 µg/dl (6,33/33,3 µg/dl) |
13,8 µg/dl (6,17/26,1 µg/dl) | ||
|
p-Wert des Vergleichs des Ausgangswerts <50 Jahre vs. ≥50 Jahre b |
0,994 | 0,574 | ||
|
Differenz nach – vor Beschallung (µg/dl) (Median, Min/Max) |
−4,3 (−15,48/1,3) |
−4,4 (−12,2/0,1) |
−3,27 (−15,19/4) |
−2,66 (−8,9/4,91) |
| 95 %-Konfidenzintervall für Median | [−6,5; −1,74] | [−5,82; −2,65] | [−6,89; −0,4] | [−3,68; −0,99] |
|
p-Wert für Vergleich Nach vs. vor Beschallung a |
<0,001 | <0,001 | <0,001 | <0,001 |
|
p-Wert für Vergleich Musik vs. Ruhe b |
0,105 | 0,011 | 0,248 | – |
|
p-Wert des Vergleichs der Differenz <50 Jahre vs. ≥50 Jahre b |
0,605 | 0,638 | 0,625 | 0,912 |
a Wilcoxon-Vorzeichen-Rang-Test
b Mann-Whitney-U-Test
Beeinflussung von Schmerzen durch Musik
Schmerz und Stress sind vielfach von Angst begleitet, sodass diese Trias beim kritisch kranken Patienten in der Intensivmedizin eine wesentliche Rolle spielt [6, 11, 43]. In einer kürzlich vorgestellten Untersuchung an 59 Patienten, die sich einer HNO-Operation unterziehen mussten, wurden 29 Patienten additiv mit einer Musikbeschallung (2-mal 30 min täglich) behandelt [14]. Das Schmerzempfinden war in der Musikgruppe signifikant geringer. In einer von Fallek und Mitarbeiter vorgestellten Studie konnte eine Verringerung von Schmerzen durch Musik ebenfalls an 150 Patienten bestätigt werden [9]. Auch bei gynäkologischen Patientinnen, die sich einer Operation unterzogen, wurde in einer umfangreichen Reviewanalyse der positive Effekt von Musik auf das Schmerzempfinden nachgewiesen [41].
Bedeutung von Musik bei Delir
Delirante Zustände sind bei Intensivpatienten nicht selten und können durch direkte (z. B. nach Schädel-Hirn-Trauma, Reanimation mit hypoxischer Schädigung, Alkoholentzug) oder durch indirekte zerebrale Schädigung (u. a. Sepsis, Hypoxie, Hyperkapnie, schwere Herzinsuffizienz, schwere Anämie, Organversagen von Leber oder Niere, endokrine Dysfunktionen) verursacht werden, wenngleich die multifaktorielle Ätiologie des Delirs noch nicht vollständig geklärt ist. Therapeutisch stehen vor allem Frühmobilisation, Reorientierung, adäquate Schmerztherapie und die Vermeidung einer Polypharmazie im Mittelpunkt [53]. Khan und Mitarbeiter wiesen kürzlich bei 117 Patienten, die auf einer Intensivstation wegen Delir behandelt wurden, in einer kontrollierten randomisierten Studie nach, dass eine Musikbeschallung über eine Stunde 2‑mal täglich zu einer signifikanten Steigerung von delirfreien Tagen führte [23]. Ähnlich positive Effekte bei Delirpatienten durch Musikbeschallung wurden auch in anderen prospektiv-kontrollierten Studien nachgewiesen [22, 24].
Sind die Effekte einer musikmedizinischen Intervention von Alter und Geschlecht abhängig?
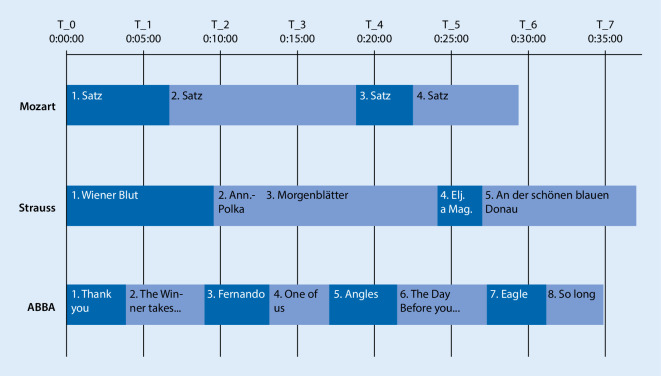
Obgleich mittlerweile viele Studien positive Effekte einer Musikbeschallung in unterschiedlichen Fachdisziplinen beschrieben haben, ist unklar, ob die Effekte der Musik von Alter und Geschlecht abhängig sind oder nicht [49]. In einer eigenen prospektiv-randomisierten kontrollierten Studie wurden 120 Probanden eingeschlossen, von denen 60 Probanden der Studiengruppe mit Musikhören und 60 Probanden einer Kontrollgruppe ohne Musikhören („Ruhe“) zugeführt wurden. Einschlusskriterien waren männliche oder weibliche Probanden zwischen 25 und 75 Jahre, die kardiologisch gesund sein mussten, d. h. keinerlei kardiale oder vaskuläre Erkrankungen haben oder gehabt haben und dementsprechend auch unter keiner medikamentösen Therapie standen. Der Blutdruck musste vor Studieneinschluss normal sein; Probanden mit bekannter labiler oder stabiler arterieller Hypertonie wurden von der Studie ausgeschlossen. Die Probanden wurden nach einem zufälligen Randomisierungsschema mit Musik von W.A. Mozart, J. Strauss jun. oder ABBA beschallt (Abb. 2). 60 Probanden, 30 Männer, 30 Frauen, 30 Probanden <50 Jahre, 30 Probanden ≥50 Jahre hörten 25 min lang verschiedene Musikwerke von Mozart, Strauss jun. und ABBA. Blutdruck, Herzfrequenz und Kortisolspiegel wurden vor und nach dem Musikhören bestimmt. Bei einer Kontrollgruppe von 60 Probanden mit identischen demographischen Daten, die keine Musik hörten, wurden die Parameter ebenfalls gemessen. Das Musikhören startete an jedem der 3 Messtage um 10.00 Uhr. Die Probanden trugen die Langzeitgeräte über die Zeit des Musikhörens hinaus bis zum Mittag (13.00 Uhr). Dadurch konnten bis 13.00 Uhr kontinuierliche EKG-Aufzeichnungen registriert werden. Auf weitere Registrierungen (z. B. über 24 h) wurde bewusst verzichtet, da der Tagesablauf der Probanden einen möglicherweise zu großen Einfluss gehabt hätte. Die Registrierungen von Blutdruck und Herzfrequenz erfolgten vor Beginn der Studie mit einem Ausgangswert (T0). Der Ausgangswert wurde unmittelbar vor Beginn der Musikbeschallung gemessen, gefolgt von 5‑minütigen Messungen (T1–T7). Als Endwert bzw. Vergleichswert am Ende des Klangszenarios wurde der letzte Wert vor Ende des Musikhörens verwendet. Als Vergleichswert für die Differenz zwischen dem Blutdruck vor und nach der Beschallung/Ruhe galt also die Differenz der Werte T0–T5, d. h. der Blutdruck circa 25 min nach Beginn. Es wurde bewusst Wert gelegt auf den Vergleich zweier Messwerte zu Beginn und zum Ende des Musikhörens. Dies galt auch für Messungen der Herzfrequenz. Das Musikhören erfolgte über Stereokopfhörer der Fa. Philips mittels eines MP3-Players (Odays S‑8 2 GB, S‑15, Fa. Odys). Die Lautstärke der Musik war bei allen Probanden mit 60 db festgelegt und nicht variierbar. Wir konnten in der Studie nachweisen, dass die Musik von Mozart und Strauss jun. bei Männern und Frauen zu einer deutlichen Senkung des systolischen und diastolischen Blutdrucks führte (Mozart: Männer RRsyst −4,5 mm Hg, RRdiast −2,5 mm Hg; Frauen: RRsyst −5 mm Hg, RRdiast −1,5 mm Hg; Strauss jun.: Männer RRsyst −4,5 mm Hg, RRdiast −4 mm Hg; Frauen: RRsyst −2 mm Hg, RRdiast 0 mm Hg), während bei ABBA diese Effekte nicht zu sehen waren (Mozart: Männer RRsyst −2 mm Hg, RRdiast −1 mm Hg; Frauen: RRsyst 0 mm Hg, RRdiast 0 mm Hg). Auch die Herzfrequenz fiel unter der Musik von Mozart und Strauss jun. mehr ab (Mozart: Männer HF −5/min, Frauen: HF −2/min; Strauss jun.: Männer HF −3/min; Frauen: HF −1,5/min mm Hg), wohingegen der Effekt bei der Musik von ABBA nicht so ausgeprägt war (Männer HF −1/min, Frauen HF −3/min). Die Unterschiede zwischen Männern und Frauen waren nicht signifikant [49]. Auch im Vergleich der Musikeffekte auf Blutdruck und Herzfrequenz gab es zwischen jüngeren und älteren Probanden keine signifikanten Unterschiede, sodass nach unseren Ergebnissen die Wirkungen von Musik alters- und geschlechtsunabhängig sind, zumindest bezogen auf die Beeinflussung von Blutdruck und Herzfrequenz.
Schlussfolgerungen
Nach vorliegenden Berichten und kürzlich publizierten prospektiv-randomisierten Studien ist ein positiver Effekt von Musik in vielen Fachdisziplinen der Medizin und auch in der Intensivmedizin beobachtet worden [4, 15]. Auch bei postoperativen Patienten, ob aus der Viszeralchirurgie, der Herzchirurgie, der Orthopädie und der Frauenheilkunde, um exemplarisch nur einige zu nennen, wurden positive Wirkungen von Musik bei kritisch Kranken hinsichtlich der Parameter Schmerz, Stress und Angst nachgewiesen [17, 25]. Trotz vorliegender randomisierter Studien bleiben im klinischen Alltag noch viele Fragen offen. Es wäre daher wünschenswert, wenn die Forschung – sowohl in den Grundlagenfächern als auch klinisch – sich des Themas annehmen und Wissenslücken schließen würde.
Einhaltung ethischer Richtlinien
Interessenkonflikt
H.-J. Trappe gibt an, dass kein Interessenkonflikt besteht.
Für diesen Beitrag wurden von den Autoren keine Studien an Menschen oder Tieren durchgeführt. Für die aufgeführten Studien gelten die jeweils dort angegebenen ethischen Richtlinien.
Literatur
- 1.Bernardi L, Porta C, Casucci G, Balsamo R, Bernardi NF, Fogari R, Sleight P. Dynamic interactions between musical, cardiovascular, and cerebral rhythms in humans. Circulation. 2009;119:3171–3180. doi: 10.1161/circulationaha.108.806174. [DOI] [PubMed] [Google Scholar]
- 2.Bernatzky G. Das „Musikament“. Arzt Prax. 2013;994:112–114. [Google Scholar]
- 3.Bernatzy G, Hesse HP. Musik in der Palliativmedizin. In: Bernatzky G, Likar R, Sittl R, editors. Schmerzbehandlung in der Palliativmedizin. Heidelberg: Springer; 2013. pp. 175–179. [Google Scholar]
- 4.Bradt J, Dileo C. Music interventions for mechanically ventilated patients. Cochrane Database Syst Rev. 2014;12:CD006902. doi: 10.1002/14651858.CD006902.pub.3. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 5.Bringman H, Giesecke K, Thörne A, Bringman S. Relaxing music as pre-medication before surgery: a randomised controlled trial. Acta Anaesthesiol Scand. 2009;53:759–764. doi: 10.1111/j.1399-6576.2009.01969.x. [DOI] [PubMed] [Google Scholar]
- 6.Bojorquez GR, Jackson KE, Andrews AK. Music therapy for surgical patients: approach for managing pain and anxiety. Crit Care Nurs Q. 2020;43:81–85. doi: 10.1097/CNQ.0000000000000294. [DOI] [PubMed] [Google Scholar]
- 7.Burrai F, Sanna GD, Moccia E, et al. Beneficial effects of listening to classical music in patients with heart failure: a randomized controll trial. J Card Fail. 2019 doi: 10.1016/j.cardfail.2019.12.005. [DOI] [PubMed] [Google Scholar]
- 8.Chlan LL, Weinert CR, Heiderscheit A, et al. Effects of patient-directed music intervention on anxiety and sedative exposure in critically ill patients receiving mechanical ventilatory support: a randomized clinical trial. JAMA. 2013;309:2335–2344. doi: 10.1001/jama.2013.5670. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 9.Fallek R, Corey K, Qamar A, et al. Soothing the heart with music: a feasibility study of a bedside music therapy intervention for critically ill patients in an urban hospital setting. Palliat Support Care. 2020;18:47–54. doi: 10.1017/S1478951519000294. [DOI] [PubMed] [Google Scholar]
- 10.Fernandez NB, Trost WJ, Vuilleumier P. Brain networks mediating the influence of background music on selective attention. Soc Cogn Affect Neurosci. 2019;14:1441–1452. doi: 10.1093/scan/nsaa004. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 11.Fernando GVMC, Wanigabadu LU, Vidanagama B, et al. Adjunctive effects of a short session of music on pain, low-mood and anxiety modulation among cancer patients—a randomized crossover clinical trial. Indian J Palliat Care. 2019;25:367–373. doi: 10.4103/IJPC.IJPC_22_19. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 12.Flink IK, Reme S, Jacobsen HB, et al. Pain psychology in the 21st century: lessons learned and moving forward. Scand J Pain. 2020 doi: 10.1515/sjpain-2019-0180. [DOI] [PubMed] [Google Scholar]
- 13.Fu VX, Oomens P, Sneiders D, et al. The effect of perioperative music on the stress response to surgery: a meta-analysis. J Surg Res. 2019;244:444–455. doi: 10.1016/j.jss.2019.06.052. [DOI] [PubMed] [Google Scholar]
- 14.Gogourlaradja A, Bakshi SS. A randomized study on the efficacy of music therapy on pain and anxiety in nasal septal surgery. Int Arch Otorhinolaryngol. 2020;24:e232–e236. doi: 10.1055/s-0039-3402438. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 15.Golino AJ, Leone R, Gollenberg A, et al. Impact of an active music therapy intervention on intensive care patients. Am J Crit Care. 2019;28:48–55. doi: 10.4037/ajcc2019792. [DOI] [PubMed] [Google Scholar]
- 16.Gruhlke LC, Patricio MC, Moreira DM. Mozart, but not the Beatles, reduces systolic blood pressure in patients with myocardial infarction. Acta Cardiol. 2015;70:703–706. doi: 10.2143/AC.70.6.3120183. [DOI] [PubMed] [Google Scholar]
- 17.Haslbeck FB, Jakab A, Held U, et al. Creative music therapy to promote brain function and brain structure in preterm infants: a randomized controlled pilot study. Neuroimage Clin. 2020;25:102171. doi: 10.1016/j.nicl.2020.102171. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 18.Hole J, Hirsch M, Ball E, Meads C. Music as an aid for postoperative recovery in adults: a systematic review and meta-analysis. Lancet. 2015;386:1659–1671. doi: 10.1016/S0140-6736(15)60169-6. [DOI] [PubMed] [Google Scholar]
- 19.Hughes JR, Fino JJ. The Mozart effect: distinctive aspects of the music-—a clue to brain coding? Clin Electroencephalogr. 2000;31:94–103. doi: 10.1177/155005940003100208. [DOI] [PubMed] [Google Scholar]
- 20.Hunter BC, Oliva R, Sahler OJ, et al. Music therapy as an adjunctive treatment in the management of stress for patients being weaned from mechanical ventilation. J Music Ther. 2010;47:198–219. doi: 10.1093/jmt/47.3.198. [DOI] [PubMed] [Google Scholar]
- 21.Jähncke L. Musik und Hirnplastizität. In: Bernatzky G, Kreutz G, editors. Musik und Medizin. Heidelberg: Springer; 2015. pp. 49–67. [Google Scholar]
- 22.Johnson K, Fleury J, McClain D. Music intervention to prevent delirium among older patients admitted to a trauma intensive care unit and a trauma orthopedic unit. Intensive Crit Care Nurs. 2018;47:7–14. doi: 10.1016/j.iccn.2018.03.007. [DOI] [PubMed] [Google Scholar]
- 23.Khan SH, Xu C, Purpura R, et al. Decreasing delirium through music: a randomized pilot trial. Am J Crit Care. 2020;29:e31–e38. doi: 10.4037/ajcc2020175. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 24.Khan SH, Wang S, Harrawood A, et al. Decreasing delirium through music (DDM) in critically ill, mechanically ventilated patients in the intensive care unit: study protocol for a pilot randomized controlled trial. Trials. 2017;18:574. doi: 10.1186/s13063-017-2324-6. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 25.Khan SH, Kitsis M, Golovyan D, et al. Effects of music intervention on inflammatory markers in critically ill and post-operative patients: a systematic review of the literature. Heart Lung. 2018;47:489–496. doi: 10.1016/j.hrtlng.2018.05.015. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 26.Koelsch S. Brain correlates of music-evoked emotions. Nat Rev Neurosci. 2014;15:170–180. doi: 10.1038/nrn3666. [DOI] [PubMed] [Google Scholar]
- 27.Kreutz G, Bernatzky G. Musik und Wohlbefinden – ein dynamisch wachsendes Forschungsgebiet. In: Bernatzky G, Kreutz G, editors. Musik und Medizin. Heidelberg: Springer; 2015. pp. 7–16. [Google Scholar]
- 28.Kühlmann AYR, de Rooij A, Kroese LF, van Dijk M, Hunink MGM, Jeekel J. Meta-analysis evaluating music interventions for anxiety and pain in surgery. Br J Surg. 2018;105:773–783. doi: 10.1002/bjs.10853. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 29.Lemmer B. Effects of music composed by Mozart and Ligeti on blood pressure and heart rate circadian rhythms in normotensive and hypertensive rats. Chronobiol Int. 2008;25:971–986. doi: 10.1080/07420520802539415. [DOI] [PubMed] [Google Scholar]
- 30.Liao P. Mozart may prevent heart transplant rejection: discovery wins Harvard University’s Ig Nobel 2013 prize in medicine. Natl Med J India. 2013;26:381. [PubMed] [Google Scholar]
- 31.Luis M, Doss R, Zaved B, Yacoub M. Effect of live oud music on physiological and psychological parameters in patients undergoing cardiac surgery. Glob Cardiol Sci Pract. 2019;19:e201917. doi: 10.21542/gcsp.2019.17. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 32.Menon V, Levitin DJ. The rewards of music listening: response and physiological connectivity of the mesolimbic system. Neuroimage. 2005;28:175–184. doi: 10.1016/j.neuroimage.2005.05.053. [DOI] [PubMed] [Google Scholar]
- 33.Mofredi A, Alaya S, Tassaioust K, et al. Music therapy, a review of the potential therapeutic benefits for the critically ill. J Crit Care. 2016;35:195–199. doi: 10.1016/j.jcrc.2016.05.021. [DOI] [PubMed] [Google Scholar]
- 34.Nilsson U. The effect of music intervention in stress response to cardiac surgery in a randomized clinical trial. Heart Lung. 2009;38:201–207. doi: 10.1016/j.hrtlng.2008.07.008. [DOI] [PubMed] [Google Scholar]
- 35.Nilsson U. Soothing music can increase oxytocin levels during bed rest after open-heart surgery: a randomized control trial. J Clin Nurs. 2009;18:2153–2161. doi: 10.1111/j.1365-2702.2008.02718.x. [DOI] [PubMed] [Google Scholar]
- 36.Pallesen KJ, Brattico E, Bailey CJ, Korvenoja A, Gjedde A. Cognitive and emotional modulation of brain default operation. J Cogn Neurosci. 2008;21:1065–1080. doi: 10.1162/jocn.2009.21086. [DOI] [PubMed] [Google Scholar]
- 37.Peh WY, Roberts TF, Mooney R. Imaging auditory representations of song ans syllables in populations of sensorimotor neurons essential to vocal communication. J Neurosci. 2015;35:5589–5605. doi: 10.1523/JNEUROSCI.2308-14.2015. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 38.Phua J, Wenig L, Ling L, et al. Intensive care management of coronavirus disease 2019 (COVID-19): challanges and recommendations. Lancet Respir Med. 2020 doi: 10.1016/S2213-2600(20)30161-2. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 39.Ribeiro MKA, Alcantara-Silva TRM, Oliveira JCM, et al. Music therapy intervention in cardiac autonomic modulation, anxiety, and depression in mothers of preterms: a randomized controlled trial. BMC Psychol. 2018;6(1):57. doi: 10.1186/s40359-018-0271-y. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 40.Russ KA, Holochwost SJ, Perkins SM, et al. Cortisol as an acute stress biomarker in young hematopoietic cell transplant patients/caregivers: active music engagement protocol. J Altern Complement Med. 2020 doi: 10.1089/acm.2019.0413. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 41.Sin WM, Chow KM. Effect of music therapy on postoperative pain management in gynecological patients: a literature review. Pain Manag Nurs. 2015;16:978–987. doi: 10.1016/j.pmn.2015.06.008. [DOI] [PubMed] [Google Scholar]
- 42.Spahn C, Bernatzky G, Kreutz G. Musik und Medizin – ein Überblick. In: Bernatzky G, Kreutz G, editors. Musik und Medizin. Heidelberg: Springer; 2015. pp. 17–24. [Google Scholar]
- 43.Spintge R. Musikmedizinische Interventionen in der klinischen Medizin bei Schmerz, Angst und Stress. In: Bernatzky G, Kreutz G, editors. Musik und Medizin. Heidelberg: Springer; 2015. pp. 71–83. [Google Scholar]
- 44.Taets GGC, Jomar RT, Abreu AMM, Capella MAM. Effect of music therapy on stress in chemically dependent people: a quasi-experimental study. Rev Lat Am Enfermagem. 2019;27:e3115. doi: 10.1590/1518-8345.2456.3115. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 45.Trappe HJ. Musik als Therapie in der Intensivmedizin: Sinn oder Unsinn? 2020. [Google Scholar]
- 46.Trappe HJ, Breker IM. Effects of different styles of music on human cardiovascular response: a prospective controlled trial. Music Med. 2016;8:8–16. [Google Scholar]
- 47.Trappe HJ, Voit G. The cardiovascular effect of musical genres—a randomized controlled study on the effect of compositions by W.A. Mozart, J. Strauss, and ABBA. Dtsch Arztebl Int. 2016;113:347–352. doi: 10.3238/arztebl.2016.0347. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 48.Trappe HJ. Role of music in intensive care medicine. Int J Crit Illn Inj Sci. 2012;2:27–31. doi: 10.4103/2229-5151.94893. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 49.Trappe HJ. Einfluß von Musik auf Blutdruck und Herzfrequenz. Spielen Geschlecht und Alter dabei eine Rolle? Musik Tanz Kunstther. 2019;29:191–206. [Google Scholar]
- 50.Uchiyama M, Jin X, Zhang Q, Amano A, Watanabe T, Niimi M. Music exposure induced prolongation of cardiac allograft survival and generated regulatory CD4+ cells in mice. Transplant Proc. 2012;44:1076–1079. doi: 10.1016/j.transproceed.2012.02.008. [DOI] [PubMed] [Google Scholar]
- 51.Umbrello M, Sorrenti T, Mistraletti G, Formenti P, Chiumello D, Terzoni S. Music therapy reduces stress and anxiety in critically ill patients: a systematic review of randomized clinical trials. Minerva Anestesiol. 2019;85:886–898. doi: 10.23736/S0375-9393.19.13526-2. [DOI] [PubMed] [Google Scholar]
- 52.Willich SN. The center cannot hold: medicine, music, and the mind. JAMA. 2017;317:1822–1823. doi: 10.1001/jama.2017.4690. [DOI] [PubMed] [Google Scholar]
- 53.Zoremba N. Delir im Krankenhaus. Dtsch Arztebl Int. 2019;116:101–106. doi: 10.3238/arztebl.2019.0101. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 54.Zyromski NJ. Music, medicine, and mind. Am J Surg. 2020;219:386–389. doi: 10.1016/j.amjsurg.2019.11.036. [DOI] [PubMed] [Google Scholar]