Abstract
Respiratorische Komplikationen wie z. B. Belüftungsstörungen, Sekretverhalt und Störungen des Gasaustausches sind bei kritisch kranken Patienten häufig, können jedoch oft mit einfachen Verfahren der Atemtherapie behandelt und/oder verhindert werden. Hierzu gehören Atemgaskonditionierung, O2-Therapie, Inhalationstherapie und physikalische Maßnahmen. Die meisten dieser Maßnahmen können eigenständig von geschultem Intensivpflegepersonal durchgeführt werden.
Respiratorische Komplikationen wie z. B. Belüftungsstörungen, Sekretverhalt und Störungen des Gasaustausches sind bei kritisch kranken Patienten häufig, können jedoch oft mit einfachen Verfahren der Atemtherapie behandelt und/oder verhindert werden. Hierzu gehören Atemgaskonditionierung, O2-Therapie, Inhalationstherapie und physikalische Maßnahmen. Die meisten dieser Maßnahmen können eigenständig von geschultem Intensivpflegepersonal durchgeführt werden.
Physiologische Atemwegsclearance
Mukoziliäre Clearance
In der Mukosa des Respirationstraktes wird fortwährend visköses Sekret (Mukus ) gebildet. Das Sekret nimmt Fremdpartikel, Bakterien und körpereigene Zellteile auf und entfernt sie aus den Atemwegen. Der Transport des Schleims erfolgt wie auf einer Rolltreppe durch Zilienbewegungen. Die Zilien oder Flimmerhärchen schlagen mit einer Frequenz von ca. 8–15 Hz ständig in Richtung Pharynx; hierdurch wird der Mukus mit den aufliegenden Partikeln in die größeren Bronchien und von dort in die oberen Atemwege befördert. Die Funktion der mukoziliären Clearance wird von der Zusammensetzung des Mukus, der Schlagfrequenz der Zilien und der Tiefe der die Zilien umgebenden wässrigen Solschicht beeinflusst. Reduzierte Temperatur und verminderte Feuchte der Atemgase, hohe O2-Konzentrationen und aggressive Beatmungsmuster können die Transportkapazität der Zilien beeinträchtigen.
Hustenclearance
Der Hustenakt beginnt mit einer tiefen Inspiration, die Glottis wird verschlossen und der intrathorakale Druck durch die kontrahierte Bauchmuskulatur drastisch erhöht. Bei der schlagartigen Öffnung der Glottis entsteht so ein zentral gerichteter Gasfluss, der durch die Reduktion des Bronchialdurchmessers (Vorstülpen der Pars membranacea) noch verstärkt wird.
Auswirkungen der endotrachealen Intubation oder Kanülierung
Die Umgehung der oberen Atemwege durch einen künstlichen Atemweg ( Endotrachealtubus oder Trachealkanüle) schaltet den oberen Respirationstrakt funktionell aus. Damit entfallen die Reinigungs-, Befeuchtungs- und Erwärmungsfunktionen der oberen Atemwege. Außerdem bildet der Endotrachealtubus oder die Trachealkanüle eine Barriere für das bereits in die Trachea transportierte Sekret. Zusätzlich beeinträchtigen Analgosedierung, Immobilisierung des Patienten und der künstliche Atemweg die Hustenfunktion. Folgen können sein:
Abnahme der Zilienbeweglichkeit,
Sekretretention, Gefahr der Tubusobstruktion,
Zunahme des Atemwegswiderstandes,
Zunahme der Atemarbeit,
Atelektasenbildung,
Beeinträchtigung des Gasaustausches,
Infektion.
Beim allen intubierten oder tracheotomierten Intensivpatienten muss das Atemgas künstlich angefeuchtet und erwärmt werden.
Atemgaskonditionierung
Unter physiologischen Bedingungen wird das inhalierte Atemgas vorwiegend in den oberen Atemwegen erwärmt und befeuchtet. Dieser Vorgang setzt sich in der Trachea bis auf die Höhe der Luftröhrengabelung fort. Dort werden bei normaler Körperkerntemperatur 100% relative Feuchte erreicht (44 mgH2O pro Liter Atemluft bei 37°C Körpertemperatur).
Absolute Feuchte
Die absolute Feuchte beschreibt den tatsachlichen Wassergehalt eines Gasgemisches, sie wird in mg/l Atemluft angegeben.
Relative Feuchte
Die relative Feuchte beschreibt den prozentualen Wasseranteil eines Gasgemisches bezogen auf den maximal möglichen Wassergehalt.
Aktive Atemgaskonditionierung
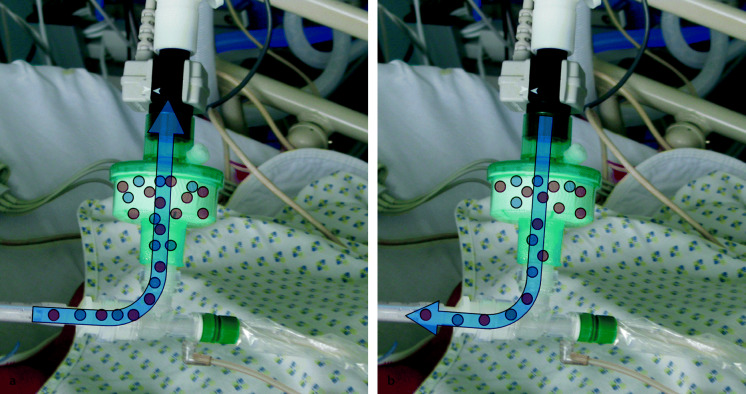
Bei aktiven Befeuchtungssystemen wird das Atemgas über eine erwärmte Wasseroberfläche geleitet. Dabei sättigt es sich mit Energie und Feuchte auf. Der Grad der Befeuchtungsleistung wird durch die Temperatureinstellung gesteuert. Diese ist in der Regel vorgegeben (z. B. Invasivmodus 37°C in der Befeuchterkammer, bis 40°C am Y-Stück), aber auch frei wählbar. Die Temperatur wird patientennah am Y-Stück gemessen, patientenfern am Ausgang der Befeuchterkammer oder nur in der Befeuchterkammer, wenn keine Schlauchheizung verwendet wird Beheizte Schlauchsysteme sind Standard. Sie verhindern den Temperatur- und Feuchteverlust zwischen Befeuchterkammer und Patient und damit auch die Bildung von hygienisch bedenklichem Kondensat. Beeinflusst werden können die aktiven Befeuchtungssystemen durch die Umgebungstemperatur, den Fluss durch den Befeuchter und die Gastemperatur am Auslass des Respirators (Abb. 54.1).

Praktisches Vorgehen
Der Wasserstand muss regelmäßig kontrolliert werden.
Nach Transporten, Inhalationstherapie oder Schlauchwechseln sollte man sich vergewissern, dass der Befeuchter wieder eingeschalten wurde.
Evtl. anfallendes Kondensat muss in Wasserfallen aufgefangen und nach hygienischen Richtlinien entsorgt werden.
Passive Atemgaskonditionierung
Bei passiven Befeuchtungssystemen, sog. HME („heat and moisture exchanger“ , Wärme- und Feuchteaustauscher, „feuchte Nase“) werden Feuchte und Wärme aus dem ausgeatmeten Atemgas des Patienten in einem speziell beschichteten (hygroskopischen, wasserspeichernden) HME-Element gespeichert und z. T. während der Inspirationsphase wieder eingeatmet. Um eine Kontamination von Schlauchsystem, Patient oder Umwelt mit pathogenen Keimen zu verhindern, sind HME zusätzlich mit elektrostatischen (geringerer Atemwegswiderstand) oder rein mechanischen Filtern (höherer Atemwegswiderstand) verfügbar (Abb. 54.2).
Praktische Hinweise
HME mit möglichst niedrigem Totraum (<50 ml) und Atemwegswiderstand (<2 cmH2O bei einem Flow von 60 l/min) sollten bevorzugt werden.
Die Befeuchtungsleistung sollte 30 mgH2O/l Atemluft nicht unterschreiten.
HME können nur dann ihre volle Leistung erbringen, wenn sie möglichst tubusnah platziert werden.
Kontraindikationen und Anwendungsbeschränkungen müssen beachtet werden.
Probleme der Atemgaskonditionierung
Hygiene
Lange Zeit wurde die aktive Atemgaskonditionierung als Mitverursacher für die respirator- bzw. tubusassoziierte Pneumonie angesehen.
Mittlerweile konnten aber zahlreiche Studien zeigen, dass die Art der Atemgaskonditionierung (aktiv/passiv) keinen Einfluss auf die Häufigkeit der beatmungsassoziierten Pneumonie hat.
Auch die Verwendung von Filtern und häufige Wechsel der Beatmungsschläuche zeigten keine solche Wirkung.
Mechanische Eigenschaften
Problematisch ist der Einsatz eines HME bei der lungenprotektiven Beatmung bzw. bei schwieriger Entwöhnung von der Beatmung. Hier können Totraum und erhöhter Atemwegswiderstand hohe CO2-Werte mit nachfolgender respiratorischer Azidose hervorrufen und so wiederum höhere Beatmungsdrücke, -volumina und -frequenzen erfordern. Unter Spontanatmung steigt die Atemarbeit gerade bei schwierigem Weaning signifikant an.
Atemgaskonditionierung und NIV
Durch die ständig vorhandenen Leckagen während der NIV wird die Leistung eines passiven Befeuchters deutlich reduziert, da ein Großteil der Ausatemluft nicht zum HME gelangt, dort also auch keine Feuchte und Wärme gespeichert werden kann. Des Weiteren beeinträchtigen Totraum und Widerstand die Effizienz der Beatmung.
Leistung
Beim Einsatz der unterschiedlichen Befeuchtungsmethoden ist die angegebene Befeuchtungsleistung zu beachten. So können aktive Befeuchter theoretisch Werte bis zur Vollsättigung erreichen, leistungsfähige HME dagegen maximal 32 mgH2O/l Atemluft. Eine reduzierte Befeuchtungsleistung kann aber gerade bei Hypersekretion, zähem oder blutigem Sekret zum Sekretverhalt oder zur Tubusobstruktion führen.
Klinische Bewertung der Atemgaskonditionierung
Mit der aktiven und passiven Atemgaskonditionierung stehen sich zwei Methoden gegenüber, die sich deutlich in Leistungsspektrum und Kosten unterscheiden (Tab. 54.1). Für die Praxis haben sich Algorithmen bewährt, bei denen beide Verfahren patientenbezogen eingesetzt werden (Abb. 54.3).
| Aktive Befeuchter | Passive Befeuchter |
|---|---|
| Nachteile | Nachteile |
| – Hohe Anschaffungskosten | – Hoher Totraum |
| – Netzabhängig | – Erhöhter Atemwegswiderstand |
| – Geringere Befeuchtungsleistung | |
| – Kontraindikationen | |
| Vorteile | Vorteile |
| – Keine Kontraindikationen | – Kostengünstig |
| – Hohe Befeuchtungsleistung | – Einfache Handhabung |
| – Mobil |
Sauerstofftherapie
Sauerstoff ist das am meisten verwendete „Medikament“ in der Intensivmedizin. Dabei wird oftmals vergessen, dass es auch hier auf eine exakte Dosierung ankommt, zumal v. a. zu hohe O2-Konzentrationen Schädigungen verschiedener Gewebe hervorrufen können.
Indikationen
Grundlegende Indikation für die Zufuhr von Sauerstoff sind Oxygenierungsstörungen der Lunge, erkennbar am Abfall des arteriellen pO2 (Hypoxie ) und nachfolgend der arteriellen O2-Sättigung. Ab welchem Grenzwert des paO2 Sauerstoff zugeführt werden sollte, lässt sich wegen der individuellen Hypoxietoleranz nicht genau festlegen; auch muss hierbei der Gesamtsauerstoffgehalt des Blutes berücksichtigt werden. Kritisch sind aber paO2-Werte von 55–65 mmHg, weil in diesem Bereich die O2-Bindungskurve sehr steil verläuft und daher die O2-Sättigung des Hämoglobins stark abnimmt. Bei normaler O2-Sättigung ist die zusätzliche O2-Gabe in der Regel ohne Nutzen und daher nicht indiziert.
In der Akut- und Intensivmedizin sollten O2-Sättigungswerte zwischen 94 und 98% angestrebt werden sofern keine chronischen Störungen bzw. Kontraindikationen vorliegen.
Methoden der Sauerstoffzufuhr
Grundsätzlich werden Low-flow- und High-flow-Applikatoren unterschieden (Abb. 54.4).

Low-flow-Systeme bieten nur einen geringen Gasfluss, der weit unter dem Inspirationsfluss des Patienten liegt. (z. B. 2 l/min). Zur Deckung des Gesamtflows muss demnach Umgebungsluft von außen beigemischt werden. Die effektive inspiratorische O2-Konzentration hängt vom Atemmuster, dem O2-Fluss und der Tiefe der Inspiration ab, und kann daher nicht sicher benannt werden. Bei High-flow-Systemen liegt der gelieferte Gasfluss nahe oder über dem Inspirationsfluss des Patienten. In dieser Situation wird also nur wenig oder keine Raumluft zusätzlich zum gelieferten Gasgemisch mit eingeatmet. Die effektive inspiratorische O2-Konzentration bleibt weitgehend konstant.
Sauerstoffsonden und Sauerstoffbrillen
Zu den am häufigsten eingesetzten Applikatoren gehören O2-Sonden und -Brillen (Abb. 54.5). Hier dient der Nasopharynx als Reservoir, in dem die mit Sauerstoff angereicherte Luft gespeichert wird. Üblicherweise werden Gasflüsse von 2–6 l/min verwendet. Von höheren Flussraten ist abzusehen, da es zu Schädigungen an der Schleimhaut kann. Während O2-Brillen nur ca. 1 cm in die Nase ragen, werden O2-Sonden im Pharynx platziert.

Sauerstoffmasken
Gebräuchlich sind einfache Sauerstoffmasken und Masken mit Nichrückatemventilen.
Einfache Sauerstoffmasken
Diese Masken vergrößern das Sauerstoffreservoir des Nasopharynx durch den Maskenkörper, in den der Sauerstoff eingeleitet wird. Die Inspiration und auch die Exspiration erfolgen durch Öffnungen im Maskenkörper. Eine Flussrate von 5 l/min sollte nicht unterschritten werden da es sonst zu einer CO2-Anreicherung im Maskenkörper kommen kann. Die effektive inspiratorische O2-Konzentration beträgt bei einfachen Masken zwischen 40 und 60%.
Sauerstoffmasken mit Nichtrückatmungsventilen
Diese Masken ermöglichen die Zufuhr höherer O2-Konzentrationen. Hierfür steht ein Reservoir zur Verfügung, in das der Sauerstoff kontinuierlich eingeleitet wird. Inspiration und Exspiration werden durch ein Ventilsystem getrennt (Abb. 54.6). Während der Inspiration öffnet sich das Ventil zum Reservoir, die Exspirationsventile im Maskenkörper bleiben geschlossen. In der Exspirationsphase entweicht die Luft durch die Ventile im Maskenkörper nach außen, während das Reservoir mit Frischgas gefüllt wird. Bei einer dicht sitzenden Maske können so O2-Konzentrationen von bis zu 90% erreicht werden.
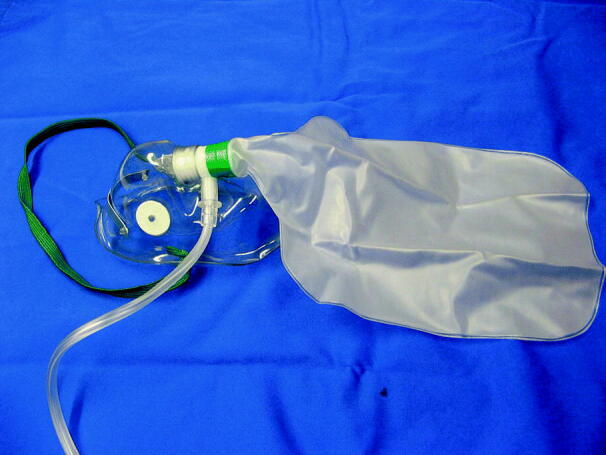
Bei Masken mit Nichtrückatemventilen muss der inspiratorische Gasfluss so hoch eingestellt werden, dass der Reservoirbeutel während der Inspirationsphase nicht kollabiert.
Masken nach dem Venturi-Prinzip
Die Venturi-Maske ermöglicht eine kontrollierte O2-Abgabe von 24, 28, 30, 35, 40, 50 oder 60%. Der Sauerstoff wird durch eine sich verjüngende Düse geleitet (Abb. 54.7). Durch den dabei entstehenden Unterdruck wird Umgebungsluft entsprechend der Größe der Öffnungen angesaugt und mit dem zugeführten Sauerstoff in einem festen Verhältnis gemischt. Wird der Flow durch die Düse erhöht, nimmt auch die angebotene Frischgasmenge entsprechend dem Mischverhältnis zu, jedoch nicht die inspiratorische O2-Konzentration. Venturi-Masken eignen sich speziell für Patienten, bei denen die Gefahr einer Hyperkapnie durch unkontrollierte O2-Gabe besteht (z. B. COPD).
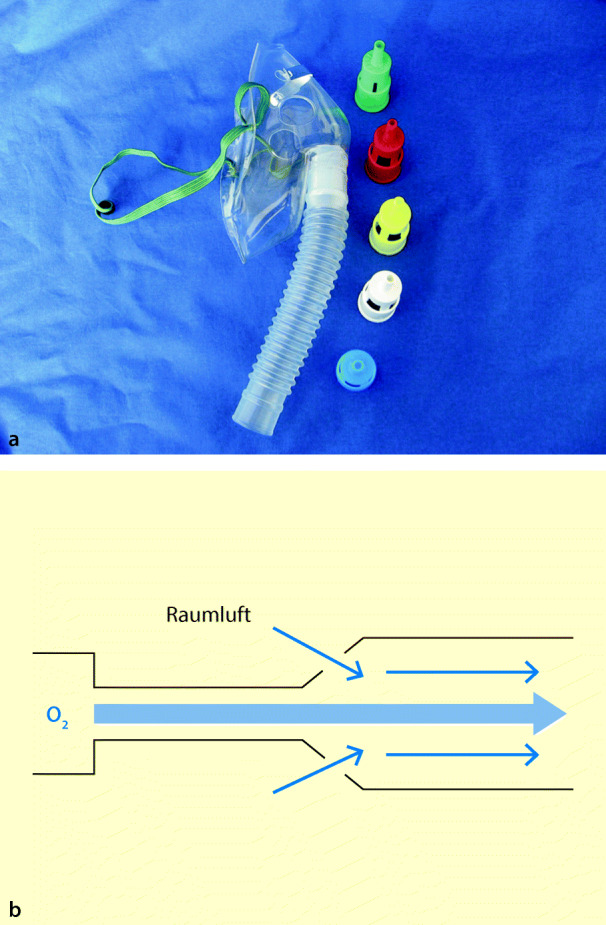
Eine Erhöhung des O2-Flusses bewirkt bei Venturi-Masken keine Erhöhung der inspiratorischen O2-Konzentration!
Nasale High-flow-Sauerstofftherapie
Bei der nasalen High-flow-O2-Therapie wird Sauerstoff und Druck- oder Umgebungsluft in einem Mischer zusammengeführt und mit stufenlos regelbarem Flow (10–55 l/min) in das Schlauchsystem geleitet (Abb. 54.8). Die O2-Konzentration wird ebenfalls stufenlos reguliert (30–100%) und kann mit einer O2-Messzelle bestimmt und angezeigt werden. Da bei hohen Gasflüssen mit einer Austrocknung und nachfolgender Schädigung der Schleimhäute im Nasen-Rachen-Raum zu rechnen ist, muss die nasale High-flow-O2-Therapie zwingend mit einem aktiven Befeuchtungssystem kombiniert werden. Als Interface zwischen Patient und System können spezielle, großlumige Nasenbrillen verwendet werden. Aufgrund des hohen Oxygenierungspotenzials bei maximalem Patientenkomfort erfreut sich dieses System großer Beliebtheit bei Anwendern und Patienten. Die nasale High-flow-O2-Therapie eignet sich besonders gut für Patienten, bei denen eine NIV-Therapie kontraindiziert ist, weiterhin zur Überbrückung von NIV-Pausen, bei Interventionen und in Palliativsituationen.
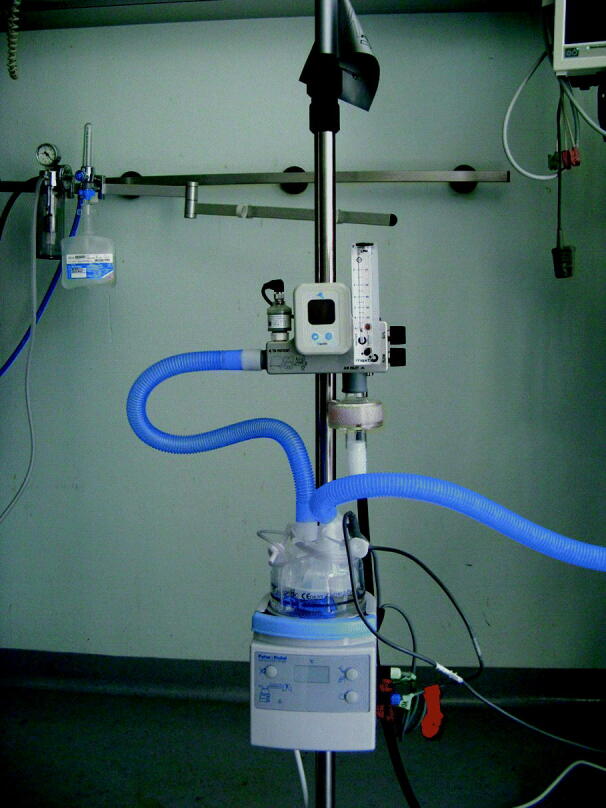
Die nasale High-Flow-O2-Therapie darf nur als Bindeglied zwischen konventioneller O2-Gabe und NIV angesehen werden, nicht als deren Ersatz.
Inhalationstherapie
Die Inhalationstherapie nimmt einen wichtigen Platz in der Versorgung von Intensivpatienten ein. Neben den „klassischen“ Medikamenten zur Bronchialdilatation und Entzündungshemmung werden auch Antibiotika, Mukolytika, Sekretolytika und Vasodilatatoren appliziert (Tab. 54.2).
| Antiobstruktiva (Bronchodilatatoren) | Salbutamol, Ipratropium, Tioptropium, Salmeterol, Fenoterol, … |
|---|---|
| Kortikosteroide | Budesonid, Beclomethason |
| Antiinfektiva | Colistin, Tobramycin, Gentamycin |
| Mukolytika | RhDNase, Ambroxol |
| Vasodilatatoren | NO, Prostazycline |
Grundlagen der Inhalationstherapie
Aerosole
Als Aerosole werden Mischungen aus flüssigen oder festen Schwebeteilchen in einem Gas oder Gasgemisch bezeichnet.
Deposition
Unter der pulmonalen Deposition versteht man die Abscheidung eines Aerosols in den Atemwegen. Diese ist von mehreren Faktoren wie z. B. der Teilchengröße und Verteilung des Aerosols, Atemfluss und Atemzugvolumen des Patienten und der Größe der Atemwege abhängig. Die Deposition selbst kann in drei Phasen unterteilt werden.
Impaktion
Hier werden größere Aerosolpartikel (>5 µm) beim ersten Aufprall auf eine Oberfläche abgelegt. Dies geschieht vorwiegend bei abrupten Richtungsänderungen wie z. B. am Kniestück des Beatmungssystems oder an der Rachenhinterwand bei der Spontanatmung.
Sedimentation
Kleinere Aerosolpartikeln (1–5 µm) sinken aufgrund der Schwerkraft auf den „Boden“ der Atemwege. Neben der Größe ist hier die Verweildauer der Partikel in den Bronchien ausschlaggebend.
Diffusion
Kleinste Partikel (<0,5 µm) gelangen durch Diffusion an ihren Bestimmungsort. Auch hier ist neben der Größe wieder die Verweildauer der Partikel in den Atemwegen depositionsfördernd.
Dosieraerosole (MDI, „metered dose inhaler“)
Bei den Dosieraerosolen befindet sich das Medikament zusammen mit Konservierungsstoffen, oberflächenaktiven Substanzen und flüssigem Treibmittel in einem unter Druck stehenden Container. Die Applikation des Medikaments erfolgt entweder über ein beiliegendes Mundstück oder – bei beatmeten Patienten – mit einem sog. MDI-Adapter, der entweder separat eingebaut werden muss oder bereits in das Beatmungs- oder geschlossene Absaugsystem integriert ist. Bei Anpassungsproblemen können sog. „Spacer“ Abhilfe schaffen.
Dosieraerosol: Optimale Technik
- Unter Spontanatmung:
- Inhalation vorbereiten: Schutzkappe entfernen, schütteln
- Ausatmen
- Mundstück mit den Lippen fest umschließen
- Kopf leicht zurückneigen
- Inhalation auslösen u. gleichzeitig langsam einatmen
- Atem anhalten
- Ausatmen
- Kappe aufsetzen
- Unter Beatmung:
-
9.Endotracheales Absaugen (wenn Sekret vorhanden)
-
10.MDI schütteln und in der Hand erwärmen
-
11.MDI auf Spacer oder Adapter aufsetzen
-
12.„Heat and moisture exchanger“ (HME, wenn vorhanden) entfernen
-
13.Medikamentenapplikation mit Beginn der Inspiration
-
14.15 s zwischen den Einzelgaben
-
15.HME wieder einsetzen (wenn vorhanden)
-
16.Dokumentation
-
9.
Pulverinhalatoren (DPI, „dry powder inhaler“)
Bei Pulverinhalatoren wird das Medikament verblistert, als Kapsel oder direkt im Inhalator bevorratet. Durch Aktivierung des Inhalators bzw. durch das Aufstechen der Kapsel wird das Medikament freigesetzt. Durch eine kräftige Inhalation entwickelt sich das Aerosol das dann inhaliert werden kann. Wichtig ist hierbei, dass der Patient über ein ausreichendes Atemzugvolumen bzw. eine ausreichende Kraft für eine tiefe, schnelle Inspiration verfügt. Für die Akuttherapie sind diese Applikatoren in der Regel nicht geeignet.
Pulverinhalator: Optimale Technik
-
2.
Aufrechte Körperhaltung
-
3.
Inhalation vorbereiten
-
4.
Ausatmen
-
5.
Gerät an den Mund nehmen und schnell einatmen
-
6.
Atem anhalten, 5–10 s
-
7.
Ausatmen, bevorzugt über die Nase oder Lippenbremse
-
8.
Nächste Inhalation
Feuchtinhalation
Die sog. Feuchtinhalationen können bei spontan atmenden und bei beatmeten Patienten angewendet werden. Ihr Vorteil liegt in der weitgehenden Unabhängigkeit vom erzeugten Atemfluss und der Koordinationsfähigkeit des Patienten sowie in der einfachen Handhabung durch Patient und Personal.
Jet-Vernebler
Bei Düsenverneblern wird Gas (Druckluft von extern oder vom Respirator) nach dem Venturi-Prinzip durch eine enge Düse gepresst. Dadurch wird die Medikamentenlösung aus der Medikamentenschale in eine Zuleitung gesaugt und vom Gasstrom zerstäubt. Größere Teilchen bleiben in der Verneblerkammer zurück, inhalierbare Aerosolpartikel werden vom Gasstrom des Respirators zum Patienten transportiert.
Ultraschallvernebler
Beim Ultraschallvernebler werden Schwingungen (>1 MHz) durch ein piezoelektrisches Element (Kristall) erzeugt, die von einem Kontaktmedium (destilliertes Wasser) an das zu vernebelnde Medikament weitergeleitet werden. Von der Oberfläche des in einer Medikamentenschale befindlichen Medikamentes werden dann Aerosolpartikel abgelöst und in den Atemstrom geleitet. Ultraschallvernebler steigern im Betrieb die Temperatur des Medikaments und sind daher für die Applikation von Peptiden und Proteinen (Denaturierung!) nicht geeignet.
Aerosol-Generator
Bei den Aerosolgeneratoren wird eine kleine Lochplatte durch ein vibrierendes Element in Bewegung versetzt (100.000 Schwingungen/min). Das zu vernebelnde Medikament wird durch 1.000 kleinste Öffnungen gepumpt und es entsteht so ein Aerosol von gleichmäßiger Größe. Der Aerosolgenerator benötigt keine Druckluft, der Antrieb erfolgt elektrisch.
Feuchtinhalatoren: Optimale Technik
- Unter Spontanatmung:
- Aufrechte Körperhaltung
- Inhalation vorbereiten
- Gerät einschalten
- Mundstück mit den Lippen fest umschließen
- Langsame, tiefe Inspiration, - kurze Pause – normale Exspiration
- Unter Beatmung:
-
6.Endotracheales Absaugen (wenn Sekret vorhanden)
-
7.Medikation in die Verneblerkammer einfüllen (Einzelapplikation!)
-
8.Vernebler zwischen Y−Stück und Inspirationsschlauch platzieren
-
9.„Heat and moisture exchanger“ (HME, wenn vorhanden) entfernen
-
10.Verneblerzyklus am Beatmungsgerät starten
-
11.Nach Ende des Verneblerzyklus Verneblerkammer entfernen
-
12.HME wieder einsetzen (wenn vorhanden)
-
13.Dokumentation
-
6.
Physikalische Atemtherapie
Maßnahmen der physikalischen Atemtherapie müssen entsprechend erlernt und unter Anleitung eines erfahrenen Physio- oder Atmungstherapeuten in die Praxis umgesetzt werden.
Hustenunterstützung
Viele intensivmedizinisch relevante Krankheitsbilder gehen mit einer Schwächung der Hustenfunktion einher. Als Beispiele seien neuromuskuläre Erkrankungen wie die amyotrophe Lateralsklerose (ALS) oder das Guillain-Barré-Syndrom (GBS) genannt. Lange, schwere Krankheitsverläufe und eine Critical Ilness Polyneuropathie oder eine Critical Illness Myopathie können die Hustenfunktion nachhaltig beeinträchtigen. Die Hustenschwäche kann durch einfache Beobachtung („Husten sie mal!“) oder durch die Messung des Hustenstoßes mit einem Peak-Flowmeter festgestellt werden.
Baging und Air-Stacking
Beim Baging wird ein zu geringes Atemzugvolumen mit Hilfe eines Beatmungsbeutels manuell erhöht, um so einen wirksamen Hustenstoß auszulösen. Der Patient sollte sich bei diesem Manöver möglichst in einer die Atmung erleichternden Position befinden. Zu Beginn versucht der Atemtherapeut, die Eigenatmung des Patienten leicht zu unterstützen. Auf Absprache erfolgt dann eine tiefe, unterstützte Inspiration mit der nachfolgenden Aufforderung zum Husten.
Das sog. Air-Stacking funktioniert nach dem gleichen Prinzip, nur werden anstelle einer tiefen Inspiration mehrere Atemhübe „aufeinandergestapelt“.
Das Baging kann ebenso wie das Air-Stacking über einen künstlichen Atemweg oder nichtinvasiv über Maske oder Mundstück angewendet werden.
Alle hustenunterstützenden Maßnahmen erfolgen in Absaugbereitschaft!
Cough-assist
Eine maschinelle Unterstützung der Hustenfunktion bietet der sog. In-/Exsufflator oder auch Cough-assist. Hierbei handelt es sich um Turbinengeräte, die nach einem Inspirationsmanöver mit vorgewähltem Druck schlagartig auf einen Sog umschalten. Diese Geräte können in einem manuellen Modus (Einstellparameter: Druck, Sog, Anstiegsgeschwindigkeit, Inspiration und Exspiration werden vom Therapeuten gesteuert) oder einem automatischen Modus (Einstellparameter: Druck, Sog, Anstiegsgeschwindigkeit, Inspirationszeit, Pausendauer, Exspirationszeit) betrieben werden. Angewendet werden diese Verfahren mindestens 3-mal tgl. zu je 3 Zyklen oder bei Bedarf. Als Bindeglied zwischen Patient und Gerät können wieder Tubus, Trachealkanüle oder Maske dienen.
Indikationen
Indiziert sind diese Verfahren bei allen Erkrankungen, die mit einer Sekretretention aufgrund einer Hustenschwäche einhergehen.
Kontraindikationen
Kontraindiziert sind diese Maßnahmen bei bestehendem oder vorangegangenem Pneumothorax, beim Lungenemphysem und bei hämodynamischer Instabilität.
Vibration
Hierunter wird die Anwendung feiner, schüttelnder Bewegungen über der betroffenen Lungenpartie oder über dem gesamten Thorax verstanden. Die Bewegungen können entweder mit der Hand oder mit einem Vibrationsgerät (z. B. Vibrax, „The Vest“) ausgeführt werden. Die Technik dient der verbesserten Durchblutung der Muskulatur. Ob mit dem Verfahren Sekret mobilisiert wird, ist bisher nicht erwiesen.
Atemtherapie mit PEP-Systemen
PEP-Systeme („positive expiratory pressure“) werden verwendet, um dem Atemwegskollaps eines instabilen Bronchialsystems (COPD) zu verhindern und so der Sekretretention entgegenzuwirken. Der sich in der Exspirationsphase aufbauende Druck schient die Atemwege und gibt so den Weg für das zu transportierende Sekret frei. Prinzipiell werden PEP-Systeme in oszillierende (PEP + Oszillation zur Sekretolyse – Flutter, RC Cornet, Acapella) und nichtoszillierende (nur PEP – BA Tube, Pari-PEP, EzPAP) unterteilt.
PEP-Übungen können bei invasiv beatmeten Patienten nicht angewendet werden, jedoch in der postoperativen Phase, nach der Extubation und während der NIV. Das EzPAP kann auch bei tracheotomierten Patienten eingesetzt werden.
Inzentive Spirometrie
Die inzentive (von engl. incentive: anspornende) Spirometrie (IS) gehört zu den die Lunge ausdehnenden (expandierenden) Techniken. Das Verfahren zwingt den nicht intubierten Patienten zu einer langsamen und maximalen Einatmung. Als Ansporn dient eine optische Kontrolle des Erfolgs am Gerät.
Atemübungen
Diese Übungen können nur bei kooperativen Patienten durchgeführt werden. Sie erfordern Geduld und Einfühlungsvermögen. Die Übungen sollen den pulmonalen Gasaustausch prä- und postoperativ verbessern. Für die Übungen wird die normale Atemmechanik so weit ausgenutzt, dass eine maximale Ausdehnung der betroffenen Seite oder beider Thoraxhälften erreicht wird. Physiotherapeuten können mit verschiedener Techniken, unterstützenden Griffe und zusätzlicher manueller Reibung die Übungsart variieren und individuell auf den Patienten abstimmen. Es werden verschiedene Zielsetzungen wie die Verbesserung der Ein- und oder Ausatmung, der Thoraxmobilität und der Dehnfähigkeit des Brustkorbes verfolgt. Diese Ziele werden mit Atemübungen unter physiotherapeutischer Atemtherapie umgesetzt.
Lagerung
Der Patient wird möglichst bequem gelagert, um eine maximale Ausdehnung der Thoraxwand zu erleichtern. Eine gute Muskelentspannung wird erreicht, wenn der Patient auf dem Rücken liegt und hierbei der Kopf leicht angehoben und das Kopfteil des Bettes etwas erhöht wird. Die Knie und Arme des Patienten werden etwas gebeugt und durch Kissen unterstützt. Hierdurch werden die Bauchmuskeln entspannt und die Beweglichkeit des Zwerchfells verbessert. Der Patient kann auch seine Arme über den Kopf legen, denn hierdurch wird die Lungenausdehnung ebenfalls begünstigt.
Als therapeutische Lagerung können weitere Techniken angewandt werden. Eine Unterlagerung mit Kissen zur Unterstützung verschiedener Lungenareale zeigt z. B. die VATI-Lagerung in Rückenlage. Die Seitenlage ist für die unterschiedliche Belüftung unterschiedlicher Lungenareale ebenfalls vorteilhaft und kann mit physiotherapeutischen Übungen kombiniert werden. Die Bauchlagerung wird als therapeutische Lagerung v. a. beim Lungenversagen eingesetzt.
Zwerchfellatmung
Eine tiefe und entspannte Atmung kann durch die Zwerchfellatmung erreicht werden. Zu Beginn wird der Patient auf die Bewegungen seines Zwerchfells während der Atmung aufmerksam gemacht. Die Pflegekraft legt ihre Hände auf die vordere Basis der Rippen; die Hände üben dort einen leichten Druck aus. Dann wird der Patient aufgefordert, gleichmäßig durch die Nase zu atmen und das Zwerchfell zu benutzen, „um seinen Bauch aufzufüllen“. Während dieses Vorgangs soll der Patient die Ausdehnung der unteren Rippen und das Auffüllen des Bauches bei der Abwärtsbewegung des Zwerchfells fühlen.
Anschließend soll der Patient gleichmäßig durch den Mund ausatmen. Hierbei wird wiederum leichter Druck auf die Rippenbasis ausgeübt. Hat der Patient die Übung genau verstanden, wird er gebeten, die Knöchel seiner Hände auf die Rippenbasis zu legen und die Zwerchfellatmung selbstständig durchzuführen.
Patienten mit Störungen im Bereich des Zwerchfells profitieren von der Physiotherapie. Hierbei können osteopathische Techniken und Kräftigungs- oder Bewegungsübungen zur Verbesserung der Zwerchfellfunktion eingesetzt werden.
Einseitige basale Ausdehnung
Die Pflegekraft legt ihre Hände seitlich auf den Thorax, um die Seitenatmung zu kontrollieren und zu unterstützen. Die gegenüberliegende Thoraxseite muss entspannt sein. Nun wird der Patient aufgefordert, gleichmäßig durch die Nase einzuatmen und ebenso gleichmäßig durch den Mund wieder auszuatmen. Während der Exspiration wird leichter Druck ausgeübt. Der Patient wird aufgefordert, während der Inspiration seine Rippen nach auswärts, in Richtung der Druck ausübenden Hand, auszudehnen. Mit zunehmender Inspiration wird der Druck der Hand vermindert, bis er schließlich so stark ist wie bei der Exspiration. Der Patient soll langsam ausatmen; die Rippen sollen hierbei vollkommen entspannt werden. Während der Exspiration wird leichter Druck ausgeübt. Anschließend wird die gesamte Übung wiederholt. Auch hier führt der Patient die weiteren Übungen selbstständig durch. Diese Übung kann auch in Seitenlage geübt werden.
Beidseitige basale Ausdehnung
Hierbei wird die gleiche Technik, wie für die einseitige basale Ausdehnung beschrieben, angewandt. Allerdings werden beide Hände auf die Thoraxseiten gelegt und üben dort Druck aus. Diese Übung soll der Patient ebenfalls selbstständig ausführen.
Obere seitliche Ausdehnung
Die Technik entspricht der für die einseitige basale Ausdehnung; die Hände werden jedoch etwas unterhalb der Achselhöhle auf die Thoraxwand gelegt.
Ausdehnung der Lungenspitzen
Bei dieser Methode wird während der Inspiration ein leichter Gegendruck unterhalb der Klavikula ausgeübt. Der Patient soll seinen Brustkorb nach vorn aufwärts gegen den Druck der Fingerspitzen ausdehnen. Die meisten Patienten mit pulmonalen Erkrankungen neigen dazu, bei dieser Technik ihre Atemhilfsmuskeln einzusetzen. Dann wird die Methode nicht angewandt oder durch Aufstützen der Arme in therapeutischen Sitzpositionen wie Kutschersitz, Torwarthaltung o. Ä. die Funktion der Muskulatur unterstützt.
Pharmakologische Atemtherapie
Bei einigen Intensivpatienten reichen die physikalischen Methoden der Atemtherapie und die Anfeuchtung der Atemluft nicht aus, um die Atemwege freizuhalten. Hier ist meist eine gezielte medikamentöse Therapie erforderlich. Die eingesetzten Medikamente wirken entweder erweiternd auf die Bronchien oder sie verflüssigen bzw. vermindern die Bronchialsekrete. Nicht selten müssen beide Substanzgruppen miteinander kombiniert werden, so z. B. wenn ein Bronchospasmus und gleichzeitig eine Sekreteindickung und Sekretverhaltung bestehen. Außerdem werden diese Medikamente bei chronischen Lungenerkrankungen eingesetzt, die mit pathologischen Veränderungen der Atemwege einhergehen.
Die Hauptziele der pharmakologischen Atemtherapie sind somit:
Erweiterung von funktionell verengten Bronchien,
Verflüssigung eingedickter Sekrete.
Hierzu werden folgende Substanzgruppen angewandt:
Bronchodilatatoren (Broncholytika; Tab. 54.3)
Sekretolytika.
| Bronchodilatator | Substanz | Zufuhr |
|---|---|---|
| Sympathikomimetika | Adrenalin (Suprarenin), Salbutamol (Sultanol), Terbutalin (Bricanyl), Fenoterol (Berotec) | s.c., per inhalationem, oral, (i.v.) |
| Phosphodiesterasehemmer | Theophyllin (Euphyllin, Perphyllon) | i.v., oral, rektal |
| Kortikosteroide | Kortisol (Hydrocortison), Dexamethason (Fortecortin) | i.v., i.m., s.c., p.o., per inhalationem |
Die Zufuhr dieser Substanzen erfolgt per Inhalation als Aerosol, i.v., i.m., s.c. oder p.o.
Broncholytika
Adrenalin (Suprarenin)
Adrenalin besitzt eine α- und eine β-adrenerge Wirkung (10.1007/978-3-662-50444-4_2). Die Substanz wird wegen der kardiovaskulären Nebenwirkung nur noch ausnahmsweise für die Inhalationstherapie eingesetzt.
Wirkungen
α-adrenerge Wirkung: Gefäßkonstriktion in der Bronchialschleimhaut mit Abnahme von Ödem und Schwellung (Asthma),
β-adrenerge Wirkung: Bronchodilatation.
Nebenwirkungen
Tachykardie, Blutdruckanstieg, Herzrhythmusstörungen, Angst, Herzklopfen.
Anwendung
Dosierung von Adrenalin
- s.c.
- Erwachsene: 0,2–0,5 ml der Lösung 1 : 1000 (1 ml = 1 mg); evtl. alle 20 min wiederholen
- Kinder: 0,01 ml/kgKG etwa alle 4 h
- Als Aerosol
- 0,25–0,5 ml der Lösung 1 : 100 (10 mg/ml) in 3–5 ml physiologischer Kochsalzlösung
Rasche Toleranzentwicklung bis hin zur Wirkungslosigkeit, besonders bei Azidosen.
Bei i.v.-Injektion kann der Tod durch ventrikuläre Herzrhythmusstörungen oder Hirnblutung (durch exzessiven Blutdruckanstieg) eintreten.
Terbutalin ( Bricanyl)
Bevorzugte Wirkung auf die β2-Rezeptoren
Wirkung
Bronchodilatation durch β2-Stimulation. Hierbei 2-mal stärker wirksam als Orciprenalin bei wesentlich geringerer Herzwirkung. Wirkdauer ca. 3–5 h.
Nebenwirkungen
Tremor, Tachykardie.
Anwendung
Dosierung von Terbutalin
0,25–0,5 mg s.c. mehrmals täglich, ist auch oral wirksam
Nicht i.v. injizieren, da dann Herzwirkungen ausgeprägter sind.
Salbutamol ( Sultanol)
Dies ist die Substanz mit der geringsten β1-Wirkung; keine α-Wirkung; ist kein Katecholamin.
Wirkung
Bronchodilatation durch β2-Stimulation; Wirkdauer bis zu 6 h nach der Inhalation. Auch oral wirksam.
Nebenwirkung
Tachykardie, Tremor, Unruhe
Anwendung
Dosierung von Salbutamol
10 Tropfen/1 Amp. oder 1–2 Hübe per inhalationem; mehrmals täglich nach Bedarf
Ipratropium (Atrovent)
Wirkung
Bronchodilatation durch Vagolyse, Wirkdauer bis zu 6 h nach der Inhalation.
Nebenwirkungen
Mundtrockenheit, Miktionsstörungen, Sehstörungen
Anwendung
Dosierung von Ipratropium
Max. 20 Hübe der Lösung (Atrovent LS) oder 1–2 Hübe per Dosieraerosol 3- bis 4-mal tgl.
Kortikosteroide
Die Kortikosteroide werden u. a. zur Behandlung des Asthmas und der infektexazerbierten COPD eingesetzt. Die Wirkungen sind:
Konstriktion der Blutgefäße in der Bronchialschleimhaut,
Relaxierung der Bronchialmuskulatur,
Verminderung des Schleimhautödems,
antiallergisch, entzündungshemmend.
Im Status asthmaticus werden die Kortikosteroide i.v. gegeben; sie können sonst auch oral oder per Inhalation als Aerosol zugeführt werden.
Budesonid (Pulmicort )
Wirkung
Hemmung der Schleimsekretion, Entzündungshemmung, Aufbau von neuem Bronchialepithel
Nebenwirkung
Mundsoor, Heiserkeit
Anwendung
Dosierung von Budesonid
Je nach Schweregrad, max. 1,6 mg tgl. verteilt auf 4 Inhalationen
Sekretolytika , Mukolytika
Diese Medikamentengruppe wird eingesetzt, um die Viskosität des Schleims herabzusetzen und so den Sekrettransport und die Sekretelimination zu erleichtern. Der Nutzen von Sekretolytika und Mukolytika wird immer wieder kontrovers diskutiert, entgegen der Auffassung vieler Anwender ist die Wirksamkeit dieser Substanzen keineswegs gesichert.
Acetyl-L-Cystein (ACC)
Wirkung
ACC spaltet die Disulfid-Brücken im Mukus und reduziert so die Viskosität. Neben der mukolytischen Wirkung wird ACC eine antioxidative Wirkung zugeschrieben.
Nebenwirkung
Sehr selten Haut- und Schleimhautveränderungen, Bronchospastik bei Inhalation.
Anwendung
Dosierung von Acetyl-L-Cystein
p.o.: 3×200 mg
i.v.: 1–2 Amp
inhalativ: 2 Amp/Tag
RhDNAse (Pulmozyme)
Wirkung
RhDNAse spaltet die DNA neutrophiler Granulozyten, die bevorzugt in eitrigem Sekret zu finden sind und verbessert so die Flusseigenschaften des Sekrets.
Nebenwirkung
Bisher wurden nur geringfügige Nebenwirkungen wie z. B Heiserkeit o.ä. beobachtet.
Anwendung
RhDNAse wird entweder inhalativ oder direkt im Rahmen der Beatmung in das Bronchialsystem appliziert. In der Regel werden 2 Einzeldosen verabreicht; von einer abendlichen Gabe ist abzusehen, da sonst die Maßnahmen zur Sekretelimination in die Ruhezeit der Patienten fallen. Bisher ist dieses Medikament nur zur Behandlung der zystischen Fibrose (CF) zugelassen: Im Rahmen von Heilversuchen und klinischen Studien wurde es jedoch auch bei beatmeten Patienten eingesetzt.
Footnotes
Unter Mitarbeit von N. Schwabbauer
Contributor Information
Collaborators: Tobias Fink and Tilmann Müller-Wolff
Nachschlagen und Weiterlesen
- [1].Schwabbauer N, Riessen R. Sekretmanagement in der Beatmungsmedizin. Bremen: UNI-MED Science; 2010. [Google Scholar]
- [2].Driscoll O', et al. Guideline for emergency oxygen use in adult patients. Thorax. 2008;63(6):1–68. doi: 10.1136/thx.2008.102947. [DOI] [PubMed] [Google Scholar]
Internet
- [3].Deutsche Atemwegsliga. Richtig inhalieren. www.atemwegsliga.de