Abstract
Die endotracheale Intubation und die Tracheotomie sind ein wesentlicher Bestandteil der respiratorischen Behandlung des Intensivpatienten. Sie schützen zuverlässig vor pulmonaler Aspiration, ermöglichen die Zufuhr hoher O2-Konzentrationen unter Spontanatmung und das Absaugen von Bronchialsekreten. Beim Intensivpatienten werden zwei Verfahren des künstlichen Atemwegs angewandt: endotracheale Intubation (oral oder nasal) oder Tracheotomie (konventionell oder perkutan).
Die endotracheale Intubation und die Tracheotomie (10.1007/978-3-662-50444-4_8) sind wesentliche Bestandteile der respiratorischen Behandlung des Intensivpatienten. Sie schützen zuverlässig vor pulmonaler Aspiration, ermöglichen die Zufuhr hoher O2-Konzentrationen unter Spontanatmung und das Absaugen von Bronchialsekreten. Beim Intensivpatienten werden zwei Verfahren des künstlichen Atemwegs angewandt: endotracheale Intubation (oral oder nasal) oder Tracheotomie (konventionell oder perkutan).
Endotracheale Intubation
Die endotracheale Intubation des Intensivpatienten kann oral oder nasal erfolgen (Einzelheiten: 10.1007/978-3-662-50444-4_8). Die nasale Intubation wird meist besser toleriert und ermöglicht eine bessere Mundpflege, führt aber häufig zu Entzündungen der Nasennebenhöhlen (meist der Kieferhöhle) mit der Gefahr der Bakteriämie und der lebensbedrohlichen Sepsis. Bei der orotrachealen Intubation tritt diese Komplikation dagegen wesentlich seltener auf; auch werden Verletzungen der Nasenmuscheln und Drucknekrosen im Bereich der Nasenflügel vermieden. Zudem kann ein größerer Tubus eingeführt werden; hierdurch werden der Atemwegswiderstand und die Atemarbeit bei Spontanatmung vermindert.
Wegen der erhöhten Sinusitisgefahr durch die nasotracheale Intubation wird derzeit beim Erwachsenen die orale Intubation bevorzugt.
Fixierung des oralen Tubus
Orale Tuben müssen sicher fixiert werden, um Dislokationen, mechanische Reizungen und Fehllagen zu vermeiden. Hierfür sind spezielle Tubusfixationssysteme besonders geeignet. Die jeweils gewählte Fixierung muss den Tubus sicher am Kopf des Patienten befestigen. Meist wird hierfür ein auf die Gesichtshaut geklebtes Hilfsmittel verwendet. Pflasterstreifen eignen sich für vorübergehende Fixierungen.
Praktisches Vorgehen
Zunächst korrekte Lage des Tubus auskultatorisch kontrollieren, wenn nötig korrigieren (10.1007/978-3-662-50444-4_8),
dann den Abstand zwischen Tubusspitze und Zahnreihe oder Mundwinkel ermitteln und mit wasserfestem Stift markieren (z. B. 20 cm bei Frauen und 22 cm bei Männern); Markierungspunkt dokumentieren,
Tubus in einem der Mundwinkel platzieren, b. B. Beißschutz einführen; ggf. Tubuslage mit Thoraxröntgenaufnahme kontrollieren.
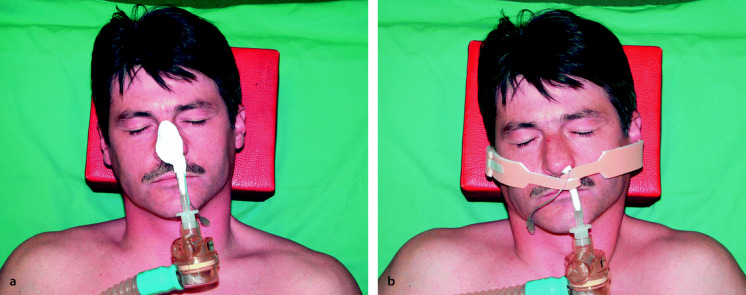
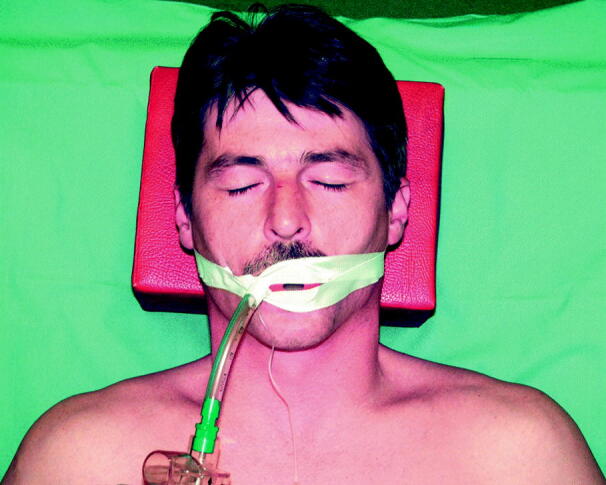
- Fixierung mit zwei Pflasterstreifen: Abb. 55.1.
- Den ersten Pflasterstreifen auf die Wange kleben, faltenfrei über der Oberlippe zum Tubus führen und direkt am Eintritt in den Mund kreisförmig um den Tubus kleben, dann auf der anderen Wange befestigen, ohne Hautfalten zu erzeugen. An einem Pflasterende eine Umschlagfalte bilden, um das Pflaster leichter lösen zu können.
- Danach den 2. Pflasterstreifen unterhalb der Unterlippe auf der Wange befestigen, dann kreisförmig um den Tubus kleben und auf der anderen Wange ankleben. An einem Pflasterende eine Umschlagfalte bilden.
- Alternative: 2. Pflasterstreifen ebenfalls oberhalb der Oberlippe befestigen, kreisförmig um den Tubus führen und auf der gleichen Wangenseite unterhalb der Unterlippe befestigen.
- Tubuslage durch erneute Auskultation überprüfen.
- Während der gesamten Prozedur fixiert die Pflegefachkraft mit einer Hand den Tubus am Kopf des Patienten, bei Bedarf unterstützt durch eine zweite Pflegekraft.
- Tubuslage durch erneute Auskultation prüfen.
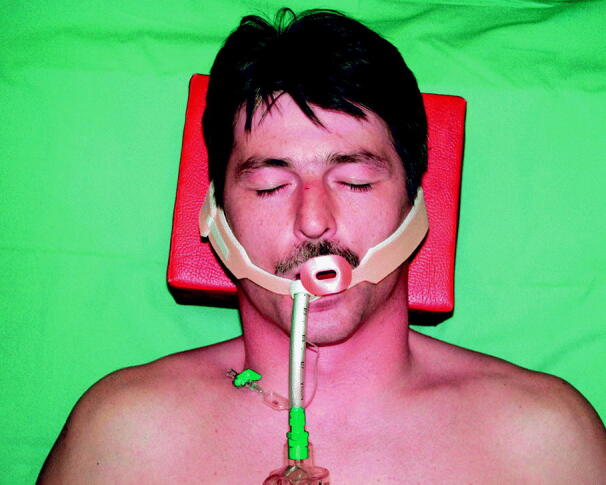
- Fixierung mit Klettband: Abb. 55.2.
- Tubus direkt am Mund mit Pflasterstreifen umwickeln.
- Dann Klettband fest um diesen Pflasterstreifen am Tubus wickeln.
- Klettband um den Kopf des Patienten führen, z. B. rechts oberhalb des Ohres, links unterhalb. Dann Klettverschluss schließen.
- Tubuslage durch erneute Auskultation überprüfen.
Umlagern des Tubus
Der orale Tubus sollte in regelmäßigen Abständen umgelagert werden, am besten im Zusammenhang mit der Mundpflege, um Druckschäden der Mundwinkel und der Mundhöhle zu vermeiden.
Praktisches Vorgehen
Zubehör vorbereiten,
Einmalhandschuhe anziehen, Cuffdruck kontrollieren, dann Mundhöhle absaugen,
Tubusbefestigung vollständig entfernen (Vorsicht: Extubationsgefahr!); Mundwinkel und Mundhöhle auf Druckschäden inspizieren,
Pflasterreste vorsichtig entfernen, Hautschutz mit Platten,
Tubus vorsichtig über den Zungengrund hinweg in den anderen Mundwinkel schieben, dabei die Tubustiefe nicht verändern (Markierung beachten!),
Kontrolle der Tubuslage, Fixierung und Dokumentation.
Fixierung des nasalen Tubus
Nasale Tuben können ebenfalls mit Pflasterstreifen oder mit Klettband fixiert werden (Abb. 55.3). Die Tuben werden so befestigt, dass möglichst wenig Druck auf die Nase ausgeübt wird.
Praktisches Vorgehen
Korrekte Tubuslage durch Auskultation überprüfen, Tubusende direkt am Austritt aus der Nase mit wasserfestem Stift markieren.
- Befestigung mit Pflasterstreifen:
- Direkt oberhalb der Markierung einen schmalen, ca. 15 cm langen Pflasterstreifen schräg über einen Nasenflügel führen, dann kreisförmig um den Tubus wickeln und auf dem anderen Nasenflügel befestigen, Hautschutz mit Platten.
- Alternative: breiten Pflasterstreifen (ca. 10 cm lang) bis zur Mitte einschneiden, dann den nicht aufgeschnittenen Pflasteranteil auf den Nasenrücken kleben; danach den einen Schenkel des Pflasters direkt am Austritt aus den Nase um den Tubus kleben, dann den anderen Schenkel; die Enden beider Schenkel auf einem Nasenflügel festkleben.
- Befestigung mit klebefreiem Fixierband:
- Pflasterstreifen am Austritt aus der Nase kreisförmig um den Tubus kleben.
- Industriell vorgefertigtes Fixierband auf dem zirkulären Tubuspflaster befestigen; das eine Ende des Bandes oberhalb des einen Ohres, das andere Ende unterhalb des anderen Ohres um den Kopf führen und verschließen. Beim nächsten Verbandwechsel die Ohrführung wechseln, um Druckstellen in diesem Bereich zu vermeiden.
- Bei mehrtägiger Intubationsdauer sind kommerzielle Befestigungssystem wie Anchor Fast vorteilhaft.
Cuffdruckmessung
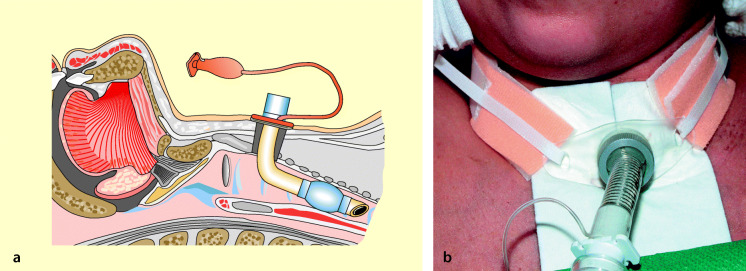
Um Druckschäden der Trachea zu vermeiden, werden in der Intensivmedizin grundsätzlich Endotrachealtuben mit Niederdruckmanschette verwendet. Sicherheitshalber sollte aber der Cuffdruck mit einem speziellen Manometer (sog. Cuffwächter, Abb. 55.4) kontinuierlich überwacht und wenn erforderlich korrigiert werden. Für die länger dauernde Intubation sollte die kontinuierliche, automatische Cuffdruckmessung eingesetzt werden.

“Controlled Pressure Cuff”
Bei diesem speziellen Tubus steht die Manschette über einen Druckausgleich mit einem außerhalb befindlichen Reservoirbeutel in Verbindung. Hierdurch wird der Druck in der Manschette automatisch im gewählten Bereich gehalten.
Praxistipp
Der Cuffdruck des Endotrachealtubus sollte im Bereich von 15 bis max. 25 cmH2O gehalten werden. Außerdem sollte der Cuffdruck in der Verlaufskurve dokumentiert werden.
Hohe Cuffdrücke
Sind hohe Cuffdrücke erforderlich, um die Dichtigkeit des Tubus zu erreichen, sollte immer nach den Ursachen gesucht werden. Mögliche Ursachen sind:
zu kleiner Tubus im Vergleich zur Weite der Trachea: Tubus auswechseln,
herausgerutschter Tubus mit Cufflage in der Glottis: Tubus korrekt platzieren.
Undichter Cuff
Beim beatmeten Patienten muss der Cuff dicht schließen. Treten Leckagen auf, muss umgehend die Ursache beseitigt werden. Mögliche Ursachen sind u. a.:
Cuff, Zuleitung oder Kontrollballon defekt: Tubus auswechseln,
hoher Beatmungsdruck: Tubus nachblocken.
Tubuspflege
Tubusüberwachung
Der Tubus gehört zu den sog. „Lebenslinien“; er darf daher niemals durch eingedicktes Sekret, geronnenes Blut, Ballonhernie o. ä. verlegt werden. Solche Komplikationen lassen sich durch folgende Maßnahmen verhindern:
ausreichende Befeuchtung der Atemluft (Atemgasklimatisierung),
gründliches Absaugen (Häufigkeit nach Bedarf!),
täglich mehrfache Kontrolle der Tubusdurchgängigkeit mit dem Absaugkatheter,
sorgfältige Atem- und Physiotherapie.
In Bettnähe des Intensivpatienten muss immer ein funktionsfähiges Notfallintubationsbesteck bereitgehalten werden.
Bei akuter, nicht mehr zu beseitigender Verlegung des Tubus muss wegen der großen Erstickungsgefahr der Tubus sofort herausgezogen, der Patient überbrückend mit Maske/Beutel beatmet und ein neuer Tubus eingeführt werden. Ist dies nicht möglich, können zur Überbrückung ein Larynxtubus, eine Larynxmaske oder ein Combitubus eingeführt werden (10.1007/978-3-662-50444-4_8).
Nasenpflege
Bei nasaler Intubation sollte die betroffene Nasenseite mehrmals täglich auf Durchblutungsstörungen und Druckschäden kontrolliert werden. Die Nasenpflege wird im Allgemeinen 1- bis 2-mal pro Tag durchgeführt.
Praktisches Vorgehen
Zubehör bereitstellen: geeigneter Absaugkatheter, Einmalhandschuhe, mehrere Wattestäbchen und Kompressen, physiologische Kochsalzlösung, Nasensalbe, Fixiermaterial.
Den Patienten über das geplante Vorgehen informieren.
Tubusfixierung entfernen und Sekrete im Tubusbereich vorsichtig absaugen.
Nase mit NaCl 0,9%getränkten Wattestäbchen reinigen; Verkrustungen vorsichtig lösen und entfernen.
Nase auf Durchblutungsstörungen und Druckschäden inspizieren, wenn erforderlich Arzt hinzuziehen (Frage der Umintubation!).
Nasensalbe mit Wattestäbchen im Bereich des Tubus auf die Nasenschleimhaut auftragen.
Tubus neu fixieren.
Tubuslage durch Auskultation überprüfen.
Ist die Haut durch den Druck des Tubus bereits geschädigt worden, sollten die betreffenden Stellen mit Hautschutzplatten abgedeckt und die Pflasterstreifen auf den Platten befestigt werden.
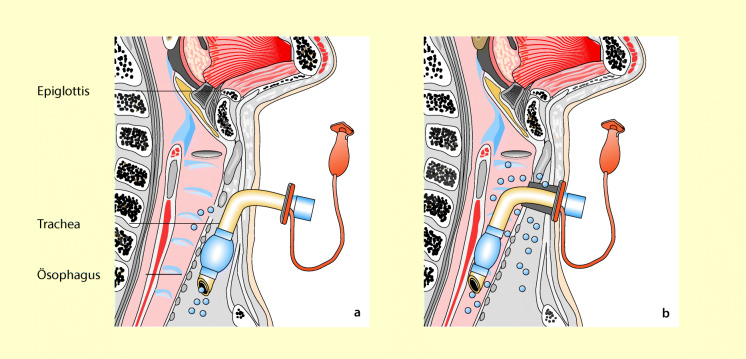
Absaugen des subglottischen Raums
Beim endotracheal intubierten Patienten sammelt sich oberhalb des Cuffs Sekret aus dem Mund-Nasen-Rachenraum. Die darin enthaltenen Keime können durch sog. Mikroaspirationen am Cuff vorbei in das Bronchialsystem gelangen und Infektionen hervorrufen. Bei Verwendung spezieller Tuben mit subglottischer Absaugmöglichkeit können die Sektrete entfernt werden. Hierdurch können die Häufigkeit der ventilatorassoziierten Pneumonie, die Gesamtdauer der Beatmung und die Dauer der Intensivbehandlung gesenkt werden. Daher sollten diese Tuben bei einer absehbaren Beatmungsdauer von >72 h den konventionellen Tuben vorgezogen werden.
Tracheotomie
Definitionen
Tracheotomie
Operative Eröffnung der Luftröhre im vorderen Halsbereich mit anschließender Kanülierung der Trachea.
Perkutane Tracheotomie
Perkutanes Einführen einer Kunststoffkanüle zwischen den Trachealringen (2–4) in die Luftröhre.
Minitracheotomie
Perkutanes Einführen einer Spezialkanüle mit kleinem Durchmesser durch die Membran zwischen Schild- und Ringknorpel des Kehlkopfes für die Bronchialtoilette.
Tracheostoma
Die durch eine Tracheotomie geschaffene Öffnung der Luftröhre nach außen.
Tracheostomie
Chirurgische Technik, bei der die Haut mit der Vorderwand der Trachea vernäht wird, um einen permanenten Luftweg zu schaffen.
Bei der Tracheotomie wird die Luftröhre im vorderen Halsbereich operativ eröffnet und anschließend kanüliert. Wann der Intensivpatient tracheotomiert werden soll, ist nach wie vor umstritten, v. a. deshalb, weil keine Einigkeit darüber besteht, wie lange ein Endotrachealtubus, ohne Schädigungen hervorzurufen, belassen werden kann. Die entsprechenden Angaben differieren zwischen 24 und 48 h bzw. 14 Tagen. Unstrittig ist hingegen die Indikation zur Tracheotomie bei Verletzungen des Kehlkopfs und bei bestimmten Erkrankungen im oberen Respirationstrakt.
Vorteile der Tracheotomie
Die wichtigsten Vorteile der Tracheotomie im Vergleich mit der oralen und nasalen Intubation sind:
größere und kürzere Kanülen, daher geringerer Widerstand und weniger Atemarbeit für den spontan oder unterstützt atmenden Patienten,
einseitige Intubation sehr selten,
bessere Fixierung der Kanüle,
bessere Mund- und Nasenpflege,
leichtere Schluckmöglichkeiten für den Patienten
einfacheres und effektiveres Absaugen des Bronchialsystems,
Verminderung des Totraums,
größerer Patientenkomfort.
Indikationen
Meist wird der Intensivpatient zunächst oral oder nasal intubiert und später elektiv tracheotomiert (sekundäre Tracheotomie). Wann dieser Zeitpunkt am günstigsten ist, wird nicht einheitlich beurteilt. Eine primäre Tracheotomie ist u. a. in folgenden Situationen indiziert:
schwere Verletzungen des Kehlkopfs,
Verätzungen im Mund und Rachenbereich,
Unmöglichkeit der oralen oder nasalen Intubation.
Eine Notfalltracheotomie ist gefährlich und sollte nur ausnahmsweise durchgeführt werden, d. h. wenn die orale Intubation misslingt.
Trachealkanülen
Trachealkanülen gibt es, wie Endotrachealtuben, aus unterschiedlichen Materialien und in verschiedenen Größen. Der äußere Durchmesser reicht von 3,5–14 mm, der innere Durchmesser von 2,5–10,5 mm, die Länge von etwa 4,5–10 cm. Die Kanülen sind aus Metall oder Kunststoff. Kunststoffkanülen (Abb. 55.5) werden in der Intensivmedizin am häufigsten eingesetzt; ihre Blockmanschetten sind den Niederdruckmanschetten der Endotrachealtuben nachgebildet, entsprechen ihnen jedoch nicht vollständig. Wenn der Patient nicht mehr beatmet werden muss und außerdem keine Aspirationsgefahr besteht, können spezielle Sprechkanülen verwendet werden.

Technik der konventionellen Tracheotomie
Die Tracheotomie wird, möglichst als Wahleingriff, in Intubationsnarkose durchgeführt, und zwar im Operationssaal – im Bett der Intensivstation hingegen nur in Ausnahmefällen. Notfalltracheotomien sind sehr komplikationsreich! Dennoch muss auch auf Intensivstationen eine entsprechende Material für eine Tracheotomie vorhanden sein.
Wichtiges Tracheotomiezubehör
Komplettes, steriles Tracheotomiebesteck
Trachealkanülen
OP-Lampe
Absauggerät und Absaugkatheter
Narkosezubehör einschließlich EKG-Monitor
Die Operation wird in Rückenlage ausgeführt, der Hals dabei überstreckt. Die Haut wird zwischen dem Ringknorpel und dem Jugulum in Längsrichtung gespalten. Die eigentliche Tracheotomie erfolgt meist in Höhe des 3. oder 4. Trachealringes (mediane Tracheotomie). Hierzu wird in die Trachea ein Fenster in der Größe des einzuführenden Tubus geschnitten. Bei Kindern wird hingegen kein Knorpel exzidiert, um nicht die Entstehung einer Trachealstenose zu begünstigen. Anschließend wird der Endotrachealtubus herausgezogen und die größtmögliche Trachealkanüle eingeführt. Die richtige Kanülenlage wird zunächst durch Auskultation des Brustkorbs überprüft; später wird ein Röntgenbild des Thorax angefertigt. Nach Abschluss der Tracheotomie muss die Kanüle sicher fixiert werden: Hierzu wird ein elastisches Band um den Hals geführt (Abb. 55.6). Als Verband sollte ein spezieller Tracheostomaverband angebracht werden.
Komplikationen der Tracheotomie
Die Komplikationen der Tracheotomie entsprechen z. T. denen der endotrachealen Intubation; meist handelt es sich um Druckschäden im Bereich der Trachea. Druckschäden des Kehlkopfs und der Nasenwege werden, anders als bei der endotrachealen Intubation, durch die Tracheotomie nicht hervorgerufen. Daneben können jedoch als eher typische Tracheotomieschäden folgende, z. T. lebensbedrohliche Komplikationen auftreten:
massive Blutungen durch Arrosion von Gefäßen,
Kanülenfehllage (Abb. 55.7),
Hautemphysem (Abb. 55.7),
Pneumothorax, Pneumomediastinum,
Wundinfektion,
Tracheoösophagealfistel,
Stenosen im Stomabereich.
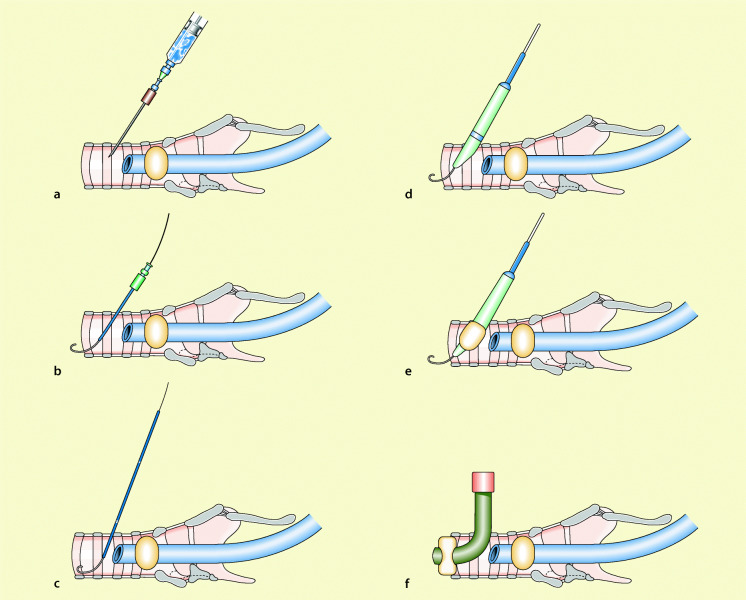
Perkutane Dilatationstracheotomie
Bei diesem Verfahren (Abb. 55.8) wird die Trachea zunächst zwischen den Trachealringen (2–4) mit einer Kanüle punktiert, dann ein flexibler Seldinger-Draht durch die Kanüle in die Trachea vorgeschoben und anschließend die Trachealöffnung mit Dilatatoren erweitert; schließlich wird die Trachealkanüle eingeführt. Das Vorgehen erfolgt jeweils unter fiberoptischer Kontrolle durch einen zweiten Arzt. Der Eingriff erfolgt entweder in Kurznarkose oder unter Lokalanästhesie. Im Gegensatz zur konventionellen Tracheotomie, die überwiegend durch Chirurgen oder HNO-Ärzte erfolgt, wird die perkutane Technik vorwiegend von Intensivmedizinern ausgeführt.
Die perkutane Dilatationstracheotomie ist einfacher und oft auch schneller durchzuführen (ca. 15–30 min) als die Tracheotomie, außerdem ist sie weniger aufwendig und billiger. Spezifische Gefahren sind Fehlpunktionen und Trachealverletzungen, die aber durch fiberoptische Kontrollen während des Eingriffs meist vermieden werden können, außerdem intraoperative Blutungen, besonders aus der A. thyreoidea.
Die übrigen Komplikationen entsprechen im Wesentlichen denen der konventionellen Tracheotomie.
Kontraindikationen
Zu den wichtigsten Kontraindikationen der perkutanen Dilatationstracheotomie gehören:
ausgeprägte Struma,
schwerste Gerinnungsstörungen,
HWS-Frakturen,
Tracheomalazie,
Tumoren und Stenosen der oberen Luftwege,
Kindes- und Jugendalter,
sehr lange Rehabilitation des Patienten zu erwarten.
Treten intraoperativ Komplikationen auf, sollte das Verfahren nicht fortgesetzt werden. Die folgenden Techniken sind derzeit gebräuchlich.
Ciagla-Technik
Zunächst wird durch eine Punktionskanüle ein Führungsdraht in die Trachea vorgeschoben, dann über den Draht Dilatatoren zunehmender Größe (Abb. 55.8). Bei entsprechender Aufweitung der Trachealöffnung wird zum Schluss die Trachealkanüle eingeführt.
Ciagla-Blue-Rhino-Technik
Bei dieser Modifikation des Ciagla-Verfahrens wird die Trachea in der oben beschriebenen Weise mit der Seldinger-Technik punktiert und dann in einem Schritt mit einem gebogenen und speziell beschichteten Dilatator erweitert. Anschließend wird ein Führungsstab eingeführt und darüber die Trachealkanüle in die Luftröhre vorgeschoben.
Methode von Griggs
Zunächst wird die Trachea mit einer Kanüle punktiert, dann durch die Kanüle ein Draht vorgeschoben und anschließend die Punktionsstelle so weit dilatiert, dass eine sog. Dilatationspinzette eingeführt werden kann. Danach wird die Punktionsstelle mit der Pinzette aufgeweitet und schließlich eine Trachealkanüle über den Draht eingeführt.
PerkuTwist-Methode
Bei dieser Technik wird ein spezieller Dilatator über den Führungsdraht vorsichtig durch das Gewebe geschraubt bis die Trachealwand durchtrennt ist. Danach wird der Dilatator zurückgedreht und über den Draht die Trachealkanüle eingeführt.
Perkutane translaryngeale Dilatationstracheotomie nach Fantoni
Zunächst wird der entblockte Tubus (vorher Mund-Rachen-Raum sorgfältig absaugen) unter fiberoptischer Kontrolle zurückgezogen, bis der Cuff im Glottisbereich liegt. Nach erneuter Blockung des Cuffs mit wenigen ml wird die Trachea mit der gebogenen Kanüle des Tracheotomie-Sets zwischen dem 2. und 3. Trachealring punktiert, dann ein Draht durch die Kanüle, am Tubus vorbei, nach oben in den Oropharynx geschoben. Liegt der Draht im Oropharynx, wird er mit der Magill-Zange gefasst, aus dem Mund herausgeführt und mit der Trachealkanüle verbunden. Nun erfolgt die Umintubation des Patienten mit einem dünnen Tubus aus dem Set (ID 5 mm). Danach wird die Trachealkanüle durch Zug an dem aus dem Hals ragenden Ende des Drahtes durch den Pharynx und dann den Kehlkopf (translaryngeal) und schließlich durch die Trachealwand und die Halsweichteile nach außen gezogen. Meist muss hierzu die Haut im Halsbereich 0,5–1 cm mit dem Skalpell inzidiert werden. Nun wird das geschliffene Kanülenende abgeschnitten, der dünne Endotrachealtubus entfernt, die Trachealkanüle um 180° gedreht und dann an die Beatmungsschläuche angeschlossen.
Wichtigster Vorteil des Verfahrens ist die geringere Verletzungsgefahr für die Trachea, da die Kanüle, im Gegensatz zu den anderen Methoden, nach außen gezogen wird. Nachteilig ist der größere technische Aufwand. Bei bekannten Intubationsschwierigkeiten ist das Verfahren nicht indiziert.
Zubehör und praktisches Vorgehen
Das verwendete Zubehör richtet sich v. a. nach der gewählten Methode der Dilatationstracheotomie. Hierfür werden praktisch nur kommerzielle Sets eingesetzt.
Zubehör für die perkutane Dilatationstracheotomie
Punktionstracheotomieset
Konventionelles Tracheotomieset und Intubationsbesteck in Bereitschaft
Passende Trachealkanülen (3 Größen)
Fiberbronchoskop mit Zubehör
i.v.-Anästhetikum und Opioid
Skalpell, Schere, Klemme (steril)
Handschuhe und Kittel (steril), Mundschutz, Haube
Unterlage (aufsaugend, wasserdicht)
Lokalanästhetikum
Hautdesinfektionsmittel
Sterile Abdecktücher
Lagerungshilfsmittel für Kopf und Schulter
Verbandmaterial
Praktisches Vorgehen
Die Dilatationstracheotomie kann auf der Station im Patientenbett durchgeführt werden. Der Eingriff erfolgt meist in Narkose; Lokalanästhesie ist jedoch ebenfalls möglich.
Erforderliche Personen: 2 Ärzte, 1–2 Fachpflegekräfte,
Operateur: steriler Kittel, sterile Handschuhe, Mundschutz, Kopfhaube,
Einleitung einer i.v.-Anästhesie (z. B. Propofol + Remifentanil; 10.1007/978-3-662-50444-4_10),
Lagerung des Patienten mit überstrecktem Kopf, Fixierung des Kopfes mit Lagerungsmitteln, z. B. Kopfring,
Unterlage unter Kopf, Hals und Schultern legen,
Mund-Rachen-Raum gründlich absaugen,
wenn keine i.v.-Narkose: Lokalanästhesie des Punktionsbereichs,
Hautdesinfektion von Kinn, Hals und oberem Brustkorb,
Assistenzarzt: Führt das Bronchoskop durch den Endotrachealtubus ein und kontrolliert von endotracheal die Punktion und Dilatation durch den Operateur, um Verletzungen zu verhindern; bei liegendem Bronchoskop zunächst Tubus entblocken und in den Glottisbereich zurückziehen; dann erneut mit wenigen ml blocken; Beatmung fortsetzen,
Punktionsstelle lokalisieren, dann die Trachea mit der Kanüle und aufgesetzter Kochsalzspritze punktieren; Eindringen von Luftblasen in die Spritze zeigt die Lage der Kanüle in der Trachea an,
danach Seldinger-Draht unter bronchoskopischer Kontrolle durch den Assistenzarzt in die Trachea einführen und vorschieben,
weiteres Vorgehen je nach gewählter Methode: ► oben.
Nach Einführen der Trachealkanüle: bronchoskopische Lagekontrolle, dann Blocken des Cuffs, Verband anlegen, Cuffdruck kontrollieren,
Röntgenkontrolle durchführen,
Dokumentation der Maßnahme in der Patientenkurve.
Komplikationen der Dilatationstracheotomie
Blutungen mit Notwendigkeit einer Intervention,
Dislokation oder Verstopfung der Kanüle,
notfallmäßige Koniotomie,
Stomainfektion,
operativer Verschluss des Stomas erforderlich,
subglottische Stenose.
Minitracheotomie
Bei diesem Verfahren wird – wie bei der Koniotomie – durch die Membrana cricothyroidea des Kehlkopfs zwischen Schild- und Ringknorpel perkutan eine dünne Kanüle in die Trachea vorgeschoben. Über die Kanüle kann der spontan atmende Patient endotracheal abgesaugt werden. Eine O2-Zufuhr über die Kanüle ist ebenfalls möglich. Für das Absaugen der Trachea werden Absaugkatheter der Größe 10 Charr verwendet.
Praktisches Vorgehen
Spezielles (Mini-Trach-Set) und allgemeines Zubehör bereitstellen.
Den Patienten über die geplante Maßnahme informieren, dann mit überstrecktem Kopf lagern, bei Bedarf Kissen unter die Schultern legen.
Vorderen Halsbereich desinfizieren und steril abdecken.
Evtl. Lokalanästhesie der Punktionsstelle.
Quere Inzision der Haut über der Punktionsstelle mit dem Skalpell, dann Vorschieben der Einführhilfe durch die Membrana cricothyroidea in die Luftröhre.
Kanüle über die Einführhilfe vorschieben.
Bei korrekter Lage Einführhilfe entfernen und Kanüle fixieren.
Überwachung der Trachealkanüle und des Tracheostomas
Die Grundsätze der Tubuspflege gelten auch für die Trachealkanüle (Abschn. 55.1.4):
Durchgängigkeit der Trachealkanüle jederzeit erhalten,
Cuffdruck kontrollieren, zu hohe Cuffdrücke aber auch Undichtigkeiten der Manschette vermeiden.
Bei nicht zu behebender Verlegung der Trachealkanüle muss die Kanüle sofort herausgezogen und der Patient mit dem Atembeutel über eine Gesichtsmaske beatmet werden. Hierzu muss das offene Tracheostoma luftdicht mit einer Kompresse abgedeckt werden. Anschließend wird entweder orotracheal intubiert oder eine neue Trachealkanüle eingeführt.
Praktisches Vorgehen
Hände desinfizieren, sterile Handschuhe anziehen.
Verunreinigten Tracheostomaverband entfernen. Haut um das Stoma herum mit 0,9%iger NaCl-Lösung reinigen und bei Bedarf mit einem geeigneten Mittel desinfizieren. Danach Haut mit sterilen Tupfern trocknen.
Tracheostomaverband (nichtfasernde Schlitzkompresse) anlegen; Kanüle hierbei nicht herausreißen.
Stoffbänder durch die seitlichen Öffnungen der Kanüle ziehen und festknoten; dann um den Hals herumführen und seitlich miteinander verbinden. Band nicht zu locker befestigen, sonst gleitet die Kanüle in der Trachea auf- und abwärts.
Liegt eine Doppelkanüle, so ist die Pflege mit der oben beschriebenen Technik identisch. Zusätzlich wird die innere Kanüle nach Herstellerangaben herausgezogen und wieder eingesetzt. Solange die innere Kanüle entfernt ist, muss ein Adapter auf die äußere Kanüle gesetzt werden, damit das Beatmungsgerät angeschlossen werden kann. Am günstigsten ist es, die innere Kanüle durch eine andere zu ersetzen (teuer).
Kanülenwechsel
Innerhalb der ersten 48 h nach der konventionellen Tracheotomie darf die Trachealkanüle nicht ohne vitale Indikation gewechselt werden, da sich noch kein richtiger Kanal gebildet hat. Hierdurch besteht die Gefahr, dass nach der Dekanülierung die neue Kanüle nicht mehr eingesetzt werden kann. Die Folge ist Erstickungsgefahr.
Im Gegensatz zur konventionellen Tracheotomie ist das Tracheostoma bei der Dilatationstracheotomie in den ersten Tagen sehr instabil und kollabiert sehr rasch nach Entfernung der Trachealkanüle. Meist gelingt es dann nicht, die Kanüle erneut einzuführen. Wegen dieser Gefahr sollte ein elektiver Kanülenwechsel erst 7 Tage nach der Dilatationstracheotomie erfolgen.
Bei versehentlicher Dekanülierung muss der Patient umgehend orotracheal intubiert werden. Die erneute Kanülierung sollte danach vorsichtshalber über einen Dilatator erfolgen.
Zubehör für den Kanülenwechsel
Trachealkanülen, Kanülenband, Blockerspritze
Trachealspreizer
Einführungsmandrin
Lichtstarke Lampe
Notfallintubationsbesteck
Sterile Absaugkatheter
Sterile Einmalhandschuhe
Steriles Abdecktuch
Sterile Tupfer, Watteträger und Schlitzkompressen
Hautdesinfektionsmittel
Praktisches Vorgehen
Trachealkanülen werden im Allgemeinen nach Bedarf bzw. 1- bis 2-mal pro Woche gewechselt. Vor Kanülenwechsel 4 h Nahrungskarenz.
Der erste Kanülenwechsel erfolgt durch den Arzt, weitere Wechsel durch 1–2 erfahrene Fachpflegepersonen; Anfänger werden angeleitet. Pflegende müssen mit der Technik des Kanülenwechsels vertraut sein, damit sie bei Dekanülierung oder Obstruktion sofort richtig reagieren können.
Erforderliche Ausrüstung einschließlich Lampe und Notfallbesteck in Bettnähe aufbauen. Dichtigkeit der neuen Manschette überprüfen.
Patient absaugen, präoxygenieren (Pulsoxymeterkontrolle!), Oberkörper (20)–30–40° erhöht lagern, Kopf leicht überstrecken.
Alte Kanüle entfernen.
Neue Kanüle behutsam durch das Tracheostoma einführen. Fehllagen unbedingt vermeiden.
Manschette langsam blocken, Beatmungsgerät anschließen, Lungen auf seitengleiche Belüftung auskultieren.
Gelingt das Einführen der Kanüle nicht auf Anhieb, kann eine Einführungshilfe verwendet oder zunächst oral intubiert werden: hierbei muss die Tubusmanschette unterhalb des Tracheostomas liegen. Als Alternative wird das Stoma mit einer sterilen Platte abgedeckt, sodass der Patient mit Beutel und Maske beatmet werden kann. Anschließend wird ein neuer Versuch unternommen.
Entfernen der Trachealkanüle
Für das Entfernen der Trachealkanüle beim Intensivpatienten gelten die gleichen Grundsätze wie für das Entfernen des Endotrachealtubus; auch das Vorgehen ist ähnlich.
Praktisches Vorgehen
Patienten über die geplanten Maßnahmen informieren,
4-stündige Nahrungskarenz vor dem Entfernen der Kanüle,
Mund-Rachen-Raum gründlich absaugen,
Oberkörper hoch lagern,
Trachealkanüle entblocken und herausziehen,
Zunächst Sauerstoff über Gesichtsmaske zuführen,
Wunde mit einem sterilen Verband abdecken,
Epithelialisiertes Tracheostoma chirurgisch mit Naht verschließen (Analgesie beachten!), anschließend steriler Verband,
Verbandwechsel zunächst 1-mal pro Tag,
Bei anhaltender Heiserkeit und Schluckstörungen: HNO-Kontrolle.
Lungenpflege
Die Lungenpflege spielt beim intubierten und beatmeten Patienten eine zentrale Rolle. Durch die endotracheale Intubation werden physiologische Funktionen des oberen Respirationstraktes wie Anfeuchtung, Erwärmung, Filterung und Reinigung der Atemluft ausgeschaltet. Der Hustenmechanismus ist meist gestört oder eingeschränkt; durch die relative Immobilisierung des Patienten wird der Sekretverhalt in den Bronchien gefördert und die Entstehung hypostatischer Atelektasen begünstigt.
Insgesamt kann – paradoxerweise – die respiratorische Therapie den pulmonalen Gasaustausch verschlechtern. Diese unerwünschten Nebeneffekte müssen durch Pflegemaßnahmen und Prophylaxen verhindert werden. Diese Maßnahmen umfassen v. a.:
Anfeuchtung und Erwärmung der Atemluft,
Absaugen des Bronchialsekretes,
physikalische Atemtherapie.
Die theoretischen Grundlagen dieser Maßnahmen sind in den entsprechenden Kapiteln beschrieben.
Zur Überwachung und Therapiekontrolle der Lungenpflege muss das Intensivpflegepersonal die Grundprinzipien der Thoraxuntersuchung beherrschen.
Untersuchung des Thorax
Die klinische Untersuchung des Thorax umfasst folgende Maßnahmen:
Inspektion,
Palpation,
Perkussion,
Auskultation.
Inspektion des Thorax
Bei der Inspektion des Thorax wird v. a. auf folgende Faktoren geachtet:
Atemfrequenz,
Atemtyp,
verminderte Beweglichkeit einer Thoraxseite,
paradoxe Beweglichkeit der Thoraxwand.
Atemfrequenz
Die Atemfrequenz beträgt in Ruhe beim Erwachsenen etwa 12–20/min. Sie ist u. a. gesteigert bei: Fieber, Lungenerkrankungen, Lungenödem oder Erregung.
Atemtyp
Der Rhythmus der normalen Atmung ist relativ gleichmäßig. Pathologische Atemtypen sind:
Cheyne-Stokes-Atmung : periodisches An- und Abschwellen der Atemtiefe und des Abstandes der einzelnen Atemzüge,
Biot-Atmung : wiederkehrende kurz dauernde Atemstillstände; dazwischen ist die Atmung regelmäßig und normal tief,
Kussmaul-Atmung : regelmäßig und tief; Azidoseatmung,
Maschinenatmung: tiefe und schnelle Atemzüge mit Hyperventilation, z. B. bei Schädel-Hirn-Trauma,
Schnappatmung: 10.1007/978-3-662-50444-4_46.
Verminderte Thoraxbeweglichkeit
Sie tritt u. a. auf bei:
ausgedehnter Infiltration der Lunge,
schmerzhaften Pleuraerkrankungen,
Rippenfrakturen, Rippenprellung,
Atelektase,
Pleuraerguss.
Paradoxe Beweglichkeit
Im Gegensatz zur normalen Atmung wird die Thoraxwand bei der Inspiration paradoxerweise eingezogen, bei Exspiration dagegen vorgewölbt, z. B. bei:
instabilem Thorax, z. B. durch Rippenserienfraktur,
unkoordinierten Zwerchfellbewegungen.
Palpation des Thorax
Hierunter versteht man das Betasten des Thorax. Von besonderer Bedeutung ist in der Intensivmedizin das subkutane Emphysem („Hautemphysem“). Hierbei handelt es sich um eine Luftansammlung im Unterhautgewebe. Bei der Palpation knirscht es unter den Fingern („Schneeballknirschen“). Ursachen können sein:
Pneumothorax bei Verletzung der Pleura parietalis,
Mediastinalemphysem, z. B. durch Bronchusruptur,
Verletzungen von Pleura und Lunge ohne Pneumothorax,
Eintritt von Luft durch eine offene Thoraxwandverletzung.
Die Luft kann sich, besonders unter maschineller Beatmung, über den ganzen Körper ausbreiten. Eine Therapie ist meist nicht erforderlich; es gilt aber:
Bei subkutanem Emphysem muss immer ein Pneumothorax ausgeschlossen werden.
Perkussion des Thorax
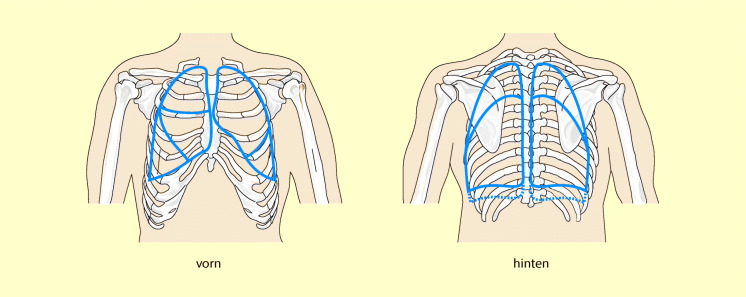
Bei der Perkussion wird die Thoraxwand mit dem Finger beklopft. Dabei schlägt der Mittelfinger der rechten Hand auf das Endglied des linken Mittelfingers (Abb. 55.9). Bei der vergleichenden Perkussion werden immer entsprechende Punkte auf beiden Thoraxseiten beklopft. Durch Perkussion sollen pathologische Veränderungen innerhalb der Thoraxhöhle festgestellt werden.

Normaler Klopfschall wird als sonor bezeichnet. Veränderungen des Klopfschalls sind:
hypersonor: tief, laut, lang (als ob auf eine leere Schachtel geklopft wird); hypersonorer Klopfschall tritt auf bei vermehrtem Luftgehalt des Thorax, z. B. durch Pneumothorax oder Lungenemphysem,
gedämpft: leise, hoch, kurz (als ob auf den Schenkel geklopft wird); gedämpfter Klopfschall entsteht, wenn der Luftgehalt der Lunge vermindert ist, z. B. bei Pleuraerguss, Pneumonie oder Hämatothorax.
Auskultation
Die Auskultation dient dem Erkennen pathologischer Atemgeräusche.
Normales Atemgeräusch
Normales Atemgeräusch entsteht durch Vibrationen. Zwei Arten können unterschieden werden: Vesikuläratmen („Bläschenatmen“) und Bronchialatmen:
Vesikuläratmen: klingt weich und säuselnd, ist während der gesamten Inspiration hörbar, bei der Exspiration ebenfalls, jedoch schwächer. Vesikuläratmen ist über allen Lungenabschnitten zu hören (Ausnahme rechte Lungenspitze: hier bronchiovesikulär).
Bronchialatmen: klingt scharf wie das Fauchen einer Katze. Ist am deutlichsten über der Trachea zu hören und klingt hier während der In- und Exspiration nahezu gleich laut. Außerdem kann man Bronchialatmen leiser über den Hauptbronchien und im Rücken nahe dem 7. HWS-Dornfortsatz hören. An allen anderen Stellen des Thorax ist Bronchialatmen pathologisch.
Rasselgeräusche
Rasselgeräusche sind pathologisch; sie entstehen zusätzlich zum normalen Atemgeräusch. Zwei Arten werden unterschieden: trockene Rasselgeräusche und feuchte Rasselgeräusche.
Trockene Rasselgeräusche: Sie entstehen, wenn Luft durch Bronchien strömt, die durch Sekretmembranen oder Sekretfäden verengt sind. Sie werden auch als bronchitische Rasselgeräusche bezeichnet und sind während des gesamten Atemzyklus hörbar, während der Exspiration sogar meist deutlicher. Sie klingen wie Brummen, Schnurren, Pfeifen, Giemen. Exspiratorisches Giemen ist auch beim Bronchospasmus zu hören. Trockene Rasselgeräusche sind typisch für den nicht abgesaugten Intensivpatienten; in der Allgemeinmedizin typisch für Bronchitis.
- Feuchte Rasselgeräusche: Sie werden nur mit einiger Übung gehört. Sie entstehen, wenn Luft durch dünnflüssige Sekrete im Tracheobronchialbaum und in den Alveolen strömt. Sie wechseln in Größe, Verteilung, Lautstärke usw., je nachdem, welche Art von Sekret vorliegt und welche Bereiche betroffen sind (Trachea, Bronchien, Bronchiolen, Alveolen). Unterschieden werden:
- feinblasige Rasselgeräusche: scharf, knackend, durch Flüssigkeit in den Alveolen,
- mittelblasige Rasselgeräusche: durch Sekrete in den Bronchiolen,
- grobblasige Rasselgeräusche: laut, gurgelnd; durch Exsudat in Trachea, Bronchien und kleineren Bronchien.
Wichtigste Ursachen: Pneumonie, Lungenödem.
Pleurareiben
Knarrendes Geräusch, bevorzugt während der späten Inspirationsphase und frühen Exspirationsphase. Klingt wie Lederknarren, ist oft von außen mit der Hand fühlbar. Entsteht durch entzündliche Veränderungen der beiden Pleurablätter, die nicht mehr reibungsfrei aufeinander gleiten.
Fehlendes oder abgeschwächtes Atemgeräusch
Wichtigste Ursachen: Atelektase, Pneumothorax, verstopfter Bronchus, Hämatothorax, Pleuraerguss, Pleuraschwarte.
Perkussion und Auskultation können nur dann sinnvoll durchgeführt werden, wenn man die Projektion der Lungengrenzen auf den knöchernen Thorax kennt. Diese sog. Topographie ist in Abb. 55.10 dargestellt.
Untersuchungsbefunde ausgewählter Krankheitsbilder
Sekretverhalt beim Intensivpatienten
Inspektion normal,
Palpation normal,
Klopfschall normal,
trockene Rasselgeräusche über den betroffenen Lungenpartien.
Pneumonie
Schnelle Atmung, Nasenflügeln, Zyanose, evtl. einseitig verminderte Atembewegungen,
gedämpfter Klopfschall, wenn betroffener Bereich ausreichend groß,
Bronchialatmen und feinblasige Rasselgeräusche.
Atelektase
Asymmetrische Atembewegungen, lokale Einziehungen der Thoraxwand,
gedämpfter Klopfschall,
abgeschwächtes Atemgeräusch.
Pleuraerguss
Nachschleppen der erkrankten Seite, Interkostalräume vorgewölbt,
gespannte Interkostalräume,
absolut gedämpfter Klopfschall,
Atemgeräusch stark abgeschwächt oder aufgehoben.
Auch beim Hämatothorax ist der Klopfschall gedämpft und das Atemgeräusch aufgehoben.
Lungenödem (intraalveolär)
Schaumiges, rötlich-tingiertes Sekret,
laute in- und exspiratorische feuchte Rasselgeräusche, von der Lungenspitze bis zur Basis, oft auch exspiratorisches Giemen. Bei subakutem Verlauf häufig auch feinblasige Rasselgeräusche über der Lungenbasis.
Der Arzt ist umgehend zu benachrichtigen bei akutem Auftreten oder Verdacht auf:
Pneumothorax
Hämatothorax
Lungenödem
Schwere Atelektase
Bronchusobstruktion
Über Anfeuchtung und Erwärmung der Atemluft: 10.1007/978-3-662-50444-4_54.
Endotracheales Absaugen, Bronchialtoilette
Das endotracheale Absaugen bedarf einer strikten Indikationsstellung. Abgesaugt wird der Patient nur, wenn Sekrete vorhanden sind. Ob Sekrete vorhanden sind, wird meist durch Auskultation des Thorax überprüft. Das Absaugen muss strukturiert, unter sterilen Bedingungen und atraumatisch durchgeführt werden. Dabei sind immer sterile Handschuhe und Materialien sowie ein Mund-Nasen-Schutz (zum Selbstschutz) erforderlich.
Offenes Absaugen
Zu unterscheiden ist zwischen offener und geschlossener Absaugung: Bei der offenen Absaugung mit sterilem Einmalkatheter wird der Patient vom Beatmungsgerät diskonnektiert.
Bei der geschlossenen Absaugung ist keine Diskonnektion erforderlich. Der mehrfach zu verwendende Absaugkatheter befindet sich in einer schützenden Ummantelung.
Absaugkatheter
Das Absaugen des Bronchialsystems erfolgt in der Regel mit Einmalkathetern. Hierbei kann zwischen „atraumatischen“ und konventionellen Absaugkathetern unterschieden werden.
Atraumatische Katheter weisen an der Spitze einen ringförmigen Wulst auf. Unmittelbar oberhalb des Wulstes befinden sich zusätzliche kleine Öffnungen, die beim Anschluss an den Sog der Absaugvorrichtung einen Luftkisseneffekt erzeugen Hierdurch sollen das Ansaugen der Schleimhaut verhindert und die Gefahr der Schleimhautschädigung verringert werden.
Konventionelle Absaugkatheter weisen ebenfalls eine zentrale Öffnung auf, jedoch fehlt der Wulst, auch sind seitlich nur 1–2 größere Öffnungen angebracht, um ein Festsaugen an der Trachealwand zu verhindern.
Praktische Grundsätze beim offenen Absaugen
Schwerkranke Patienten werden unmittelbar vor dem Absaugen mit 100%igem O2 präoxygeniert, um die pulmonalen O2-Speicher zu vergrößern und einen schlagartigen Abfall des paO2 während des Absaugens zu verhindern.
Der Absaugkatheter soll nicht größer als 1/3 des inneren Tubusdurchmessers sein. Meist genügt ein 12- oder 14 F-Katheter.
Sterile Technik ist der beste Kontamination- und Infektionsschutz.
Jeder Katheter wird nur einmal verwendet.
Katheter, mit denen zuvor Mund, Nase oder Rachen abgesaugt worden sind, dürfen nicht für das endotracheale Absaugen verwendet werden.
Der Absaugvorgang sollte so zügig wie möglich durchgeführt werden, max. 10–15 s. Zu langes Absaugen kann bei Patienten, die hohe O2-Konzentrationen und/oder PEEP bzw. CPAP benötigen eine bedrohliche Bradykardie auslösen.
Beim Absaugen Pulsoxymeter, EKG-Monitor und den Patienten beobachten!
Material
Absauggerät
Absaugpfanne oder Y-Stück, Fingertip
Steriler Absaugkatheter passender Größe
Sterile Handschuhe
Mundschutz
Spritze mit steriler physiologischer Kochsalzlösung
Praktisches Vorgehen
Patienten ca. 3 min lang mit 100% Sauerstoff präoxygenieren.
Kurz vor dem Absaugen Respiratoralarm vorübergehend unterbrechen.
Katheterverpackung öffnen, dabei Sterilität wahren.
Sterilen Handschuh über die rechte Hand ziehen.
Mit der einen Hand Beatmungsgerät (Swivel-Konnektor) oder T-Stück abnehmen und auf eine sterile Unterlage platzieren legen.
Mit der anderen Hand Absaugkatheter entnehmen und an das Absauggerät anschließen, Absauggerät einschalten.
Wenn erforderlich Tubus mit 1–2 ml NaCl 0,9% benetzen.
Absaugkatheter in den Endotrachealtubus einführen; bei Widerstand nicht gewaltsam vorschieben. Beim Einführen herkömmlicher Katheter nicht absaugen! Bei Verwendung von „Aero-Flow-Kathetern“ wird hingegen auch beim Einführen ein Sog ausgeübt, weil sich hierdurch ein schützendes Luftkissen um die Katheterspitze bilden soll.
Mit dem Daumen Öffnung der Absaugpfanne oder des Y-Stückes verschließen und den Katheter langsam herausziehen.
Absauggerät abstellen.
Handschuh über den Absaugkatheter streifen; beides abwerfen
Patienten an den Respirator anschließen;
Bei Bedarf Lunge manuell blähen (100% O2).
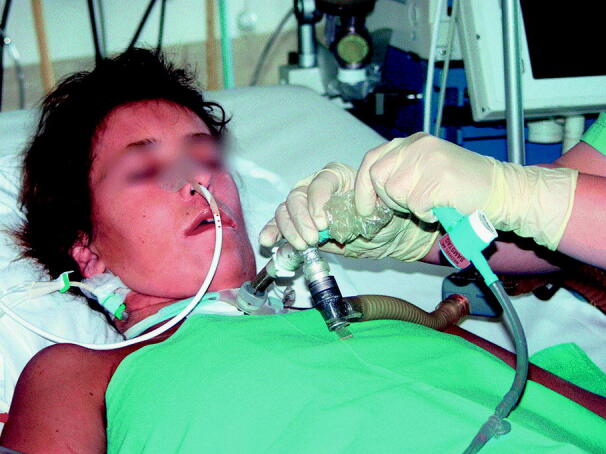
Geschlossene Absaugung
Das geschlossene System (Abb. 55.11) besteht aus einem Ansatzstück mit einer Öffnung für den Tubus oder die Trachealkanüle und einer Öffnung für die Beatmungsschläuche, einem Saugventil mit Anschlussstück für das Absauggerät und einer Schutzhülle, in der sich der sterile Absaugkatheter befindet. Spülungen oder die Gabe von Medikamenten können über die Ansatzstücke oder das Saugventil erfolgen.
Wichtigste Vorteile des geschlossenen Systems sind:
Beatmung wird während des Absaugens fortgeführt, PEEP bleibt erhalten, dadurch größere Sicherheit bei Patienten mit schweren Oxygenierungsstörungen,
ermöglicht Absaugen bei extremen Patientenlagerungen,
schützt den Patienten vor Kreuzinfektionen,
schützt das Personal vor Infektionskrankheiten des Patienten,
ist rascher und weniger aufwendig durchzuführen als das offene Absaugen.
Von Nachteil ist die systembedingte eingeschränkte Beweglichkeit des Patienten.
Indikationen
FiO2 >0,5,
PEEP >6–8 mbar,
Beatmung mit erwünschtem intrinsischen PEEP (z. B. IRV),
Patienten mit Problemkeimen (z. B. Tbc, HIV, MRSA),
Verhinderung von Kreuzinfektionen (z. B. MRSA),
immunsupprimierte Patienten,
voraussichtliche Beatmungsdauer von >48 h,
akutes Lungenödem,
spezielle Lagerungen, z. B. Bauchlage,
sich selbst absaugender Patienten,
Pädiatrie: NO-Beatmung, HFO-Beatmung.
Praktisches Vorgehen
Vorbereitung wie bei offener Absaugung. Auf die Präoxygenierung kann evtl. verzichtet werden.
Absaugkatheter an das geschlossene System anschließen, dabei die Verbindung zum Tubus mit einer Hand festhalten.
Dann Absaugkatheter mit der anderen Hand ohne Sog vorschieben, maximal 0,5–1 cm über die Tubusspitze hinaus.
Sog durch Drücken des Saugventils auslösen und den Katheter vorsichtig in die Ausgangslage zurückziehen.
Spritze mit 5–10 ml steriler 0,9%iger NaCl-Lösung am Spülzugang aufsetzen, Saugventil drücken und Kochsalzlösung langsam einspritzen, um den Katheter durchzuspülen.
Danach Spülzugang verschließen, Katheter diskonnektieren und Sog ausschalten.
Bronchoskopisches Absaugen
Die gezielte Absaugung des Bronchialsystems über ein fiberoptisches oder auch starres Bronchoskop ist v. a. indiziert bei Atelektasen, weiterhin bei der Aspiration von Fremdkörpern oder festem Mageninhalt sowie für die Entnahme von Untersuchungsmaterial aus bestimmten Lungenabschnitten.
Periodisches Blähen der Lunge
Gesunde atmen etwa 6- bis 8-mal in der Stunde in Form von Schnüffeln, Gähnen, Husten oder Seufzen tief ein. Hierdurch werden die Alveolen erweitert und der Surfactant erneut aktiviert. Unter maschineller Beatmung sind diese Mechanismen – auch als Seufzeratmung bezeichnet – aufgehoben. Daher besitzen zahlreiche Respiratoren eine sog. Seufzereinrichtung, über die der Patient mehrmals in der Stunde in wiederkehrenden Abständen mit einem hohen Atemzugvolumen beatmet werden kann. Hierdurch sollen die gleichförmigen Beatmungszüge unterbrochen und die Atelektasen- und Shuntentwicklung verhindert werden. Das Verfahren ist allerdings umstritten, weil der Nutzen nicht belegt ist. „Seufzer“ können jedoch auch mit dem Atembeutel oder mit dem „inspiratory iold“ des Respirators verabreicht werden.
Sputumgewinnung
Je nach ärztlicher Anordnung oder Hygieneprotokoll werden mehrmals in der Woche steril gewonnene Sputumproben für Bakterienkultur- und Empfindlichkeitstests in das Hygienelabor geschickt. Das Sputum wird am besten in spezielle, sterile Auffangvorrichtungen gesaugt, um das Risiko einer Kontamination zu vermindern (10.1007/978-3-662-50444-4_41).
Versehentliche Extubation oder Dekanülierung
Die versehentliche Extubation oder Dekanülierung des beatmeten Patienten ist lebensbedrohlich und erfordert sofortiges Handeln.
Extubation
Nichtspontan atmende Patienten sofort mit Atembeutelmaske (100% O2) beatmen. Um Hilfe rufen (Lebensgefahr!). Reintubation vorbereiten lassen. Erneute Intubation durch einen Erfahrenen.
Dekanülierung
Zunächst wie oben Verfahren, dann sofort Manschette entblocken, Hals des Patienten überstrecken und Kanüle neu einführen.
Gelingt die Rekanülierung nicht auf Anhieb: Tracheostoma abdecken und mit Atembeutelmaske beatmen, bis Arzt eintrifft und das Stoma mit einer neuen Kanüle intubiert.
Extubation
Der Patient wird extubiert, wenn sein klinischer Zustand und die gemessenen Atemgrößen und Blutgaswerte darauf hinweisen, dass er ausreichend spontan atmen und außerdem seine Atemwege selbst freihalten kann.
Praktisches Vorgehen
Patienten vollständig über die geplante Maßnahme aufklären; behutsam auf möglichen Misserfolg hinweisen.
Sämtliches Zubehör für Reintubation bereitstellen und Funktion überprüfen.
Oberkörper des Patienten so hoch wie möglich lagern, Lungen einige Minuten präoxygenieren.
Trachea und Mund sorgfältig absaugen.
Den Patienten maximal tief einatmen lassen, dann Manschette entblocken und Tubus rasch herausziehen. Beim Herausziehen Sekrete, die sich oberhalb des Cuffs angesammelt haben, absaugen!
Patient zum Abhusten auffordern; wenn erforderlich, Rachen absaugen. Oft werden große Mengen Sekret, die bisher oberhalb der Manschette in der Trachea lagen, in die Mundhöhle befördert.
O2-Therapie einleiten, z. B. über Maske.
Wenn erforderlich, atemtherapeutische Maßnahmen fortsetzen,
Dokumentation,
Patientenbeobachtung und -überwachung verstärken.
Footnotes
Unter Mitarbeit von R. Dubb, A. Kaltwasser, T. Müller-Wolff
Contributor Information
Collaborators: Tobias Fink and Tilmann Müller-Wolff
Nachschlagen und Weiterlesen
- [1].Byhan C, Lischke V, Westphal K. Tracheotomie. Indikation und Anwendung in der Intensivmedizin. Berlin Heidelberg: Springer; 2000. [Google Scholar]
- [2].Gründling M, Quintel M. Perkutane Dilatationstracheotomie. Indikationen, Techniken, Komplikationen. Anästhesist. 2005;54:929–944. doi: 10.1007/s00101-005-0894-2. [DOI] [PubMed] [Google Scholar]
- [3].Gründling M, Kuhn SO, Pavolvic D, Feyerherd F, Wendt M. Atemwegsmanagement bei Dilatationstracheotomie. Anästh Intensivmed. 2006;47:505–514. [Google Scholar]
- [4].Kaltwasser A, Dubb R, Pavolvic D, Feyerherd F, Wendt M. Atemwegsmanagement bei Dilatationstracheotomie. Anästh Intensivmed. 2006;47:505–514. [Google Scholar]
- [5].Klemm E, Nowak A. Kompendium der Tracheotomie. Berlin Heidelberg: Springer; 2011. [Google Scholar]
Internet
- [6].Komplikationen und Schäden durch Intubation. Literaturzusammenstellung. www.Ima-deutschland.de/download.php?id=23099,281,1