Abstract
目的
探讨临床药师开展万古霉素个体化药学服务的临床价值,初步建立万古霉素临床监测流程。
方法
收集2017年1月~2018年12月期间开展万古霉素个体化药学服务(试验组:144例)和未开展药学服务(对照组:884例)的病例资料,基于纳入排除标准和倾向评分匹配法,筛选出两组基线数据保持基本一致的患者病例纳入研究(每组各62例,共124例),统计比较试验组和对照组之间的疗效、安全性和经济性指标。
结果
疗效比较时,试验组治疗效果总有效率绝对值(95.16% vs 91.94%)大于对照组,但差异无统计学意义(P>0.05);两组之间使用万古霉素前中性粒细胞分类比例和使用后降钙素原差异有统计学意义(P < 0.05)。安全性比较时,试验组不良反应发生率绝对值低于对照组(8.06% < 9.68%)但其差异无统计学意义(P>0.05);两组之间使用万古霉素后肌酐差异有统计学意义(P < 0.05)。经济性比较时,用药天数、万古霉素费用及费用占比差异有统计学意义(P < 0.05);成本—效果分析试验组经济性优于对照组(50052.78 vs 57601.23);万古霉素使用强度试验组使用强度低于对照组(0.11 < 0.36)。
结论
临床药师的参与可提高万古霉素的临床获益,建立的万古霉素临床监测流程值得推荐。
Keywords: 万古霉素, 倾向评分匹配, 临床价值, 成本—效果分析
Abstract
Objective
To assess the clinical value of individualized pharmaceutical services for patients receiving vancomycin for severe infections and establish clinical monitoring procedures during vancomycin treatment.
Methods
Data were collected from patients with severe infections who received vancomycin treatment with individualized pharmacy services (test group, 144 cases) or without such services (control group, 884 cases) between January, 2017 and December, 2018. Using propensity score matching, the patients in the two groups with comparable baseline data were selected for inclusion in the study (62 in each group), and the efficacy, safety and economic indicators were compared between the two groups.
Results
The curative effects of the treatment did not differ significantly between the two groups, with the overall response rates of 95.16% in the test group and 91.94% in the control group (P > 0.05). The percentage of neutrophils before vancomycin treatment and calcitonin level after the treatment differed significantly between the two groups (P < 0.05). No significant difference was found in the incidence of adverse events associated with the treatment between the test and control groups (8.06% vs 9.68%, P > 0.05); a significant difference in creatinine level was noted between the two groups after vancomycin treatment (P < 0.05). The number of days of medication, the cost of vancomycin and its proportion in the total expenses differed significantly between the two groups (P < 0.05). Cost-effectiveness analysis showed a better cost-effectiveness in the test group than in the control group (50052.78 vs 57601.23). The intensity of vancomycin use was also lower in the test group than in the control group (0.11 vs 0.36).
Conclusion
The participation of clinical pharmacists during the treatment can improve the clinical benefits of vancomycin in patients with severe infections.
Keywords: vancomycin, propensity score matching, clinical value, cost-effectiveness analysis
为积极响应《医疗机构药事管理暂行规定》[1]政策的号召,我院进行了多种药物的临床药学服务。因首个糖肽类抗菌药物万古霉素[2]的疗效和不良反应与药物的血药浓度密切相关,但是在临床治疗过程中发现了万古霉素血药浓度之间存在个体差异[3],受年龄、体重、给药剂量、血清白蛋白、肌酐清除率、胱抑素C、重症感染、高血压等[4-8]因素的影响,同时对于重症感染这一类危重症患者来说,其特殊的病理及生理状态,导致万古霉素药动学方面产生了差异,如何开展科学合理的万古霉素个体化用药已成为临床上亟待解决的问题[9],所以我院临床药师为重症感染并使用万古霉素治疗的患者提供了个体化的用药指导。
临床药师开展万古霉素个体化药学服务虽然有一定实际意义,但临床药师开展个体化药学服务需要进行血药浓度监测、用药监护、用药教育、用药剂量调整等服务,在中国只有血药浓度监测可以收费(约100元/次),而临床药师开展的其他服务内容无法收取相关费用,因此开展个体化药学服务对于患者是否获益以及临床药师存在的必要性在中国还存在较大的争议。
目前国内缺乏对临床药师干预重症感染患者万古霉素治疗过程的临床获益相关研究。本研究拟选取2017年1月~2018年12月期间重症感染患者接受万古霉素治疗的真实世界数据,采用倾向评分匹配(PSM)用于平衡试验组和对照组之间的混杂因素,对两组之间的疗效、安全性及经济性指标进行比较,用于评估临床药师是否可以在重症感染患者的万古霉素治疗中发挥积极作用,为临床药师参与万古霉素临床合理使用提供理论依据和支持,并初步建立万古霉素临床监测流程。
1. 资料和方法
1.1. 研究对象及分组
2017年1月~2018年12月期间在蚌埠医学院第一附属医院住院并接受万古霉素治疗的重症感染患者。根据患者在住院期间是否接受临床药师开展万古霉素个体化药学服务,分为试验组和对照组,试验组为接受临床药师药学服务,对照组为未接受药学服务。
1.2. 伦理与临床试验注册
该研究获得了蚌埠医学院第一附属医院临床医学研究伦理委员会的伦理批准(科研项目批准文号:2018KY008),并在中国临床试验注册中心进行了试验注册(注册号:ChiCTR1900025803)。
1.3. 万古霉素个体化药学服务指引
所有患者被分为两组,即试验组和对照组,试验组患者由临床药师依据万古霉素药物使用说明书、《万古霉素临床应用剂量中国专家共识》[9]、2011年《万古霉素临床应用中国专家共识》[10]、《万古霉素个体化给药临床药师指引》[2]和2016年《中国万古霉素治疗药物监测指南》[11]等相关指南并结合患者实际情况,进行万古霉素血药浓度监测并给予个体化用药指导,对照组患者仅在住院期间接受过万古霉素治疗但并未开展个体化药学服务,临床药师监测流程图如图 1所示。
1.

临床药师监测流程图
Flow chart of clinical monitoring of vancomycin use by pharmacists.
1.4. 纳入排除标准
纳入标准:(1)纳入的患者均为重症感染患者(APACHE Ⅱ评分 > 15分);(2)试验组为接受万古霉素血药浓度监测并给予个体化用药指导的住院患者,对照组为临床药师未干预的住院患者;(3)试验组收集的血药浓度数据为万古霉素的谷浓度,而非峰浓度或给药后立即监测的浓度;(4)用于匹配的临床资料完整;(5)性别、入院科室不限;(6)患者疾病种类不限。
排除标准:(1)试验组监测的万古霉素血药浓度为峰值浓度;(2)万古霉素尚未在临床治疗中用于治疗感染;(3)患者用于匹配的一些基本信息丢失和/或临床数据不完整;(4)局部给药的患者;(5)围术期临时预防用药的患者。
1.5. 资料收集
1.5.1. 混杂因素
根据相关研究[12-14]和临床实际情况确定本次研究的混杂因素有:APACHE Ⅱ评分,性别,年龄,过敏史,吸烟史,酗酒史,输血史,手术及操作次数,体温,入院方式,住院科室,伴随疾病(糖尿病、高血压、冠心病、类风湿性关节炎、心脏病、慢性支气管炎、乙型肝炎和结核),主要感染部位,多重感染,联合用药(碳青霉烯类、β-内酰胺类、氟喹诺酮类、抗真菌类、氨基糖苷类、大环内酯类、糖肽类)。
1.5.2. 结局指标
根据相关研究[12-13, 15-16]和临床专家意见制定的结局指标包括疗效、安全性及经济性3个方面:
1.5.2.1. 疗效指标
治疗效果[17]:依据《医院感染诊断标准》,重症感染患者的治疗效果分为显效、有效和无效。显效,患者治疗后临床疗效确切,无明显不良症状者;有效,患者治疗后各项临床指标均有一定改善,不良症状基本消失;无效,患者治疗后各临床指标和不良症状无改善或者更为严重者。
 |
白细胞计数正常参考值范围:成人(4.0~10.0)×109/L、儿童(5.0~12.0)×109/L、新生儿(15.0~20.0)×109/L;中性粒细胞分类比例正常参考值范围:40%~75%;C反应蛋白正常参考值范围:0~10 mg/L;降钙素原正常参考值范围:成人及儿童 < 0.15 ng/mL、新生儿 < 2 ng/mL。
1.5.2.2. 安全性指标
万古霉素不良反应发生率:根据万古霉素药物使用说明书,万古霉素的不良反应主要有皮疹、恶心、静脉炎、耳鸣、听力减退,肾功能损害、白细胞降低、血清氨基转移酶升高、类过敏反应等。
肌酐正常参考值范围:30~110 μmol/L;尿素正常参考值范围:成人3.2~7.1 mmol/L、儿童1.8~6.5 mmol/L;胱抑素C正常参考值范围:0.51~1.09 mg/L;尿酸正常参考值范围:男149~416 μmol/L、女89~357 μmol/L。
1.5.2.3. 经济性指标
万古霉素用药天数;患者住院天数;万古霉素药品费用;总成本;以及用于计算万古霉素抗菌药物使用强度的万古霉素使用剂量。
总成本=综合医疗服务费+诊断类费用+治疗类费用+康复费+中医治疗费+西药费+中药类费用+血液和血液制品类费用+耗材类费用+其他费用=总费用
综合医疗服务费:一般医疗服务费、一般治疗操作费、护理费和其他费用
诊断类费用:病理诊断费、实验室诊断费、影像学诊断费和临床诊断项目费
治疗类费用:非手术治疗项目费,包括临床物理治疗费在内;手术治疗费,包括麻醉费和手术费在内
西药费:包括抗菌药物费用在内
中药类费用:中成药费和中草药费
血液和血液制品类费用:血费、白蛋白类制品费、球蛋白类制品费、凝血因子类制品费和细胞因子类制品费
耗材类费用:检查用一次性医用材料费、治疗用一次性医用材料费和手术用一次性医用材料费。
1.6. 数据的标准化
统计分析之前需要对数据库进行标准化[18-19]。标准化过程包括从患者基本信息中删除重复数据,对处方条款进行标准化,对剂量单位进行标准化以及对各种检验指标进行标准化。标准化的目的是确保:有关研究患者的信息的唯一性;信息表之间的相关性;以及药物单位和检验结果的有效性,以便进行完整而有效的分析。
1.7. 结局指标评价方法
本研究的临床综合价值(结局指标)从3个方面进行评价,分别为疗效、安全性和经济性。在疗效及安全性分析中,分别对试验组与对照组万古霉素使用前后的有效率、不良反应发生率及达标率进行统计分析,其中有效率等于显效例数加上有效例数占总组例数的比例,不良反应发生率等于发生不良反应的例数占总组例数的比例,达标率等于达到正常参考值范围的例数占总组例数的比例。经济性指标中除对万古霉素用药天数、患者住院天数及其占比,万古霉素的治疗费用、患者住院期间总成本及其占比进行比较外,还增加了两组间万古霉素抗菌药物使用强度及成本—效果的比较。
由于经济学成本中的间接成本(因伤病或死亡所造成的工资损失)及隐性成本(因疾病引起的疼痛,精神上的痛苦、紧张和不安,生活与行动的某些不便,或因诊断治疗过程中带来的担忧、痛苦等)较难统计,故本次研究统计的均为可以直接通过医院HIS系统收集到的直接成本(包括直接医疗成本和直接非医疗成本)。其中万古霉素抗菌药物使用强度通过统计两组的万古霉素使用剂量,通过公式1(万古霉素DDD=2.0 g),计算两组的万古霉素抗菌药物使用强度,值较低组,抗菌药物使用强度越低;成本—效果比通过两组的总成本和有效率,求两者之间的比例,即成本—效果比,比值越小说明在相同的治疗效果下,使用的费用越低,则经济性越强,成本增加的同时,效果反而下降,则经济性较弱,同时为减少不确定因素对结果的影响,进行了±10%的成本—效果敏感度分析。
 |
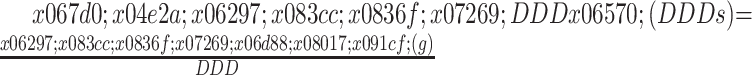 |
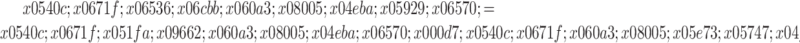 |
公式1 |
1.8. 统计分析
本研究的采用R4.0.0进行倾向评分匹配,匹配法采用1:1最近邻匹配法,匹配容差设置为0.03;使用IBM SPSS 25.0进行统计学处理,计量资料先进行正态分布分析,符合或近似正态分布的计量资料表示为平均值±标准差,采用t检验比较各指标组间差异性;不符合正态分布的计量资料以中位数(四分位数)[M(P25,P75)]表示,采用Mann-Whitney U检验比较各组间差异性,计数资料均用百分比表示,各组之间的比较采用χ2检验。P < 0.05表示差异具有统计学意义。
2. 结果
2.1. 患者纳入和倾向评分匹配结果
在2017年1月~2018年12月期间,重症感染患者接受万古霉素治疗的患者共有1028例,完全遵循万古霉素个体化给药临床药师指引原则的有144例,纳入试验组;未开展万古霉素治疗药物监测仅凭临床医生经验给药或未完全遵循个体化药学服务的共884例,纳入对照组。通过制定的纳入排除标准筛选后,试验组143例,对照组319例。对试验组与对照组通过倾向评分匹配(匹配容差:0.03)两组间的混杂因素后,两组各保留62例。
2.2. 倾向评分匹配前后的患者基线数据
分别对PSM前后的各混杂因素进行统计学分析(表 1)。在PSM前存在9个混杂因素有统计学差异(P < 0.05),PSM后各变量明显趋于一致,差异均无统计学意义(P > 0.05,图 2、3)。
1.
匹配前后患者基线数据的比较
Comparison of baseline data of patients before and after propensity score matching (PSM)
| Mixed factors (%) | Baseline data for patients before PSM | Baseline data for patients after PSM | |||||
| Test group (n=143) | Control group (n=319) | P | Test group (n=62) | Control group (n=62) | P | ||
| APACHE II | 36.00 (27.00, 41.50) | 31.00 (22.00, 40.00) | 0.013 | 33.53±9.36 | 32.65±10.79 | 0.629 | |
| Gender | 0.010 | 0.549 | |||||
| Male | 103 (72.03) | 190 (59.56) | 43 (69.35) | 46(74.19) | |||
| Female | 40 (27.97) | 129 (40.44) | 19 (30.65) | 16 (25.81) | |||
| Age (year) | 49.00 (4.50, 64.00) | 52.00 (42.00, 65.50) | 0.007 | 50.50 (14.75, 66.00) | 46.50 (25.50, 61.50) | 0.429 | |
| Allergy | 15 (10.49) | 29 (9.10) | 0.636 | 4 (6.45) | 3 (4.83) | 1.000 | |
| Smoking | 23 (16.08) | 30 (9.40) | 0.037 | 9 (14.52) | 10 (16.13) | 0.803 | |
| Alcoholism | 15 (10.49) | 26 (8.15) | 0.414 | 8 (12.90) | 10 (16.13) | 0.610 | |
| Blood | 43 (30.07) | 87 (27.27) | 0.537 | 20 (32.26) | 20 (32.26) | 1.000 | |
| Times | 0.704 | 0.905 | |||||
| < 2 | 84 (58.74) | 185 (57.99) | 37 (59.68) | 38 (61.29) | |||
| 2-4 | 36 (25.17) | 90 (28.21) | 16 (25.81) | 14 (22.58) | |||
| > 4 | 23 (16.08) | 44 (13.79) | 9 (14.52) | 10 (16.13) | |||
| Temperature (℃) | 37.80 (37.05, 38.50) | 37.60 (36.80, 38.50) | 0.188 | 37.93±0.97 | 37.99±1.04 | 0.737 | |
| Admission | 0.00 | 1.000 | |||||
| Emergency | 41 (28.67) | 37 (11.60) | 16 (25.81) | 16 (25.81) | |||
| Outpatient | 102 (71.33) | 282 (88.40) | 46(74.19) | 46(74.19) | |||
| Department | 0.00 | 0.684 | |||||
| Respiratory | 40 (27.97) | 10(3.13) | 12 (19.35) | 10 (16.13) | |||
| ICU | 37 (25.87) | 25 (78.37) | 10 (16.13) | 16 (25.81) | |||
| Pediatrics | 36 (25.17) | 15 (4.70) | 15 (24.19) | 12 (19.35) | |||
| Infectious | 9 (6.29) | 34 (10.66) | 7(11.29) | 9 (14.52) | |||
| Neurology | 7 (4.90) | 75 (23.51) | 7(11.29) | 8 (12.90) | |||
| Other | 14 (9.79) | 160 (50.16) | 11 (17.74) | 7 (11.29) | |||
| Disease | |||||||
| Diabetes | 21 (14.69) | 31 (9.72) | 0.118 | 6 (9.68) | 7 (11.29) | 0.769 | |
| Hypertension | 30 (20.98) | 107 (33.54) | 0.006 | 14 (22.58) | 17 (27.42) | 0.534 | |
| Coronary | 2 (1.40) | 13 (4.08) | 0.224 | 2 (3.23) | 2 (3.23) | 1.000 | |
| Rheumatoid | 5 (3.50) | 5 (1.57) | 0.331 | 2 (3.23) | 1 (1.61) | 1.000 | |
| Heart | 6 (4.20) | 7 (2.19) | 0.369 | 3 (4.83) | 0 (0.00) | 0.244 | |
| Bronchitis | 4 (2.80) | 3 (0.94) | 0.272 | 0 (0.00) | 1 (1.61) | 1.000 | |
| Hepatitis | 6 (4.20) | 4 (1.25) | 0.096 | 4 (6.45) | 2 (3.23) | 0.676 | |
| Tuberculosis | 9 (6.29) | 3 (0.94) | 0.002 | 1 (1.61) | 2 (3.23) | 1.000 | |
| Site | 0.00 | 0.906 | |||||
| Lung | 83 (58.04) | 111 (34.80) | 38 (61.29) | 32 (51.61) | |||
| Celiac | 7 (4.90) | 11 (3.45) | 3 (4.83) | 3 (4.83) | |||
| Intracranial | 20 (13.99) | 79 (24.76) | 12 (19.35) | 14 (22.58) | |||
| Urinary | 3 (2.10) | 5 (1.57) | 2 (3.23) | 1 (1.61) | |||
| Nervous | 6 (4.20) | 5 (1.57) | 2 (3.23) | 3 (4.83) | |||
| Intrauterine | 20 (13.99) | 6(1.88) | 3 (4.83) | 5 (8.06) | |||
| Incision | 1 (0.70) | 90(28.21) | 1 (1.61) | 3 (4.83) | |||
| Bloodstream | 2 (1.40) | 2 (0.63) | 1 (1.61) | 1 (1.61) | |||
| Other | 1 (0.70) | 10(3.13) | 0 (0.00) | 0 (0.00) | |||
| Multiple | 17(11.89) | 33 (10.34) | 0.622 | 9(14.52) | 13 (20.97) | 0.347 | |
| Medicine | |||||||
| Carbapenems | 28 (19.58) | 84 (26.33) | 0.117 | 13 (20.97) | 16 (25.81) | 0.524 | |
| Lactams | 12 (8.39) | 33 (10.34) | 0.513 | 6 (9.68) | 4 (6.45) | 0.510 | |
| Fluoroquinolones | 8 (5.59) | 24 (7.52) | 0.450 | 3 (4.83) | 3 (4.83) | 1.000 | |
| Antifungal | 3 (2.10) | 4 (1.25) | 0.784 | 1 (1.61) | 1 (1.61) | 1.000 | |
| Aminoglycosides | 7 (4.90) | 19 (5.96) | 0.647 | 3 (4.83) | 4 (6.45) | 1.000 | |
| Macrolides | 3 (2.10) | 1(0.31) | 0.170 | 1 (1.61) | 1 (1.61) | 1.000 | |
| Glycopeptides | 2 (1.40) | 0 (0.00) | 0.095 | 0 (0.00) | 0 (0.00) | - | |
2.

匹配前后倾向得分的分布图
Distribution map of propensity scores before and after matching.
3.
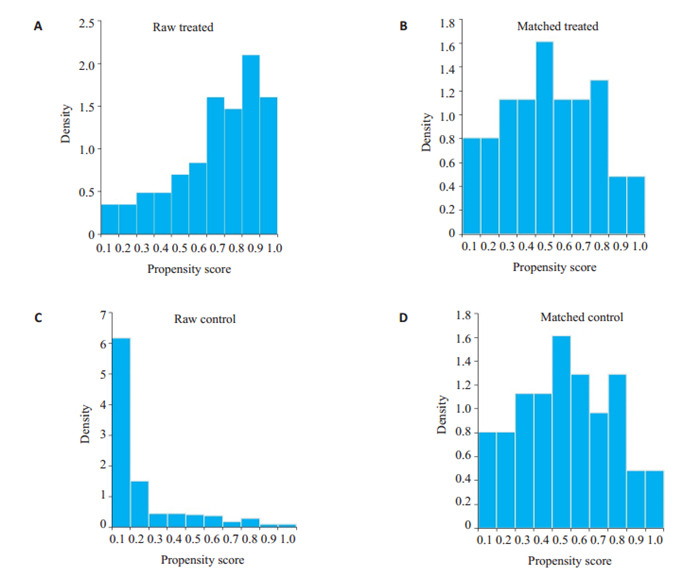
匹配前后倾向得分密度分布图
Propensity score density distribution map before and after matching.
2.3. 疗效比较
治疗效果方面,试验组显效20例(32.26%)、有效39例(62.90%)、无效3例(4.84%),总有效率为95.16%;对照组显效5例(8.06%)、有效52例(83.87%)、无效5例(8.06%),总有效率为91.94%,治疗效果总有效率试验组大于对照组,但两组之间无统计学差异(P > 0.05)。其余4项指标,组内(患者接受万古霉素治疗前后的检测指标之间)和组间(试验组和对照组之间)比较结果如表 2所示。
2.
组间和组内疗效比较
Comparison of therapeutic efficacy between and within the two groups
| Outcome indicators | Medication node | Group | P | ||
| Test | Control | ||||
| White blood cell count (109/L) | |||||
| Before | 12.53 (6.83, 18.81) 32.26% |
10.19(7.05, 15.21) 37.10% |
0.292 | ||
| After | 7.77 (5.70, 11.20) 64.52% |
7.61 (5.30, 12.11) 43.55% |
0.901 | ||
| P | 0.003 | 0.039 | |||
| Neutrophil (%) | |||||
| Before | 82.75 (69.10, 90.28) 29.03% |
77.35 (60.15, 84.88) 33.87% |
0.024 | ||
| After | 66.29±16.03 62.90% |
70.05 (56.08, 81.05) 43.55% |
0.642 | ||
| P | 0.00 | 0.139 | |||
| C-reactive protein (mg/r) | |||||
| Before | 77.84 (7.80, 90.00) 29.03% |
28.51 (5.64, 74.75) 29.03% |
0.069 | ||
| After | 24.30 (5.50, 79.00) 37.10% |
20.10(3.50, 65.10) 40.23% |
0.310 | ||
| P | 0.098 | 0.385 | |||
| Procalcitonin(ng/mL) | |||||
| Before | 1.02 (0.19, 5.68) 20.97% |
1.10(0.15, 6.16) 29.03% |
0.851 | ||
| After | 0.11 (0.050.14) 82.26% |
0.28(20, 4.18) 43.55% |
0.00 | ||
| P | 0.00 | 0.072 | |||
2.4. 安全性比较
试验组不良反应发生率为8.06%,共5例,肾功能损害(衰竭)3例,发热1例,转氨酶升高1例,其中3例换为其它抗生素进行治疗,1例进行了万古霉素减量治疗,1例使用了异甘草酸镁进行了保肝治疗;对照组不良反应发生率为9.68%,共6例,肾功能损害(衰竭)2例,皮疹1例,白细胞降低2例,红颈综合症1例,其中4例换为其它抗生素进行治疗,1例进行了万古霉素减量治疗,1例使用了西替利嗪进行了抗过敏治疗,两组之间无统计学差异(P > 0.05)。其余指标组内和组间比较结果如表 3所示。
3.
组间和组内安全性比较
Comparison of safety between and within the two groups
| Outcome indicators | Medication node | Group | P | |
| Test | Control | |||
| Creatinine (μmol/L) | ||||
| Before | 60.50 (52.00, 83.25) 79.03% |
59.00 (43.50, 69.75) 85.48% |
0.133 | |
| After | 62.00 (52.78, 71.50) 87.10% |
54.00 (41.25, 66.75) 87.10% |
0.034 | |
| P | 0.730 | 0.217 | ||
| Urea (mmol/L) | ||||
| Before | 5.09 (3.49, 7.12) 62.90% |
4.39 (3.67, 5.81) 83.87% |
0.233 | |
| After | 4.49 (3.11, 6.22) 61.29% |
4.56 (3.00, 6.05) 61.29% |
0.509 | |
| P | 0.103 | 0.838 | ||
| Cystatin C (mg/L) | ||||
| Before | 1.46 (0.91, 2.01) 25.81% |
1.27 (0.95, 1.70) 32.26% |
0.500 | |
| After | 1.10 (0.78, 1.46) 45.16% |
1.18 (1.00, 1.52) 35.48% |
0.188 | |
| P | 0.032 | 0.386 | ||
| Uric acid (μmol/L) | ||||
| Before | 263.00 (175.00, 327.50) 72.58% |
217.50 (151.75, 309.00) 66.13% |
0.224 | |
| After | 211.00 (138.25, 320.25) 72.58% |
175.50 (129.25, 290.25) 69.35% |
0.318 | |
| P | 0.125 | 0.189 | ||
2.5. 经济性比较
经济性比较时,结果均采用均数±标准差表示(表 4)。同时统计得出试验组总有效率为95.16%,其中显效率为32.26%(成本:1 098 744.33元),有效率为62.90%(成本:3 664 277.76元);对照组总有效率为91.94%,其中显效率为8.06%(794 453.58元),有效率为83.87%(4 501 403.66元),成本—效果分析中成本为每组显效成本和有效成本之和,效果为总有效率,本次研究根据相关数据进行了成本—效果分析[20-21](表 5)及按±10%进行成本—效果的敏感度分析(表 6)。
4.
组间和组内经济性比较
Comparison of economic parameters between the two groups
| Group | Medication days | Hospitalization days | Proportion | Vancomycin cost (yuan) | Total cost (yuan) | Proportion | AUD |
| AUD: Antibiotics Use Density. | |||||||
| Test | 13.32±8.63 | 29.42±20.09 | 0.52±0.25 | 1517.91±1435.67 | 91 990.19±107 610.00 | 0.04±0.05 | 0.11 |
| Control | 9.60±6.83 | 25.60±20.28 | 0.44±0.22 | 4514.09±3917.56 | 89 254.02±99 700.77 | 0.13±0.21 | 0.36 |
| P | 0.003 | 0.122 | 0.056 | 0.00 | 0.596 | 0.00 | |
5.
两组患者的成本—效果分析
Cost-effectiveness analysis in the two groups
| Group | C (yuan) | E (%) | C/E | ΔC/ΔE |
| ΔC: Ctest-Ccontrol; ΔE: Etest-Econtrol. | ||||
| Test | 4 763 022.09 | 95.16 | 50 052.78 | - |
| Control | 5 295 857.24 | 91.94 | 57 601.23 | -165 476.76 |
6.
两组之间的敏感性分析
Sensitivity analysis in the two groups
| Group | C1/yuan | C2/yuan | E/% | C1/E | C2/E | ΔC1/AE | ΔC2/AE |
| C1: Cost+10%; C2: Cost-10%; ΔC1: C1test-C1control; ΔC2: C2test-C2control; ΔE:Etest-Econtrol. | |||||||
| Test | 5 239 324.30 | 4 286 719.88 | 95.16 | 55 058.05 | 45 047.50 | - | - |
| Control | 5 825 442.96 | 4 766 271.51 | 91.94 | 63 361.35 | 51 841.11 | -182 024.43 | -148 929.08 |
3. 讨论
随着个体化用药的发展,临床药师在各个药物的临床治疗过程中的具体干预流程及作用备受关注。既往文献虽然对临床药师开展万古霉素个体化用药有诸多研究[12-13, 22-26],但与本次研究有众多不同之处,特别是从经济学方面评估临床药师开展个体化药学服务临床价值的研究甚少,但治疗药物监测工作规范专家共识(2019版)指出[27],在开展治疗药物监测时,进行经济学评价是值得被推荐的,同时本研究也进一步证实了治疗药物监测在临床用药中的重要性及对个体化用药的指导意义,最后本次研究在方法学上进行了创新,采用了PSM平衡两组之间的混杂因素。PSM广泛用于大样本,非随机观察性研究[28-30],可以解决随机对照试验的某些伦理和经济问题,尤其是随机对照试验中严格的纳入和排除标准使得研究结果难以推广的问题[31],所获得的结果更具权威性和真实性,适用于更广泛的患者群,更益于推广至临床治疗的大环境中,同时匹配后,除了暴露因素和结果指标外,两组变量应保持平衡并具有可比性,这等效于后随机化,观察到的结果数据将类似于随机分配的数据[32-33],使得本次验机的结论比没有匹配的结果更为可靠。本研究的PSM在一定程度上平衡了混杂因素的影响,图 2和图 3可看出,PSM后的数据更为集中且更接近正态分布,表明匹配效果良好。
在疗效比较中,试验组的总有效率大于对照组;白细胞计数、中性粒细胞分类比例、C反应蛋白和降钙素原等结局指标结果在组内比较时,万古霉素使用后达标率均大于使用前;在组间比较中,除C反应蛋白外,试验组在使用万古霉素后达标率均大于对照组。白细胞计数、中性粒细胞分类比例、C反应蛋白和降钙素原均为临床上常用的细菌感染指标[34-36],用于反映治疗前后和两组患者的细菌清除情况,结果反映了万古霉素能够有效治疗细菌感染,在临床药师参照万古霉素临床监测流程的干预下万古霉素的疗效会更好。这与部分学者[12-13, 22-24, 26]的研究结果相似,但谢玲[12]、闫立国[22]和薛盛敏[23]的研究对象为肾功能损伤患者、儿科和肾功能亢进的特殊人群,孙钟慧[24]的研究主要是通过经典案例分析得出临床药师提供的药学服务可以增加药物治疗的有效性,既往研究与本次研究的结果都表明临床药师的参与能够有效提高住院患者的万古霉素疗效。C反应蛋白的结果与其他指标结果相反的原因可能有:首先,试验组患者的情况更为复杂,干预前的依从率可能远低于对照组。其次,患者的采血时间可能有所不同,这可能导致生化和血常规的改变,从而影响结局指标,最终导致结果出现异常。最后,这项研究中包括的病例数量较少,结局指标分析中可能存在错误。
在安全性比较中,虽然两组之间的不良反应发生率没有统计学差异,且不良反应的发生与药物因素、患者因素和给药因素等众多因素有关,但试验组的不良反应发生率较对照组更低,两组在进行用药调整后不良反应均得到有效改善,说明临床药师在一定程度上可以减轻不良反应的发生。同时据报道[37],万古霉素治疗期间急性肾损伤的发生率可高达40%,同时根据Hermsen及其同事的研究[38],在成人患者中,较高的万古霉素血药浓度与较高的肾毒性有关。因此在万古霉素治疗过程中需密切关注患者的用药安全性,以避免可能导致肾功能损害的风险。本研究选取尿酸、肌酐、尿素和胱抑素C等用于检测肾脏损伤的早期迹象的指标反映重症感染患者在使用万古霉素期间的安全性,特别是半胱氨酸蛋白酶抑制剂C评估了肾功能受损[39],因为Cys C仅通过肾小球滤过被清除,并在近曲小管重吸收后完全代谢分解,不再重返血液中,所以其血液浓度完全取决于肾小球滤过率(GFR),不受性别、年龄、炎症、饮食摄入等因素的影响,是反应肾小球滤过率变化的理想内源性标志物[40-43]。本次研究结果显示使用万古霉素后两组尿素达标率均低于使用前,这可能与万古霉素使用期间出现肾功能损伤有关,但在本次研究中虽然万古霉素使用前试验组的情况较对照组更为复杂,但仍能得出在使用万古霉素后试验组的肌酐、尿素、胱抑素C和尿酸达标率大于或等于对照组,说明临床药师对患者治疗期间的安全性能够起到保护监督作用,既往研究主要通过不良反应发生情况[12, 22, 26]或经典案例[24]分析用药期间的安全性,与本研究的安全性评价方面存在较大区别。为保证用药的安全性,建议以1 g的剂量,每8 h一次的给药频率和每天不超过4 g的剂量给予万古霉素,以使肾功能损害的风险相对较低[44],并随时监测肾功能变化。
目前国内缺乏对重症感染患者万古霉素使用期间的经济学评价。本次研究试验组的用药天数、住院天数及其占比均大于对照组,与谢玲[12]的研究用药疗程(用药天数)干预组大于对照组相符,这可能与试验组纳入的研究对象情况更为复杂有关,但同时也进一步证明了在情况更为复杂的试验组中,由于临床药师的干预,万古霉素的费用明显下降,治疗效果更好,更具经济性。同时本次研究除对常见的直观经济学指标进行分析外,还对两组之间的万古霉素抗菌药物使用强度进行了分析,试验组的AUD值为0.11,对照组的AUD值为0.36,虽然国外有研究表明细菌耐药率与抗菌药物AUD相关性的研究结果差异性较大,耐药原因复杂,受多种因素影响[45],但仍有研究表明细菌耐药率与抗菌药物AUD存在密切的相关性,因为抗菌药物的暴露增加了细菌的耐药率[46],因此试验组的AUD值小于对照组更有利于避免患者出现耐药情况,从而减少万古霉素的使用剂量,降低万古霉素的花费,保证万古霉素的治疗效果。最后本次研究进行的成本—效果分析,根据药物经济学的原理,C/E越小意味着单位效果所需成本越低,该组的经济性越好,△C/△E越小意味着单位增量效果所需追加的成本越低,该组在经济性上实际意义越大,敏感性分析也证实了本次研究试验组的成本降低疗效反而上升,试验组的经济优势更为明显,进一步验证了临床药师的干预有助于提高药物经济性。国外的相关研究[47-48]表明,临床药师的干预可减轻患者经济负担,虽本次研究的总成本对照组大于试验组,但试验组较对照组的总成本多了血药浓度监测的费用,万古霉素使用费用还是低于对照组的,成本—效果分析得结果也表明试验组的经济学更优于对照组。
综上所述,临床药师的参与可以提高重症感染患者万古霉素治疗过程中的疗效、安全性和经济性,在患者的个体化治疗中起重要作用,并且建立的监测流程值得推荐。本次研究为回顾性研究,同时中国的临床药师人数不足,无法完全保证在给药前后同一时间段采集血样,因此可能会影响研究结果,仍需增加样本量或进行前瞻性研究以获得更准确、更有效的结果,形成更加完善的监测流程。
Biography
陈海琴,硕士,E-mail: Chq1114@126.com
Funding Statement
北京医卫健康基金(YWJKJJHKYJJ-B183073);蚌埠医学院研究生科研创新计划项目(Byycx1960)
Contributor Information
陈 海琴 (Haiqin CHEN), Email: Chq1114@126.com.
石 庆平 (Qingping SHI), Email: sir_shi@126.com.
孔 令提 (Lingti KONG), Email: konglingti@163.com.
References
- 1.医疗机构药事管理暂行规定[J].中国医院, 2002, 5: 56-8.
- 2.何 志超, 伍 俊妍, 邱 凯锋. 万古霉素个体化给药临床药师指引. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=guangdyx201502004. 今日药学. 2015;25(2):78–82. [何志超, 伍俊妍, 邱凯锋.万古霉素个体化给药临床药师指引[J].今日药学, 2015, 25(2): 78-82.] [Google Scholar]
- 3.宋 志飞, 陶 丽源, 马 辉. 万古霉素血药浓度监测的临床应用. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=sdyy201822026. 首都食品与医药. 2018;25(22):30–2. [宋志飞, 陶丽源, 马辉.万古霉素血药浓度监测的临床应用[J].首都食品与医药, 2018, 25(22): 30-2.] [Google Scholar]
- 4.申 庆荣, 李 刚, 卢 秋玉, et al. 万古霉素血药浓度的影响因素分析. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=zgksszz201705021. 中国抗生素杂志. 2017;42(5):429–34. [申庆荣, 李刚, 卢秋玉, 等.万古霉素血药浓度的影响因素分析[J].中国抗生素杂志, 2017, 42(5): 429-34.] [Google Scholar]
- 5.唐 喆, 曹 静, 帅 维维, et al. 新生儿万古霉素血药谷浓度影响因素分析. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=zgksszz201904017. 中国抗生素杂志. 2019;44(4):493–502. [唐喆, 曹静, 帅维维, 等.新生儿万古霉素血药谷浓度影响因素分析[J].中国抗生素杂志, 2019, 44(4): 493-502.] [Google Scholar]
- 6.代 伟, 陈 瑞祥, 温 瑾, et al. 重症肺炎患者应用万古霉素后血药谷浓度影响因素. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=rdyxzz201806025. 热带医学杂志. 2018;18(6):795–8, 834. [代伟, 陈瑞祥, 温瑾, 等.重症肺炎患者应用万古霉素后血药谷浓度影响因素[J].热带医学杂志, 2018, 18(6): 795-8, 834.] [Google Scholar]
- 7.岑 菡婧, 杜 为扬, 何 艳玲. 儿童万古霉素血药浓度影响因素分析. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=guangdyx201904010. 今日药学. 2019;29(4):251–4. [岑菡婧, 杜为扬, 何艳玲.儿童万古霉素血药浓度影响因素分析[J].今日药学, 2019, 29(4): 251-4.] [Google Scholar]
- 8.许 建文, 黄 品芳, 林 慧芬, et al. 肾功能正常患者万古霉素稳态谷浓度分布及影响因素分析. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=zgksszz202002017. 中国抗生素杂志. 2020;45(2):199–203. [许建文, 黄品芳, 林慧芬, 等.肾功能正常患者万古霉素稳态谷浓度分布及影响因素分析[J].中国抗生素杂志, 2020, 45(2): 199-203.] [Google Scholar]
- 9.李 光辉. 万古霉素临床应用剂量中国专家共识. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=zhcrbzz201211001. 中华传染病杂志. 2012;30(11):641–6. [李光辉.万古霉素临床应用剂量中国专家共识[J].中华传染病杂志, 2012, 30(11): 641-6.] [Google Scholar]
- 10.万古霉素临床应用中国专家共识(2011版) [J].中国新药与临床杂志, 2011, 30(8): 561-73.
- 11.Ye ZK, Chen YL, Chen K, et al. Therapeutic drug monitoring of vancomycin: a guideline of the Division of Therapeutic Drug Monitoring, Chinese Pharmacological Society. J Antimicrob Chemother. 2016;71(11):3020–5. doi: 10.1093/jac/dkw254. [Ye ZK, Chen YL, Chen K, et al. Therapeutic drug monitoring of vancomycin: a guideline of the Division of Therapeutic Drug Monitoring, Chinese Pharmacological Society[J]. J Antimicrob Chemother, 2016, 71(11): 3020-5.] [DOI] [PubMed] [Google Scholar]
- 12.谢 玲, 刘 代华, 黄 义昆. 临床药师干预模式下肾功能损伤患者万古霉素的用药效果. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=gxyx201819006. 广西医学. 2018;40(19):2272–4. [谢玲, 刘代华, 黄义昆.临床药师干预模式下肾功能损伤患者万古霉素的用药效果[J].广西医学, 2018, 40(19): 2272-4.] [Google Scholar]
- 13.陈 玥, 朱 曼, 王 秀英, et al. 临床药师干预下万古霉素用药行为分析. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=zgywyyyjc201805010. 中国药物应用与监测. 2018;15(5):295–7, 318. [陈玥, 朱曼, 王秀英, 等.临床药师干预下万古霉素用药行为分析[J].中国药物应用与监测, 2018, 15(5): 295-7, 318.] [Google Scholar]
- 14.蔡 云东, 费 爱华. 万古霉素临床疗效相关影响因素的探讨. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=gwyx-slblkxylcfc201510028. 临床与病理杂志. 2015;35(10):1842–6. [蔡云东, 费爱华.万古霉素临床疗效相关影响因素的探讨[J].临床与病理杂志, 2015, 35(10): 1842-6.] [Google Scholar]
- 15.刘 鑫, 李 林娟, 冯 义朝, et al. 评价口服万古霉素治疗原发性硬化性胆管炎的有效性和安全性的临床研究. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=wcbxhgbxzz201812023. 胃肠病学和肝病学杂志. 2018;27(12):1433–6. [刘鑫, 李林娟, 冯义朝, 等.评价口服万古霉素治疗原发性硬化性胆管炎的有效性和安全性的临床研究[J].胃肠病学和肝病学杂志, 2018, 27(12): 1433-6.] [Google Scholar]
- 16.徐 长伟. 利奈唑胺与万古霉素治疗老年呼吸机相关性肺炎的疗效与安全性研究. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=zglyyx201809030. 中国疗养医学. 2018;27(9):966–8. [徐长伟.利奈唑胺与万古霉素治疗老年呼吸机相关性肺炎的疗效与安全性研究[J].中国疗养医学, 2018, 27(9): 966-8.] [Google Scholar]
- 17.陈 涛. 不同抗菌药物联用对ICU重症感染患者抗感染治疗的临床疗效及其对病原菌清除的影响. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=kgryx201809022. 抗感染药学. 2018;15(9):1528–30. [陈涛.不同抗菌药物联用对ICU重症感染患者抗感染治疗的临床疗效及其对病原菌清除的影响[J].抗感染药学, 2018, 15(9): 1528-30.] [Google Scholar]
- 18.杨 伟, 易 丹辉, 谢 雁鸣, et al. 基于GBM倾向评分法对疏血通注射液导致谷丙转氨酶异常变化的影响分析. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=zgzyzz201318025. 中国中药杂志. 2013;38(18):3039–47. [杨伟, 易丹辉, 谢雁鸣, 等.基于GBM倾向评分法对疏血通注射液导致谷丙转氨酶异常变化的影响分析[J].中国中药杂志, 2013, 38 (18): 3039-47.] [PubMed] [Google Scholar]
- 19.庄 严, 谢 邦铁, 翁 盛鑫, et al. 中药上市后再评价HIS "真实世界"集成数据仓库的构建与实现. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=zgzyzz201120037. 中国中药杂志. 2011;36(20):2883–6. [庄严, 谢邦铁, 翁盛鑫, 等.中药上市后再评价HIS "真实世界"集成数据仓库的构建与实现[J].中国中药杂志, 2011, 36(20): 2883-6.] [Google Scholar]
- 20.Tolordava G, Yagudina R, Arinina E. Cost-effectiveness analysis of ACEI and ARBS Ⅱ drugs in patients with arterial hypertension. Value Heal. 2017;20(9):A617. [Tolordava G, Yagudina R, Arinina E. Cost-effectiveness analysis of ACEI and ARBS Ⅱ drugs in patients with arterial hypertension[J]. Value Heal, 2017, 20(9): A617.] [Google Scholar]
- 21.莫 亚玲, 张 剑霄, 赵 德运, et al. 三种方案治疗儿童社区获得性肺炎的疗效及药物经济学评价. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=zgyyyypjyfx201911005. 中国医院用药评价与分析. 2019;19(11):1296–8, 1302. [莫亚玲, 张剑霄, 赵德运, 等.三种方案治疗儿童社区获得性肺炎的疗效及药物经济学评价[J].中国医院用药评价与分析, 2019, 19(11): 1296-8, 1302.] [Google Scholar]
- 22.闫 立国, 赵 志刚. 儿童患者中开展万古霉素血药浓度监测的研究. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=zglcylxzz201610020. 中国临床药理学杂志. 2016;32(10):933–5. [闫立国, 赵志刚.儿童患者中开展万古霉素血药浓度监测的研究[J].中国临床药理学杂志, 2016, 32(10): 933-5.] [Google Scholar]
- 23.薛 盛敏, 唐 莲, 方 洁, et al. 临床药师参与肾功能亢进患者万古霉素个体化用药的临床实践. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=yxfwyyj201903017. 药学服务与研究. 2019;19(3):222–5. [薛盛敏, 唐莲, 方洁, 等.临床药师参与肾功能亢进患者万古霉素个体化用药的临床实践[J].药学服务与研究, 2019, 19(3): 222-5.] [Google Scholar]
- 24.孙 钟慧, 姚 鸿萍, 孙 利. 临床药师参与万古霉素抗感染治疗的药学服务. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=yxfwyyj201901011. 药学服务与研究. 2019;19(1):36–40. [孙钟慧, 姚鸿萍, 孙利.临床药师参与万古霉素抗感染治疗的药学服务[J].药学服务与研究, 2019, 19(1): 36-40.] [Google Scholar]
- 25.白 向荣, 褚 燕琦. 临床药师在干预万古霉素血药浓度监测的作用研究. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=zgywjj201507014. 中国药物警戒. 2015;12(7):439–41, 443. [白向荣, 褚燕琦.临床药师在干预万古霉素血药浓度监测的作用研究[J].中国药物警戒, 2015, 12(7): 439-41, 443.] [Google Scholar]
- 26.林 美玲. 万古霉素类药物应用的干预及其分析. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=haixyx201706032. 海峡药学. 2017;29(6):76–9. [林美玲.万古霉素类药物应用的干预及其分析[J].海峡药学, 2017, 29(6): 76-9.] [Google Scholar]
- 27.张 相林, 缪 丽燕, 陈 文倩, et al. 治疗药物监测工作规范专家共识(2019版) http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=zgyyyypjyfx201908001. 中国医院用药评价与分析. 2019;19(8):897–8, 902. [张相林, 缪丽燕, 陈文倩, 等.治疗药物监测工作规范专家共识(2019版)[J].中国医院用药评价与分析, 2019, 19(8): 897-8, 902.] [Google Scholar]
- 28.Melduni RM, Schaff HV, Lee H, et al. Impact of left atrial appendage closure during cardiac surgery on the occurrence of early postoperative atrial fibrillation, stroke, and mortality: a propensity scorematched analysis of 10 633 patients. Circulation. 2017;135(4):366–78. doi: 10.1161/CIRCULATIONAHA.116.021952. [Melduni RM, Schaff HV, Lee H, et al. Impact of left atrial appendage closure during cardiac surgery on the occurrence of early postoperative atrial fibrillation, stroke, and mortality: a propensity scorematched analysis of 10 633 patients[J]. Circulation, 2017, 135(4): 366-78.] [DOI] [PMC free article] [PubMed] [Google Scholar]
- 29.Thourani VH, Kodali S, Makkar RR, et al. Transcatheter aortic valve replacement versus surgical valve replacement in intermediate- risk patients: a propensity score analysis. Lancet. 2016;387(10034):2218–25. doi: 10.1016/S0140-6736(16)30073-3. [Thourani VH, Kodali S, Makkar RR, et al. Transcatheter aortic valve replacement versus surgical valve replacement in intermediate- risk patients: a propensity score analysis[J]. Lancet, 2016, 387(10034): 2218-25.] [DOI] [PubMed] [Google Scholar]
- 30.Branch-Elliman W, Ripollone JE, O'Brien WJ, et al. Risk of surgical site infection, acute kidney injury, and Clostridium difficile infection following antibiotic prophylaxis with vancomycin plus a beta-lactam versus either drug alone: a national propensity-scoreadjusted retrospective cohort study. PLoS Med. 2017;14(7):e1002340. doi: 10.1371/journal.pmed.1002340. [Branch-Elliman W, Ripollone JE, O'Brien WJ, et al. Risk of surgical site infection, acute kidney injury, and Clostridium difficile infection following antibiotic prophylaxis with vancomycin plus a beta-lactam versus either drug alone: a national propensity-scoreadjusted retrospective cohort study[J]. PLoS Med, 2017, 14(7): e1002340.] [DOI] [PMC free article] [PubMed] [Google Scholar]
- 31.Sturmer T, Joshi M, Glynn RJ, et al. A review of the application of propensity score methods yielded increasing use, advantages in specific settings, but not substantially different estimates compared with conventional multivariable methods. https://pubmed.ncbi.nlm.nih.gov/16632131/ J Clin Epidemiol. 2006;59(5):437–47. doi: 10.1016/j.jclinepi.2005.07.004. [Sturmer T, Joshi M, Glynn RJ, et al. A review of the application of propensity score methods yielded increasing use, advantages in specific settings, but not substantially different estimates compared with conventional multivariable methods[J]. J Clin Epidemiol, 2006, 59(5): 437-47.] [DOI] [PMC free article] [PubMed] [Google Scholar]
- 32.Rosenbaum PR, Rubin DB. The central role of the propensity score in observational studies for causal effects. Biometrika. 1983;70(1):41–55. doi: 10.1093/biomet/70.1.41. [Rosenbaum PR, Rubin DB. The central role of the propensity score in observational studies for causal effects[J]. Biometrika, 1983, 70 (1): 41-55.] [DOI] [Google Scholar]
- 33.Hansen BB, Bowers J. Covariate balance in simple, stratified and clustered comparative studies. Stat Sci. 2008;23(2):219–36. doi: 10.1214/08-STS254. [Hansen BB, Bowers J. Covariate balance in simple, stratified and clustered comparative studies[J]. Stat Sci, 2008, 23(2): 219-36.] [DOI] [Google Scholar]
- 34.梁 涛, 杨 诚, 吴 苏源, et al. 多项指标联合检测在细菌感染性疾病中的诊断价值. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=lcxyxzz201912001. 临床血液学杂志(输血与检验) 2019;32(6):905–8, 912. [梁涛, 杨诚, 吴苏源, 等.多项指标联合检测在细菌感染性疾病中的诊断价值[J].临床血液学杂志(输血与检验), 2019, 32(6): 905-8, 912.] [Google Scholar]
- 35.卢 飞艳, 蒋 铁汉, 周 金萍, et al. 胎盘病理炎性改变与新生儿细菌感染指标的相关性研究. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=cqyx201916023. 重庆医学. 2019;48(16):2793–6. [卢飞艳, 蒋铁汉, 周金萍, 等.胎盘病理炎性改变与新生儿细菌感染指标的相关性研究[J].重庆医学, 2019, 48(16): 2793-6.] [Google Scholar]
- 36.陈 取永. PCT、IL-6、IL-8、CRP及PLT和MPV等指标对新生儿细菌感染性败血症的临床诊断价值分析. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=zgcfy201903002. 中国处方药. 2019;17(3):1–3. [陈取永. PCT、IL-6、IL-8、CRP及PLT和MPV等指标对新生儿细菌感染性败血症的临床诊断价值分析[J].中国处方药, 2019, 17(3): 1-3.] [Google Scholar]
- 37.Lee AYY, Peterson EA, Wu C. Clinical practice guidelines on cancer-associated thrombosis: a review on scope and methodology. Thromb Res. 2016;140:S119–27. doi: 10.1016/S0049-3848(16)30110-4. [Lee AYY, Peterson EA, Wu C. Clinical practice guidelines on cancer-associated thrombosis: a review on scope and methodology [J]. Thromb Res, 2016, 140: S119-27.] [DOI] [PubMed] [Google Scholar]
- 38.Hermsen ED, Hanson M, Sankaranarayanan J, et al. Clinical outcomes and nephrotoxicity associated with vancomycin trough concentrations during treatment of deep-seated infections. Expert Opin Drug Saf. 2010;9(1):9–14. doi: 10.1517/14740330903413514. [Hermsen ED, Hanson M, Sankaranarayanan J, et al. Clinical outcomes and nephrotoxicity associated with vancomycin trough concentrations during treatment of deep-seated infections[J]. Expert Opin Drug Saf, 2010, 9(1): 9-14.] [DOI] [PubMed] [Google Scholar]
- 39.李 政波, 王 雪. 血清胱抑素C与肾功能损害的关系及血清胱抑素C对早期高血压肾损害患者的临床观察分析. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=jilinyx201801020. 吉林医学. 2018;39(1):55–8. [李政波, 王雪.血清胱抑素C与肾功能损害的关系及血清胱抑素C对早期高血压肾损害患者的临床观察分析[J].吉林医学, 2018, 39(1): 55-8.] [Google Scholar]
- 40.刘 继来, 黄 彦. 胱抑素C等多项指标在2型糖尿病早期肾损伤诊断中的意义(附70例分析. http://www.cnki.com.cn/Article/CJFDTotal-FJYY201006065.htm. 福建医药杂志. 2010;32(6):99–100. [刘继来, 黄彦.胱抑素C等多项指标在2型糖尿病早期肾损伤诊断中的意义(附70例分析) [J].福建医药杂志, 2010, 32(6): 99-100.] [Google Scholar]
- 41.张 丽琴, 张 俊英. 2型糖尿病患者血清胱抑素C、尿微量清蛋白检测的临床应用. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=gwyx-lcsw201113056. 国际检验医学杂志. 2011;32(13):1514–5. [张丽琴, 张俊英. 2型糖尿病患者血清胱抑素C、尿微量清蛋白检测的临床应用[J].国际检验医学杂志, 2011, 32(13): 1514-5.] [Google Scholar]
- 42.Grubb A, Bjork J, Nyman U, et al. Cystatin C, a marker for successful aging and glomerular filtration rate, is not influenced by inflammation. Scand J Clin Lab Investig. 2011;71(2):145–9. doi: 10.3109/00365513.2010.546879. [Grubb A, Bjork J, Nyman U, et al. Cystatin C, a marker for successful aging and glomerular filtration rate, is not influenced by inflammation[J]. Scand J Clin Lab Investig, 2011, 71(2): 145-9.] [DOI] [PMC free article] [PubMed] [Google Scholar]
- 43.Fried LF, Shlipak MG, Crump C, et al. Renal insufficiency as a predictor of cardiovascular outcomes and mortality in elderly individuals. J Am Coll Cardiol. 2003;41(8):1364–72. doi: 10.1016/S0735-1097(03)00163-3. [Fried LF, Shlipak MG, Crump C, et al. Renal insufficiency as a predictor of cardiovascular outcomes and mortality in elderly individuals[J]. J Am Coll Cardiol, 2003, 41(8): 1364-72.] [DOI] [PubMed] [Google Scholar]
- 44.Lodise TP, Lomaestro BM, Graves J, et al. Larger vancomycin doses (at least four grams per day) are associated with an increased incidence of nephrotoxicity. Antimicrob Agents Chemother. 2008;52(4):1330–6. doi: 10.1128/AAC.01602-07. [Lodise TP, Lomaestro BM, Graves J, et al. Larger vancomycin doses (at least four grams per day) are associated with an increased incidence of nephrotoxicity[J]. Antimicrob Agents Chemother, 2008, 52(4): 1330-6.] [DOI] [PMC free article] [PubMed] [Google Scholar]
- 45.Ogutlu A, Guclu E, Karabay O, et al. Effects of Carbapenem consumption on the prevalence of Acinetobacter infection in intensive care unit patients. Ann Clin Microbiol Antimicrob. 2014;13(1):7. doi: 10.1186/1476-0711-13-7. [Ogutlu A, Guclu E, Karabay O, et al. Effects of Carbapenem consumption on the prevalence of Acinetobacter infection in intensive care unit patients[J]. Ann Clin Microbiol Antimicrob, 2014, 13(1): 7.] [DOI] [PMC free article] [PubMed] [Google Scholar]
- 46.Maortua H, Caunt A, I banez B, et al. Relationship between inhospital bacterial resistance and antimicrobial use over a 13-year period. Enferm Infecc Microbiol Clin. 2009;27(8):441–8. doi: 10.1016/j.eimc.2008.09.017. [Maortua H, Caunt A, I banez B, et al. Relationship between inhospital bacterial resistance and antimicrobial use over a 13-year period[J]. Enferm Infecc Microbiol Clin, 2009, 27(8): 441-8.] [DOI] [PubMed] [Google Scholar]
- 47.Imaura M, Kohata Y, Kobayashi K, et al. Effect of pharmacists' intervention on the antibiotic therapy for the methicillin-resistant Staphylococcus aureus (MRSA) infectious diseases in the intensive care unit. Yakugaku Zasshi-J Pharm Soc Jpn. 2011;131(4):563–70. doi: 10.1248/yakushi.131.563. [Imaura M, Kohata Y, Kobayashi K, et al. Effect of pharmacists' intervention on the antibiotic therapy for the methicillin-resistant Staphylococcus aureus (MRSA) infectious diseases in the intensive care unit[J]. Yakugaku Zasshi-J Pharm Soc Jpn, 2011, 131(4): 563- 70.] [DOI] [PubMed] [Google Scholar]
- 48.Bond C, Raehl CL. Clinical and economic outcomes of pharmacistmanaged aminoglycoside or vancomycin therapy. https://academic.oup.com/ajhp/article/62/15/1596/5135749. Am J HealSyst Pharm. 2005;62(15):1596–605. doi: 10.2146/ajhp040555. [Bond C, Raehl CL. Clinical and economic outcomes of pharmacistmanaged aminoglycoside or vancomycin therapy[J]. Am J HealSyst Pharm, 2005, 62(15): 1596-605.] [DOI] [PubMed] [Google Scholar]


