RÉSUMÉ
CONTEXTE:
Il faudra prendre des mesures continues contre la transmission communautaire du coronavirus du syndrome respiratoire aigu sévère 2 (SRAS-CoV-2) pour prévenir d’autres vagues d’infection. Nous avons exploré les effets des interventions non pharmacologiques sur la transmission projetée du SRAS-CoV-2 au Canada.
MÉTHODES:
Nous avons créé un modèle de la population canadienne à base d’agents intégrant l’âge qui simule les effets des mesures de santé publique, selon leur intensité actuelle et projetée, sur la transmission du SRAS-CoV-2. Les mesures étudiées sont le dépistage et l’isolement des cas, la recherche de contacts et la mise en quarantaine, l’éloignement sanitaire et la fermeture des espaces partagés. Nous avons évalué l’effet des mesures prises individuellement et celui des mesures combinées.
RÉSULTATS:
En l’absence de mesures, 64,6 % (intervalle de crédibilité [ICr] à 95 % : 63,9 %–65,0 %) des Canadiens contracteraient le SRAS-CoV-2 (taux d’attaque global), et 3,6 % (ICr à 95 % 2,4 %–3,8 %) des personnes infectées en mourraient. En poursuivant le dépistage et la recherche de contacts à la même intensité que pendant la période de référence, sans maintenir l’éloignement sanitaire ou refermer certains endroits, le pays connaîtrait un taux d’attaque global de 56,1 % (ICr à 95 % 0,05 %–57,1 %); si ces mesures étaient accrues, le taux d’attaque chuterait à 0,4 % (ICr à 95 % 0,03 %–23,5 %). En combinant ce dernier scénario et le maintien de l’éloignement sanitaire, le taux tomberait à 0,2 % (ICr à 95 % 0,03 %–1,7 %). Ce scénario est le seul qui garderait la demande en soins hospitaliers et intensifs sous la capacité, qui préviendrait presque tous les décès et qui mettrait fin à l’épidémie. La prolongation de la fermeture des écoles aurait un effet minime, mais réduirait la transmission en milieu scolaire. Par contre, la prolongation de la fermeture des lieux de travail et des lieux publics réduirait de manière marquée le taux d’attaque et mettait habituellement ou toujours fin à l’épidémie, selon les différents scénarios simulés.
INTERPRÉTATION:
Le contrôle de la transmission du SRAS-CoV-2 passera par l’amélioration et le maintien des mesures, tant communautaires qu’individuelles. Autrement, il y aura une recrudescence de l’épidémie, et un risque de surcharger le système de santé.
Le 11 mars 2020, l’Organisation mondiale de la Santé a officiellement déclaré le statut de pandémie pour la maladie causée par le coronavirus du syndrome respiratoire aigu sévère 2 (SRAS-CoV-2), la maladie à coronavirus 2019 (COVID-19)1,2. En date du 28 juin, on comptait plus de 10 millions de cas confirmés et environ 500 000 décès dans 188 pays et territoires3. Les personnes infectées par le SRAS-CoV-2 peuvent être asymptomatiques ou présenter des symptômes légers à graves4. Les hospitalisations et les décès surviennent surtout chez les personnes âgées ou immunodéprimées5,6. Des études semblent montrer que les personnes asymptomatiques peuvent transmettre le virus7, et que la contagion précède l’apparition des symptômes8–10. Ces caractéristiques, qui diffèrent de celles des autres coronavirus humains, ont posé des défis importants dans le contrôle de la transmission du SRAS-CoV-2 à l’échelle locale et mondiale.
Au départ, la santé publique canadienne misait sur le dépistage chez les voyageurs de retour au pays, afin d’isoler les cas importés. Le premier cas de COVID-19, rapporté le 25 janvier, était effectivement une personne revenant de l’étranger11. Les premiers cas détectés en février étaient des voyageurs ou des personnes ayant eu des contacts étroits avec des voyageurs12. Peu après on remarquait une transmission locale, qui s’est accélérée rapidement en mars, le nombre de cas acquis localement surpassant le nombre de cas liés aux voyages à partir du 15 mars12. L’approche de la santé publique est alors passée de l’endiguement à la prévention. Des mesures non pharmacologiques ont été mises en place, comme le dépistage et l’isolement des cas, l’identification des contacts pour les mettre en quarantaine, les mesures d’éloignement sanitaire, notamment la fermeture des espaces partagés, les restrictions de voyage et l’interdiction des grands rassemblements, et d’autres mesures visant à réduire les contacts entre personnes. L’ensemble des provinces et des territoires ont imposé de rigoureuses mesures d’éloignement sanitaire à la mi-mars, qui ont jusqu’à maintenant permis de contrôler l’épidémie13. On prévoit toutefois qu’en l’absence de mesures continues de prévention de la transmission communautaire, d’autres vagues d’infection suivront. Puisque les mesures utilisées pour endiguer la COVID-19 sont sans précédent et que leur efficacité demeure inconnue, la modélisation de leurs effets probables dans une variété de scénarios peut faciliter la prise de décisions14–16.
La dynamique de transmission des maladies infectieuses est habituellement modélisée à l’aide de modèles compartimentaux à l’échelle populationnelle17,18. Les modèles à base d’agents, quant à eux, fonctionnent avec des simulations par ordinateur faisant intervenir des agents qui représentent des personnes, des endroits ou des objets. Ces modèles sont stochastiques, et les agents sont programmés pour interagir entre eux dans l’environnement défini. Comme les agents peuvent avoir des caractéristiques uniques et qu’une hétérogénéité est possible, ce type de modèle convient à la simulation d’événements qui arrivent par hasard, par exemple la contagion à l’apparition des premiers symptômes et l’élimination du virus se produit dans les derniers stades de la maladie. Les modèles à base d’agents sont particulièrement adaptés à l’étude de l’efficacité des mesures de prévention, puisque celles-ci dépendent largement de la structure communautaire et de la dynamique dans la population19,20. Nous présentons ici un modèle à base d’agents conçu à l’Agence de la santé publique du Canada, qui sert à prédire la transmission du SRAS-CoV-2 selon l’imposition de différentes mesures au Canada.
Méthodes
Les détails techniques du modèle, dont les paramètres dérivés d’études publiées et de données canadiennes, sont présentés à l’annexe 1 (accessible ici : www.cmaj.ca/lookup/doi/10.1503/cmaj.200990/tab-related-content). Notre modèle a été créé à l’aide d’AnyLogic Professional 8.5.2 (The AnyLogic Company). De multiples éclosions étant en cours au Canada, le modèle donne une estimation générale de la situation et ne tient pas compte de la dispersion géographique des cas.
Mesures et scénarios du modèle
Le modèle intègre 4 mesures (dépistage et isolement des cas, recherche de contacts et mise en quarantaine, éloignement sanitaire permettant de réduire le taux de contacts quotidiens, et fermeture des espaces partagés), qu’il étudie de manière séparée et combinée (tableau 1). Nous avons comparé l’efficacité de chaque mesure à celle de l’absence de mesures pour évaluer la progression libre de la COVID-19 dans une population naïve. Nous avons modélisé les mesures séparément pour connaître leur effet indépendant, et nous avons estimé leur intensité actuelle pour générer des données de référence. Ces données décrivent la situation au Canada pour la période du 7 février au 10 mai 2020, date où les espaces partagés ont commencé à rouvrir. Nous estimons que pendant la période de référence, environ 20 % des cas symptomatiques ont été détectés par dépistage et isolés pour le reste de la période de contagion21; 50 % des membres des ménages des cas identifiés se sont aussi isolés (estimation); 50 % des personnes exposées ont été repérées par la recherche de contacts et mises en quarantaine avant d’être contagieuses (estimation); 100 % des écoles, 40 % des lieux de travail et 50 % des lieux publics ont été fermés du 16 mars au 10 mai22,23; et l’éloignement sanitaire à l’extérieur du domicile a fait diminuer le taux de contacts de 20 % supplémentaires24,25. Les données de référence ont été validées selon le nombre de cas acquis localement au Canada (annexe 1, figure S2).
Tableau 1:
Mesures non pharmacologiques modélisées
| Mesure | Effets | Agents concernés |
|---|---|---|
| Dépistage et isolement des cas | Dépistage visant la détection des cas symptomatiques et l’isolement des personnes testées positives chez elles pendant 14 jours, et donc la réduction de la transmission communautaire. Une certaine proportion des membres du ménage s’isolent aussi, sauf s’ils ont déjà été infectés et donc qu’ils sont immunisés. | Symptômes légers* |
| Au moment où les agents commencent à avoir des symptômes légers, ils sont déjà contagieux depuis 1 à 3 jours, mais leur isolement à ce moment prévient 3 à 7 jours supplémentaires de transmission communautaire potentielle. Les agents isolés peuvent toujours infecter ceux qui vivent avec eux, mais à un taux de contacts estimé de 50 %, car nous présumons que les personnes malades imposeront une forme d’éloignement sanitaire dans le ménage. | ||
| Recherche de contacts et mise en quarantaine | Recherche de contacts visant à repérer les personnes exposées infectées, mais qui ne sont pas encore contagieuses. Cette mesure est l’une des plus efficaces, parce qu’un agent mis en quarantaine pendant 14 jours après l’exposition ne transmettra à aucun moment la maladie. | Exposés |
| Éloignement sanitaire | Réduit le nombre de contacts par jour; peut être appliqué à toute la population ou à des groupes d’âge ciblés. N’a été imposé qu’à l’extérieur du ménage. | Tous les états de santé |
| Fermeture des espaces partagés | Fermeture des écoles, des lieux de travail et des lieux publics définie soit par une proportion (100 % des écoles) soit par un seuil (lieux de travail comptant 50 agents ou plus). Les agents assignés à un espace partagé fermé restent à la maison jusqu’à la réouverture. | S.O. |
Remarque : S.O. = sans objet.
On suppose que les personnes présentant des symptômes graves sont trop malades pour sortir; le dépistage et l’isolement s’appliquent donc uniquement aux agents présentant des symptômes légers.
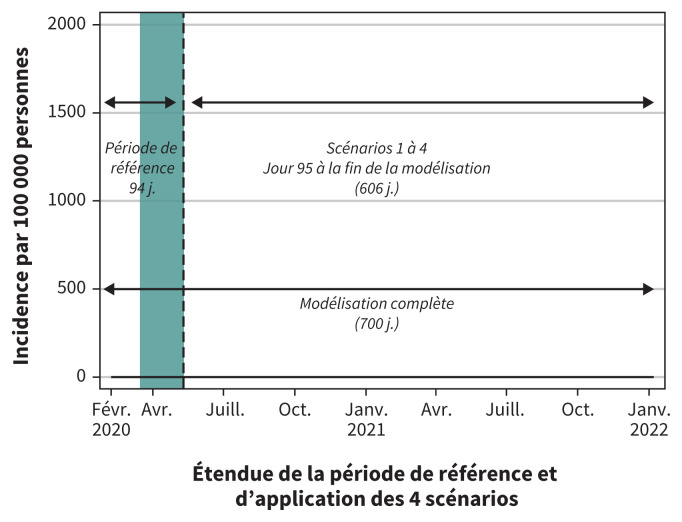
À partir de la situation de référence, nous avons modélisé 4 scénarios pour la période du 11 mai 2020 au 7 janvier 2022, qui illustrent des trajectoires potentielles de transmission du SRASCoV-2 au Canada selon l’intensité des mesures mises en place pour compenser la réouverture des espaces partagés (figure 1). Les scénarios sont les suivants : mesures de prévention minimales (dépistage et isolement des cas, recherche de contacts et mise en quarantaine à la même intensité que durant la période de référence, et abandon de l’éloignement sanitaire); maintien de l’éloignement sanitaire; dépistage et recherche de contacts accrus, et mesures combinées (maintien de l’éloignement sanitaire, et dépistage et recherche de contacts accrus) (tableau 2). Tous ont été créés à partir de cibles canadiennes jugées réalistes compte tenu des mesures en place. Puis nous nous sommes servis des scénarios pour comparer et explorer les effets de la fermeture prolongée des écoles et des espaces partagés. Nous avons modélisé des fermetures qui se prolongeraient jusqu’en septembre 2020. Lorsque nous supposions une prolongation de la fermeture des écoles, nous levions la fermeture des lieux de travail et des lieux publics, et vice versa. Comme les écoles sont de toute façon fermées pendant l’été, nous avons pu faire une comparaison pour une même période.
Figure 1:
Les données de référence sont appliquées aux 4 scénarios pour les 94 premiers jours de la simulation. À partir du 95e jour (11 mai 2020), une autre combinaison de mesures de santé publique est appliquée dans chaque scénario. Remarque : La simulation complète s’étend sur 700 jours, du 7 février 2020 au 7 janvier 2022. La bande verte représente les 8 semaines de fermeture des espaces partagés (lieux de travail, écoles, lieux publics — centres commerciaux, bibliothèques, etc.) pendant la période de référence, du 16 mars au 10 mai 2020.
Tableau 2:
Résumé de la situation canadienne de référence et intensité des mesures de santé publique mises en place dans les 4 scénarios à l’étude
| Mesure | Situation de référence (7 février au 10 mai 2020) | Scénarios et intensité des mesures (11 mai 2020 au 7 janvier 2022) | |||
|---|---|---|---|---|---|
| Mesures minimales (aucun changement aux mesures après la réouverture, et non-maintien de l’éloignement sanitaire) | Maintien de l’éloignement sanitaire | Dépistage et recherche de contacts accrus | Mesures combinées | ||
| Dépistage et isolement des cas | 20 % des cas sont dépistés et isolés (50 % des membres du ménage s’isolent aussi) | 20 % des cas sont dépistés et isolés (50 % des membres du ménage s’isolent aussi) | 20 % des cas sont dépistés et isolés (50 % des membres du ménage s’isolent aussi) | 50 % des cas sont dépistés et isolés* (50 % des membres du ménage s’isolent aussi) | 50 % des cas sont dépistés et isolés* (50 % des membres du ménage s’isolent aussi) |
| Recherche de contacts et mise en quarantaine | 50 % des contacts des 20 % de cas dépistés sont retracés et mis en quarantaine | 50 % des contacts des 20 % de cas dépistés sont retracés et mis en quarantaine | 50 % des contacts des 20 % de cas dépistés sont retracés et mis en quarantaine | 100 % des contacts des 50 % de cas dépistés sont retracés et mis en quarantaine* | 100 % des contacts des 50 % de cas dépistés sont retracés et mis en quarantaine* |
| Éloignement sanitaire (réduction du taux de contacts quotidiens) | Réduction de 20 % du taux de contacts pendant 8 semaines (du 16 mars au 10 mai 2020) | S.O. | Maintien de la réduction de 20 % du taux de contacts* | S.O. | Maintien de la réduction de 20 % du taux de contacts* |
| Fermeture des espaces partagés | 100 % des écoles, 40 % des lieux de travail et 50 % des lieux publics sont fermés pendant 8 semaines (du 16 mars au 10 mai 2020) | S.O. | S.O. | S.O. | S.O. |
Remarque : S.O. = sans objet.
Mesures intensifiées ou maintenues après la période de référence.
Variables et analyses statistiques
Avec le modèle, nous avons produit un cumulatif et un décompte quotidiens des cas pour chaque groupe d’âge et pour chaque état de santé. Parmi les variables évaluées, citons le taux d’attaque global (total des nouveaux cas divisé par la population totale), le taux d’attaque clinique, le taux de cas asymptomatiques, le nombre d’hospitalisations, le nombre d’admissions aux soins intensifs et le taux de mortalité par groupes d’âge. Nous avons aussi construit des courbes épidémiques représentant l’incidence et la prévalence quotidiennes de la maladie par 100 000 personnes. Les résultats stochastiques sont présentés comme les médianes de 50 essais (simulations) par scénario, et les valeurs du 2,5e et du 97,5e centiles, comme l’intervalle de crédibilité (ICr) à 95 %. Le paramètre de transmission a été adapté aux données canadiennes, ce qui donne un taux de reproduction (R0; nombre moyen de personnes infectées par une même personne) de 2,7. Nous avons également réalisé des analyses de sensibilité, afin de voir l’effet de la variation entre 2,0 et 3,0 du R0 pour chacun des 4 scénarios. Enfin, nous avons fait nos analyses statistiques et créé les graphiques à l’aide de Stata 16 (StataCorp).
Approbation éthique
Aucune approbation éthique n’était nécessaire pour cette étude : toutes les données proviennent d’articles publiés ou sont accessibles au public sous forme agrégée.
Résultats
Le taux d’attaque global de la population pour la transmission communautaire en l’absence de mesures de prévention serait de 64,6 % (ICr à 95 % 63,9 %–65,0 %) et le taux de mortalité, de 3,6 % (ICr à 95 % 2,4 %–3,8 %) (annexe 1, figure S3). Nous avons modélisé les mesures séparément pour connaître leur efficacité lorsqu’elles sont utilisées seules. La mesure la plus efficace serait la fermeture partielle des espaces partagés (taux d’attaque global 7,6 %, ICr à 95 % 0,36 %–13,2 %), suivie par le maintien de l’éloignement sanitaire (taux d’attaque global 54,0 %, ICr à 95 % 53,0 %–54,7 %), le dépistage et l’isolement de 20 % des cas et le co-isolement de 50 % des membres du ménage (taux d’attaque global 59,3 %, ICr à 95 % 0,04 %–60,0 %) et enfin l’identification et la mise en quarantaine de 50 % des contacts (taux d’attaque global 62,5 %, ICr à 95 % 62,0 %–63,3 %) (annexe 1, figures S4–S7). La seule mesure qui permettrait de mettre fin à l’épidémie à elle seule serait la fermeture partielle des espaces partagés (mais après 18 mois, et il est probablement irréaliste d’appliquer aussi longtemps une mesure aussi restrictive), alors que toutes les autres mesures différeraient l’épidémie. Aux fins de comparaison, nous avons aussi modélisé les mesures combinées de la période de référence (à l’exception de la fermeture des espaces partagés); nous avons obtenu un taux d’attaque global de 42,3 % (ICr à 95 % 0,03 %–43,3 %), soit une diminution de 22,3 % comparativement à une diminution de 17,8 % pour les mêmes mesures appliquées séparément (annexe 1, figure S8; données supplémentaires disponibles sur demande auprès des auteurs).
Le taux d’attaque global pour le scénario des mesures minimales est de 56,1 % (ICr à 95 % 0,05 %–57,1 %) (tableau 3). Le taux d’attaque global le plus élevé, qui s’explique un pourcentage de personnes asymptomatiques élevé (≈ 50 %), est observé chez les 10 à 19 ans, le taux d’attaque clinique le plus élevé, chez les 20 à 54 ans, les taux d’hospitalisation et de mortalité les plus élevés, chez les personnes de 75 ans et plus, et le taux d’admission aux soins intensifs le plus élevé, chez les 65 à 84 ans (parce que la plupart des personnes de 85 ans et plus décèdent avant de se rendre) (données disponibles sur demande auprès des auteurs). Le scénario des mesures minimales, qui correspond au dépistage et à la recherche de contacts à la même intensité qu’à la période de référence a permis de réduire efficacement le taux d’attaque global, mais ne suffisait pas à endiguer l’épidémie ou à contrôler une recrudescence de l’épidémie à la levée des mesures restrictives (fermetures) (figure 2).
Tableau 3:
Résumé des résultats de la modélisation pour les 4 scénarios à l’étude*
| Variable | Mesures minimales | Maintien de l’éloignement sanitaire | Dépistage et recherche de contacts accrus | Mesures combinées |
|---|---|---|---|---|
| Taux d’attaque global, % (ICr à 95 %) | 56,1 (0,05–57,1) | 41,6 (0,04–43,4) | 0,36 (0,03–23,5) | 0,25 (0,03–1,7) |
| Taux d’attaque clinique, % (ICr à 95 %) | 34,5 (0,03–35,1) | 25,4 (0,03–26,6) | 0,23 (0,02–14,3) | 0,16 (0,02–1,0) |
| Taux de cas asymptomatiques, % (ICr à 95 %) | 21,6 (0,01–22,1) | 16,2 (0,01–16,9) | 0,13 (0,01–9,2) | 0,09 (0,01–0,7) |
| Proportion de cas asymptomatique sur le nombre total de cas, % (ICr à 95 %) | 38,5 (26,7–42,5) | 38,8 (28,6–40,2) | 38,9 (24,1–40,5) | 36,9 (28,6–42,8) |
| Cas cliniques légers (pas hospitalisés), % (ICr à 95 %) | 89,1 (4,1–21,2) | 89,5 (84,0–94,9) | 89,7 (80,0–93,0) | 90,0 (60,9–93,6) |
| Cas cliniques hospitalisés (y compris aux soins intensifs), % (ICr à 95 %) | 10,9 (4,1–21,2) | 10,5 (5,1–16,0) | 10,3 (7,0–20,0) | 10,0 (6,5–39,1) |
| Cas cliniques admis aux soins intensifs, % (ICr à 95 %) | 2,8 (0,0–7,9) | 2,7 (0,0–5,9) | 2,6 (0,0–5,0) | 2,7 (0,0–6,2) |
| Cas hospitalisés admis aux soins intensifs, % (ICr à 95 %) | 25,4 (0,0–50,0) | 25,4 (0,0–50,0) | 25,4 (0,0–40,0) | 24,1 (0,0–57,1) |
| Taux de mortalité parmi les cas cliniques, % (ICr à 95 %) | 3,2 (0,0–3,5) | 2,9 (0,0–4,8) | 1,7 (0,0–4,0) | 1,4 (0,0–5,3) |
| Total des cas (cliniques et asymptomatiques) par 100 000 personnes, médiane (ICr à 95 %) | 56 148 (45–57 068) | 41 579 (44–43 455) | 358 (29–23 408) | 247 (28–1679) |
| Total des cas cliniques par 100 000 personnes, médiane (ICr à 95 %) | 34 463 (31–35 087) | 25 413 (30–26 626) | 227 (22–14 301) | 157 (20–991) |
| Total des cas asymptomatiques par 100 000 personnes, médiane (ICr à 95 %) | 21 615 (12–22 101) | 16 152 (14–16 881) | 129 (7–9249) | 94 (8–688) |
| Total des cas hospitalisés par 100 000 personnes, médiane (ICr à 95 %) | 3747 (2–3903) | 2661 (3–2824) | 25 (2–1464) | 16 (4–105) |
| Total des cas admis aux soins intensifs par 100 000 personnes, médiane (ICr à 95 %) | 950 (0–1031) | 665 (0–748) | 7 (0–387) | 4 (0–28) |
| Total des décès par 100 000 personnes, médiane (ICr à 95 %) | 1113 (0–1208) | 739 (0–830) | 4 (0–296) | 2 (0–13) |
| Infections acquises à l’école, % (ICr à 95 %) | 9,1 (1,7–9,7) | 8,9 (0,0–9,4) | 9,1 (0,0–13,3) | 4,8 (0,0–10,8) |
| Infections acquises au travail, % (ICr à 95 %) | 14,2 (9,1–20,5) | 13,7 (5,3–19,5) | 13,1 (5,8–25,8) | 13,3 (5,8–19,4) |
| Infections acquises dans des lieux publics, % (ICr à 95 %) | 25,4 (14,3–28,2) | 24,0 (12,3–27,2) | 23,2 (11,1–27,8) | 22,4 (13,6–30,3) |
| Infections acquises à domicile, % (ICr à 95 %) | 51,2 (50,8–68,2) | 53,3 (52,9–64,9) | 56,2 (53,1–69,2) | 58,4 (51,6–69,7) |
| Nombre d’infections acquises à l’école par 100 000 personnes, médiane (ICr à 95 %) | 5134 (1–5336) | 3759 (0–3920) | 18 (0–2365) | 11 (0–159) |
| Nombre d’infections acquises au travail par 100 000 personnes, médiane (ICr à 95 %) | 7947 (4–8239) | 5655 (2–6000) | 43 (2–3107) | 33 (3–217) |
| Nombre d’infections acquises dans des lieux publics, médiane (ICr à 95 %) | 14 225 (6–14 694) | 9941 (6–10 503) | 83 (2–5511) | 56 (3–371) |
| Nombre d’infections acquises à domicile par 100 000 personnes (ICr à 95 %) | 28 659 (24–29 137) | 22 176 (23–23 080) | 210 (16–12 591) | 142 (15–942) |
Remarque : ICr = intervalle de crédibilité.
Le tableau donne la médiane pour 50 simulations et les valeurs du 2,5e centile et du 97,5e centile, qui délimitent l’ICr à 95 %. Un ICr important indique un résultat dichotomique entre les simulations (p. ex. poursuite ou fin de l’épidémie). La médiane correspond au résultat le plus probable des 50 simulations.
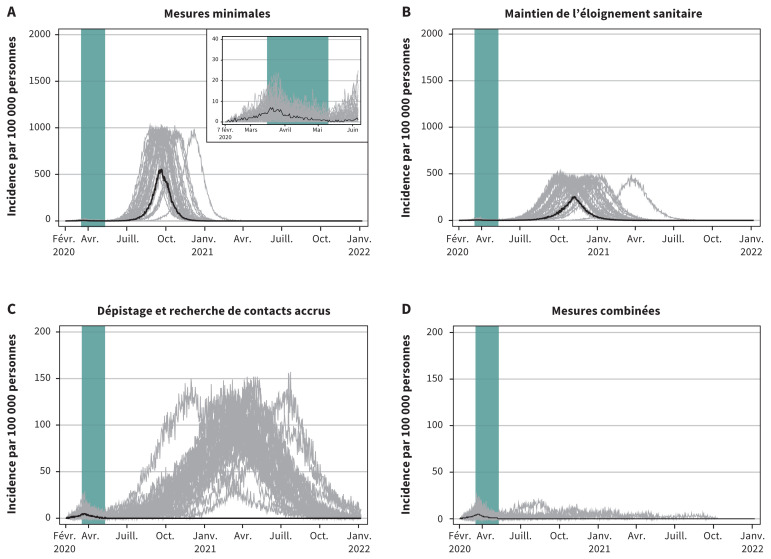
Figure 2:
Courbes épidémiques projetées du nombre quotidien de cas par 100 000 personnes pour les 4 scénarios. Dans chaque scénario, les mesures de santé publique s’intensifient graduellement suivant la réouverture des espaces partagés. Remarque : La bande verte représente la période du 16 mars au 10 mai 2020, soit la période de fermeture. La comparaison des 4 scénarios montre à quel point le retrait de certaines mesures, avec le maintien ou l’accroissement d’autres mesures, entraînerait une perte de contrôle de l’épidémie au Canada alors que la transmission communautaire se poursuit. La ligne noire représente la médiane. Chaque ligne grise représente 1 simulation; il y en a 50 par scénario. Remarque : L’échelle de l’axe des y est 10 fois plus petite pour le scénario de dépistage et de recherche de contacts accrus et le scénario des mesures combinées que pour les 2 autres scénarios.
Le scénario des mesures minimales, accompagné du maintien de l’éloignement sanitaire, donne un taux d’attaque global réduit à 41,6 % (ICr à 95 % 0,04 %–43,4 %). En comparaison, le scénario du dépistage et de la recherche de contacts accrus fait tomber le taux d’attaque global à 0,4 % (ICr à 95 % 0,03 %–23,5 %). Dans le dernier scénario, qui combine ces mesures et l’éloignement sanitaire, le taux d’attaque global est de 0,2 % (ICr à 95 % 0,03 %–1,7 %). Toutefois, seul le scénario des mesures combinées éradique l’épidémie, malgré certaines simulations indiquant qu’elle pourrait ne pas être contrôlée avant l’automne 2021 (figure 2).
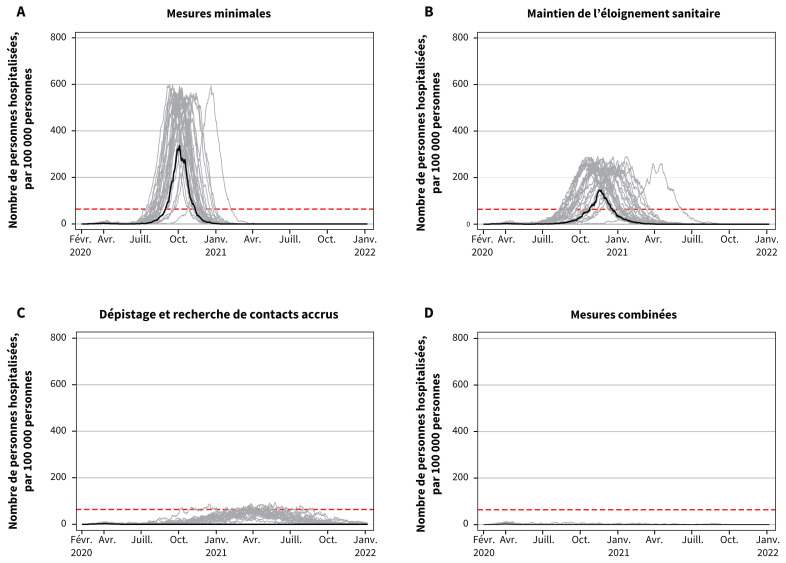
Les effets comparés des 4 scénarios sur les cas cliniques, les hospitalisations et les admissions aux soins intensifs vont dans le même sens que les effets sur le taux d’attaque global (tableau 3). Nous sommes arrivés à un total de 1113 morts par 100 000 personnes (ICr à 95 % 0–1208) pour les mesures minimales, 739 (ICr à 95 % 0–830) pour le maintien de l’éloignement sanitaire, 4 (ICr à 95 % 0–296) pour le dépistage et la recherche de contacts accrus et 2 (ICr à 95 % 0–13) pour les mesures combinées. Comparativement à l’absence de mesures de santé publique, les mesures minimales préviendraient 5312 cas cliniques, 798 hospitalisations et 320 décès par 100 000 personnes, alors que les mesures combinées préviendraient 39 618 cas cliniques, 4529 hospitalisations et 1431 décès par 100 000 personnes (données disponibles sur demande auprès des auteurs). Dans les scénarios des mesures minimales et du maintien de l’éloignement sanitaire, la demande de soins hospitaliers et intensifs excéderait la capacité maximale (figures 3 et 4). Dans celui du dépistage et de la recherche de contacts accrus, la demande reste sous la capacité dans la plupart des simulations, mais la dépasse dans certaines. Seules les mesures combinées permettent dans tous les cas de rester sous la capacité maximale des hôpitaux et des services de soins intensifs.
Figure 3:
Projections de la demande en lits d’hôpital, montrant le total quotidien de cas hospitalisés par 100 000 personnes pour les 4 scénarios. Remarque : Le nombre de personnes hospitalisées comprend les patients admis en soins généraux et admis à l’hôpital avant ou après un passage aux soins intensifs en raison de la maladie à coronavirus 2019. La capacité maximale des hôpitaux canadiens est représentée par la ligne traitillée rouge. La ligne noire représente la médiane. Chaque ligne grise représente 1 simulation; il y en a 50 par scénario.
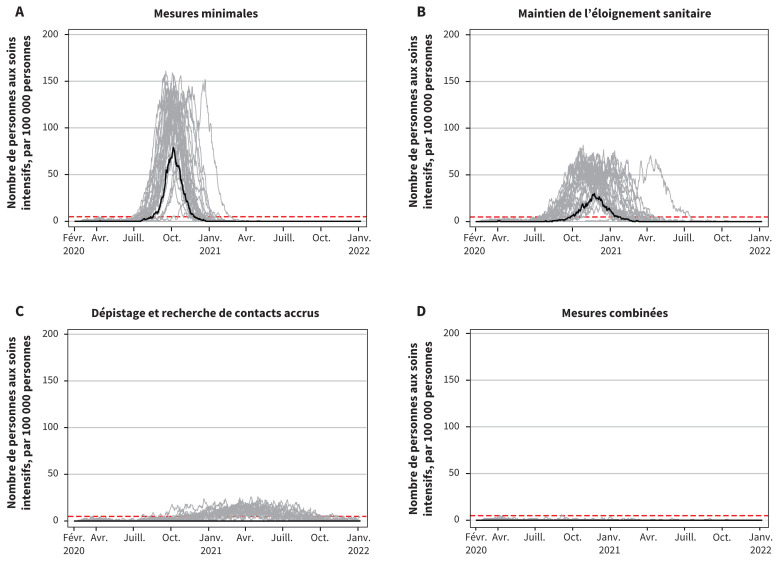
Figure 4:
Projections de la demande en lits de soins intensifs, montrant le total quotidien de personnes aux soins intensifs par 100 000 personnes pour les 4 scénarios. Remarque : La capacité maximale des services de soins intensifs canadiens est représentée par la ligne traitillée rouge. La ligne noire représente la médiane. Chaque ligne grise représente 1 simulation; il y en a 50 par scénario.
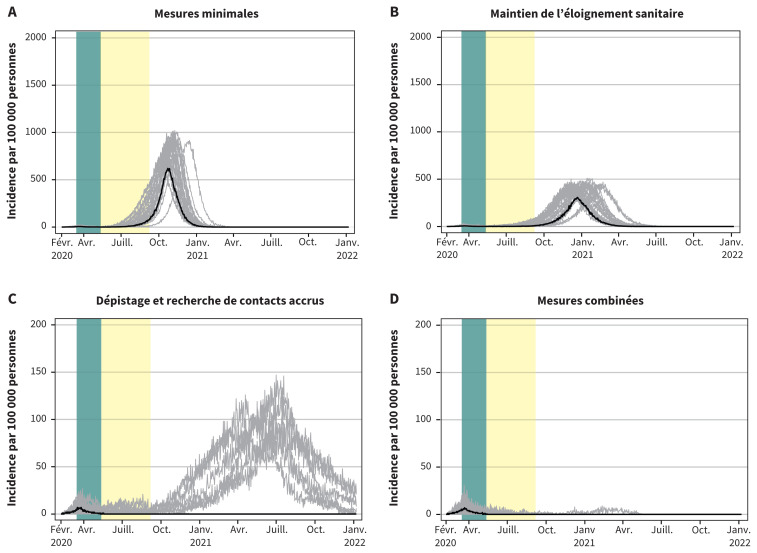
La prolongation de la fermeture des écoles dans les scénarios des mesures minimales et de maintien de l’éloignement sanitaire réduit très peu le taux d’attaque global par rapport aux scénarios seuls (tableau 4) et ne fait qu’allonger l’épidémie (figure 5). Cela dit, elle préviendrait 924 cas cliniques, 95 hospitalisations et 26 décès par 100 000 personnes (tableaux 3 et 4) comparativement aux mesures minimales seules, et 351 cas cliniques, 71 hospitalisations et 28 décès par 100 000 personnes comparativement au seul maintien de l’éloignement sanitaire. En outre, elle réduirait le nombre d’infections acquises dans les établissements scolaires de 935 par 100 000 personnes avec des mesures minimales et de 310 par 100 000 personnes avec le maintien de l’éloignement sanitaire, par rapport aux scénarios seuls, mais son influence sur l’épidémie serait minime en raison de la poursuite de la transmission communautaire. La fermeture des écoles ferait augmenter la transmission à domicile (379 et 287 infections supplémentaires par 100 000 personnes, respectivement), ce qui limite l’avantage de la transmission réduite dans les écoles. Dans le scénario de dépistage et de recherche de contacts accrus et le scénario des mesures combinées, la prolongation de la fermeture des écoles assure le contrôle de l’épidémie dans la plupart des simulations (figure 5).
Tableau 4:
Résumé des résultats de la modélisation pour les 4 scénarios à l’étude, avec prolongation de la fermeture des écoles*
| Variable | Mesures minimales | Maintien de l’éloignement sanitaire | Dépistage et recherche de contacts accrus | Mesures combinées |
|---|---|---|---|---|
| Taux d’attaque global, % (ICr à 95 %) | 54,7 (0,02–57,2) | 41,0 (0,04–42,6) | 0,3 (0,05–22,5) | 0,3 (0,03–1,0) |
| Taux d’attaque clinique, % (ICr à 95 %) | 33,5 (0,02–35,1) | 25,1 (0,02–26,2) | 0,2 (0,04–13,7) | 0,19 (0,0–0,6) |
| Taux de cas asymptomatiques, % (ICr à 95 %) | 21,1 (0,0–22,1) | 15,8 (0,01–16,7) | 0,1 (0,02–8,8) | 0,11 (0,01–0,4) |
| Proportion de cas asymptomatique sur le nombre total de cas, % (ICr à 95 %) | 38,5 (16,7–42,6) | 38,7 (31,5–43,9) | 38,1 (28,6–43,5) | 37,3 (25,0–44,5) |
| Cas cliniques légers (pas hospitalisés), % (ICr à 95 %) | 89,0 (78,0–93,2) | 89,5 (80,0–91,4) | 89,8 (81,2–94,2) | 89,9 (81,2–94,7) |
| Cas cliniques hospitalisés (y compris aux soins intensifs), % (ICr à 95 %) | 11,0 (6,8–22,0) | 10,5 (8,6–20,0) | 10,2 (5,8–18,8) | 10,1 (5,3–18,8) |
| Cas cliniques admis aux soins intensifs, % (ICr à 95 %) | 2,8 (0,0–6,2) | 2,7 (0,0–8,7) | 2,8 (0,9–12,5) | 2,4 (0,0–6,9) |
| Cas hospitalisés admis aux soins intensifs, % (ICr à 95 %) | 25,6 (0,0–50,0) | 25,5 (0,0–66,7) | 29,3 (9,1–66,7) | 22,5 (0,0–50,0) |
| Taux de mortalité parmi les cas cliniques, % (ICr à 95 %) | 3,2 (0,0–4,0) | 2,9 (0,0–4,0) | 1,6 (0,0–5,3) | 1,4 (0,0–4,0) |
| Total des cas (cliniques et asymptomatiques) par 100 000 personnes, médiane (ICr à 95 %) | 54 668 (24–57 177) | 41 003 (35–42 579) | 313 (56–22 533) | 297 (28–990) |
| Total des cas cliniques par 100 000 personnes, médiane (ICr à 95 %) | 33 539 (20–35 083) | 25 062 (23–26 158) | 198 (37–13 722) | 191 (18–625) |
| Total des cas asymptomatiques par 100 000 personnes, médiane (ICr à 95 %) | 21 082 (4–22 064) | 15 955 (12–16 661) | 118 (22–8811) | 110 (8–365) |
| Total des cas hospitalisés par 100 000 personnes, médiane (ICr à 95 %) | 3652 (5–3979) | 2490 (3–2835) | 21 (4–1409) | 19 (2–67) |
| Total des cas admis aux soins intensifs par 100 000 personnes, médiane (ICr à 95 %) | 930 (0–996) | 658 (0–727) | 6 (1–348) | 4 (0–17) |
| Total des décès par 100 000 personnes, médiane (ICr à 95 %) | 1088 (0–1203) | 712 (0–790) | 3 (0–252) | 3 (0–12) |
| Infections acquises à l’école, % (ICr à 95 %) | 8,0 (0,0–9,2) | 8,5 (0,0–9,4) | 4,4 (1,2–10,0) | 3,3 (0,0–12,3) |
| Infections acquises au travail, % (ICr à 95 %) | 14,4 (5,6–15,6) | 13,6 (5,6–20,6) | 13,4 (5,5–20,0) | 13,9 (0,0–20,6) |
| Infections acquises dans des lieux publics, % (ICr à 95 %) | 25,6 (16,8–32,8) | 24,2 (19,4–31,0) | 23,3 (14,7–32,1) | 23,6 (15,4–31,8) |
| Infections acquises à domicile, % (ICr à 95 %) | 51,8 (51,0–64,0) | 53,5 (52,9–72,2) | 59,7 (51,1–64,5) | 58,9 (51,5–68,2) |
| Nombre d’infections acquises à l’école par 100 000 personnes, médiane (ICr à 95 %) | 4199 (0–5169) | 3449 (0–3874) | 12 (2–2114) | 10 (0–40) |
| Nombre d’infections acquises au travail par 100 000 personnes, médiane (ICr à 95 %) | 7943 (1–8340) | 5611 (2–5930) | 43 (6–3008) | 44 (0–124) |
| Nombre d’infections acquises dans des lieux publics, médiane (ICr à 95 %) | 14 190 (7–14 618) | 9924 (7–10 450) | 63 (10–5286) | 68 (5–254) |
| Nombre d’infections acquises à domicile par 100 000 personnes (ICr à 95 %) | 28 280 (10–29 259) | 21 889 (17–22 795) | 186 (32–12 074) | 167 (15–580) |
Remarque : ICr = intervalle de crédibilité.
Le tableau donne la médiane pour 50 simulations et les valeurs du 2,5e centile et du 97,5e centile, qui délimitent l’ICr à 95 %. Un ICr important indique un résultat dichotomique entre les simulations (p. ex. poursuite ou fin de l’épidémie). La médiane correspond au résultat le plus probable des 50 simulations.
Figure 5:
Courbes épidémiques projetées montrant le nombre quotidien de cas par 100 000 personnes pour les 4 scénarios si l’on prolongeait la fermeture des écoles. Remarque : Dans chaque scénario, les mesures de santé publique s’intensifient graduellement. La bande verte représente la période de fermeture des espaces partagés, du 16 mars au 10 mai 2020. La bande jaune représente la période de fermeture des écoles sans la prolongation, du 11 mai au 8 septembre 2020. La ligne noire représente la médiane. Chaque ligne grise représente 1 simulation; il y en a 50 par scénario. L’échelle de l’axe des y est 10 fois plus petite pour le scénario de dépistage et de recherche de contacts accrus et pour le scénario des mesures combinées que pour les 2 autres scénarios.
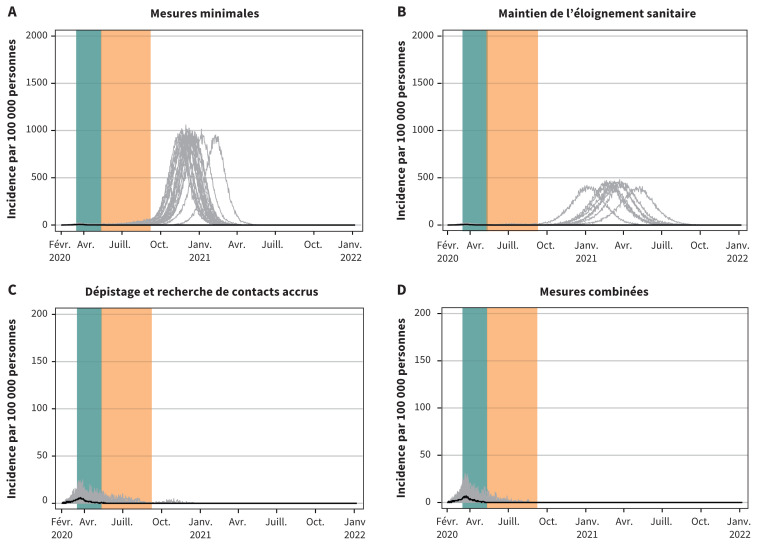
En comparaison, la prolongation de la fermeture des lieux de travail et des lieux publics donne des taux d’attaque global beaucoup moins élevés avec les mesures minimales (0,4 %; ICr à 95 % 0,1 %–57,0 %) et avec le maintien de l’éloignement sanitaire (0,3 %; ICr à 95 % 0,04 %–43,3 %) (tableau 5). L’épidémie prend fin dans plus de la moitié des simulations de prolongation selon ces scénarios, contre toutes les simulations pour le dépistage et la recherche de contacts accrus ou les mesures combinées (figure 6). Si la fermeture partielle des lieux de travail et des lieux publics est plus efficace que la fermeture des écoles, c’est parce qu’une plus grande proportion des infections sont acquises en milieu de travail (12,4 %–14,4 %) et dans les lieux publics (22,5 %–25,6 %) que dans les écoles (3,3 %–9,0 %), quel que soit le scénario. La différence s’explique par le fait qu’il y a beaucoup plus de gens sur le marché du travail et dans la communauté qu’à l’école et par la poursuite de la transmission communautaire et à domicile malgré la fermeture des écoles.
Tableau 5:
Résumé des résultats de la modélisation pour les 4 scénarios à l’étude, avec prolongation de la fermeture des espaces partagés (lieux de travail et lieux publics)*
| Variable | Mesures minimales | Maintien de l’éloignement sanitaire | Dépistage et recherche de contacts accrus | Mesures combinées |
|---|---|---|---|---|
| Taux d’attaque global, % (ICr à 95 %) | 0,4 (0,1–57,0) | 0,3 (0,04–43,3) | 0,2 (0,03–0,9) | 0,2 (0,07–0,9) |
| Taux d’attaque clinique, % (ICr à 95 %) | 0,3 (0,06–34,9) | 0,2 (0,03–26,5) | 0,1 (0,02–0,6) | 0,2 (0,05–0,5) |
| Taux de cas asymptomatiques, % (ICr à 95 %) | 0,2 (0,03–22,2) | 0,1 (0,01–16,8) | 0,1 (0,01–0,3) | 0,1 (0,02–0,3) |
| Proportion de cas asymptomatique sur le nombre total de cas, % (ICr à 95 %) | 38,5 (33,8–42,6) | 38,8 (28,0–43,6) | 37,9 (25,3–44,7) | 37,5 (27,4–44,3) |
| Cas cliniques légers (pas hospitalisés), % (ICr à 95 %) | 89,0 (85,5–93,1) | 89,6 (83,3–93,8) | 89,5 (82,2–93,2) | 89,6 (79,7–93,1) |
| Cas cliniques hospitalisés (y compris aux soins intensifs), % (ICr à 95 %) | 11,0 (6,9–14,5) | 10,4 (6,2–16,7) | 10,5 (6,8–17,8) | 10,4 (6,9–20,3) |
| Cas cliniques admis aux soins intensifs, % (ICr à 95 %) | 2,8 (0,7–5,2) | 2,6 (0,0–42,9) | 2,7 (0,0–7,4) | 2,8 (0,4–6,1) |
| Cas hospitalisés admis aux soins intensifs, % (ICr à 95 %) | 25,6 (5,3–57,1) | 24,7 (0,0–42,9) | 25,9 (0,0–55,6) | 23,8 (4,0–46,7) |
| Taux de mortalité parmi les cas cliniques, % (ICr à 95 %) | 3,2 (0,0–4,7) | 1,7 (0,0–4,8) | 1,4 (0,0–4,3) | 1,5 (0,0–5,1) |
| Total des cas (cliniques et asymptomatiques) par 100 000 personnes, médiane (ICr à 95 %) | 436 (96–56 988) | 290 (42–43 333) | 237 (30–886) | 226 (70–869) |
| Total des cas cliniques par 100 000 personnes, médiane (ICr à 95 %) | 263 (58–34 923) | 169 (29–26 531) | 143 (22–549) | 145 (46–543) |
| Total des cas asymptomatiques par 100 000 personnes, médiane (ICr à 95 %) | 166 (34–22 192) | 119 (13–16 802) | 89 (7–337) | 91 (22–326) |
| Total des cas hospitalisés par 100 000 personnes, médiane (ICr à 95 %) | 27 (4–3922) | 18 (5–2758) | 16 (2–54) | 15 (5–60) |
| Total des cas admis aux soins intensifs par 100 000 personnes, médiane (ICr à 95 %) | 11 (1–1019) | 5 (0–705) | 5 (0–15) | 4 (1–16) |
| Total des décès par 100 000 personnes, médiane (ICr à 95 %) | 5 (0–1218) | 3 (0–784) | 2 (0–12) | 2 (0–9) |
| Infections acquises à l’école, % (ICr à 95 %) | 9,0 (1,0–11,6) | 4,2 (0,0–9,4) | 4,0 (0,0–8,2) | 4,0 (0,0–8,7) |
| Infections acquises au travail, % (ICr à 95 %) | 14,2 (3,8–20,5) | 13,6 (8,3–18,4) | 12,4 (5,3–18,9) | 12,5 (7,1–23,0) |
| Infections acquises dans des lieux publics, % (ICr à 95 %) | 25,3 (13,1–33,9) | 22,8 (16,3–28,4) | 22,5 (12,2–29,1) | 22,5 (16,2–30,5) |
| Infections acquises à domicile, % (ICr à 95 %) | 54,7 (50,9–62,7) | 59,6 (53,0–67,1) | 60,2 (56,7–75,0) | 59,8 (52,2–64,1) |
| Nombre d’infections acquises à l’école par 100 000 personnes, médiane (ICr à 95 %) | 29 (1–5307) | 11 (0–3900) | 9 (0–53) | 10 (0–60) |
| Nombre d’infections acquises au travail par 100 000 personnes, médiane (ICr à 95 %) | 62 (5–8194) | 41,5 (5–5948) | 30 (1–105) | 31 (6–125) |
| Nombre d’infections acquises dans des lieux publics, médiane (ICr à 95 %) | 109 (17–14 513) | 60 (8–10 461) | 52 (4–201) | 47 (14–199) |
| Nombre d’infections acquises à domicile par 100 000 personnes (ICr à 95 %) | 243 (52–29 116) | 173 (22–22 991) | 138 (15–541) | 139 (35–508) |
Remarque : ICr = intervalle de crédibilité.
Le tableau donne la médiane pour 50 simulations et les valeurs du 2,5e centile et du 97,5e centile, qui délimitent l’ICr à 95 %. Un ICr important indique un résultat dichotomique entre les simulations (p. ex. poursuite ou fin de l’épidémie). La médiane correspond au résultat le plus probable des 50 simulations.
Figure 6:
Courbes épidémiques projetées montrant le nombre quotidien de cas par 100 000 personnes pour les 4 scénarios si l’on prolongeait la fermeture des écoles. Remarque : Dans chaque scénario, les mesures de santé publique s’intensifient graduellement. La bande verte représente la période de fermeture des espaces partagés, du 16 mars au 10 mai 2020. La bande orange représente la période de fermeture des écoles sans la prolongation, du 11 mai au 8 septembre 2020. La ligne noire représente la médiane. Chaque ligne grise représente 1 simulation; il y en a 50 par scénario. L’échelle de l’axe des y est 10 fois plus petite pour le scénario de dépistage et de recherche de contacts accrus et pour le scénario des mesures combinées que pour les 2 autres scénarios.
Selon l’analyse de sensibilité, les résultats du modèle dépendent du paramètre de transmission (β) et du taux de reproduction (R0) associé. Lorsque le R0 est abaissé à 2,4 (comparativement à l’estimation pour la situation de référence, R0 = 2,7), toutes les simulations des scénarios de dépistage et de recherche de contacts accrus et des mesures combinées montrent la fin de l’épidémie et le maintien de la demande sous la capacité des hôpitaux et des services de soins intensifs. Lorsque le R0 est abaissé à 2,0, la capacité des hôpitaux et des unités de soins intensifs est aussi respectée pour le scénario du maintien de l’éloignement sanitaire, et même dans la plupart des simulations du scénario des mesures minimales. Au contraire, lorsque le R0 est augmenté à 3,0, aucun scénario ne permet le contrôle de l’épidémie, et seul le scénario des mesures combinées ne fait pas déborder les hôpitaux et les unités de soins intensifs (annexe 1, figures S13–S24).
Interprétation
L’objectif était d’estimer la situation de la transmission du SRASCoV-2 au pays et de modéliser les défis auxquels nous devrons probablement faire face à la réouverture des espaces partagés au Canada. Malgré leur efficacité, les fermetures ont eu des effets néfastes sur le plan économique, sociale et de la santé. Le moment de la réouverture dépendra largement de la situation dans les provinces et territoires13,26. Notre modèle à base d’agents montre que toutes les mesures étudiées permettraient de réduire la transmission à un certain degré, mais que l’accroissement du dépistage pour isoler 50 % des cas et l’intensification de la recherche visant à mettre en quarantaine tous les contacts de ces cas constituent la méthode la plus efficace, surtout lorsqu’on la combine avec le maintien de l’éloignement sanitaire qui réduirait de 20 % le taux de contacts dans la population. Ces mesures devront rester en place jusqu’à ce que l’épidémie prenne fin (grâce à l’immunité collective ou à la vaccination), sans quoi il y aura une résurgence des cas.
La fermeture partielle des espaces partagés est la seule mesure étudiée qui permettrait à elle seule d’endiguer l’épidémie. Les résultats portent à croire que c’est principalement la fermeture des lieux de travail et des lieux publics, et non des écoles, qui serait efficace. La fermeture des écoles, bien qu’elle puisse prévenir la transmission en milieu scolaire, n’augmente que peu l’effet de la fermeture partielle des espaces partagés et ne suffit pas pour réduire le taux d’attaque global et contrôler l’épidémie, surtout si la transmission communautaire — majoritairement due aux personnes asymptomatiques et présymptomatiques contagieuses — persiste. Sans autres mesures de santé publique, elle ne ferait que prolonger l’épidémie14. Nos conclusions concordent avec celles des premières études, qui indiquaient que la fermeture des écoles pourrait ne pas être aussi efficace que d’autres mesures moins restrictives27. La fermeture des lieux de travail et des espaces partagés se révèle beaucoup plus efficace, parce que la transmission se fait principalement dans ces endroits. Comme des études examinant la situation d’autres pays14,28, nous avons conclu qu’en l’absence de mesures, environ les deux tiers des Canadiens seraient infectés. Nous avons fait des projections pour des mesures réalistes et cohérentes avec les directives en vigueur au Canada afin de réduire la proportion de la population infectée, qui diminuera quelque peu ou presque entièrement selon la trajectoire des mesures prises dans les prochains mois, tel que démontré dans d’autres modèles14,16. Le taux d’attaque réel dépendra du degré d’accroissement du dépistage et de l’isolement ainsi que de la recherche de contacts et de la mise en quarantaine21,29, et de la mesure dans laquelle la population canadienne adopte les mesures d’éloignement sanitaire et de protection individuelle22,24,30. Si nous rouvrons les espaces partagés sans mettre en place d’autres mesures de santé publique, l’épidémie reprendra dans une ampleur tributaire de nos efforts à venir, ce qui fera déborder le système de santé et obliger les autorités à réinstaurer des mesures de confinement.
Limites de l’étude
De nombreuses caractéristiques épidémiologiques importantes du SRAS-CoV-2 demeurent inconnues, particulièrement la susceptibilité (possiblement inférieure) des enfants à l’infection par rapport aux adultes, le taux réel d’infections asymptomatiques et l’apparition d’une immunité durable. Nous avons créé un modèle national qui tente d’agréger des épidémies régionales hétérogènes; il pourrait donc ne pas être représentatif de la transmission du SRAS-CoV-2 dans toutes les collectivités. Néanmoins, nous avons calibré le modèle à partir de données canadiennes, et les résultats montrent une bonne correspondance avec les cas acquis localement. Notre modèle ne tient pas compte de la transmission parmi les travailleurs de la santé et les résidents des établissements de soins de longue durée, qui sont la source de multiples éclosions au pays. Comme la transmission dans ces 2 groupes n’a pas la même ampleur dans toutes les provinces et tous les territoires, un modèle national ne permet pas d’étudier ces grappes à l’échelle régionale et locale. De plus, les milieux où surviennent les éclosions sont confrontés à des enjeux uniques qui exigent souvent des mesures de contrôle et de prévention des infections plus intenses que celles mises en place dans la population générale31. Notre modèle est représentatif de la situation nationale et donne une projection de référence de la transmission communautaire au Canada. C’est pourquoi il faut interpréter les résultats en tenant compte que, dans certaines circonstances, des éclosions locales pourraient mener à un nombre de cas, d’hospitalisations et de décès plus élevé que prévu.
Conclusion
Le modèle fournit des estimations provisoires de la transmission de la COVID-19 dans la population canadienne et des effets des mesures combinées en matière de réduction et d’élimination de la transmission au pays. Les premières mesures de contrôle de l’épidémie ont été très efficaces, mais lorsque les mesures restrictives seront levées, il faudra intensifier d’autres mesures pour prévenir la transmission, réduire au minimum le nombre de cas et ne pas surcharger les systèmes de santé.
Remerciements
Les auteurs remercient Lujie Duan de l’Université de la Saskatchewan, André Jacques de SimWell Consulting and Technologies et Deirdre Hennessy de Statistique Canada pour leur aide sur le plan technique.
Footnotes
Voir la version anglaise de l’article ici : www.cmaj.ca/lookup/doi/10.1503/cmaj.200990; voir le commentaire connexe (en anglais) ici : www.cmaj.ca/lookup/doi/10.1503/cmaj.201758
Intérêts concurrents: Aucun déclaré.
Cet article a été révisé par des pairs.
Collaborateurs: Victoria Ng, Aamir Fazil et Nicholas Ogden ont contribué à la conceptualisation. Ainsley Otten, Lisa Waddell et Nicole Atchessi ont contribué à la collecte de données. Victoria Ng a contribué à l’analyse. Christina Bancej et Patricia Turgeon ont contribué à l’interprétation des données. Victoria Ng, Christina Bancej et Patricia Turgeon ont rédigé l’ébauche de l’article, que tous les auteurs ont révisé. Tous les auteurs ont donné leur approbation finale pour la version soumise pour publication et assument l’entière responsabilité de tous les aspects du travail.
Partage des données: Toutes les données issues des modélisations peuvent être obtenues sur demande auprès de l’auteure de correspondance, tout comme les données épidémiologiques utilisées. Les données liées au nombre de cas de COVID-19, au nombre d’hospitalisations et à la mortalité seront sujettes aux lois sur la confidentialité. Les personnes intéressées peuvent communiquer avec l’auteure de correspondance, qui les mettra en contact avec la source des données d’origine.
Références
- 1.Allocution liminaire du Directeur général de l’OMS lors du point de presse sur la COVID-19 – 11 Mars 2020. Genève: Organisation mondiale de la Santé; 2020. Accessible ici : https://www.who.int/fr/dg/speeches/detail/who-director-general-s-opening-remarks-at-the-media-briefing-on-covid-19--11-march-2020 (consulté le 2 mai 2020). [Google Scholar]
- 2.Coronavirus disease 2019 (COVID-19): situation report, 51. Geneva: World Health Organization; 2020:1–9. [Google Scholar]
- 3.COVID-19 Dashboard by the Center for Systems Science and Engineering (CSSE) at Johns Hopkins University. Baltimore: Université John Hopkins; Accessible ici : https://gisanddata.maps.arcgis.com/apps/opsdashboard/index.html#/bda7594740fd40299423467b48e9ecf6 (consulté le 28 juin 2020). [Google Scholar]
- 4.Wu Z, McGoogan JM. Characteristics of and important lessons from the coronavirus disease 2019 (COVID-19) outbreak in China: summary of a report of 72 314 cases from the Chinese Center for Disease Control and Prevention. JAMA 2020;323:1239–42. 10.1001/jama.2020.2648. [DOI] [PubMed] [Google Scholar]
- 5.Garg S, Kim L, Whitaker M, et al. Hospitalization rates and characteristics of patients hospitalized with laboratory-confirmed coronavirus disease 2019 — COVID-NET, 14 states, March 1–30, 2020. MMWR Morb Mortal Wkly Rep 2020;69: 458–64. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 6.Wang D, Hu B, Hu C, et al. Clinical characteristics of 138 hospitalized patients with 2019 novel coronavirus-infected pneumonia in Wuhan, China. JAMA 2020;323:1061–9. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 7.Hu Z, Song C, Xu C, et al. Clinical characteristics of 24 asymptomatic infections with COVID-19 screened among close contacts in Nanjing, China. Sci China Life Sci 2020;63:706–11. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 8.Xia W, Liao J, Li C, et al. Transmission of corona virus disease 2019 during the incubation period may lead to a quarantine loophole. medRxiv 8 Mars 2020. 10.1101/2020.03.06.20031955. [DOI] [Google Scholar]
- 9.Tong Z-D, Tang A, Li K-F, et al. Potential presymptomatic transmission of SARS-CoV-2, Zhejiang Province, China, 2020. Emerg Infect Dis 2020;26:1052–4. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 10.Wei WE, Li Z, Chiew CJ, et al. Presymptomatic transmission of SARS-CoV-2 — Singapore, January 23–March 16, 2020. MMWR Morb Mortal Wkly Rep 2020;69: 411–5. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 11.Silverstein WK, Stroud L, Cleghorn GE, et al. First imported case of 2019 novel coronavirus in Canada, presenting as mild pneumonia. Lancet 2020;395:734. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 12.Maladie à coronavirus de 2019 (COVID-19) : Mise à jour quotidienne sur l’épidémiologie. Ottawa: Agence de la santé publique du Canada; Modifié le 20 juillet 2020. Accessible ici : https://sante-infobase.canada.ca/covid-19/resume-epidemiologique-cas-covid-19.html (consulté le 10 juin 2020). [Google Scholar]
- 13.Federal/provincial/territorial COVID-19 interventions [document interne]. Ottawa: Santé Canada; 4 Mai 2020. Accessible sur demande auprès de l’auteur. [Google Scholar]
- 14.Ferguson N, Laydon D, Nedjati-Gilani G, et al. Report 9: Impact of non-pharmaceutical interventions (NPIs) to reduce COVID-19 mortality and healthcare demand. London (UK): Imperial College London; 2020. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 15.Hellewell J, Abbott S, Gimma A, et al. Feasibility of controlling COVID-19 outbreaks by isolation of cases and contacts. Lancet Glob Health. 2020;8:e488–96. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 16.Tuite AR, Fisman DN, Greer AL. Mathematical modelling of COVID-19 transmission and mitigation strategies in the population of Ontario, Canada. CMAJ 2020;192:E497–505. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 17.Kermack W, McKendrick A. A contribution to the mathematical theory of epidemics. Proc R Soc Lond, A Contain Pap Math Phys Character 1927;115:700–21. 10.1098/rspa.1927.0118. [DOI] [Google Scholar]
- 18.Althaus CL. Estimating the reproduction number of Ebola virus (EBOV) during the 2014 outbreak in West Africa. PLoS Curr. 2014;6. 10.1371/currents.outbreaks.91afb5e0f279e7f29e7056095255b288. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 19.Chao DL, Oron AP, Srikrishna D, et al. Modeling layered non-pharmaceutical interventions against SARS-CoV-2 in the United States with Corvid. medRxiv 11 Avril 2020. 10.1101/2020.04.08.20058487. [DOI] [Google Scholar]
- 20.Davies NG, Kucharski AJ, Eggo RM, et al. Centre for the Mathematical Modelling of Infectious Diseases COVID-19 working group. Effects of non-pharmaceutical interventions on COVID-19 cases, deaths, and demand for hospital services in the UK: a modelling study. Lancet Public Health 2020;5:e375–85. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 21.Using a delay-adjusted case fatality ratio to estimate under-reporting. Londres (Royaume-Uni): Centre for Mathematical Modeling of Infectious Diseases, London School of Hygiene & Tropical Medicine; 22 Mars 2020, modifié le 21 juin 2020. Accessible ici : https://cmmid.github.io/topics/covid19/global_cfr_estimates.html (consulté le 21 juin 2020). [Google Scholar]
- 22.COVID-19 Community Mobility Report. Google Canada; 2020. Accessible ici : www.gstatic.com/covid19/mobility/2020-05-09_CA_Mobility_Report_en.pdf (consulté le 9 mai 2020).
- 23.Série d’enquêtes sur les perspectives canadiennes 1 : La COVID-19 et travailler de la maison, 2020. Ottawa: Statistique Canada. Le Quotidien; 2020. Accessible ici : https://www150.statcan.gc.ca/n1/daily-quotidien/200417/dq200417a-fra.pdf (consulté le 17 avril 2020). [Google Scholar]
- 24.Comment les Canadiens vivent-ils la situation liée à la COVID-19? [infographie]. Ottawa: Statistique Canada; Modifié le 20 avril 2020. Accessible ici : https://www150.statcan.gc.ca/n1/pub/11-627-m/11-627-m2020029-fra.htm (consulté le 19 avril 2020). [Google Scholar]
- 25.Tang B, Scarabel F, Bragazzi NL, et al. De-escalation by reversing the escalation with a stronger synergistic package of contact tracing, quarantine, isolation and personal protection: feasibility of preventing a COVID-19 rebound in Ontario, Canada, as a case study. Biology (Basel) 2020;9:100. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 26.COVID-19 Canada : Tableau de bord de l’état de la situation. Ottawa: Agence de la santé publique du Canada; Accessible ici : https://experience.arcgis.com/experience/f16b85c700c94729a2cd1c6efe5f6839/ (consulté le 27 juin 2020). [Google Scholar]
- 27.Viner RM, Russell SJ, Croker H, et al. School closure and management practices during coronavirus outbreaks including COVID-19: a rapid systematic review. Lancet Child & Adolesc Health 2020;4: 397–404. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 28.Kwok KO, Lai F, Wei WI, et al. Herd immunity — estimating the level required to halt the COVID-19 epidemics in affected countries. J Infect 2020;80:e32–3. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 29.Scarabel F, Pellis L, Bragazzi NL, et al. Canada needs to rapidly escalate public health interventions for its COVID-19 mitigation strategies. Infect Dis Model 2020;5:316–22. 10.1016/j.idm.2020.03.004. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 30.Chu DK, Akl EA, Duda S, et al. auteurs de l’étude COVID-19 Systematic Urgent Review Group Effort (SURGE). Physical distancing, face masks, and eye protection to prevent person-to-person transmission of SARS-CoV-2 and COVID-19: a systematic review and meta-analysis. Lancet 2020;395:1973–87. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 31.Callaghan AW, Chard AN, Arnold P, et al. Screening for SARS-CoV-2 infection within a psychiatric hospital and considerations for limiting transmission within residential psychiatric facilities — Wyoming, 2020. MMWR Morb Mortal Wkly Rep 2020;69:825–9. [DOI] [PMC free article] [PubMed] [Google Scholar]