Abstract
目的
通过体外模型比较计算机辅助设计/计算机辅助制造个性化基台(computer aided design/computer aided manufacturing customized abutments,CCA)与成品基台(stock abutments,SA)对粘接剂残留的影响,同时初步评价数字化三维扫描技术定量评估残留粘接剂的可行性。
方法
本研究所需20个工作模型皆取自同一例已在北京大学口腔医院牙周科接受了右上中切牙种植手术的患者。通过个性化愈合基台成形植体周软组织后,测得植体平台位于颊侧黏膜下5 mm。利用个性化转移杆取模后灌制20副工作模型,并根据基台种类及粘接边缘位置将工作模型分为四组,每组5个:CCA1(穿黏膜高度5 mm,即平齐黏膜粘接边缘)、CCA2(穿黏膜高度4 mm,即黏膜下1 mm粘接边缘)、SA1(穿黏膜高度3 mm,即黏膜下2 mm粘接边缘)和SA2(穿黏膜高度1 mm,即黏膜下4 mm粘接边缘)。在工作模型上模拟临床粘接过程并清除多余粘接剂后,利用三维扫描技术获得残留粘接剂的体积,利用数码相机拍摄二维图像获得残留粘接剂面积百分比,利用称量的方式获得残留粘接剂的质量,并分析三维扫描方法获取的体积与传统评价方法所得的面积百分比及质量的相关性。
结果
所有冠-基台复合体粘接边缘均有粘接剂残留。其中,CCA组残留粘接剂的体积明显小于SA组[(0.635 3±0.535 4) mm3 vs. (2.293 8±0.943 8) mm3,P<0.001],面积百分比及质量也显著低于SA组[面积百分比:7.57%±2.99% vs. 22.68%±10.06%,P<0.001;质量:(0.001 5±0.001 0) g vs. (0.003 7±0.001 4) g,P<0.001],而三者在CCA组及SA组内差异均无统计学意义(P>0.05)。三维扫描所得残留粘接剂的体积与传统评价方法所得残留粘接剂的面积百分比及残留粘接剂的质量间均具强相关性(r>0.75,P<0.001)。
结论
与SA相比,CCA能更有效地减少粘接剂的残留。基于三维扫描技术数字化评估残留粘接剂的方法切实可行,但其效度和信度还需进一步研究。
Keywords: 种植体-基台设计; 计算机辅助设计; 牙料粘固剂; 成像, 三维; 体外研究
Abstract
Objective
To compare the residual cement between computer aided design/computer aided manufacturing customized abutments (CCA) and stock abutments (SA), and to evaluate the feasibility of digital measurement for residual cement volume by three-dimensional scanning.
Methods
Twenty master models needed in this study were all taken from one 47-year-old patient with arrested periodontitis, who had already had an implant placed at his right upper central incisor site in the Department of Periodonto-logy, Peking University School and Hospital of Stomatology. After 4 weeks of soft tissue conditioning by means of customized healing abutment, the height of peri-implant soft tissue was measured, from the implant platform to mucosal margin, as 5 mm. Using customized impression coping, the impression was taken and twenty models were fabricated and allocated to 4 groups according to the type of abutments: CCA1 (5 mm transmucosal height CCA, with margin at tissue level), CCA2 (4 mm transmucosal height CCA, with 1 mm submucosal margin), SA1 (3 mm transmucosal height SA, with 2 mm submucosal margin) and SA2 (1 mm transmucosal height SA, with 4 mm submucosal margin). Crowns were cemented to the abutments, which were seated on the working models. Excess cement was removed by a prosthodontic specialist. Thereafter, the volume of residual cement was evaluated by using three-dimensional scanning technique. The area proportion of residual cement was calculated on photographs taken by a single lens reflex camera. The weight of residual cement was weighed by an analytical balance. And the correlation of residual cement volume data with residual cement area proportion or weight of residual cement acquired by traditional methods was analyzed.
Results
Residual cement was observed on all the experiment samples. The residual cement volume of CCA was significantly less than that of SA [(0.635 3±0.535 4) mm3 vs. (2.293 8±0.943 8) mm3, P < 0.001]. Consistently, CCA had less residual cement area proportion and weight than those of SA [area proportion: 7.57%±2.99% vs. 22.68%±10.06%, P < 0.001; weight: (0.001 5±0.001 0) g vs. (0.003 7±0.001 4) g, P < 0.001]. The residual cement volume was strongly correlated with the residual cement area proportion and residual cement weight (r>0.75, P < 0.001).
Conclusion
These in vitro results suggest that CCA minimized the residual cement more effectively than SA. The method to digitally evaluate the residual cement volume is feasible, but its validity and reliability need to be further studied.
Keywords: Dental implant-abutment design; Computer-aided design; Dental cements; Imaging, three-dimensional; In vitro
种植基台是连接上部修复结构和下方种植体的关键部件,基台的材料、结构组成、临床设计与制作技术对于成功的种植修复来说非常重要。粘接固位是种植修复中常用的固位方式[1]。然而在修复体的粘接过程中,多余的粘接剂常溢出修复体与基台的交界面,进入植体周组织,难以彻底清除[2-3]。残留的粘接剂是导致植体周炎的危险因素之一,可造成骨吸收,进而影响种植体的预后及存留率[4-7]。因此,如何避免粘接剂的残留是保证种植修复体长期稳定、健康的关键因素之一。
学者们提出过不同的方法以减少粘接剂的残留。Ichikawa等[8]提出在修复体上制作粘接剂排溢孔引导粘接剂的排出,以减少冠边缘处的粘接剂排溢到植体周组织中。Galván等[9]在粘接前制作基台代型,后将组织面涂匀粘接剂的修复体先在代型上就位一次,最后再进行口内粘接。Seo等[10]利用橡皮障和排龈线来阻止粘接剂向深部组织排溢。但上述方法都被证明并不能完全防止粘接剂残留[11]。
个性化基台(customized abutment,CA)又称定制基台,是根据种植体植入的位置和方向、软组织形态及缺牙间隙,由医师和技师个别设计的基台。根据制作工艺的不同,个性化基台可分为铸造基台、蜡型-扫描-研磨基台以及计算机辅助设计/计算机辅助制造(computer aided design/computer aided manufacturing,CAD/CAM)基台。Linkevicious[11]在2011年的研究表明,铸造个性化基台较成品基台(stock abutment,SA)利于残余粘接剂的清除,并分析其原因是个性化基台边缘相较成品基台而言更符合患者个性化的软组织形态,从而避免了某些位点的边缘位于黏膜下过深的情况。然而,铸造个性化基台存在金属收缩形变、精确度差、美学效果差等问题[12]。随着CAD/CAM技术在口腔领域的广泛应用,CAD/CAM个性化基台以其制作简便、精确度高、美学效果好的特性弥补了铸造个性化基台的不足[13],逐渐被更多医师采用。那么CAD/CAM个性化基台在保证穿黏膜轮廓和穿黏膜高度适应植体周软组织形态及厚度的前提下,相较于SA,是否能减少粘接剂的残留?本研究即在体外模拟因牙周炎失牙位点的种植修复情况,采用先进的数字化方法,测量并比较CAD/CAM个性化基台与成品基台在体外粘接时残留粘接剂的状况,同时观察基台边缘位置对粘接剂残留的影响,为因牙周炎失牙位点种植修复时基台的选择提供参考。
1. 资料与方法
1.1. 体外模型建立及分组
本研究所需的20个工作模型皆取自1例47岁男性患者,该患者2019年8月因右上中切牙缺失于北京大学口腔医院牙周科就诊,要求种植修复缺失牙。在纳入研究前,该患者右上中切牙位置已植入一枚种植体(直径3.5 mm,长度11.5 mm,NobelBiocare Replace NP,瑞典)并成功形成骨结合。在二期手术前,利用硅橡胶(Silagum,DMG,德国)制取口内印模,并利用Ⅳ型石膏(Dentona,AG,德国)灌注石膏模型后制作个性化愈合基台,用以初步成型植体周软组织。在二期术后4周,软组织形态基本稳定后,测量得到植体平台位于右上中切牙颊侧黏膜下5 mm。
告知患者全部研究方案,患者充分知情并同意其种植位点的工作模型作为本研究的试验模板。在体外将患者的个性化愈合基台与替代体连接,制作个性化开窗式转移杆,口内就位后取开窗式印模,待印模材料定型后取下,安装直径为3.5 mm的种植替代体(NobelBiocare Replace,瑞典),利用硅橡胶(凯蒙,中国)制作人工牙龈以最大程度模仿口内植体周软组织,并利用Ⅳ型石膏灌注20个相同的口外模型。
根据基台种类将工作模型分为CAD/CAM个性化基台组(DENFAC,高峰,中国;CCA组,n=10)和成品基台组(Esthetic AbutmentNobelReplace NP 3 mm,瑞典;SA组,n=10)。根据粘接边缘位置,将CCA组分为CCA1(穿黏膜高度5 mm,即粘接边缘平齐黏膜,n=5)和CCA2(穿黏膜高度4 mm,即粘接边缘位于黏膜下1 mm,n=5),将SA组分为SA1(穿黏膜高度3 mm,即粘接边缘位于黏膜下2 mm,n=5)与SA2(穿黏膜高度1 mm,即粘接边缘位于黏膜下4 mm,n=5)。按照分组订购基台,获得共20个实验对象(图 1)。
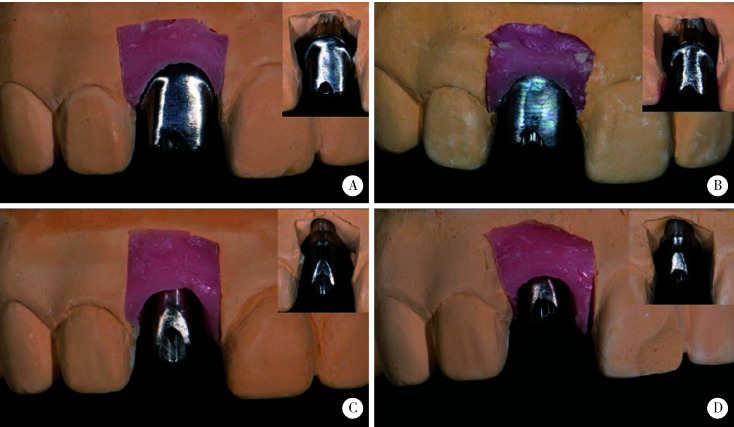
图 1.
基台的种类和分组
Allocation of different abutments
A, CAD/CAM customized abutments (CCA) with 5 mm transmucosal height, margins at tissue level (CCA1); B, CCA with 4 mm transmucosal height, 1 mm submucosal margins (CCA2); C, stock abutments (SA) with 3 mm transmucosal height, 2 mm submucosal margins (SA1); D, SA with 1 mm transmucosal height, 4 mm submucosal margins (SA2).
1.2. 修复体粘接
在修复体表面开孔,以便在粘接后作为螺丝通道,使冠-基台复合体可被摘取。牙冠和基台可能会接触到人工牙龈的部位,都在粘接前用抛光橡皮轮充分抛光。在粘接前,基台螺丝孔道用红蜡(GEO Crowax,Renfert,德国)覆盖,修复体的开孔用光固化树脂(Beautifil E,Shofu,日本)填实,以防粘接剂堵塞螺丝孔道,并阻断粘接剂可能从开孔溢出的通路,使得粘接剂均从修复体与基台边缘溢出,同时更好地模拟上部修复的标准临床粘接过程。粘接前将冠试戴在基台上,用尖探针在2.5倍放大镜下检查冠与基台边缘的密合性,并观察修复体切缘,检查切缘是否与对侧同名牙切缘平齐,并将此作为粘接时的就位标准。将所有对象的修复体和基台在无粘接剂下就位于扫描仪内的替代体上,分别扫描得到粘接前三角网格模型(standard tessellation language,STL)数据文件。在此之后,选用树脂改性玻璃离子水门汀(Fuji Plus,GC,日本)作为粘接剂,根据预实验所测得的粘接剂所需的用量,每个修复体采用相同质量的粉和相同滴数的液调拌粘接剂,并将粘接剂均匀且菲薄地涂布于修复体的全部组织面,迅速运用指力按压就位,使其切缘与对侧同名牙切缘平齐。多余的粘接剂由另一位不知晓样本分组的修复专科医师用探针(EXD57,Hu-Friedy,美国)和牙线(CLINICA,Lion,日本)去除,直至不再有新的粘接剂被器械探及或带出。将修复体螺丝孔道内的树脂及基台螺丝孔道内的蜡去除,卸下中央螺丝,获得种植体冠-基台复合体,再次在2.5倍放大镜下检查冠与基台边缘的密合性,若不密合,则需将冠脱位后重新粘接,若就位良好,收集该样本以待数据的测量。
1.3. 残留粘接剂体积的测量
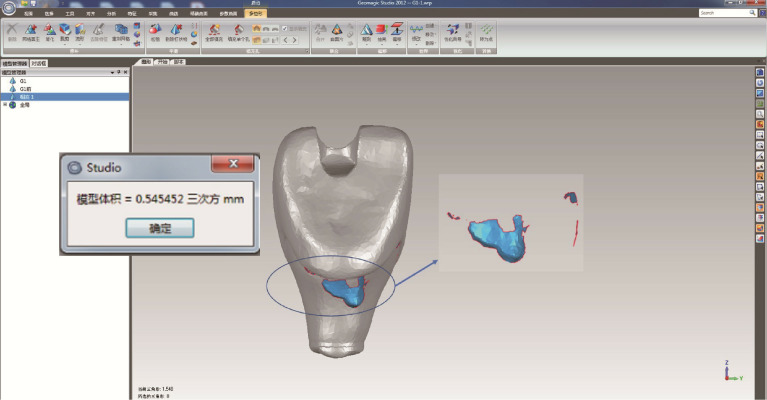
本研究采用数字化手段获取残留粘接剂的STL数据,以便计算体积。将获得的冠-基台复合体通过螺丝固位于相应的替代体上,利用硅橡胶印模材料(Silagum,DMG,德国)使扫描对象垂直竖立在模型扫描仓(Freedom,DOF,韩国)内,以单侧石膏模型模式扫描20个对象获得20个STL数据,并导入逆向工程软件(Geomagic Studio 2012,美国),利用布尔运算将粘接后的数据与相应的粘接前数据相减,得到残留粘接剂三维数据,并计算后者体积(mm3,图 2)。
图 2.
数字化方法测量残留粘接剂的体积
Digital measurement of residual cement volume
1.4. 残留粘接剂面积百分比的测量
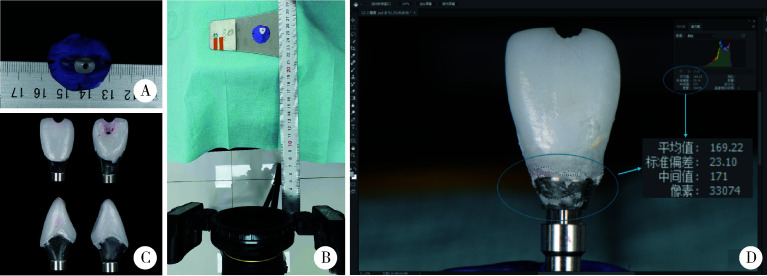
将获得的冠-基台复合体通过螺丝固位于相应的替代体上,并利用硅橡胶印模材料使扫描对象垂直竖立。保持样本与相机(Nikon D300s,日本)镜头之间250 mm的恒定标准距离,并确保镜头中心与基台-替代体交界面始终保持同一水平,调节参数至感光度200、光圈值36、快门速度1/150 s,为每个样本拍摄四个面(近中、远中、颊侧、腭侧)的二维图像数据,共80个图像数据。将数据导入图像处理软件(Adobe Photoshop CC 2018,英国),利用“pen tool”和“make path”两个工具标记出图像中的粘接剂边界及整个样本的截面范围,计算粘接剂图像的像素数目和整个截面像素数目的比值(图 3),即为残留粘接剂面积百分比(%)。
图 3.
残留粘接剂面积百分比的测量方法
Measurement of residual cement area proportion
A, the abutment and crown were erected using silicone rubber material; B, taking photo with a single lens reflex camera at a constant distance (250 mm); C, four aspects (buccal-, lingual-, mesial-and distal-) of each sample were snapshotted for analysis; D, calculating residual cement area proportion using software.
1.5. 残留粘接剂质量的称量
取20个Eppendorf管并对应20个样本进行编号,分别在分析天平(METTLER-TOLEDO,瑞士)上称重并记录,将摘取下的冠-基台复合体上残留的粘接剂利用纯钛刮治器(ErgoMix,LM,芬兰)去除并收集在相应的Eppendorf管内,用分析天平称量,计算Eppendorf管前后质量差值即为残留粘接剂的质量(g),共获得20个称量数据。
1.6. 统计学方法
通过SPSS 18.0(IBM,美国)进行统计学分析。计算残留粘接剂的体积、面积百分比以及质量的均值和标准差,对CCA组和SA组数据做独立样本t检验后,验证CCA1、CCA2、SA1及SA2四个亚组样本的方差齐性和正态性,并进行单因素方差分析(one-way ANOVA)。若结果为总体均数不全相等,则利用最小显著性差异法进一步做多个样本均数的两两比较。将三维扫描测量的残留粘接剂体积与残留粘接剂的面积百分比、残留粘接剂的质量进行相关性分析,分别计算Spearman秩相关系数后,对系数进行假设检验。假设检验均以α=0.05作为检验水准进行双侧检验。
2. 结果
2.1. CCA组残留粘接剂少于SA组
所有的实验样本粘接边缘处均有粘接剂残留,三种测量方法分别显示,CCA组残留粘接剂的体积、面积百分比和质量均显著小于SA组,差异具有统计学意义(表 1)。
表 1.
CCA组残留粘接剂少于SA组
Less residual cement in CCA group than in SA group
| Group | Volume/mm3 | Area proportion/% | Weight/g |
| CCA, CAD/CAM customized abutments; SA, stock abutments. Independent-samples t test. Data are shown as x±s. | |||
| CCA | 0.635 3±0.535 4 | 7.57±2.99 | 0.001 5±0.001 0 |
| SA | 2.293 8±0.943 8 | 22.68±10.06 | 0.003 7±0.001 4 |
| t | 5.044 | 4.908 | 4.236 |
| P | <0.001 | <0.001 | <0.001 |
2.2. CCA组中残留粘接剂的体积显著小于SA组
CCA1残留粘接剂的体积显著小于SA1及SA2(P=0.012,P=0.004),CCA2残留粘接剂的体积也显著小于SA1(P=0.007)及SA2(P=0.002);而CCA组和SA组内部两个亚组间残留粘接剂体积差异均无统计学意义(P=0.775,P=0.564,表 2)。
表 2.
CCA组与SA组残留粘接剂量的比较
Comparison of the amount of residual cement between CCA group and SA group
| Items | CCA1 group | CCA2 group | SA1 group | SA2 group |
| Post Hoc multiple comparisons using least significant difference method. Data are shown as x±s. *P < 0.05, **P < 0.01, vs. CCA1; #P < 0.05, ##P < 0.01, vs. CCA2. | ||||
| Volume/mm3 | 0.709 2±0.526 2 | 0.561 4±0.595 3 | 2.144 2±1.165 1*## | 2.443 4±0.768 7**## |
| Area proportion/% | 7.81±2.63 | 7.32±3.62 | 22.10±13.77*## | 23.26±6.10**## |
| Weight/g | 0.001 6±0.001 3 | 0.001 3±0.000 9 | 0.003 5±0.001 5*# | 0.004 0±0.001 4*## |
2.3. CAD/CAM个性化基台组中残留粘接剂的面积百分比显著小于成品基台组
CCA1残留粘接剂的面积百分比小于SA1(P=0.011)及SA2(P=0.007),CCA2残留粘接剂的面积百分比也小于SA1(P=0.009)及SA2(P=0.005),而CCA组和SA组内部两个亚组间残留粘接剂的面积百分比差异均无统计学意义(P=0.922,P=0.081,表 2)。
2.4. CCA组残留粘接剂的质量显著小于SA组
CCA1残留粘接剂的质量小于SA1(P=0.039)及SA2(P=0.011),CCA2残留粘接剂的质量也小于SA1(P=0.017)及SA2(P=0.005),而CCA组和SA组内部两个亚组间残留粘接剂的质量差异无统计学意义(P=0.688,P=0.547,表 2)。
2.5. 残留粘接剂的体积与面积百分比及质量间的相关性分析
残留粘接剂体积与面积百分比(r=0.798)及质量(r= 0.912)间均成正相关,且具有统计学意义(P<0.001)。
3. 讨论
粘接固位是种植修复中的一种常用固位方式,相较于螺丝固位,它具有较好的美观性,能最大程度保证修复体的被动就位,调 简便且机械并发症低[14],但残留的粘接剂是该固位方式的主要弊端[15],也是植体周黏膜炎和植体周炎的危险因素[16]。目前尚无可以完全避免粘接剂残留的方法,尤其当修复体边缘位于黏膜下时[3, 17-19],且残留粘接剂更易引起有牙周炎病史患者的植体周炎,尤其当种植位点患牙因牙周炎拔除,嵴顶软组织较厚时[7]。因此,本研究先复制1例因牙周炎失牙、行种植修复患者的临床状况,在体外评价CAD/CAM个性化基台相较于成品基台减少粘接剂残留的效果。
简便且机械并发症低[14],但残留的粘接剂是该固位方式的主要弊端[15],也是植体周黏膜炎和植体周炎的危险因素[16]。目前尚无可以完全避免粘接剂残留的方法,尤其当修复体边缘位于黏膜下时[3, 17-19],且残留粘接剂更易引起有牙周炎病史患者的植体周炎,尤其当种植位点患牙因牙周炎拔除,嵴顶软组织较厚时[7]。因此,本研究先复制1例因牙周炎失牙、行种植修复患者的临床状况,在体外评价CAD/CAM个性化基台相较于成品基台减少粘接剂残留的效果。
粘接剂残留是否一定导致植体周炎尚存在争议。有研究指出,粘接固位的种植修复体发生植体周炎风险并不比螺丝固位高[20-21]。同时,也有研究指出粘接剂的残留与植体周黏膜炎和植体周炎之间具有强相关性,可引起出血,形成脓肿及炎症,导致附着丧失,甚至植体失败[4-7]。本研究在所有的研究对象上均观察到粘接剂的残留,此结果与其他研究结果类似[3],因此,为保证种植体的长期预后,如何最大程度地减小粘接剂残留仍是目前粘接固位种植基台设计的重要目标之一。
有研究报道,基台粘接边缘的位置可能影响粘接剂的残留,黏膜上粘接边缘或平齐黏膜粘接边缘的基台设计相较于黏膜下粘接边缘,可以一定程度地减少残余粘接剂的量[3]。但在面对复杂的临床情况时,临床医师常常不能避免设计带有黏膜下粘接边缘的上部修复体。植体周软组织厚度是影响粘接边缘设计的重要因素,软组织厚度是覆盖牙槽嵴顶的软组织的垂直高度,在植体安装基台后,这个厚度会转化为植体上部修复体的穿黏膜高度。2017年Fuchigami等[22]研究发现,在非牙周炎失牙的位点,种植修复前软组织厚度为1~7 mm,平均厚度为3.6 mm,而在因牙周炎失牙的位点,软组织厚度为1.5~9.0 mm,平均厚度为3.8 mm,且与拔牙前牙周炎症程度呈正相关[23]。成品基台的穿黏膜高度通常为1~3 mm,难于匹配软组织厚度过大的位点,致使粘接边缘位于临床难以彻底清除粘接剂的深度。以本研究所用种植系统为例,NobelReplace Esthetic Abutment®成品基台的穿黏膜高度仅有1 mm和3 mm可供术者选择,对于嵴顶黏膜厚度超过4 mm的常见临床状况,选用成品基台后粘接边缘位于黏膜下2 mm或以上,增加了粘接剂清除的难度。相较而言,本研究采用的CAD/CAM个性化基台可根据穿黏膜轮廓及黏膜厚度个性化设计边缘位置,从而使边缘在植体四周都位于黏膜下1 mm内的位置,避免了成品基台穿黏膜高度设计的局限性。
本研究结果显示,不论采用哪种检测方法,CCA1组与CCA2组间残留的粘接剂并无明显差异,SA1组与SA2组间残留的粘接剂亦无明显差异(表 2),但CCA组较SA组能显著减少粘接剂的残留,差异具有统计学意义。首先,可能是由于CAD/CAM个性化基台的边缘位置可根据黏膜厚度,将其设计在黏膜下1 mm以内的位置,不会出现粘接边缘位于黏膜下过深位置的现象,从而有利于粘接剂的清除[24]。其次,可能是成品基台的近远中径常显著小于实际缺牙区的近远中径,从而导致粘接界面与穿黏膜轮廓间出现倒凹(undercut)(图 4),即粘接边缘至穿黏膜轮廓边缘存在水平向间隙,很大程度妨碍了术者对粘接剂的清理,可加重粘接剂残留的现象[25],而个性化设计制作的基台的穿黏膜轮廓完全顺应植体周软组织的边缘形态,无倒凹,便于粘接剂的清除。再次,成品基台穿黏膜高度通常为1~3 mm,本研究采用的1 mm及3 mm成品基台,相对于患者5 mm的牙龈高度,粘接边缘分别位于黏膜下2 mm或4 mm,较深的粘接位置增加了临床有效清除粘接剂的难度[26]。因此,本研究结果显示,CAD/CAM个性化基台较成品基台利于临床工作中清除多余的粘接剂,从而有效减少粘接剂的残留,提示临床设计时应根据软组织厚度情况,将基台边缘设计在黏膜下1 mm内,以最大可能减少粘接剂残留,从而获得更好的临床效果。此外,尽管CCA1齐龈粘接边缘组残留粘接剂较CCA2龈下1 mm粘接边缘组多,但两组间的差异没有统计学意义。这与国际口腔种植学会共识报告相符[27],即肩台设计深度若超过龈下1.5 mm,粘接剂残留的风险将显著增加,而在龈下1.5 mm以内的不同肩台位置对粘接剂残留则无明显影响。本研究中CCA组间差异未见统计学意义,可能是由于测量误差,还需要在后续相关研究中优化条件,例如采用与全瓷冠色差较大的磷酸锌水门汀作为粘接剂以避免测量误差。
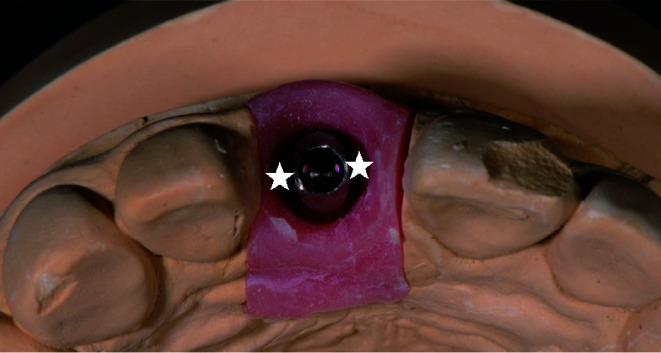
图 4.
成品基台周围的倒凹
Undercuts around stock abutments
☆, the undercut is the distance between the cementation line and the restoration emergence profile margin.
对于残留粘接剂的量化评估,传统方法存在一定的局限性。粘接剂的面积测量存在不同拍摄角度之间相同区域的粘接剂面积重复计算的现象,例如在图像分析唇面和近中面时,近中唇轴角处的粘接剂面积会在这两个角度重复算入,导致面积比例计算结果比实际大。而残留粘接剂的称重测量,不能反映粘接剂残余的面积及位置分布。实际上,残留粘接剂的危害,主要是作为局部刺激因素加速菌斑积聚[11, 28],其作用的强弱可能更多地和残留粘接剂的面积及分布位置有关。同样质量的粘接剂可能因为分散程度的不同而呈现出不同的危害性,此差异难以用称重的方式评估。牙颌模型三维扫描技术的兴起,使得数据的测量变得更为简便,以往在石膏模型上难以测量的数据可由实验者运用扫描技术准确获取[29]。本研究采用模型扫描的方法获取实验对象的三维立体数据,并通过布尔运算得到样本残余粘接剂的体积,能够直观且客观地反映出残留粘接剂的量及分布情况。本研究结果也进一步证实,三维扫描获取的残留粘接剂体积数据与残留粘接剂的面积百分比及其重量的测量数据高度相关,对评估残留粘接剂的量及位置分布有重要指导意义及临床参考价值。
综上所述,本研究结果提示,CAD/CAM个性化基台较成品基台能更有效地减少粘接剂的残留,从而更有利于植体周组织的长期健康和稳定。本研究结果初步说明三维扫描技术可以通过获取残留粘接剂的体积数据来反映粘接剂残留的量及位置分布,但其作为检测手段的效度和信度还需与实际体积做分析和比较以进一步验证。
Funding Statement
北京大学口腔医学院青年科研基金(YS020217)
Supported by Research Foundation of Peking University School and Hospital of Stomatology (YS020217)
References
- 1.Jung RE, Pjetursson BE, Glauser R, et al. A systematic review of the 5-year survival and complication rates of implant-supported single crowns. Clin Oral Implants Res. 2008;19(2):119–130. doi: 10.1111/j.1600-0501.2007.01453.x. [DOI] [PubMed] [Google Scholar]
- 2.Chee W, Felton DA, Johnson PF, et al. Cemented versus screw-retained implant prostheses: Which is better? Int J Oral Maxillofac Implants. 1999;14(1):137–141. [PubMed] [Google Scholar]
- 3.Linkevicius T, Vindasiute E, Puisys A, et al. The influence of margin location on the amount of undetected cement excess after delivery of cement-retained implant restorations. Clin Oral Implants Res. 2011;22(12):1379–1384. doi: 10.1111/j.1600-0501.2010.02119.x. [DOI] [PubMed] [Google Scholar]
- 4.Staubli N, Walter C, Schmidt JC, et al. Excess cement and the risk of peri-implant disease: A systematic review. Clin Oral Implants Res. 2017;28(10):1278–1290. doi: 10.1111/clr.12954. [DOI] [PubMed] [Google Scholar]
- 5.Korsch M, Obst U, Walther W. Cement-associated peri-implantitis: A retrospective clinical observational study of fixed implant-supported restorations using a methacrylate cement. Clin Oral Implants Res. 2014;25(7):797–802. doi: 10.1111/clr.12173. [DOI] [PubMed] [Google Scholar]
- 6.Wilson TG Jr. The positive relationship between excess cement and peri-implant disease: A prospective clinical endoscopic study. J Periodontol. 2009;80(9):1388–1392. doi: 10.1902/jop.2009.090115. [DOI] [PubMed] [Google Scholar]
- 7.Linkevicius T, Puisys A, Vindasiute E, et al. Does residual cement around implant-supported restorations cause peri-implant disease? A retrospective case analysis. Clin Oral Implants Res. 2013;24(11):1179–1184. doi: 10.1111/j.1600-0501.2012.02570.x. [DOI] [PubMed] [Google Scholar]
- 8.Ichikawa T, Ishida O, Watanabe M, et al. A new retrieval system for cement-retained implant superstructures: A technical report. J Prosthodont. 2008;17(6):487–489. doi: 10.1111/j.1532-849X.2008.00329.x. [DOI] [PubMed] [Google Scholar]
- 9.Galván G, Kois JC, Chaiyabutr Y, et al. Cemented implant restoration: A technique for minimizing adverse biologic consequences. J Prosthet Dent. 2015;114(4):482–485. doi: 10.1016/j.prosdent.2014.10.017. [DOI] [PubMed] [Google Scholar]
- 10.Seo CW, Seo JM. A technique for minimizing subgingival residual cement by using rubber dam for cement-retained implant crowns. J Prosthet Dent. 2017;117(2):327–328. doi: 10.1016/j.prosdent.2016.08.024. [DOI] [PubMed] [Google Scholar]
- 11.Linkevicius T. Zero bone loss concepts. Illinois: Quintessence Publishing Co; 2019. [Google Scholar]
- 12.Lewis S, Beumer J 3rd, Hornburg W, et al. The "UCLA" abutment. Int J Oral Maxillofac Implants. 1988;3(3):183–189. [PubMed] [Google Scholar]
- 13.戴 文雍, 汤 春波. 种植体修复个性化基台研究现状及展望. 口腔医学. 2012;32(11):685–687. [Google Scholar]
- 14.宿 玉成. 口腔种植学. 北京: 人民卫生出版社; 2014. pp. 403–404. [Google Scholar]
- 15.Shapoff CA, Lahey BJ. Crestal bone loss and the consequences of retained excess cement around dental implants. Compend Contin Educ Dent. 2012;33(2):94–101. [PubMed] [Google Scholar]
- 16.Schwarz F, Derks J, Monje A, et al. Peri-implantitis. J Clin Periodontol. 2018;45(Suppl 20):S246–S266. doi: 10.1111/jcpe.12954. [DOI] [PubMed] [Google Scholar]
- 17.Andersson B, Odman P, Lindvall AM, et al. Cemented single crowns on osseointegrated implants after 5 years: Results from a prospective study on CeraOne. Int J Prosthodont. 1998;11(3):212–218. [PubMed] [Google Scholar]
- 18.Linkevicius T, Vindasiute E, Puisys A, et al. The influence of the cementation margin position on the amount of undetected cement. A prospective clinical study. Clin Oral Implants Res. 2013;24(1):71–76. doi: 10.1111/j.1600-0501.2012.02453.x. [DOI] [PubMed] [Google Scholar]
- 19.Kappel S, Eiffler C, Lorenzo-Bermejo J, et al. Undetected resi-dual cement on standard or individualized all-ceramic abutments with cemented zirconia single crowns: A prospective randomized pilot trial. Clin Oral Implants Res. 2016;27(9):1065–1071. doi: 10.1111/clr.12691. [DOI] [PubMed] [Google Scholar]
- 20.Kotsakis GA, Zhang L, Gaillard P, et al. Investigation of the association between cement retention and prevalent peri-implant diseases: A cross-sectional study. J Periodontol. 2016;87(3):212–220. doi: 10.1902/jop.2015.150450. [DOI] [PubMed] [Google Scholar]
- 21.Daubert DM, Weinstein BF, Bordin S, et al. Prevalence and predictive factors for peri-implant disease and implant failure: A cross-sectional analysis. J Periodontol. 2015;86(3):337–347. doi: 10.1902/jop.2014.140438. [DOI] [PubMed] [Google Scholar]
- 22.Fuchigami K, Munakata M, Kitazume T, et al. A diversity of peri-implant mucosal thickness by site. Clin Oral Impl Res. 2017;28(2):171–176. doi: 10.1111/clr.12778. [DOI] [PubMed] [Google Scholar]
- 23.张 众, 孟 焕新, 韩 劼, et al. 软组织垂直厚度对牙周炎患者种植修复临床效果的影响. 北京大学学报(医学版) 2020;52(2):332–338. [Google Scholar]
- 24.Dumbrigue HB, Abanomi AA, Cheng LL. Techniques to minimize excess luting agent in cement-retained implant restorations. J Prosthet Dent. 2002;87(1):112–114. doi: 10.1067/mpr.2002.119418. [DOI] [PubMed] [Google Scholar]
- 25.Vindasiute E, Puisys A, Maslova N, et al. Clinical factors influencing removal of the cement excess in implant-supported restorations. Clin Implant Dent Relat Res. 2015;17(4):771–778. doi: 10.1111/cid.12170. [DOI] [PubMed] [Google Scholar]
- 26.Andersson B, Odman P, Lindvall AM, et al. Single-tooth restorations supported by osseointegrated implants: results and experiences from a prospective study after 2 to 3 years. Int J Oral Maxillofac Implants. 1995;10(6):702–711. [PubMed] [Google Scholar]
- 27.Higginbottom F, Belser U, Jones JD, et al. Prosthetic management of implants in the esthetic zone. Int J Oral Maxillofac Implants. 2004;19(Suppl):62–72. [PubMed] [Google Scholar]
- 28.Berglundh T, Lindhe J, Marinello C, et al. Soft tissue reaction to de novo plaque formation on implants and teeth. An experimental study in the dog. Clin Oral Implants Res. 1992;3(1):1–8. doi: 10.1034/j.1600-0501.1992.030101.x. [DOI] [PubMed] [Google Scholar]
- 29.高 鹏程, 谢 理哲, 严 斌. 牙颌模型三维数字化技术及其在口腔正畸学中的应用进展. 口腔生物医学. 2014;5(3):152–157. [Google Scholar]