Summary
Pseudomonas æruginosa est parmi les germes les plus incriminés dans les infections chez les brûlés. Les souches isolées sont souvent multirésistantes, compliquant la prise en charge de ces patients. Notre objectif était d’étudier les densités d’incidence de la colonisation et de l’infection à Pseudomonas æruginosa ainsi que la résistance aux antibiotiques des souches isolées chez les patients hospitalisés dans le service de réanimation des brûlés du Centre de Traumatologie et des Grands Brûlés (CTGB) en Tunisie. Il s’agit d’une étude rétrospective incluant 1 649 souches non répétitives de Pseudomonas æruginosa isolées durant une période de 8 ans (2012-2019). Pseudomonas æruginosa était le germe dominant de l’écologie bactérienne dans le service de réanimation des brûlés au CTGB (15%). Les densités d’incidence de la colonisation et de l’infection à Pseudomonas æruginosa étaient de 16,1‰ journées d’hospitalisations (JH) et 16,5‰ JH, respectivement. Une corrélation positive et statistiquement significative a été retrouvée entre la colonisation et l’infection à Pseudomonas æruginosa (rs=1; p=0,004). Les souches de colonisation étaient essentiellement des souches de colonisation cutanée (25,1%) et de cathéters centraux (22,3%). Les bactériémies dominaient les infections (19,5%). Elles étaient à point de départ cutané dans 22,1% des cas et liées aux cathéters dans 18,3% des cas. Les taux d’antibiorésistance étaient élevés allant jusqu’à 72,4% pour la pipéracilline- tazobactame (TZP), 49,4% pour la ceftazidime (CAZ), 74% pour le méropénème (MEM), 70,5% pour l’imipénème (IPM), 74,6% pour l’amikacine (AMK), 56,5% pour la ciprofloxacine (CIP) et 35,3% pour la fosfomycine (FOF). Aucune souche n’était résistante à la colistine (CST). Le taux des bactéries multi-résistantes était de 78%. Le taux des souches productrices de métallo-carbapénèmase était de 14,4%.
Keywords: Pseudomonas æruginosa, colonisation, infection, brûlés, antibiorésistance
Abstract
Pseudomonas æruginosa (PA) is among the major agents of infection in burns. Multidrug-resistant strains are commonly isolated, which hampers the management of these patients. Our purpose was to study the incidence density of PA colonization and PA infection and to investigate the antibiotic susceptibility of strains isolated in patients hospitalized in the Trauma and Burn Center’s Burn Unit (TBC-BU) in Tunisia. It is a retrospective study including 1649 non-repetitive strains of PA during an 8-year period (2012- 2019). PA was the most common organism in TBC-BU bacterial ecology (15%). The incidence density of PA colonization and PA infection was 16.1‰ days of in-patient stay (DH) and 16.5‰ DH, respectively. A positive and statistically significant correlation was found between PA colonization and PA infection (rs=1; p=0,004). The colonization strains were mainly isolated from skin (25.1%) and central catheters (22.3%). Bacteremia was the most common infection (19.5%). The skin was the most common source of bacteremia (22.1%) followed by central catheters (18.3%). The highest rates of antibiotic resistance were found with piperacillin-tazobactam (72.4%), ceftazidime (49.4%), meropenem (74%), imipenem (70.5%), amikacin (74.6%), ciprofloxacin (56.5%) and fosfomycin (35.3%). We did not identify any colistin-resistant strain. The multidrug resistance rate was 78%. The metallo-carbapenemase-producing strains rate was 14.4%.
Introduction
Pseudomonas æruginosa (P. æruginosa) est un germe opportuniste, essentiellement responsable d’infections nosocomiales. Le grand brûlé, patient immunodéprimé, nécessitant souvent des procédures invasives et ayant une flore déséquilibrée par des prises répétées d’antibiotiques, est particulièrement à risque d’être colonisé et infecté par cette bactérie.1,2
En effet, P. æruginosa est parmi les premiers germes incriminés dans les infections chez les brûlés dans le monde entier.3-5 Les infections à P. æruginosa sont responsables d’une morbi-mortalité surajoutée, d’une prolongation de la durée et augmentation du coût du séjour hospitalier.6 Les infections à P. æruginosa sont parmi les premières causes de mortalité chez le grand brûlé.7 Cette gravité est le résultat d’une virulence accrue sur un terrain fragilisé et d’un niveau élevé d’antibiorésistance aussi bien naturelle qu’acquise.8-11 Ce germe ubiquiste est capable de contaminer l’environnement, en particulier hydrique, et de survivre longtemps sur les surfaces inertes, facilitant ainsi sa transmission. Plusieurs études indiquent que les points d’eau représentent un réservoir important de P. æruginosa et une source de contamination dans les unités de réanimation.12
Ceci expliquerait, en partie, que cette bactérie sévisse à l’état endémique dans plusieurs centres hospitaliers, avec des pics épidémiques.2,13 Le but de notre travail était d’étudier les densités d’incidence de la colonisation et de l’infection à P. æruginosa ainsi que la résistance aux antibiotiques des souches isolées chez les patients hospitalisés dans le service de réanimation des brûlés du Centre de Traumatologie et des Grands Brûlés (CTGB) de Ben Arous en Tunisie sur une période de 8 ans (2012-2019).
Matériel et méthodes
Nous avons mené une étude rétrospective descriptive transversale unicentrique, menée sur une période de 8 ans (janvier 2012 – décembre 2019). Elle a eu lieu dans le service de réanimation des brûlés du CTGB à Ben Arous en Tunisie. Pendant la période d’étude, le nombre moyen d’admissions était de 347 par an et le nombre moyen de journées d’hospitalisation était de 6 313 par an. Notre étude a concerné toutes les souches non répétitives de P. æruginosa isolées chez les patients hospitalisés dans le service de réanimation des brûlés du CTGB pendant la période d’étude, qu’elles soient des souches de colonisation ou des souches d’infection. Les souches isolées à partir des prélèvements d’hygiène n’ont pas été incluses dans notre étude. Les souches de P. æruginosa dont l’antibiogramme n’a pas été réalisé, faute de moyens techniques (manque de disques d’antibiotiques), ont été exclues de notre étude. L’analyse des différents prélèvements bactériologiques parvenus au laboratoire de biologie médicale du CTGB était réalisée selon les recommandations du Référentiel en Microbiologie médicale.14 L’identification bactérienne a été faite selon les méthodes conventionnelles en se basant sur des caractères morphologiques (bacille à Gram négatif avec une mobilité polaire), culturaux (pigmentation verte sur gélose ordinaire, odeur fruitée de raisin) et biochimiques (présence de cytochrome oxydase). Une identification biochimique par Api 20NE (Bio Mérieuxâ) a été réalisée chaque fois que la souche n’était pas pigmentée. L’étude de la sensibilité aux antibiotiques des souches isolées a été réalisée selon les normes du Comité de l’Antibiogramme de la Société Française de Microbiologie, actualisées chaque année. L’antibiogramme a été réalisé par la technique de diffusion en milieu gélosé Mueller Hinton. La concentration minimale inhibitrice (CMI) de la colistine a été déterminée par la méthode E-test® (bioMérieux®) pour les souches isolées avant mai 2017 et par micro-dilution en milieu liquide Umic® (Biocentric®) pour les souches isolées après mai 2017. Un test phénotypique à l’EDTA a été réalisé chez les souches résistantes à l’imipénème. Une souche a été définie comme répétitive si elle a été isolée à partir du même type de prélèvement, à moins de 30 jours d’intervalle, avec un même antibiotype.15 Une souche multirésistante (BMR) a été définie par la résistance à au moins une molécule dans au moins trois familles d’antibiotiques.16 Une colonisation cutanée a été retenue devant une souche de P. æruginosa isolée à partir d’un écouvillonnage cutané des zones saines ou des zones brûlées en dehors de signes cliniques d’infection cutanée. Les souches isolées à partir des cathéters centraux (veineux ou artériels) étaient considérées des souches de colonisation en l’absence de signes cliniques d’infection. Une colonisation digestive et une colonisation nasale ont été retenues devant une souche de P. æruginosa isolée à partir d’écouvillonnage rectal ou nasal réalisé systématiquement à la recherche de BMR chez tous les patients à l’admission. Une infection cutanée a été retenue devant une souche isolée à partir d’un écouvillonnage cutané en présence de signes cliniques d’infection cutanée.17 Les souches isolées à partir d’hémocultures, des prélèvements respiratoires, urinaires, des pus et des ponctions étaient considérées des souches d’infections. Une bactériémie liée au cathéter (BLC) était définie par au moins une hémoculture périphérique positive à P. æruginosa chez un patient porteur de cathéter central ou dans les 24 heures suivant le retrait de ce dernier, avec une culture positive du cathéter (> 103 UFC/ml) à la même souche que celle isolée dans l’hémoculture périphérique (même antibiogramme).18 Une bactériémie à point de départ cutané était définie par au moins une hémoculture positive à P. æruginosa chez un patient ayant un prélèvement cutané positif à la même souche isolée dans l’hémoculture (même antibiogramme). Étaient considérés des anti-pseudomonas majeurs les antibiotiques suivants : TZP, CAZ, IPM, AMK et CIP.19,20 Les données ont été saisies et exploitées par le logiciel Excel. Le test de corrélation des rangs de Spearman (rs) a été utilisé pour l’étude de la corrélation entre la colonisation et l’infection à P. æruginosa ainsi que pour l’étude de l’évolution annuelle des taux, des densités d’incidence et de la résistance aux antibiotiques. Le seuil de signification (p) a été fixé à 0,05 pour tous les tests statistiques.
Résultats
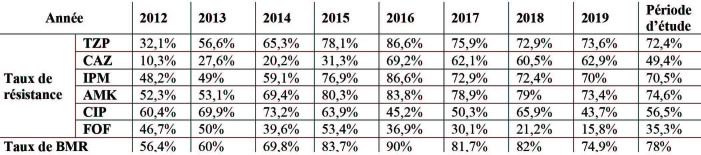
répétitives de P. æruginosa ont été colligées, représentant ainsi la principale espèce bactérienne isolée dans le service de réanimation des brûlés du CTGB avec un taux moyen de 15% de l’écologie du service. Le taux d’isolement des souches de P. æruginosa est passé de 10,6% en 2012 à 20,1% en 2016 (rs=0,9 ; p=0,08) puis a diminué d’une façon non significative pour atteindre 10,4% en 2019 (rs= -1 ; p=0,08- Fig.1). On dénombrait 815 souches de colonisation (49,4%) et 834 souches d’infection (50,6%). Les densités d’incidences (DI) de colonisation et d’infection à P. æruginosa dans le service de réanimation des brûlés étaient de 16,1‰ journées d’hospitalisation (JH) et 16,5‰ JH, respectivement. De 2012 à 2017, la DI de la colonisation a augmenté d’une façon statistiquement significative (rs=0,8 ; p=0,05- Fig. 2). Pendant la même période, l’augmentation de la DI de l’infection était statistiquement non significative (rs=0,7 ; p=0,1- Fig. 2). À partir de 2017, les DI de la colonisation et de l’infection ont progressivement diminué mais de façon non significative (rs=-1 ; p=0,3- Fig. 2). L’étude statistique a montré une corrélation positive et significative entre la colonisation et l’infection à P. æruginosa (rs=0,9 ; p=0,004). Les souches de colonisation étaient essentiellement retrouvées dans des prélèvements cutanés (25,1%) et des cultures de cathéters (22,3%) (Tableau I). Les infections étaient dominées par les bactériémies (19,5%) et les infections cutanées (12%), suivies par les infections urinaires (9,5%) et les infections respiratoires (7,8%) (Tableau I). La porte d’entrée des bactériémies a été microbiologiquement identifiée dans 55,6% des cas (Tableau II). La plus fréquente était la porte d’entrée cutanée (22,1%). Les BLC représentaient 18,3% des bactériémies. Les portes d’entrée urinaire et respiratoire ne représentaient que 9% et 6,2%, respectivement. Les taux de résistance aux β-lactamines étaient de 72,4% pour TZP, de 49,4% pour CAZ, de 74% pour MEM et de 70,5% pour IPM. Les taux de résistance à AMK, CIP et FOF étaient de 74,6%, 56,5% et 35,3%, respectivement. Parmi nos souches, 78% étaient des BMR mais restaient toutes sensibles à la CST. Pendant la période d’étude, le taux de résistance à CAZ a augmenté d’une façon statistiquement significative (rs=0,8 ; p=0,02). De 2012 à 2016, les taux de résistance à TZP, IPM et AMK ont augmenté d’une façon statistiquement significative, ainsi que le taux de BMR (rs=1 ; p=0,01 pour toutes ces variables). Puis, de 2016 à 2019, ces taux ont diminué, mais d’une façon non significative (rs= [-1 à -0,8] ; p= [0,08 à 0,3]). De 2012 à 2019, le taux de résistance à CIP oscillait entre 43% et 73% sans tendance évolutive particulière (rs=-0,5 ; p=0,1). Le taux de résistance à FOF, quant à lui, a diminué d’une façon significative pendant la même période (2012-2019) (rs=-0,8 ; p=0,01- Tableau III). Il n’y avait pas de différence statistiquement significative des taux de résistances aux antibiotiques chez les souches de colonisation par rapport aux souches d’infection (p>0,05- Tableau IV). Parmi toutes les souches résistantes à l’imipénème, 21,2% (246/1162) avaient un test phénotypique à l’EDTA qui était positif. Ainsi, le taux des souches productrices de métallo-carbapénèmase, parmi toutes les souches étudiées, était de 14,9% (246/1649).
Fig. 1. Évolution annuelle du taux d’isolement des souches de Pseudomonas æruginosa (2012-2019).
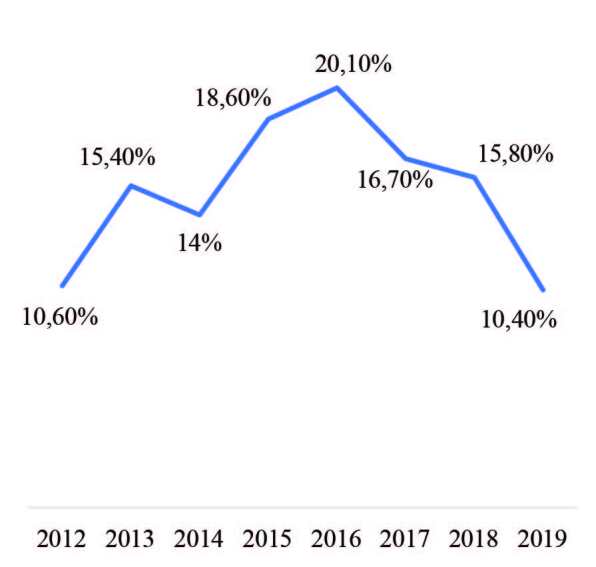
Fig. 2. Évolution annuelle des densités d’incidence de la colonisation et de l’infection à Pseudomonas æruginosa (2012-2019).
Tableau I. Répartition des souches de Pseudomonas æruginosa isolées dans le service de réanimation des brûlés selon le type de prélèvement (2012-2019).
Tableau II. Évolution annuelle des souches de Pseudomonas æruginosa responsables de bactériémies et leur répartition selon la porte d’entrée (2012-2019).
Tableau III. Évolution annuelle des taux de résistance aux antibiotiques des souches de Pseudomonas æruginosa (2012-2019).
Tableau IV. Comparaison des taux de résistance entre les souches de colonisation et les souches d’infection à Pseudomonas æruginosa (2012-2020).

Discussion
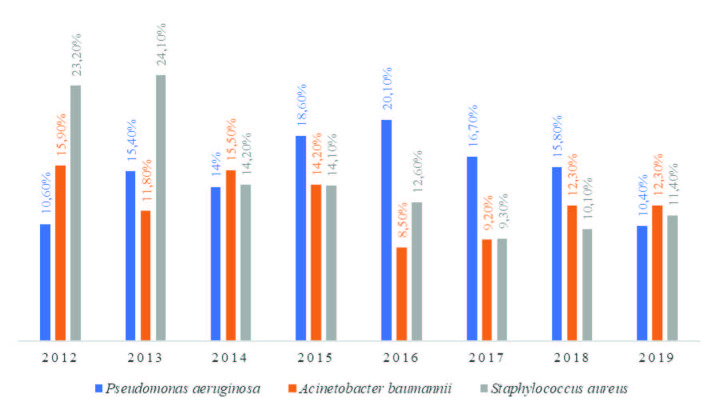
P. æruginosa est parmi les germes les plus incriminés dans les infections chez les brûlés dans le monde entier.3-5,21-22 Les infections à P. æruginosa sont souvent difficiles à traiter en raison des nombreux mécanismes de résistance de ces bactéries, de leur pouvoir de production de biofilm et de leur persistance dans l’environnement, en particulier hydrique, compliquant ainsi la prise en charge des grands brûlés.9,23,24 Elles sont responsables d’une morbi-mortalité surajoutée, de prolongation de la durée et d’une augmentation du coût du séjour hospitalier. 6 Notre étude rétrospective s’est intéressée à la colonisation et à l’infection à P. æruginosa chez les brûlés hospitalisés dans le service de réanimation des brûlés du CTGB, durant une période de huit ans (2012-2019). P. æruginosa était le germe dominant de l’écologie bactérienne dans notre service avec un taux moyen de 15%. Des taux aussi élevés sont également observés dans d’autres unités de soins intensifs, à cause du terrain fragilisé des patients et de la fréquence des manoeuvres invasives.13,22,25,26 De 2012 à 2015, Staphylococcus aureus dominait l’écologie de notre service.27 Pendant cette période, le taux d’isolement de P. æruginosa a augmenté progressivement pour devenir dominant de 2016 jusqu’à 2018. En 2019, P. æruginosa occupait la troisième place après Acinetobacter baumannii et Staphylococcus aureus (Fig. 3). Les densités d’incidence de la colonisation et de l’infection à P. æruginosa dans notre service étaient de 16,1‰ JH et 16,5‰ JH, respectivement. Elles avaient une évolution parallèle au cours des années, avec une corrélation positive et statistiquement significative. Ceci suggère la présence d’une relation de causalité entre la colonisation et l’infection à P. æruginosa. En effet, dans la littérature, il a été démontré qu’une colonisation antérieure par P. æruginosa est un facteur de risque d’infection par ce germe.28,29 Cohen et al. ont montré qu’un patient colonisé par P. æruginosa est plus à risque de développer une infection par comparaison à un patient non colonisé avec un Hazard Ratio = 14,6 (p=0,0002).29 Dans notre étude, les souches de colonisation étaient essentiellement cutanées (25,1%). Ceci s’expliquerait par l’altération de la barrière cutanée chez le grand brûlé avec diminution importante des défenses immunitaires locales. La zone brûlée, étant une zone peu vascularisée, chaude et humide, constitue un milieu propice pour le développement de cette bactérie.30 Le risque de colonisation et d’infection à P. æruginosa s’accroît avec la durée de l’hospitalisation, les traitements antibiotiques antérieures et la diminution des défenses de l’organisme.28,31,32 En plus de l’origine endogène à partir d’un site colonisé (peau, tube digestif…), l’infection à P. æruginosa peut avoir une origine exogène à partir des réservoirs environnementaux, du matériel contaminé ou par le personnel soignant (manuportage).12,26,28,33 Le taux d’acquisition exogène de P. æruginosa en milieu de réanimation est de 50% en moyenne, pouvant atteindre jusqu’à 70%.12,28 En effet, P. æruginosa est un germe ubiquiste pouvant survivre longtemps en milieu hydrique, même pauvre en nutriments (lavabos, humidificateurs, respirateurs…) et même dans certaines solutions antiseptiques telles que les ammoniums quaternaires.12,28 Dans notre étude, les bactériémies dominaient les infections avec un taux de 19,5%. En effet, les patients hospitalisés aux unités de soins intensifs, ayant une immunité compromise, tels que les grands brûlés, sont à haut risque de développer une bactériémie à P. æruginosa.34
Fig. 3. - Évolution annuelle des taux d’isolement de Pseudomonas æruginosa, Acinetobacter baumannii et Satphylococcus aureus(2012-2019).
Ceci est expliqué par une virulence complexe caractéristique de ce germe, qui s’exprime préférentiellement chez le sujet immunodéprimé, faisant ainsi de cette bactérie l’exemple type de bactérie opportuniste. 8 Le taux de BLC était de 18,3%. La présence d’un cathéter central augmente le risque de colonisation et d’infection par P. æruginosa.35,36 Ceci s’expliquerait, sur le plan physiopathologique, par la capacité de cette bactérie à produire un biofilm lui permettant d’adhérer aux surfaces inertes, de se protéger contre les défenses de l’hôte et de réduire la diffusion de certains antibiotiques.24,36 Le risque lié au cathéter central augmente avec le nombre de lumières, la fréquence des manipulations et la durée du cathétérisme.37 Dans notre travail, les infections respiratoires ne représentaient que 7,8%, moins que les infections cutanées (12%) et les infections urinaires (9,5%). Ceci rejoint les résultats d’une étude colombienne récente, réalisée dans un centre de brûlés, qui a retrouvé un taux d’infections respiratoires de 8,6%, inférieur aux infections urinaires (19%) et cutanées (14,7%).38 En revanche, des études américaines et européennes, réalisées sur une population hétérogène de patients hospitalisés dans différents services (médicaux, chirurgicaux, réanimation, oncohématologie…) ont montré que les voies aériennes sont le principal site d’isolement de P. æruginosa.39,40 L’étude de la sensibilité aux antibiotiques a montré des taux très élevés de résistance aux anti-pseudomonas majeurs : 72,4% à TZP, 49,4% à CAZ, 70,5% à IPM, 74,6% à AMK et 56,5% à CIP. Une autre étude, réalisée dans notre service de 2008 à 2011 avait montré des taux plus faibles de résistance : 34% à CAZ, 37,1% à IPM, 29,6% à AMK et 27,1% à CIP.41 Par ailleurs, des études plus récentes réalisées chez les brûlés dans différents pays ont montré des résultats aussi élevés que les nôtres. 5,42,43 Le taux de BMR dans notre série était de 78%. Ce taux élevé, retrouvé également dans d’autres études, pose un vrai problème de santé publique à l’échelle mondiale.5,43,44 En effet, le sepsis dû à des souches de BMR, en chef de file P. æruginosa, est la principale cause de décès chez le brûlé.7,45,46 Parmi les facteurs de risque d’acquisition d’une souche BMR de P. æruginosa, on retrouve dans la littérature : la consommation antérieure de carbapénèmes et de fluoroquinolones, la présence de cathéter veineux central, l’étendue de la surface cutanée brûlée, l’alimentation parentérale et l’immunodépression. 9,13,31,47-49 Toutes nos souches BMR étaient sensibles à la colistine, qui reste parfois, malgré ses effets indésirables, l’option thérapeutique ultime devant des souches multi et hautement résistantes de P. æruginosa.30,34,43 De 2012 à 2016, les taux de résistance à TZP, CAZ, IPM et AMK ont augmenté de façon significative. Cette tendance à la hausse des taux de résistance aux anti-pseudomonas majeurs les plus prescrits a été rapportée par d’autres auteurs. 5,11,42 Elle s’expliquerait par la capacité de cette bactérie à s’adapter au milieu hospitalier, notamment dans les unités de soins intensifs, où la pression de sélection des antibiotiques est très importante. La sélection de mutants résistants est d’autant plus favorisée par la prescription d’antibiotiques à des doses suboptimales.50 P. æruginosa est caractérisé par la plasticité de son génome, lui permettant une acquisition facile et rapide de nouveaux mécanismes de résistances très divers.34 Pendant la période 2016- 2019, les taux de résistance à TZP, IPM et AMK ont diminué d’une façon non significative. Ceci pourrait s’expliquer par une baisse de la consommation de ces antibiotiques dans le service de réanimation des brûlés du CTGB pendant la même période (étude en cours, résultats non encore publiés). En effet, plusieurs études montrent un parallélisme entre le niveau de consommation d’un antibiotique et le taux de résistance correspondant.51,52 Parmi toutes les souches résistantes à l’imipénème, 21,2% étaient productrices de métallo-carbapénèmase. Ce taux est similaire à ceux retrouvés dans d’autres études réalisées chez des patients brûlés hospitalisés dans des unités de réanimation.53,54 En revanche, dans une autre étude réalisée sur 255 souches de P. æruginosa résistants à l’imipénème isolées chez des patients brûlés, aucun test à l’EDTA n’était positif et l’étude moléculaire n’a confirmé la présence de métallo-carbapénèmase que chez 9 souches seulement (3,5%).55
Une étude antérieure, réalisée sur des souches de P. æruginosa résistantes à l’imipénème et isolées dans le service de réanimation des brûlés du CTGB a montré la prédominance du gène blaVIM-2.56c Devant l’émergence de souches multi et hautement résistantes de P. æruginosa, les mesures de prévention doivent être prises et appliquées rigoureusement. Ces mesures consistent essentiellement à isoler les patients porteurs de souches multirésistantes, renforcer les mesures d’hygiène (lavage des mains, port des équipements de protection individuelle…), rationnaliser la prescription des antibiotiques, surveiller régulièrement les résistances bactériennes afin d’adapter les schémas thérapeutiques et contrôler régulièrement l’environnement afin de limiter la transmission des souches environnementales.28,57,58 Notre étude avait l’avantage d’étudier une population assez particulière de patients qui sont les grands brûlés, sur une longue période de huit ans. De plus, très peu d’auteurs se sont intéressés à la fois à la colonisation et à l’infection à P. æruginosa dans une même étude. Cependant, elle avait certaines limites telles que l’absence d’analyse des données démographiques et des caractéristiques cliniques des patients et l’absence de confirmation moléculaire de la production de métallo-carbapénèmase. Par ailleurs, l’étude de la clonalité des souches de P. æruginosa responsables de colonisation et d’infection, ainsi que celles isolées dans l’environnement hospitalier, serait intéressante pour déterminer le réservoir du P. æruginosa et son mode de transmission, et mieux contrôler ainsi les infections dues à ce germe.
Conclusion
Notre étude a montré des densités d’incidences élevées de colonisation et d’infection à P. æruginosa avec une corrélation significative entre la colonisation et l’infection. Un taux élevé de BMR, notamment des souches productrices de métallo-carbapénèmases, a été retrouvé aussi bien chez les souches responsables de colonisation que celles d’infections. Ceci impose le renforcement des mesures d’hygiène et le bon usage des antibiotiques afin de limiter la diffusion de cette bactérie et la sélection de mutants résistants.
References
- 1.Siah S, Belefqih R, Elouennass M. L’infection nosocomiale en réanimation des brûlés. Ann Burns Fire Disasters. 2009;22:72–78. [PMC free article] [PubMed] [Google Scholar]
- 2.Berthelot P, Grattard F, Mallaval FO. Épidémiologie des infections nosocomiales à Pseudomonas æruginosa, Burkholderia cepacia et Stenotrophomonas maltophilia. Pathol Biol. 2005;53:341–348. doi: 10.1016/j.patbio.2004.09.006. [DOI] [PubMed] [Google Scholar]
- 3.Yin S, Chen P, You B, Zhang Y. Molecular typing and carbapenem resistance mechanisms of Pseudomonas æruginosa isolated from a Chinese burn center from 2011 to 2016. Front Microbiol. 2018 doi: 10.3389/fmicb.2018.01135. téléchargeable depuis: https://www.frontiersin.org/articles/10.3389/fmicb.2018.01135/full . [DOI] [PMC free article] [PubMed] [Google Scholar]
- 4.Sousa D, Ceniceros A, Galeiras R, Pértega-Díaz S. Microbiology in burns patients with blood stream infections: trends over time and during the course of hospitalization. Infect Dis. 2018;50:122. doi: 10.1080/23744235.2017.1397738. [DOI] [PubMed] [Google Scholar]
- 5.Dou Y, Huan J, Guo F. Pseudomonas æruginosa prevalence, antibiotic resistance and antimicrobial use in Chinese burn wards from 2007 to 2014. J Int Med Res. 2017;45:1124–1137. doi: 10.1177/0300060517703573. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 6.Morales E, Cots F, Sala M. Hospital costs of nosocomial multi-drug resistant Pseudomonas æruginosa acquisition. BMC Health Serv Res. 2012;12:122. doi: 10.1186/1472-6963-12-122. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 7.Williams F, Herndon D, Hawkins H. The leading causes of death after burn injury in a single pediatric burn center. Crit Care. 2009;13:R183. doi: 10.1186/cc8170. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 8.De Bentzmann S. Pseudomonas æruginosa: une virulence complexe. Rev Francoph Lab. 2011:73–81. [Google Scholar]
- 9.Palavutitotai N, Jitmuang A, Tongsai S. Epidemiology and risk factors of extensively drug-resistant Pseudomonas æruginosa infections. PLoS ONE. 2018;13:20188. doi: 10.1371/journal.pone.0193431. téléchargeable depuis: https://www.ncbi.nlm.nih.gov/pmc/articles/ PMC5823452/ [DOI] [PMC free article] [PubMed] [Google Scholar]
- 10.Breidenstein E, de la Fuente-Núñez C, Hancock R. Pseudomonas æruginosa: all roads lead to resistance. Trends Microbiol. 2011;19:419–426. doi: 10.1016/j.tim.2011.04.005. [DOI] [PubMed] [Google Scholar]
- 11.Mérens A, Delacour H, Plésiat P, Cavallo J-D. Pseudomonas æruginosa et résistance aux antibiotiques. Rev Francoph Lab. 2011;2011:49–62. [Google Scholar]
- 12.Floret N, Bertrand X, Thouverez M. Infections nosocomiales à Pseudomonas æruginosa : origine exogène ou endogène de la bactérie responsable ? Pathol Biol. 2009;57:9–12. doi: 10.1016/j.patbio.2008.07.011. [DOI] [PubMed] [Google Scholar]
- 13.Fournier A, Voirol P, Krähenbühl M. Antibiotic consumption to detect epidemics of Pseudomonas æruginosa in a burn centre: a paradigm shift in the epidemiological surveillance of Pseudomonas æruginosa nosocomial infections. Burns. 2016;42:564–570. doi: 10.1016/j.burns.2015.10.030. [DOI] [PubMed] [Google Scholar]
- 14.Société Française de Microbiologie. REMIC : Référentiel en microbiologie médicale. 5ème édition. Paris,: Société Française de Microbiologie; 2015. [Google Scholar]
- 15.Résistance bactérienne aux antibiotiques. Données de l’observatoire national de l’épidemiologie de la résistance bactérienne (ONERBA). Med Mal Infect. 2005;35:155–169. doi: 10.1016/j.medmal.2004.07.030. [DOI] [PubMed] [Google Scholar]
- 16.Magiorakos A-P, Srinivasan A, Carey R. Multidrug-resistant, extensively drug-resistant and pandrug-resistant bacteria: an international expert proposal for interim standard definitions for acquired resistance. Clin Microbiol Infect. 2012;18:268–281. doi: 10.1111/j.1469-0691.2011.03570.x. [DOI] [PubMed] [Google Scholar]
- 17.Ravat F, Le-Floch R, Vinsonneau C. Antibiotics and the burn patient. Burns. 2011;37(1):16–26. doi: 10.1016/j.burns.2009.10.006. [DOI] [PubMed] [Google Scholar]
- 18.Mermel L, Allon M, Bouza E. Clinical practice guidelines for the diagnosis and management of intravascular catheter-related infection: 2009 update by the Infectious Diseases Society of America. Clin Infect Dis. 2009;49:1–45. doi: 10.1086/599376. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 19.Buhl M, Peter S, Willmann M. Prevalence and risk factors associated with colonization and infection of extensively drug-resistant Pseudomonas æruginosa: a systematic review. Expert Rev Anti Infect Ther. 2015;13:1159–1170. doi: 10.1586/14787210.2015.1064310. [DOI] [PubMed] [Google Scholar]
- 20.ECDC, EFSA and EMA Joint Scientific Opinion on a list of outcome indicators as regards surveillance of antimicrobial resistance and antimicrobial consumption in humans and food-producing animals. EFSA J. 2017;15:e05017. doi: 10.2903/j.efsa.2017.5017. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 21.Branski L, Al-Mousawi A, Rivero H. Emerging infections in burns. Surg Infect. 2009;10:389–397. doi: 10.1089/sur.2009.024. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 22.Singh NP, Goyal R, Manchanda V. Changing trends in bacteriology of burns in the burns unit, Delhi, India. Burns. 2003;29:129–132. doi: 10.1016/s0305-4179(02)00249-8. [DOI] [PubMed] [Google Scholar]
- 23.Jabalameli F, Mirsalehian A, Khoramian B. Evaluation of biofilm production and characterization of genes encoding type III secretion system among Pseudomonas æruginosa isolated from burn patients. Burns. 2012;38:1192–1197. doi: 10.1016/j.burns.2012.07.030. [DOI] [PubMed] [Google Scholar]
- 24.Ghanbarzadeh Corehtash Z, Khorshidi A, Firoozeh F. Biofilm formation and virulence factors among Pseudomonas æruginosa isolated from burn patients. Jundishapur J Microbiol. 2015 doi: 10.5812/jjm.22345. téléchargeable depuis: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4644346/ [DOI] [PMC free article] [PubMed] [Google Scholar]
- 25.Trubiano J, Padiglione A. Nosocomial infections in the intensive care unit. Anaesth Intensive Care Med. 2015;16:598–602. [Google Scholar]
- 26.Abdallah H, Noomen S, Khélifa A. Profil de sensibilité aux antibiotiques des souches de Pseudomonas æruginosa isolées dans la région de Monastir. Med Mal Infect. 2008;38:554–556. doi: 10.1016/j.medmal.2008.05.002. [DOI] [PubMed] [Google Scholar]
- 27.Krir A, Dhraief S, Messadi AA. Profil bactériologique et résistance aux antibiotiques des bactéries isolées dans un service de réanimation des brûlés durant sept ans. Ann Burns Fire Disasters. 219;32:197–202. [PMC free article] [PubMed] [Google Scholar]
- 28.Cabrolier N, Lafolie J, Bertrand X. Épidémiologie et facteurs de risques des infections liées à Pseudomonas æruginosa. J Anti-Infect. 2014;16:8–12. [Google Scholar]
- 29.Cohen R, Babushkin F. A prospective survey of Pseudomonas aeruginosa colonization and infection in the intensive care unit. Antimicrob Resist Infect Control. 2017;6(1):7. doi: 10.1186/s13756-016-0167-7. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 30.Norbury W, Herndon D, Tanksley J. Infection in burns. Surg Infect. 2016;17:250–255. doi: 10.1089/sur.2013.134. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 31.Samonis G, Vardakas K, Kofteridis D. Characteristics, risk factors and outcomes of adult cancer patients with extensively drug-resistant Pseudomonas æruginosa infections. Infection. 2014;42:721–728. doi: 10.1007/s15010-014-0635-z. [DOI] [PubMed] [Google Scholar]
- 32.Macedo J, Santos J. Bacterial and fungal colonization of burn wounds. Mem Inst Oswaldo Cruz. 2005;100:535–539. doi: 10.1590/s0074-02762005000500014. [DOI] [PubMed] [Google Scholar]
- 33.Tredget E, Shankowsky H, Joffe A. Epidemiology of infections with Pseudomonas æruginosa in burn patients: the role of hydrotherapy. Clin Infect Dis. 1992;15:941–949. doi: 10.1093/clind/15.6.941. [DOI] [PubMed] [Google Scholar]
- 34.Pachori P, Gothalwal R, Gandhi P. Emergence of antibiotic resistance Pseudomonas æruginosa in intensive care unit: a critical review. Genes Dis. 2019;6:109–119. doi: 10.1016/j.gendis.2019.04.001. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 35.Fortaleza C, Figueiredo L, Beraldo C. Risk factors of oropharyngeal carriage of Pseudomonas aeruginosa among patients from a Medical-Surgical Intensive Care Unit. Braz J Infect Dis. 2009;13:173–176. doi: 10.1590/s1413-86702009000300004. [DOI] [PubMed] [Google Scholar]
- 36.Donlan R. Biofilms and device-associated infections. Emerg Infect Dis. 2001;7:277–281. doi: 10.3201/eid0702.010226. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 37.Timsit JF. Réactualisation de la douzième conférence de consensus de la Société de Réanimation de Langue Française (SRLF) : infections liées aux cathéters veineux centraux en réanimation. Ann Fr Anesth Réanim. 2005;24:315–322. doi: 10.1016/j.annfar.2004.12.022. [DOI] [PubMed] [Google Scholar]
- 38.Ramirez-Blanco C, Ramirez-Rivero C, Diaz-Martinez L. Infection in burn patients in a referral center in Colombia. Burns. 2017;43:642–653. doi: 10.1016/j.burns.2016.07.008. [DOI] [PubMed] [Google Scholar]
- 39.Nesher L, Rolston K, Shah D. Fecal colonization and infection with Pseudomonas æruginosa in recipients of allogeneic hematopoietic stem cell transplantation. Transpl Infect Dis. 2015;17:33–38. doi: 10.1111/tid.12323. [DOI] [PubMed] [Google Scholar]
- 40.Van Eldere J. Multicentre surveillance of Pseudomonas æruginosa susceptibility patterns in nosocomial infections. J Antimicrob Chemother. 2003;51:347–352. doi: 10.1093/jac/dkg102. [DOI] [PubMed] [Google Scholar]
- 41.Thabet L, Zoghlami A, Boukadida J. Etude comparative de la résistance aux antibiotiques des principales bactéries isolées au service de Réanimation de brûlés durant deux périodes (2005- 2008, 2008-2011) et dans deux structures hospitalières (Hôpital Aziza Othmana, Centre de traumatologie et grands brûlés Ben Arous). Tunis Med. 2013;91:5. [PubMed] [Google Scholar]
- 42.Singh N, Rani M, Gupta K. Changing trends in antimicrobial susceptibility pattern of bacterial isolates in a burn unit. Burns. 2017;43(5):1083–1087. doi: 10.1016/j.burns.2017.01.016. [DOI] [PubMed] [Google Scholar]
- 43.Bhatt P, Rahti K, Hazra S. Prevalence of multidrug resistant Pseudomonas æruginosa infection in burn patients at a tertiary care centre. Indian Journal of Burns. 2015;23:56–59. [Google Scholar]
- 44.Almeida Silva K, Calomino MA, Deutsch G. Molecular characterization of multidrug-resistant (MDR) Pseudomonas æruginosa isolated in a burn center. Burns. 2017;43:137–143. doi: 10.1016/j.burns.2016.07.002. [DOI] [PubMed] [Google Scholar]
- 45.Anvarinejad M, Japoni A, Rafaatpour NJ. Burn patients infected with metallo-beta-lactamase-producing Pseudomonas æruginosa: multidrug-resistant strains. Arch Trauma Res. 2014;3:e181–e182. doi: 10.5812/atr.18182. téléchargeable depuis: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4139692/ [DOI] [PMC free article] [PubMed] [Google Scholar]
- 46.Safaei H, Moghim S, Isfahani B. Distribution of the strains of multidrug-resistant, extensively drug-resistant, and pandrugresistant Pseudomonas æruginosa isolates from burn patients. Adv Biomed Res. 2017;6:74. doi: 10.4103/abr.abr_239_16. téléchargeable depuis: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5501067/ [DOI] [PMC free article] [PubMed] [Google Scholar]
- 47.Falagas M. Risk factors for the isolation of multidrug-resistant Acinetobacter baumannii and Pseudomonas æruginosa:a systematic review of the literature. J Hosp Infect. 2006;64:7–15. doi: 10.1016/j.jhin.2006.04.015. [DOI] [PubMed] [Google Scholar]
- 48.Holt A, Severin J, Lesaffre E. A systematic review and meta-analyses show that carbapenem use and medical devices are the leading risk factors for carbapenem-resistant Pseudomonas æruginosa. Antimicrob Agents Chemother. 2014;58:2626–2637. doi: 10.1128/AAC.01758-13. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 49.Theodorou P, Thamm O, Perbix W. Pseudomonas æruginosa bacteremia after burn injury - the impact of multiple-drug resistance. J Burn Care Res. 2013;34:649–658. doi: 10.1097/BCR.0b013e318280e2c7. [DOI] [PubMed] [Google Scholar]
- 50.Richard P, Le Floch R, Chamoux C. Pseudomonas aeruginosa outbreak in a Burn Unit: role of antimicrobials in the emergence of multiple resistant strains. J Infect Dis. 1994;171(2):377–383. doi: 10.1093/infdis/170.2.377. [DOI] [PubMed] [Google Scholar]
- 51.Monnet D. Consommation d’antibiotiques et résistance bactérienne. Ann Fr Anesth Réanim. 2000;19:409–417. doi: 10.1016/s0750-7658(00)90211-9. [DOI] [PubMed] [Google Scholar]
- 52.Messadi AA, Lamia T, Kamel B. Association between antibiotic use and changes in susceptibility patterns of Pseudomonas æruginosa in an intensive care burn unit: a 5-year study 2000-2004. Burns. 2008;34:1098–1102. doi: 10.1016/j.burns.2008.03.014. [DOI] [PubMed] [Google Scholar]
- 53.Kalantar E, Torabi V, Salimizand H. First survey of metallo-β–lactamase producers in clinical isolates of Pseudomonas æruginosa from a referral burn center in Kurdistan province. Jundishapur J Nat Pharm Prod. 2012;7:23–26. doi: 10.17795/jjnpp-3546. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 54.Kumar S, De A, Baveja S. Prevalence and risk factors of metallo β-lactamase producing Pseudomonas æruginosa and Acinetobacter species in burns and surgical wards in a tertiary care hospital. J Lab Physicians. 2012;4:39–42. doi: 10.4103/0974-2727.98670. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 55.Lari A, Azimi L, Soroush S. Low prevalence of metallobeta-lactamase in Pseudomonas æruginosa isolated from a tertiary burn care center in Tehran. Int J Immunopathol Pharmacol. 2015;28:384–389. doi: 10.1177/0394632015578343. [DOI] [PubMed] [Google Scholar]
- 56.Belotti PT, Thabet L, Laffargue A. Description of an original integron encompassing blaVIM-2, qnrVC1 and genes encoding bacterial group II intron proteins in Pseudomonas æruginosa. J Antimicrob Chemother. 2015;70:2237–2240. doi: 10.1093/jac/dkv103. [DOI] [PubMed] [Google Scholar]
- 57.Mohapatra S, Deb M, Agrawal K. Bacteriological profile of patients and environmental samples in burn intensive care unit: a pilot study from a tertiary care hospital. Indian Journal of Burns. 2014;22:62–66. [Google Scholar]
- 58.Le Floch R, Naux E, Arnould JF. L’infection bactérienne chez le patient brûlé. Ann Burns Fire Disasters. 2015;28:94–104. [PMC free article] [PubMed] [Google Scholar]