Abstract
目的
探讨 Crowe Ⅳ 型髋关节发育不良(developmental dysplasia of the hip,DDH)患者人工全髋关节置换术(total hip arthroplasty,THA)翻修原因及翻修假体的选择。
方法
回顾分析 2008 年 1 月—2018 年 5 月行翻修术的 14 例(15 髋)Crowe Ⅳ 型 DDH 患者临床资料。男 1 例(1 髋),女 13 例(14 髋);翻修术时年龄 27~63 岁,平均 45.0 岁。左髋 7 例,右髋 6 例;双髋 1 例。初次置换假体摩擦界面类型:金属-聚乙烯界面(metal-on-polyethylene,MOP)9 髋,陶瓷-陶瓷界面(ceramic-on-ceramic,COC)4 髋,陶瓷-聚乙烯界面(ceramic-on-polyethylene,COP)和陶瓷-金属界面各 1 髋。初次置换至翻修术时间为 3~204 个月,平均 65.0 个月。翻修原因:假体无菌性松动 7 髋,反复脱位 3 髋,感染 2 髋,骨溶解、截骨处不愈合、股骨柄前倾角偏小各 1 髋。术前髋关节 Harris 评分为(54.1±17.8)分,髋关节屈曲达(92.7±20.2)°。术前 X 线片检查显示髋臼侧骨缺损 11 髋,股骨侧骨溶解 4 髋。翻修术中假体摩擦界面 5 髋选择 COP,其余患者均采用 COC。11 髋行髋臼及股骨侧翻修,4 髋仅行股骨侧翻修。
结果
手术时间 1.5~6.0 h,平均 3.7 h;术中出血量为 200~2 000 mL,平均 940.0 mL。术后患者均获随访,随访时间 16~142 个月,平均 73.9 个月。X 线片复查显示,初次置换术后及翻修术后臼杯外展角及前倾角比较,差异均无统计学意义(P>0.05)。翻修术后旋转中心高度及股骨偏心距均高于初次置换术后,其中股骨偏心距差异有统计学意义(P<0.05)。末次随访时,Harris 评分为(85.0±7.3)分,髋关节屈曲达(115.0±17.0)°,均较术前明显提高(t=8.909,P=0.000;t=4.911,P=0.000)。翻修术后 3 例再次进行翻修。末次随访时 15 髋假体均稳定,未观察到透亮线;股骨柄均为中立位,未发生松动或下沉。
结论
Crowe Ⅳ 型 DDH 患者 THA 术后翻修主要原因为假体无菌性松动。由于患者均相对年轻且关节活动度大,为了延长假体使用寿命,初次置换时不应使用 MOP 界面,COC 界面更优。翻修术中使用金属垫块、加强环和 Cup-cage 均可达到良好的髋臼重建效果。S-ROM 假体应作为初次置换及翻修的首选假体。
Keywords: Crowe Ⅳ型髋关节发育不良, 人工全髋关节置换术, 翻修原因, 假体选择
Abstract
Objective
To investigate revision reasons and prosthesis selection of Crowe Ⅳ developmental dysplasia of the hip (DDH) after total hip arthroplasty (THA).
Methods
A clinical data of 14 patients (15 hips) with Crowe Ⅳ DDH, who underwent a revision hip arthroplasty between January 2008 and May 2018, was retrospectively reviewed. There were 1 male (1 hip) and 13 females (14 hips). The age ranged from 27 to 63 years (mean, 45.0 years). There were 7 cases of left hip, 6 cases of right hip, and 1 case of bilateral hips. The prosthetic interfaces of primary THA were metal-on-polyethylene (MOP) in 9 hips, ceramic-on-ceramic (COC) in 4 hips, ceramic-on-polyethylene (COP) in 1 hip, and ceramic-on-metal in 1 hip. The time from primary THA to revision was 3-204 months (mean, 65.0 months). The causes of revision included aseptic loosening in 7 hips, dislocation in 3 hips, periprosthetic joint infection in 2 hips, osteolysis in 1 hip, nonunion of osteotomy in 1 hip, and a small-angle of femoral anteversion in 1 hip. Preoperative Harris score was 54.1±17.8 and the range of motion (ROM) of flexion was (92.7±20.2)°. Preoperative X-ray films showed the acetabular bone defect in 11 hips and osteolysis of femoral side in 4 hips. During the revision, the prostheses with COP and COC interfaces were used in 5 hips and 10 hips, respectively. Both acetabular and femoral revisions were performed in 11 hips and only femoral revision was performed in 4 hips.
Results
The mean operation time was 3.7 hours (range, 1.5-6.0 hours). The mean intraoperative blood loss was 940.0 mL (range, 200-2 000 mL). All patients were followed up 16-142 months (mean, 73.9 months). Postoperative X-ray films showed no difference in inclination and anteversion between primary THA and revision (P>0.05). The height of rotation center and offset after revision were higher than those after primary THA, and the difference in offset was significant (P<0.05). At last follow-up, the Harris score and ROM of flexion were 85.0±7.3 and (115.0±17.0)°, respectively, which were significantly higher when compared with those before revision (t=8.909, P=0.000; t=4.911, P=0.000). Three hips underwent a re-revision operation. All protheses were fixed well and no radiolucent line, loosening, or subsidence was observed at last follow-up.
Conclusion
The most common reason for revision in patients with Crowe Ⅳ DDH after THA was aseptic loosening. Due to high activity demand of this population, the prosthesis with MOP interface should be prevented and the prosthesis with COC interface could be alternative. Metal block, cup-cage, and reinforcement ring were reasonable solutions for reconstruction of acetabulum with severe bone defects and have satisfactory effectiveness. S-ROM prosthesis should be the preferred stem for neither primary THA or revision.
Keywords: Crowe Ⅳdevelopmental dysplasia of the hip, total hip arthroplasty, revision reason, prosthesis selection
髋关节发育不良(developmental dysplasia of the hip,DDH)是以髋臼对股骨头覆盖不足为特点的常见髋部疾病[1]。人工全髋关节置换术(total hip arthroplasty,THA)是治疗 DDH 继发骨关节炎的有效方法[2-3]。Crowe Ⅳ 型 DDH 因存在股骨头高脱位、股骨近端髓腔狭窄、髋臼浅且前壁薄弱的异常解剖结构,给 THA 带来了很大困难,术后各种并发症发生率较高[4-6]。近年来,随着假体松动、内衬磨损、骨溶解等问题的出现,已有部分 Crowe Ⅳ 型 DDH 患者进行了翻修术,但是目前缺少探讨翻修原因的相关研究。为了降低初次置换的失败率以及指导翻修,有必要对翻修原因进行分析。此外,Crowe Ⅳ 型 DDH 的翻修常伴随严重骨缺损,包括股骨近端和髋臼侧骨缺损,甚至骨盆不连续,以及术中假体取出时易带出部分骨质。当骨缺损区域较大时,选择普通生物型假体翻修无法获得稳定固定,此时假体类型的选择也是影响翻修术疗效的重要因素,需要重点关注。为此,我们回顾分析了 2008 年 1 月—2018 年 5 月,于中国人民解放军总医院第一医学中心行翻修术的 14 例(15 髋)Crowe Ⅳ 型 DDH 患者临床资料,探讨翻修原因以及翻修时假体类型的选择。报告如下。
1. 临床资料
1.1. 一般资料
本组男 1 例(1 髋),女 13 例(14 髋);初次 THA 时年龄 23~62 岁,平均 39.1 岁;翻修术时年龄 27~63 岁,平均 45.0 岁。体质量指数为 18.0~29.2 kg/m2,平均 22.9 kg/m2。左髋 7 例,右髋 6 例;双髋 1 例。于本院行初次置换手术 6 例(7 髋),外院手术 8 例(8 髋)。初次置换假体摩擦界面类型:金属-聚乙烯界面(metal-on-polyethylene,MOP)9 髋,陶瓷-陶瓷界面(ceramic-on-ceramic,COC)4 髋,陶瓷-聚乙烯界面(ceramic-on-polyethylene,COP)和陶瓷-金属界面(ceramic-on-metal,COM)各 1 髋。初次置换术后,1 例(1 髋)曾于外院行髋臼造盖术 1 次以及髋臼造盖术后翻修 3 次;1 例 (1 髋)于我院行 3 次打压植骨、髋关节翻修术。
本次翻修原因:假体无菌性松动 7 髋,其中臼杯松动 3 髋、股骨柄松动 2 髋、臼杯及股骨柄均松动 2 髋;反复脱位 3 髋;感染 2 髋,细菌培养结果分别为肠球菌和凝固酶阴性葡萄球菌;骨溶解、截骨处不愈合、股骨柄前倾角偏小各 1 髋。初次置换至翻修术时间 3~204 个月,平均 65.0 个月。术前髋关节 Harris 评分[7]为(54.1±17.8)分,髋关节屈曲达(92.7±20.2)°。X 线片检查显示髋臼侧骨缺损 11 髋,根据 Paprosky 分型标准[8] ⅡA 型 4 髋、ⅡB 型 2 髋、ⅡC 型 2 髋、ⅢA 型 2 髋、ⅢB 型 1 髋;股骨侧骨溶解 4 髋,根据 Gruen 等[9]和 DeLee 等[10]分区法均为 1、2、6、7 区。
1.2. 手术方法
手术均由同一位高年资主任医师完成。其中,2 例(2 髋)因感染翻修者行一期占位器植入、二期翻修,两期手术间隔 6 个月;其余患者均行一期翻修。1 例双髋患者分别于初次置换术后 6、12 年行两侧髋翻修。采用原切口入路,按照常规髋关节翻修术进行操作。
本组假体摩擦界面 5 髋选择 COP,其中 1 髋未更换臼杯,选用原型号内衬进行更换;4 髋使用高交联聚乙烯内衬。其余患者均采用 COC。
11 髋行髋臼侧翻修,其中 1 髋骨缺损 Paprosky ⅢB 型采用 Cup-cage 结合 56 mm TM 杯;2 髋 ⅢA 型及 1 髋 ⅡC 型分别使用 54、55、57 mm 加强环结合同种异体颗粒骨(中国人民解放军总医院全军骨科研究所)打压植骨;1 髋 ⅡC 型使用多孔金属臼杯加钽块;6 髋使用更大号的普通或多孔生物型金属臼杯,其中 1 髋术前骨缺损为 ⅡA 型患者,术中取臼杯时将内下方骨块带出,造成前下方臼底漏,使用大直径多孔金属臼杯加强固定。
15 髋行股骨侧翻修,其中 13 髋使用 S-ROM 假体,2 髋使用 MP 假体。2 髋术中因股骨柄难以取出,使用大粗隆延长截骨技术,予以 Cable-Ready 钢板捆绑固定并使用 MP 股骨柄。2 髋因大粗隆处骨质薄弱,分别采用克氏针制成张力带固定及 Cable-Ready 钢板捆绑固定。术中发现 3 髋股骨近端内侧骨缺损而外侧骨质良好,打入袖套时采用反置安放以获得稳定。3 髋使用高偏心距股骨柄。
1.3. 术后处理
术后常规使用抗生素及低分子肝素,以预防感染及下肢静脉血栓形成。术后医生根据骨缺损程度和假体稳定性,指导患者进行功能锻炼及负重行走。
1.4. 观测指标
① 记录翻修术手术时间、术中出血量以及术中、随访期间并发症发生情况。采用 Harris 评分评价髋关节功能。
② 于初次置换术后 3 d 及翻修术后 3 d 髋关节正侧位 X 线片,测量臼杯外展角及前倾角、旋转中心高度及股骨偏心距。臼杯外展角,即臼杯外缘长轴连线与两泪滴连线形成的夹角。臼杯前倾角,采用 Ackland 等[11]的三角函数法通过测量臼杯外缘长轴和短轴来计算。旋转中心高度,即臼杯中心至闭孔上缘连线的距离。股骨偏心距,即旋转中心至股骨干轴线的垂直距离。
③ 于翻修术前髋关节正侧位 X 线片,采用 Paprosky 分型标准[8]对髋臼侧骨缺损进行评估,根据 Gruen 等[9]和 DeLee 等[10]分区法对股骨侧骨溶解进行分区。于翻修术后末次随访时髋关节正侧位 X 线片,观察假体是否稳定及臼杯有无松动。臼杯松动定义为移位超过 4 mm 或者在 3 个 DeLee 分区均出现超过 2 mm 的完全连续透亮线。
1.5. 统计学方法
采用 SPSS21.0 统计软件进行分析。数据以均数±标准差表示,手术前后比较采用配对 t 检验;检验水准取双侧 α=0.05。
2. 结果
本组手术时间 1.5~6.0 h,平均 3.7 h;术中出血量为 200~2 000 mL,平均 940.0 mL。术后患者均获随访,随访时间 16~142 个月,平均 73.9 个月。X 线片复查显示,初次置换术后及翻修术后臼杯外展角及前倾角比较,差异均无统计学意义(P>0.05)。翻修术后旋转中心高度及股骨偏心距均高于初次置换术后,其中股骨偏心距差异有统计学意义(P<0.05)。见表 1。末次随访时,Harris 评分为(85.0±7.3)分,髋关节屈曲达(115.0±17.0)°,均较术前明显提高,差异有统计学意义(t=8.909,P=0.000;t=4.911,P=0.000)。
表 1.
Comparison of postoperative radiographic parameters between primary THA and revision (n=15,
 )
)
患者初次置换术后及翻修术后影像学测量指标比较(n=15,
 )
)
| 时间
Time |
外展角(°)
Inclination (°) |
前倾角(°)
Anteversion (°) |
旋转中心高度(cm)
Height of rotation center (cm) |
股骨偏心距(cm)
Offset (cm) |
| 初次置换术后
After primary THA |
45.1±4.3 | 20.7±3.3 | 2.05±0.67 | 2.70±0.57 |
| 翻修术后
After revision |
45.8±7.4 | 23.0±6.1 | 2.16±0.73 | 3.04±0.51 |
| 统计值
Statistic |
t=1.870
P=0.083 |
t=0.415
P=0.684 |
t=1.105
P=0.288 |
t=2.186
P=0.046 |
本次翻修术后 3 例(3 髋)再次进行翻修。其中,1 例术后 5 个月摔倒致股骨远端骨折,假体位置良好,未见松动,行切开复位钢板内固定术,末次随访时骨折已完全愈合。1 例术后 4 年发生臼杯松动、内陷且大粗隆处钛缆松弛,行翻修术更换臼杯及钛缆,末次随访时臼杯骨长入良好,未见松动。1 例术后 8 年间反复脱位 4 次,均予手法复位成功,后因摔倒致大粗隆处骨折行翻修术;术中见炎性假瘤,更换衬垫并使用 Cable-Ready 钢板捆绑固定大粗隆,至末次随访时未再发生脱位,且骨折处愈合良好。末次随访时 15 髋假体均稳定,未观察到透亮线;股骨柄均为中立位,未发生松动或下沉(图 1)。3 髋加强环及 1 髋 Cup-cage 均未出现金属弯曲、疲劳断裂等现象。患者详细资料见表 2。
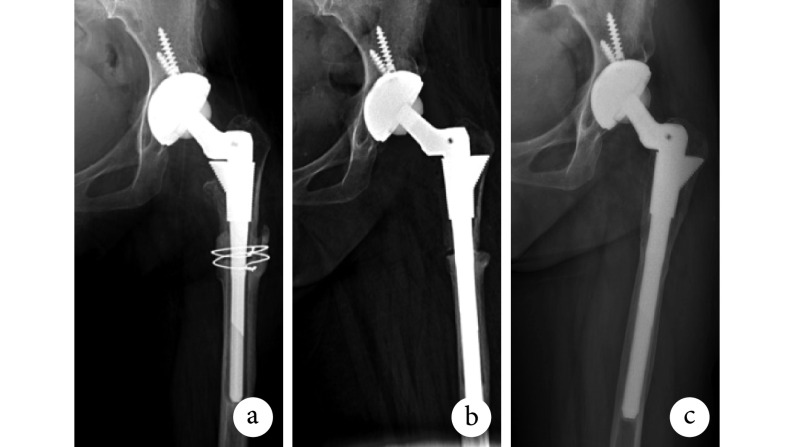
图 1.
X-ray films of a 63-year-old female patient with left revision because of osteotomy nonunion after 1 year of THA
患者,女,63 岁,左髋关节 THA 术后 1 年因截骨处不愈合行翻修术 X 线片
a. 术前;b. 术后即刻;c. 术后 5.5 年
a. Before operation; b. At immediate after operation; c. At 5.5 years after operation
表 2.
Clinical data of all patients
患者临床资料
| 序号
No. |
初次置换
Primary THA |
翻修前
Before revision |
翻修后
After revision |
||||||
| 界面
Interface |
骨缺损分型
Type of bone defect |
骨溶解分区
Zone of osteolysis |
翻修原因
Cause of revision |
界面
Interface |
特殊的臼杯假体
Special acetabular prothesis |
股骨假体
Femoral stem |
|||
| 1 | MOP | ⅡA | − | 无菌性松动 | COC | − | S-ROM | ||
| 2 | MOP | ⅡA | 1、2、6、7 | 骨溶解 | COC | − | S-ROM | ||
| 3 | COC | ⅡA | − | 感染 | COC | − | S-ROM | ||
| 4 | COP | ⅡA | − | 反复脱位 | COC | − | S-ROM | ||
| 5 | MOP | − | 1、2、6、7 | 无菌性松动 | COP | − | MP | ||
| 6 | COC | − | 1、2、6、7 | 截骨处不愈合 | COC | − | S-ROM | ||
| 7 | MOP | ⅢA | − | 无菌性松动 | COP | 加强环 | S-ROM | ||
| 8 | MOP | ⅢA | − | 无菌性松动 | COP | 加强环 | S-ROM | ||
| 9 | COC | − | 1、2、6、7 | 无菌性松动 | COC | − | S-ROM | ||
| 10 | COC | ⅡC | − | 反复脱位 | COC | 钽块 | MP | ||
| 11 | COM | − | − | 股骨柄前倾角偏小 | COC | − | S-ROM | ||
| 12 | MOP | ⅡB | − | 无菌性松动 | COC | − | S-ROM | ||
| 13 | MOP | ⅡB | − | 反复脱位 | COC | − | S-ROM | ||
| 14 | MOP/MOP | ⅡC/ⅢB | − | 感染/无菌性松动 | COP/COP | 加强环/Cup-cage 结合 TM 杯 | S-ROM/S-ROM | ||
3. 讨论
3.1. 翻修原因分析
对于 Crowe Ⅳ 型 DDH 患者,THA 后翻修的主要原因为假体无菌性松动。髋臼内衬磨损产生的颗粒会造成假体周围骨溶解,导致无菌性松动,尤其是传统聚乙烯内衬,其耐磨性能不如陶瓷和高交联聚乙烯内衬,更易产生磨损颗粒[12-14]。并且磨损的内衬会使臼杯受力不均匀,长期发展易导致臼杯松动。本研究 7 髋假体无菌性松动中,6 髋初次置换时使用传统聚乙烯内衬。Vendittoli 等[13]进行了一项临床随机对照试验,对 116 例(140 髋)THA 患者随访 9~15 年,结果显示 COC 及 MOP 假体翻修率分别为 1.4% 和 11.6%,MOP 组翻修均为聚乙烯内衬磨损造成,包括 4 例伴轻微骨溶解的无菌性松动,3 例严重聚乙烯内衬磨损。上述研究及本研究结果均提示,聚乙烯内衬磨损可导致假体翻修率增高。并且就传统聚乙烯内衬而言,年轻患者磨损率明显高于老年患者[15]。Kahlenberg 等[16]对<35 岁的 82 例患者(108 髋)进行研究,发现导致翻修的常见原因为臼杯松动(30.1%)、股骨柄松动(23.7%)及聚乙烯内衬磨损(24.7%)。由于 Crowe Ⅳ 型 DDH 患者在初次 THA 时往往较年轻,术后日常活动量及活动度均较大,而高活动度更容易产生界面磨损,是 THA 术后假体无菌性松动的危险因素之一[14]。
所以,对于年轻的 Crowe Ⅳ 型 DDH 患者,由聚乙烯内衬磨损导致的假体无菌性松动是翻修的主要原因。为保证在高活动度前提下,尽可能延长假体使用寿命,应避免使用传统聚乙烯内衬,尤其在初次置换时。相比之下,COC 是更好的选择,如果由于尺寸限制无法选择 COC,则应该尽量选择高交联聚乙烯内衬,从而减少磨损及骨溶解的发生[17-18]。
本研究中反复脱位是导致翻修的第二大因素。贾金领等[19]通过对 428 例初次 THA 患者资料进行分析,发现年龄、合并肢体或精神疾病、手术入路方式、人工股骨头直径、手术史、假体位置是 THA 术后出现关节脱位的危险因素。本研究中,3 例脱位患者初次置换后假体位置均良好,臼杯外展角和前倾角均位于 Lewinnek 安全区[20]内。但翻修术中发现 2 例股骨柄前倾角过小,另 1 例则有多次打压植骨手术史,二者均是导致脱位的危险因素。所以在初次置换以及翻修时,应保证良好的假体位置及角度,并且选择合适的假体维持关节周围软组织张力,以有效预防脱位的发生。
3.2. 髋臼侧假体选择
在 Crowe Ⅳ 型 DDH 翻修术中,髋臼侧常存在严重骨缺损,选择合适的重建假体是翻修术成功的关键。本研究中,对于部分 PaproskyⅡ型骨缺损患者,通过使用更大号的生物型金属臼杯进行重建。Park 等[21]对 138 例髋关节翻修患者进行至少 20 年随访,结果显示生物型臼杯 20 年存活率高达 95%。对于情况较复杂的部分Ⅱ型及Ⅲ型骨缺损,需采用特殊假体行髋臼重建,本研究中采用了金属垫块、加强环和 Cup-cage。Park 等[21]和 Whitehouse 等[22]回顾了使用骨小梁金属垫块翻修的 56 例患者临床资料,结果显示 10 年假体在位率为 92%。Park 等[23]随访了 48 例使用加强环重建的髋关节翻修患者,平均随访时间 11.4 年,假体在位率为 71%。Symeonides 等[24]研究了 57 例使用 Cup-cage 重建髋臼缺损的患者,在 5~21 年随访期间失败率仅为 10.5%。本组末次随访时金属垫块、加强环及 Cup-cage 均达到了良好稳定性,且未发生金属弯曲、疲劳断裂等现象。
3.3. 股骨侧假体选择
在股骨侧翻修中,本研究主要使用的假体类型是 S-ROM 假体,其余 2 髋为 MP 假体。这两种假体均能适应 Crowe Ⅳ 型 DDH 狭窄髓腔。Wang 等[25]对股骨侧使用 S-ROM 假体的 103 例 Crowe Ⅳ 型 DDH 患者进行观察,平均随访 65.6 个月,术后仅 2 例出现股骨柄松动,其余均在位良好。翻修术中使用 S-ROM 假体时,由于部分患者股骨近端髓腔已经硬化,三角形袖套难以植入,此时可选用轴向稳定性不如三角形袖套的 Cone 型袖套。若股骨近端存在骨缺损,袖套无法获得固定,则应选用 MP 假体。在近端骨质良好情况下,S-ROM 假体应作为初次置换及翻修的首选[3,26]。
综上述,Crowe Ⅳ型 DDH 患者 THA 后翻修的主要原因为假体无菌性松动。由于患者相对年轻且关节活动度大,为了延长假体使用寿命,宜选择 COC 界面假体。翻修术中髋臼侧重建方法包括金属垫块、加强环和 Cup-cage,均可达到良好重建效果。在股骨近端骨质良好的情况下,S-ROM 假体应作为初次置换及翻修的首选。但本研究存在一定局限性,如样本量较小、随访时间相差较大,部分患者初次置换手术与翻修手术不是同一中心同一术者完成,且初次置换的相关资料存在缺失,以及部分患者已有多次翻修史等,研究存在一定偏倚。因此,本研究结论有待大样本、多中心的临床随机对照研究进一步验证。
作者贡献:沈俊民负责论文撰写、数据处理以及科研设计、实施;周勇刚、陈继营负责课题设计及论文修改;孙菁阳、马海洋、杜银桥负责数据收集及统计分析;高志森、彭亚文负责统计分析验证及论文修改。
利益冲突:所有作者声明,在课题研究和文章撰写过程中不存在利益冲突。
机构伦理问题:研究方案经中国人民解放军总医院医学伦理委员会批准。中国临床试验注册中心注册号:ChiCTR-INR-17013267。
References
- 1.Jacobsen S, Sonne-Holm S, Søballe K, et al Hip dysplasia and osteoarthrosis: a survey of 4151 subjects from the Osteoarthrosis Substudy of the Copenhagen City Heart Study. Acta Orthop. 2005;76(2):149–158. doi: 10.1080/00016470510030517. [DOI] [PubMed] [Google Scholar]
- 2.朱建辛, 王跃, 庞健, 等 人工全髋关节置换术治疗重度成人髋关节发育不良疗效分析. 中国修复重建外科杂志. 2014;28(3):335–338. doi: 10.7507/1002-1892.20140075. [DOI] [Google Scholar]
- 3.孙菁阳, 周勇刚, 高志森, 等 人工全髋关节置换术治疗 Crowe Ⅳ 型髋关节发育不良术中应用粗隆下截骨的相关研究. 中国修复重建外科杂志. 2018;32(2):152–156. [Google Scholar]
- 4.Argenson JN, Ryembault E, Flecher X, et al Three-dimensional anatomy of the hip in osteoarthritis after developmental dysplasia. J Bone Joint Surg (Br) 2005;87(9):1192–1196. doi: 10.1302/0301-620X.87B9.15928. [DOI] [PubMed] [Google Scholar]
- 5.刘宏伟, 徐南伟, 张云坤, 等 Crowe Ⅳ 型成人发育性髋关节发育不良股骨近段形态研究及其临床意义. 中国修复重建外科杂志. 2015;29(8):931–935. doi: 10.7507/1002-1892.20150201. [DOI] [Google Scholar]
- 6.Greber EM, Pelt CE, Gililland JM, et al Challenges in total hip arthroplasty in the setting of developmental dysplasia of the hip. J Arthroplasty. 2017;32(9S):S38–S44. doi: 10.1016/j.arth.2017.02.024. [DOI] [PubMed] [Google Scholar]
- 7.Harris WH Traumatic arthritis of the hip after dislocation and acetabular fractures: treatment by mold arthroplasty. An end-result study using a new method of result evaluation. J Bone Joint Surg (Am) 1969;51(4):737–755. doi: 10.2106/00004623-196951040-00012. [DOI] [PubMed] [Google Scholar]
- 8.Paprosky WG, Perona PG, Lawrence JM Acetabular defect classification and surgical reconstruction in revision arthroplasty. A 6-year follow-up evaluation. J Arthroplasty. 1994;9(1):33–44. doi: 10.1016/0883-5403(94)90135-X. [DOI] [PubMed] [Google Scholar]
- 9.Gruen TA, McNeice GM, Amstutz HC “Modes of failure” of cemented stem-type femoral components: a radiographic analysis of loosening. Clin Orthop Relat Res. 1979;(141):17–27. [PubMed] [Google Scholar]
- 10.DeLee JG, Charnley J Radiological demarcation of cemented sockets in total hip replacement. Clin Orthop Relat Res. 1976;(121):39–41. [PubMed] [Google Scholar]
- 11.Ackland MK, Bourne WB, Uhthoff HK Anteversion of the acetabular cup. Measurement of angle after total hip replacement. J Bone Joint Surg (Br) 1986;68(3):409–413. doi: 10.1302/0301-620X.68B3.3733807. [DOI] [PubMed] [Google Scholar]
- 12.Gallo J, Goodman SB, Konttinen YT, et al Particle disease: biologic mechanisms of periprosthetic osteolysis in total hip arthroplasty. Innate Immun. 2013;19(2):213–224. doi: 10.1177/1753425912451779. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 13.Vendittoli PA, Rivière C, Lavigne M, et al Alumina on alumina versus metal on conventional polyethylene: a randomized clinical trial with 9 to 15 years follow-up. Acta Orthop Belg. 2013;79(2):181–190. [PubMed] [Google Scholar]
- 14.Ryu KJ What host factors affect aseptic loosening after THA and TKA? Clin Orthop Relat Res. 2015;473(8):2710–2711. doi: 10.1007/s11999-015-4251-8. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 15.Maloney WJ, Galante JO, Anderson M, et al Fixation, polyethylene wear, and pelvic osteolysis in primary total hip replacement. Clin Orthop Relat Res. 1999;(369):157–164. doi: 10.1097/00003086-199912000-00016. [DOI] [PubMed] [Google Scholar]
- 16.Kahlenberg CA, Swarup I, Krell EC, et al Causes of revision in young patients undergoing total hip arthroplasty. J Arthroplasty. 2019;34(7):1435–1440. doi: 10.1016/j.arth.2019.03.014. [DOI] [PubMed] [Google Scholar]
- 17.万国杨, 孙俊英, 查国春, 等 第三代陶对陶人工全髋关节置换术治疗中青年髋关节疾病的中远期疗效. 中国修复重建外科杂志. 2015;29(9):1057–1061. doi: 10.7507/1002-1892.20150229. [DOI] [Google Scholar]
- 18.Bryan AJ, Calkins TE, Karas V, et al Primary total hip arthroplasty in patients less than 50 years of age at a mean of 16 years: highly crosslinked polyethylene significantly reduces the risk of revision. J Arthroplsty. 2019;34(7S):S238–S241. doi: 10.1016/j.arth.2019.02.025. [DOI] [PubMed] [Google Scholar]
- 19.贾金领, 侯文根, 张君, 等 髋关节置换术后发生脱位的危险因素分析. 中国矫形外科杂志. 2016;24(17):1624–1627. [Google Scholar]
- 20.Lewinnek GE, Lewis JL, Tarr R, et al Dislocations after total hip-replacement arthroplasties. J Bone Joint Surg (Am) 1978;60(2):217–220. doi: 10.2106/00004623-197860020-00014. [DOI] [PubMed] [Google Scholar]
- 21.Park DK, Della Valle CJ, Quigley L, et al Revision of the acetabular component without cement. A concise follow-up, at twenty to twenty-four years, of a previous report. J Bone Joint Surg (Am) 2009;91(2):350–355. doi: 10.2106/JBJS.H.00302. [DOI] [PubMed] [Google Scholar]
- 22.Whitehouse MR, Masri BA, Duncan CP, et al Continued good results with modular trabecular metal augments for acetabular defects in hip arthroplasty at 7 to 11 years. Clin Orthop Relat Res. 2015;473(2):521–527. doi: 10.1007/s11999-014-3861-x. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 23.Park KS, Seon JK, Lee KB, et al Revision total hip arthroplasty using an acetabular reinforcement ring with a hook: a precise follow-up, at average 11.4 years, of a previous report. J Arthroplasty. 2017;32(2):503–509. doi: 10.1016/j.arth.2016.07.010. [DOI] [PubMed] [Google Scholar]
- 24.Symeonides PP, Petsatodes GE, Pournaras JD, et al The effectiveness of the Burch-Schneider antiprotrusio cage for acetabular bone deficiency: five to twenty-one years’ follow-up. J Arthroplasty. 2009;24(2):168–174. doi: 10.1016/j.arth.2007.10.009. [DOI] [PubMed] [Google Scholar]
- 25.Wang S, Zhou Y, Ma H, et al Mid-term results of total hip replacement with subtrochanteric osteotomy, modular stem, and ceramic surface in Crowe Ⅳ hip dysplasia. Arthroplast Today. 2017;4(3):363–369. doi: 10.1016/j.artd.2017.07.003. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 26.Moreta J, Uriarte I, Foruria X, et al Medium-term outcomes of the S-ROM modular femoral stem in revision hip replacement. Eur J Orthop Surg Traumatol. 2018;28(7):1327–1334. doi: 10.1007/s00590-018-2213-z. [DOI] [PubMed] [Google Scholar]