Abstract
目的
对 Prodisc-C 假体行全颈椎人工间盘置换术(total cervical disc replacement,TDR)患者 10 年以上远期疗效进行评价。
方法
回顾分析 2005 年 12 月—2008 年 4 月采用 Prodisc-C 假体行 TDR 治疗的 118 例单节段至 3 节段颈椎间盘退变疾病(cervical disc degeneration disease,CDDD)患者临床资料。其中男 66 例,女 52 例;年龄 25~62 岁,平均 46.8 岁。神经根型颈椎病 38 例,脊髓型颈椎病 28 例,混合型颈椎病 52 例。手术节段为 C3~7,其中单节段 90 例,连续双节段 20 例,连续 3 节段 8 例。术中共使用 154 个 Prodisc-C 假体。手术前后临床疗效采用疼痛视觉模拟评分(VAS)、颈椎功能障碍指数(NDI)、日本骨科协会(JOA)评分、Odom 分级评价。影像学评价指标包括颈椎活动度(range of motion,ROM)、矢状位前凸角、椎间隙高度(intervertebral disc height,IDH),并观察有无假体移位、下沉、松动、锁死及异位骨化(heterotopic ossification,HO)、邻近节段退变(adjacent segment degeneration,ASD)等并发症发生。并根据有无发生 HO 或 ASD 分组,比较患者手术节段 ROM。
结果
术后患者均获随访,随访时间 121~150 个月,平均 135.8 个月。随访期间无 1 例行翻修手术。术后 1 周及末次随访时 VAS、NDI、JOA 评分及 Odom 分级均较术前显著改善(P<0.05);其中末次随访时 VAS 和 NDI 评分较术后 1 周进一步改善(P<0.05);术后 1 周及末次随访时的 JOA 评分及改善率比较差异无统计学意义(P>0.05)。颈椎整体和手术节段 ROM 在术后 1 周和 10 年后较术前有所减小(P<0.05),其余各时间点差异均无统计学意义(P>0.05);上位邻近节段(upper adjacent segment,UAS)和下位邻近节段(lower adjacent segment,LAS)的 ROM 术后各时间点间比较差异均无统计学意义(P>0.05)。手术前后各时间点颈椎矢状位前凸角比较差异均无统计学意义(P>0.05);手术节段前凸角在术后 1 周、6 个月、1 年、2 年较术前显著增加(P<0.05)。术后各时间点手术节段 IDH 均较术前显著改善(P<0.05),而术后各时间点间 UAS 和 LAS 的 IDH 比较差异均无统计学意义(P>0.05)。术后各时间点均未发生假体移位、下沉和松动;从术后 6 个月起,各时间点间假体移位和下沉距离比较差异均无统计学意义(P>0.05)。而末次随访时假体锁死/融合发生率达 10.4%,但与术后 6 个月(1.9%)比较差异有统计学意义(P<0.05)。术后 1 周上位 ASD 和下位 ASD 发生率分别为 1.3% 和 2.6%,随时间延长其发生率逐渐增加,各时间点间比较差异均有统计学意义(P<0.05);ASD 组患者术后各时间点手术节段 ROM 均小于无 ASD 组,但差异无统计学意义(P>0.05)。术后 6 个月起有 58.4% 节段出现 HO,随时间延长 HO 发生率均较术后 6 个月逐渐显著增加(P<0.05);HO 组患者手术节段 ROM 在术后 6 个月、2 年、5 年、10 年显著小于无 HO 组患者(P<0.05)。
结论
TDR 术后对邻近节段影响较小,尽管出现部分影像学并发症,但对整体临床疗效的改善无明显影响;使用 Prodisc-C 假体行 TDR 治疗 CDDD 可获得安全、明确的远期临床疗效。
Keywords: Prodisc-C假体, 全颈椎人工间盘置换术, 远期疗效
Abstract
Objective
To evaluate long-term radiographic and clinical effectiveness of total cervical disc replacement (TDR) with Prodisc-C prosthesis at a minimum of 10 years follow-up.
Methods
The clinical data of 118 patients with cervical disc degeneration disease (CDDD) treated with TDR by using Prodisc-C prosthesis between December 2005 and April 2008 were retrospectively analyzed. There were 66 males and 52 females, with the age of 25-62 years (mean, 46.8 years). There were 38 cases of cervical spondylotic radiculopathy, 28 cases of cervical spondylotic myelopathy, and 52 cases of mixed cervical spondylotic myelopathy. The operative segments were C3-7, including 90 cases of single segment, 20 cases of continuous double segments, and 8 cases of continuous three segments. A total of 154 Prodisc-C prostheses were used during the operation. The clinical effectiveness was evaluated by pain visual analogue scale (VAS) score, neck disability index (NDI), Japanese Orthopaedic Association (JOA) score, and Odom grade before and after operation. Imaging evaluation indicators included range of motion (ROM), sagittal lordosis angle, intervertebral disc height (IDH), and prosthesis displacement, subsidence, loosening, locking, and heterotopic ossification (HO), adjacent segment degeneration (ASD), and other complications. Patients were grouped according to whether HO or ASD occurred or not, the ROM of surgical segment was compared.
Results
All patients were followed up 121-150 months (mean, 135.8 months). No revision operation was performed during the follow-up period. The VAS, NDI, JOA scores and Odom grades were significantly improved at 1 week after operation and last follow-up when compared with preoperative ones (P<0.05); VAS and NDI scores were further improved at last follow-up than those at 1 week after operation (P<0.05); there was no significant difference in JOA scores and improvement rates between at 1 week after operation and at last follow-up (P>0.05). The ROM of the whole cervical spine and the operative segment decreased at 1 week and 10 years after operation when compared with preoperative ones (P<0.05), but there was no significant difference in the other time points (P>0.05); there was no significant difference in the ROM between the upper adjacent segment (UAS) and the lower adjacent segment (LAS) at each time point after operation (P>0.05). There was no significant difference in sagittal lordosis angle of cervical spine before and after operation (P>0.05); the sagittal lordosis angle of operative segment increased significantly at 1 week, 6 months, 1 year, and 2 years after operation (P<0.05). The IDH of operative segment was significantly improved at each time point after operation (P<0.05), but there was no significant difference in IDH between UAS and LAS at each time point after operation (P>0.05). No prosthesis displacement, subsidence, or loosening occurred at each time point after operation. There was no significant difference of the prosthetic displacement and subsidence distance between all time points after 6 months after operation (P>0.05). At last follow-up, the incidence of prosthetic locking/fusion was 10.4%, showing no significant difference when compared with 6 months (1.9%) (P<0.05). The incidence of upper ASD and lower ASD was 1.3% and 2.6% respectively at 1 week after operation. The incidence of upper ASD and lower ASD increased gradually with time prolonging, and there were significant differences between different time points (P<0.05). The ROM of operative segment in ASD group was lower than that in non-ASD group at each time point after operation, but there was no significant difference (P>0.05). HO appeared in 58.4% of the segments at 6 months after operation, and the incidence of HO increased significantly with time, which was significantly different from that at 6 months after operation (P<0.05). The ROM of operative segments in HO group was significantly lower than that in non-HO group at 6 months, 2 years, 5 years, and 10 years after operation (P<0.05).
Conclusion
TDR has little effect on adjacent segments, although there are some imaging complications, it has no significant effect on the improvement of overall clinical effectiveness. Prodisc-C prosthesis can provide long-term, safe, and definite clinical effectiveness in the treatment of CDDD.
Keywords: Prodisc-C prosthesis, total cervical disc replacement, long-term effectiveness
全颈椎人工间盘置换术(total cervical disc replacement,TDR)作为一种代替颈前路椎间盘切除融合术(anterior cervical discectomy and fusion,ACDF)的术式,在治疗颈椎间盘退变疾病(cervical disc degeneration disease,CDDD)方面,在过去十余年已被广泛接受[1-3]。通过大量生物力学试验,理论上认为 TDR 可以保留手术节段的活动度、减轻邻近节段的应力[4-5]。但既往文献报道的各种各样人工间盘或多或少会出现一些并发症,如异位骨化(heterotopic ossification,HO)[6]、邻近节段退变(adjacent segment degeneration,ASD)[7]、假体移位等,可能会影响临床疗效[8]。
颈椎间盘假体 Prodisc-C(Synthes 公司,美国)作为最早问世的动态稳定装置之一,已被证明在 TDR 术后短期和中期随访中疗效确切[4, 9],但关于长期应用 Prodisc-C 假体疗效评估的报道较少[10],而且术后远期可能会增加上述影像学并发症发生率。尽管有文献报道并发症可能不会显著影响临床疗效,例如 HO 的出现并不会明确产生颈部僵硬或术后颈肩痛[5-6],但因缺乏远期随访数据,针对 TDR 术后的影像学参数、并发症及临床疗效仍存在研究价值,而目前 Prodisc-C 假体术后远期的影像学和临床结果仍不明确。因此,现回顾分析 2005 年 12 月—2008 年 4 月采用 Prodisc-C 假体行 TDR 治疗的单节段至 3 节段 CDDD 患者随访 10 年以上临床资料,评价该术式远期临床疗效。报告如下。
1. 临床资料
1.1. 患者选择标准
纳入标准:① 单节段至 3 节段 C3~7 颈椎间盘突出或退变患者,包括神经根型、脊髓型或混合型颈椎病;② 患者保守治疗 6 个月无效;③ 行前路 TDR 手术患者,随访时间>10 年,随访资料完整。排除标准:① 存在重度小关节退变;② 存在后纵韧带骨化;③ 手术节段失稳;④ 存在重度骨质疏松;⑤ 既往曾行颈椎手术者;⑥ 存在畸形、感染、炎症和肿瘤等。2005 年 12 月—2008 年 4 月共 118 例患者符合选择标准纳入研究。本研究获北京大学人民医院医学伦理委员会批准,患者均知情同意。
1.2. 一般资料
本组男 66 例,女 52 例;年龄 25~62 岁,平均 46.8 岁。体质量指数 16.0~35.8 kg/m2,平均 24.6 kg/m2。诊断为神经根型颈椎病 38 例,脊髓型颈椎病 28 例,混合型颈椎病 52 例。病程 1~469 个月,平均 44.6 个月。手术节段:单节段 90 例,包括 C3、4 6 例、C4、5 12 例、C5、6 64 例、C6、7 8 例;连续双节段 20 例,包括 C3~5 2 例、C4~6 13 例、C5~7 5 例;连续 3 节段 8 例,包括 C3~6 2 例、C4~7 6 例。
所有手术均由同一术者完成,均采用 Prodisc-C 假体行 TDR 手术治疗。Prodisc-C 假体是由钴铬合金-超高分子量聚乙烯(UHMWPE)复合材料组成的限制性球窝关节假体[11]。该假体在靠近椎间盘中心位置有固定的旋转中心,位于手术节段的下位椎体,可以提供不同的深度和高度组合[9]。上下方终板各有 1 根垂直龙骨,用于插入邻近椎体提供即刻稳定性。本组共使用 154 个 Prodisc-C 假体。
1.3. 疗效评价指标
1.3.1. 临床疗效评估
术前、术后 1 周和末次随访时采用疼痛视觉模拟评分(VAS)评价疼痛改善情况,取颈肩部和上肢评分平均值;颈椎功能障碍指数(NDI)评分评价患者颈部功能;日本骨科协会(JOA)评分评价患者神经功能状态,并按以下公式计算 JOA 评分改善率:(术后 JOA 评分-术前 JOA 评分)/(17-术前 JOA 评分)×100%;并采用 Odom 分级评价整体满意度,分为优、良、可、差 4 个等级[10]。此外,记录翻修手术情况。
1.3.2. 影像学指标
手术前后摄正侧位和动力位 X 线片,术前行 CT 和 MRI 检测。测量术前,术后 1 周、6 个月、1 年、2 年、5 年、10 年及末次随访时的以下指标:① 活动度(range of motion,ROM):于屈伸位 X 线片上测量,包括颈椎整体(C2~C7)、手术节段、上位邻近节段(upper adjacent segment,UAS)和下位邻近节段(lower adjacent segment,LAS)的 ROM;② 矢状位前凸角:于侧位 X 线片上测量,包括颈椎整体(C2~C7)和手术节段的前凸角,正值代表前凸,负值代表后凸;③ 椎间隙高度(intervertebral disc height,IDH):于侧位 X 线片上测量 IDH(假体 2 个终板之间的距离)[11],包括手术节段、UAS 和 LAS 的 IDH。
同时于术后 1 周、6 个月、1 年、2 年、5 年、10 年及末次随访时在 X 线片上观察有无以下情况发生:① 假体移位:冠状位和矢状位上平行于椎体终板滑动超过 3 mm[2, 12],包括冠状面和矢状面移位。② 假体下沉:与术后即刻相比,假体垂直于椎体终板下移超过 3 mm[12]。③ 假体松动:动力位 X 线片示假体与骨面对合不良,并且假体周围有骨吸收现象,伴或不伴假体位置变化[13]。④ 假体锁死/融合:有超过 50% 的骨小梁桥接并且无活动度(≤2°)[12]。⑤HO:根据 McAfee 等[14]分级系统分为 0 级至 4 级,0 级:无 HO;1 级:骨赘未侵入椎间隙;2 级:骨赘侵入椎间隙但不影响假体活动度;3 级:骨赘影响假体活动度;4 级,骨桥形成,假体被骨质包绕。0 级定义为无 HO,1~4 级均定义为发生 HO。⑥ASD:前纵韧带骨化进行性加重、椎间隙塌陷超过 30% 并且前方骨桥形成[7],包括上位 ASD(upper ASD,UASD)和下位 ASD(lower ASD,LASD)。根据有无发生 HO 或 ASD 分组,比较患者 ROM。
1.4. 统计学方法
采用 SPSS22.0 统计软件进行分析。计量资料以均数±标准差表示,手术前后各时间点间比较采用重复测量方差分析,两两比较采用配对 t 检验,两组间比较采用独立样本 t 检验;计数资料比较采用 χ2 检验或 Fisher 确切概率法;等级资料比较采用秩和检验;检验水准 α=0.05。
2. 结果
2.1. 临床疗效评价
术后患者均获随访,随访时间 121~150 个月,平均 135.8 个月。随访期间无 1 例患者行翻修手术。术后 1 周及末次随访时 VAS 评分、NDI 评分、JOA 评分和 Odom 分级均较术前显著改善,差异有统计学意义(P<0.05);其中末次随访时 VAS 评分和 NDI 评分较术后 1 周进一步改善,差异有统计学意义(P<0.05)。术后 1 周及末次随访时的 JOA 评分及改善率比较差异无统计学意义(P>0.05)。见表 1。
表 1.
Comparison of clinical evaluation indexes at different time points before and after operation (n=118)
患者手术前后各时间点临床评价指标比较(n=118)
| 时间
Time |
VAS 评分
VAS score |
NDI 评分
NDI score |
JOA 评分
JOA score |
Odom 分级
Odom classification |
|||||
| 评分
Score |
改善率(%)
Improvement rate (%) |
优
Excellent |
良
Good |
可
Fair |
差
Poor |
||||
|
*与术前比较 P<0.05,#与术后 1 周比较 P<0.05
*Compared with preoperative value, P<0.05;#compared with postoperative value at 1 week, P<0.05 | |||||||||
| 术前
Preoperative |
5.85±2.44# | 29.92±3.66# | 12.80±2.79# | − | 0 | 8 | 51 | 59 | |
| 术后 1 周
Postoperative at 1 week |
2.27±1.66* | 18.97±4.15* | 15.71±1.53* | 72.46±32.57 | 62 | 39 | 13 | 4 | |
| 末次随访
Last follow-up |
1.22±1.30*# | 15.97±4.05*# | 15.81±1.84* | 75.61±48.03 | 74 | 32 | 10 | 2 | |
| 统计值
Statistic |
F=100.105
P= 0.000 |
F=194.083
P= 0.000 |
F=38.404
P= 0.000 |
t=–0.417
P= 0.677 |
Z=130.646
P= 0.000 |
||||
2.2. 影像学指标
2.2.1. 影像学测量
① ROM:颈椎 ROM 除术后 1 周、6 个月及 10 年较术前有所减小,差异有统计学意义(P<0.05)外,其余各时间点间颈椎 ROM 比较差异均无统计学意义(P>0.05)。手术节段 ROM 除术后 1 周和末次随访时较术前有所减小,差异有统计学意义(P<0.05)外,其余各时间点间手术节段 ROM 比较差异均无统计学意义(P>0.05)。UAS 和 LAS 的 ROM 术后各时间点间比较差异均无统计学意义(P>0.05)。见表 2。
表 2.
Comparison of imaging measurements at different time points before and after operation (
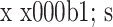 )
)
患者手术前后各时间点影像学测量指标比较(
 )
)
| 时间
Time |
ROM (°) | 矢状位前凸角(°)
Sagittal lordosis angle (°) |
IDH (mm) | ||||||||
| 颈椎
Cervical spine |
手术节段
Operative segment |
UAS | LAS | 颈椎
Cervical spine |
手术节段
Operative segment |
手术节段
Operative segment |
UAS | LAS | |||
|
*与术前比较 P<0.05
*Compared with preoperative value, P<0.05 | |||||||||||
| 术前
Preoperative |
42.45±16.52 | 8.94±5.70 | − | − | 18.37±13.33 | 2.03±4.81 | 4.36±0.88 | − | − | ||
| 术后 1 周
Postoperative at 1 week |
33.65±13.02* | 6.74±3.54* | 6.43±4.40 | 6.57±4.98 | 16.36±11.55 | 5.34±6.34* | 5.50±1.86* | 4.76±0.71 | 4.95±1.10 | ||
| 术后 6 个月
Postoperative at 6 months |
37.10±12.77* | 8.15±3.79 | 7.83±5.36 | 7.61±5.32 | 20.08±10.23 | 6.26±6.10* | 6.83±0.90* | 4.71±0.74 | 4.77±0.96 | ||
| 术后 1 年
Postoperative at 1 year |
39.93±12.73 | 8.39±3.84 | 7.96±4.16 | 8.14±5.76 | 21.33±10.77 | 5.90±6.45* | 6.90±0.93* | 4.66±0.71 | 4.78±1.01 | ||
| 术后 2 年
Postoperative at 2 years |
38.18±12.74 | 7.89±4.01 | 7.72±4.97 | 8.61±5.61 | 20.79±10.95 | 5.63±7.15* | 6.78±0.86* | 4.69±0.72 | 4.83±0.90 | ||
| 术后 5 年
Postoperative at 5 years |
38.15±12.78 | 8.43±3.68 | 7.60±4.44 | 8.45±5.16 | 21.96±11.14 | 4.81±6.73 | 6.78±0.90* | 4.71±0.70 | 4.73±1.06 | ||
| 术后 10 年
Postoperative at 10 years |
37.04±11.14* | 7.80±3.67 | 7.59±3.86 | 7.41±4.31 | 20.42± 9.88 | 4.58±6.56 | 6.73±0.87* | 4.71±0.72 | 4.64±0.95 | ||
| 末次随访
Last follow-up |
37.91±12.14 | 7.30±3.55* | 7.38±3.55 | 7.71±4.33 | 20.84± 8.61 | 4.39±7.13 | 6.72±0.93* | 4.69±0.72 | 4.66±0.96 | ||
| 统计值
Statistic |
F=2.184
P=0.035 |
F=2.278
P=0.027 |
F=0.902
P=0.494 |
F=1.041
P=0.398 |
F=1.640
P=0.122 |
F=3.015
P=0.007 |
F=92.296
P= 0.000 |
F=1.001
P=0.424 |
F=0.657
P=0.684 |
||
② 矢状位前凸角:手术前后各时间点颈椎矢状位前凸角比较差异均无统计学意义(P>0.05)。术后各时间点手术节段矢状位前凸角均大于术前,其中术后 1 周、6 个月、1 年、2 年的前凸角与术前比较差异有统计学意义(P<0.05);但术后 10 年及末次随访时与术前比较差异无统计学意义(P>0.05)。见表 2。末次随访时 33 个椎间盘(21.8%)出现节段后凸。
③ IDH:术后各时间点手术节段 IDH 均较术前显著改善,差异有统计学意义(P<0.05);术后 6 个月及之后各时间点手术节段 IDH 较术后 1 周进一步改善,差异有统计学意义(P<0.05)。术后各时间点间 UAS 和 LAS 的 IDH 比较差异均无统计学意义(P>0.05)。见表 2。
2.2.2. 影像学并发症
① 假体移位、下沉、松动:术后各时间点均未发生假体冠状位移位、矢状位移位、下沉和松动。以术后 1 周为基线(此时各参数均为 0),各时间点假体移位距离以及下沉距离与基线数据比较差异均有统计学意义(P<0.01);但术后 6 个月后各时间点间比较,差异均无统计学意义(P>0.05)。见表 3。② 假体锁死/融合:术后 1 周无假体锁死表现;但术后 6 个月出现 3 例(1.9%)假体锁死现象,且锁死病例数逐渐增加,末次随访时达 16 例(10.4%),但与术后 6 个月比较差异无统计学意义(P>0.05)。见表 3。③ ASD:术后 1 周 UASD 和 LASD 发生率分别为 1.3%(2/154)和 2.6%(4/154),随时间延长其发生率逐渐增加,各时间点间比较差异均有统计学意义(P<0.05)。进一步分析显示,ASD 组患者术后各时间点手术节段 ROM 均小于无 ASD 组,但比较差异均无统计学意义(P>0.05)。见表 3、4。④ HO:术后 1 周无手术节段出现 HO;而术后 6 个月有 58.4%(90/154)手术节段出现 HO,多数以低级别 HO 为主(49.4%),但有 3 例椎间隙出现了 4 级 HO;随时间延长 HO 发生率逐渐增加,与术后 6 个月比较差异均有统计学意义(P<0.05)。进一步分析显示,HO 组患者术后各时间点手术节段 ROM 均小于无 HO 组患者,其中术后 6 个月、2 年、5 年、10 年时两组间比较差异有统计学意义(P<0.05)。见表 3、5,图 1。
表 3.
Comparison of imaging complications at different time points after operation
患者术后各时间点影像学并发症指标比较
| 时间
Time |
假体移位(mm)
Prosthesis migration (mm) |
假体下沉
(mm) Prosthesis subsidence (mm) |
假体锁死/融合例数(%)
Number of prosthetic locking/fusion (%) |
ASD 例数(%)
Number of ASD (%) |
HO 等级
HO grading |
|||||||
| 冠状位
Coronal |
矢状位
Sagittal |
UASD | LASD | 0 | 1 | 2 | 3 | 4 | ||||
|
*与基线比较P<0.05
*Compared with baseline, P<0.05 | ||||||||||||
| 术后 1 周
Postoperative at 1 week |
0 | 0 | 0 | 0 | 2 ( 1.3) | 4 ( 2.6) | 0 | 0 | 0 | 0 | 0 | |
| 术后 6 个月
Postoperative at 6 months |
0.16±0.37* | 0.13±0.24* | 0.10±0.17* | 3 ( 1.9) | 6 ( 5.0)* | 7 ( 5.9) | 64 (41.6) | 58 (37.7) | 18 (11.7) | 11( 7.1) | 3 ( 1.9) | |
| 术后 1 年
Postoperative at 1 year |
0.16±0.26* | 0.15±0.27* | 0.13±0.24* | 5 ( 3.2) | 13 (10.9)* | 9 ( 7.6)* | 52 (33.8) | 57 (36.3) | 22 (14.3) | 16 (10.4) | 7 ( 5.1) | |
| 术后 2 年
Postoperative at 2 years |
0.24±0.31* | 0.21±0.32* | 0.18±0.26* | 6 ( 3.9) | 16 (13.4)* | 14 (11.8)* | 46 (29.9) | 61 (40.2) | 22 (14.3) | 17 (10.5) | 8 ( 5.2) | |
| 术后 5 年
Postoperative at 5 years |
0.21±0.27* | 0.24±0.31* | 0.19±0.26* | 8 ( 5.2) | 19 (16.0)* | 19 (16.0)* | 33 (22.1) | 64 (41.6) | 21 (13.1) | 23 (14.3) | 13 ( 9.0) | |
| 术后 10 年
Postoperative at 10 years |
0.31±0.45* | 0.23±0.33* | 0.24±0.25* | 13 ( 8.4) | 26 (21.8)* | 24 (20.2)* | 20 (13.0) | 54 (35.1) | 42 (27.3) | 22 (14.3) | 16 (10.4)* | |
| 末次随访
Last follow-up |
0.29±0.39* | 0.27±0.38* | 0.24±0.29* | 16 (10.4) | 27 (22.7)* | 25 (21.0)* | 18 (11.7) | 41 (26.6) | 51 (33.1) | 28 (18.2) | 16 (10.4) | |
| 统计值
Statistic |
F=8.412
P=0.000 |
F=7.738
P=0.000 |
F=10.379
P= 0.000 |
χ2=0.207
P=0.649 |
χ2=4.188
P=0.041 |
χ2=4.912
P=0.027 |
Z=21.517
P= 0.000 |
|||||
表 4.
Comparison of operative segment ROM between ASD group and non-ASD group at different time points after operation (°,
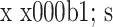 )
)
ASD 组和无 ASD 组患者术后各时间点手术节段 ROM 比较(°,
 )
)
| 组别
Group |
术后 1 周
Postoperative at 1 week |
术后 6 个月
Postoperative at 6 months |
术后 1 年
Postoperative at 1 year |
术后 2 年
Postoperative at 2 years |
术后 5 年
Postoperative at 5 years |
术后 10 年
Postoperative at 10 years |
末次随访
Last follow-up |
| ASD 组
ASD group |
6.85±1.98 | 7.90±3.99 | 7.87±3.92 | 7.17±4.07 | 7.86±4.08 | 7.19±3.80 | 7.05±4.08 |
| 无 ASD 组
Non-ASD group |
8.60±3.62 | 9.47±5.77 | 9.07±4.80 | 9.34±4.58 | 9.12±3.41 | 8.25±3.08 | 7.87±2.86 |
| 统计值
Statistic |
t=–1.391
P= 0.143 |
t=0.406
P=0.686 |
t=0.895
P=0.375 |
t=1.349
P=0.154 |
t=0.646
P=0.279 |
t=1.316
P=0.193 |
t=0.248
P=0.621 |
表 5.
Comparison of operative segment ROM between HO group and non-HO group at different time points after operation (°,
 )
)
HO 组和无 HO 组患者术后各时间点手术节段 ROM 比较(°,
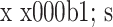 )
)
| 组别
Group |
术后 1 周
Postoperative at 1 week |
术后 6 个月
Postoperative at 6 months |
术后 1 年
Postoperative at 1 year |
术后 2 年
Postoperative at 2 years |
术后 5 年
Postoperative at 5 years |
术后 10 年
Postoperative at 10 years |
末次随访
Last follow-up |
| HO 组
HO group |
− | 5.89±1.85 | 7.04±3.71 | 6.01±2.60 | 6.97±3.18 | 6.03±3.14 | 6.29±3.53 |
| 无 HO 组
Non-HO group |
6.74±3.54 | 8.19±2.86 | 8.49±3.84 | 7.90±3.02 | 8.52±2.42 | 8.00±3.67 | 7.45±3.51 |
| 统计值
Statistic |
− |
t=–2.965
P= 0.012 |
t=–1.329
P= 0.188 |
t=–2.506
P= 0.032 |
t=–1.985
P= 0.043 |
t=–2.507
P= 0.014 |
t=–1.584
P= 0.117 |
图 1.
Lateral X-ray films of postoperative HO progression of a 55-year-male patient with double-level (C4-6) CDDD after TDR
患者,男,55 岁,C4~6双节段 CDDD 行 TDR 术后 HO 进展侧位 X 线片
a. 术前;b. 术后即刻双节段均未出现 HO;c. 术后 1 年双节段均出现 1 级 HO;d. 术后 2 年双节段均出现 2 级 HO;e. 术后 10 年 C4、5 为 3 级 HO,C5、6 为 4 级 HO,但患者临床效果满意
a. Preoperation; b. No HO was found in both levels at immediate after operation; c. Both levels were of grade 1 of HO at 1 year after operation; d. Both levels were of grade 2 of HO at 2 years after operation; e. C4, 5 was of grade 3 of HO while C5, 6 was of grade 4 of HO at 10 years after operation, but satisfactory effectiveness was acquired

3. 讨论
自颈椎人工间盘出现,关于 TDR 治疗 CDDD 的疗效进行了不间断研究。多数文献报道与 ACDF 相比,TDR 同样能够获得满意的临床疗效[1-3]。一项关于采用 Prodisc-C 假体行 TDR 和 ACDF 的随机对照试验首次进行了为期 7 年的随访,证实 TDR 治疗单节段 CDDD 是安全有效的,而且再手术率小于 ACDF[4]。但是关于 TDR 的远期疗效仍不明确,这造成了使用 TDR 治疗 CDDD 的不确定性,致使术者在一定程度上倾向于采用相对经济和疗效确切的 ACDF[5, 15]。而关于使用 Mobi-C 假体、Prodisc-C 假体和 Prestige-LP 假体的系统综述及 meta 分析均支持 TDR 手术疗效更优的结论[16-17]。由于既往研究 TDR 疗效的随访时间较短[10, 18],因此本研究开展了使用 Prodisc-C 假体行 TDR 长达 10 年以上的随访。结果显示,尽管 TDR 存在或多或少的影像学并发症,但自术后即刻至末次随访,临床症状较术前均显著改善。
3.1. 影像学测量指标
TDR 的最终目的是通过长期维持手术节段 ROM 来减小 ASD 发生率[10]。关于 TDR 术后 24 个月随访表明,单节段 TDR 术后维持了手术节段和颈椎整体的 ROM[9];王岩等[19]研究了 TDR 术后 2 年颈椎整体(C3~7)ROM 平均为 42.8°。本研究中,末次随访时颈椎整体和手术节段 ROM 分别为(37.91±12.14)° 和(7.30±3.55)°,同既往文献一致。然而,关于对邻近节段避免出现过载的、“最适”手术节段的 ROM,尚无统一标准[8]。例如,Murrey 等[20]采用 Prodisc-C 假体行 TDR,术后 2 年随访手术节段平均 ROM 为 8.4°,其他影像学参数均处于正常范围;而 Heller 等[21]报道使用 Bryan 假体手术节段 ROM 较 Murrey 等[20]降低约 2°(平均为 6.5°),但同样获得了满意的影像学参数。因而无法对“较适合”手术节段 ROM 作出判断。
在体研究和生物力学试验均已证实,TDR 术后手术节段 ROM 会有所增加。DiAngelo 等[22]通过体外生物力学证实单节段 Prodisc-C 模型手术节段 ROM 为 13.1°;Lanman 等[23]报道双节段使用 Prestige-LP 假体术后 84 个月,手术节段 ROM 均>6°。本研究中,除术后 1 周外,大部分随访时间点中颈椎和手术节段 ROM 较术前差异无统计学意义,与 Lanman 等结论一致。但是,手术节段 ROM 增加的临床意义尚未明确,在理论上或许可以维持手术节段小关节活动,而避免发生自发融合[11]。本研究末次随访时,有 10.4% 椎间隙发生融合,但大多数节段活动度保留,且获得满意的临床结局。另外,Zeng 等[10]通过 6 年的随访研究证实,使用 Prestige-LP 假体行 TDR 能够保留中长期手术节段活动度,并避免邻近节段活动度过度增加。本研究中邻近节段 ROM 术后各随访时间点较术前差异无统计学意义,远期邻椎 ROM 维持满意,与 Zeng 等得出的避免邻近节段 ROM 过大是一致的。
颈椎曲度是 TDR 术后重要的影像学参数,有报道证实颈椎曲度维持或增加可以改善临床疗效[24-25]。Fong 等[26]认为采用 Bryan 假体行 TDR 术后手术节段后凸与终板变性存在正相关。既往文献表明,使用 Bryan 假体行 TDR,在适当选择患者和手术技术保证的前提下,可以恢复并维持手术节段前凸[27-28];而 Prodisc-C 假体基于球窝关节设计理念,或许更易恢复手术节段前凸[29]。本研究中与术前相比,手术节段术后 1 周前凸平均增加了 3.31°,但术后 10 年仅平均增加了 2.36°,并且末次随访时 20% 患者出现手术节段后凸。而颈椎整体前凸维持良好,至末次随访时仍无患者出现后凸。
IDH 与椎间盘退变、ROM 和矢状位曲度密切相关[11]。Johnson 等[30]对有症状的 CDDD 患者研究发现,由于该节段 IDH 的丢失而出现了局部的后凸畸形。IDH 的恢复虽然很重要,但存在较大异质性,不同假体尺寸可影响术后的运动机能,而且假体尺寸的非连续性也不可能完全匹配生理间盘退变前的尺寸[31]。唯一一致的是,假体的试模高度为统一的 5 mm、6 mm 和 7 mm,但不足够或不恰当的假体型号会增加畸形和假体移位的风险[32]。本研究术后手术节段 IDH 显著增加,改善了 IDH 的丢失和不良事件的出现,并且 IDH 在随访期间基本保持稳定。UAS 和 LAS 的 IDH 术后未受明显影响,提示手术节段 IDH 的适当重建甚至增加或许并不会影响邻近节段。
3.2. 影像学并发症
假体移位在长期随访中的报道极少,Zhang 等[33]报道了 3 例患者(5.4%)假体向前移位 2~3 mm,但无相关临床症状;Yang 等[5]进行系统综述,得出假体移位为小概率事件,但在人工间盘的发生率要高于椎间融合器,但论证等级不高。本研究同样显示无假体移位出现,从该参数角度认为 TDR 是安全的。影像学结局与假体的运动学机能或动态稳定特性是相关的[8]。例如,非“龙骨”锚定的假体 Prodisc-Vivo,在设计上通过上下终板的 6 个倒齿提供初始稳定性。对于人口统计学相似的队列,对比经典的“龙骨”锚定假体如 Kineflex-C 和 Prodisc-C,Prodisc-Vivo 更易出现假体移位[34]。当然,由于“龙骨”插入椎体需去除更多骨质,Prodisc-C 造成骨质劈裂的风险也相应增加[8, 35],但本研究中无骨质劈裂发生。对椎体后缘后纵韧带的充分松解和适当位置的假体植入,或许在防止假体移位方面有重大意义[8]。假体下沉同样在 TDR 中罕见,但证据等级较低。Zigler 等[2]对实施 TDR 的 209 例患者进行 5 年随访,发现仅有 1 例(0.5%)出现下沉;而 Coric 等[36]和 Zhang 等[33]均未发现下沉者。本研究同样无假体下沉节段出现。
既往多数研究未提及假体松动,因此对其所产生的影响也是模棱两可的结论[5]。Nabhan 等[37]研究显示,TDR 术后 1 年患者无假体松动出现。Coric 等[36]和Philips 等[15]的临床随机对照研究分别报道了 TDR 术后有 0 例和 6 例(3.1%)假体松动发生,但与 ACDF 术后假体松动发生率比较差异无统计学意义。假体锁死/融合在 TDR 患者中无系统报道,有文献曾报道了假体完全融合,但例数较少[38]。根据既往文献报道,几乎所有锁死/融合的人工间盘均为限制型或半限制型间盘[39]。而 Heary 等[40]首次报道了 1 例患者使用非限制型假体 Discover Disc 60 个月后出现锁死/融合的现象,但患者临床疗效满意。本研究假体锁死/融合例数逐年增多,在末次随访时为 10.4%(16/154),低于Suchomel 等[25]报道的使用 Prodisc-C 假体术后 4 年融合率 18%,且所有出现锁死/融合的患者均未主诉不适。Kraemer 等[7]对 ASD 的定义进行系统综述,指出目前关于 ASD 的定义多达 7 种但均未达到共识。Coric 等[34]通过 X 线片从术前至末次随访时评价 ASD,将其分为无、轻度、中度、重度 4 个级别;而 Kellgren 等[38]通过 Kellgren-Lawrence 分级进行评价。其他文献有通过邻近节段再手术率来代替 ASD 发生率的报道,但均无法找到合适的影像学参数[5]。TDR 相对于 ACDF 的一大优势在于可防止邻近节段退变或邻椎病[11],但短期随访发现两者 ASD 发生率差异无统计学意义[38-39]。Coric 等[34]报道 ASD 从 TDR 术前的 52% 增加至术后 2 年的 62%,但 ASD 发生率与 ACDF 无差异;而关于 TDR(Prodisc-C)和 ACDF 7 年随访的随机对照试验显示,ACDF 组邻近节段再手术率高,提示 TDR 对邻近节段有保护作用[4],随着随访时间延长,TDR 相对于 ACDF 的优势可能更加明显。然而,关于 TDR 和 ACDF 术后发生 ASD 的论证等级较低,需要高质量文献的支持[5]。本研究显示 UAS 和 LAS 的 ASD 发生率随时间延长均有所增加,但同期随访无明显差异。本研究的 ASD 发生率与既往文献报道基本一致,但由于 ASD 定义本身存在异质性且本研究并无 ACDF 作为对照组,因此该结论的论证强度并不高。
3 级和 4 级 HO 在临床上意义较大,可以影响到单位节段 ROM 及功能,这违背了 TDR 手术的初衷[41]。有报道“龙骨”锚定的假体如 Prodisc-C 发生 HO 几率更大,可能因其设计外形,使得在植入时要更多地破坏前方皮质骨,并且需要扩大植入床[8]。Yi 等[41]发现随访 12 个月后,使用 Prodisc-C 假体发生 HO 比例已高达 71.4%,而 Bryan 假体为 21.0%;但目前临床疗效和 HO 的分级以及发生率之间的相关性尚不明确。有报道术后 12 个月随访的 HO 发生率为 17.8%~72.3%(3 级和 4 级为 4.2%~23.1%),术后 24 个月 HO 发生率为 28.8%~78.5%(3 级和 4 级 HO 为 8.5%~32.3%)。本研究术后 1、2 年随访时 HO 发生率分别为 66.2% 和 70.1%,与既往报道相似[42-43],在术后第 1 年内 HO(66.2%)进展速度最快。本研究提示 4 级 HO 自术后 6 个月即出现,考虑“龙骨”锚定假体为重要因素,但末次随访时 HO 的发生率(88.3%)与 Suchomel 等[25]报道的术后 4 年 HO 发生率(88%)相比是可以接受的,并且较少患者出现与之相关的临床症状。
3.3. 临床疗效评价
大量研究已证实无论随访周期长短或假体类型相同与否,TDR 术后均取得满意疗效[12, 44-45]。本研究中,TDR 术后各时间点 NDI、JOA、VAS 评分和 Odom 分级较术前均有显著提高。末次随访时仍存在 2 例 Odom 分级“差”者,此 2 例患者均伴有颈部不适而无上肢疼痛及功能减退,而且通过保守治疗有所改善。因此,使用 Prodisc-C 假体行 TDR 在恢复神经功能和改善生活质量上是长期安全有效的。翻修手术致使患者出现躯体和经济上的双重负担[46-47]。一项 7 年随访的成本效益分析显示相对于 ACDF,TDR 或许能通过降低再手术率产生最终的经济优势[48]。TDR 相比于 ACDF 可以降低远期翻修率,特别是在邻近节段[12, 49]。Delamater 等[49]发现相比于 ACDF,术后 5 年 TDR 组再手术率更低,而 ACDF 较 TDR 的再手术率高达 5 倍,主要因假关节和邻近节段病而进行翻修。Hisey 等[50]通过 48 个月随访的随机对照研究显示,TDR 术后翻修率仅为 0.6%,而 ACDF 组为 3.7%。本研究中,尽管末次随访时有 2 例疗效“差”者,但无患者因内植物失败或 ASD 行二次手术。
综上述,通过对使用 Prodisc-C 假体行 TDR 术后远期随访分析显示,尽管术后远期出现部分影像学并发症,但术后临床疗效显著提高。术后颈椎整体 ROM、矢状位前凸角和手术节段 IDH 保持稳定,并且 TDR 对邻近节段影像学参数影响较小。总之,TDR 在治疗 CDDD 时可以提供有效和安全的远期临床结局。但本研究还存在一些不足:首先,本研究为单中心回顾性研究,缺少对照组,无法与 ACDF 比较得出证据等级更高的结论;其次,研究纳入样本量较小,还需进一步扩大样本量进行研究;最后,本研究 HO 和 ASD 的诊断未借助 CT 或 MRI,而且由于对 ASD 的定义缺乏共识,使得关于 ASD 发生率的结论存在一定局限性。
Funding Statement
国家重点研发计划资助项目(2016YFC0105606)
National Program on Key Basic Research Project of China (2016YFC0105606)
References
- 1.Jawahar A, Cavanaugh DA, Kerr ER, et al Total disc arthroplasty does not affect the incidence of adjacent segment degeneration in cervical spine: results of 93 patients in three prospective randomized clinical trials. Spine J. 2010;10(12):1043–1048. doi: 10.1016/j.spinee.2010.08.014. [DOI] [PubMed] [Google Scholar]
- 2.Zigler JE, Delamarter R, Murrey D, et al ProDisc-C and anterior cervical discectomy and fusion as surgical treatment for single-level cervical symptomatic degenerative disc disease: five-year results of a Food and Drug Administration study. Spine (Phila Pa 1976) 2013;38(3):203–209. doi: 10.1097/BRS.0b013e318278eb38. [DOI] [PubMed] [Google Scholar]
- 3.洪瑛, 邓宇骁, 刘浩, 等 单节段颈椎间盘置换术中颈椎体位对术后颈椎中立位生理轴线重建的影响. 中国修复重建外科杂志. 2013;27(1):62–65. [PubMed] [Google Scholar]
- 4.Janssen ME, Zigler JE, Spivak JM, et al ProDisc-C total disc replacement versus anterior cervical discectomy and fusion for single-level symptomatic cervical disc disease: seven-year follow-up of the prospective randomized U.S. Food and Drug Administration Investigational device exemption study. J Bone Joint Surg (Am) 2015;97(21):1738–1747. doi: 10.2106/JBJS.N.01186. [DOI] [PubMed] [Google Scholar]
- 5.Yang X, Janssen T, Arts MP, et al Radiological follow-up after implanting cervical disc prosthesis in anterior discectomy: a systematic review. Spine J. 2018;18(9):1678–1693. doi: 10.1016/j.spinee.2018.04.021. [DOI] [PubMed] [Google Scholar]
- 6.Cho YH, Kim KS, Kwon YM Heterotopic ossification after cervical arthroplasty with ProDisc-C: time course radiographic follow-up over 3 years. Korean J Spine. 2013;10(1):19–24. doi: 10.14245/kjs.2013.10.1.19. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 7.Kraemer P, Fehlings MG, Hashimoto R, et al A systematic review of definitions and classification systems of adjacent segment pathology. Spine (Phila Pa 1976) 2012;37(22 Suppl):S31–39. doi: 10.1097/BRS.0b013e31826d7dd6. [DOI] [PubMed] [Google Scholar]
- 8.Mehren C, Heider F, Sauer D, et al. Clinical and radiological outcome of a new total cervical disc replacement design. Spine (Phila Pa 1976), 2018. [Epub ahead of print]
- 9.Park JJ, Quirno M, Cunningham MR, et al Analysis of segmental cervical spine vertebral motion after prodisc-C cervical disc replacement. Spine (Phila Pa 1976) 2010;35(8):E285–289. doi: 10.1097/BRS.0b013e3181c88165. [DOI] [PubMed] [Google Scholar]
- 10.Zeng J, Liu H, Rong X, et al Clinical and radiographic outcomes of cervical disc arthroplasty with Prestige-LP Disc: a minimum 6-year follow-up study. BMC Musculoskelet Disord. 2018;19(1):285. doi: 10.1186/s12891-018-2201-9. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 11.Duggal N, Bertagnoli R, Rabin D, et al ProDisc-C: an in vivo kinematic study . J Spinal Disord Tech. 2011;24(5):334–339. doi: 10.1097/BSD.0b013e3181fbf8aa. [DOI] [PubMed] [Google Scholar]
- 12.Loumeau TP, Darden BV, Kesman TJ, et al A RCT comparing 7-year clinical outcomes of one level symptomatic cervical disc disease (SCDD) following ProDisc-C total disc arthroplasty (TDA) versus anterior cervical discectomy and fusion (ACDF) Eur Spine J. 2016;25(7):2263–2270. doi: 10.1007/s00586-016-4431-6. [DOI] [PubMed] [Google Scholar]
- 13.李志宇, 田伟, 韦祎, 等 颈椎人工间盘置换术后假体松动一例. 中华医学杂志. 2018;98(41):3374–3376. doi: 10.3760/cma.j.issn.0376-2491.2018.41.017. [DOI] [Google Scholar]
- 14.McAfee PC, Cunningham BW, Devine J, et al Classification of heterotopic ossification (HO) in artificial disk replacement. J Spinal Disord Tech. 2003;16(4):384–389. doi: 10.1097/00024720-200308000-00010. [DOI] [PubMed] [Google Scholar]
- 15.Phillips FM, Lee JY, Geisler FH, et al A prospective, randomized, controlled clinical investigation comparing PCM cervical disc arthroplasty with anterior cervical discectomy and fusion. 2-year results from the US FDA IDE clinical trial. Spine (Phila Pa 1976) 2013;38(15):E907–918. doi: 10.1097/BRS.0b013e318296232f. [DOI] [PubMed] [Google Scholar]
- 16.Chen C, Zhang X, Ma X Durability of cervical disc arthroplasties and its influence factors: A systematic review and a network meta-analysis. Medicine (Baltimore) 2017;96(6):e5947. doi: 10.1097/MD.0000000000005947. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 17.Gornet MF, Burkus JK, Shaffrey ME, et al Cervical disc arthroplasty with prestige LP disc versus anterior cervical discectomy and fusion: seven-year outcomes. Int J Spine Surg. 2016;10:24. doi: 10.14444/3024. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 18.Quan GM, Vital JM, Hansen S, et al Eight-year clinical and radiological follow-up of the Bryan cervical disc arthroplasty. Spine (Phila Pa 1976) 2011;36(8):639–646. doi: 10.1097/BRS.0b013e3181dc9b51. [DOI] [PubMed] [Google Scholar]
- 19.王岩, 蔡斌, 张雪松, 等 Bryan 人工颈椎间盘置换治疗单节段颈椎病的前瞻性临床研究. 中华外科杂志. 2008;46(5):328–332. doi: 10.3321/j.issn:0529-5815.2008.05.004. [DOI] [Google Scholar]
- 20.Murrey D, Janssen M, Delamarter R, et al Results of the prospective, randomized, controlled multicenter Food and Drug Administration investigational device exemption study of the ProDisc-C total disc replacement versus anterior discectomy and fusion for the treatment of 1-level symptomatic cervical disc disease. Spine J. 2009;9(4):275–286. doi: 10.1016/j.spinee.2008.05.006. [DOI] [PubMed] [Google Scholar]
- 21.Heller JG, Sasso RC, Papadopoulos SM, et al Comparison of BRYAN cervical disc arthroplasty with anterior cervical decompression and fusion: clinical and radiographic results of a randomized, controlled, clinical trial. Spine (Phila Pa 1976) 2009;34(2):101–107. doi: 10.1097/BRS.0b013e31818ee263. [DOI] [PubMed] [Google Scholar]
- 22.DiAngelo DJ, Foley KT, Morrow BR, et al In vitro biomechanics of cervical disc arthroplasty with the ProDisc-C total disc implant . Neurosurg Focus. 2004;17(3):E7. [PubMed] [Google Scholar]
- 23.Lanman TH, Burkus JK, Dryer RG, et al Long-term clinical and radiographic outcomes of the Prestige LP artificial cervical disc replacement at 2 levels: results from a prospective randomized controlled clinical trial. J Neurosurg Spine. 2017;27(1):7–19. doi: 10.3171/2016.11.SPINE16746. [DOI] [PubMed] [Google Scholar]
- 24.刘浩, 邓宇骁, 刘子扬, 等 Pretic-Ⅰ人工颈椎间盘置换术治疗颈椎间盘突出症的早期疗效观察. 中国修复重建外科杂志. 2017;31(5):513–518. [Google Scholar]
- 25.Suchomel P, Jurak L, Benes VR, et al Clinical results and development of heterotopic ossification in total cervical disc replacement during a 4-year follow-up. Eur Spine J. 2010;19(2):307–315. doi: 10.1007/s00586-009-1259-3. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 26.Fong SY, DuPlessis SJ, Casha S, et al Design limitations of Bryan disc arthroplasty. Spine J. 2006;6(3):233–241. doi: 10.1016/j.spinee.2006.01.007. [DOI] [PubMed] [Google Scholar]
- 27.Tian W, Yan K, Han X, et al Comparison of the clinical and radiographic results between cervical artificial disk replacement and anterior cervical fusion: a 6-year prospective nonrandomized comparative study. Clin Spine Surg. 2017;30(5):E578–E586. doi: 10.1097/BSD.0000000000000206. [DOI] [PubMed] [Google Scholar]
- 28.Dejaegher J, Walraevens J, van Loon J, et al 10-year follow-up after implantation of the Bryan Cervical Disc Prosthesis. Eur Spine J. 2017;26(4):1191–1198. doi: 10.1007/s00586-016-4897-2. [DOI] [PubMed] [Google Scholar]
- 29.Rabin D, Bertagnoli R, Wharton N, et al Sagittal balance influences range of motion: an in vivo study with the ProDisc-C . Spine J. 2009;9(2):128–133. doi: 10.1016/j.spinee.2008.01.009. [DOI] [PubMed] [Google Scholar]
- 30.Johnson JP, Lauryssen C, Cambron HO, et al Sagittal alignment and the Bryan cervical artificial disc. Neurosurg Focus. 2004;17(6):E14. doi: 10.3171/foc.2004.17.6.14. [DOI] [PubMed] [Google Scholar]
- 31.Pickett GE, Rouleau JP, Duggal N Kinematic analysis of the cervical spine following implantation of an artificial cervical disc. Spine (Phila Pa 1976) 2005;30(17):1949–1954. doi: 10.1097/01.brs.0000176320.82079.ce. [DOI] [PubMed] [Google Scholar]
- 32.Garcia M, Ghanayem A, Tzermiadianos M, et al Effect of cervical disc prosthesis height on kinematics and foraminal size. Spine J. 2006;6(5):72S–73S. [Google Scholar]
- 33.Zhang HX, Shao YD, Chen Y, et al A prospective, randomised, controlled multicentre study comparing cervical disc replacement with anterior cervical decompression and fusion. Int Orthop. 2014;38(12):2533–2541. doi: 10.1007/s00264-014-2497-5. [DOI] [PubMed] [Google Scholar]
- 34.Coric D, Nunley PD, Guyer RD, et al Prospective, randomized, multicenter study of cervical arthroplasty: 269 patients from the Kineflex|C artificial disc investigational device exemption study with a minimum 2-year follow-up: clinical article. J Neurosurg Spine. 2011;15(4):348–358. doi: 10.3171/2011.5.SPINE10769. [DOI] [PubMed] [Google Scholar]
- 35.Mehren C, Heider F, Siepe CJ, et al Clinical and radiological outcome at 10 years of follow-up after total cervical disc replacement. Eur Spine J. 2017;26(9):2441–2449. doi: 10.1007/s00586-017-5204-6. [DOI] [PubMed] [Google Scholar]
- 36.Coric D, Kim PK, Clemente JD, et al Prospective randomized study of cervical arthroplasty and anterior cervical discectomy and fusion with long-term follow-up: results in 74 patients from a single site. J Neurosurg Spine. 2013;18(1):36–42. doi: 10.3171/2012.9.SPINE12555. [DOI] [PubMed] [Google Scholar]
- 37.Nabhan A, Ahlhelm F, Shariat K, et al The ProDisc-C prosthesis: clinical and radiological experience 1 year after surgery. Spine (Phila Pa 1976) 2007;32(18):1935–1941. doi: 10.1097/BRS.0b013e31813162d8. [DOI] [PubMed] [Google Scholar]
- 38.Kellgren JH, Lawrence JS Radiological assessment of osteo-arthrosis. Ann Rheum Dis. 1957;16(4):494–502. doi: 10.1136/ard.16.4.494. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 39.Shi R, Li J, Liu H, et al Clinical comparison of 2 implantation systems for single-level cervical disk replacement. Orthopedics. 2014;37(2):e161–168. doi: 10.3928/01477447-20140124-20. [DOI] [PubMed] [Google Scholar]
- 40.Heary RF, Goldstein IM, Getto KM, et al Solid radiographic fusion with a nonconstrained device 5 years after cervical arthroplasty. J Neurosurg Spine. 2014;21(6):951–955. doi: 10.3171/2014.8.SPINE14101. [DOI] [PubMed] [Google Scholar]
- 41.Yi S, Kim KN, Yang MS, et al Difference in occurrence of heterotopic ossification according to prosthesis type in the cervical artificial disc replacement. Spine (Phila Pa 1976) 2010;35(16):1556–1561. doi: 10.1097/BRS.0b013e3181c6526b. [DOI] [PubMed] [Google Scholar]
- 42.Lee JH, Jung TG, Kim HS, et al Analysis of the incidence and clinical effect of the heterotopic ossification in a single-level cervical artificial disc replacement. Spine J. 2010;10(8):676–682. doi: 10.1016/j.spinee.2010.04.017. [DOI] [PubMed] [Google Scholar]
- 43.Leung C, Casey AT, Goffin J, et al Clinical significance of heterotopic ossification in cervical disc replacement: a prospective multicenter clinical trial. Neurosurgery. 2005;57(4):759–763. doi: 10.1227/01.NEU.0000175856.31210.58. [DOI] [PubMed] [Google Scholar]
- 44.Burkus JK, Haid RW, Traynelis VC, et al Long-term clinical and radiographic outcomes of cervical disc replacement with the Prestige disc: results from a prospective randomized controlled clinical trial. J Neurosurg Spine. 2010;13(3):308–318. doi: 10.3171/2010.3.SPINE09513. [DOI] [PubMed] [Google Scholar]
- 45.Phillips FM, Geisler FH, Gilder KM, et al Long-term outcomes of the US FDA IDE prospective, randomized controlled clinical trial comparing PCM cervical disc arthroplasty with anterior cervical discectomy and fusion. Spine (Phila Pa 1976) 2015;40(10):674–683. doi: 10.1097/BRS.0000000000000869. [DOI] [PubMed] [Google Scholar]
- 46.Auerbach JD, Anakwenze OA, Milby AH, et al Segmental contribution toward total cervical range of motion: a comparison of cervical disc arthroplasty and fusion. Spine (Phila Pa 1976) 2011;36(25):E1593–1599. doi: 10.1097/BRS.0b013e31821cfd47. [DOI] [PubMed] [Google Scholar]
- 47.Rajaee SS, Bae HW, Kanim LE, et al Spinal fusion in the United States: analysis of trends from 1998 to 2008. Spine (Phila Pa 1976) 2012;37(1):67–76. doi: 10.1097/BRS.0b013e31820cccfb. [DOI] [PubMed] [Google Scholar]
- 48.Radcliff K, Lerner J, Yang C, et al Seven-year cost-effectiveness of ProDisc-C total disc replacement: results from investigational device exemption and post-approval studies. J Neurosurg Spine. 2016;24(5):760–768. doi: 10.3171/2015.10.SPINE15505. [DOI] [PubMed] [Google Scholar]
- 49.Delamarter RB, Zigler JE, Murrey DB, et al Seven-year reoperation rates: results of a prospective randomized clinical trial: cervical total disc replacement versus fusion. Spine J. 2012;12(9):S96–S96. doi: 10.1097/BRS.0b013e3182797592. [DOI] [PubMed] [Google Scholar]
- 50.Hisey MS, Bae HW, Davis RJ, et al Prospective, randomized comparison of cervical total disk replacement versus anterior cervical fusion: results at 48 months follow-up. J Spinal Disord Tech. 2015;28(4):E237–243. doi: 10.1097/BSD.0000000000000185. [DOI] [PubMed] [Google Scholar]


