Hinweis
Lesen Sie hier ein Update zum Leitthemenbeitrag aus Der Nephrologe 1/2021: Salzberger B et al. (2021) SARS-CoV-2/COVID-19 – Epidemiologie und Prävention; 10.1007/s11560-020-00472-0.
Im Dezember 2019 wurden erste Infektionen mit SARS-CoV‑2 („severe acute respiratory syndrome coronavirus 2“) entdeckt; die Erkrankung wurde als COVID-19 („coronavirus disease 2019“) bezeichnet. Die Epidemiologie wurde bis zum September in dieser Zeitschrift zusammengefasst [9]. Bis Mitte Juli 2021 wurden global mehr als 188 Mio. Infektionen und mehr als 4 Mio. Todesfälle berichtet [11]. Die aktuelle Epidemiologie wird wesentlich durch 2 Entwicklungen beeinflusst: Einerseits findet eine Selektion von Virusvarianten mit erhöhter Infektiosität und einem höheren Komplikationsrisiko statt, andererseits sind wirksame Impfstoffe entwickelt, zugelassen und breit eingeführt worden. Hier stellen wir die aktuellen Neuigkeiten und Entwicklung in der Epidemiologie von SARS-CoV‑2 seit Oktober 2020 dar.
Epidemiologie in Deutschland (10/2020 bis 6/2021)
In Deutschland sind 4 Perioden erkennbar, und zwar eine 1. Welle ab der 10. Woche des Jahres 2020 bis Ende Juni 2020, anschließend eine Periode mit niedriger Inzidenz bis September 2020, ab Oktober 2020 bis Januar 2021 eine 2. Infektionswelle und ab Februar bis 6/2021 eine 3. Welle (Abb. 1). In Deutschland wurden mehr als 3,7 Mio. Infektionen und 91.000 Todesfälle gemeldet. Daten zur Hospitalisierung sind nicht systematisch erhoben; es sind mehr als 110.000 Intensivbehandlungen bisher registriert [6].
Virusvarianten und Basisreproduktionszahl R0
Seit Beginn der Pandemie ist eine Evolution des Virus zu beobachten. Veränderungen im Bereich der rezeptorbindenden Domäne haben zur höheren Infektiosität geführt, andere Mutationen führen zu einem partiellen Immun-Escape. Weltweit findet ein Monitoring dieser Entwicklung statt, die regional variiert. Varianten, die besondere Eigenschaften aufweisen (z. B. höhere Übertragbarkeit, schwerere Verläufe, Immun-Escape), werden von der Weltgesundheitsorganisation (WHO) je nach Grad dieser Eigenschaften klassifiziert in zu beobachtende Varianten („variants of interest“) und besorgniserregende Varianten („variants of concern“).
Mehrere dieser Varianten haben sich konsekutiv in Ausbrüchen als dominante Varianten durchgesetzt, in Europa nach der Nomenklatur der WHO zuletzt die Alpha- und danach die Deltavariante.
Schätzungen für die Basisreproduktionszahl des ursprünglichen Wildtypvirus gehen von einem Wert zwischen 2,8 und 3,8 aus. Die Alphavariante hat gegenüber den vorher zirkulierenden Virusstämmen eine nach der sekundären „attack rate“ etwa um 60 % höhere Infektiosität, die Deltavariante eine noch einmal um rund 60 % höhere. Die Basisreproduktionszahl R0 steigt damit für SARS-CoV‑2 geschätzt auf einen Wert von über 6 bis 9 an. Diese Korrektur hat auch einen Einfluss auf den Bevölkerungsschutz, der durch spezifische Impfraten erreicht werden kann [5].
Altersverteilung der Infektionen
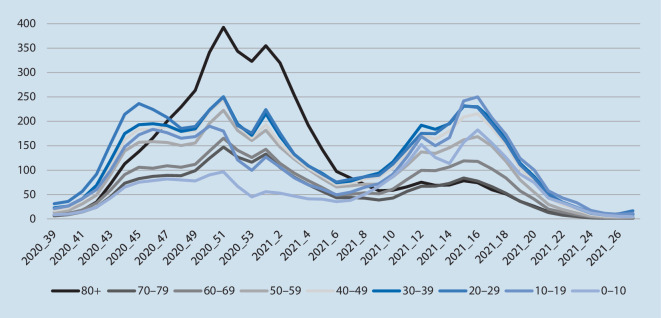
Die Mehrzahl der Fälle trat initial in den Altersgruppen zwischen 20 und 60 Jahren auf; im Gegensatz zu anderen respiratorischen Virusinfektionen waren Infektionen in der Altersgruppe unter 10 Jahren bis Anfang 2021 seltener diagnostiziert worden. Mit Auftreten der Alphavariante zeigte sich eine Verlagerung der Infektionen in jüngere Altersgruppen (Abb. 2), möglicherweise durch die höhere Infektiosität. Dagegen waren die Inzidenzen in der Altersgruppe über 80 Jahre in der 3. Welle in Deutschland deutlich niedriger [6].
Klinischer Schweregrad und Folgen
In allen 4 Perioden zeigt sich eine stark altersabhängige „case fatality rate“ (CFR; Tab. 1). Ob die niedrigere CFR nach der 1. Welle durch Fortschritte in der Therapie oder eine niedrigere Dunkelziffer bedingt ist, ist nicht zu entscheiden. Die Gesamt-CFR für eine Periode ist stark abhängig von der Altersverteilung, insbesondere in der 4. Episode führen eine niedrigere Inzidenz und Todesrate in den hohen Altersgruppen zu einer insgesamt niedrigeren CFR (Abb. 3). In den Altersgruppen 40 bis 49 und 50 bis 59 Jahre zeigt sich die höhere klinische Komplikationsrate der Alphavariante, wie sie auch aus Großbritannien bekannt ist (Abb. 3; Tab. 1; [2]).
| Zeitraum (Monat/Jahr) | ||||
|---|---|---|---|---|
| Altersgruppe (Jahre) | 3/2020–6/2020 (%) | 7/2020–9/2020 (%) | 10/2020–1/2021 (%) | 2/2021–6/2021 (%) |
| 40–49 | 0,23 | 0,06 | 0,08 | 0,13 |
| 50–59 | 0,77 | 0,31 | 0,32 | 0,51 |
| 60–69 | 3,98 | 1,38 | 2,3 | 2,0 |
| 70–79 | 13,5 | 4,8 | 9,3 | 7,5 |
| 80 und älter | 26,4 | 16,3 | 19,9 | 18,8 |
| Gesamt | 3,8 | 0,7 | 3,0 | 1,3 |
Bei der Deltavariante wurde zunächst eine höhere Rate von Hospitalisierungen gemeldet. Allerdings zeigt sich beim derzeitigen Ausbruch in Großbritannien aufgrund der fortgeschrittenen Impfung der erwachsenen Bevölkerung nur eine geringe Zahl von Todesfällen, die einen Vergleich schwierig macht.
Entwicklung und Einführung wirksamer Impfstoffe
Bereits im Januar 2020 wurde die Herstellung von Impfstoffen geplant, erste Phase-III-Studien begannen im Juli 2020. Bis Ende des Jahres 2020 wurden in Europa und den USA 3 Impfstoffe aufgrund der Daten zur Wirksamkeit und Sicherheit zugelassen und breit eingeführt [4, 10]. Großbritannien und Israel haben aufgrund günstiger Lieferverträge besonders rasch ihre Bevölkerung geimpft und damit auch die Daten zur Wirksamkeit in großen Bevölkerungsteilen bestätigt. In Israel zeigte sich in großen populationsweiten Studien eine Wirksamkeit einer Zweifachimpfung mit einem mRNA-Impfstoff von über 90 % für die Endpunkte Infektion, asymptomatische Infektion, Hospitalisierung und Tod durch COVID-19 [7].
Spätere Phase-III-Studien mit anderen Impfstoffen wurden auch in Regionen mit Verbreitung der Beta- und Gammavarianten durchgeführt und zeigten eine etwas niedrigere Wirksamkeit für Infektionen; die Wirksamkeit der Impfstoffe in der Vermeidung von Hospitalisierung war in allen diesen Studien deutlich höher [3, 8].
Bei den in Europa zirkulierenden Varianten zeigte die Alphavariante keine Änderung der Impfwirksamkeit; dies ist bei der seit Mai 2021 in Großbritannien zirkulierenden Deltavariante anders. Die Impfwirksamkeit nach der ersten Dosis beträgt nur noch 34 %, nach der zweiten Dosis 88 % [1]. Auch in einer großen Kohorte von Mitarbeitern im Gesundheitswesen zeigt sich eine zunehmende Zahl von Durchbruchsinfektionen als Hinweis auf eine geringere Impfwirksamkeit.
Kann ein Bevölkerungsschutz oder gar eine Viruseradikation erreicht werden?
Neben dem Schutz vor einer Infektion oder einer komplizierten Infektion ist eine mögliche populationsweite Wirkung einer Impfung auch die der Verhinderung der Ausbreitung bei einer entsprechend hohen Immunitätsrate in der Bevölkerung. Dieser Bevölkerungsschutz wird auch als Herdenimmunität bezeichnet. Eine Schätzung für die benötigte Impfrate ergibt sich aus der Formel Immunitätsrate = 1 − 1/R0. Für die initiale Schätzung von R0 mit 2,8–3,8 ergäbe dies eine Impfrate von 67–75 %, mit einer Basisreproduktionszahl von 6 bis 9 müsste die Immunitätsrate in einer Bevölkerung bei über 85–90 % liegen. Bei sehr hoher Wirksamkeit einer (>95 %) könnte man diesen Wert auch für die Impfrate nehmen. Mit den neuen Virusvarianten wird dies nicht mehr erreicht; hier ergibt sich eine Wirksamkeit von 2 Impfdosen von 88 %. Rein rechnerisch müsste damit die Impfquote noch einmal um etwa 10 % auf über 95–99 % erhöht werden. Eine solche Impfrate ist allerdings als unrealistisch anzusehen.
Kann die Impfung aber v. a. die Risikopatienten vor einer schweren Erkrankung schützen? Eine solche Situation zeichnet sich beim derzeitigen Ausbruch mit der Deltavariante in Großbritannien ab: Hier sind die Zahlen der Hospitalisierungen und Todesfälle in einer weitgehend geimpften Bevölkerung (67 % der erwachsenen Bevölkerung 2‑mal geimpft) sehr viel niedriger als bei den früheren Ausbrüchen, die CFR liegt bei insgesamt 0,2 % [5].
Eine Eradikation des Virus erscheint derzeit nicht wahrscheinlich: Die Rate asymptomatischer Infektionen ist hoch, und ein tierisches Reservoir ist noch nicht sicher identifiziert – beides sind Eigenschaften, die nach allem Wissen gegen die Möglichkeit einer Eradikation sprechen.
Einhaltung ethischer Richtlinien
Interessenkonflikt
B. Salzberger, F. Buder, B. Lampl, B. Ehrenstein, F. Hitzenbichler, S. Bauernfeind, T. Holzmann, B. Schmidt und F. Hanses geben an, dass kein Interessenkonflikt besteht.
Für diesen Beitrag wurden von den Autoren keine Studien an Menschen oder Tieren durchgeführt. Für die aufgeführten Studien gelten die jeweils dort angegebenen ethischen Richtlinien.
Footnotes

QR-Code scannen & Beitrag online lesen
Literatur
- 1.Bernal JL, Andrews N, Gower C, et al. Effectiveness of COVID-19 vaccines against the B.1.617.2 variant. medRxiv. 2021 doi: 10.1101/2021.05.22.21257658. [DOI] [PubMed] [Google Scholar]
- 2.Challen R, Brooks-Pollock E, Read JM, et al. Risk of mortality in patients infected with SARS-CoV-2 variant of concern 202012/1: matched cohort study. BMJ. 2021;372:n579. doi: 10.1136/bmj.n579. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 3.Heath PT, Galiza EP, Baxter DN, et al. Safety and efficacy of NVX-CoV2373 Covid-19 vaccine. N Engl J Med. 2021 doi: 10.1056/NEJMoa2107659. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 4.Polack FP, Thomas SJ, Kitchin N, et al. Safety and efficacy of the BNT162b2 mRNA Covid-19 vaccine. N Engl J Med. 2020 doi: 10.1056/NEJMoa2034577. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 5.Public Health England . SARS-CoV-2 variants of concern and variants under investigation in England. 2021. [Google Scholar]
- 6.RKI . Täglicher Lagebericht des RKI zur Coronavirus-Krankheit-2019 (COVID-19) 13.07.2021 – Aktualisierter Stand für Deutschland. Berlin: Robert-Koch-Institut; 2021. [Google Scholar]
- 7.Rossman H, Shilo S, Meir T, et al. COVID-19 dynamics after a national immunization program in Israel. Nat Med. 2021 doi: 10.1038/s41591-021-01337-2. [DOI] [PubMed] [Google Scholar]
- 8.Sadoff J, Gray G, Vandebosch A, et al. Safety and efficacy of single-dose Ad26.COV2.S vaccine against Covid-19. N Engl J Med. 2021 doi: 10.1056/NEJMoa2101544. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 9.Salzberger B, Buder F, Lampl B, et al. SARS-CoV-2/COVID-19-epidemiology and prevention. Nephrologe. 2020 doi: 10.1007/s11560-020-00472-0:1-7. [DOI] [Google Scholar]
- 10.Voysey M, Clemens SAC, Madhi SA, et al. Safety and efficacy of the ChAdOx1 nCoV-19 vaccine (AZD1222) against SARS-CoV-2: an interim analysis of four randomised controlled trials in Brazil, South Africa, and the UK. Lancet. 2020 doi: 10.1016/s0140-6736(20)32661-1. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 11.WHO (2021) WHO Coronavirus (COVID-19) dashboard. https://covid19.who.int. Zugegriffen: 18. Juli 2021