Abstract
La campagne vaccinale contre la Covid-19 a été marquée par une grande appréhension vis-à-vis du risque allergique, en particulier vis-à-vis des excipients vaccinaux : polyéthylène glycol (PEG), polysorbate ou encore trométamol. Une allergie confirmée à ces derniers ou après la première dose de vaccin constitue une contre-indication vaccinale. Nous rapportons le cas d’un patient présentant une allergie avérée au PEG et une sensibilisation cutanée au vaccin COMIRNATY® (PEG dans sa composition). Il a pu bénéficier de ce vaccin dans le cadre d’un protocole d’induction de tolérance en 5 étapes. Conclusions : une prise en charge allergologique spécifique doit être proposée aux patients suspects d’hypersensibilité sévère au PEG ou à d’autres excipients vaccinaux. Nous proposons ici un protocole ayant permis, sur un cas d’allergie avérée au PEG, d’administrer le vaccin COMIRNATY® sans réaction secondaire.
Mots clés: Allergie, Anaphylaxie, Hypersensibilité, Polyethylene glycol (PEG), Vaccin Covid, Induction de tolérance, tests cutanés, Vaccin ARN
Abstract
Vaccination is the most efficient way to fight the Covid epidemic. However, suspicion of severe hypersensitivity to PEG (PolyEthylen Glycol) usually constitutes a vaccine contraindication. We report the case of a patient with a proven allergy to PEG and skin sensitization to the COMIRNATY vaccine (PEG in its composition). He was able to benefit from the vaccine under the 5-step desensitization protocol. Conclusions: Specific allergological management should be offered to patients suspected of severe hypersensitivity to PEG and other vaccine excipients. We propose a solution for Comirnaty administration for patients with a proven severe allergy to PEG.
Keywords: Allergy, Anaphylaxis, Hypersensitivity, Covid-19 vaccines, Desensitization, Polyethylene glycol (PEG), Skin test, mRNA vaccine
1. Introduction
La vaccination contre la covid-19 représente le meilleur outil de prévention et de lutte contre la pandémie.
Cependant, la mise en place de la campagne vaccinale a été marquée par une grande appréhension vis-à-vis du risque allergique. Ce dernier se vérifie parfois, bien que très rarement puisqu’il représente, selon le dernier rapport des Centers for Disease Control and Prevention (CDC) américains, respectivement 5,0 et 2,8 cas d’anaphylaxie pour un million de doses pour les vaccins de Pfizer-BioNTechet Moderna [1].
En France, le point de situation sur la surveillance des vaccins contre la COVID-19 publié le 16 avril 2021 sur le site de l’ANSM [2] fait état de 58 réactions d’hypersensibilité ou d’anaphylaxie de grade II et III avec le vaccin à ARN COMIRNATY® (Pfizer/BioNTech) à la date du 08/04/21 après plus de 10 millions de doses injectées, soit une fréquence de 0,56 pour 100 000 injections.
Lors de la dernière actualisation au 29/07/2021 [3] (rapport ANSM du 06/08/2021), plus de 4 603 000injections ont été réalisées, dont :
-
•
plus de 57 232 000 injections avec COMIRNATY ®(Pfizer/BioNTech) ;
-
•
plus de 6 996 000 injections avec le vaccin à ARN COVID-19 VACCINE (Moderna).
La Haute Autorité de santé (HAS), dans une mise à jour du 18 février 2021, stipule que « La vaccination est contre-indiquée uniquement en cas d’antécédents d’allergie immédiate à un des composants du vaccin. » [4].
En cas d’allergie avérée à des vaccins issus de technologies « classiques », des protocoles d’induction de tolérance ont été décrits dans la littérature, avec une sécurité et une efficacité démontrées [5].
Concernant le vaccin contre la Covid-19, peu de rapports ont été publiés jusqu’à présent chez nos patients allergiques, avec seulement deux premiers cas rapportés d’induction de tolérance chez deux patients ayant présenté une réaction à la première dose du vaccin Moderna [6].
À notre connaissance, il s’agit du premier cas communiqué de désensibilisation à un vaccin à ARN contre la covid-19 en France.
Cas clinique
Il s’agit d’un homme de 38 ans, infirmier, connu pour des réactions d’hypersensibilité attribuées au polyéthylène glycol (PEG), jamais explorées jusqu’à présent.
-
•
la réaction initiale remonte à 2002, au décours immédiat d’une préparation colique, avec la survenue d’une hypersensibilité immédiate de grade III (urticaire généralisée, dyspnée et malaise) ;
-
•
les années suivantes ont été marquées par des réactions à des formes orales de SPIFEN®400mgcomprimé (ibuprofène, pelliculage avec macrogol 4000) et DULCOLAX®comprimé (bisacodyl, enrobage avec macrogol 6000) ;
-
•
certains cosmétiques (shampoings, crèmes) ont également entraîné des érythèmes de contact avec constatation a posteriori par le patient de la présence de PEG.
Au fil des années, le patient a fait de lui-même le lien entre les réactions présentées et la présence PEG, avec une éviction minutieuse depuis 2013.
Cependant, le trométamol semble bien supporté, avec la notion d’un angioscanner bien toléré.
Nos explorations allergologiques, réalisées mi-avril 2021, ont confirmé le caractère allergique au PEG avec une sensibilisation croisée avec le polysorbate 80 (Fig. 1 ).
Fig. 1.
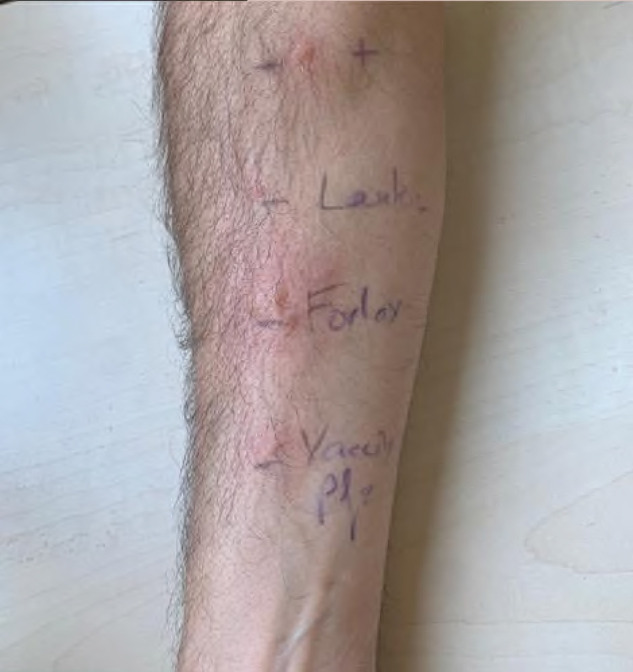
Tests cutanés ; Prick Histamine 6/20 mm ; Lantus® négatif ; Forlax® 13/40 mm ; vaccin COMIRNATY®5/20 mm.
Les prick tests au Macrogol (PEG) 4000(FORLAX®) à 4 g/50 mL d’eau ppi et à la Picloxydine (VITABACT®) 0,05 % collyre (polysorbate 80 comme excipient) en concentration pure sont revenus positifs, respectivement à 13/40 mm et 5/20 mm (versus un témoin, l’histamine, à 6/20 mm) (Fig. 1).
Le prick test à l’insuline glargine (LANTUS®) à 100UI/mL (polysorbate 20 comme excipient) pur était négatif.
Le vaccin COMIRNATY® (Pfizer/BioNTech) a également pu être testé (grâce à un fond de flacon récupéré viale centre de vaccination adjacent) : le prick test COMIRNATY® était également positif à 5/20 mm (concentration de la solution reconstituée : 0,1 mg/mL).
Nos explorations ont donc confirmé une hypersensibilité allergique sévère au PEG, avec une sensibilisation croisée au polysorbate 80.
Le patient n’étant pas éligible et refusant catégoriquement une vaccination par les vaccins à vecteurs viraux VAXZEVRIA® d’AstraZeneca ou le COVID-19 VACCINE Janssen® (Johnson&Johnson) par appréhension d’un risque thomboembolique chez le sujet jeune, ce dossier a été discuté en réunion de concertation pluridisciplinaire avec l’équipe d’infectiologie. Il a été acté l’administration du vaccin COMIRNATY® (Pfizer/BioNTech) selon un protocole d’induction de tolérance, avec un consentement éclairé validé par le patient.
Nous avons adapté, pour le vaccin COMIRNATY®, le protocole d’induction de tolérance en 5 doses proposé par l’équipe de Mustafa pour le vaccin Moderna (Tableau 1 ).
Tableau 1.
Protocole d’induction de tolérance en 5 étapes – Vaccin COMIRNATY®a.
| Palier | Dose et concentration | % dose habituelle (0,3 mL) |
|---|---|---|
| 1 | 0,05 mL de dilution à 1/100 du vaccinb | 0,17 % |
| 2 | 0,05 mL de dilution à 1/10 du vaccinb | 1,67 % |
| 3 | 0,05 mL du vaccin pur | 16,67 % |
| 4 | 0,10 mL du vaccin pur | 33,33 % |
| 5 | 0,15 mL du vaccin pur | 50 % |
| Total = 101,84 % |
Injection en intramusculaire/15 min.
Dans eau stérile pour préparation injectable (ppi).
Le protocole a été réalisé en milieu sécurisé (hôpital de jour) et sous prémédication par 5 mg de desloratadine et 40 mg de prednisolone, la veille et le matin même des injections.
Le protocole s’est déroulé sans incident significatif, hormis la présence d’un érythème et d’un prurit minime aux sites d’injection.
Un dosage des anticorps anti-spike a été réalisé à 30 jours de la première injection et a mis en évidence une séroconversion effective (sérologie initiale négative).
2. Discussion
Notre cas clinique présente deux principaux points d’intérêt.
Tout d’abord, ce cas confirme une orientation possible de la vaccination avec des tests cutanés simples au vaccin. Ces explorations possèdent en effet une bonne sensibilité et spécificité [7] et le rapprochement entre allergologues et centres de vaccination facilite la mise à disposition de fonds de flacons pour la réalisation de ces tests.
A posteriori, des tests cutanés au FORLAX®, VITABACT®, LANTUS® et COMIRNATY® ont été réalisés sur 5 volontaires sains afin de s’assurer de leurs spécificité. Ces prick tests étaient négatifs. Les concentrations utilisées lors des prick tests au FORLAX® (4 g/50 mL), VITABACT® (pur) et LANTUS® (100UI/mL) sont conformes aux recommandations françaises de février 2021 [8]. La concentration de 0,1 mg/mL utilisée pour le prick test au vaccin COMIRNATY® est celle utilisée pour la vaccination des patients, avec une stabilité de 6 h à température ambiante après reconstitution des flacons [9].
Bien que l’allergie avérée au PEG soit extrêmement rare, elle peut être sévère [10], [11]. À l’heure actuelle, des protocoles de désensibilisation au PEG existent, notamment dans pour permettre l’administration de thérapies pégylées dans certaines hémopathies malignes [12]. En cas d’allergie confirmée à un vaccin issu de technologies « classiques », le protocole d’administration de vaccins en doses progressives en 5 étapes publié en 2012 par Kelso et al. [5] semble avoir prouvé son efficacité et sa sécurité. Cependant, ce dernier ne prend pas en compte les hypersensibilités aux nouvelles générations de vaccins, notamment ceux contenant du PEG et du polysorbate.
Ainsi, notre protocole d’induction de tolérance au vaccin COMIRNATY®, est une version inspirée à la fois du protocole de Kelso et al. pour les vaccins classiques [5], de celui de Mustapha pour le vaccin Moderna [6] et de celui d’Erdeljic Turk et al. pour les vaccins à ARN [11], adapté pour une dose vaccinale de 0,3 mL. Le Tableau 2 permet une comparaison de notre protocole à ceux de Kelso et al. et Erdeljic Turk et al.
Tableau 2.
Tableau comparatif des protocoles d’induction de tolérance en 5 étapes.
| Protocole pour l’administration du vaccin COMIRNATY® | Protocole pour l’administration du vaccin Moderna selon Mustafa et al. 2021 [6], inspiré de Kelso et al. 2012 [5] | Protocole pour l’administration du vaccin COMIRNATY® selon Erdeljic et al. 2021 (15) | |
| Profil des patients | 1 patient naïf de vaccin Covid Hypersensibilité immédiate de grade 3 au PEG |
2 patients Hypersensibilité de grade 1 à la 1re dose de MODERNA |
|
| Tests allergologiques | Pricks positifs pour PEG, polysorbate 80 et vaccin | Pricks négatifs (PEG, polysorbate et vaccin) IDR vaccin positive (concentration inconnue) |
|
| Prémédication | Oui | Non | NR |
| Paliera | Dose et concentration | % dose habituelle (0,3 mL) | Dose et concentration | % dose habituelle (0,5 mL) | Dose et concentration | % dose habituelle (0,3 mL) |
|---|---|---|---|---|---|---|
| 1 | 0,05 mL de dilution à 1/100 du vaccinb | 0,17 % | 0,05 mL de dilution à 1/10 du vaccinb | 1 % | 0,03 mL de dilution à 1/10 du vaccin | 1 % |
| 2 | 0,05 mL de dilution à 1/10 du vaccinb | 1,67 % | 0,05 mL vaccin pur | 10 % | 0,03 mL vaccin pur | 10 % |
| 3 | 0,05 mL vaccin pur | 16,67 % | 0,1 mL vaccin pur | 20 % | 0,06 mL vaccin pur | 20 % |
| 4 | 0,10 mL vaccin pur | 33,33 % | 0,15 mL vaccin pur | 30 % | 0,09 mL vaccin pur | 30 % |
| 5 | 0,15 mL vaccin pur | 50 % | 0,2 mL vaccin pur | 40 % | 0,12 mL vaccin pur | 40 % |
| Total = 101,84 % | Total = 101 % | Total = 101 % |
Injection en intramusculaire/15 min.
Dans eau stérile pour préparation injectable (ppi).
Nous avons en particulier ajouté un palier de dilution préalable (1/100) devant la sévérité potentielle de l’allergie au PEG (anaphylaxie grade 3 présentée par notre patient). Cependant, nous ne pouvons pas confirmer avec certitude la stabilité de la solution à cette dilution puisque nous sommes en dessous des concentrations utilisées dans les essais cliniques de phase 1/2 du vaccin COMIRNATY® (concentrations comprises entre 0,006 à 0,2 mg/mL) [13].
Nous avons également eu recours à une prémédication par antihistaminique et corticoïdes, par homologie aux protocoles d’induction de tolérance aux venins en UltraRush réalisés dans notre service, bien que seuls les antihistaminiques aient l’indication effective dans les protocoles d’induction de tolérance [11].
En termes d’efficacité vaccinale, le fractionnement des doses a démontré, comme dans l’étude de Mustafa et al. pour le vaccin Moderna [6], une élévation des IgG anti-spike chez notre patient. À l’instar des administrations monodoses de vaccin, cette séroconversion présage d’une efficacité vaccinale, néanmoins sans certitude démontrable en l’état actuel des connaissances.
Concernant la stratégie vaccinale devant ces cas d’allergie au PEG avec sensibilisation croisée effective au polysorbate [14], [15], les 4 vaccins actuellement disponibles en France sont théoriquement contre indiqués : COMIRNATY® (PEG), COVID-19 VACCINE® de Moderna(PEG et trométamol), VAXZERIA® (Polysorbate 80) et COVID-19 VACCINE Janssen® (Polysorbate 80).
Une solution pragmatique aurait été d’attendre la commercialisation d’un prochain vaccin ne contenant ni PEG ni polysorbate [16], mais ces derniers risquent de ne pas être disponibles en France avant plusieurs mois (aucun vaccin répondant à ces critères n’est actuellement en phase 3).
Dans le cas de notre patient, le motif impérieux du fait de sa profession d’infirmier et l’absence d’alternative thérapeutique justifient le recours à un protocole d’induction de tolérance.
La seconde dose sera administrée selon le même schéma fractionné.
Ces protocoles d’induction de tolérance ont toute leur place dans la stratégie de lutte contre la covid-19 dans ces cas d’absence d’alternative thérapeutique et de bénéfice avéré [17]. À ce jour, différentes versions de ces protocoles existent ; de futures cohortes pourront permettre de les standardiser.
En conclusion
Une prise en charge allergologique spécifique doit être proposée aux patients suspects d’hypersensibilité sévère au PEG ou à d’autres excipients vaccinaux, sans contre-indiquer définitivement la vaccination.
Nous proposons ici un protocole ayant permis, sur un cas d’allergie avérée au PEG, l’administration du vaccin COMIRNATY®, avec une bonne tolérance.
Cette solution nécessite cependant une évaluation individualisée de la balance bénéfices/risques. Des études avec des cohortes plus importantes sont à poursuivre pour le suivi et l’amélioration de la prise en charge de ces rares patients.
Déclaration de liens d’intérêts
Les auteurs déclarent ne pas avoir de liens d’intérêts.
Références
- 1.Shimabukuro T., Covid C. 2021. COVID-19 vaccine safety update [Internet] https://www.cdc.gov/vaccines/acip/meetings/downloads/slides-2021-01/06-COVID-Shimabukuro.pdf [cité 01 juillet 2021] [Google Scholar]
- 2.2021. Actualité - Point de situation sur la surveillance des vaccins contre la COVID-19 - Période du 16/04/2021 au 22/04/2021 - ANSM [Internet] https://ansm.sante.fr/actualites/point-de-situation-sur-la-surveillance-des-vaccins-contre-la-covid-19-periode-du-16-04-2021-au-22-04-2021 [cité 29 juin 2021] [Google Scholar]
- 3.Actualité - Point de situation sur la surveillance des vaccins contre la COVID-19 - Période du 23/07/2021 au 29/07/2021 - ANSM [Internet] 2021 https://ansm.sante.fr/actualites/point-de-situation-sur-la-surveillance-des-vaccins-contre-la-covid-19-periode-du-23-07-2021-au-29-07-2021 [cité le 23 aout 2021]
- 4.Karine P. 2021. Stratégie de vaccination contre le SARS-CoV-2 – Extension des compétences vaccinales des professionnels de santé [Internet] p. 20. https://www.has-sante.fr/jcms/p_3240087/fr/strategie-de-vaccination-contre-le-sars-cov-2-extension-des-competences-vaccinales-des-professionnels-de-sante. [Google Scholar]
- 5.Kelso J.M., Greenhawt M.J., Li J.T., Nicklas R.A., Bernstein D.I., Blessing-Moore J., et al. Adverse reactions to vaccines practice parameter 2012 update. J Allergy Clin Immunol. 2012;130:25–43. doi: 10.1016/j.jaci.2012.04.003. [DOI] [PubMed] [Google Scholar]
- 6.Mustafa S.S., Ramsey A., Staicu M.L. Administration of a Second Dose of the Moderna COVID-19 Vaccine After an Immediate Hypersensitivity Reaction With the First Dose: Two Case Reports. Ann Intern Med. 2021;L21–0104 doi: 10.7326/L21-0104. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 7.Banerji A., Wickner P.G., Saff R., Stone C.A., Robinson L.B., Long A.A., et al. mRNA Vaccines to Prevent COVID-19 Disease and Reported Allergic Reactions: Current Evidence and Suggested Approach. J Allergy Clin Immunol Pract. 2021;9:1423–1437. doi: 10.1016/j.jaip.2020.12.047. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 8.Carole P. 2021. Vaccination contre la Covid-19 et antécédents allergiques : résumé des recommandations françaises (CNP allergologie/FFAL/SFA/TRAM) pour les allergologues [Internet] https://sfa.lesallergies.fr/vaccination-contre-la-covid-19/ [cité 26 juin 2021] [Google Scholar]
- 9.ANSM; 2021. Vaccin - Comirnaty (Pfizer & BioNTech) - ANSM [Internet] https://ansm.sante.fr/tableau-vaccin/comirnaty-pfizer-biontech [cité 1 juill 2021] [Google Scholar]
- 10.Wenande E., Garvey L.H. Immediate-type hypersensitivity to polyethylene glycols: a review. Clin Exp Allergy. 2016;46:907–922. doi: 10.1111/cea.12760. [DOI] [PubMed] [Google Scholar]
- 11.Bruusgaard-Mouritsen M.A., Johansen J.D., Garvey L.H. Clinical manifestations and impact on daily life of allergy to polyethylene glycol (PEG) in ten patients. Clin Exp Allergy. 2021;51:463–470. doi: 10.1111/cea.13822. [DOI] [PubMed] [Google Scholar]
- 12.Concha S., Barriga F., Ovalle P., Hoyos-Bachiloglu R. A 12-steps desensitization protocol for pediatric patients with hypersensitivity to pegylated asparaginase. Ann Allergy Asthma Immunol. 2020;124:208–210. doi: 10.1016/j.anai.2019.11.001. [DOI] [PubMed] [Google Scholar]
- 13.Walsh E.E., Frenck R.W., Falsey A.R., Kitchin N., Absalon J., Gurtman A., et al. Safety and Immunogenicity of Two RNA-Based Covid-19 Vaccine Candidates. N Engl J Med. 2020;383:2439–2450. doi: 10.1056/NEJMoa2027906. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 14.Sokolowska M., Eiwegger T., Ollert M., Torres M.J., Barber D., Giacco S.D., et al. EAACI statement on the diagnosis, management and prevention of severe allergic reactions to COVID-19 vaccines. Allergy. 2021;76:1629–1639. doi: 10.1111/all.14739. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 15.Stone C.A., Liu Y., Relling M.V., Krantz M.S., Pratt A.L., Abreo A., et al. Immediate hypersensitivity to polyethylene glycols and polysorbates: more common than we have recognized. J Allergy Clin Immunol Pract. 2019;7:1533–1540. doi: 10.1016/j.jaip.2018.12.003. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 16.Erdeljic Turk V. Anaphylaxis associated with the mRNA COVID-19 vaccines: approach to allergy investigation. Clin Immunol. 2021;227:108748. doi: 10.1016/j.clim.2021.108748. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 17.Castells M.C. A new era for drug desensitizations. J Allergy Clin Immunol Pract. 2015;3:639–640. doi: 10.1016/j.jaip.2015.05.006. [DOI] [PubMed] [Google Scholar]


