Abstract
目的
探讨利用 3D 打印技术制备、经多巴胺表面修饰及负载软骨源性形态发生蛋白 1(cartilage derived morphogenetic protein 1,CDMP1)的聚己内酯(polycaprolactone,PCL)-羟基磷灰石(hydroxyapatite,HA)三维多孔支架,体外诱导人 BMSCs(human BMSCs,hBMSCs)成软骨分化的可行性。
方法
采用 3D 打印技术制备 PCL-HA 支架,经多巴胺表面修饰后,将 CDMP-1 负载于支架上,扫描电镜观察支架表面微结构,并检测孔隙率和水静态接触角。体外成软骨分化实验:分为 A 、B、C 3 组,A 组为 PCL-HA 支架,B 组为多巴胺表面修饰的 PCL-HA 支架,C 组为多巴胺表面修饰及负载 CDMP-1 的 PCL-HA 支架;将 hBMSCs 植入 3 组支架,成软骨诱导培养后比较细胞黏附率、细胞增殖(MTT 法)和细胞活性(Live/Dead 染色法),并采用实时荧光定量 PCR 检测Ⅱ型胶原和聚集蛋白聚糖(Aggrecan)的基因表达。
结果
3 组支架均呈三维多孔圆柱体状,孔洞相互联通,孔径为 400~500 μm,孔隙率为 56%,材料纤维走向为 0°/90°。经多巴胺表面修饰后,支架颜色由初始的白色变为棕色;水静态接触角也由 76° 降为 0°。体外培养 24 h,A、B、C 组细胞黏附率分别为 34.3%±3.5%、48.3%±1.5%、57.4%±2.5%,比较差异均有统计学意义(P<0.05)。Live/Dead 染色显示 3 组细胞均有较好的细胞活性。MTT 检测显示各组 hBMSCs 均生长良好,吸光度(A)值随培养时间延长而增大;培养 4、7、14、21 d 时,C 组 A 值显著高于 A、B 组,B 组高于 A 组,差异均有统计学意义(P<0.05)。随培养时间延长,3 组Ⅱ型胶原 mRNA 和 Aggrecan mRNA 表达均持续增加;培养 7、14、21 d Ⅱ型胶原 mRNA 相对表达量及培养 14、21 d Aggrecan mRNA 相对表达量,C 组均显著高于 A、B 组,B 组高于 A 组,比较差异有统计学意义(P<0.05)。
结论
采用3D 打印技术制备、经多巴胺表面修饰及负载 CDMP-1 的 PCL-HA 三维多孔支架,体外与 hBMSCs 共培养,可促进细胞黏附、增殖及成软骨分化。
Keywords: 3D打印技术, 多巴胺, 聚己内酯, 羟基磷灰石, 复合支架, 软骨源性形态发生蛋白 1, BMSCs, 软骨组织工程
Abstract
Objective
To prepare dopamine modified and cartilage derived morphogenetic protein 1 (CDMP1) laden polycaprolactone-hydroxyapatite (PCL-HA) composite scaffolds by three-dimensional (3D) printing and evaluate the effect of 3D scaffolds on in vitro chondrogenic differentiation of human bone marrow mesenchymal stem cells (hBMSCs).
Methods
A dimensional porous PCL-HA scaffold was fabricated by 3D printing. Dopamine was used to modify the surface of PCL-HA and then CDMP-1 was loaded into scaffolds. The surface microstructure was observed by scanning electron microscope (SEM) and porosity and water static contact angle were also detected. The cytological experiment in vitro were randomly divided into 3 groups: group A (PCL-HA scaffolds), group B (dopamine modified PCL-HA scaffolds), and group C (dopamine modified and CDMP-1 laden PCL-HA scaffolds). The hBMSCs were seeded into three scaffolds, in chondrogenic culture conditions, the cell adhesive rate, the cell proliferation (MTT assay), and cell activity (Live-Dead staining) were analyzed; and the gene expressions of collagen type Ⅱ and Aggrecan were detected by real-time fluorescent quantitative PCR.
Results
The scaffolds in 3 groups were all showed a cross-linked and pore interconnected with pore size of 400–500 μm, porosity of 56%, and fiber orientation of 0°/90°. For dopamine modification, the scaffolds in groups B and C were dark brown while in group A was white. Similarly, water static contact angle was from 76° of group A to 0° of groups B and C. After cultured for 24 hours, the cell adhesion rate of groups A, B, and C was 34.3%±3.5%, 48.3%±1.5%, and 57.4%±2.5% respectively, showing significant differences between groups (P<0.05). Live/Dead staining showed good cell activity of cells in 3 groups. MTT test showed that hBMSCs proliferated well in 3 groups and the absorbance (A) value was increased with time. The A value in group C was significantly higher than that in groups B and A, and in group B than in group A after cultured for 4, 7, 14, and 21 days, all showing significant differences (P<0.05). The mRNA relative expression of collagen type Ⅱ and Aggrecan increased gradually with time in 3 groups. The mRNA relative expression of collagen type Ⅱafter cultured for 7, 14, and 21 days, and the mRNA relative expression of Aggrecan after cultured for 14 and 21 days in group C were significantly higher than those in groups A and B, and in group B than in group A, all showing significant differences (P<0.05).
Conclusion
Co-culture of dopamine modified and CDMP1 laden PCL-HA scaffolds and hBMSCs in vitro can promote hBMSCs’ adhesion, proliferation, and chondrogenic differentiation.
Keywords: Three-dimensional printing technology, dopamine, polycaprolactone, hydroxyapatite, composite scaffold, cartilage derived morphogenetic protein 1, bone marrow mesenchymal stem cells, cartilage tissue engineering
各种创伤和病理因素导致的关节软骨损伤在骨科临床极其常见。由于关节软骨自我修复能力较差,在缺乏适当保护的情况下可加速其退行性变,最终导致严重的骨关节炎,给患者和社会造成极大经济负担和损失[1]。目前对有症状的骨软骨损伤,临床上有保守治疗、关节镜修复术、关节表面置换术及关节融合术等多种治疗方案[2]。对早期有症状的软骨损伤修复仍是骨科医生面临的挑战。近年来,随着 3D 打印技术的快速发展,为个性化软骨缺损修复提供了新方法。3D 打印技术采用分层加工、叠加成形的方法,可构建具有复杂三维结构的医用高分子支架材料,且其外形及内部结构可控、机械强度高,是修复骨软骨损伤的理想支架材料[3]。本研究利用经多巴胺表面修饰并负载软骨源性形态发生蛋白 1(cartilage derived morphogenetic protein 1,CDMP-1)的 3D 打印聚己内酯(polycaprolactone,PCL)-羟基磷灰石(hydroxyapatite,HA)三维多孔支架,接种人 BMSCs(human BMSCs,hBMSCs)并在体外培养观察,探讨其向软骨细胞分化的可行性,为最终构建简便高效、具备个性化 3D 形态的无细胞软骨修复材料提供理论依据。
1. 材料与方法
1.1. 主要试剂、仪器
HA、PCL、盐酸多巴胺(Sigma 公司,美国);L-DMEM 培养基、胰蛋白酶、FBS(GIBCO 公司,美国);hBMSCs(南京森贝伽生物科技有限公司);Live/Dead 试剂盒(Molecular Probes 公司,美国);DNA 提取试剂盒(Qiagen 公司,德国)。3K15 离心机(Sigma 公司,美国);CO2 培养箱、–80℃ 深低温冰箱(SANYO 公司,日本);S4800 扫描电镜(Hitachi 公司,日本);DM16000B 倒置荧光显微镜(Leica 公司,德国);酶联免疫检测仪(Bio-Rad 公司,美国);UV-2450 紫外分光光度计(Shimadzu 公司,日本);实时荧光定量 PCR 仪(Applied Biosystems 公司,美国);激光共聚焦显微镜(Zeiss 公司,德国);3D FDM3000 系统(Stratasys 公司,美国);SL200B 接触角测试仪(Kino 公司,美国);Micro-CT(Siemens 公司,德国)。Geomagic Studio 11.0 软件(3D systems 公司,美国)。
1.2. 支架材料的制备及相关观测
1.2.1. 3D 打印技术制备 PCL-HA 三维多孔支架材料
参照 Yao 等[4]方法,基于熔融沉积造型技术制备 3D 打印 PCL-HA 圆柱体状三维多孔支架材料。先利用 Geomagic Studio 11.0 软件进行 PCL-HA 三维多孔支架的计算机辅助设计,然后转换成 STL 格式并输入 3D 生物打印机,采用生物挤压方法进行打印。3D 生物打印机采用直径 200 μm 喷头,行走速度 3 mm/min,层厚 200 μm,由打印机按预设参数熔融材料后在 x、y、z 轴 3 个方向分别喷涂成型完成支架打印。将初步制备的支架材料行支撑材料修整及边角修饰。
1.2.2. 多巴胺修饰及 CDMP-1 加载
参照 Poh 等[5]方法,用多巴胺对 3D 打印制备的 PCL-HA 三维多孔支架进行表面修饰。以 10 mmol/L Tris-HCl 缓冲液为溶剂配制 2 mg/mL 多巴胺溶液;将 PCL-HA 三维多孔支架浸入多巴胺溶液中,室温避光磁力搅拌(1 000 r/min)24 h 后,蒸馏水反复冲洗去除未聚合的多巴胺,于 60℃ 烘干过夜。然后将上述经多巴胺修饰的 PCL-HA 三维多孔支架置于 100 ng/mL CDMP-1 溶液中,低速(400 r/min)搅拌 24 h,于 37℃ 真空干燥箱充分干燥后常温保存。
1.2.3. 实验分组及支架性能观测
取 PCL-HA 三维多孔支架、经多巴胺修饰的 PCL-HA 三维多孔支架及经多巴胺修饰并加载 CDMP-1 的 PCL-HA 三维多孔支架,分别设为 A、B、C 组,进行以下检测。① 扫描电镜观察:将 3 组支架材料用导电胶带固定于铜测试台上,表面喷金处理(喷金平均厚度为 24 nm),于扫描电镜下观测支架形貌特征。② 孔隙率测量:应用 Micro-CT 扫描 3 组支架材料(n=5),并用 Inveon research workplace 软件进行三维重建,根据阈值对比法得到空隙体积,根据以下公式计算孔隙率:孔隙率=空隙体积/总体积×100%。③ 支架表面水静态接触角测试:采用 SL200B 接触角测试仪对 3 组支架材料表面水静态接触角进行测试,表征其表面亲水性。测试方法:以蒸馏水作为滴定液体,在室温和合适湿度下,将蒸馏水缓慢滴至支架表面,记录液滴与支架材料表面接触瞬间的图像,计算得到水静态接触角;每个支架测试 3 个不同的表面区域,取平均值。
1.3. 支架材料促进 hBMSCs 成软骨分化相关检测
1.3.1. hBMSCs 培养及传代
取出液氮保存的 hBMSCs,用含 10%FBS 的 L-DMEM 培养液重悬细胞,复苏接种(4.0×104 个/cm2 密度)于 T25 培养瓶中,于 37℃、5%CO2以及饱和湿度培养箱中静置培养; 24 h 后半量换液,此后每隔 2~3 d 换液 1 次;当贴壁细胞铺满瓶底达 70%~80% 融合时,0.25% 胰蛋白酶消化传代,按 1∶3 比例将细胞接种至新的培养瓶,取第 3 代细胞用于后续实验。
1.3.2. 支架材料的消毒
将 3 组支架材料置于 24 孔板中,加入 75% 乙醇浸泡 4 h,移弃乙醇,置超净台的无菌器皿中晾干 1 h,同时行紫外灯照射。将消毒处理后的支架材料用于后续细胞实验。
1.3.3. 细胞黏附实验
取 3 组支架材料(n=9)置于 6 孔培养板底部,每个支架按 5×104 个/10 μL 的量接种 hBMSCs(此时细胞量记为 C0)细胞悬液,将细胞悬液用滴管缓慢滴于支架上,尽量使细胞悬液不要溢出支架。之后迅速将 6 孔板置于 37℃、5%CO2以及饱和湿度培养箱中培养 2 h,以便细胞充分黏附到支架上。加入成软骨诱导培养液(含 1 nmol/L 地塞米松、6.25 μg/mL 胰岛素、37.5 μg/mL 2-磷酸抗坏血酸盐、10 ng/mL TGF-
 的 H-DMEM 培养液),培养 24 h。弃培养液,取出细胞-支架复合物转移至新的 6 孔培养板,PBS 洗 2 遍,加入 0.25% EDTA-胰蛋白酶消化细胞;然后加入血清终止消化,移入 10 mL 离心管,以离心半径 10 cm、800 r/min 离心 5 min;弃上清,以 L-DMEM 培养液混悬细胞,同时行每孔底细胞计数,细胞量记为 C1。按以下公式计算支架上细胞黏附率:细胞黏附率=(C0–C1)/C0×100%。
的 H-DMEM 培养液),培养 24 h。弃培养液,取出细胞-支架复合物转移至新的 6 孔培养板,PBS 洗 2 遍,加入 0.25% EDTA-胰蛋白酶消化细胞;然后加入血清终止消化,移入 10 mL 离心管,以离心半径 10 cm、800 r/min 离心 5 min;弃上清,以 L-DMEM 培养液混悬细胞,同时行每孔底细胞计数,细胞量记为 C1。按以下公式计算支架上细胞黏附率:细胞黏附率=(C0–C1)/C0×100%。
1.3.4. 细胞增殖实验
当 3 组细胞-支架复合物成软骨诱导培养 1、4、7、14、21 d 后,弃孔板中的培养基。将 MTT 溶液经新鲜培养基稀释 10 倍后,加入培养板孔并置于 37℃ 培养箱避光孵育 4 h。然后自每个样品吸取 200 μL 混合液加入 96 孔板,置酶标仪 450 nm 波长下测定各孔吸光度(A)值,每组设 5 个复孔。
1.3.5. 细胞活性检测
3 组细胞-支架复合物成软骨诱导培养 1、7、14 d 后,用 Live/Dead 试剂盒检测细胞活性。将细胞-支架复合物用 PBS 洗涤 3 遍后,与 Live/Dead 试剂盒的工作液(2 μmol/L Calcein AM 和 4 μmol/L EthD-1)室温孵育 60 min,最后用激光共聚焦显微镜检测细胞荧光信号,活细胞显示为绿色,死细胞为红色。
1.3.6. 实时荧光定量 PCR 检测软骨特异基质基因表达
3 组细胞-支架复合物成软骨诱导培养 7、14、21 d 后,采用实时荧光定量 PCR 检测软骨特异基质Ⅱ型胶原和聚集蛋白聚糖(Aggrecan)基因表达。所有引物设计合成均由南京凯基生物技术有限公司完成,引物序列参照文献[6]:GAPDH 为内参,上游引物:5’-TCGGAGTGAACGGATTTGG-3’,下游引物:5’-GCCAGAGTTAAAAGCAGCCCT-3’;Ⅱ型胶原上游引物:5’-CAGGTGAAGGTGGGAAACCA-3’,下游引物:5’-ACCCACGAGGCCAGGAG-3’;Aggrecan 上游引物;5’-CCCAACCAGCCTGACAA-3’;下游引物:5’-CCTTCTCGTGCCAGATCATCA-3’。将 3 组标本称重后置于冰上,加入 Trizol 试剂,并加入氯仿、异丙醇提取 RNA。采用实时荧光定量 PCR 检测样本中Ⅱ型胶原 mRNA 和 Aggrecan mRNA相对表达量,每个样本重复检测 3 次。
1.4. 统计学方法
采用 SPSS13.0 统计软件进行分析。数据以均数±标准差表示,组间比较采用单因素方差分析,两两比较采用 SNK 检验;检验水准 α=0.05。
2. 结果
2.1. 支架材料相关观测
2.1.1. 大体观察及扫描电镜观察
3 组 PCL-HA 三维多孔支架均为直径 7 mm、高 2 mm 的圆柱体形状;A 组支架颜色为白色,经多巴胺表面修饰后 B、C 组支架颜色均为较深的棕色。扫描电镜观察示,支架为三维多孔状结构,孔洞相互联通,孔径为 400~500 μm,孔隙率 56%,材料纤维走向为 0°/90°。见图 1。
图 1.
General observation and scanning electron microscope observation of scaffold materials in 3 groups
3 组支架材料大体观察及扫描电镜观察
从左至右依次为 A、B、C 组 a. 大体观察;b. 扫描电镜观察(×30)
From left to right for groups A, B, and C respectively a. General observation; b. Scanning electron microscope observation (×30)
2.1.2. 支架表面水静态接触角检测
A 组支架材料表面水静态接触角为 76°;经多巴胺改性后的 B、C 两组支架材料表面水静态接触角均为 0°。见图 2。
图 2.
The water static contact angle of the scaffold surface in 3 groups
3 组支架材料表面水静态接触角
a. A 组;b. B 组;c. C 组
a. Group A; b. Group B; c. Group C

2.2. 支架材料促 hBMSCs 成软骨分化相关观测
2.2.1. 细胞黏附实验
成软骨诱导培养后 24 h,A、B、C 组细胞黏附率分别为 34.3%±3.5%、48.3%±1.5%、57.4%±2.5%,C 组细胞黏附率显著高于 A 、B 组,B 组高于 A 组,差异均有统计学意义(P<0.05)。
2.2.2. 细胞增殖实验
3 组细胞在支架上的 A 值均随培养时间延长而增大。培养后 4、7、14、21 d,C 组 A 值显著高于 A、B 组,B 组高于 A 组,差异均有统计学意义(P<0.05)。见图 3。
图 3.
Cell adhesion detection of scaffolds in 3 groups at different time points by MTT method
MTT 法检测培养不同时间点 3 组支架上细胞黏附情况
2.2.3. 细胞活性检测
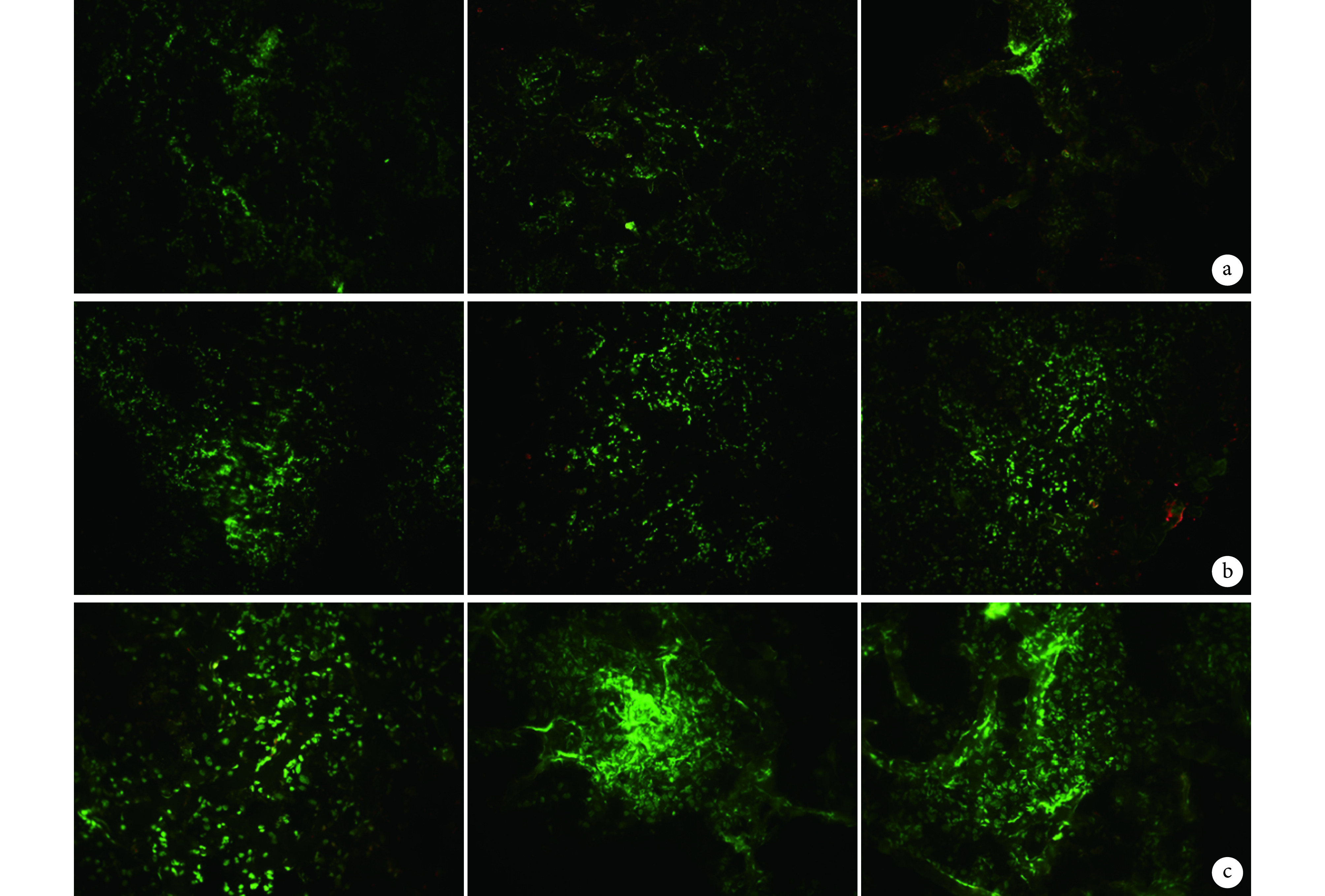
荧光显微镜观察示,培养 1、7、14 d,3 组支架内的细胞几乎均被染成绿色,有较好的细胞活性。见图 4。
图 4.
Cell activity detection of each group at different time points
培养各时间点各组支架内细胞活性检测(荧光显微镜×100)
从左至右依次为培养后 1、7、14 d a. A 组;b. B 组;c. C 组
From left to right for cultured for 1, 7, and 14 days respectively a. Group A; b. Group B; c. Group C
2.2.4. 实时荧光定量 PCR 检测软骨特异基质基因表达
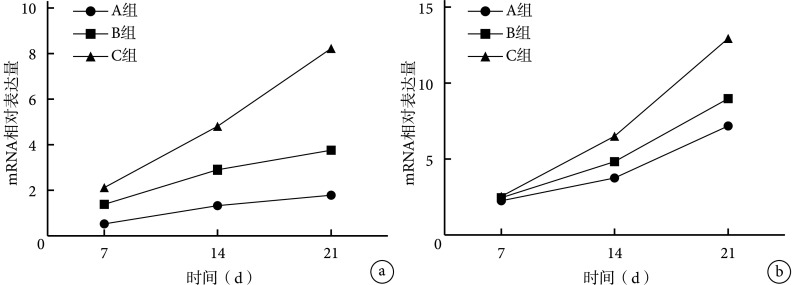
随培养时间延长,3 组支架Ⅱ型胶原 mRNA 和 Aggrecan mRNA 相对表达量均逐渐增加。培养后 14、21 d,C 组 Aggrecan mRNA 相对表达量均显著高于 A、B 组,B 组高于 A 组,差异均有统计学意义(P<0.05);但培养后 7 d,3 组间比较差异无统计学意义(P>0.05)。而培养后各时间点 A、B、C 组间Ⅱ型胶原 mRNA 相对表达量比较差异均有统计学意义(P<0.05)。见图 5。
图 5.
Specific gene expression detection of cartilage matrix in each group by real-time fluorescence quantitative PCR
实时荧光定量 PCR 检测各组软骨特异基质基因表达
a. Ⅱ型胶原;b. Aggrecan
a. Collagen type Ⅱ; b. Aggrecan
3. 讨论
3.1. 3D 打印技术在软骨组织工程支架制备中的应用
软骨缺损修复是骨科临床难题。组织工程技术的发展,给软骨缺损修复带来了希望,其中支架材料的机械及生物属性是软骨再生的关键因素。软骨组织工程支架的设计,既要考虑到细胞及组织的生长,也要考虑到支架的机械性能及降解速度等。以往的组织工程技术(尤其是第二、三代组织工程软骨修复技术)主要是模仿细胞外基质制备生物支架,在体外将细胞种植于支架上,这种支架材料制备方法不能控制支架的几何学参数(如孔径、多孔性等),并且也无法制备复杂的三维结构[7-8]。近年来借助于计算机辅助设计和 3D 打印技术,使用医用高分子材料构建的 3D 打印多孔支架,其外形及内部结构可控、机械强度高,是修复软骨损伤的理想支架材料[9]。
3D 打印技术采用分层加工、叠加成形的方法,可以制造出任意复杂的三维结构,成形过程与人体关节的复杂程度无直接关系[10]。同时,通过调节打印粉末颗粒的大小或改变切层的填充方式,就可以改变孔隙率和孔径大小,非常适合制造符合组织工程学需要、适应细胞生长的人工骨软骨支架。同时 3D 打印技术制备人工支架材料具有生产周期短和成本低等优点,能满足临床上的大量需求。随着精密制造技术在生物材料领域应用的不断发展,实现骨软骨个性化修复已日益明晰[10]。
3.2. 无细胞支架及其负载生物活性因子方法的局限性
PCL 是目前研究最多、应用最广的脂肪族聚酯类生物材料,由于其酯键容易发生水解而导致主链断裂,在人体内可以完全降解,产物为 CO2 和 H2O,并通过新陈代谢排出体外[11]。我们在前期研究中使用质量比为 7∶3 的 PCL-HA 混合材料构建了 3D 打印支架,并与自体骨髓血相复合,进行体外直接诱导培养和体内植入实验,得到了具有特定形状与良好机械性能的新生软骨组织;但该支架在软骨诱导过程中不具备稳定可靠的透明软骨再生能力,易产生纤维软骨样组织[4]。由于尚无有效的技术手段对其进行调控,这也是迄今制约软骨组织工程技术进一步发展与临床应用急需解决的关键问题[12]。
为了实现可靠的透明软骨再生,我们需要深入了解软骨诱导分化过程中支架材料内种子细胞的生物学行为与支架内透明软骨基质积聚的关系,从而解决上述问题。研究表明,使用特定生长因子实现对细胞增殖、分化、透明软骨基质表达的调控,提高软骨支架再生性能[13],并由此产生了无细胞支架材料的概念。无细胞支架不仅摒弃了负载各种源性干细胞涉及的伦理问题,而且负载的生物活性因子能促进其与期望的细胞底物间相互作用并增强细胞功能。
支架材料表面生物活性因子的负载方式大体可分为可溶性和固定化两种,两种方式负载的生物活性因子均与细胞上的受体结合[14]。但研究表明,可溶性生物活性因子会参与宿主细胞的胞吞作用,随之快速降解,使得它对细胞的作用时间及效能非常有限;而固定化生物活性因子却能抑制宿主细胞的胞吞作用,显著抑制其浓度的快速下降,对细胞的作用时间和效能维持长久[14]。为了达到生物活性因子在材料底物上的固定化附着,大多需要复杂的程序及对底物和生长因子的广泛修饰。理论上固定生物活性因子的方案,最好能利用因子蛋白表面暴露的功能基团,如氨基、羧基和硫醇基等,使其与合适的底物之间形成化学共价键[14-15]。如果生物活性因子的蛋白质或多肽未能形成化学共价键的功能基团,则需要对材料底物表面进行预处理来达到目的。Sharon 等[15]为将 VEGF 较牢固地附着于 PLGA 上,事先用高碘酸盐氧化预处理,然后通过醛糖氧化糖蛋白上的多糖残基使 VEGF 稳定地与酰肼衍生化的 PLGA 结合。但由此带来的弊端是改变了材料底物本身的生物效应。因此,支架材料表面生物活性因子的固定化,应尽可能使用简便有效的功能化程序,才不会改变植入材料和生长因子的效能。
3.3. 多巴胺对生物材料表面改性和负载 CDPM-1 支架的应用
有研究发现,来源于海洋贝类生物的黏附蛋白可在溶液中发生氧化聚合,并能在多种材料的表面形成黏附层,是一种天然的胶黏剂[16]。而多巴胺就是这种黏附蛋白的关键成分,几乎可以黏附在任何材料表面,有效改善材料表面的亲水性和细胞相容性;尤为重要的是,其形成的聚多巴胺层可以作为二级反应平台,在材料表面进一步修饰生物活性分子,赋予材料优异的生物学性能[16-17]。
由于多巴胺改性过程无溶剂、无毒、简便高效,因此国内外有很多相关报道[17-20]。Lai 等[18]和 Chien 等[19]均对 Ti 合金表面进行了改性并引入 BMP-2 等活性物质,研究表明均能促进 BMSCs 的增殖分化、ALP 分泌及矿化。Kim 等[20]利用多巴胺将乳铁蛋白固定在 PLGA 多孔微球表面,诱导兔脂肪干细胞成骨分化,结果显示提高了 ALP 分泌、钙沉积及成骨相关基质蛋白 mRNA 表达。
本实验就利用了多巴胺优异的生物黏附性能。首先我们采用溶液浇铸法,使多巴胺在 3D 打印支架表面发生氧化自聚合,反应产物(聚多巴胺)均匀覆盖于材料表面[21];然后借助它的二级反应平台,通过迈克尔加成反应(Michael addition reaction)或席夫碱反应(Schiff base reaction)[16],从而将生物活性物质 CDMP-1 引入到材料表面。结果显示多巴胺的引入对 PCL-HA 三维多孔支架材料的生物学性能影响较大,降低了材料表面水静态接触角,改善了材料的亲水性能。将 hBMSCs 以静态培养法接种于 3 组支架,结果发现经多巴胺改性后的材料对细胞黏附和增殖都有明显促进作用,且对细胞活性无毒性作用。
CDMP-1 是 Hotten 等[22]首先从人胚胎 cDNA 库中发现的一种多肽生长因子,研究证明其作用于大鼠肢体芽细胞可诱导间质聚合和软骨形成。此外,CDMP-1 作用于人软骨细胞,可抑制软骨细胞外基质相关降解酶——基质金属蛋白酶 13 和 ADAMTS4 的表达,同时呈剂量依赖性增强软骨合成代谢相关基因 SOX9 和 Aggrecan 的表达[23]。本研究利用多巴胺的黏附特性,在 PCL-HA 三维多孔支架表面引入 CDMP-1,与 hBMSCs 成软骨诱导培养后进行基因检测来验证其促软骨分化的功能特性。结果显示各组软骨特异基质Ⅱ型胶原 mRNA 和 Aggrecan mRNA 表达均呈明显上升趋势;且培养 7、14、21 d Ⅱ型胶原 mRNA 相对表达量及培养 14、21 d Aggrecan mRNA 相对表达量,3 组间比较差异均有统计学意义。因此,多巴胺作为天然黏附剂,对干细胞无毒性,且对 CDMP-1 的生物功效无不良影响,保留了 CDMP-1 体外刺激 hBMSCs 成软骨分化的生物活性。
本研究局限性在于:首先,100 ng/mL CDMP-1 浓度是参照文献报道使用的浓度,我们并未优化选择浓度;其次,本研究的体外培养时间终点为 21 d,未来尚需培养更长时间后检测,同时还需了解无细胞支架体内植入后的促软骨再生作用;最后,仍需进一步探讨其他软骨分化特异基质,如Ⅹ型胶原、SOX9 基因和蛋白水平的变化。
Funding Statement
南京市卫生局重点项目(ZKX15024);徐州市科技计划社会发展项目(XM13B086)
Nanjing Municipal Health Bureau Key Projects (ZKX15024); Xuzhou Science and Technology Planning Social Development Projects (XM13B086)
References
- 1.Grande DA, Schwartz JA, Brandel E, et al Articular Cartilage Repair: Where We Have Been, Where We Are Now, and Where We Are Headed. Cartilage. 2013;4(4):281–285. doi: 10.1177/1947603513494402. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 2.裴福兴 中国髋、膝关节置换的现状及展望. 中国骨与关节杂志. 2012;1(1):4–8. [Google Scholar]
- 3.Lee CH, Cook JL, Mendelson A, et al Regeneration of the articular surface of the rabbit synovial joint by cell homing: a proof of concept study. Lancet. 2010;376(9739):440–448. doi: 10.1016/S0140-6736(10)60668-X. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 4.Yao Q, Wei B, Liu N, et al Chondrogenic regeneration using bone marrow clots and a porous polycaprolactone-hydroxyapatite scaffold by three-dimensional printing. Tissue Eng Part A. 2015;21(7-8):1388–1397. doi: 10.1089/ten.tea.2014.0280. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 5.Poh CK, Shi Z, Lim TY, et al The effect of VEGF functionalization of titanium on endothelial cells in vitro. Biomaterials. 2010;31(7):1578–1585. doi: 10.1016/j.biomaterials.2009.11.042. [DOI] [PubMed] [Google Scholar]
- 6.Park K, Huang J, Azar F, et al Scaffold-free, engineered porcine cartilage construct for cartilage defect repair in vitro and in vivo study. Artif Organs. 2006;30(8):586–596. doi: 10.1111/j.1525-1594.2006.00267.x. [DOI] [PubMed] [Google Scholar]
- 7.Steadman JR, Rodkey WG, Briggs KK Microfracture to treat full-thickness chondral defects: surgical technique, rehabilitation, and outcomes. J Knee Surg. 2002;15(3):170–176. [PubMed] [Google Scholar]
- 8.Li WJ, Tuli R, Okafor C, et al A three dimensional nanofibrous scaffold for cartilage tissue engineering using human mesenchymal stem cells. Biomaterials. 2005;26(6):599–609. doi: 10.1016/j.biomaterials.2004.03.005. [DOI] [PubMed] [Google Scholar]
- 9.Lee M, Wu BM Recent advances in 3D printing of tissue engineering scaffolds. Methods Mol Biol. 2012;868:257–267. doi: 10.1007/978-1-61779-764-4_15. [DOI] [PubMed] [Google Scholar]
- 10.吴天琦, 杨春喜 可用于骨修复的 3D 打印多孔支架研究进展. 中国修复重建外科杂志. 2016;30(4):509–513. [PubMed] [Google Scholar]
- 11.Oh SH, Park IK, Kim JM, et al In vitro and in vivo characteristics of PCL scaffolds with pore size gradient fabricated by a centrifugation method. Biomaterials. 2007;28(9):1664–1671. doi: 10.1016/j.biomaterials.2006.11.024. [DOI] [PubMed] [Google Scholar]
- 12.Hardingham T, Tew S, Murdoch A Tissue engineering: chondrocytes and cartilage. Arthritis Res. 2002;4 Suppl 3:S63–68. doi: 10.1186/ar561. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 13.Heng BC, Cao T, Lee EH Directing stem cell differentiation into the chondrogenic lineage in vitro. Stem Cells. 2004;22(7):1152–1167. doi: 10.1634/stemcells.2004-0062. [DOI] [PubMed] [Google Scholar]
- 14.Place ES, Evans ND, Stevens MM Complexity in biomaterials for tissue engineering. Nat Mater. 2009;8(6):457–470. doi: 10.1038/nmat2441. [DOI] [PubMed] [Google Scholar]
- 15.Sharon JL, Puleo DA Immobilization of glycoproteins, such as VEGF, on biodegradable substrates. Acta Biomater. 2008;4(4):1016–1023. doi: 10.1016/j.actbio.2008.02.017. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 16.Lee YB, Shin YM, Lee JH, et al Polydopamine-mediated immobilization of multiple bioactive molecules for the development of functional vascular graft materials. Biomaterials. 2012;33(33):8343–8352. doi: 10.1016/j.biomaterials.2012.08.011. [DOI] [PubMed] [Google Scholar]
- 17.Poh CK, Shi Z, Lim TY, et al The effect of VEGF functionalization of titanium on endothelial cells in vitro. Biomaterials. 2010;31(7):1578–1585. doi: 10.1016/j.biomaterials.2009.11.042. [DOI] [PubMed] [Google Scholar]
- 18.Lai M, Cai K, Zhao L, et al Surface functionalization of TiO2 nanotubes with bone morphogenetic protein 2 and its synergistic effect on the differentiation of mesenchymal stem cells. Biomacromolecules. 2011;12(4):1097–1105. doi: 10.1021/bm1014365. [DOI] [PubMed] [Google Scholar]
- 19.Chien CY, Tsai WB Poly (dopamine)-assisted immobilization of Arg-Gly-Asp peptides, hydroxyapatite, and bone morphogenic protein-2 on titanium to improve the osteogenesis of bone marrow stem cells. ACS Appl Mater Interfaces. 2013;5(15):6975–6983. doi: 10.1021/am401071f. [DOI] [PubMed] [Google Scholar]
- 20.Kim SE, Yun YP, Shim KS, et al Effect of lactoferrin-impregnated porous poly (lactide-co-glycolide) (PLGA) microspheres on osteogenic differentiation of rabbit adipose-derived stem cells (rADSCs) Colloids Surf B Biointerfaces. 2014;122:457–464. doi: 10.1016/j.colsurfb.2014.06.057. [DOI] [PubMed] [Google Scholar]
- 21.Haeshin L, Dellatore SM, Miller WM, et al Mussel-inspired surface chemistry for multifunctional coatings. Science. 2007;318(5849):426–430. doi: 10.1126/science.1147241. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 22.Hotten GC, Matsumoto T, Kimura M, et al Recombinant human growth/differentiation factor 5 stimulates mesenchyme aggregation and chondrogenesis responsible for the skeletal development of limbs. Growth Factors. 1996;13(1-2):65–74. doi: 10.3109/08977199609034567. [DOI] [PubMed] [Google Scholar]
- 23.Enochson L, Stenberg J, Brittberg M, et al GDF5 reduces MMP13 expression in human chondrocytes via DKK1 mediated canonical Wnt signaling inhibition. Osteoarthritis Cartilage. 2014;22(4):566–577. doi: 10.1016/j.joca.2014.02.004. [DOI] [PubMed] [Google Scholar]